Пересадили печень после отравления грибами
Обновлено: 23.04.2024
Судебно-гистологическое отделение Белгородского бюро судебно-медицинской экспертизы, Белгород, Россия, 308017
ФГБУ "Российский центр судебно-медицинской экспертизы" Минздравсоцразвития России
ФГБУ Российский центр судебно-медицинской экспертизы Минздравсоцразвития России
Особенности морфологических проявлений поражения печени при отравлении бледной поганкой
Журнал: Судебно-медицинская экспертиза. 2017;60(3): 23‑26
Судебно-гистологическое отделение Белгородского бюро судебно-медицинской экспертизы, Белгород, Россия, 308017
Рассмотрены морфологические особенности массивного некроза печени при отравлении ядами бледной поганки (Amanita phalloides) в сравнении с другими его причинами. Показано наличие пролиферации в перипортальных зонах печени и участие механизмов апоптоза при гибели гептоцитов. Уточнен темп умирания при данном отравлении.
Судебно-гистологическое отделение Белгородского бюро судебно-медицинской экспертизы, Белгород, Россия, 308017
ФГБУ "Российский центр судебно-медицинской экспертизы" Минздравсоцразвития России
ФГБУ Российский центр судебно-медицинской экспертизы Минздравсоцразвития России
Использование методов иммуногистохимии (ИГХ) находит все большее применение в современной морфологии [1]. Не исключение и судебная медицина. Причины массивного некроза печени (МНП), его клинические и морфологические проявления, в частности при отравлении грибами, описаны давно [2—5]. Особенности повреждения паренхимы и реакции на него, характерные для различных причин МНП, до сих пор оставались вне внимания исследователей. Между тем их выявление может дать ключ не только к познанию патогенеза МНП, но и к пониманию функциональной морфологии печени в норме. В число функций этого органа входит обезвреживание неиммуногенных ксенобиотиков путем их метаболизма и выделения с желчью либо подготовки к выделению с мочой. Токсическое поражение печени возникает в случае, если происходит срыв ее детоксикационной функции.
В настоящее время исследователи слишком много внимания уделяют исследованиям на молекулярном и ультраструктурном уровнях, пренебрегая светооптическим исследованием. Между тем синтез обнаруженных ими фактов, переход от частностей к целостным теориям изучаемых явлений требуют изучения каждого явления на всех уровнях организации, и светооптические исследования еще далеко не исчерпали своих возможностей. Наблюдаемые при них феномены, являясь интегральными, могут играть эвристическую роль для поиска перспективных путей изучения тех же явлений на молекулярно-биологическом и субклеточном уровнях.
В современной литературе нет подробных данных об иммуногистохимическом или электронно-микроскопическом исследовании печени при отравлении бледной поганкой. По-видимому, это объясняется предпочтением исследователей экспериментального материала секционному и тем, что они не подозревают о возможности существенных различий МНП, вызванных различными этиологическими факторами, и используют для моделирования МНП более доступный тетрахлорметан.
Цель исследования — описание морфологических особенностей реакции печени человека на токсины бледной поганки на органном, тканевом и клеточном уровнях, а также установление темпа умирания при таких отравлениях.
Материал и методы
Исследовали смертельное отравление бледной поганкой (Amаnita phalloides) 9 лиц мужского пола в возрасте от 2 до 44 лет и девочки 4 лет. Некоторые из пострадавших утверждали, что собирали маслята или сыроежки, другие не могли описать грибы; только один пострадавший указал морфологические признаки бледной поганки. Диагноз был установлен на основании клинической картины и не вызывал сомнений. Смерть наступила в стационаре на 5—7-е сутки после употребления грибов. Ведущим клиническим синдромом была печеночная недостаточность, непосредственной причиной смерти служила печеночная кома, которая в ряде случаев развивалась на фоне желудочно-кишечного кровотечения.
Две группы сравнения составили 10 наблюдений смертельного отравления хлорпроизводными углеводородов: дихлорэтаном — 8, сочетанием дихлорэтана и этиленгликоля — 1, тетрахлорметаном — 1 и 9 наблюдений вирусного гепатита В с фульминантным течением, завершившихся смертью.
Отравились хлорпроизводными углеводородов женщина 50 лет и 9 мужчин в возрасте от 23 до 66 лет. Трое приняли яд с целью суицида, 2 — в качестве суррогата алкоголя, 1 — случайно; в остальных случаях обстоятельства отравлений остались неизвестными. Смерть одного пострадавшего наступила на месте происшествия, остальных — в стационаре через 2—7 ч после приема яда; только 2 пострадавших прожили 2 сут с момента отравления, несмотря на интенсивную терапию. Печеночная недостаточность явилась причиной смерти только одного: пострадавший выпил тетрахлорметан. У остальных в плазме крови было повышено содержание билирубина и трансфераз, что указывало на поражение печени, но смерть была связана с токсическим действием дихлорэтана на головной мозг и/или сердце.
Фульминантный вирусный гепатит явился причиной смерти 5 мужчин и 4 женщин в возрасте от 21 года до 40 лет, не злоупотреблявших алкоголем. Их смерть наступила от печеночной комы в стационаре на 5—7-е сутки от начала болезни.
Результаты и обсуждение
Макроскопически при отравлении бледной поганкой и тетрахлорметаном наблюдали классическую картину МНП: размеры и масса печени уменьшены (масса у взрослых 1300—1400 г), ткань дряблая, распластывается на столе, на разрезе пестрого вида, с чередованием участков темно-красного и охряно-желтого, почти оранжевого цвета. В одном случае имелись также серовато-зеленоватые поля. Обнаружили также признаки медленной смерти (белые свертки в полостях сердца), отека мозга и геморрагического синдрома. У большинства умерших от вирусного гепатита масса составляла от 2000 до 2500 г, отмечали увеличение лимфатических узлов воротной вены и селезенки.
Микроскопически при отравлениях бледной поганкой, помимо собственно МНП, обнаружили ряд особенностей.
1. Массивные поля некроза захватывали все гепатоциты, кроме перипортальных. В центрах долек — распад печеночных клеток, их лизис с явлениями коллапса стромы.
Ближе к портальным трактам гепатоциты еще сохраняли форму, хотя многие были лишены ядер и находились чаще всего в состоянии крупнокапельной жировой дистрофии. Признаков холестаза не наблюдалось (рис. 1). Некоторые гибнущие клетки давали положительную ИГХ-реакцию на bcl-2 (рис. 2). В почках пигментных цилиндров немного, они имели не характерный для желчных пигментов зеленоватый цвет, а золотисто-буроватый, указывающий на их гемоглобиновую или миоглобиновую природу.

Рис. 1. Массивный некроз печени без признаков холестаза при отравлении бледной поганкой. Коллапс стромы со сближением центральных вен. Ув. 100. Здесь и на рис. 3—4: окраска гематоксилином и эозином.

Рис. 2. Апоптоз в зонах гибели гепатоцитов. ИГХ с АТ к bcl-2. Ув. 400.
В противоположность этому при фульминантном гепатите отмечали признаки холестаза в виде обесцвечивания кала (клинические и секционные данные), скоплений желчи в ткани печени и пигментных цилиндров с характерным зеленым оттенком в почках. При отравлении тетрахлорметаном все эти признаки также присутствовали, но, кроме того, произошло образование кристаллов оксалатов в канальцах почек, а желчные пигменты окрасили эти кристаллы в необычный зеленовато-коричневый цвет.
2. Среди погибающих и погибших, но еще нелизированных гепатоцитов встречаются клетки, жировая дистрофия в которых еще не достигла степени крупнокапельной (рис. 3). В их цитоплазме множество мелких округлых жировых капель с четкими границами, которые, даже заполнив всю клетку, не сливаются друг с другом, не оттесняют ядро на периферию, из-за чего клетка похожа на ягоду малины. Такая форма жировой дистрофии встречалась нам только при острых отравлениях гепатотропными ядами (токсины бледной поганки, галогенпроизводные углеводородов) и ни разу не наблюдалась при ином происхождении стеатоза печени.

Рис. 3. Жировая дистрофия гепатоцитов с образованием множества мелких округлых жировых капель с четкими границами, не сливающихся друг с другом и не оттесняющих ядро на периферию, при отравлении бледной поганкой. Ув. 400.
При фульминантном вирусном гепатите преобладала баллонная дистрофия, тогда как жировая отсутствовала или имела характер очаговой средне- и мелкокапельной, причем в каждом гепатоците была лишь одна липидная вакуоля, оттесняющая ядро на периферию. Кроме того, наблюдали гиалиново-капельную дистрофию, внутриядерные включения и аномалии формы и размера гепатоцитов и их ядер. Таким образом, донекротические изменения печеночных клеток при различной этиологии МНП имеют совершенно разный характер.
3. При отравлениях бледной поганкой перипортально отмечалась пролиферация базофильных полиморфных гепатоцитов с крупными ядрами с диспергированным хроматином. Эти клетки образовывали примитивные трабекулы, реже тубулы (рис. 4). Высокое ядерно-цитоплазматическое соотношение в клетках пролифератов и их гиперхромия свидетельствуют об их активном размножении. Эти же клетки давали положительную ИГХ-реакцию на маркер пролиферации Ki-67. Все это соответствует данным литературы [6], согласно которым камбиальные предшественники паренхиматозных элементов печени находятся вблизи портальных трактов. Пролиферация желчевыводящих протоков отсутствовала.

Рис. 4. Перипортальная пролиферация гепатоцитов при отравлении бледной поганкой. Ув. 200.
При фульминантном вирсном гепатите, хотя смерть пациентов наступала в те же сроки, признаки пролиферации полностью отсутствовали. В случае отравления тетрахлометаном их также не было, но это могло быть связано с быстрой смертью пострадавшего.
В зонах некроза, особенно по их периферии, отмечали активацию ретикулоэндотелия и лимфомакрофагальную инфильтрацию с примесью сегментоядерных нейтрофилов.
При фульминантном гепатите нейтрофилы обнаруживали в небольшом количестве только в одном наблюдении. В остальных случаях инфильтрат состоял исключительно из лимфоцитов и макрофагов, причем встречались погибшие гепатоциты, окруженные лимфоцитами, а также имеющие дефекты ткани, в которые внедрялись лимфоциты (признаки аутоиммунной реакции). В случаях токсической природы МНП подобные явления не встречались.
5. При отравлениях некроз всегда появлялся раньше и был выражен сильнее в центрах долек, при вирусном поражении нередко начинался перипортально или с мостовидного варианта, т. е. очаги некроза сначала соединяли портальные тракты друг с другом или с центральными венами и только потом распространялись на остальную паренхиму.
Маркеров иных заболеваний печени не обнаружили ни в одном наблюдении.
В других органах выявили признаки синдрома диссеминированного внутрисосудистого свертывания, а в почках — умеренно выраженный некротический нефроз. Клинически им соответствовали снижение протромбинового индекса, содержания общего белка, фибриногена и количества тромбоцитов в крови, гипокоагуляция, повышение концентрации креатинина и мочевины и проявления геморрагического синдрома (тяжелые рецидивирующие желудочно-кишечные кровотечения, макрогематурия и др.). При фульминантном гепатите признаков диссеминированного внутрисосудистого свертывания не наблюдали, а в почках доминировал пигментный нефроз.
Таким образом, отсутствие желчных цилиндров в почечных канальцах при отравлениях бледной поганкой в некоторой степени может быть объяснено патоморфозом отравлений под влиянием современной детоксикационной и инфузионной терапии. В 50-е годы ХХ века больные умирали чаще всего через 2—3 дня после приема грибов [3], а в настоящее время летальный исход наступает на 5—7-е сутки, и продукты распада гепатоцитов успевают удалиться с мочой. Судя по различной степени повреждения и лизиса гепатоцитов, они гибнут не одновременно. Некроз печени при отравлениях бледной поганкой прогрессирует, и смерть от печеночной недостаточности наступает, если он охватывает примерно 90% паренхимы, т. е. когда сохраняются лишь камбиальные элементы и немногочисленные тяжело поврежденные зрелые гепатоциты. Если некроз развивается не одномоментно и продолжает прогрессировать почти до самой смерти, то в почках должно быть хотя бы немного желчных пигментов. Их полное отсутствие можно объяснить только ранним нарушением биосинтетических функций гепатоцитов, предшествующим их некрозу, т. е. влиянием токсинов бледной поганки на органеллы, в которых происходит биосинтез, — эндоплазматический ретикулум.
Этим же объясняется своеобразная форма жировой дистрофии, при которой мелкие капли липидов соприкасаются, но не сливаются. Такая ситуация возможна в случае, если они отграничены друг от друга мембраной, т. е. накопление жира вначале происходит в эндоплазматическом ретикулуме и только при его повреждении липиды выходят в цитоплазму.
В генезе холестаза, наблюдаемого при других вариантах МНП, важную роль играют частичное сохранение паренхиматозных элементов и функционирование некоторых поврежденных гепатоцитов. Отсутствие холестаза при отравлении бледной поганкой должно быть связано с полным прекращением функции гепатоцитов. Это означает, что сохранившие жизнеспособность малодифференцированные камбиальные элементы, образующие перипортальные регенераты, способны пролиферировать, но не могут выполнять биосинтетические функции [7]. Аналогично зрелые гепатоциты, пребывающие в состоянии дистрофии, но сохранившие жизнеспособность, также не способны их осуществлять, что приводит к смерти. Такую функциональную несостоятельность можно объяснить дефицитом энергии и пластических субстанций в условиях глубокой дистрофии и/или интенсивной пролиферации, а также специфическим действием токсинов бледной поганки на процессы биосинтеза.
Общеизвестно, что аманитины — наиболее токсичные вещества из этого гриба — блокируют синтез белка [4, 5]. Это должно вести и к прекращению синтеза небелковых соединений, поскольку осуществляющие его ферменты также являются белками. По мнению ряда исследователей, блокада РНК-полимераз — главный, но не единственный механизм действия токсинов бледной поганки. По-видимому, имеются и иные, пока неизученные механизмы, которые определяют селективную гепатотропность этих ядов и избирательное подавление специализированных функций печеночных клеток при относительном сохранении их способности к пролиферации и самоподдержанию.
В противоположность этому при вирусном гепатите наиболее тяжело поражаются перипортальные зоны, где находятся камбиальные элементы. По-видимому, именно с этим связано отсутствие признаков регенерации при фульминантном гепатите. Возможно, поражение камбиальных элементов играет роль и в развитии нарушений регенерации при выживании больных вирусным гепатитом типа В.
Существенные различия в морфологических изменениях гепатоцитов, предшествующих МНП различной этиологии, указывают на разные механизмы повреждений этих клеток при действии вирусных и токсических факторов.
Учитывая длительный период времени от употребления грибов до развития повреждения печени, можно предположить существование так называемого летального синтеза, т. е. ведущую патогенетическую роль не самих токсинов, а их метаболитов, которые также являются неизученными. Темп умирания в основной группе может быть оценен как замедленный с развитием печеночно-почечной недостаточности и ДВС-синдрома.
Заключение
Исследование позволило выявить различия морфологических проявлений МНП при действии разных этиологических факторов — токсинов бледной поганки и вируса гепатита В; наметить перспективные направления научных исследований в области патофизиологии и патоморфологии печени. Необходимо изучение печени при МНП разного происхождения электронно-микроскопическими, химико-токсикологическими методами для определения последовательности изменений структуры органелл и нарушений различных биосинтетических процессов, а также выявления основных метаболитов аманитинов и их токсичности. Это позволит понять не только патогенез отравлений бледной поганкой, но и особенности детоксикационной функции печени и ее реакций на повреждение в различных условиях.
Полученные результаты могут быть использованы в судебно-медицинской практике для диагностики смертельных отравлений гепатотропными ядами, а также в клинической медицине для разработки патогенетической терапии при этих отравлениях. В частности, при невозможности пересадки печени наиболее перспективны активная детоксикация путем плазмафереза и гемодиализа вплоть до 5—7-х суток после употребления грибов, а также переливание плазмы для замещения белоксинтезирующей функции печени.
Показана роль апоптоза в гибели гепатоцитов при отравлении изученными грибными ядами.
Трансплантация органов у пациента с отравлением
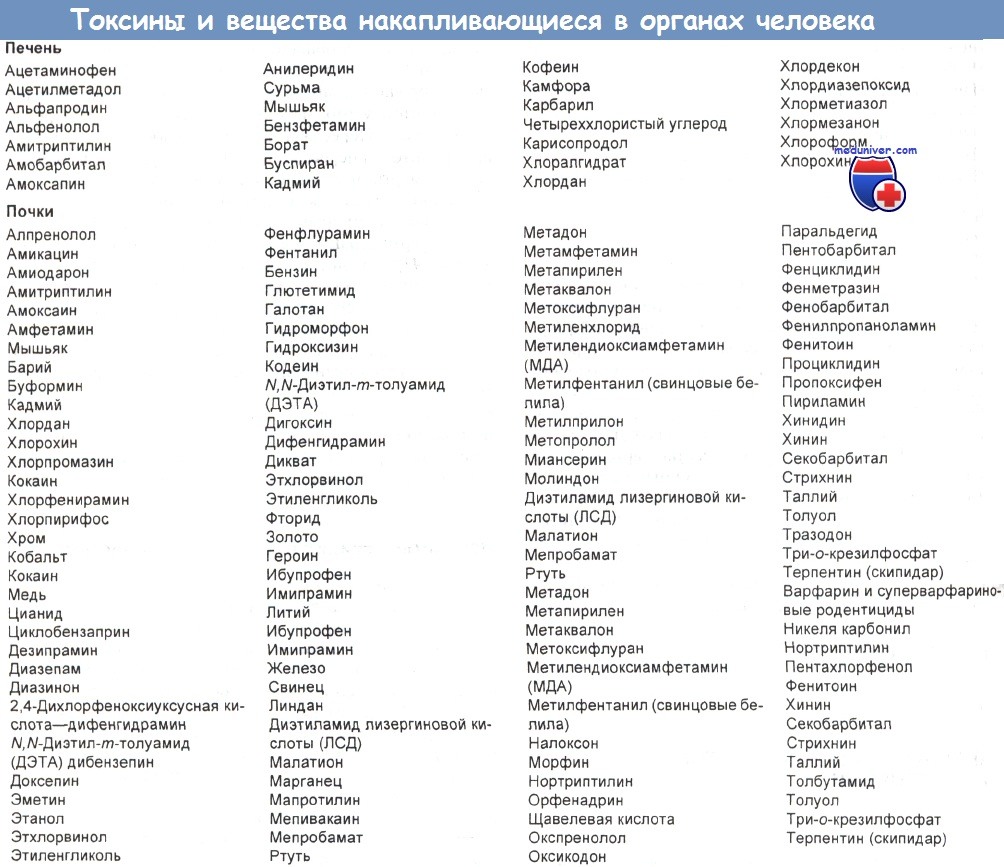
Реципиенты органов при отравлении. Пересадка печени, по-видимому, целесообразна при ее недостаточности, вызванной интоксикацией. Реципиентами могут быть хронические алкоголики, которые воздерживались от спиртного более 6 мес, а также лица, отравившиеся вальпроевой кислотой, ацетаминофеном и грибами.
Доноры органов при отравлении. Leikin и соавт. сообщают о 93 % успеха при пересадке почек от жертв отравления (алкоголем, кокаином, окисью углерода, барбитуратами, свинцом). При пересадке взятой у них печени успех отмечен примерно в 71 % случаев.

Пересаженная печень работает 1 год у 60 % реципиентов, а пересаженная почка — у 78 %. Таким образом, смерть от отравления, по-видимому, не является противопоказанием к донорству печени и почек. Успешно трансплантировали различные органы, взятые от жертв отравления цианидом, в том числе роговица.
Хорошо приживались почечные трансплантаты, если их доноры умерли от отравления цианидом серебра. Умершие от отравления угарным газом могут служить донорами почек, если функция последних в момент забора органа не нарушена. Правда, некоторые реципиенты умирали от хронического гепатита и отторжения почечных трансплантатов.
Пересадка органов от умерших от отравления доноров — относительно новая область медицины. Для более точного определения критериев, определяющих успех трансплантации, необходимы дальнейшие исследования.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Отравление бледной поганкой (аматоксином) и его лечение
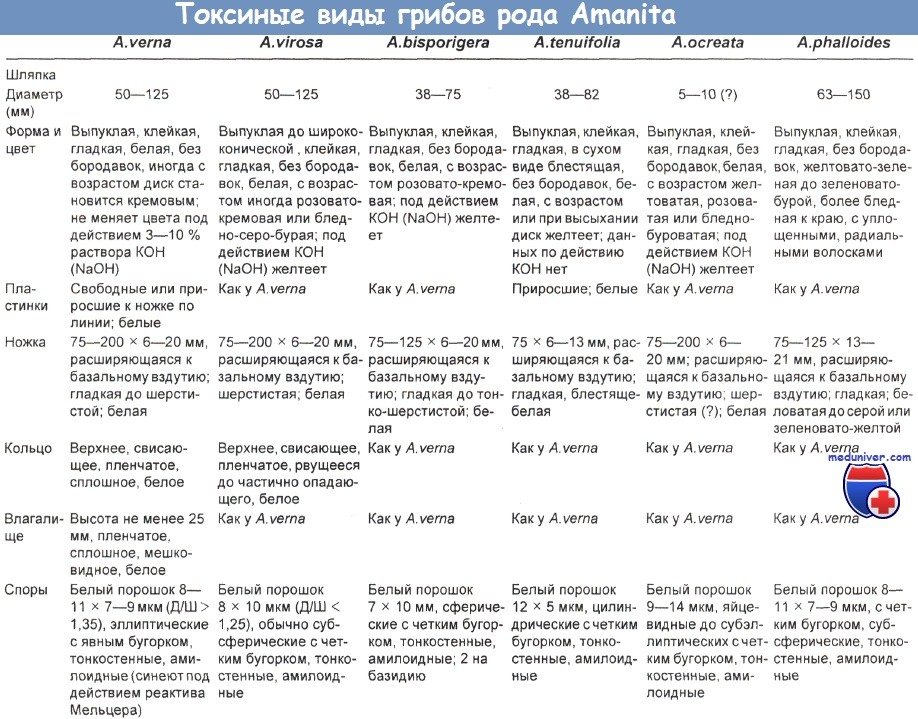
Аматоксины появляются в сыворотке только через 30 ч после потребления содержащего их гриба, и их концентрация составляет 0,5—24 нг/мл, а их экскреция с мочой продолжается до 72 ч с момента поступления в организм. Их высокие концентрации отмечаются в гастродуоденальном соке в течение 100 ч после употребления гриба в пищу. Признаки, позволяющие различать токсичные виды Amanita и виды Galerina в таблицах ниже.
а) Этанол. По-видимому, мыши выживают после отравления бледной поганкой (Amanita phalloides), если перед ее потреблением им введен этанол. Однако клиническое значение этого наблюдения еще не изучено.
б) Беременность. У беременной женщины в возрасте 21 года, отравившейся бледной поганкой, через 10 ч после употребления грибов в пищу отмечались такие симптомы, как тошнота, рвота, боль в животе и понос. Диагноз был подтвержден анализом на альфа-аманитин в крови и амниотической жидкости. Его сывороточная концентрация составляла 18,5 нг/мл (по данным жидкостной хроматографии высокого разрешения), а в амниотической жидкости он не выявлялся. По-видимому, альфа-аманитин с молекулярной массой 900 не проникает через плацентарный барьер даже через 24 ч после употребления в пищу бледной поганки. Из 77 человек, отравившихся содержащими аматоксин видами Lepiota (L.helveola и L.castanea) в Турции, 14 умерли от печеночной недостаточности. Летальные исходы при почечной недостаточности не отмечены.
в) Лабораторные данные отравления бледной поганкой (аматоксином). Альфа- и бета-аманитины в плазме, моче, гастродуоде-нальном соке, фекалиях и тканях можно количественно определять по отдельности методом жидкостной хроматографии высокого разрешения (ЖХВР) с разделением этих веществ на аналитической колонке с обратимой фазой и ультрафиолетовой детекцией. Предел обнаружения составляет 5 нг/мл для обоих соединений. Выявление в плазме их концентрации 2 нг/мл возможно при использовании ЖХВР с амперметрическим детектором.
- Уровни в крови, моче и гастродуоденальном соке. При отравлениях бледной поганкой Jaeger и соавт. определяли в плазме 8—190 нг/мл альфа-аматоксина и 23,5— 162 нг/мл бета-аматоксина. Экскреция с мочой соответствовала 32,18 мкг/ч для первого соединения и 80,15 мкг/ч для второго. Обычно аматоксины выявляются в плазме не дольше 36 ч с момента их приема, однако в моче они сохраняются до четвертого дня. Корреляции между их уровнями в плазме и тяжестью клинической картины или исходом отравления не наблюдается.
Максимальное количество аматоксинов выделяется с мочой в течение 72 ч после потребления грибов, а высокие уровни в гастродуоденальных аспиратах отмечаются в период с 48 по 110 ч после него. Предложен метод ЖХВР для определения альфа- и бета-аманитинов в сыворотке, моче и желудочных промывных водах человека. Чувствительность его составляет до 20 мкг/мл. В исследованиях на животных не наблюдалось корреляции между концентрацией аматоксинов в плазме и клиническим исходом.
- Вспомогательные исследования. В симптоматических случаях проводят рутинные лабораторные исследования, включая клинический анализ крови, определение уровней электролитов, азота мочевины крови, креатинина, протромбинового времени, билирубина в моче и глюкозы в крови. Анализы необходимо делать ежедневно до клинического улучшения.
г) Лечение отравления бледной поганкой (аматоксином):
- Стабилизация состояния. В начале лечения необходимо восстановить водно-электролитный баланс. Пациентам с притупленной чувствительностью сразу же нужно начать внутривенное введение глюкозы, поскольку к обычным осложнениям относится гипогликемия. Больные иногда попадают в отделение неотложной помощи с остановкой сердца из-за потери жидкости и массивного желудочно-кишечного кровотечения. Кроме переливания эритроцитарной массы и введения сбалансированного раствора электролитов, им могут потребоваться свежезамороженная плазма и витамин К.
- Гемоперфузия. Если съедена летальная доза грибов (более 50 г) и с этого момента прошло менее 24 ч, необходима гемоперфузия через активированный уголь.
- Очистка пищеварительного тракта
- Форсированный диурез. Поскольку основная часть токсина выводится в течение первых 24—48 ч, необходимо начать это лечение как можно быстрее. Однако данных, подтверждающих, что так можно уменьшить количество аматоксинов в печени, нет. Судя по накопленному опыту, форсированный диурез (6—9 л/сут) не более эффективен, чем поддержание нормального или слегка увеличенного объема выделяемой мочи.
- Плазмаферез. В двух сериях наблюдений плазмаферез проводили 42 больным с отравлением бледными поганками. Трое из них умерли. Для подтверждения эффективности этого перспективного подхода необходимы дополнительные данные.
- Антидоты бледной поганки - аматоксина. Пенициллин. По-видимому, пенициллин вытесняет аматоксин из мест его связывания с белками плазмы, тем самым способствуя увеличению его почечной экскреции. Возможно, он также препятствует проникновению аматоксина в гепа-тоциты. В одном ретроспективном клиническом исследовании 205 пациентов ежедневное введение 300 000—1 000 000 ME бензилпенициллина чаще сочеталось с выживанием, чем его низкие дозы.
Однако, несмотря на обнадеживающие экспериментальные данные, общая выживаемость пациентов, получавших пенициллин, ненамного выше, чем в выборке в среднем. Результаты опытов на животных наводят на мысль об аналогичной пользе цефалоспорина, но соответствующих клинических исследований не проводилось.
- Лечение острой печеночной недостаточности:
А. Общие принципы:
1. Лица с острой печеночной недостаточностью нуждаются в госпитализации в специализированное отделение, приспособленное для лечения данной патологии.
2. Желательна отработанная методика трансплантации печени.
3. Необходим инвазивный мониторинг для обнаружения осложнений на той стадии, когда они еще не проявились клинически и поддаются лечению.
4. В любых случаях нужно установить монитор центрального венозного давления, ввести артериальный и мочевыводящий катетеры, а также назогастральную трубку.
5. Если у пациента кома III или IV степени, для предупреждения аспирации необходима эндотрахеальная интубация.
6. Требуется также непрерывная импульсная гемоксиметрия.
7. Если развивается гиперкапния (РаСО2 > 6,5 кПа) или гипоксия (РаО2 < 10 кПа), необходима искусственная вентиляция легких. Если имеются асцитная жидкость и раны, регулярно и по клиническим показаниям надо проводить посевы для выявления бактерий.
8. Необходимо регулярно проверять места введения катетеров; последние меняют с интервалом 3— 5 сут, делая посевы с их концов.
9. Гипогликемию предупреждают непрерывным вливанием 5—10 % раствора декстрозы. Это нарушение можно не заметить, если не определять уровень глюкозы у коматозных пациентов в крови через каждые 2—3 ч.
10. Если концентрация глюкозы в крови падает ниже 60 мг/100 мл, ее немедленно корректируют вливанием 50 % раствора декстрозы, соответственно отрегулировав скорость введения.
11. Если с помощью растворов кристаллоидов или коллоидов не удается поддержать кровяное давление, можно ввести дофамин или при очень низком сосудистом сопротивлении дофамин с норадреналином.
12. Почечную недостаточность устраняют, проводя тщательный мониторинг объемов жидкости. Непрерывное вливание дофамина (2—4 мкг/кг в час) может обратить или замедлить поражение почек, увеличив в них кровоток.
13. Диализ или артериовенозная ультрафильтрация требуется, когда уровень креатинина в сыворотке превышает 400 мкмоль/л (4,5 мг/100 мл), а также при обычных показаниях, например при тяжелом метаболическом ацидозе, гиперкалиемии и перегрузке организма.
14. Гастродуоденальное кровотечение можно предупредить регулярными дозами Н2-антагонистов или омепразола, поддерживающими внутрижелу-дочковый рН выше 5.
Б. Печеночная энцефалопатия. Для лечения острой печеночной энцефалопатии обычно применяют лактулозу и отменяют белки в рационе. Из других средств используют метронидазол и неомицин.
В. Отек мозга. Мониторинг внутричерепного давления (ВЧД), по-видимому, помогает ориентировать терапию на профилактику грыжи ствола головного мозга, полезен при отборе пациентов для пересадки печени и проведении анестетического лечения во время последней процедуры.
- Осмотические диуретики. Если ВЧД превышает 30 мм рт.ст. на протяжении более 5 мин или в отсутствие мониторинга ВЧД наблюдаются клинические симптомы, заставляющие подозревать отек мозга, проводят быстрое внутривенное вливание 20 % раствора маннитола в дозе 1 г на 1 кг массы тела. Если осмолярность плазмы не превышает 320 мосм, вливание маннитола можно повторить.
У пациентов с почечной недостаточностью это средство надо применять только в сочетании с гемофильтрацией или ультрафильтрацией, чтобы избежать гиперосмолярности и перегрузки организма жидкостью.
- Барбитураты. Тиопентал (3—5 мг/кг) медленно вливают в течение 15 мин до исчезновения симптомов внутричерепной гипертензии или до достижения максимальной суммарной дозы 500 мг. Затем для поддержания ВЧД ниже 20 мм рт.ст. непрерывно с минимальной скоростью вливают тиопентон. Если клинические отклонения ВЧД не устраняются в течение 4 ч, вливание прекращают.
- Положение тела. В отсутствие мониторинга ВЧД пациенты с острой печеночной недостаточностью должны находиться с приподнятой головой под углом не более 30°. Гемоперфузия через активированный уголь Гемоперфузия через активированный уголь не повышает выживания по сравнению с уровнем, достигаемым при использовании одной лишь интенсивной терапии печени.
- Кортикостероиды. Кортикостероиды в плане как профилактики, так и активного лечения отека мозга при острой печеночной недостаточности бесполезны.
Г. Инфекция. Пациентам с острой печеночной недостаточностью для раннего выявления и адекватного лечения возможной бактериальной или грибковой инфекции необходимо тщательное ежедневное микробиологическое обследование. Полезно также профилактическое антимикробное лечение.
Д. Коагулопатия. При кровотечении или перед инвазивной процедурой рекомендуется свежезамороженная плазма.
Е. Гемодинамические аномалии и тканевая гипоксия. Введение циркулирующих сосудорасширяющих средств, например простациклина и N-ацетилцистеина, может предупредить развитие тканевой гипоксии у пациентов с острой печеночной недостаточностью, получающих сосудосуживающие средства.
Ж. Аппараты для поддержания функции печени. Для определения клинической эффективности экстракорпорального аппарата, поддерживающего функцию печени ("искусственная печень"), нужны дополнительные испытания.
З. Ортотопическая трансплантация печени (ОТП). Каждый пациент с острой печеночной недостаточностью должен как можно раньше, желательно еще при поступлении в больницу, пройти соответствующую оценку и быть внесенным в список на ОТП, даже если необходимость в ней пока вызывает сомнения.
- Трансплантация печени при отравлении бледной поганкой. Когда у пациента, отравившегося грибами рода Amanita, развивается печеночная кома, его шансы на выживание с использованием только терапевтического лечения минимальны. Ортотопическая трансплантация печени (ОТП) показана в следующих случаях:
1) прогрессирование энцефалопатии до II и более стадии;
2) удлинение протромбинового времени более чем в 2 раза по сравнению с нормой, несмотря на массивное вливание свежезамороженной плазмы;
3) уровень билирубина в сыворотке выше 25 мг/100 мл.
Прочим пациентам с такими симптомами, как ацидоз, гипогликемия, желудочно-кишечное кровотечение и гипофибриногенемия после выраженного повышения сывороточного уровня аминотрансфераз, также может быть показана срочная трансплантация печени еще до появления у них далеко зашедшей печеночной энцефалопатии, азотемии или желтухи.
К дополнительным критериям, говорящим о желательности ОТП после отравления грибами рода Amanita, относятся пиковое протромбиновое время менее 10 % (>100 с), концентрация фактора V ниже 10 %, лактат-ацидоз, желудочно-кишечное кровотечение и возраст менее 12 лет. Когда показана ОТП, риск интоксикации, обусловленной пересаженной печенью, по-видимому, отсутствует, поскольку спустя 4 дня циркулирующие аматоксины уже не выявляются.
Наблюдение за больными, которым может потребоваться ОТП, включает повторные клинические обследования, определение протромбинового времени, фактора V, рН, лактозы в крови, ЭЭГ и эхографию печени.
Ребенку в возрасте 4 лет, находящемуся в коме после потребления бледной поганки, через 70 ч с момента приема гриба сделана ОТП; через 24 ч он пришел в сознание.

Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Трансплантация или пересадка печени – частичная или полная замена пораженного органа реципиента (больного) здоровым донорским органом. Сегодня пересадка проводится как от мертвых, так и от живых доноров на платной или бесплатной основе.

Показания к пересадке
Трансплантация печени – радикальная мера, её назначают, когда терапевтическое лечение неэффективно.
Основные показания занесены в список национальных клинических рекомендаций:
- Рак печени. В сравнении с удалением опухоли, замена пораженного органа повышает выживаемость.
- Поликистоз. Множественное образование полостей с мертвыми клетками или жидкостью заменяет здоровую ткань, приводит к дисфункции органа. Если кисты вызваны вирусом, пересадка неэффективна.
- Муковисцидоз. Наследственное нарушение транспорта желчи, что приводит к замене желчных протоков соединительной тканью, атрофии печени и желчного пузыря.
- Печеночная недостаточность из-за отравления.
- Цирроз. Замена тканей печени фиброзной (прочной, неэластичной) соединительной тканью при гепатите С или из-за злоупотребления алкоголем. При циррозе не всегда разрешена пересадка, зависит от причины болезни.
- Билиарная атрезия – отсутствие или непроходимость желчных протоков у новорожденных. Основная причина детской трансплантации.
- Нарушение метаболизма. Заболевание Вильсона-Коновалова – накопление меди, атрофия тканей печени. Гемохроматоз – нарушение обмена железа, приводящее к дисфункции органа.
Донор печени
Донор печени – это человек, чей орган пересаживают живому, нуждающемуся пациенту. Выступить донором может живой или мертвый. В обоих случаях, помимо здоровой печени, не должно быть повреждений почек или желчных протоков.
От живого человека можно пересадить только часть железы, основные требования к донору:
- Возраст от 18, минимальный вес — 50 кг. Отсутствие беременности, если донор женщина.
- Желательно кровное родство до 4 колена включительно. Сюда входят внучатые племянники, бабушки, дедушки, тёти, дяди.
- Совместимость по группе крови. Желательно, по резус-фактору и тканевой принадлежности. Совместимость по всем параметрам даёт больше шансов на выздоровление.
- Отсутствие вирусных инфекций, перенесенных онкологических заболеваний и общее здоровье организма. Подтверждается анализами.
- Размер железы донора подходит по габаритам реципиенту.
Приоритет в трансплантации отдается печени от родственника. Орган приживется с большей вероятностью, и восстановление пройдет быстрее, так как на психологическом уровне такая пересадка переносится легче. Дополнительные преимущества – это сроки, трупную печень можно ждать до 2 лет.
От родного человека пересаживают левую часть печени: она больше по размерам и её легче изъять. Ребенку до 15 лет хватит половины этой части.
Мертвый донор – чаще это человек, умерший из-за черепно-мозговой травмы. Допустимый возраст от 2 месяцев до 55 лет. После смерти мозга, при совместимости с живым пациентом по группе крови и тканевой основе, орган изымают, помещают в стерильный контейнер и пересаживают не позже чем через 13-16 часов.
Для использования органов недавно умершего человека необходимо его прижизненное согласие на пересадку или разрешение родственников. Печень от мертвого донора можно пересадить сразу 2 пациентам: левую (большую) часть – взрослым, правую (меньшую) — детям.
Подготовка к операции
Перед пересадкой в клинике пациент проходит полное обследование, включающее в себя:
- Анализ крови на резус-фактор и группу.
- Томография брюшной полости.
- Серологический анализ на выявление ВИЧ, бруцеллеза, ЗППП или иных вирусных инфекций.
- УЗИ печени.
- Проба Манту.
- Электрокардиография.
- Заключение стоматолога.
- Заключение гинеколога.
- Сбор крови на случай обширного кровотечения во время ходе операции.
В течение полугода до операции (если она несрочная) пациент посещает нарколога и психиатра, придерживается здоровой диеты, ни в коем случае не употребляет алкоголь или табак.
В качестве предварительной медикаментозной подготовки прописывают:
- антигистаминные препараты – для предотвращения аллергических реакций;
- седативные препараты – для уменьшения эмоционального напряжения;
- препараты, снижающие артериальное давление;
- иммунодепрессанты – чтобы во время или сразу после операции организм не отторгнул орган, как чужеродное тело.
Как проходит ортотопическая трансплантация
Ортотопическая трансплантация печени – полное замещение органа реципиента на здоровый донорский орган или его часть. Пересадку выполняют хирург, гепатолог и анестезиолог, в особых случаях приглашают кардиолога и пульмонолога.

Операция по пересадке проходит в 3 этапа:
- Гепатэктомия – удаление собственной печени реципиента, длится от 2 до 4 часов. Если в ходе болезни орган утратил свою анатомическую конфигурацию или удалению предшествовали другие операции на печени, например, попытка желчеотведения при атрезии у детей, этап может затянуться. После удаления печени хирург сшивает сосуды и формирует обходной путь для венозной крови.
- Имплантация донорского органа и реваскуляризация (восстановление кровообращения) трансплантата. На этом этапе сосуды соединяют с новой печенью, проверяют состояние и цвет желчи.
- Восстановление желчных протоков. Печень пересаживают без желчного пузыря, после трансплантации хирург сшивает места соединения сосудов желчных протоков, дренирует открытую рану и зашивает полость.
Скорость операции зависит от координации бригад врачей: тех, кто изымает донорскую печень и тех, кто помещает её в организм пациента. Если донор и реципиент находятся в одной больнице, всю процедуру может проделать одна бригада. Операция длится от 12 до 20 часов.
Жизнь после операции
После успешной трансплантации пациента переводят в реанимацию на 3-7 дней.
Медикаментозная терапия после пересадки органа:
- Циклоспорин. Назначают курс иммуносупрессоров – препаратов для снижения действия антител на новый орган. Возможен пероральный прием до операции, после пересадки дозы вводят внутривенно около 7-10 дней.
- Метилпреднизолон и Азатиоприн. В случаях слабого функционирования почек.
- Такролимус. Назначают при отторжении печени.
Кровь регулярно проверяют на концентрацию лекарств. Если осложнений нет, пациента отпускают домой через 7-14 дней и назначают прием лекарств перорально.
Важно! Риск отторжения нового органа может остаться на всю жизнь, поэтому имунносупрессивную терапию продолжают не менее 5 лет.
Год после первой пересадки пациент придерживается диеты, чтобы уменьшить нагрузку на печень.
В список разрешенных продуктов входят:
- мясо на пару;
- овощи: свёкла, морковь, капуста, сладкий перец, тыква;
- фрукты: чернослив, виноград, яблоки;
- супы на овощном бульоне;
- овсянка, гречка и рис;
- ржаной хлеб.
В течение всего восстановления запрещается употреблять соленую, сладкую, жареную, острую пищу, жирные молочные продукты, алкоголь.
Важно! В 70% случаев после хорошо перенесенной операции, пациент будет жить более 5 лет. 87% детей восстанавливаются и нормально развиваются как физически, так и психологически.
Возможные осложнения
Осложнения после операции могут проявиться как у донора, так и у пациента.
Тяжелые последствия для донора
Внутреннее кровотечение или инфекция возникают менее чем в 1% случаев, они связаны с неаккуратной техникой забора органа. Уже через полгода печень восстановится до 85% начального объема.
Для реципиента
Помимо риска отторжения, возможны осложнения на протяжении от 1 до 26 недели после операции:
- 1-4 неделя: осложнения почечной, дыхательной и нервной систем, тромбоз печеночной артерии.
- 5-12 недели: вирусный гепатит С или гематит от CMV (из-за подавления иммунной системы).
- 13-26 недели: желчеистечение, клеточное отторжение, медикаментозный гепатит, рецидив исходного заболевания и тромбоз воротной вены.
Противопоказания к трансплантации
| Абсолютные | Относительные |
| 1. Активные, неизлечимый инфекционные заболевания (вирусный гепатит, туберкулез, ВИЧ). |
2. Онкология на стадии метастаза.
3. Неоперабельные нарушения внутренних органов: сердечная, дыхательная, почечная недостаточность.
4. Инфекции, локализованные в других органах.
2. Наличие ранних операций на органы брюшной полости.
3. Тромбоз воротной и брыжеечной вен.
4. Возраст более 60 лет.
5. Удаленная селезенка.
Где делают трансплантацию и сколько стоит?
Пересадку печени в России делают в институтах трансплантологии в Москве и Санкт-Петербурге, стоимость платной операции варьируется от 2,5 до 3 млн. рублей.

Важно! Официально граждане могут получить квоту на бесплатную пересадку. Однако тогда придется ждать очереди на сдачу анализов и саму операцию не менее года (если болезнь не смертельна). Ежегодно Минздравом выделяется ограниченное количество бесплатных трансплантаций, приоритет отдается тем, кто без донора не выживет.
Центры трансплантологии существуют по всему миру, больше всего операций проводят США, Германия, Израиль и Южная Корея. Средняя цена трансплантации в этих странах — 160-200 тыс. евро.
Строгая диета, употребление лекарств и регулярные обследования в трансплантологии – цена за здоровую печень и долгую жизнь. Не всегда можно дождаться операции по квоте, если есть шанс, лучше делать пересадку платно, чтобы не потерять драгоценные месяцы или годы здоровья.
Более 4% всех пищевых отравлений приходится на отравление поганками или грибами, ошибочно принятыми за съедобные. Несмотря на то, что показатель невысокий, пострадавшего могут ждать довольно серьезные последствия, в том числе и летальный исход. Что делать при первых признаках отравления грибами и растениями, как быстро помочь человеку, и, возможно, спасти ему жизнь?

Предотвращая неприятности
Классификация по признаку съедобности
Съедобные грибы. Готовятся без предварительной обработки. К ним относятся белые, маслята, шампиньоны, грузди, рыжики, сыроежки, лисички, моховики.
Условно съедобные. Перед приготовлением их нужно вымачивать, либо отваривать несколько раз, сливая воду, и заливая чистую. К данной категории относятся свинушки, волнушки, чернушки и другие.
Несъедобные. Эти грибы есть нельзя даже в том случае, если они вымочены и сварены сто раз. И после термической обработки такие грибы являются крайне ядовитыми. Одни из самых известных — это поганки, мухоморы, ложные опята и т.д.
Хранить, собранные грибы не зависимо от вида можно не более суток при температуре, не выше 10ºС. К тому же, даже съедобные грибы, на которых присутствует плесень или гниль автоматически переходят в разряд несъедобных.
Самые сложные отравления происходят из-за употребления в пищу бледной поганки, которую путают с шампиньоном или сыроежкой. Более 35% пострадавших не выживают. Лучше квалифицированных врачей о том, как лечить отравление бледной поганкой не знает никто. Поэтому чем быстрее поступит медицинская помощь, тем больше шансов на жизнь и дальнейшее здоровье у человека.
Важные симптомы отравления грибами
Отравление грибами — болезнь не просто неприятная, но и крайне опасная для здоровья и жизни пострадавшего. Важными симптомами, на которые следует обратить внимание после того, как человек поел гриб, стоит считать:
сильную тошноту и рвоту
резкие боли в области эпигастрия;
частый и очень жидкий стул (если отравление произошло бледной поганкой, возможны кровянистые выделения);
Читайте также:

