Перинатальный контакт по туберкулезу
Обновлено: 17.04.2024
Заражение туберкулезом может произойти в перинатальном периоде. Симптомы и проявления неспецифичны. Диагноз ставят на основании выделения возбудителя, а также при рентгенографии и биопсии. Лечение проводят противотуберкулезными препаратами.
Младенцы могут приобрести туберкулез (ТБ) следующими путями:
Трансплацентарное распространение через пупочную вену в печень плода
Аспирация или проглатывание зараженной амниотической жидкости
Заражение воздушно-капельным путем от тесных контактов (члены семьи или детский персонал)
Примерно у 50% детей, родившихся у матерей с активным легочным туберкулезом, в течение первого года жизни развивается заболевание, если не проводилась химиопрофилактика или не была проведена вакцинация бациллой Кальметта-Герена (БЦЖ).
Клинические проявления
Клинические проявления туберкулеза новорожденных являются неспецифическими, но обычно характеризуются вовлечением множества органов. Новорожденный может выглядеть больным острой или хронической формой, и у него могут развиться лихорадка, вялость, расстройство дыхания или резистентная пневмония, гепатоспленомегалия или нарушение быстрого роста.
Диагностика
Посев аспирата из трахеи, смывов из желудка, мочи и церепроспинальной жидкости (ЦСЖ)
Рентгенография грудной клетки
В некоторых случаях кожные тесты

Всем новорожденным с подозрением на врожденный туберкулез и детям, рожденным матерями с активной формой туберкулеза, нужно провести рентгенологическое исследование грудной клетки и посев аспиратов из трахеи, смывов из желудка и мочи на кислотоустойчивые микобактерии; следует провести люмбальную пункцию для определения количества клеток, глюкозы и белка, а также получить цереброспинальную жидкость (ЦСЖ) для посева. Плаценту нужно исследовать и предпочтительно сделать посев. Кожные пробы не являются очень чувствительными, особенно на начальном этапе, но должны быть сделаны. Специфичные для туберкулеза анализы высвобождения гамма-интерферона, которые пригодны для взрослых, не одобрены для использования у детей раннего возраста из-за низкой чувствительности. Проведение биопсии печени, лимфатических узлов, легких или плевры необходимо для подтверждения диагноза. Следует провести анализ на ВИЧ у младенца Диагностика Инфицирование вирусом иммунодефицита человека (ВИЧ) вызывает ретровирус ВИЧ-1 (реже родственный ретровирус ВИЧ-2). Инфекция приводит к прогрессирующему поражению иммунной защиты и частому развитию. Прочитайте дополнительные сведения .
Новорожденным без клинических проявлений и осложнений, чьи матери имеют положительный туберкулиновый кожный тест, отрицательную рентгенограмму грудной клетки и отсутствие признаков активного заболевания, нужно проводить тщательное наблюдение, а также обследовать всех членов семьи. Если новорожденный не контактировал с больными активным туберкулезом, он не нуждается в лечении или диагностике. Если в окружении новорожденного после родов имеется больной с активной формой туберкулеза, новорожденных нужно исследовать на подозревающийся туберкулез, как описано выше.
Здравый смысл и предостережения
Кожные пробы не являются очень чувствительными для перинатального туберкулеза, особенно на начальном этапе, но их следует проводить.
Лечение
При положительном кожном тесте или воздействии с высокой степенью риска назначают изониазид (INH)
При наличии туберкулеза следует добавить другие лекарственные средства (например, рифампицин, этамбутол, пиразинамид этионамид, аминогликозиды)
Лечение зависит от того, есть активный туберкулез или только положительный кожный тест (у матери и/или ребенка), который указывает на инфекцию без болезни.
Беременные с положительной туберкулиновой пробой
Женщин обследуют на наличие активного туберкулеза. Если активное заболевание исключено, применение изониазида может быть отложено до послеродового периода, потому что гепатотоксичность изониазида увеличивается во время беременности и потому, что риск заражения туберкулезом от матери с положительной туберкулиновой пробой выше для новорожденного, чем для плода. Тем не менее, если женщина недавно контактировала с человеком с открытой формой туберкулеза (в этом случае выгода перевешивает риск), лечение проводят в течение 9 месяцев, наряду с дополнительным назначением пиридоксина. Лечение беременной, контактировавшей с больным с активной формой туберкулеза, должно быть отложено до окончания первого триместра.
Новорожденные с положительной туберкулиновой пробой
При отсутствии клинических, лабораторных или рентгеновских признаков заболевания новорожденный должен получать изониазид в дозе 10-15 мг/кг перорально 1 раз/день в течение 9 месяцев, а также регулярно наблюдаться у врача. Новорожденные на исключительно грудном вскармливании должны получать пиридоксин в дозе 1-2 мг/кг 1 раз/день.
Беременные с активной формой туберкулеза
Изониазид, этамбутол, рифампицин в рекомендуемых дозах во время беременности не оказывали тератогенное действие на плод. Рекомендованная пероральная стартовая схема лечения в США включает: изониазид 300 мг внутрь, этамбутол 15–25 мг/кг (максимальная доза – 2,5 мг) и рифампицин 600 мг. Всем беременным и кормящим женщинам, получающим изониазид, также нужно назначать пиридоксин в дозе 25–30 мг внутрь. Все эти препараты можно назначить один раз в день. Рекомендуемая продолжительность терапии – не менее 9 месяцев; если возбудитель является лекарственно-резистентным, рекомендуется консультация инфекциониста, и, возможно, потребуется продление терапии до 18 месяцев.
Стрептомицин потенциально ототоксичен для развивающегося плода и его нельзя использовать на ранних сроках беременности, если только рифампицин не противопоказан. По возможности следует избегать применения других противотуберкулезных препаратов из-за их тератогенности (например, этионамида) или отсутствия опыта их клинического применения при беременности.
Грудное вскармливание не противопоказано матерям, получающим терапию и не являющимся контагиозными.
О больных с активными формами туберкулеза следует сообщать в местный отдел здравоохранения. Матерям с активной формой туберкулеза нужно провести исследование на ВИЧ-инфекцию.
Бессимптомные новорожденные, чьи матери или близкое окружение имеют активную форму туберкулеза
Новорожденных обследуют на наличие врожденного туберкулеза, как указанно выше, и обычно отделяют от матерей, только если эффективное лечение матери и новорожденного не реализуется в полной мере. Если врожденный туберкулез исключен и как только новорожденный начнет получать изониазид, отделение его от матери не является больше необходимым, за исключением случаев, когда мать (или бытовой контакт) заражена микобактериями с множественной лекарственной устойчивостью или плохо придерживается лечения (в том числе не носит маску при активном туберкулезе) и лечение под непосредственным наблюдением невозможно. Контактных лиц в семье нужно обследовать для выявления недиагностированного туберкулеза до того, как младенец вернется домой.
Если приверженность лечению может быть достаточно высока и в семье отсутствуют больные туберкулезом (т.е. мать находится на лечении и другие источники инфекции отсутствуют), новорожденному назначают лечение по схеме: изониазид 10-15 мг/кг перорально 1 раз/день – и выписывают домой в обычный срок. Младенцы на исключительно грудном вскармливании должны получать пиридоксин в дозе 1-2 мг/кг 1 раз/день.
Кожное тестирование необходимо провести в возрасте 3 или 4 месяцев. Если новорожденный является туберкулин-отрицательных и начальный инфекционный контакт имел удовлетворительный приверженность к лечению и имеет положительный ответ, применение изониазида останавливается. При положительном кожном тесте проводят рентгенографию грудной клетки и культуральное исследование на кислотоустойчивые микобактерии, как описано выше, и при исключении активного заболевания лечение изониазидом продолжают в общей сложности в течение 9 месяцев. Если культуральные тесты на туберкулез всегда дают положительные результаты, новорожденному нужно будет провести лечение активной формы туберкулеза.
(ВНИМАНИЕ: Вакцина БЦЖ противопоказана пациентам с иммуносупрессией и пациентам с подозрением на инфицирование ВИЧ. Тем не менее в группах высокого риска Всемирная организация здравоохранения [в отличие от Американской академии педиатрии] рекомендует, чтобы ВИЧ-инфицированные новорожденные без симптомов получали вакцину БЦЖ при рождении или вскоре после этого).
Новорожденные с активной формой туберкулеза
При врожденном туберкулезе Американская академия педиатрии (American Academy of Pediatrics) рекомендует лечение 1 раз/день с применением изониазида в дозе 10–15 мг/кг перорально, рифампицина в дозе 10–20 мг/кг перорально, пиразинамида 30–40 мг/кг перорально и аминогликозидов (например, амикацина—см. Таблица рекоммендованного дозирования некоторых аминогликозидов для новорожденных [Table Recommended Dosages of Select Aminoglycosides for Neonates] Рекомендованные дозировки некоторых аминогликозидов для новорожденных У новорожденных внеклеточная жидкость (ECF) составляет до 45% от общей массы тела, что требует введения относительно больших доз некоторых антибактериальных препаратов (например, аминогликозидов). Прочитайте дополнительные сведения ). Эта схема может быть изменена в соответствии с результатами оценки состояния ребенка. Пиридоксин назначают, если новорожденный находится исключительно на грудном вскармливании. Применения этамбутола, как правило, избегают, поскольку он приводит к токсическому поражению глаз, последствия которого невозможно оценить у новорожденных.
Для туберкулеза, заражение которым произошло после рождения, предлагается пероральная схема лечения, состоящая из приема 1 раз в день изониазида 10–15 мг/кг, рифампина 10–20 мг/кг и пиразинамида 30–40 мг/кг. Четвертый лекарственный препарат, такой как этамбутол 20-25 мг/кг перорально 1 раз/день, этионамид 7,5-10 мг/кг перорально 2 раза/день (или 5-6,67 мг/кг перорально 3 раза/день), или аминогликозиды следует дополнительно назначить, если подозреваются полирезистентность или туберкулезный менингит, или ребенок живет в районе, где распространенность ВИЧ среди больных туберкулезом составляет ≥ 5%. После первых 2 месяцев, лечения изониазид и рифампицин продолжают применять до завершения 6–12-месячного курса (в зависимости от стадии заболевания), а прием других препаратов прекращают. Младенцы на грудном вскармливании должны также получать пиридоксин.
При поражении центральной нервной системы (ЦНС) стартовая терапия туберкулеза также включает кортикостероиды (преднизон в дозе 2 мг/кг перорально 1 раз вдень [максимальная доза – 60 мг/день] в течение 4–6 недель, затем постепенно снижая). Терапия продолжается до тех пор, пока все признаки менингита не исчезнут и посевы не станут отрицательными (при 2 успешных ЛП с промежутком, как минимум, в 1 неделю). Затем терапию можно продолжить изониазидом и рифампицином 1 раз/день или дважды в неделю в течение следующих 10 мес. Кортикостероиды также могут рассматриваться для применения у младенцев и детей с тяжелым милиарным туберкулезом, плевральном или перикардиальном выпотами или эндобронхиальным туберкулезом, или с абдоминальный туберкулезом.
Туберкулез у младенцев и детей, если он не врожденный или диссеминированный, без поражения ЦНС, костей и суставов, вызван чувствительными к противотуберкулезным препаратам микроорганизмами, можно эффективно лечить курсом терапии в течение 6-9 месяцев. Возбудители, выделенные от ребенка или матери должны быть проверены на лекарственную чувствительность. Следует отслеживать наличие гематологических, печеночных и отологических симптомов для определения ответа на лечение и лекарственной токсичности. Частые лабораторные исследования обычно не являются обязательными.
Терапия под непосредственным наблюдением используется для улучшения самочувствия и успеха лечения. Многие антитуберкулезные препараты недоступны в педиатрических дозах. При возможности эти препараты детям должны выдаваться опытным персоналом.
Профилактика
Универсальное проведение вакцинации БЦЖ в развитых странах не проводиться рутинно, но может существенно уменьшить заболеваемость детским туберкулезом или снизить его тяжесть в популяциях, подверженных повышенному риску инфицирования.
Основные положения
Туберкулез может быть приобретен трансплацентарно, путем аспирации инфицированной амниотической жидкости или воздушно-капельным путем после рождения.
Проявления неонатального туберкулеза являются неспецифическими, но вовлекаются, как правило, множественные органы (включая легкие, печень, и/или центральная нервная система).
Следует провести рентгенографию органов грудной полости, культуральное исследование аспирата из трахеи, смывов из желудка, мочи и церепроспинальной жидкости.
Назначайте изониазид (INH) при положительном кожном тесте или контакте с высокой степенью риска.
При активной форме туберкулеза необходимо добавить другие препараты (например, рифампицин, этамбутол, пиразинамид, этионамид, аминогликозиды).
Туберкулез у беременных — это специфическое инфекционное заболевание с преимущественной деструкцией ткани легких, вызванное микобактериями туберкулезного комплекса, возникшее до, во время или сразу после гестации. Проявляется слабостью, потливостью, ухудшением аппетита, снижением веса, субфебрилитетом, кашлем, кровохарканьем, одышкой, болями в области грудной клетки. Диагностируется с помощью туберкулиновых проб, обзорной рентгенографии легких, микроскопии и бакпосева биологических материалов. Для лечения применяют производные этиленамидов, изоникотиновой кислоты, ансамицинов. При осложнениях возможно проведение торакальных и коллапсотерапевтических вмешательств.
МКБ-10
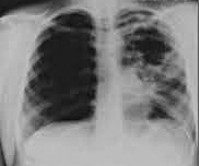
Общие сведения
Несмотря на внедрение современных методов экспресс-диагностики и успехи комплексной медикаментозной терапии, туберкулезная инфекция остается одной из наиболее распространенных в мире. Заболеваемость туберкулезом в России стабилизировалась и даже начала снижаться, однако частота поражения инфекционным процессом беременных женщин продолжает в 1,5-2 раза превышать аналогичный показатель в общей женской популяции. До 70% пациенток заражаются микобактериями в возрасте 25-34 лет.
Распространенность заболевания составляет 3-7 случаев туберкулеза на 10 тысяч родов. У 78% беременных поражение является односторонним, у 58% больных диагностируются инфильтративные формы процесса, в 18% случаев туберкулез определяется на стадии распада. До 2/3 женщин являются бактериовыделителями. Зачастую патология сочетается с другими специфическими процессами: у 15% заболевших определяется ВИЧ-инфекция, у 10% — сифилис, у 4% — вирусные гепатиты.

Причины
Возбудителями инфекционно-воспалительного процесса являются микроорганизмы из семейства микобактерий. У большинства пациенток высеивается Mycobacterium tuberculosis (палочка Коха). Намного реже заболевание вызывают другие представители микобактерийного туберкулезного комплекса — M. africanum, M. bovis, M. caprae, M. microti, M. pinnipedii, часть из которых поражает некоторых животных (крупный и мелкий рогатый скот, ластоногих, птиц, грызунов). В большинстве случаев туберкулез передается воздушно-капельным путем, иногда заражение является алиментарным (при употреблении непастеризованного молока от туберкулезных коров).
По результатам наблюдений большинства исследователей в сфере фтизиатрии, гестация неблагоприятно влияет на течение инфекционного процесса, вызывая его развитие или обострение. У беременных возможно как первичное возникновение заболевания в результате контактов с выделителем микобактерий, так и активация существующего туберкулезного очага. Наиболее часто предпосылками к началу патологического процесса становятся асоциальное окружение, низкий материальный уровень, недостаточное питание, злоупотребление спиртным, неспецифические болезни органов дыхания, обусловленные курением. Однако ряд физиологических изменений, происходящих при беременности и после родов, способствует развитию туберкулеза у социально благополучных женщин. Основными из провоцирующих факторов являются:
- Изменение клеточного иммунитета. Иммунные процессы, происходящие в организме беременной, направлены не только на защиту ребенка и женщины от возможного инфицирования, но и на предотвращение отторжения плода как чужеродного тела. При гестации существенно снижается функциональная активность Т-лимфоцитов, обеспечивающих элиминацию микобактерий.
- Активный расход кальция. Этот микроэлемент в больших количествах требуется для построения костной системы плода, что приводит к его усиленному вымыванию из тканей пациентки. В результате старые кальцинированные очаги туберкулеза размягчаются, что потенцирует реактивацию или обострение патологического процесса у ранее инфицированных больных.
- Послеродовая абдоминальная декомпрессия. Временное улучшение состояния в 3 триместре, вызванное высоким стоянием диафрагмы, после родов сменяется быстрым бронхогенным обсеменением легких. Этому способствует деструкция очагов туберкулеза при резком снижении внутрибрюшного давления с аспирацией казеозных масс в ранее здоровые отделы легких.
- Грудное вскармливание. Секреция молока сопровождается высоким расходом белка, жиров, витаминов. Дефицит питательных веществ снижает резистентность к туберкулезу. Одновременно с этим могут активироваться старые очаги из-за вымывания кальция. Особо значимыми эти факторы становятся при пребывании родильницы в плохой социально-эпидемиологической обстановке.
По мнению специалистов в сфере акушерства, дополнительными предпосылками к развитию заболевания являются мобилизация всех систем у беременных, гормональная перестройка за счет функционирования плаценты. Группу риска составляют пациентки с впервые диагностированным виражом проб на туберкулин, имеющие контакт с бактериовыделителем, страдающие тяжелой экстрагенитальной патологией (сахарным диабетом, ХОБЛ, неспецифическим пиелонефритом, язвенной болезнью желудка или двенадцатиперстной кишки). Вероятность возникновения туберкулеза повышается при длительном приеме кортикостероидов, цитостатиков, иммунодепрессантов, наличии вторичных иммунодефицитных состояний, в том числе ВИЧ-инфекции.
Патогенез
Механизм развития туберкулеза у беременной не отличается от патофизиологических изменений при туберкулезном процессе вне периода гестации. Первичное проникновение микобактерий сопровождается формированием специфического очага воспаления. В ответ на действие микроорганизма и его токсинов альвеолярные макрофаги выделяют интерлейкины и фактор некроза опухоли, потенцирующие пролиферацию T-лимфоцитов — иммунных клеток, которые играют ключевую роль в защите от возбудителя туберкулеза.
Реакция клеточного иммунитета и накопление в очаге поражения активированных макрофагов способствует образованию туберкулезной гранулемы. В специфический процесс вовлекаются внутригрудные лимфоузлы. Одновременно проникновение микобактерий стимулирует синтез плазменных антител. При адекватной защитной реакции очаг первичного туберкулеза заживает и кальцинируется. Снижение иммунитета становится причиной реактивации инфекции с дальнейшим распространением процесса.
Классификация
Точное определение варианта заболевания позволяет выработать оптимальную стратегию ведения беременности. Основными критериями, которые учитывают при систематизации болезни, являются время возникновения (первичный, вторичный туберкулез), фаза развития (инфильтрация, распад, обсеменение, рубцевание и др.), локализация процесса и его протяженность (легочной, внелегочной), наличие или отсутствие бактериовыделения (МБТ+, МБТ-), терапевтическая резистентность возбудителя, осложнения и остаточные явления. Для прогнозирования исхода беременности особенно важно учитывать клиническую форму болезни. У беременных может развиваться:
- Легочный туберкулез. Наиболее распространенный вариант заболевания в гестационном периоде. Противопоказаниями для пролонгации беременности служат фиброзно-кавернозная и кавернозная формы инфекции, хронический процесс с диссеминацией и цирротический туберкулез, осложненные легочно-сердечной недостаточностью. Гестацию также рекомендуется прервать при впервые диагностированном прогрессирующем инфильтративном туберкулезе легких с распадом.
- Внелегочной туберкулез. Специфическое воспалительное поражение микобактериями других органов у беременных наблюдается крайне редко. В казуистических случаях инфекционный процесс локализуется в кишечнике, брыжеечных лимфоузлах, брюшине, костях, суставах, ЦНС, мочевыводящих органах. Опасность в плане развития гестозов и других акушерских осложнений представляет туберкулез почек, осложненный хронической почечной недостаточностью I-III степени.
Симптомы туберкулеза у беременных
Клинические проявления заболевания, возникшего или рецидивировавшего на фоне беременности, неспецифичны. Слабость, недомогание, ухудшение аппетита, снижение веса, субфебрилитет, потливость и другие характерные признаки туберкулезной инфекции в I триместре беременности зачастую расцениваются как физиологические изменения или ранний токсикоз. Высокое стояние диафрагмы в III триместре вызывает лечебный эффект, подобный возникающему при пневмоперитонеуме. В результате типичная симптоматика даже распространенных инфильтративных и казеозно-деструктивных форм туберкулеза практически не проявляется. Наличие инфекции можно заподозрить на основании жалоб на длительный (более 3 недель) кашель с мокротой или без нее, кровохарканье, одышку, боли в грудной клетке.
Осложнения
У 54% беременных с туберкулезом течение беременности является осложненным. На фоне интоксикации, влияющей на секреторную функцию надпочечников, увеличивается частота анемий, ранних токсикозов, поздних гестозов. Нарушение легочной вентиляции и оксигенации крови сопровождается фетоплацентарной недостаточностью с возможной задержкой развития плода. Снижение прочности плодных оболочек, связанное с инфекционным воздействием, приводит к преждевременному излитию околоплодных вод. Микобактерии могут передаваться плоду через пуповину или амниотическую жидкость. В первом случае первичные туберкулезные очаги формируются в печени, во втором — в различных органах. У части пациенток отмечается бурная родовая деятельность за счет повышения активности миометрия под действием накопившей молочной кислоты. Натуживание и усиленное дыхание в период изгнания увеличивают риск возникновения спонтанного пневмоторакса и легочного кровотечения.
Хотя у большинства женщин с туберкулезной инфекцией послеродовый период протекает без осложнений, абдоминальная декомпрессия, обессиливание и кровопотеря в родах могут обострить инфекционный процесс с развитием милиарного туберкулеза, туберкулезного менингита. Несвоевременная диагностика и отсутствие адекватного лечения повышает смертность от заболевания на первом году после родов до 15-18%. 12% новорожденных от матерей с туберкулезом легких имеют признаки гипотрофии и хуже набирают массу тела после рождения. В результате гипоксического поражения мозга у них чаще наблюдаются дыхательные расстройства, изменения со стороны ЦНС.
Диагностика
Сложность своевременного диагностирования туберкулеза у беременных обусловлена неспецифичностью клинической картины, скудностью данных физикального обследования, ограниченным применением традиционного рентгенологического скрининга во время гестации. Рекомендованными методами исследований при подозрении на наличие у пациентки туберкулезной инфекции являются:
- Кожная туберкулиновая проба. Методика считается безопасной и информативной. Показана всем больным из группы риска при отсутствии сведений о недавнем проведении исследования и его результатах. Индурация более 10 мм в месте внутрикожного введения препарата или вираж пробы подтверждает заражение туберкулезом.
- Микробиологическое исследование. Для выявления микобактерий в мокроте, промывных водах бронхов применяют микроскопию и культуральный посев. Забор материала с последующим бактериоскопическим и бактериологическим анализом выполняется три дня подряд. При возможном туберкулезе почек изучается моча.
- ПЦР-исследование мокроты. Высокочувствительный и специфичный метод диагностики дает возможность обнаружить в биологическом материале единичные клетки и фрагменты ДНК возбудителя заболевания. При необходимости исследуются промывные воды бронхов, биоптаты, другие среды, в которых могут содержаться микобактерии.
- Иммунологические тесты крови. Факт наличия в организме скрытой или активной тубинфекции возможно подтвердить с помощью современных иммуноферментных анализов: интерферонового теста и теста Т-спот. Однако осуществить топическую диагностику инфекционного процесса с помощью этих методов нельзя.
- Рентгенография легких. Рентгенологическое исследование беременной выполняется в прямой проекции, что позволяет снизить возможную лучевую нагрузку на плод в 10 раз. Еще более безопасным считается обследование с использованием прорезиненного защитного фартука или выполненное на цифровых малодозных установках.
Косвенным подтверждением диагноза служат изменения в общем анализе крови (ускорение СОЭ, повышение уровня лейкоцитов с увеличением количества нейтрофилов, сдвигом лейкоцитарной формулы влево и снижением содержания лимфоцитов преимущественно за счет Т-хелперов), повышенная концентрация белка и гиперглобулинемия в плазме крови, уменьшение активности иммуноглобулинов (IgA, IgM). Для исключения внелегочного туберкулеза возможно проведение МРТ, УЗИ, инвазивных эндоскопических исследований с получением биоптата. Дифференциальная диагностика осуществляется с очаговой пневмонией, новообразованиями бронхов и легких.
Лечение туберкулеза у беременных
Дородовое сопровождение пациентки обеспечивают акушер-гинеколог и фтизиатр. Первой задачей после диагностики туберкулезной инфекции является решение вопроса о возможности пролонгации беременности. В настоящее время перечень показаний для искусственного прерывания гестации ограничен прогрессирующими деструктивными формами заболевания, активным костно-суставным туберкулезом и двухсторонним поражением почек с признаками их функциональной недостаточности. Медаборт обычно выполняется до 12-недельного гестационного срока. Более позднее прерывание беременности чревато обострением и быстрым прогрессированием туберкулеза.
Беременные, решившие вынашивать ребенка, трижды планово госпитализируются в стационар (до 12 недели, на 30-36 неделях и за 1-4 недели до родов), а в остальное время наблюдаются и лечатся в туберкулезном диспансере. Основными задачами терапии являются купирование активного инфекционного процесса, прекращение бактериовыделения, предупреждение легочных кровотечений, дыхательной недостаточности, акушерских осложнений. Пациенткам показано оздоровление в профильных санаториях, фитотерапия, богатая белком пища. Медикаментозное лечение проводится в 2 этапа — бактерицидный, длящийся 2 месяца, и 4-месячный стерилизующий. Выбор препаратов для химиотерапии туберкулеза ограничен лекарственными средствами, оказывающими минимальное воздействие на плод. Чаще всего беременным назначают так называемые медикаменты 1-го ряда:
- Производные изоникотиновой кислоты. За счет ингибирования ДНК-зависимой РНК-полимеразы и торможения синтеза миколевых кислот клеточной мембраны оказывают выраженный бактериостатический эффект на микобактерии туберкулеза. В связи с проникновением через плаценту обычно применяются в сочетании с витамином В6 или в виде лекарственной формы, содержащей в составе железо.
- Синтетические производные этилендиаминов. Препараты обладают крайне низкой токсичностью. Фактов, свидетельствующих об их тератогенном воздействии, не обнаружено. Действуют бактериостатически на интенсивно размножающиеся микроорганизмы. Нарушают липидный обмен микобактерий, структуру их рибосом и синтез белка. Используются в комбинированных схемах лечения.
- Ансамицины. Полусинтетические антибиотики этой группы подавляют синтез РНК микобактерией, благодаря чему обладают выраженным бактерицидным действием. Воздействуют на резистентные формы микроорганизмов. Еще более эффективны спиропиперидильные производные ансамицинов. Поскольку средства способны повысить тонус миометрия, в 1-м триместре они практически не назначаются.
Торакопластику, торакостомию, плеврэктомию, оперативную коллапсотерапию и другие хирургические вмешательства проводят только по жизненным показаниям при осложненном течении туберкулеза, выявлении прогрессирующей туберкуломы, деструктивных вариантах заболевания с бактериовыделением. На этапе предоперационной подготовки клинико-экспертной комиссии зачастую приходится решать вопрос о прерывании беременности. При эффективной консервативной терапии гестацию рекомендуется завершать естественными родами с применением обезболивания и спазмолитиков. Родоразрешающие операции (накладывание вакуум-экстрактора, акушерских щипцов) и кесарево сечение выполняются только при наличии соответствующих акушерских показаний (преждевременной отслойки нормально расположенной плаценты, гипоксии ребенка, клинически узкого таза, предлежания плаценты, поперечного положения плода).
Прогноз и профилактика
Еще недавно туберкулез принадлежал к числу наиболее частых медицинских показаний к прерыванию гестации. В наши дни своевременное выявление, систематическое наблюдение, комплексное лечение позволяют большинству женщин с диагностированным мелкоочаговым, ограниченным фиброзно-очаговым, гематогенно-диссеминированным легочным туберкулезом без риска выносить здорового ребенка. Профилактика предполагает планирование гестации пациентками, ранее перенесшими туберкулезную инфекцию, обязательный скрининг заболевания у родственников беременных. Рекомендовано рациональное питание с достаточным количеством белковых продуктов, отказ от курения и злоупотребления спиртным, ограничение тяжелых физических нагрузок и стрессов. Новорожденным с профилактической целью показана вакцинация БЦЖ. Кормление грудью допускается только при неактивном туберкулезе.
2. Анализ течения и исходов туберкулеза и беременности при их сочетании у пациенток репродуктивного возраста/ Яковлева А.А., Мордык А.В., Жукова Н.В., Антропова В.В., Леонтьев В.В., Николаева И.И.// Сибирское медицинское обозрение. – 2012.
3. Особенности течения туберкулеза на фоне беременности/ Мордык А.В., Кравченко Е.Н., Валеева Г.А., Пузырева Л.В.// Кубанский научный медицинский вестник. – 2014.

Туберкулез (ТБ) является хронической прогрессирующей микобактериальной инфекцией, часто имеющей латентный период после начального инфицирования. Чаще всего ТБ поражает легкие. Симптомы включают в себя кашель, повышение температуры, потерю веса и недомогание. Диагностика чаще всего проводится по результатам анализа мокроты и бактериальных посевов, и, все чаще, благодаря применению диагностических молекулярных экспресс-тестов. Лечение проводят антибактериальными лекарственными средствами в течение, по крайней мере, 6 мес.

Микобактерии являются небольшими, медленно растущими аэробными бациллами. Они отличаются сложной, богатой липидами клеточной оболочкой, обусловливающей их кислотостойкость (т.е. устойчивость к обесцвечиванию кислотой после окрашивания карбол-фуксином) и их относительную устойчивость к окрашиванию по Граму. Наиболее распространенная микобактериальная инфекция – туберкулез; другие включают проказу Проказа Лепра – хроническая инфекция, обычно вызываемая кислотоустойчивой бациллой Mycobacterium leprae, которая обладает уникальным тропизмом к периферическим нервам, коже и слизистым оболочкам. Прочитайте дополнительные сведения и различные микобактериальные инфекции, которые напоминают туберкулез Нетуберкулёзные микобактериальные инфекции Другие микобактерии, кроме туберкулезной палочки, иногда заражают людей. Эти возбудители (называемые нетуберкулезными бактериями) обычно присутствуют в почве и воде и являются намного менее. Прочитайте дополнительные сведения , такие как вызванные комплексом Mycobacterium avium.
Туберкулез является ведущей инфекционной причиной заболеваемости и смертности среди взрослых во всем мире; болезнь является причиной смерти приблизительно 1,7 миллиона человек в 2016 году, преимущественно в странах с низким и средним уровнем дохода. ВИЧ/СПИД – наиболее важный предрасполагающий фактор к инфицированию туберкулезом и смертности в некоторых регионах мира, где распространены обе инфекции.
Этиология туберкулеза
К туберкулезу правильно относить только болезнь, вызванную Mycobacterium tuberculosis (для которой люди являются основным резервуаром). Аналогичная болезнь иногда развивается в результате инфицирования тесно связанных микобактерий, а именно M. bovis, M. africanum, и M. microti, которые вместе с M. tuberculosis известны как комплекс Mycobacterium tuberculosis.
Заражение туберкулезом происходит, как правило, воздушно-капельным путем через частицы (каплеобразные ядра), содержащие M. tuberculosis. Они передаются прежде всего при кашле, пении и других дыхательных движениях людьми, которые больны активным туберкулезом легких или гортани и в чьей слюне содержится значительное количество возбудителя (достаточное, как правило, чтобы получить положительный мазок). Люди с легочными полостными кавернами являются особо заразными из-за большого количества бактерий, содержащихся в каверне.
Капли (частицы размером
Контагиозность пациентов с нелечённой активной формой туберкулеза легких широко варьируется. Некоторые штаммы M. tuberculosis являются более заразными, и пациенты с положительными результатами бактериоскопии мазков мокроты являются более заразными, чем имеющие положительные результаты только бактериального посева. Пациенты с кавернами (которые тесно связаны с микобактериальной нагрузкой в мокроте) являются более заразными, чем не имеющие их.
Также важную роль играют факторы окружающей среды. Таким образом, люди, живущие в бедности или в специальных учреждениях, находятся в условиях особого риска. Передача инфекции возрастает при частом или длительном контакте с не вылеченными пациентами, которые рассеивают большие количества туберкулезных палочек в переполненных, закрытых, плохо проветриваемых помещениях. Практикующие врачи, у которых есть тесный контакт с активными случаями, также являются группой повышенного риска.
Таким образом, оценки контагиозности широко варьируют; некоторые исследования показывают, что только 1 из 3 пациентов с невылеченным туберкулезом легких инфицирует кого-либо при тесном контакте. Однако по оценкам ВОЗ каждый невылеченный пациент может заразить от 10 до 15 человек в год. Тем не менее, у большинства инфицированных лиц активное заболевание не развивается.
Контагиозность быстро уменьшается сразу после начала эффективного лечения. Возбудители становятся менее заразными, даже при условии их сохранности в мокроте, а интенсивность кашля уменьшается. Исследования бытовых контактов показывают, что контагиозность пациентов прекращается в течение 2 недель после начала эффективного лечения.
Намного реже заражение происходит при аэрозолизации организмов после промывания инфицированных ран, работе в микобактериологических лабораториях или в секционных залах.
Туберкулёз миндалин, лимфатических узлов, органов брюшной полости, костей и суставов ранее вызывало употреблением в пищу молока или молочных продуктов (например, сыра), загрязненных M. bovis, но этот путь передачи был в значительной степени ликвидирован в развитых странах путем убоя коров, имеющих положительный результат теста на кожную туберкулиновую пробу, и пастеризацией молока. Туберкулез, вызываемый M. bovis, все еще встречается в развивающихся странах и у иммигрантов из развивающихся стран, где бычий туберкулез является эндемичным (например, некоторые латиноамериканские страны). Растущая популярность сыра из непастеризованного молока вызывает новые проблемы, особенно, если сыры прибывают из стран, имеющих проблемы с бычьим туберкулезом (например, Мексика, Великобритания).
Эпидемиология туберкулеза
Около четверти населения всего мира инфицированы (на основе результатов исследований кожных туберкулиновых проб). Из всех инфицированных, вероятно, только у 15 миллионов в данный момент времени диагностируется активная форма заболевания.
Уровни инфицированности (для туберкулеза, поддающегося лечению лекарствами) и смертности уменьшаются. Количество новых случаев снизилось на 1,5% в период между 2014 и 2015 гг., увеличивая тенденцию, которая отмечается в течение нескольких лет. Эти тенденции, скорее всего, частично связаны со всемирными усилиями по борьбе с туберкулезом, которые предоставили большему количеству людей доступ к лекарственным средствам против туберколеза и ВИЧ-инфекции.
Всплеск заболеваемости туберкулезом произошел в отдельных частях США и других развитых странах между 1985 и 1992 г.; это было связано с несколькими факторами, включая параллельное инфицирование ВИЧ, бездомность, ухудшенную инфраструктуру здравоохранения и появление мультирезистентного туберкулеза (MDR-TB). Несмотря на то, что контроль в США осуществляется эффективной системой здравоохранения и установленными мерами по инфекционному контролю в закрытых учреждениях, проблема мультирезистентного туберкулеза, включая туберкулез с широкой лекарственной устойчивостью (ШЛУ-TБ), является актуальной во всем мире. Эта ситуация усиливается нехваткой ресурсов, в том числе систем диагностики и доставки лекарственных средств.
В большинстве стран мира туберкулез с лекарственной устойчивостью не может быть быстро диагностирован и своевременно вылечен с использованием эффективных схем, в том числе с надлежащим контролем побочных эффектов лекарственных средств 2-ой линии. Эта ситуация приводит к продолжающейся контагиозности, низкому уровню излечения и формированию усиленной резистентности возбудителей. При лечении очень стойкого к препаратам туберкулеза эффективность терапии еще ниже, а смертность, напротив, значительна, особенно у пациентов, инфицированных ВИЧ, даже если они получают лечение антиретровирусными препаратами. Эффективное лечение и контроль нежелательных реакций, работа с населением, а также социальная поддержка привели к более благоприятным эпидемиологическим тенденциям снижения туберкулеза с лекарственной устойчивостью в некоторых областях (например, Перу, Томская область России). Индия и Китай только начинают реализовывать общенациональные программы по лечению МЛУ-ТБ, и заболеваемость МЛУ-ТБ в будущем может в значительной степени зависеть от успеха или неудачи этих программ.
Ссылки на эпидемиологию
1. WHO: Global Tuberculosis Report 2017: Executive Summary. Accessed on 4/5/18.
2. WHO: Tuberculosis Fact Sheet, 2017. Accessed on 4/5/18.
Патофизиология туберкулеза
Туберкулез может протекать в трех стадиях:
Туберкулезные палочки M. tuberculosis изначально вызывают первичную инфекцию, которая редко приводит к острому заболеванию. Большинство (приблизительно 95%) первичных инфекций являются бессимптомными и сопровождаются скрытой (латентной) фазой. В некоторых случаях латентные инфекции впоследствии проявляются клиническими признаками и симптомами заболевания.
Инфекция обычно не передается в начальной стадии и никогда не является контагиозной в латентном периоде.
Первичное инфицирование
Инфицирование происходит, когда вдыхаемые частицы достаточно малы и могут преодолеть защитные барьеры верхних дыхательных путей, осесть глубоко в легких, как правило, в субплевральном воздушном пространстве средних или нижних долей. Капельки большего размера склонны осаждаться в верхних отделах дыхательных путей и, как правило, не приводят к заболеванию. Заражение, как правило, начинается с одного капельного ядра, которое обычно несет несколько возбудителей. Теоретически, достаточно только одного организма, чтобы вызвать инфекцию у восприимчивых людей, но менее восприимчивым людям может потребоваться для развитие инфекции многократный контакт.
Для развития инфекции бациллы M. tuberculosis должны поглотиться альвеолярными макрофагами. Туберкулезные палочки, которые не обезврежены макрофагами, фактически воспроизводятся в них, в конечном счете убивая макрофага хозяина (с помощью лимфоцитов CD8); клетки, вызывающие воспаление, привлекаются в такую область, вызывая очаговый пневмонит, срастающийся в характерную туберкулезную гранулему, которая определяется гистологическими методами.
В первые недели инфекции некоторые зараженные макрофаги мигрируют к расположенным рядом лимфоузлам (воротные, средостенные), где они получают доступ к кровотоку. Возбудители могут распространиться через кровь к любой части тела, особенно апикально-задней части легких, эпифизу длинных костей, почкам, телу позвонков и мягким мозговым оболочкам. Гематогенная диссеминация менее вероятна у пациентов с частичным иммунитетом, являющимся результатов вакцинации или предварительного естественного инфицирования M. tuberculosis или микобактериями в окружающей среде.

В большинстве случаев после первичной инфекции развивается латентная инфекция. Примерно в 95% случаев, приблизительно через 3 недели активного роста микобактерий, иммунная система начинает подавлять размножение бацилл еще до того, как появляются клинические симптомы и признаки. Очаги с бациллами в легких или других органах преобразуются в эпителиоидные клеточные гранулемы, имеющие казеозные и некротические центры. Туберкулезные палочки могут выживать в этом материале в течение многих лет; баланс между резистентностью хозяина и вирулентностью микроба определяет, пройдет ли инфекция в конечном счете без лечения, останется скрытой или станет активной. Инфекционные очаги могут оставить фиброзно-очаговые шрамы на вершинах одного или обоих легких (очаги Симона, которые, как правило, являются результатом гематогенного посева с другого инфицированного участка) или небольших областей консолидации (очаги Гона). Очаг Гона с вовлечением лимфатических узлов является комплексом Гона, который при условии кальцинирования называют комплексом Ранке. Туберкулиновый кожный тест Кожные пробы Туберкулез (ТБ) является хронической прогрессирующей микобактериальной инфекцией, часто имеющей латентный период после начального инфицирования. Чаще всего ТБ поражает легкие. Симптомы включают. Прочитайте дополнительные сведения и анализ крови, основанный на высвобождении gamma -интерферона (IGRA IGRA (анализ, основанный на высвобождении гамма-интерферона) Туберкулез (ТБ) является хронической прогрессирующей микобактериальной инфекцией, часто имеющей латентный период после начального инфицирования. Чаще всего ТБ поражает легкие. Симптомы включают. Прочитайте дополнительные сведения ), становятся положительными в течение латентной стадии инфекции. Участки латентной инфекции являются динамическими процессами, они не находятся в состоянии покоя, как когда-то считалось.
Гораздо реже первичное поражение быстро прогрессирует, вызывая острую болезнь с пневмонией (иногда кавернозной), плевральным выпотом и явным увеличением лимфоузлов в области средостения или корня легких (у детей это может привести к сдавлению бронхов). Небольшие плевральные выпоты являются преимущественно лимфоцитарными, как правило, содержат немного микобактерий и очищаются в течение нескольких недель. Такое развитие событий более характерно для маленьких детей и недавно зараженных или повторно зараженных пациентов с ослабленным иммунитетом.

Внелегочный туберкулез Внелегочный туберкулез (ТБ) Внелегочный туберкулез обычно является следствием гематогенного распространения возбудителя. Иногда инфекция передается непосредственно от смежного органа. Симптоматика меняется в зависимости. Прочитайте дополнительные сведения с вовлечением любого органа может проявляться без признаков поражения легких. Увеличение лимфатических узлов при туберкулезе – наиболее распространенное внелегочное проявление; однако менингит – наиболее тяжелое и опасное состояние из-за высокой летальности у очень молодых и очень пожилых людей.
Активная болезнь
У здоровых людей, инфицированных туберкулезом, на протяжении жизни вероятность риска перехода заболевания в активную форму составляет приблизительно 5–10%, хотя этот процент значительно меняется в зависимости от возраста и других факторов риска.
У 50–80% заразившихся лиц туберкулез активно развивается в течение первых 2 лет, хотя он также может проявиться и через несколько десятилетий.
Любой орган, первоначально инфицированный возбудителем, может стать источником реактивации инфекции, но чаще всего она начинается в верхушках легких, по-видимому, из-за благоприятных для микроба условий, таких как высокое давление кислорода. Очаги Гона и пораженные прикертневые лимфоузлы гораздо реже становятся местами такой реактивации.

Условия, разрушающие клеточный иммунитет (что очень важно для защиты от туберкулеза), значительно облегчают реактивацию. Таким образом, среди пациентов, которые имеют ко-инфекцию ВИЧ Инфекция, вызванная вирусом иммунодефицита человека (ВИЧ) Инфекция вирусом иммунодефицита человека (ВИЧ) вызывается одним из 2 похожих ретровирусов (ВИЧ-1 и ВИЧ-2), которые разрушают CD4+ лимфоциты и ослабляют клеточный иммунитет, увеличивая риск оппортунистических. Прочитайте дополнительные сведения и не получают соответсвующую АРТ, наблюдается почти 10% ежегодный риск развития активного заболевания.
Другие условия, способствующие реактивации, но в меньшей степени, чем ВИЧ-инфекция, включают
Туберкулез — инфекционное заболевание, вызываемое различными микобактериями (МБТ) — M.humanus, M.bovis, M.avium. Однако и другие виды микобактерий могут вызывать заболевание, которое принято называть микобактериозами. Микобактериоз может разв
 |
Туберкулез — инфекционное заболевание, вызываемое различными микобактериями (МБТ) — M.humanus, M.bovis, M.avium. Однако и другие виды микобактерий могут вызывать заболевание, которое принято называть микобактериозами. Микобактериоз может развиваться при заражении M.xenopi, M.kasasii, M.ulcerans и др.
Сегодня можно констатировать, что туберкулез поражает все слои общества, все возрастные группы и особенно опасен для детей первых трех лет жизни. По нашему мнению, при инфицировании ребенка на первом году жизни практически в 100% случаев развивается заболевание.
Наряду с ростом заболеваемости значительно возросло число осложненных форм туберкулеза у детей (особенно раннего возраста), что является следствием его поздней выявляемости.
Дети чаще всего заражаются микобактериями человеческого типа от взрослых членов семьи, обычно от близких родственников. В сельской местности, неблагополучной по туберкулезу крупного рогатого скота, происходит заражение младенцев от животных (употребление парного молока) микобактерией бычьего типа.
Преимущественно МБТ проникает в организм человека аэрогенным путем при ингаляции мельчайших капелек мокроты больного, выделяемых при кашле, чихании, разговоре. Гораздо реже отмечается инфицирование через высохшую мокроту. Возможно заражение алиментарным или контактным путями (через поврежденную кожу или слизистые оболочки). Крайне редко наблюдается внутриутробное заражение с развитием так называемого врожденного туберкулеза.
Наряду с перечисленными путями проникновения туберкулезной палочки в организм существует “ятрогенное” заражение в результате вакцинации и ревакцинации БЦЖ. Наши наблюдения за 420 детьми раннего возраста позволяют считать, что дальнейшее течение туберкулезной инфекции у детей раннего возраста и особенно первого года жизни обусловлено рядом факторов:
- социальным фактором;
- анатомо-физиологическими особенностями, характерными для данной возрастной группы;
- трудностями выявления и диагностики заболевания.
Анатомо-физиологические особенности, предполагающие и определяющие развитие и течение туберкулеза, заключаются в незрелости бронхолегочного аппарата, недифференцированности лимфатической системы, незрелости иммунной системы для локализации и уничтожения МБТ и в первую очередь реакции гиперчувствительности замедленного типа, превалировании экссудативно-альтеративного компонента в воспалительных реакциях. Существенную роль в этой возрастной группе играет склонность к частым острым респираторным инфекциям, развитию рахита и дефицита железа, аллергическая настроенность организма. Все это способствует возникновению тотального казеозного поражения внутригрудных лимфатических узлов, ранней лимфогематогенной диссеминации, быстрому прогрессированию процесса с развитием осложнений. Самоизлечение туберкулеза в этой возрастной группе, в отличие от других возрастных групп, наблюдается крайне редко. Известны лишь единичные случаи частичной регрессии процесса и переход его в хронически текущий первичный туберкулез с развитием обширных кальцинированных очагов в легких и лимфоузлах.
Диагностика туберкулеза в этом возрасте весьма затруднена, особенно на первом году жизни. Клинические проявления туберкулеза не имеют специфических черт, могут протекать под масками различных заболеваний — ОРВИ, бронхита, пневмонии и т. д. — или бессимптомно.
Туберкулинодиагностика на первом году жизни в массовом порядке еще не проводится. При проведении туберкулинодиагностики среди вакцинированных детей в первые 6-8 месяцев жизни возникают трудности в дифференциальной диагностике инфекционной и поствакцинальной аллергии. При инфицировании ребенка в первые дни и недели жизни идет параллельное формирование специфической аллергии. Только к концу первого года жизни и старше туберкулинодиагностика позволяет более четко констатировать инфекционный характер аллергии (формирование высокого уровня чувствительности к туберкулину или гиперэргическая реакция).
При генерализации туберкулезного процесса (милиарный туберкулез, туберкулезный менингит) в 30-50% формируется анергия к туберкулину. Незнание этого феномена нередко приводит к диагностическим ошибкам.
При проведении рентгенодиагностики можно столкнуться с рядом трудностей, которые обусловлены особенностями рентгеносимеотики неосложненного и осложненного первичного туберкулеза и с анатомо-физиологическими особенностями рентгенограммы органов грудной клетки ребенка первых лет жизни.
Особенности рентгеносимеотики определяются патофизиологическими механизмами первичного туберкулеза. Высокая реактивность тканей к микробактериям туберкулеза проявляется в виде обширных перифокальных реакций в легочной ткани, сегментарных и лобарных легочных поражений. Склонность к генерализации и лимфотропность приводит к увеличению внутригрудных лимфатических узлов.
Анатомо-физиологические особенности заключаются в том, что в малой по размерам грудной клетке ребенка относительно большое место занимает срединная тень, образуемая сердцем и сосудами, за которыми скрываются корни легких, особенно на первом году жизни. Большая вилочковая железа прикрывает зону верхнего средостения, что также затрудняет визуализацию внутригрудных лимфатических узлов. К тому же во время исследования маленький ребенок ведет себя беспокойно, и заставить его сделать глубокий вздох невозможно. Все это очень затрудняет диагностику поражения внутригрудных лимфатических узлов. В итоге рентгенологически локальный внутригрудной туберкулез подтверждается иногда лишь при динамическом наблюдении и целенаправленном рентгенотомографическом исследовании.
Бактериологические методы лечения в педиатрии, в отличие от терапии для взрослых, менее информативны, так как дети редко выделяют МБТ, да и получение мокроты представляет большие трудности.
Поэтому диагноз устанавливается на основании многих показателей: подробно собранный анамнез — сведения о вакцинации БЦЖ, контактах с больным туберкулезом, факторами риска по развитию туберкулеза; динамическое наблюдение за течением заболевания, рентгенотомографической картины; туберкулинодиагностика.
При развитии первичного туберкулеза у детей раннего возраста в 90-92% случаев диагностируется внутригрудной процесс.
Внутригрудной туберкулез проявляется в виде бронхоаденита — 89,3% и первичного туберкулезного комплекса соответственно — 10,7%. По результатам рентгенотомографического исследования бронхоаденит протекает преимущественно в виде туморозной и инфильтративной форм. Редко встречается “малая” форма (3,2%). При этом нередко поражаются все группы внутригрудных лимфатических узлов.
 |
Первичный туберкулезный комплекс характеризуется развитием воспалительных изменений в легочной ткани, поражением регионарных внутригрудных лимфатических узлов и лимфангитом. Легочный компонент у 96,6% детей локализуется в верхних долях (сегменты 2, 3, 4, 5), реже в зоне 6-го сегмента и крайне редко в сегментах 8, 9, 10, чаще справа, как правило в пределах одного или двух сегментов. В отличие от других возрастных групп у детей раннего возраста поражение лимфоузлов редко бывает регионарным, а характеризуется вовлечением нескольких, а то и всех групп внутригрудных лимфоузлов и зачастую по туморозному типу.
Туберкулезная интоксикация выявляется крайне редко, и при отсутствии локальных туберкулезных поражений требуется поиск других причин интоксикации.
Характерным проявлением туберкулезной инфекции в раннем детском возрасте является высокий удельный вес осложнений — 55,4%, а у детей первого года жизни частота осложнений доходит до 80%. В структуре осложнений наиболее часто встречаются бронхолегочные поражения — 55,6% (ателектатически-инфильтративный процесс в пределах одного или нескольких сегментов, доли или всего легкого), милиарный туберкулез — 19,3%, генерализованные формы — 13,9%, туберкулезный менингит (менингоэнцефалит) — 11,2%.
| Причинами эпидемиологического неблагополучия по туберкулезу являются ухудшение социально-экономических, экологических условий, снижение жизненного уровня населения, рост преступности (среди пребывающих в ИТУ туберкулез диагностируется в 42 раза чаще, чем в среднем по стране); рост числа людей без определенного места жительства и занятий; миграционные процессы (распространенность туберкулеза среди беженцев и вынужденных переселенцев — от 459 до 700 случаев на 100 тыс.) |
Развитие осложнений дает нередко более яркую клиническую картину, в отличие от неосложненных форм первичного туберкулеза, что в 38,4% случаев является поводом для госпитализации ребенка в общесоматический стационар и требует проведения дифференциальной диагностики. При этом необходимо отметить, что среди детей с осложненным течением первичного туберкулеза 70-72% — дети из семей мигрантов. Этот факт имеет важное значение в диагностике туберкулеза для врачей-педиатров соматических и инфекционных больниц.
Клинические проявления туберкулеза не имеют специфических черт. В 81,8% случаев туберкулез начинается постепенно [5]. Первые признаки заболевания проявляются в виде умеренно выраженных симптомов интоксикации: снижении аппетита, изменении поведения ребенка. При осмотре обращает внимание бледность кожных покровов, понижение массы тела, тургора, эластичности тканей, увеличение периферических лимфатических узлов. На ранних этапах можно выявить увеличение печени и селезенки, эпизодические подъемы температуры до субфебрильных цифр. В гемограмме отмечается гипохромная анемия, не поддающаяся лечению препаратами железа и коррекции питанием. В формуле крови при нормальном уровне лейкоцитов — нейтрофильный сдвиг с развитием лимфопении. С присоединением осложнений (милиарный туберкулез, менингит, бронхолегочные поражения) нарастает интоксикация, значительно снижается масса тела, температура становится субфебрильной-фебрильной, нарастает одышка, появляется непродуктивный кашель, а при менингите развивается менингеальная симптоматика.
Учитывая эти факторы, врач-педиатр может своевремено провести обязательный диагностический минимум для подтверждения или исключения специфического процесса.
| Классификация постпрививочных осложнений, предложенная в 1984 году Международным союзом по борьбе с туберкулезом ВОЗ; категории осложнений: |
| I — локальные кожные поражения (холодные абсцессы, язвы) II — персистирующая и диссеминированная БЦЖ-инфекция без летального исхода (волчанка, оститы и др.) III — диссеминированная БЦЖ-инфекция по типу генерализованного поражения с летальным исходом, которое отмечается при врожденном иммунодефиците IV — пост-БЦЖ синдром (проявления заболевания, возникшие вскоре после вакцинации БЦЖ, главным образом аллергического характера, узловатая эритема и т. д.) |
Более чем 37-летние результаты использования для вакцинации и ревакцинации внутрикожного введения БЦЖ, а затем и БЦЖ-М свидетельствуют о ее благоприятном влиянии на течение первичной туберкулезной инфекции у привитых. Противотуберкулезная вакцинация уменьшает развитие таких тяжелых форм заболевания, как милиарный туберкулез, туберкулезный менингит. Отмечено, что первичное инфицирование и первичные формы туберкулеза у вакцинированных при рождении детей по сравнению с невакцинированными протекают более доброкачественно, без осложнений и приводят к сравнительно быстрому благоприятному исходу [5]. Наряду с этим необходимо отметить два важных положения.
Первое — в условиях раннего инфицирования (первые дни и недели жизни ребенка) противотуберкулезная вакцинация, проведенная на четвертый—шестой день жизни, не может предупредить развитие туберкулеза и его осложнений, так как еще не сформировался поствакцинальный иммунитет. Отсюда следует вывод о необходимости обязательного обследования всех членов семьи перед выпиской ребенка из родильного дома, независимо от того, была проведена вакцинация в родильном доме или нет.
Второе — БЦЖ-инфекция. Частота поствакцинальных осложнений на отечественную вакцину БЦЖ — 0,02% после вакцинации и 0,003% — после ревакцинации [3]. После внедрения в практику вакцины БЦЖ-М частота осложнений уменьшилась до 0,004% к числу привитых новорожденных.
Проявления БЦЖ-инфекции также многообразны, как и проявления первичного туберкулеза, но в отличие от последних протекают менее агрессивно.
В большинстве случаев осложнения после вакцинации БЦЖ носят местный характер. Это подкожные холодные абсцессы; язвы величиной 10 мм и более в диаметре на месте внутрикожного введения вакцины; лимфадениты регионарных лимфатических узлов (подмышечные, шейные, над- и подключичные) при увеличении узла до 1,5 см и более в фазе инфильтрации, абсцедирования и кальцинации. Редко, но встречаются БЦЖ-оститы и диссеминированная БЦЖ-инфекция как следствие врожденного иммунодефицита (хроническая гранулематозная болезнь).
В условиях массовой вакцинации БЦЖ высокая частота поствакцинальных осложнений привела к тому, что довольно большое количество детей, в основном первого, реже второго года жизни требует длительного консервативного, а нередко и хирургического лечения.
Таким образом, в настоящее время в окружающей среде накоплен значительный резервуар туберкулезной инфекции. Туберкулез ведет себя агрессивно, поражая все возрастные и социальные группы населения. Наиболее негативно во всех своих проявлениях он действует на детей раннего возраста и особенно первого года жизни, приводя нередко к летальному исходу.
Литература
1. Аксенова В. А., Олянишин В. Н. Сборник резюме. Екатеринбург, 1997. № 186. С. 57.
2. Митинская Л. А. Противотуберкулезная вакцинация БЦЖ. М., 1975.
3. Митинская Л. А., Юхименко Н. В., Камаева В. Ф. Вакцинация БЦЖ и укороченные курсы лечения поствакцинальных осложнений с применением раствора рифампицина с димексидом. Педиатрия, 1986. № 6. С. 94-95.
4. Хоменко А. Г. Сборник резюме. Екатеринбург, 1997. С. 5-7.
5. Чугаев Ю. П. Диагностика и лечение туберкулеза у детей раннего возраста. Автореф. дис. док. мед. наук. М., 1988.
Читайте также:

