Персистентная форма инфекции это
Обновлено: 24.04.2024
За последние пять лет увеличилось число детей в возрасте до одного года, умерших от генерализованных вирусных инфекций [4]. Велика роль герпес-вирусных инфекций, особенно цитомегаловирусной, в формировании перинатальной патологии и младенческой смертности. Риск развития внутриутробной инфекции зависит от характера взаимоотношений между организмом беременной женщины и микроорганизмом (первичное заражение во время беременности или реактивация ранее приобретенной инфекции).
Проблема врожденной инфекционной патологии является приоритетной для России [5].
Иммуногенез герпес-вирусной инфекции. Длительное нахождение герпес-вируса в организме человека становится возможным благодаря сложной стратегии противоборства и ускользания от иммунной системы хозяина. В достижении этого состояния можно выделить три пути стратегии возбудителя:
Вирус простого герпеса. В инфицированных клетках вирус простого герпеса образует внутриядерные включения и гигантские клетки, оказывает выраженное цитопатическое действие, проявляющееся округлением и образованием многоядерных клеток. Вирус является слабым индуктором интерферона, в связи с чем инактивация вирусной ДНК внутри клеток не наступает и он сохраняется внутри клеток длительное время, периодически вызывая рецидивы заболевания.
ЦМВ. Сущность проблемы ЦМВ-инфекции в том, что последняя относится к так называемым оппортунистическим инфекциям, клинические проявления которых возможно в условиях первичного или вторичного иммунодефицита.
ЦМВ поражает разнообразные клетки, чаще всего лейкоциты (лимфоциты, моноциты), эпителиальные клетки (дыхательных путей, слюнных желез, почек). С клеток крови ЦМВ с большим постоянством переходит на эндотелий, тропизм к которому у него весьма выражен. Поврежденные эндотелиальные клетки постоянно обнаруживаются в токе крови при активной/реактивированной ЦМВ-инфекции. Повреждение эндотелия сосудов имеет собственное патогенетическое значение в формировании органных поражений, так как вызывает ишемию или кровоизлияния в различные ткани [6].
В раннем неонатальном периоде (0–7 дней) у детей с ЦМВ-инфекцией наблюдались симптомы интоксикации, серый колорит кожи, выраженная мышечная гипотония, большая первоначальная потеря массы тела, синдром рвоты или срыгиваний, признаки угнетения ЦНС. В позднем неонатальном периоде (от 7 дней до одного мессяца) анализ клинических проявлений острой ЦМВ-инфекции выявляет поражение многих органов и систем. Так, у всех детей обнаруживаются гипоксически-ишемическая энцефалопатия с трансформацией синдрома угнетения в синдром гипервозбудимости, проявления анемии, патологическая гипербилирубинемия, увеличение печени и селезенки.
ВЭБ относится к подсемейству бета-герпес-вирусов. Вирусный геном заключен в нуклеокапсид, который покрыт гликопротеидным тегументом gp350, являющимся фактором рецепторного взаимодействия [7]. Проникновение вируса в В-лифоциты осуществляется через рецептор этих клеток CD21-рецептор к C3d-компоненту комплемента. ВЭБ-инфекция широко распространена среди людей, причем первичное инфицирование, как правило, происходит в антенатальном или детском возрасте, но манифестация ВЭБ-инфекции в виде отчетливых клинических проявлений инфекционного мононуклеоза в большинстве случаев происходит в школьном возрасте при различного рода иммунопатологических реакциях. Манифестация инфекции в виде инфекционного мононуклеоза может осложняться поражением печени, слизистой оболочки желудка, ткани почек, лимфоидного аппарата.
Особый характер взаимодействия микро- и макроорганизма при хронических персистирующих инфекциях обусловливают трудности лабораторной диагностики. Обнаружение возбудителя не может быть единственным критерием подтверждения диагноза. Необходима комплексная оценка клинических и лабораторных данных для постановки диагноза.
Цель исследования. Определить клинические особенности течения персистирующих герпес-вирусных инфекций у детей и оценить значимость комплекса лабораторных исследований, в том числе показателей общей иммунологической реактивности у больных при персистирующем у них инфекционном процессе.
Материал и методы исследований. Под наблюдением находилось 63 пациента в возрасте от одного месяца до 7 лет, из них детей до одного года было 25, от одного года до трех лет — 22 и старше трех лет — 15 больных. Среди обследованных детей преобладали пациенты первых двух лет жизни — 47 детей (74,6%) и старше двух лет было 15 больных (25,4%).
Результаты. В клинической диагностике персистирующих инфекций у детей следует отводить первостепенное значение неблагополучию акушерского анамнеза матерей больных детей.
Беременность и роды были осложненными у большинства матерей наблюдаемых детей, чаще всего у них отмечались гестозы и угроза выкидыша, рождение недоношенных, в родах гипоксия плода, преждевременная отслойка плаценты, кесарево сечение и др. У 32 женщин из 63 (50,7%) были различные соматические заболевания (хронический пиелонефрит, кольпит, анемия, аутоиммунный тиреоидит и др.). При обследовании беременных женщин было выявлено как моноинфицирование (у 30 из 63–47,6%), так и сочетания инфекций (у 16 из 63–25,4%). Наиболее часто обнаруживались герпес-вирусы и цитомегаловирусы (суммарно у 27 женщин из 63–43%) и реже другие возбудители — хламидии, микоплазмы (у 11 беременных — 17,4%). Высокая частота вышеуказанных осложнений свидетельствует о несомненной роли инфекции как отягощающего фактора в течение гестационного периода и родов.
Заподозрить внутриутробную или персистирующую инфекцию у детей можно было по высокой степени поражения у детей различных органов и систем: ЦНС (71,4%), органов дыхания (88,8%), желудочно-кишечного тракта (95,2%), поражению глаз (31,7%), лимфатического аппарата (15,9%).
В процессе наблюдения за детьми в недалеком прошлом все дети обследовались на состояние микробиоценоза кишечника.
У всех детей обнаруживались нарушения как в основных компонентах биоценоза, так и в составе условно-патогенной флоры. Следует отметить, что у всех пациентов проводилась коррекция микробиоценоза повторными курсами пре- и пробиотиков, однако восстановления микрофлоры до нормобиоценоза не наблюдалось ни у одного пациента. Следовательно, без выявления и адекватного лечения основного заболевания не удается курировать дисбиотические нарушения в организме ребенка.
Закономерен вопрос о правильности выбора комплекса диагностики внутриутробной и персистирующей инфекции у детей. В зависимости от возраста пользуются разными методами диагностики. Важное значение отводится сбору семейного анамнеза. Диагностика внутриутробных инфекций у детей должна опираться на клинические проявления как общего характера, так и на типоспецифические ее признаки, а также основываться на анализе комплекса лабораторных методов обследования [8].
При оценке клинических анализов крови у наблюдаемых детей обращали на себя внимание значительные отклонения в различных показателях гемограммы: выраженная анемизация (у 31,7% пациентов), нейтропения (у 19%), лимфоцитоз (у 27%), лейкопения с лимфоцитопенией (36,5%), ускорение СОЭ (у 27%), что в совокупности свидетельствовало о наличии воспалительного процесса в организме с выраженным снижением иммунореактивности у детей.
При скрининговом серологическом обследовании методом ИФА на внутриутробные инфекции у детей наиболее часто выявлялись положительные титры типоспецифических антител класса IgM и/или IgG к герпес-вирусам. Диагностические титры антител класса IgM и IgG определялись к ЦМВ (у 9 детей), к HV 1-го, 2-го типа (у 9 детей). Антитела к антигенам ВЭБ обнаруживались у 20 детей, из них у 10 детей были антитела класса IgG к раннему антигену ВЭБ и антитела класса IgM к капсидному антигену ВЭБ, что свидетельствовало об активной фазе ВЭБ-инфекции. Остальные 10 пациентов имели антитела класса IgG к нуклеарному (ядерному) антигену ВЭБ, что расценивалось как поздняя стадия инфекции.
У детей при персистирующем течении с реактивацией инфекции, которое чаще возникало после провоцирующих воздействий (ротавирусные диареи, ОРВИ, профилактические прививки) ПЦР-тесты при исследовании биосубстратов: кровь, осадок мочи, секрет из зева давали положительные результаты с последующим нарастанием титра типоспецифических антител по данным ИФА.
Совокупность проведенных исследований позволила выделить у обследованных больных следующие формы инфекций: моноинфекции были у 21 пациента — 31,8% (ЦМВ — у 5 детей, HV 1-го, 2-го типа — у 6 детей и ВЭБ — у 10), у 42 детей из 63 (68,2%) обнаруживались микст-инфекции. У 23 детей была ассоциация ЦМВ с герпес-вирусами (у 9 детей с HV 1-го, 2-го типа, у 3 детей — с HV 6-го типа и у 11 детей — с C. albicans и хламидиями). Микст-формы герпеса 1-го, 2-го типа были выявлены у 9 больных, у них были ассоциации с микоплазмами и хламидиями. Ассоциации ВЭБ были обнаружены у 10 детей (5 больных имели ассоциацию с ЦМВ, пациента — с HV 6-го типа и 2 больных — с Yersinia pseudotuberculosis).
Из 63 больных у 21 (33,3%) с моноинфекцией течение заболевания расценивалось как латентное (с ЦМВ-инфекцией у 5 и HV 1-го, 2-го типа у 6) и как персистирующее (у 10 детей с ВЭБ-инфекцией). У 14 детей из 42 с микст-инфицированием (у 1/3) было персистирующее течение инфекционного процесса (у 3 детей с ЦМВ-инфекцией в ассоциации с HV 6-го типа и у 11 детей с ЦМВ-инфекцией в ассоциации с C. albicans и хламидиями). У 28 детей из 43 (у 2/3) наблюдалось персистирующее течение с реактивацией инфекции (у 9 детей с ЦМВ-инфекцией в ассоциации с HV 1-го, 2-го типа; у 9 детей с HV 1-го, 2-го типа в ассоциации с хламидиями или микоплазмами и у 10 детей с ВЭБ инфекцией в ассоциации с ЦМВ, HV 6-го типа и ВЭБ в ассоциации с Y. pseudotuberculosis).
Коэффициент фагоцитарной защиты у детей с моноинфицированием и микст-формами герпесвирусной инфекции оказался достоверно сниженным по сравнению со средневозрастной нормой для здоровых детей (0,634 ± 0,05 усл. ед. и 0,540 ± 0,03 усл. ед. соответственно при норме 0,946 ± 0,03, Р1–2 и Р2–3 < 0,001 и < 0,001 соответственно). При микст-инфицировании герпес-вирусами КФЗ имел более низкие значения по сравнению с таковым у детей с -моноинфекцией, однако разница недостоверна (Р1–2 > 0,05). Недостаточность защиты клеточно-фагоцитарного звена иммунитета играет важную роль в патогенезе герпес-вирусных инфекций, что должно учитываться в лечении этих заболеваний.
Отклонение величины показателя ИЛМП имело противоположную направленность, она оказывалась достоверно повышенной как при моноинфекции, так и при микст-формах герпес-вирусных инфекций по сравнению с контролем (Р1–3 и Р2–3 < 0,001 и < 0,001 соответственно). Величины показателя ИЛМП у детей с микст-инфицированием была большей по сравнению с таковой при моноинфекции, однако разница недостоверна Р1–2 > 0,05. Увеличение показателя ИЛМП у детей с герпес-вирусной инфекцией еще раз подтверждает лимфотропность вирусных антигенов.
ЛИИ оказался достоверно повышенным у больных с микст-формами герпес-вирусной инфекции по сравнению со средневозрастной нормой в контроле (Р2–3 < 0,001). Средние значения ЛИИ у детей с моноинфекцией достоверно не отличались от норматива (Р1–3 > 0,05), они имели лишь тенденцию к повышению. Однако при оценке индивидуальных показателей ЛИИ у детей с моноинфицированием герпес-вирусами выявились существенные особенности. У 13 детей из 21 (61,9%) ЛИИ был ниже возрастной нормы, что отражало фазу положительной анергии к совершенно определенному антигену. Это свидетельствует, что организм защищен сейчас только от специфических антигенов, однако он остается уязвимым в отношении других патогенов, то есть низкий индекс интоксикации отнюдь не указывает на полное благополучие организма.
Полученные результаты исследований подтверждают выраженность иммунного дисбаланса как в клеточно-фагоцитарном звене иммунитета, так и в гуморальном, а также свидетельствуют о значимости эндогенной интоксикации у больных с микст-формами герпес-вирусной инфекции и уязвимости иммунной защиты у детей и при моноинфицировании.
Клинический пример. Андрей С., 2 года 5 мес., поступил в стационар с жалобами на высокую температуру — 39 °С, однократную рвоту, сниженный аппетит и жидкий стул 5 раз в сутки. Болен в течение двух недель ОРВИ, получил амбулаторно симптоматическое лечение. К концу второй недели ухудшилось состояние, рецидив лихорадки — 39 °C и дисфункция кишечника. Направлен на госпитализацию.
Анамнез жизни. От первой беременности, протекала с угрозой выкидыша, нефропатией, преэклампсией в родах. Во время беременности перенесла ОPВИ с лимфаденитом. Обследование на пренатальные инфекции, обнаруживались антитела класса IgG к антигенам ЦМВ и вирусу герпеса 1-го, 2-го типа. Лечение не проводилось. Роды в срок, масса при рождении 3500 г, длина 51 см. К груди приложен сразу, сосал активно, грудное вскармливание до года, прикормы вводились в 5 и 6 месяцев. Адаптация к пище нормальная. В массе прибавки достаточные, в 2 г. 5 мес — масса 14 кг 810 г, рост 93 см.
Состояние здоровья в течение первого года жизни неблагополучное. Длительно держалась желтуха, в возрасте 3 недель: общий билирубин — 315,1 мкмоль/л, непрямой — 297,3 мкмоль/л, прямой — 17,8 мкмоль/л. Одновременно с желтухой был неустойчивый стул. В 1-месячном возрасте неврологом установлен диагноз перинатального поражения ЦНС, гипоксическо-ишемического генеза, гипертензионный синдром.
К возрасту 6 мес были обнаружены изменения в гемограмме: гемоглобин — 112 г/л, эритроциты — 4,2 × 10 12 /л, лейкоциты — 7,8 × 10 9 /л, сегментоядерные нейтрофилы — 12%, лимфоциты — 67%, моноциты — 12%, эозинофилы — 8%, базофилы — 1%, СОЭ — 3 мм/час. В повторных анализах крови во 2-м полугодии продолжала выявляться нейтропения. Консультирован гематологом, установлен диагноз доброкачественной нейтропении детского возраста. В 10 мес в анализе крови выявлена анемия (гемоглобин — 107 г/л, эритроциты — 3,81 × 10 12 /л, цветовой показатель — 0,84, тромбоциты — 280 × 10 9 /л, сегментоядерные нейтрофилы — 11%, лимфоциты — 76%, моноциты — 90%, эозинофилы — 3%, базофилы — 1%). Гематологом назначено лечение Сорбифером дурулесом, курс 1 месяц.
Осмотрен ортопедом: отмечено ограниченное отведение бедер. В один год на УЗИ органов брюшной полости определялся перегиб в области шейки желчного пузыря, холестаз. Осмотр генетика: диагностирована недифференцированная дисплазия соединительной ткани с поражением костно-мышечной системы. В 1 г. 5 мес перенес острый энтероколит неуточненной этиологии, госпитализировался в стационар на 10 дней, получал лечение метронидазолом и Энтеролом. В течение 1,5 лет переносит частые ОРВИ с повышением температуры до 38,8 °С в течение 3–4 дней и катаральными явлениями.
Объективные данные. При последней госпитализации отмечались явления назофарингита в течение 5 дней, лихорадка до 39 °С 2 дня, кожные покровы без сыпи. При осмотре — гиперемия зева и увеличение подчелюстных, передних и заднешейных лимфоузлов, стул учащенный до 3 раз в сутки, с 5 дня лечения — оформленный. ЛОР-врачом диагностирован хронический тонзиллит и аденоидит, в фазе обострения.
Обследование. В мазке из зева — высев гемолитического стрептококка. Посевы на патогенную кишечную флору отрицательные. ИФА на ротавирус — отрицательный. Реакция непрямой гемагглютинации (РНГА) с кишечными диагностикумами — отрицательные.
Гемограмма при поступлении: гемоглобин 104 г/л, эритроциты — 3,7 × 10 12 /л, цветовой показатель — 0,85, лейкоциты — 6,4 × 10 9 /л, палочкоядерные нейтрофилы — 4%, сегментоядерные — 72%, лимфоциты — 18%, моноциты — 4%, эозинофилы — 2%, СОЭ — 4 мм/час.
Гемограмма в динамике: гемоглобин — 109 г/л, эритроциты — 3,4 × 10 12 /л, лейкоциты — 7,8 × 10 9 /л, палочкоядерные нейтрофилы — 19%, сегментоядерные — 42%, лимфоциты — 28% (широкоплазменные лимфоциты), моноциты — 8%, плазматические клетки — 1%, эозинофилы — 2%, СОЭ — 13 мм/час. В дальнейшем — красная кровь оставалась без динамики, число лейкоцитов не изменялось, нарастал лимфоцитоз до 43% (широкоплазменные формы), моноцитов до 12%, СОЭ повысилась до 20 мм/час.
Анализ мочи без отклонений от нормы (пятикратно). В биохимическом анализе крови — умеренная гипоальбуминемия, печеночные пробы — в норме. ИФА на специфические антитела к антигенам ЦМВ класса IgM — отрицательный, класса IgG — положительный. Маркеры ДНК-ЦМВ в осадке мочи и в секрете из зева методом ПЦР не найдены. ИФА на специфические антитела к хламидийному антигену (Chlamydia pneumoniae) — положительный в титре 1:80. Маркеры ДНК Ch. pneumoniae в мазке из носоглотки методом ПЦР — положительный. ИФА с микоплазменным антигеном — IgM и IgG — отрицательные, с герпес-вирусами 1-го, 2-го типа — IgM и IgG отрицательные. ИФА на специфические антитела к антигенам ВЭБ: IgM к капсидному антигену — отрицательный, IgG к раннему антигену — положительный и IgG к ядерному антигену (IgGNA) — положительный (> 0,5 ед.). Совокупность данного анализа была индикатором активной фазы мононуклеозной инфекции.
После проведенного обследования ребенку была назначена адекватная комплексная терапия (Cумамед, Ликопид с последующим переходом на Виферон, витамины А, Е, Пиридоксин, пробиотики — курс Примадофилуса). Наблюдение за ним продолжается.
Выводы
- В пользу диагностики персистирующих инфекций у детей свидетельствует отягощенный акушерско-гинекологический и соматический анамнез, а также инфекционный фактор беременных женщин.
- Заподозрить внутриутробное инфицирование у детей раннего возраста можно по высокой степени поражения различных органов и систем: ЦНС, органов дыхания, пищеварения, лимфатического аппарата.
- Диагностика внутриутробных инфекций должна базироваться на клинических проявлениях болезни и основываться на комплексе лабораторных и иммунологических методов исследования с их оценкой в динамике (в 1 мес, 3 мес, 6 мес и в 1 год жизни).
- Правильность выбора комплекса клинических и лабораторных тестов (ИФА в динамике, ПЦР-тесты с различными биосубстратами) приводит к своевременной диагностике внутриутробных инфекций и позволяет выявить моноинфицирование или микст-формы при их длительной персистенции.
- Для суждения о состоянии общей иммунологической реактивности детей с персистирующими герпесвирусными инфекциями может использоваться оценка интегральных показателей (КФЗ и ИЛМП): чем меньше величина КФЗ, тем больше выражен риск прорыва защитного барьера на пути инфекции.
- Наиболее неблагоприятное персистирующее течение имеют микст-формы герпесвирусной инфекции (ЦМВ, герпес, ВЭБ) или их сочетания с внутриклеточными возбудителями.
Литература
Ф. Н. Рябчук, кандидат медицинских наук, доцент
З. И. Пирогова, кандидат медицинских наук, доцент
СПбМАПО, Санкт-Петербург
Персистентные инфекции в легких. Латентная инфекция в легких.
В последнее десятилетие в центре внимания исследователей различного профиля находятся сложные формы воспаления, явно отступающие от общепринятых канонов острых защитных реакций и характеризуемые своеобразными дисбалансами иммуноглобулинов и цитокинов. Эти формы воспаления характерны, прежде всего, для вирусной персистенции. Персистенция (постоянство, упорство) - понятие достаточно широкое и неоднозначное, которое, по современным представлениям, включает в себя несколько подвариантов: персистентная, латентная, хроническая и медленная инфекции, а также бессимптомное вирусоносительство.
Персистентными называют инфекции, при которых вирус либо его антигены в течение продолжительного времени обнаруживаются в организме человека. Указанное пребывание сопровождается определенными специфическими иммунологическими сдвигами. Клинические проявления заболевания могут быть выраженными, слабыми либо маскироваться симптомами общего хронического заболевания (кашель, слабость, субфебрилитет, одышка и т.д.), что нередко наблюдается у больных с хронической обструктивной болезнью легких и бронхиолите с облитерацией при нерсистенции респираторно-синцитиального вируса.
Латентная инфекция - это практически пожизненная инфекция, при которой вирус (чаще герпес) находится в наиболее тесном взаимодействии с геномом клетки и пребывает преимущественно то в дефектной (ДНК-транскрипт), то в полной инфекционной форме, что соответствует ремиссии и обострению. Активация латентной инфекции происходит, как правило, под влиянии других инфекций (чаще грипп), переохлаждения, перегрева, солнечной радиации, психических травм и т.д.
Наиболее типичным примером хронической инфекции является инфекция, вызываемая аденовирусами. Для нее характерна частая смена клинических ремиссий и обострений, но относительно благоприятный прогноз при своевременном и правильном лечении.
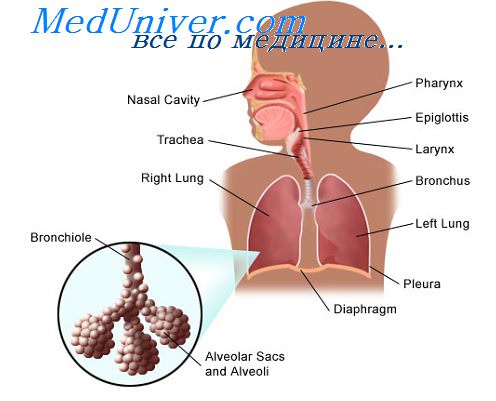
Медленная инфекция - имеет неизбежно летальный исход, характеризуется многомесячным или даже многолетним инкубационным периодом с последующим медленным, но неуклонным развитием симптомов заболевания (вирусы СПИД и спонгиозных энцефалитов).
Классификация вирусной персистенции весьма условна. При наличии отличительных свойств многие ее формы имеют общие черты: при всех вариантах весьма распространено формирование дефектных форм вируса, их тесное взаимодействие с геномом клетки-хозяина, чередование фаз обострения и клинической ремиссии. Вероятны переходы одной разновидности персистенция в другую, например персистентной инфекции в латентную или хроническую.
Как показали исследования, проведенные в Государственном научном центре пульмонологии (МЗ РФ), персистенция достаточно широко распространена не только при хронической, но и острой бронхолегочной патологии. При тяжелых полисегментарных пневмониях и острых абсцессах нередко отмечается замедленная элиминация респираторных вирусов и их компонентов из организма больного, что подтверждается и более длительными сроками образования специфических противовирусных иммуноглобулинов класса М и G. Персистенция сопровождается низкими показателями клеточного иммунитета (прежде всего Т-активные клетки), натуральной киллерной активности, всех видов интерферона. Иммуносупрессия, обусловленная вирусами, способствует более выраженной активации бактериальной флоры как аэробного, так и анаэробного плана.
При затяжных и рецидивирующих бронхитах, особенно с явлениями бронхоспазма, вирусы и вирусные компоненты удается обнаружить до 1,5-2 месяцев от начала заболевания. Их элиминация прямо коррелирует с исчезновением признаков воспаления бронхов.
При хронической обструктивной болезни легких и бронхиолите с явлениями облитерации у детей респираторно-синцитиальный вирус чрезвычайно часто выявляется как в период обострения, так и относительной клинической ремиссии.
У больных с ЛОР-патологией: аденоидитами, хроническими тонзиллитами и отитами основным персистирующим агентом является аденовирус. При одновременном наличии аденоидитов и шейных лимфоденитов чаще всего наблюдается ассоциация хронических аденовирусных и микоплазменных инфекций.
Особенности воспалительных реакций организма при вирусной персистенции чрезвычайно разнообразны, весьма вариабельны и зависят от громадного количества факторов, определяемых как макро-, так и микроорганизмами.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
На основании собственных многолетних данных произведен ретроспективный анализ особенностей динамики активной репликации персистирующих инфекций у детей. В статье описано, как изменяются показатели активной репликации геномов облигатных внутриклеточных пар
Based on our own multi-year data, a retrospective analysis of the dynamics of active replication of persistent infections in children was made. The article describes how the indicators of active replication genomes of obligate intracellular parasites and herpesviruses vary with age and seasonal changes.
Персистирующие инфекции могут являться причиной целого ряда заболеваний. Некоторые из них характеризуются тяжелым клиническим течением, особенно в раннем возрасте. В России, к сожалению, сохраняется высокий уровень детской инфекционной заболеваемости [1]. Известно, что в основном передача инфекции осуществляется в первые годы жизни человека, иногда — внутриутробно. Так, заражение герпес-вирусами человека 1–2, а также 4–6 типов в большинстве случаев реализуется в возрасте до двух лет. Источником инфекции чаще всего является ближайшее окружение ребенка, которое в первые два года его жизни представлено членами семьи и/или обслуживающим персоналом (няни, воспитатели и пр.). За последние пять лет увеличилось число детей в возрасте до одного года, умерших от генерализованных вирусных инфекций [2]. При этом, по данным литературы, у детей маркеры активной персистирующей инфекции выявляют чаще, чем у взрослых [3]. Одним из факторов, обусловливающих высокий уровень репликации инфекционных агентов, является незрелость иммунной системы в раннем возрасте [4]. Несмотря на обилие научных работ, посвященных проблеме персистирующих инфекций, вопрос особенностей динамики их активности остается открытым.
Объект и материалы исследования
Предметом анализа явились данные, полученные при обследовании детей и подростков, находившихся на стационарном лечении в клинике Московского НИИ педиатрии и детской хирургии (в последние годы — Обособленное структурное подразделение Научно-исследовательский клинический институт педиатрии им. акад. Ю. Е. Вельтищева ФГБОУ ВО РНИМУ им. Н. И. Пирогова) Минздрава РФ, и их родителей.
Проанализированы результаты обследования 1079 пациентов, из которых 1064 (98,6%) составили дети и подростки в возрасте от 2 месяцев до 17 лет и 15 (1,4%) взрослых в возрасте от 23 до 52 лет.
У каждого пациента одновременно исследовали от одного до трех образцов различных биологических материалов, всего 2051 образец. Из них осадков мочи — 877 (42,8%); буккальных соскобов — 104 (5,1%); объединенного материала, включающего осадок мочи и буккальный соскоб, — 901 (43,9%); крови — 169 (8,2%) (табл. 1).
Методы исследования
Оценивали активность репликации следующих микроорганизмов: Chlamydia trachomatis, Mycoplasma hominis, Ureaplasma urealyticum, цитомегаловирус, вирус Эпштейна–Барр, вирус простого герпеса 1–2 типов.
Среди пациентов девочки и женщины составили 56,7% от числа обследованных, мальчики и мужчины — 43,3%.
Возрастная характеристика пациентов отражена в табл. 2: возраст большинства пациентов составил от двух до 16 лет.
При определении периодов активной репликации персистирующих инфекций в зависимости от возраста фрагмент исследования включал данные, полученные при обследовании 876 пациентов.
Основным критерием отбора явилось одновременное исследование в материале не менее 3 инфекций (герпес-вирусов 4–6 типов и/или облигатных внутриклеточных паразитов). У каждого больного, соответственно, исследовали 3 или 6 инфекций. Такой подход позволил снизить избирательность выборки по той или иной инфекции.
Результаты исследования и их обсуждение
Выявлены следующие закономерности (рис. 1):
Отчетливая закономерность показана для цитомегаловируса: частота выявления ДНК в образцах стабильно снижается до 0 у обследованных взрослых, что можно рассматривать как доказательство зависимости активной репликации цитомегаловируса именно от зрелости иммунной системы (рис. 2).
Аналогичные, хотя и не столь четко выраженные изменения частоты активной репликации в зависимости от возраста можно проследить и для вирусов Эпштейна–Барр и вируса простого герпеса 1–2 типов.
Для ответа на вопрос, существуют ли сезонные изменения активности персистирующих инфекций, мы проанализировали частоту положительных проб в течение двух полных лет; был обследован 871 пациент.
Диаграмма отражает закономерности изменения количества положительных проб Chlamydia trachomatis, Mycoplasma hominis и Ureaplasma urealyticum в течение года (рис. 3).
Вопреки ожиданиям, наибольшая активность Chlamydia trachomatis приходится на период с апреля по июнь. Отмечаются существенные колебания показателя в первом полугодии с максимумом в июне и минимумом в марте и стабильно низкие показатели во втором полугодии.
Частота выявления ДНК Ureaplasma urealyticum крайне нестабильна с декабря по июнь, а в июле резко уменьшается и сохраняется на относительно низком уровне до ноября. В декабре значение показателя возрастает, достигая максимума. Таким образом, общим для исследованных внутриклеточных паразитов является нестабильность и более высокие значения показателя в первом полугодии (для Ureaplasma urealyticum — с декабря по июнь) и, напротив, относительно низкое и стабильное число положительных проб во втором полугодии. Не исключено, что снижение и стабилизация показателя в период с июля по декабрь вызвана улучшением метаболизма, а значит, и адаптивного иммунитета во второй половине лета и осенью.
Для персистирующих герпес-вирусов какой-либо четкой сезонной закономерности не выявлено, однако частота выявления ДНК вируса простого герпеса 1–2 типов стабильно повышается, в мае достигая максимума, а затем снижается к концу года до минимального значения (рис. 4).
Выводы
Проведенное нами исследование позволило сделать следующие выводы:
При исследовании сезонной активности всех облигатных внутриклеточных паразитов выявлена ее существенная вариативность в первом полугодии с максимумом в июне и относительное снижение и стабилизация во втором полугодии.
Литература
- Мазанкова Л. Н., Захарова И. Н. // Рос. вест. перинат. и педиатрии. 2010. № 5. С. 8–11.
- Лобзин Ю. В. Проблемы детских инфекций на современном этапе // Инфекционные болезни. 2009. № 2. С. 7–12.
- Учайкин В. Ф., Нисевич Н. И., Шамшева О. В. Инфекционные болезни и вакцинопрофилактика у детей. М.: ГЭОТАР-медиа. 2006. 688 с.
- Щеплягина Л. А., Круглова И. В. Возрастные особенности иммунитета у детей // РМЖ. № 23, 2009, с. 1564.
Е. И. Шабельникова 1 , кандидат медицинских наук
В. С. Сухоруков, доктор медицинских наук, профессор
Е. А. Ружицкая, кандидат медицинских наук
А. В. Семенов, кандидат медицинских наук
М. В. Кушнарева, доктор медицинских наук, профессор
ФГБОУ ВО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
Различных терминов, связанных с инфекциями, которые поселяются в организме, много. И не во всех из них люди разбираются досконально. При этом понимать очень хочется, чтобы можно было хотя бы примерно оценивать риски. Итак, многие часто задаются вопросом: что такое персистирующие вирусные инфекции?
Персистирующие вирусные инфекции — это различные патологии, которые вызываются вирусами, обитающими в человеческом организме. Причем стоит помнить, что некоторые патогены никак не влияют на состояние человека, другие же приводят к определенным угрозам. И защитные механизмы иммунной системы постоянно держат таких возбудителей под контролем. Длительное пребывание таких спящих микроорганизмов как раз нередко и становится причиной проявления инфекции.
Сама по себе персистенция — это способность патогенных микроорганизмов долго жить в организме человека, не проявляя себя никак. Ярким примером может служить герпес, находящийся большую часть времени именно в спящем режиме. Но при сопутствующих условиях такие микоорганизмы могут приводить к активизации инфекционных процессов.
Когда проявляются персистирующие вирусные инфекции?
Триггерами для запуска инфекционного процесса могут выступать следующие условия:
- Снижение иммунитета, например, на фоне частых недосыпов, стрессов, переохлаждений и т. д.
- Снижение защитных функций из-за активизации другого заболевания.
Если патоген себя никак не проявляет, то говорят о латентной форме, она же бессимптомная. Выявляется в этом случае вирус случайно, например, при определенном обследовании. Тут стоит понимать, что отсутствие ярких клинических признаков нельзя считать положительным моментом, ведь хронические процессы прогрессируют, и это иногда может давать проявления соматики.
Какие патогены вызывают персистирующие вирусные инфекции?
Не все вирусы, как отмечают медики, могут жить в организме человека и не выдавать себя никак. Чтобы им такое удавалось, они должны уметь жить внутри клеток. В числе таких патогенов:
- герпес;
- гепатит;
- ВИЧ;
- токсоплазмы.
Все они стараются, чтобы иммунная система не могла их найти и обезвредить. За счет интеграции с геномом человека инфекционные процессы на фоне попадания таких возбудителей в организм идут медленно.

Наличие или отсутствие такого рода инфекции подтверждается исключительно лабораторными методами. Понятно, что вирус герпеса нередко видно невооруженным взглядом, если он высыпает на губах. Но есть и такие его типы, которые проявляются нетипично. Как правило, для постановки диагноза используют следующие методы:
- цистоскопическое исследование;
- диагностика на молекулярном уровне;
- анализ методом ИФА.
Терапия персистирующих инфекций обычно предполагает использование противовирусных препаратов и назначение иммунных средств. Решение о длительности курса принимает исключительно врач в зависимости от того, как протекает процесс, какие есть сопутствующие отягчающие нюансы у пациента и т. д.
Персистирующие вирусные инфекции зачастую неизлечимы, поэтому остаются все в том же спящем состоянии. Однако за здоровьем человеку, у которого они есть, надо обязательно следить, чтобы хронические прогрессирующие процессы не нанесли ему серьезного урона. Обязательным пунктом является укрепление иммунитета, а значит, коррекция образа жизни, режима труда и отдыха, питания и т. д.
Читайте также:

