Пневмококковый менингит что это такое
Обновлено: 24.04.2024
Пневмококковый менингит (ПМ) отличается тяжелым течением, высокими показателями летальности, развитием осложнений. Рассмотрены особенности заболевания, обусловленные низкой биодоступностью возбудителя, и подходы к лечению. Указаны основные направления сов
Pneumococcal meningitis (PM) is distinguished by severe clinical course, high indices of mortality, development of complications. Characteristics of the disease conditioned by low availability of the agent and approaches to the treatment were considered. Main directions of PM therapy improvement were stated.
Пневмококковый менингит (ПМ) по данным бактериологических исследований занимает второе, после менингококкового менингита (ММ), место в этиологической структуре бактериальных гнойных менингитов (БГМ). Так, в РФ удельный вес ПМ среди других гнойных менингитов составляет 9,5–26%, в г. Москве за период 2005–2011 гг. — от 10,4% до 21% [1–5]. Учитывая то, что ПМ не входит в РФ в число инфекционных заболеваний, подлежащих официальной регистрации, а также то, что частота бактериологического подтверждения диагноза БГМ составляет по РФ от 16% до 38%, истинная заболеваемость и смертность, а также многие актуальные аспекты патогенеза, клиники и лечения ПМ изучены недостаточно [6–11].
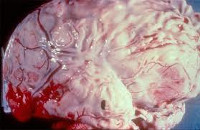
ПМ отличается тяжелым течением, высокими показателями летальности, развитием осложнений, нередко приводящих к инвалидизации больных [4, 12–14]. Особенности ПМ обусловлены свойствами возбудителя и характером патологического процесса. Наиболее контрастно эти различия видны при сравнении с ММ. Основными факторами патогенности пневмококка являются капсула и тейхоевая кислота клеточной стенки. Капсула препятствует фагоцитозу, поэтому в патологическом материале пневмококк всегда располагается внеклеточно. Таким образом, при пневмококковой инфекции фагоцитоз не выполняет своей роли — самого раннего механизма защиты при бактериальных инфекциях. Тейхоевая кислота взаимодействует с С-реактивным белком и таким образом инициирует активацию системы комплемента и продукцию медиаторов острой фазы воспаления. Это сопровождается резким повышением сосудистой проницаемости и формированием экссудата с высоким содержанием фибриногена, который в результате активации системы гемостаза образует сгустки фибрина. В их толще пневмококк не доступен действию антител против антигенов его капсулы, которые являются основным фактором защиты при пневмококковой инфекции. При менингококковой инфекции капсула менингококка не препятствует его фагоцитозу, поэтому менингококк располагается внутриклеточно, в цитоплазме лейкоцитов, причем, как было установлено нами иммунофлюоресцентным методом на раннем этапе инфекции, при низком содержании липополисахарида (ЛПС) фагоцитоз является завершенным и только при потреблении миелопероксидазы лейкоцитов становится незавершенным, а при потреблении компонентов системы комплемента при фульминантных формах менингококковой инфекции вообще подавляется. Основной фактор патогенности менингококка — ЛПС — является мощным инициатором системного воспаления, обладает высокой фибринолитической активностью, поэтому значительного образования фибрина не происходит и менингококк более доступен действию факторов защиты и тяжесть течения инфекционного процесса в большей степени обусловлена токсикозом, вплоть до развития инфекционно-токсического шока (ИТШ) [14, 15]. В связи с подавлением фагоцитоза пневмококк из оболочек мозга рано проникает по периваскулярным пространствам в вещество мозга. Экссудат формируется непосредственно на поверхности мозга, и, в отличие от ММ, при ПМ уже в ранние сроки развивается картина менингоэнцефалита с выраженным отеком-набуханием головного мозга (ОНГМ), снижением мозгового кровотока и повреждением вещества мозга (рис. 1).
_575.jpg)
В то же время лихорадочно-интоксикационный синдром и поражение центральной нервной системы (ЦНС), свойственные менингококковой инфекции, при ПМ развиваются не столь бурно, как при ММ, примерно у половины больных развитию ПМ предшествует риносинусит, отит, пневмония, поэтому больные госпитализируются позже, что также отрицательно влияет на эффективность лечения. Так, при ММ больные госпитализируются в среднем через 1,7 ± 0,3 суток от начала болезни, при ПМ через 3,4 ± 0,4 суток (р < 0,01).
До разработки методов этиотропной терапии летальность при ММ была близка к 50%, а при ПМ составляла почти 100%, однако применение сульфаниламидов, а затем антибиотиков не привело при ПМ к столь впечатляющим, как при ММ, результатам. Показатели летальности при БГМ в зависимости от возраста пациента, клинических форм болезни и от этиологического агента в развитых странах составляют в среднем 3–19%, а в развивающихся — от 37% до 69%. По нашим данным (проанализированы 1876 историй болезни больных ММ и 384 истории болезни ПМ) за последние 40 лет летальность при ПМ снизилась с 27,6% до 17,9% за счет внедрения методов реанимации и интенсивной терапии. За тот же период времени летальность при ММ снизилась с 9,8% до 4,2%, однако при ММ летальность в основном связана с ИТШ, а менингит является причиной летальных исходов примерно у 1 из 10 умерших. При ПМ около 45% больным требуется оказание помощи в условиях отделения реанимации и интенсивной терапии [1, 16, 17].
Как уже говорилось, высокая летальность при ПМ обусловлена тяжестью поражения головного мозга, что видно при сравнении симптоматики с ММ в табл. 1.
Основной причиной этих различий является низкая биодоступность возбудителя при ПМ, что подтверждается исследованиями динамики уровня лактата СМЖ, наиболее информативного показателя биологической активности возбудителя, так как лактат является продуктом анаэробного гликолиза [19, 20]. Данные об уровне лактата СМЖ у 28 больных ПМ и 50 больных ММ представлены на рис. 2.
Как видно из рис. 2, при ПМ уровень лактата не снижается на 4–7 дни лечения, а на 2–3 неделе значительно превышает норму, в то время как при ММ наблюдается быстрое и резкое снижение уровня лактата и на 2–3 неделе он достигает референсного значения. Низкая доступность пневмококка обусловлена двумя факторами: 1) снижением мозгового кровотока в результате резко выраженного ОНГМ и уменьшения вследствие этого пассажа антибиотиков через гематоэнцефалический барьер, а также наличием зон бионедоступности возбудителя: очагов размягчения мозгового вещества, гематом, и особенно наличием фибринозно-гнойного экссудата на поверхности и в оболочках мозга, что хорошо подтверждается патоморфологическими данными (рис. 1) и исследованиями концентрации Д-димера фибрина (ДДФ) в СМЖ, который является основным продуктом фибринолиза и наиболее информативным показателем наличия фибринового сгустка в исследуемом субстрате [11, 21]. Результаты определения ДДФ в СМЖ у 28 больных ПМ и 49 больных ММ представлены на рис. 3.
При ПМ фибринолиз длительно находится на высоком уровне без тенденции к снижению, что говорит о сохранении большого количества фибрина в поздние сроки и хорошо соотносится с патоморфологической картиной ПМ. Следует также остановиться на значительном различии уровня летальности при симптоматическом лечении ММ и ПМ, что может быть связано с низкой эффективностью естественных факторов саногенеза. Как говорилось, при ПМ по сравнению с ММ имеет место более слабая лейкоцитарная реакция, отсутствует фагоцитоз. В отечественной и зарубежной литературе широко представлены работы об особенностях иммунопатогенеза БГМ [3, 10, 14, 22). Установленно значительное снижение фагоцитарной активности нейтрофилов, дефицит компонентов комплемента, клеток С0З+, С04+, С08+, что указывает на важную роль в патогенезе ПМ нарушения иммунного гомеостаза с депрессией местного и системного иммунитета. Нами исследованы показатели местного иммунитета в СМЖ. В табл. 2 представлены наиболее существенные различия показателей иммунитета у 22 больных ПМ и 36 больных ММ.
Как видно из табл. 1, при ПМ провоспалительная активность в СМЖ ниже. Снижение ИРИ за счет меньшей пролиферации Т-хелперов, снижения местной продукции иммуноглобулинов также может способствовать более тяжелому течению болезни. Представленные данные указывают на основные направления совершенствования терапии ПМ. Во-первых, учитывая низкую биодоступность возбудителя, следует использовать препараты, хорошо проникающие через гематоэнцефалический барьер (фторхинолоны, меропенем) или позволяющие использование сверхвысоких доз (бензилпенициллин до 500–1,0 мкл/кг массы, меропенем 6 г в сутки), при низкой проницаемости сочетать внутривенное и эндолюмбальное введение препарата (ванкомицин). Во-вторых, даже при отсутствии явного клинического эффекта не производить замены другим препаратом в течение 5–7 суток. Абсолютное показание для смены препарата — устойчивость к нему возбудителя, выявленная при определении чувствительности данного штамма возбудителя. В-третьих, при чувствительности возбудителя к применяемому препарату и отсутствии явного эффекта следует дополнительно назначить второй препарат из группы альтернативных или резервных препаратов. В-четвертых, отказаться от применения кортикостероидов, так как они снижают пассаж антибиотиков через гематоэнцефалический барьер. Важнейшее значение имеет раннее применение искусственной вентиляции легких до развития гипоксемии, по клиническим показаниям: глубокие расстройства сознания, судороги, снижение биоэлектрической активности мозга. Необходимо также применение препаратов, улучшающих мозговой кровоток (пентоксифиллин и др.). Необходимо проведение целенаправленных исследований о влиянии средств патогенетической терапии на проницаемость гематоэнцефалического барьера для антибиотиков, повышение биодоступности возбудителя, использование фибринолитиков, препаратов, активизирующих местные факторы саногенеза. Наконец, следует учитывать, что при наличии гнойного очага (отит, синусит и др.) необходима его экстренная хирургическая санация.
Литература
Ю. Я. Венгеров*, доктор медицинских наук, профессор
М. В. Нагибина*, кандидат медицинских наук
Е. П. Михалинова*
С. Е. Раздобарина*
Т. Н. Молотилова**, кандидат медицинских наук
Ю. Г. Пархоменко**, доктор медицинских наук, профессор
Н. В. Мозгалева**
Т. Ю. Смирнова**
Т. С. Свистунова**, кандидат медицинских наук
* ГБОУ ВПО МГМСУ им. А. И. Евдокимова МЗ РФ, ** ГКУЗ ИКБ № 2 ДЗМ, Москва
Общие сведения
Этиология и патогенез менингита
Менингит может возникать несколькими путями инфицирования. Контактный путь — возникновение менингита происходит в условиях уже существующей гнойной инфекции. Развитию синусогенного менингита способствует гнойная инфекция околоносовых пазух (гайморит), отогенного — сосцевидного отростка или среднего уха (отит), одонтогенного происхождения — патология зубов.Занос инфекционных агентов в мозговые оболочки возможен лимфогенным, гематогенным, чрезплацентарным, периневральным путями, а также в условиях ликвореи при открытой черепно-мозговой травме или позвоночно-спинномозговой травмы, трещине или переломе основания черепа.
Возбудители инфекции, попадая в организм через входные ворота (бронхи, ЖКТ, носоглотка), вызывают воспаление (серозного или гнойного типа) мозговых оболочек и прилегающих тканей мозга. Последующий их отек приводит к нарушению микроциркуляции в сосудах мозга и его оболочках, замедлению резорбции цереброспинальной жидкости и ее гиперсекреции. При этом повышается внутричерепное давление, развивается водянка мозга. Возможно дальнейшее распространение воспалительного процесса на вещество мозга, корешки черепных и спинномозговых нервов.
Классификация менингитов
Менингиты классифицируются по нескольким критериям.
По этиологии:
- бактериальные (пневмококковый, туберкулезный, менингококковый и др.)
- вирусные (вызванный энтеровирусами Коксаки и ЕСНО, острый лимфоцитарый хориоменингит и др.)
- грибковые (криптококкозный, кандидозный и др.)
- протозойные (при малярии, при токсоплазмозе и др.)
По характеру воспалительного процесса:
- гнойный (в ликворе преобладают нейтрофилы)
- серозный (в ликворе преобладают лимфоциты)
По патогенезу:
- первичные (в анамнезе отсутствует общая инфекция или инфекционное заболевание какого-либо органа)
- вторичные (как осложнение инфекционного заболевания)
По распространенности процесса:
По темпу течения заболевания:
- молниеносные
- острые
- подострые
- хронические
По степени тяжести:
- легкой формы
- средней тяжести
- тяжелой формы
- крайне тяжелой формы
Клиническая картина менингита
Симптомокомплекс любой формы менингита включает в себя общеинфекционные симптомы (жар, озноб, повышение температуры тела), учащение дыхания и нарушение его ритма, изменение ЧСС (в начале заболевания тахикардия, по мере прогрессирования заболевания — брадикардия).
В состав менингеального синдрома входят общемозговые симптомы, проявляющиеся тоническим напряжением мышц туловища и конечностей. Нередко появляются продормальные симптомы (насморк, боли в животе и др.). Рвота при менингите не связана с приемом пищи, а появляется сразу после смены положения или при усилении головной боли. Головные боли, как правило, распирающего характера очень мучительны для пациента, могут локализоваться в затылочной области и отдавать в шейный отдел позвоночника. Кроме того, пациенты болезненно реагируют на малейший шум, прикосновения, свет, поэтому стараются избегать разговоров и лежат с закрытыми глазами. В детском возрасте возможно появление судорог.
Для менингита характерна гиперестезия кожи и болезненность черепа при перкуссии. В начале заболевания отмечается повышение сухожильных рефлексов, но с развитием заболевания они снижаются и нередко исчезают. В случае вовлечения в воспалительный процесс вещества мозга развиваются параличи, патологические рефлексы и парезы. Тяжелое течение менингита обычно сопровождается расширением зрачков, диплопией, косоглазием, нарушение контроля над тазовыми органами (в случае развития психических расстройств).
Симптомы менингита в старческом возрасте атипичны: слабое проявление головных болей или полное их отсутствие, тремор головы и конечностей, сонливость, психические расстройства (апатия или, наоборот, психомоторное возбуждение).
Диагноз и диффдиагноз
Основным методом диагностирования (или исключения) менингита является люмбальная пункция с последующим исследованием цереброспинальной жидкости. В пользу данного метода говорят его безопасность и простота, поэтому проведение люмбальной пункции показано во всех случаях подозрения на менингит. Для всех форм менингита характерно вытекание жидкости под высоким давлением (иногда струей). При серозном менингите цереброспинальная жидкость прозрачная (иногда слегка опалесцирующая), при гнойном менингите — мутная, желто-зеленого цвета. С помощью лабораторных исследований цереброспинальной жидкости определяют плеоцитоз (нейтрофилы при гнойных менингитах, лимфоциты при серозных менингитах), изменение соотношения количества клеток и повышенное содержание белка.
В целях выяснения этиологических факторов заболевания рекомендовано определение уровня глюкозы в цереброспинальной жидкости. В случае туберкулезного менингита, а также менингита, вызванного грибами, уровень глюкозы снижается. Для гнойных менингитов типично значительное (до нуля) снижение уровню глюкоза.
Главные ориентиры невролога в дифференциации менингитов — исследование цереброспинальной жидкости, а именно определение соотношения клеток, уровня сахара и белка.
Лечение менингита
В случае подозрения на менингит госпитализация пациента обязательна. При тяжелом течении догоспитального этапа (угнетение сознания, лихорадка) пациенту вводят преднизолон и бензилпенициллин. Проведение люмбальной пункции на догоспитальном этапе противопоказано.
Основа лечения гнойного менингита — раннее назначение сульфаниламидов (этазол, норсульфазол) или антибиотиков (пенициллина). Допускает введение бензилпенициллина интралюмбально (в крайне тяжелом случае). Если подобное лечение менингита в течение первых 3 дней оказывается неэффективным, следует продолжить терапию полусинтетическими антибиотиками (ампициллин+оксациллин, карбенициллин) в сочетании с мономицином, гентамицином, нитрофуранами. Доказана эффективность такого сочетания антибиотиков до выделения патогенного организма и выявления его чувствительности к антибиотикам. Максимальный срок такой комбинационной терапии — 2 недели, после чего необходимо перейти на монотерапию. Критериями для отмены также служат снижение температуры тела, нормализация цитоза (до 100 клеток), регресс общемозговых и менингеальных симптомов.
Основу комплексного лечения туберкулезного менингита состоит в непрерывном введении бактериостатических доз двух-трех антибиотиков (например, изониазид+стрептомицин). При появлении возможных побочных эффектов (вестибулярные расстройства, нарушение слуха, тошнота) отмена данного лечения не требуется, показано уменьшение дозы антибиотиков и временное добавление к лечению десенсибилизирующих препаратов (дифенгидрамин, прометазин), а также других противотуберкулезных препаратов (рифампицин, ПАСК, фтивазид). Показания к выписке пациента: отсутствие симптомов туберкулезного менингита, санация цереброспинальной жидкости (спустя 6 месяцев от начала заболевания) и улучшение общего состояние пациента.
Лечение вирусного менингита может ограничиться применением симптоматических и общеукрепляющих средств (глюкоза, метамизол натрия, витамины, метилурацил). В тяжелых случаях (выраженные общемозговые симптомы) назначают кортикостероиды и диуретики, реже — повторную спинномозговую пункцию. В случае наслоения бактериальной инфекции возможно назначение антибиотиков.
Прогноз
В дальнейшем прогнозе важную роль играют форма менингита, своевременность и адекватность лечебных мероприятий. В качестве резидуальных симптомов после туберкулезного и гнойного менингита зачастую остаются головные боли, внутричерепная гипертензия, эпилептические припадки, нарушения зрения и слуха. По причине запоздалого диагностирования и устойчивости возбудителя к антибиотикам высок уровень смертности от гнойных менингитов (менингококковая инфекция).
Профилактика
В качестве профилактических мер по предупреждению менингита предусматривается регулярное закаливание (водные процедуры, спорт), своевременная терапия хронических и острых инфекционных заболеваний, а также короткие курсы иммуностимулирующими препаратами (элеутерококк, женьшень) в очагах менингококкового менингита (детский сад, школа и др.).
Гнойный менингит — воспалительный процесс, возникающий в мягкой оболочке головного мозга при проникновении в нее гноеродных микроорганизмов (пневмококков, менингококков, стрептококков и пр.). Гнойный менингит характеризуется высокой температурой тела, интенсивной головной болью, тошнотой, рвотой, нарушениями со стороны черепно-мозговых нервов, ранним появлением менингеальных симптомов, гиперестезией, расстройством сознания, психомоторным возбуждением. Диагностировать гнойный менингит можно на основании типичной клинической картины и данных анализа цереброспинальной жидкости. Гнойный менингит является показанием к обязательному проведению антибиотикотерапии. Применяются противоотечные препараты, глюкокортикостероиды, транквилизаторы, противосудорожные средства и пр. симптоматическая терапия.
МКБ-10
Общие сведения
Гнойный менингит — это воспаление мозговых оболочек (менингит), имеющее бактериальную этиологию. Гнойный менингит встречается с частотой 3,3 случаев на 100 тыс. населения. Заболеванию подвержены все возрастные категории, но наиболее часто гнойный менингит развивается у детей до 5 лет. Отмечено, что гнойный менингит часто возникает на фоне ослабленного состояния иммунной системы. Повышение заболеваемости наблюдается в зимне-весенний период. С начала 90-х годов прошлого века произошло существенное снижение заболеваемости гнойным менингитом, уменьшение числа летальных исходов и случаев развития тяжелых осложнений.

Причины возникновения гнойного менингита
К развитию гнойного менингита может приводить не только менингококковая инфекция, но также пневмококки, гемофильная палочка и другие бактерии. Почти половина случаев гнойного менингита приходится на долю гемофильной палочки. В 20% причиной гнойного менингита является менингококк, в 13% случаев — пневмококк. У новорожденных гнойный менингит зачастую возникает в результате стрептококковой инфекции, сальмонеллеза или инфицирования кишечной палочкой.
В зависимости от механизма проникновения возбудителя в оболочки головного мозга в неврологии выделяют первичный и вторичный гнойный менингит. Первичный гнойный менингит развивается при гематогенном распространении возбудителя из полости носа или глотки, куда он попадает из внешней среды. Заражение происходит от больных лиц и носителей воздушно-капельным и контактным путем. Прямое инфицирование мозговых оболочек возможно при переломе черепа и открытой черепно-мозговой травме, открытых повреждениях сосцевидного отростка и придаточных пазух носа, недостаточно тщательном соблюдении правил асептики в ходе нейрохирургических вмешательств.
Вторичный гнойный менингит возникает на фоне имеющегося в организме первичного септического очага, инфекция из которого проникает в оболочки головного мозга. Контактное распространение гноеродных микроорганизмов может наблюдаться при абсцессе головного мозга, остеомиелите костей черепа, септическом синустромбозе. Гематогенное и лимфогенное распространение возбудителя возможно из инфекционного очага любой локализации, но наиболее часто происходит при длительно протекающих инфекциях лор-органов (остром среднем отите, хроническом гнойном среднем отите, синуситах).
Проникновению возбудителей гнойного менингита через гематоэнцефалический барьер способствует ослабленное состояние иммунной системы организма, которое может быть вызвано частыми ОРВИ, гиповитаминозом, перенесенным стрессом, физическими перегрузками, резкой сменой климата.
Классификация гнойного менингита
В зависимости от тяжести клинических проявлений гнойный менингит классифицируется на легкую, среднетяжелую и тяжелую формы. Тяжелые формы заболевания наблюдаются в основном на фоне резкого снижения иммунитета и у пациентов с удаленной селезенкой.
По особенностям течения выделяют молниеносный, абортивный, острый и рецидивирующий гнойный менингит. Наиболее часто встречается острый гнойный менингит с типичными общемозговыми и оболочечными симптомами. Молниеносное течение гнойного менингита с первых часов заболевания характеризуется быстрым нарастанием отека головного мозга, приводящего к нарушению сознания и витальных функций. Абортивный вариант отличается стертой клинической картиной, в которой на первый план выходят симптомы интоксикации. Рецидивирующий гнойный менингит может наблюдаться при недостаточном или запоздалом лечении острой формы заболевания, а также при наличии в организме хронического очага гнойной инфекции.
Симптомы гнойного менингита
Инкубационный период первичного гнойного менингита в среднем длится от 2 до 5 суток. Типично острое начало с резкого повышения температуры тела до 39-40°С, сильного озноба, интенсивной и нарастающей головной боли, тошноты и многократной рвоты. Могут наблюдаться психомоторное возбуждение, бред, нарушения сознания. В 40% случаев гнойный менингит протекает с судорожным синдромом. Специфичные для менингита оболочечные симптомы (симптом Кернига, Брудзинского, Гийена, ригидность затылочных мышц) выражены с первых часов заболевания и усиливаются на 2-3-й день. Типичны выраженная гиперестезия и снижение брюшных рефлексов на фоне общего повышения глубоких рефлексов. Возможно появление диффузной сыпи геморрагического характера.
Очаговая симптоматика, сопровождающая гнойный менингит, чаще всего заключается в нарушении функций различных черепно-мозговых нервов. Наиболее часто наблюдается поражение глазодвигательных нервов, приводящее к двоению, развитию косоглазия, опущению верхнего века и появлению разницы в размере зрачков (анизокории). Реже отмечается неврит лицевого нерва, поражение тройничного нерва, расстройство функции зрительного нерва (выпадение полей зрения, снижение остроты зрения) и преддверно-улиткового нерва (прогрессирующая тугоухость). Более тяжелая очаговая симптоматика свидетельствует о распространении воспалительных изменений на вещество головного мозга или о развитии сосудистых нарушений по типу ишемического инсульта, обусловленных васкулитом, рефлекторным спазмом или тромбозом сосудов головного мозга.
При переходе воспалительного процесса на вещество мозга говорят о развитии менингоэнцефалита. При этом гнойный менингит протекает с присоединением характерной для энцефалита очаговой симптоматики в виде парезов и параличей, нарушений речи, изменений чувствительности, появления патологических рефлексов, повышения мышечного тонуса. Возможны гиперкинезы, галлюцинаторный синдром, нарушения сна, вестибулярная атаксия, расстройства поведенческих реакций и памяти. Распространение гнойного процесса на желудочки мозга с развитием вентрикулита проявляется спастическими приступами по типу горметонии, сгибательными контрактурами рук и разгибательными ног.
Осложнения гнойного менингита
Ранним и грозным осложнением, которым может сопровождаться гнойный менингит, является отек головного мозга, приводящий к сдавлению мозгового ствола с расположенными в нем жизненно важными центрами. Острый отек головного мозга, как правило, возникает на 2-3-й день заболевания, при молниеносной форме — в первые часы. Клинически он проявляется двигательным беспокойством, нарушением сознания, расстройством дыхания и нарушениями со стороны сердечно-сосудистой системы (тахикардия и артериальная гипертензия, в терминальной стадии сменяющиеся брадикардией и артериальной гипотонией).
Среди прочих осложнений гнойного менингита могут наблюдаться: септический шок, надпочечниковая недостаточность, субдуральная эмпиема, пневмония, инфекционный эндокардит, пиелонефрит, цистит, септический панофтальмит и др.
Диагностика гнойного менингита
Типичные клинические признаки, наличие менингеальных симптомов и очаговой неврологической симптоматики в виде поражения черепно-мозговых нервов, как правило, позволяют неврологу предположить у пациента гнойный менингит. Более затруднительна диагностика в случаях, когда гнойный менингит имеет абортивное течение или возникает вторично на фоне симптомов существующего септического очага другой локализации. Чтобы подтвердить гнойный менингит необходимо произвести люмбальную пункцию, в ходе которой выявляется повышенное давление ликвора, его помутнение или опалесцирующая окраска. Последующее исследование цереброспинальной жидкости определяет увеличенное содержание белка и клеточных элементов (в основном за счет нейтрофилов). Выявление возбудителя производится в ходе микроскопии мазков цереброспинальной жидкости и при ее посеве на питательные среды.
С диагностической целью производят также анализ крови и отделяемого элементов кожной сыпи. При предположении о вторичном характере гнойного менингита проводятся дополнительные обследования, направленные на поиск первичного инфекционного очага: консультация отоларинголога, пульмонолога, терапевта; рентгенография околоносовых пазух, отоскопия, рентгенография легких.
Дифференцировать гнойный менингит необходимо от вирусного менингита, субарахноидального кровоизлияния, явлений менингизма при других инфекционных заболеваниях (сыпном тифе, лептоспирозе, тяжелых формах гриппа и др.).
Лечение гнойного менингита
Все имеющие гнойный менингит пациенты подлежат лечению в условиях стационара. Таким больным должна быть неотложно проведена люмбальная пункция и бактериоскопическое исследование ликвора. Сразу же после установления этиологии менингита пациенту назначается антибиотикотерапия. В большинстве случаев она представляет собой сочетание ампициллина с препаратами цефалоспоринового ряда (цефтриаксоном, цефотаксимом, цефтазидимом). При гнойном менингите неустановленной этиологии стартовая терапия заключается во внутримышечном введении аминогликозидов (канамицина, гентамицина) или их комбинации с ампициллином. Тяжело протекающий гнойный менингит может потребовать внутривенного или интратекального введения антибиотиков.
С целью уменьшения гидроцефалии и отека мозга при гнойном менингите назначают дегидратационную терапию (фуросемид, маннитол). Патогенетическое лечение гнойного менингита также включает применение глюкокортикостероидных препаратов (дексаметазона, преднизолона), дозы которых зависят от тяжести заболевания. Наряду с этим производится необходимая симптоматическая терапия. При нарушениях сна назначаются транквилизаторы; для купирования психомоторного возбуждения и судорог — литические смеси (хлорпромазин, дифенгидрамин, тримеперидина), диазепам, вальпроевая кислота; при гиповолемии и развитии инфекционно-токсического шока проводится инфузионная терапия.
В восстановительном периоде после перенесенной острой фазы гнойного менингита рекомендован прием ноотропных и нейропротекторных препаратов, витаминотерапия и общеукрепляющее лечение. Лечение пациентов, имеющих вторичный гнойный менингит, должно включать ликвидацию первичного септического очага, в том числе и путем хирургического вмешательства (санирующая операция при среднем отите, фронтотомия, этмоидотомия, сфенотомия, удаление внутримозгового абсцесса и т. п.).
Прогноз гнойного менингита
По некоторым данным в 14% случаев гнойный менингит приводит к летальному исходу. Однако при своевременно начатом и корректно проведенном лечении гнойный менингит имеет в основном благоприятный прогноз. После перенесенного менингита может наблюдаться астения, ликворно-динамические нарушения, нейросенсорная тугоухость, отдельные слабо выраженные очаговые симптомы. Тяжелые последствия гнойного менингита (гидроцефалия, амавроз, глухота, деменция, эпилепсия) в наше время являются редкостью.
Профилактика гнойного менингита
На сегодняшний день наиболее эффективным способом, позволяющим предупредить гнойный менингит, является вакцинация. Прививки проводится против основных возбудителей гнойного менингита: гемофильной палочки, менинго- и пневмококков. В России эти вакцины не считаются обязательными и вводятся по показаниям или по желанию пациентов.
Вакцинация против гемофильной инфекции проводится в основном детям в возрасте от 3 месяцев до 5 лет и людям, страдающим иммунодефицитными состояниями в результате ВИЧ-инфекции, проведения иммуносупрессивной терапии онкозаболеваний, удаления тимуса или селезенки и т. п. Вакцинация против менингококковой инфекции рекомендована детям после 18 месяцев и взрослым. Детям до 18 месяцев вакцинация проводится по эпидемическим показаниям (например, если менингококковый гнойный менингит диагностирован у одного из членов семьи). В регионах, опасных по менингококковому гнойному менингиту, вакцинация должна проводиться пациентам с иммунодефицитом и людям, имеющим анатомические дефекты черепа. Вакцинация против пневмококковой инфекции показана часто болеющим детям, пациентам с частыми пневмониями и отитами, в случаях пониженного иммунитета.
Пневмококковые инфекции — группа бактериальных заболеваний, которые проявляются проявляющихся гнойно-воспалительными изменениями в разных органах и системах, чаще всего проходящих в легких по типу крупозной пневмонии и в ЦНС по типу гнойного менингита.
Пневмококки постоянно живут в верхних дыхательных путях взрослых и детей, потому их относят к условно-патогенным микроорганизмам. У большинства здоровых детей пневмококки обнаруживают в посевах слизи из ротоглотки. Носители данного возбудителя это в основном дети раннего возраста и пожилые люди. Предполагают, что во время носительства формируется иммунитет – скорее типоспецифический, чем напряженный. Болезнь в этих случаях может развиться, только если резко снизилась иммунная реактивность организма во время тяжелых форм гриппа и ОРВИ, долговременного применения кортикостероидных гормонов, цитостатиков и т. д.
Эпидемии возникают из-за клонов пневмококков с большей вирулентностью и инвазивностью. Они зарождаются при неблагоприятных условиях внешней среды у ослабленных детей. Этому способствует скученность (например, в детских коллективах), холодное время года, повышенная заболеваемость ОРВИ). Инфекцию всегда переносит человек – как больной, так и носитель. Пути передачи пневмококковой инфекции: воздушно-капельный, контактно-бытовой.
Заболеванию подвержены дети с дефицитом типоспецифических антител. Особенно тяжело протекает болезнь у малышей с серповидно-клеточной анемией или дефицитом С3.
Что провоцирует / Причины Пневмококковой инфекции у детей:
Изначальное название пневмококков – Diphcoccus pneumoniae. На сегодня возбудитель переименован на Streptococcus pneumonia и отнесен к семейству Streptococcaceae, роду Streptococcus.
Пневмококки представляют собой грамположительные овальные или сферические кокки, размер которых от 0,5 до 1,25 мкм. Располагаются они попарно, иногда – короткими цепочками. Ранее кокки назывались ланцетовидными диплококками за свою форму ланцета (дистальный конец каждой пары заостренный). Пневмококки имеют хорошо организованную капсулу. Выделяют более 85 сероваров пневмококков по полисахаридному составу капсулы.
Пневмококки имеют капсульные антигены, а также соматические, которых насчитывается три. Разрушение пневмококков сопровождается высвобождением эндотоксина. Во внешней среде пневмококки устойчивы. Могут сохраняться 1-2 месяца в высушенной мокроте, а на зараженных пеленках около 1-2 недель. Мгновенно погибают при кипячении. Около 10 минут могут жить при температуре среды 50-60 ˚С. Пневмококки имеют высокую чувствительность к распространенным дезинфицирующим средствам.

Патогенез (что происходит?) во время Пневмококковой инфекции у детей:
По лимфе и крови пневмококки распространяются из первичного очага поражения, что приводит к пролонгированной бактериемии. Она может проходить без симптомов или как инфекционно-токсический синдром. Если организм ребенка ослаблен, пневмококки могут преодолеть гематоэнцефалический барьер и вызвать менингит/ менингоэнцефалит.
Распространение инфекции контактным бронхогенным путем может привести к гнойному плевриту, среднему отиту, гаймориту, перикардиту, мастоидиту, эпидуральному абсцессу, эмпитеме. Пневмококковая бактериемия в некоторых случаях может привести к гнойному артриту, остеомиелиту, абсцессу мозга.
Тяжелые формы пневмококковой инфекции свойственны в основном грудничкам. Тяжесть болезни зависит от вирулентности возбудителя и от реактивности макроорганизма. Болезнь проходит особенно тяжело в случае массивной бактериемии. В тяжелых случаях пневмококкые заболевания сопровождаются развитием реологических и гемодинамических нарушений вплоть до возникновения острой надпочечниковой недостаточности, диссеминированного внутрисосудистого свертывания крови, отека и набухания вещества мозга.
Симптомы Пневмококковой инфекции у детей:
Пневмококковую инфекцию у детей классифицируют по критерию очага поражения. Выделяют такие виды:
- крупозная пневмония
- пневмококковый менингит
- эндокардит
- остеомиелит .
Такая форма как крупозная пневмония представляет собой острое воспаление легких с быстрым вовлечением в процесс доли легкого и прилегающего участка плевры. Болезни подвержены в основном дети школьного возраста и подростки. Крайне редко случается крупозная пневмония у грудничков. Морфологические изменения при данном заболевании происходят по стадиям. Патологический процесс, как правило, начинается в задних и заднебоковых отделах правого легкого в виде небольшого фокуса воспалительного отека, который быстро увеличивается, формируя фазу гиперемии и серозной экссудации (стадия прилива) с размножением в экссудате пневмококков. Далее наступает фаза миграции лейкоцитов и выпадения фибрина (стадия гепатизации) с последующим постепенным рассасыванием элементов экссудата — лейкоцитов и фибрина на стадии разрешения.
Крупозная пневмония у детей начинается остро с таких симптомов как озноб и боли в боку, которые становятся сильнее при глубоких вдохах, сухой кашель, слабость, головная боль, повышенная температура (доходит до 39 - 40 °С), разбитость, возбужденность, в некоторых случаях бредовые состояния.
Вскоре появляются такие симптомы:
- гиперемия щек;
- короткий болезненный кашель с выделением небольшого количества вязкой стекловидной мокроты;
- учащенное поверхностное дыхание;
- раздувание крыльев носа;
- герпетические высыпания на крыльях носа;
- герпетические высыпания на губах; губ (в некоторых случаях);
- цианоз кончиков пальцев (в некоторых случаях).
Наблюдается отставание грудной клетки при дыхании на стороне поражения. Если процесс локализирован в нижней доле правого легкого, болит не только грудная клетка, но и живот, потому есть шанс спутать крупозную пневмонию у детей с болезнями брюшной полости, такими как перитонит, аппендицит, панкреатит и прочие. У детей может отмечаться частый жидкий стул, повторная рвота, вздутие живота. Эти симптомы также могут указывать на острую кишечную инфекцию, что утрудняет диагностический процесс.
Когда процесс локализирован в верхней доле правого легкого, могут возникнуть такие менингеальные симптомы как судороги, ригидность мышц затылка, резкая головная боль, частая рвота и проч. В тяжелых состояниях возможен бред.
Изменения в легких претерпевают весьма характерное развитие. В типичных случаях в первые сутки на пораженной стороне отмечают отметить тимианический оттенок перкуторного звука, потом всего за несколько часов звук становится притупленным. Под конец первых суток заболевания на высоте вдоха выслушивают крепитацию и мелкопузырчатые влажные или сухие хрипы.
Пик крупозной пневмонии приходится на 2-3-й день от начала заболевания. На пике притупление в зоне поражения становится резко выраженным и над очагом поражения начинает выслушиваться бронхиальное дыхание, иногда шум трения плевры, голосовое дрожание и бронхофония. При этом кашель становится сильнее, более влажным и болезненным. Мокрота в некоторых случаях становится красновато-коричневого оттенка. Одышка нарастает, а цианоз губ и лица усиливается.
Анализ крови на пике болезни показывает нейтрофильный лейкоцитоз, увеличение содержания палочкоядерных до 10— 30%, может быть сдвиг формулы до юных и миелоцитов. В частых случаях выявляется токсическая зернистость нейтрофилов, типичны анэозинофилия, умеренный моноцитоз, повышение СОЭ.
Рентген показывает основные стадии развития крупозной пневмонии. На стадии прилива видно небольшое прозрачности в зоне пораженного участка, усиление легочного рисунка из-за полнокровия сосудов. Стадия гепатизации отмечается выраженным понижением прозрачности участка пораженного легкого, картина похожа на ателектаз (спадение доли легкого). На стадии разрешения ренгенограмма показывает медленное восстановление прозрачности пораженного участка легкого. В некоторых случаях бывает жидкость в плевральной полости, что называется плевропневмонией. Болезнь длится в общем примерно 3-4 недели (зависит от каждого индивидуального случая). Лихорадочный период (повышенная температура) длится от 7 до 10 суток. Структура и функции легких полностью восстанавливаются спустя 1-1,5 месяца.
Пневмококковый менингит является самой тяжелой формой гнойного менингита у детей. Болезнь характерна для детей от 6 до 12-ти месяцев. До 5-ти месяцев жизни это заболевание встречается крайне редко. У детей старшего возраста пневмококковый менингит обычно возникает после травмы черепа или хронических заболеваний придаточных пазух носа, а также болезнь характерна для детей с нарушениями иммунитета (как врожденными, так и приобретенными). В группе риска – дети с онкологическими заболеваниями или серповидно-клеточной анемией. Поражение мозговых оболочек – вторичное явление, сначала следуют другие проявления инфекции, вызванной пневмококками.
Пневмококковый менингит, как правило, имеет острое начало, температура тела сильно повышена. Но если ребенок ослаблен, температура может достигать субфебрильных значений, а в редких случаях остается в норме. У детей проявляется беспокойство, они срыгивают и кричат. Среди первых симптомов часто отмечают тремор, судороги, выбухание большого родничка, гиперестезию, а в тяжелых случаях и потерю сознания. Менингеальный синдром неярко выраженный и часто неполный. В большинстве случаев болезнь начинается сразу как менингоэнцефалит. В таких случаях с первых суток отмечают нарушение сознания, судороги, тремор конечностей, резкое психомоторное возбуждение, что переходит в сопор и кому.
Спинномозговая жидкость гонойная, мутная, зеленовато-серого оттенка. Отстаивание приводит к выпадению осадка. В жидкости наблюдается нейтрофильный плеоцитоз, высокое содержание белка, пониженное количество сахара и хлоридов.
Анализ крови показывает лейкоцитоз с резким сдвигом влево, моноцитоз, анэозинофилию. Вероятная также умеренная анемия. СОЭ выше нормы.
Пневмококки в ряде случаев выступают возбудителями гнойного артрита, среднего отита, перикардита, остеомиелита, первичного перитонита, эндокардита и пр. Эти болезни могут быть как самостоятельными, так и возникают на фоне пневмонии, трахеита, бронхита. Они характерны в основном для детей раннего возраста. По симптоматике они неотличимы от болезней, вызванных иными гноеродными бактериями.
Диагностика Пневмококковой инфекции у детей:
Диагностика пневмококковой инфекции у детей требует выделения возбудителя из очага поражения или крови больного ребенка. При подозрении на крупозную пневмонию берут мокроту для исследования. При подозрении на сепсис для анализов используют кровь, а при подозрении на другие болезни пневмококковой природы берут воспалительный экссудат или гнойное отделяемое.
Патологический материал отправляют на микроскопическое исследование. Основанием для предварительной диагностики выступает обнаружение грамположительпых диплококков ланцетовидной формы, окруженных капсулой. Далее устанавливают принадлежность обнаруженных кокков к пневмококкам с помощью комбинированных типоспецифических сывороток, содержащих в высоких титрах антитела ко всем серотипам пневмококка. В первые несколько суток от начала пневмококкового менингита есть шанс найти возбудитель в спинномозговой жидкости. В ней он может располагаться внеклеточно или внутриклеточно. Чтобы выделить чистую культуру, делают посев исследуемого материала на кровяной, асцитический или сывороточный агар.
Пневмококк на питательных средах дает рост мелких прозрачных колоний. Чтобы выделить чистую культуру, в некоторых случаях применяют биологическую пробу. Для этой цели заражают белых мышей внутрибрюшинно исследуемым материалом. Если в материале есть патогенные пневмококки, мыши погибают через сутки-двое.
Лечение Пневмококковой инфекции у детей:
Лечение пневмококковой инфекции должно быть комплексным. Выраженные формы требуют лечения антибиотиками.
Легкие и среднетяжелые формы (такие как бронхит, назофарингит и отит) можно лечить фепоксиметилпенициллином (вепикомбином). Доза 50000—100000 ЕД на 1 кг тела в сутки, разделенная на 4 приема (принимают внутрь). Или назначается пенициллин в аналогичной дозе, 3 раза в сутки, вводится внутримышечно. Курс – от 5 до 7 дней. Другой вариант – назначается азитромицин (сумамед) из расчета 10 мг/кг в день, курс 3 суток.
Больных крупозной пневмонией или менингитом лечат цефалоспориновым антибиотиком 3-го и 4-го поколения. В ходе антибиотикотерапии рекомендуется проверять чувствительность выделенных пневмококков к назначенному препарату и при необходимости его заменять. В последние годы часто выделяют штаммы пневмококков, которые устойчивы ко многим антибиотикам.
Тяжелые формы пневмококковой инфекции лечат не только антибиотиками, но и инфузионной, патогенетической, общеукрепляющей и симптоматической терапией по принципам, аналогичным таковым при иных инфекционных заболеваниях.
При пневмококковом менингите летальные исходы составляют 10-20%. При других формах болезни летальные исходы случаются редко. Смертью болезнь может кончиться у детей с врожденным или приобретенным иммунодефицитом, длительно леченных иммуносупрессивными препаратами, у детей с врожденными уродствами.
Профилактика Пневмококковой инфекции у детей:
Ее вводят детям от 2-х лет из группы риска по пневмококковой инфекции: детям с асготенией, иммунодефицитами, хронической патологией почек, серповидно-клеточной анемией, хронической патологией сердца. Вакцина вводится единоразово подкожно или внутримышечно, доза составляет 0,5 мл. Эта вакцина редко вызывает побочные реакции, обладает высокой иммуногенностыо. После вакцинации антитела в крови сохраняются до 5-ти лет. Противопоказанием к введению пневмококковой вакцины является гиперчувствительность к составным компонентам вакцины.
Детям с иммунодефицитным состоянием в случае контакта с больным пневмококковой инфекцией можно вводить гамма-глобулин по 0,2 мл/кг внутримышечно.
К каким докторам следует обращаться если у Вас Пневмококковая инфекция у детей:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Пневмококковой инфекции у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Менингит (от греч. meninx - мозговая оболочка) - воспаление оболочек головного и спинного мозга. Менингит может быть вызван различными вирусами и бактериями, и даже грибком.
Пневмококковый менингит вызывает Streptococcus pneumonie, окрашивается по Граму положительно. Источником инфекции являются больные различными формами пневмококковой инфекции и носители пневмококка. Основной путь передачи - воздушно-капельный. Болеют, преимущественно, дети старше 10 лет.
Что провоцирует / Причины Пневмококкового менингита:
Пневмококковый менингит стоит на втором месте после менингококкового менингита. Возбудителями являются пневмококки различных типов. Болеют данной формой менингита обычно дети раннего возраста.
Возбудитель менингита - Streptococcus pneumoniae (пневмококк) - серологически неоднороден и насчитывает 84 серовара. Возбудитель впервые был выделен Пастером (1881). Микроб неподвижен, спор и капсул не образует, аэроб или факультативный анаэроб. Представляет собой овальные или ланцетоподобные кокки диаметром около 1 мкм. В мазках из клинического материала располагается парами, которые окружены толстой капсулой. Хорошо растет на средах с добавлениями крови или сыворотки, 0,1% раствора глюкозы при температуре 37 °С.
Путь передачи возбудителя воздушно-капельный, источником инфекции являются больны и носители. Пик заболеваемости приходится на осеннее зимний период.
Роль пневмококка как этиологического фактора в возникновении гнойного менингита впервые установлена Netter в 1909 г., когда были описаны случаи заболевания у ряда больных с тяжелыми формами пневмонии. Позднее было доказано (Э. Д. Гинзбург, 1936; А. Л. Декельман, 1949; Г. Фанкони, А. Вальгрен, 1960), что пневмококковый менингит чаще носит вторичный характер, осложняя течение не только пневмонии, но и гнойного отита, мастоидита, синусита, острого бактериального кардита. Так, по статистическим данным С. Л. Кипнис (1957), пневмония выявлена в 18 из 42 случаев пневмококкового менингита. В наблюдениях А. Л. Декельман (1948) пневмония предшествовала менингиту или возникала почти одновременно с ним в 26,5% случаев. Л. К. Коровицкий и Р. П. Наумова (1957) сообщают о 26 случаях пневмонии у 63 больных пневмококковым менингитом.
Развитию заболевания предшествует наличие гнойного очага:
- отиты;
- гаймориты;
- пневмонии.
Патогенез (что происходит?) во время Пневмококкового менингита:
Симптомы Пневмококкового менингита:
Принято различать две основные формы пневмококкового менингита:
1) острую, с вариантом злокачественного синдрома типа Утерхауза - Фридрихсена (молниеносная форма);
2) затяжную и разновидность ее - рецидивирующую.
Острые формы пневмококкового менингита встречаются в основном у детей старшего возраста и взрослых. Они характеризуются внезапным началом с повышением температуры до 38°, реже до более высоких цифр, тяжелым начальным токсикозом с общемозговыми явлениями (нарушение сознания) и энцефалитическими реакциями (тремор конечностей, судороги). В ряде случаев в первые дни болезни выявляется парез черепномозговых нервов, чаще отводящего и глазодвигательного. Изредка встречаются моно- и гемипарезы.
Начало заболевания острое. Характерен резкий подъем температуры тела до 39-40°С, быстрое нарастание интоксикации: общая слабость, бледность кожи, периорбитальный цианоз, отказ от еды и питья. Появляются беспокойство, сильнейшая головная боль, многократная рвота. Для детей раннего возраста характерен монотонный стонущий крик; большой родничок выбухает и напряжен, возможно расхождение швов черепа с увеличением окружности головы. На 2-3 день болезни определяются менингеальные симптомы, особенно выражена ригидность затылочных мышц. У большинства больных пневмококковый менингит с первых дней болезни протекает как менингоэнцефалит. Характерно быстрое угнетение сознания, повторные судороги, появление очаговой симптоматики в виде гемипареза, глазодвигательных расстройств, гиперкинезов, атаксии. Постепенно, к 3-4 дню болезни развивается судорожно-коматозный статус с нарастанием симптомов дислокации и вклинения ствола мозга.
При развитии сепсиса может отмечаться поражение других органов: геморрагическая сыпь на коже (по типу менингококцемии), пневмония, эндо- и перикардит, артриты и др.
Пневмококковый менингит, возникший на фоне имеющегося первичного очага воспаления (гнойный отит, мастоидит, синусит, пневмония) начинается подостро, малосимптомно, но отличается особо тяжелым течением и чаще, чем первичный пневмококковый менингит, заканчивается летально. При септическом течении болезни возможно появление на коже геморрагической сыпи, по характеру и локализации напоминающей менингококковую. Однако в начале заболевания сыпь может быть розеолезно-папулезной и только в последующие дни болезни трансформироваться в геморрагическую. В отличие от менингококковой сыпи, при пневмококковом менингите она более стойкая, медленно поддается обратному развитию. Неблагоприятные исходы такого течения болезни обусловлены, как правило, поздней диагностикой и поздно начатым этиотропным лечением. Именно этим объясняется характерная для пневмококкового менингита частота рецидивов заболевания, а также тот факт, что у 22–24 % детей после перенесенного заболевания остаются неврологические осложнения в виде отчетливой неврологической симптоматики: глухоты, слепоты, амнезии, параличей, других признаков поражений ЦНС.
Исходы пневмококкового менингита во многом зависят от своевременной диагностики и адекватно начатого лечения. При несоблюдении этих правил болезнь принимает затяжное течение и нередко заканчивается летально. Выделяют три группы причин летальных исходов. Основной причиной летальных исходов является менингоэнцефалит с выраженными признаками отека-набухания мозга. Другая причина - выраженная легочно-сердечная недостаточность, развившаяся на фоне поражения ЦНС. И третьей причиной является септический процесс с развитием тромбо¬геморрагического синдрома на фоне поражения ЦНС.
Клиническая картина менингита проявляется общеинфекционным, общемозговым и менингеальным синдромами; лабораторно - воспалительными изменениями в цереброспинальной жидкости.
Общеинфекционный синдром. Типичным является острое начало болезни с повышения температуры тела до фебрильных цифр, нередко гипертермия, озноб, вялость, бледность кожи, отказ от еды и питья. Со стороны сердечно-сосудистой системы - приглушение тонов сердца, изменение частоты пульса, неустойчивость артериального давления.
Общемозговой синдром. Характерные симптомы:
- интенсивная головная боль, диффузная (распирающего характера) или преобладающая в лобно-височной области;
- рвота повторная или многократная, не связанная с приемом пищи, не приносящая облегчения;
- нарушение сознания (психомоторное возбуждение, сомнолентность, сопор, кома);
- судороги (от судорожных подергиваний отдельных мышц до генерализованного судорожного припадка);
- выраженная венозная сеть на голове, веках;
- расширение вен на глазном дне.
У детей раннего возраста: монотонный, "мозговой" крик; выбухание и напряжение большого родничка; расхождение швов черепа; "звук треснувшего горшка" при перкуссии черепа (симптом Мацевена).
Менингеальный синдром. Наиболее важными симптомами являются:
- вынужденное положение ребенка в кровати (запрокинутая голова, руки согнуты в локтях; приведены к туловшцу, ноги согнуты в коленях и тазобедренных суставах);
- ригидность затылочных мышц (пассивное сгибание головы больного к груди не удается из-за напряжения мышц, разгибающих голову);
- симптом Кернига (лежащему на спине больному сгибают ногу под прямым углом в коленном и тазобедренном суставах; пассивное разгибание ноги в коленном суставе, при согнутом бедре не удается вследствие напряжения задней группы мышц бедра);
- симптом Брудзинского I (исследуется одновременно с ригидностью затылочных мышц: при пассивном сгибании головы больного, лежащего на спине, ноги сгибаются в коленных и тазобедренных суставах);
- симптом Брудзинского II (такое же сгибание ног при надавливании на лонное сочленение);
- симптом Брудзинского III (исследуется одновременно с симптомом Кернига; при попытке согнуть ногу в коленном суставе вторая нога сгибается в колене и приводится к животу);
- симптом Лессажа (грудного ребенка берут за подмышечные впадины обеими руками, придерживая указательными пальцами голову со стороны спины, и поднимают, возникает непроизвольное подтягивание ножек к животу за счет сгибания их в тазобедренных и коленных суставах);
- симптом Мондонези (надавливание на глазные яблоки через закрытые веки болезненно);
- симптом Бехтерева (локальная болезненность при поколачивании по скуловой дуге);
- общая гиперестезия, гиперакузия, светобоязнь.
У детей полный менингеальныи синдром наблюдается редко, Характерна диссоциация симптомов: наиболее постоянно выявляется ригидность затылочных мышц, несколько реже - симптом Кернига.
Синдром воспалительных изменений в цереброспинальный жидкости. Ликвор продуцируют сосудистые сплетений (plexus chorioideus) 3 и 4 желудочков (0,35 мл/мин, за сутки - 500-600 мл). Превышение продукции ликвора (>1 мл/мин) резко затрудняет отток цереброспинальной жидкости через пахионовы грануляции в мягкую мозговую оболочку. Давление цереброспинальной жидкости измеряется специальным монометром или градуированной стеклянной трубочкой и выражается в миллиметрах водного столба (мм вод. ст.) В положении лежа нормальное давление ликвора при люмбальной пункции равняется 100-150 мм вод. ст. Давление ликвора часто оценивается количеством вытекающих из пункционной иглы капель в течение одной минуты (норма - 40-60 капель/мин).
В норме цереброспинальная жидкость прозрачная, бесцветная. Содержит клетки мононуклеарного ряда (лимфоциты, моноциты), количество которых с возрастом уменьшается и составляет: у новорожденных - 20-25 кл в 1 мкл; в 6 мес- 12-15 кл в 1 мкл; с 1 года- 1-5 кл в 1 мкл. Повышение содержания клеток в цереброспинальной жидкости называется плеоцитоз.
Содержание белка в цереброспинальной жидкости колеблется от 0,10 до 0,33 г/л, сахара - 0,45-0,65 г/л, хлоридов - 7,0-7,5 г/л.
Воспалительные изменения в оболочках мозга сопровождаются следующими признаками в цереброспинальной жидкости:
- повышением ликворного давления - вытекает, как правило, струёй или частыми каплями, возможно редкими каплями (при повышении содержания белка или блоке подоболочечного пространства воспалительным экссудатом);
- возможным изменением прозрачности (мутная) или цвета (белый, желто-зеленый и др.);
- плеоцитозом с преобладанием нейтрофилов, лимфоцитов или смешанным;
- повышением содержания белка;
- изменением уровня сахара и хлоридов.
Синдром менингизма. В остром периоде различных инфекционных заболеваннй возможно развитии клинической картины менингита без воспалительных изменений в. цереброспинальной жидкости. В основе этого состояния - рефлекторная дисфункция сосудистых сплетений и повышение продукции ликвора. Наиболее часто данный синдром возникает у детей с неблагоприятным преморбидным фоном (гипертензионно-гидроцефальный синдром, минимальная мозговая дисфункция, органическое поражение головного мозга). Окончательный диагноз возможен только после проведения люмбальной пункции и исследования цереброспинальной жидкости. У подавляющего большинства больных ликворное давление повышено; жидкость прозрачная, бесцветная, количество клеток в норме; концентрация белка не изменена. Характерным является быстрая обратная динамика общемозговых и менингеальных симптомов (в течение 1- 2 дней) на фоне снижения интоксикации и дегидратационной терапии.
Диагностика Пневмококкового менингита:
Лабораторная диагностика пневмококкового менингита
Общий анализ крови. В периферической крови обычно отмечается лейкоцитоз с резким сдвигом формулы крови влево до юных и миелоцитов, анэозинофилия, значительно повышенная СОЭ до 30–60 мм/час. В ряде случаев наблюдаемая лейкопения является плохим прогностическим признаком.
Исследование ликвора. Цереброспинальная жидкость мутная, часто с зеленоватым оттенком, вязкая, выражен нейтрофильный плеоцитоз (500–1500 клеток в 1 мкл), значительно увеличено количество белка (1–10 г/л) и снижено содержание глюкозы.
Бактериологическое исследование. Материалом для выявления возбудителя являются мокрота, кровь, гной и цереброспинальная жидкость, которые сеют на кровяной или сывороточный агар.
Бактериоскопическое исследование. На пневмококковую природу заболевания указывает наличие нейтрофилов и грамположительных ланцетовидных диплококков (не менее 10 в поле зрения) в мазках клинического материала. При бактериоскопическом исследовании ликвора обнаруживаются пневмококки в виде грамположительных диплококков ланцетовидной формы, расположенных вне- и внутриклеточно.
Для дифференцировки пневмококка от других стрептококков используют:
а) пробу с оптохином (угнетает рост стрептококков);
б) дезоксихолатную пробу (способность пневмококка ферментировать инсулин и чувствительность к желчи отличает его от зеленящих стрептококков);
в) возбудитель, выделенный из цереброспинальной жидкости, который необходимо серотипировать с помощью коммерческих реагентов для реакций латекс-агглютинации или коагглютинации, выявляющих капсульные антигены.
Лечение Пневмококкового менингита:
При подозрении на менингит необходима срочная госпитализация ребенка в специализированный стационар. При нарушениях сознания и дыхания транспортировку больного осуществляет реанимационная бригада. В стационаре проводят комплексное лечение, включающее охранительный режим, рациональное питание, этиотропную, патогенетическую и симптоматическую терапию. В остром периоде болезни необходимо соблюдение постельного режима. После проведения люмбальной пункции в течение 3 дней показан строгий постельный режим с укладкой на щите для профилактики постпункциональных осложнений.
Диета полноценная, высококалорийная, механически и химически щадящая. Детям первого года жизни проводят кормление сцеженным грудным молоком или адаптированными смесями с сохранением физиологического режима питания.
С целью профилактики кандидоза при массивной и длительной антибактериальной терапии показано назначение нистатина, дифлюкана, амфитерицина Б (фунгизона).
С иммуностимулирующей и заместительной целью применяют иммуноглобулины для внутривенного введения (эндобулин, сандоглобулин, пентаглобин) или специфические иммуноглобулины (против вируса клещевого энцефалита, противостафилококковый и др.).
Патогенетическая терапия направлена на борьбу с интоксикацией, на нормализацию внутричерепного давления и церебральной гемодинамики. При проведении дезинтоксикации необходимо обеспечить введение жидкости с учетом физиологической потребности и электролитного баланса. Введение жидкости осуществляется путем оральной регидратации (чай, 5 % раствор глюкозы, морс) или внутривенной инфузии. Для парентерального введения используют глюкозо-солевые (10 % глюкоза, 0,9 % NaCl, Рингера) и коллоидные (реополиглюкин, реомакродекс, гемодез) растворы в соотношении 3:1.
Одновременно назначают дегидратационную терапию (объем определяется степенью внутричерепного давления). В качестве стартового препарата в 1 - 2 сутки заболевания используют лазикс в дозе 1 - 2 мг/кг/сутки. Мочегонный эффект препарата начинается через 3 - 5 мин, достигает максимума через 30 мин и длится 1,5 - 3 часа.
Для улучшения кровоснабжения мозга и профилактики ишемии мозговой ткани используют сосудистые средства - трентал, кавинтон. Уменьшение энергодефицита нейронов и восстановление межнейрональных связей достигается применением препаратов ноотропного ряда (пирацетама, пантогама, перидитола) и вазоактивных нейрометаболитов (актовегина, инстенона). Длительность курса - до 6 мес. В тяжелых случаях ослабленным детям вводят лейковзвесь, свежезамороженную плазму; проводят сеансы УФО крови.
Основой комплексной интенсивной терапии отека-набухания головного мозга является адекватная респираторная поддержка (увлажненный кислород, эндотрахеальная интубация, ИВЛ), направленная на коррекцию кислотно-основного состояния и снижение выхода плазмы в периваскулярное пространство.
Широкое распространение получили осмодиуретики, действие которых основано на создании осмотического градиента между плазмой и мозговой тканью. С этой целью используют 15 % раствор манитола внутривенно (из расчета 0,5 - 1,0 г сухого вещества на 1 кг массы тела). Мочегонный эффект начинается через несколько минут и достигает максимума через 2 - 3 часа. Вследствие повреждения гематоэнцефалического барьера может возникнуть синдром "отдачи" - перемещение осмотически активного вещества из сосудистого русла в ткань мозга и усиление отёка. Для предупреждения данного состояния через 2 часа после начала введения манитола вводят лазикс.
В качестве этиотропных средств для лечения пневмококковой инфекции применяют бензилпенициллин в суточной дозе в зависимости от формы инфекции от 1 200 000 до 6 000 000 ЕД, при менингите для взрослых от 18 000 000 до 48 000 000 ЕД в сутки внутривенно, при эндокардите - 12 000 000 ЕД. Эффективны также препараты цефалоспоринового ряда, причем для лечения менингита можно использовать только цефотаксим и цефтриаксон, которые удовлетворительно проникают через гематоэнцефалический барьер. Препаратами второго ряда являются тетрациклины, ванкомицин, бисептол, сульфаниламиды.
Профилактика Пневмококкового менингита:
Профилактика пневмококковой инфекции посредством вакцинации остается наиболее рациональным подходом в борьбе с данным заболеванием. Ведущие мировые эксперты в области детских инфекций подчеркивают необходимость внедрения пневмококковых вакцин в повседневную практику стандартной вакцинации детей, начиная с первых месяцев жизни. Это отражено в официальных рекомендациях Всемирной Оранизации Здравоохранения (ВОЗ), национальных комитетов по вакцинации и иммунизации, консультативных советов Министерств здравоохранения стран ЕС, в которых говорится, что пневмококковая вакцинация должна стать частью стандартного календаря прививок для детей в европейских странах. Как пример - Министерство здравоохранения Великобритании ввело вакцинацию от пневмококковой инфекции детей с возраста 2 месяцев в стандартный календарь иммунизации в сентябре 2006 г.
Пневмококковая вакцина защищает от бактерий-возбудителей менингита. Существует два типа пневмококковой вакцины. Пневмококковую конъюгационную вакцину обычно вводят детям младше двух лет, а также детям в возрасте от 2 до 5 лет, которые принадлежат к группе риска. Пневмококковая полисахаридная вакцина рекомендована взрослым старше 65 лет. Полисахаридную вакцину также вводят взрослым среднего возраста с ослабленным иммунитетом и определенными хроническими заболеваниями.
К каким докторам следует обращаться если у Вас Пневмококковый менингит:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Пневмококкового менингита, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Читайте также:

