Почему невозможно вылечить вич
Обновлено: 19.04.2024
Данная схема приема терапии не просто спасала жизни людей, живущих с ВИЧ (при условии доступа к необходимым услугам здравоохранения), она также восстанавливала пораженную вирусом иммунную систему, что позволило людям, принимающим высокоактивную антиретровирусную терапию (АРТ), вести нормальную и здоровую жизнь.
Однако по-прежнему оставались серьезные вызовы, такие как угроза безопасности и труднопереносимые побочные эффекты. Кроме того, необходимо было принимать большое число таблеток в разные часы в течение суток, что создавало проблемы с выполнением условий данных схем. Ситуация со временем улучшилась, и на сегодняшний день большинство ЛЖВ имеют примерно такую же продолжительность жизни, что и люди, живущие без ВИЧ.
Зачем нужно лекарство?
Тем не менее создание лекарства от ВИЧ по-прежнему является труднодостижимой задачей. Даже несмотря на наличие эффективного лечения и профилактики, лекарство от ВИЧ — важная цель. Разумеется, для ЛЖВ изобретение лекарства положит конец в пожизненной необходимости проходить терапию. На сегодняшний день будущее за препаратами долгосрочного действия, однако для 38 миллионов ЛЖВ в мире излечение стало бы идеальной целью. Мировое сообщество смогло бы приблизиться к полному искоренению ВИЧ/СПИДа и снять нагрузку с системы здравоохранения как национального, так и муниципального, и регионального уровней.
В силу этих причин целый ряд государственных деятелей, научные круги, НКО и частный сектор прилагают активные усилия по разработке безопасного и доступного лекарства от ВИЧ. По аналогии с современными схемами антиретровирусной терапии — для полного излечения от ВИЧ могут понадобиться комбинации препаратов и процедур, которые по-разному работают с вирусом. Из-за того что ВИЧ умеет коварно таиться в организме человека, создавая резервуары, не распознаваемые иммунной системой, излечение от ВИЧ может потребовать использование одной из двух основных форм либо их совместное применение (по мнению исследователей, их появление на практике состоится минимум через десятилетие). Эти два подхода носят следующие названия: 1) ремиссия без приема АРТ и 2) полное искоренение вируса.
Неопределяемые без терапии
Большинство подходов, направленных на достижение ремиссии без приема АРТ, включают в себя модификацию иммунной системы с целью установить долгосрочный контроль над вирусом. Исследователи пытаются манипулировать иммунной системой с целью заставить ее распознавать и обезвреживать зараженные ВИЧ клетки или изменять их функционирование, чтобы те лучше справлялись с инфекцией.
Перспективным методом достижения ремиссии без приема АРВТ являются нейтрализующие антитела широкого спектра действия (bNAbs). Эти белки могут предотвратить заражение человеческих клеток практически всеми штаммами ВИЧ и способствовать уничтожению уже инфицированных клеток. Несмотря на то, что такие антитела производятся организмом самостоятельно у некоторых ЛЖВ, обычно их количество слишком мало, чтобы оказать ощутимую пользу, или их выработка производится на слишком позднем сроке после заражения, в результате чего они не способны контролировать быстро размножающийся и мутирующий вирус.
В настоящее время проводятся исследования на животных и людях, принимающих АРТ, с целью определить, способны ли периодические инфузии и инъекции данных антител удерживать ВИЧ в подавленном состоянии после прекращения приема АРТ. Ученые разрабатывают варианты такого вида антител с улучшенными характеристиками, в том числе с большей эффективностью и более длительным пребыванием в организме, а также тестируют лечение комбинациями двух или трех вариантов таких антител.
Полное удаление вируса из организма
Укрепление иммунных клеток для борьбы с ВИЧ. При отсутствии необходимого лечения ВИЧ уничтожает иммунную систему большинства ЛЖВ, со временем приводя к оппортунистическим заболеваниям, связанной с ВИЧ онкологией и к смерти. Тем не менее небольшая доля ЛЖВ не принимает АРТ, при этом их вирус регулярно находится в подавленном состоянии. Каким-то образом их иммунные системы естественным путем защищают организм от вируса и его разрушительного влияния.
С этим также связан феномен людей, которые имели рискованные контакты с ВИЧ-положительными партнерами, но при этом остались не инфицированными — таким образом, их иммунная система защищает их от ВИЧ. Если у исследователей получится воссоздать аналогичный уровень резистентности организма к ВИЧ среди большинства ЛЖВ, то остановка распространения вируса и излечение будут возможными.
Пересадка стволовых клеток. В начале 1990-х ряд исследований показал, что люди с более высокой природной защитой от ВИЧ часто имели мутации в гене, который кодирует белок под названием ССR5 (этот белок возникает на поверхности иммунных клеток человека и используется вирусом для проникновения в клетку с целью дальнейшего инфицирования). Если белок CCR5 не функционирует должным образом или в принципе отсутствует, ВИЧ больше не может поглощать иммунные клетки. Если ученым удастся заблокировать функционирование ССR5 или совсем исключить появление этого белка на поверхности иммунных клеток, у них появится возможность лучше контролировать ВИЧ-инфекцию либо полностью избавить от нее организм.
По предположениям некоторых ученых, если человеку, живущему с ВИЧ, пересадят костный мозг, используя в качестве донора человека с мутацией белка ССR5, его новые клетки смогут восстановить у реципиента иммунную систему, имеющую резистентность к ВИЧ. Однако пересадка костного мозга является сложной и крайне рискованной процедурой, поэтому эту теорию можно протестировать только на тех ЛЖВ, которым жизненно необходима пересадка костного мозга для лечения тяжелой формы рака.
Браун (1996 г. р.) умер в 2020 году после рецидива рака, Кастильехо (родился в Венесуэле в 1980 г.) продолжает жить здоровой жизнью.
Главным вызовом при использовании метода генетического редактирования в клинической практике на данный момент является поиск ответа на вопрос, как доставить редактирующие гены ферменты ко всем клеткам, составляющим резервуар ВИЧ, не подвергая при этом риску безопасность пациента, — для этого необходимо проведение большего количества дополнительных исследований.
Но когда?

Обзор
Распространенность СПИДа в мире на 2009 год.
Автор
Редакторы

Спонсор конкурса — дальновидная компания Thermo Fisher Scientific. Спонсор приза зрительских симпатий — фирма Helicon.
Иммунная система

Рисунок 1. Упрощенная схема иммунного ответа. Молниями указано, как один тип клеток активирует другие. Мф — макрофаг, Б — бактерия, ТХ — Т-хелпер, ВКл — B-клетка, ПлКл — плазматическая клетка, Ат — антитела, Б+Ат — бактерия, покрытая антителами, привлекающими макрофагов, В — вирус, ЗМф — зараженный макрофаг, ТК — Т-киллер, ЗК — клетка, зараженная вирусом, УК — умирающая (апоптотирующая) клетка, В+Ат — вирус, покрытый антителами.
рисунок автора статьи
Жизненный цикл ВИЧ
Видео. Жизненный цикл ВИЧ.

Таким образом, после того как копия вируса в геноме клетки начинает действовать, на её поверхности появляются знакомые нам белки gp41 и gp120, в цитоплазме — остальные вирусные белки и вирусная РНК. И через некоторое время от зараженной клетки начинают отпочковываться всё новые и новые копии ВИЧ.
Способы уничтожения иммунной системы
При отпочковывании вирус использует клеточную мембрану клетки, и со временем это должно вызвать ее разрушение. К тому же, вирусный белок Vpu вызывает увеличение проницаемости мембраны клетки [6]. При активации вируса в клетке появляется неинтегрированная в геном двуцепочечная ДНК [19], наличие которой может рассматриваться клеткой как повреждение ее генетического материала и индуцировать ее смерть через апоптоз (С точки зрения организма такая клетка потенциально может стать раковой). Помимо этого, вирусные белки напрямую нарушают баланс про- и противоапоптотических белков в клетке. К примеру, вирусная протеаза p10 может разрезать противоапоптотический фактор Bcl-2. Белки Nef [26], Env [22] и Tat [24] вовлечены в возрастание количества клеточных белков CD95 и FasL, служащих индукторами апоптоза по т.н. Fas-опосредованному пути. Белок Tat положительно регулирует каспазу 8 [2] — ключевой фактор индукции апоптоза.
Если же клетки не погибли сами, они активно уничтожаются Т-киллерами. (Это стандартный ответ иммунитета на заражение любыми вирусами.)
Помимо этого, при производстве gp120 и Tat часть их выбрасывается зараженной клеткой в кровоток, а это оказывает токсическое действие на организм [4], [28]. gp120 оседает на все СD4 + -клетки (в том числе и здоровые), что имеет три последствия:
- Белок СD4 важен для взаимодействия Т-хелпера с фагоцитом, при слипании же СD4 с gp120 T-хелпер перестает выполнять эту функцию.
- На gp120 как на чужеродный белок образуются антитела; после оседания gp120 на здоровые клетки, последние маркируются антителами, и иммунная система их уничтожает [9].
- После обильного связывания Т-хелпером gp120 клетка умирает сама. Дело в том, что CD4 — это корецептор. Он усиливает сигнал от TCR (T-cell receptor) — главного белка, позволяющего выполнять Т-клеткам функцию иммунитета. В норме эти рецепторы активируются вместе. Если же активируется один тип рецепторов, но не активируется другой, это является сигналом, что что-то пошло не так, и клетка умирает посредством апоптоза.
Антитела, призванные препятствовать инфекции, в случае с ВИЧ часто, наоборот, ее усиливают [28]. Почему так происходит — не совсем понятно. Одну причину мы рассмотрели выше. Возможно, дело в том, что антитела сшивают несколько вирусных частиц вместе, и в клетку попадает не один, а сразу много вирусов. Помимо этого, антитела активируют клетки иммунитета, а в активированной клетке вирусные белки синтезируются быстрее.
Вдобавок, gp120 и gp41 имеют участки, похожие на участки некоторых белков, участвующих в иммунитете (например, MHC-II [25], IgG [23], компонент системы комплемента Clq-A [14]). В результате на эти участки образуются антитела, способные помимо вируса маркировать совершенно здоровые клетки (если на них будут эти белки), с соответствующими для них последствиями.
Так как на поверхности зараженной клетки появляется gp120, то она, как и вирусная частица, будет сливаться с другими СD4-содержащими клетками, образуя огромную многоядерную клетку (синцитий), неспособную выполнять какие-либо функции и обреченную на смерть.
На самом деле, помимо Т-хелперов, СD4 содержатся во множестве других клеток — предшественниках Т-киллеров/Т-хелперов, дендритных клетках, макрофагах/моноцитах, эозинофилах, микроглии (последние четыре — разновидности фагоцитов), нейронах (!), мегакариоцитах, астроцитах, олигодендроцитах (последние две — клетки, питающие нейроны), клетках поперечно-полосатых мышц и хорионаллантоиса (присутствует в плаценте) [29]. Все эти клетки способны заражаться ВИЧ, но сильно токсичен он лишь для Т-хелперов. Это и определяет основное клиническое проявление СПИДа — сильное снижение количества Т-хелперов в крови. Однако для других клеток заражение тоже не проходит бесследно — у больных СПИДом часто снижена свертываемость крови, имеются неврологические и психиатрические отклонения [16], наблюдается общая слабость.
Пути заражения ВИЧ
Внимание! Ввиду того, что СПИД является венерическим заболеванием, информация, приведенная в этом разделе, может вас оскорбить либо вызвать неприятные эмоции при прочтении. Будьте осторожны.
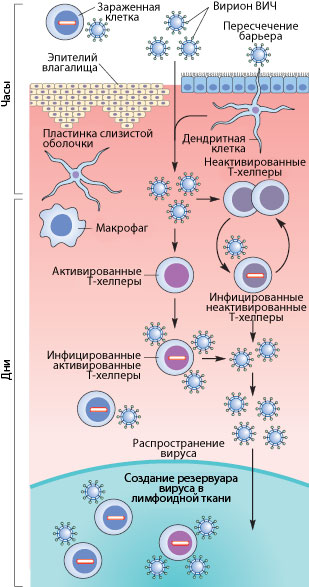
Рисунок 3. Пути проникновения ВИЧ в организм при половом контакте. Слева указано примерные временные рамки каждого этапа.
Как же происходит первичное заражение человека ВИЧ? Думаю, что с переливанием крови или с использованием общего шприца при употреблении наркотиков читателю все понятно — вирус доставляется напрямую из зараженной крови в здоровую. При вертикальном способе передачи инфекции (от матери к ребенку) заражение может произойти во время внутриутробного развития, в момент родов или в период кормления ребенка грудью (т.к. вирус и зараженные вирусом клетки содержатся в молоке матери) [17], [20]. Тем не менее, даже у ребенка, рожденного от ВИЧ-инфицированной матери, есть шанс остаться здоровым, особенно если мать использует ВААРТ (высокоактивную антиретровирусную терапию) [5]. А почему же люди заражаются при половом контакте?
Механизмы передачи вируса при половом акте не до конца ясны. Тем не менее, они понятны в общих чертах. Итак, рассмотрим барьеры, которые необходимо преодолеть вирусу, чтобы добраться до макрофагов и Т-хелперов. К сожалению, рассматривать особо нечего: барьер только один — это слой эпителиальных клеток и вырабатываемая ими слизь, находящиеся во влагалище (а также пенисе, прямой кишке, глотке). Барьер этот тонок — он может быть всего одну клетку в толщину, — но для вируса труднопреодолим, доказательством чего может служить сравнительно небольшой процент заражений — примерно 1–2 случая на 100 половых контактов. Итак, и какими же путями преодолевает вирус это препятствие?
Наиболее очевидный механизм — это микротравмы. При обычном половом контакте, а особенно при анальном сексе, почти неизбежно появляются микротрещины; при наличии же венерических заболеваний часто возникают изъязвления слизистой. Через эти микротравмы вирус, содержащийся в сперме и влагалищном секрете, может проникнуть к иммунокомпетентным клеткам [17], [20].
Помимо дендритных клеток, в кишечнике существует другой тип клеток, предназначенный для ознакомления организма с антигенами внешней среды. Это так называемые М-клетки, пропускающие через себя довольно крупные объекты неповрежденными из просвета кишечника. В т.ч. через них может проходить и вирион ВИЧ.
Свой вклад в заражение вносит и провоспалительный процесс, в норме присутствующий в женских половых путях из-за наличия в них спермы. Благодаря ему Т-клетки подвержены активации, что способствует их восприимчивости к инфекции.
Итак, риск заразиться ВИЧ возрастает в ряду (Классический секс → Анальный секс → переливание крови / использование общих шприцов при принятии наркотиков). Что же касается орального секса, то весьма небольшой шанс заразиться есть только у принимающей стороны — слюна и тем более желудочный сок инактивирует ВИЧ. Теоретически, этим способом может заразиться и мужчина, но для этого необходимы ранки на пенисе.
При поцелуях и обычных бытовых контактах вирус не передается — он очень неустойчив в окружающей среде .
Заключение
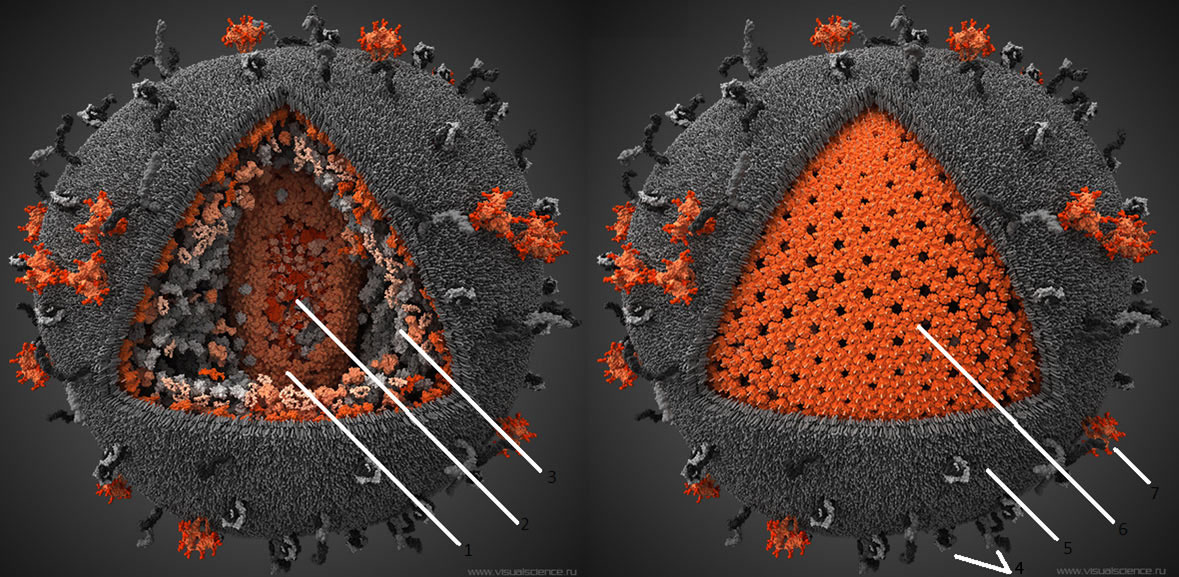
. Все эти факты позволяют надеяться, что вскоре ВИЧ, как и оспа, останется в прошлом.
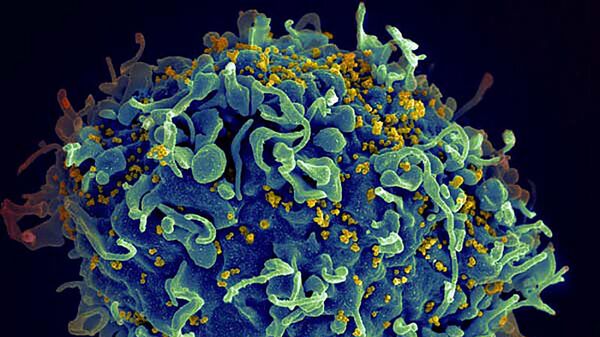
Заражение ВИЧ и многими другими опасными вирусами обычно протекает в два этапа. Сначала вирус активно размножается в организме новой жертвы, что приводит к активации иммунитета и появлению недомогания, похожего по симптомам на грипп. Когда организм начинает бороться с вирусом, инфекция переходит в хроническую стадию, постепенно истощая иммунитет.
Сегодня больные ВИЧ могут прожить десятки лет благодаря приему антиретровирусных препаратов – веществ, подавляющих различные этапы репликации вируса в клетках тела. Так как они часто обладают сильными побочными эффектами, медики часто вынуждены прекращать их прием на несколько недель.

При прекращении их приема ВИЧ "вылезает из окопов" и начинает интенсивно копировать себя, зачастую возвращаясь к начальным масштабам инфекции за три или две недели. В последние годы ученые активно пытаются найти лекарства или антитела, которые помогали бы избежать подобной "контратаки" вируса, или позволяли бы "выгнать" вирус из клеток.
Крайне малое число носителей ВИЧ, примерно 0,3% больных, не нуждается в подобной терапии - их иммунитет по пока неизвестным причинам более эффективно борется с инфекцией и сдерживает ее распространение без помощи лекарств. Многие подобные люди, так называемые "нонпрогрессоры", живут с инфекцией уже более трех десятков лет, не страдая от резкого снижения в уровне CD4-клеток.
Генетики, вирусологи и молекулярные биологи уже много лет изучают их лимфоциты и ДНК в надежде понять, что защищает их иммунитет от истощения, и трансплантировать эти уникальные особенности в организм других больных, которым повезло меньше.
Кауфманн и его коллеги провели одно из самых масштабных исследований такого рода, организовав своеобразную "перепись" среди Т-клеток и прочих иммунных телец, присутствующих в образцах крови у обычных носителей ВИЧ и людей, на которых вирус почти не действует.
Ученых интересовало то, работа каких генов в этих клетках у них отличалась и как эти отличия могли влиять на взаимодействия между вирусом и организмом человека. Дополнительно биологи проанализировали то, как изменилась работа тех же самых генов у больных, проходивших антиретровирусную терапию.
Это позволило им проследить за тем, как лекарства влияли на иммунные клетки, а также тем, было ли их действие похоже на то, что происходит в организме "нонпрогрессоров". Этот анализ раскрыл несколько важных сходств и различий в работе лимфоцитов у всех трех категорий больных.
К примеру, в иммунных тельцах людей, необычно хорошо сопротивлявшихся ВИЧ, а также в немногочисленных выживших лимфоцитах "обычных" больных были активны гены, связанные с работой и ростом трех подтипов Т-клеток –TH-1, TH-17 и TH-22. Они, как отмечают ученые, особенно активно распознавали вирусные частицы и уничтожали их, что, вероятно, помогает "нонпрогрессорам" сдерживать инфекцию.
Что интересно, подобные клетки чаще встречаются не в крови, а в кишечнике человека, где, как сегодня считают исследователи, протекает острая фаза заражения ВИЧ и его фактическое проникновение в организм. Скорее всего, они играют ведущую роль в сдерживании инфекции, так как снижение активности связанных с ними генов или пониженное число этих телец ведет к ускоренному развитию инфекции.
Антиретровирусная терапия, как обнаружили Кауфманн и его коллеги, тоже воздействует на эти участки ДНК, но не так, как это происходит в организме "нонпрогрессоров". Активность части генов вырастает, тогда как другие оказались подавлены, что заметно ослабило способность иммунитета сопротивляться инфекции.
Соответственно, если понять, как "переключить" гены в нужное положение, то можно создать средство, которое не излечит человека от ВИЧ, но переведет инфекцию в такое состояние, что она перестанет прогрессировать. Что для этого надо сделать, ученые планируют выяснить в ближайшее время.

Методы, с помощью которых второй в истории пациент с ВИЧ полностью избавился от болезни, не применимы в общей практике. Об этом РБК заявила старший научный сотрудник Федерального центра СПИД Наталья Ладная.
Имя пациента не называлось, однако издание BELatina пишет, что излечившимся является 40-летний житель Венесуэлы Адам Кастильехо. О его ремиссии сообщалось еще год назад. У пациента выявили ВИЧ в 2003 году, а в 2012 году диагностировали лимфому Ходжкина — одну из разновидностей рака крови. Ему пересадили стволовые клетки костного мозга от донора с редкой мутацией, которая делала его невосприимчивым к ВИЧ.


Брендинг под копирку: зачем компании выпускают продукты-клоны

Полиграф и тест на наркотики: как кандидата проверяют при трудоустройстве

Meta* в опале: что это значит для бизнеса и поможет ли VPN
По каким отраслям экономики России кризис ударит сильнее всего

Вам необходимо снизить фонд оплаты труда. Как сделать это законно

Нужен диалог: как производителям продуктов реагировать на санкции

Ни слова о недовольстве: как быть с негативными эмоциями в коллективе

Культура потребления как в 2015-м: 3 неявных плюса блокировки Instagram*

Заведующий отделом по профилактике и борьбе со СПИДом Центрального научно-исследовательского института (ЦНИИ) эпидемиологии Роспотребнадзора Вадим Покровский также уверен, что технология пересадки костного мозга не подходит для массового использования.
По его словам, клинические испытания подобных методик лечения ВИЧ сейчас ведутся.
Исцеление – не то слово, которое часто используется в связи с термином "ВИЧ-инфекция". 35 лет прошло с момента обнаружения вируса и большую часть времени врачи рассматривали полное выздоровление скорее как фантазию, а не возможную перспективу. Всю потому, что ВИЧ не похож ни на один другой вирус. Он уничтожает те самые иммунные клетки, которые предназначены для того, чтобы с ним бороться. Он разрушает иммунную защиту месяцами, а иногда – годами.
На сегодняшний день с заболеванием живут 37 млн человек по всему миру. Однако сегодня ученые больше понимают о том, как вирус "скрывается" в клетках организма и почему наша бдительная иммунная система "не замечает" его.
Национальные институты здравоохранения (NIH) США финансируют усилия по лечению ВИЧ, а фонды – например AmfAR – ищут ресурсы, которые позволят полностью искоренить эпидемию.
"Абсолютно точно, что ВИЧ можно излечить, – говорит Ровена Джонстон, вице-президент и директор по исследованиям AmfAR. – Вопрос на миллиард долларов: "Как это сделать?".
Профессор медицины из Медшколы при Университете Джона Хопкинса Роберт Силичано одним из первых идентифицировал резервуары ВИЧ.
"Проблема в том, что такая форма ВИЧ не видна иммунной системе и на нее не влияют лекарственные препараты", – говорит Силичано. По словам доктора, вирус покидает свою укреплённую башню и идёт на штурм лишь тогда, когда человек перестаёт принимать лекарства.
В одном из докладов, которые представили на конференции по ретровирусам и оппортунистическим инфекциям 2018 года в Бостоне, исследователи обнаружили убедительные доказательства того, что резервуары могут быть активированы и устранены, по крайней мере – у животных. Дэн Барух и его коллеги из Медицинского центра Beth Israel Deaconess и Гарвардской медицинской школы показали, что препарат, который стимулирует иммунную систему и активирует резервуары, в сочетании с мощным антителом может нейтрализовать ВИЧ у инфицированных обезьян на полгода.
"Я думаю, что наши данные повышают вероятность получить препарат для полного вызоровления. Это возможно", – заявил Барух.
Такой метод в научной среде называют shock and kill: он основан на "выталкивании" спящего вируса из резеруаров и последующем уничтожении. Это шаг к избавлению людей от пожизненной зависимости от АРВ-препаратов.
Этот метод еще не был протестирован на людях и вопрос полного выздоровления еще в процессе изучения. Исследователи напоминают, что на сегодняшний день единственным полностью излечившимся от ВИЧ человеком является "берлинский" пациент, которому пересадили костный мозг от донора с особой мутацией, которая не позволяет вирусу иммунодефицита "прикрепляться" к клеткам. Браун прекратил прием АРВ-препаратов после пересадки. Прошло уже больше 10 лет и его тест на ВИЧ остаётся отрицательным.
[Подробнее об излечении Тимоти Рэя Брауна – в материале СПИД.ЦЕНТРа]
Случай Брауна доказывает, что полное выздоровление возможно, но врачи дожны добраться до "каждого закутка" организма, где может прятаться вирус, говорит доктор Стивен Дикс, профессор медицины Калифорнийского университета в Сан-Франциско.
Сейчас некоторые исследователи даже полагают, что возможно полностью реконструировать иммунную систему человека, чтобы она была способна успешно устранить любой вирус. Этим уже пользуются онкологи в борьбе с опухолями: иммунную систему программируют таким образом, что та сама атаковала злокачественные клетки.
"Я настроен оптимистично, поскольку параллели в терапии ВИЧ-инфекции и онкологии настолько тесны, что мы сможем применять товые технологии и в терапии ВИЧ", – говорит Дикс.
Никто из специалистов не ожидает, что ВИЧ будет побежден в следующем году или ближайшие пару лет. Но они более чем уверены, что в будущем мы победим эпидемию.
Читайте также:

