Подагра и половые инфекции
Обновлено: 24.04.2024
Инфекции мочевыводящих путей — частое заболевание в повседневной урологической практике. Значительный прогресс в лечении инфекций мочевыводящих путей наблюдается за последние двадцать лет. В статье затрагиваются такие важные проблемы, как этиология, патогенез и лечение инфекций мочевыводящих путей у взрослых.
Инфекции мочевыводящих путей (ИМП) представляют собой серьезную проблему из-за их распространенности и связанной с ними заболеваемости. По статистике на них приходится примерно 20% всех внебольничных и примерно 50% нозокомиальных инфекций. Достижения последних десятилетий способствовали лучшему пониманию патогенеза инфекций мочевыводящих путей и выяснили важную роль как бактериальных, так и зависимых от пациентов факторов в развитии или предотвращении инфекции.
Динамичное развитие антибактериальной терапии значительно облегчило правильное лечение ИМП, но неправильное и широкое злоупотребление антибактериальными препаратами привело к увеличению лекарственной устойчивости микроорганизмов.
Эпидемиология ИМП
Инфекции мочевыводящих путей — одно из самых распространенных инфекционных заболеваний человека.
Частота возникновения ИМП зависит от пола и возраста обследуемых, а также от конкретных характеристик исследуемой популяции.
Риск ИМП возрастает, когда существует препятствие для оттока мочи или когда обстоятельства способствуют колонизации и росту бактерий. К физиологическим факторам, предрасполагающим к ИМП, относятся беременность, пожилой возраст и такие заболевания, как диабет и мочекаменная болезнь.
Этиология и патогенез ИМП
Наиболее частыми факторами, вызывающими ИМП, являются бактерии, реже вирусы, грибки или паразиты. Распространенность определенных типов бактерий, выделенных из мочи пациентов, во многом зависит от изучаемой популяции. Совершенно иначе обстоит дело у пациентов, находящихся на амбулаторном лечении, чем в больницах.
В физиологических условиях мочевыводящие пути стерильны, за исключением конца уретры. Первый эпизод ИМП в амбулаторных условиях в 80% случаев вызывается Escherichia coli, в 10-15% — Staphylococcus saprophyticus (кроме группы молодых сексуально активных женщин, в которой он составляет около 30%), другими грамотрицательными бактериями (Proteus mirabilis, Klebsiella spp.) или грамположительными (стафилококки, стрептококки, энтерококки). 70% рецидивов внебольничных инфекций вызваны к ишечной палочкой . Также наиболее частые нозокомиальные инфекции вызываются кишечной палочкой (около 50%), Enterobacter spp., Pseudomonas spp., Serratia marcescens, а также стафилококками, энтерококками и грибками.

Кишечная палочка
У 95% пациентов ИМП является результатом заражения одним штаммом бактерий. Заражение несколькими штаммами наблюдается у 5% пациентов, преимущественно у катетеризованных больных, с ослабленным иммунитетом, нейрогенными нарушениями мочевого пузыря или дефектами мочевыделительной системы.
Инфекция мочевыделительной системы может происходить восходящим путем (урогенные инфекции), кровотоком (гематогенные инфекции — очень редко вызваны, главным образом, золотистым стафилококком), лимфатическим путем или непрерывно (при наличии урогенитального или урогенитального свища).
ИМП почти всегда вызывается попаданием бактерий через уретру. В физиологических условиях бактерии часто попадают в мочевыводящие пути, однако из-за защитных механизмов организма развитие ИМП происходит редко.
Наиболее важные естественные механизмы защиты от ИМП:
- длина уретры у мужчин;
- перистальтика мочеточника, нормальная функция пузырно-мочеточниковых клапанов;
- подкисление и концентрация мочи;
- правильная бактериальная флора влагалища и области вокруг уретры;
- антибактериальные свойства секрета простаты;
- механизмы предотвращения бактериальной адгезии в мочевыводящих путях: механическое воздействие струи мочи, мукополисахариды стенки мочевого пузыря, антитела IgG и IgA.
Инфекции мочевыводящих путей редко возникают у здоровых людей с нормальной анатомической структурой и физиологической функцией мочевыводящих путей. В случае затрудненного оттока мочи или ослабления организма из-за системных заболеваний (диабет, подагра , опухолевый процесс) мы часто сталкиваемся с воспалительными изменениями мочевыделительной системы.

Подагра
К наиболее частым факторам, способствующим развитию инфекции мочевыводящих путей, относятся:
- 1-я беременность,
- старый возраст,
- препятствие оттоку мочи — мочекаменная болезнь, аденома простаты,
- атрогенные факторы — инструментарий мочевыводящих путей (цистоскопия, катетеризация мочевого пузыря, восходящая пиелография),
- врожденные пороки мочевыводящих путей — двойная чашечно-тазовая система, ретроградный пузырно-мочеточниковый отток,
- диабет, подагра,
- неврогенный мочевой пузырь,
- конечная стадия почечной недостаточности (диализ),
- половые отношения,
- длительная иммобилизация в постели.
Моча в мочевыводящих путях здорового человека стерильна. Наличие в нем бактерий свидетельствует об инфицировании.
Основным симптомом, позволяющим диагностировать ИМП, является так называемая значительная бактериурия, когда количество бактерий в 1 мл свежей, собранной в асептических условиях мочи превышает 100000.
Возникновение значительной бактериурии по полу и возрасту представлено ниже:
Что такое подагра? Причины возникновения, диагностику и методы лечения разберем в статье доктора Шестернина А. С., ревматолога со стажем в 12 лет.
Над статьей доктора Шестернина А. С. работали литературный редактор Елена Бережная , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Подагра — системное заболевание, которое развивается в связи с воспалительным процессом, возникшим в месте отложения кристаллов моноурата натрия у людей с повышенным уровнем мочевой кислоты в сыворотке крови (более 360 мкмоль/л). Гиперурикемия возникает под воздействием как внешнесредовых, так и генетических факторов.
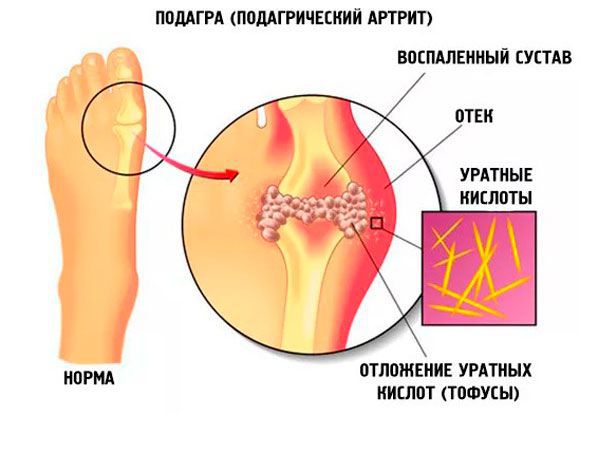
Роль мочевой кислоты в развитии подагры
Подагра — заболевание, вызванное повышением уровня мочевой кислоты в крови, или гиперурикемией. Чем длительнее и тяжелее протекает гиперурикемия, тем вероятнее развитие подагры. Чаще всего гиперурикемия возникает при нарушенном выведении почками мочевой кислоты.
Эпидемиология
Распространённость подагры среди взрослого населения в европейских странах составляет 0,9–2,5 %, в США достигает 3,9 % [21] .
Особенности заболевания у мужчин и женщин
Подагрой страдают преимущественно мужчины, составляя 80-90 % заболевших. Пик заболеваемости у мужчин приходится на возраст 40-50 лет, у женщин — после 50 лет, с наступлением климакса. Подагра у мужчин встречается в 6-7 раз чаще, чем среди женщин; в старческом возрасте — в 3 раза чаще. Однако в последние годы подагра стала более распространена среди женщин [21] .
Факторы риска
Причинами подагры могут быть:
- наследственность (предрасположенность к нарушению обмена пуринов);
- избыток в пище пуринов;
- нарушение функции почек, когда теряется их способность выводить мочевую кислоту (хроническая почечная недостаточность, поликистоз почек, гидронефроз, нефропатия в связи со злоупотреблением нестероидными противовоспалительными препаратами, при голодании);
- увеличение распада пуриновых нуклеотидов (цитостатическая терапия, лучевая и химиотерапия, хирургические вмешательства, гемолиз). [1][19]
Особенности современного течения подагры:
- значительный рост заболеваемости;
- увеличение частоты встречаемости у женщин;
- увеличение коморбидных состояний;
- начало заболевания в молодом возрасте.
Распространенность подагры растет, и это можно связать с ростом уровня жизни населения. Бессимптомная гиперурикемия встречается часто, однако далеко не всегда при этом развивается подагра.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы подагры
Боли при подагре. Заболевание сопровождается нестерпимой, быстронарастающей и быстропроходящей за несколько часов или суток суставной болью, кожа над суставом краснеет, сам он увеличивается в объеме.
Из других симптомов — повышенная температура тела, слабость, потливость.
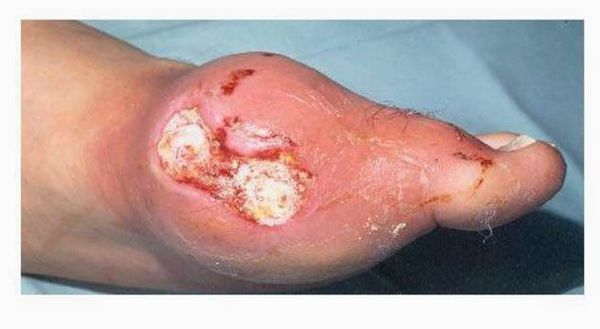
Тофусы. При переходе в хроническую форму заболевания вокруг поражённых суставов образуются тофусы, суставы деформируются. Тофусы — это единичные или множественные узелки белого и жёлтого цвета. Чаще всего возникают на пальцах, кистях, стопах, локтях. Тофусы также могут развиться под кожей на ушах, в почках или других органах.
Боли в пояснице, кровь в моче. В почках образуются уратные камни, провоцируя тянущие боли в пояснице и периодическое появление крови в моче, никтурию (больше мочи выделяется ночью). [2] [3]
Воспаление околосуставных тканей. При воспалении околосуставных тканей пациент испытывает выраженную боль. Сустав отёчный, кожа над ним приобретает багрово-синюшный оттенок. Местные симптомы сопровождаются общим недомоганием и лихорадкой.
Ограничение подвижности в суставе. При остром подагрическом артрите возникает ограничение подвижности в суставе длительностью 5-14 дней, затем функции полностью восстанавливаются.
Патогенез подагры
Поскольку образование уратов растет и нарушается выведение их почками, образуется избыток мочевой кислоты в крови, и происходит накопление уратов в тканях организма. Когда происходит отложение кристаллов моноурата в полости сустава, возникает воспалительный процесс из-за активации различных провоспалительных цитокинов. Кроме того, эти кристаллы откладываются в почечной ткани, приводя к развитию нефропатии и уратного нефролитиаза. [7]
Классификация и стадии развития подагры
Выделяют пять клинических форм подагры: бессимптомную гиперурикемию, острый подагрический артрит, межприступную подагру, хронический подагрический артрит, хроническую тофусную подагру.
Клинические формы подагры
Бессимптомная гиперурикемия — повышение уровня мочевой кислоты в крови без клинических проявлений подагры.
Острый подагрический артрит. Приступ обычно наступает на утро после застолья, злоупотребления алкоголем, после повышенной физической нагрузки и инфекционных заболеваний. При остром подагрическом артрите возникает резкая, невыносимая боль в большом пальце стопы, температура тела повышается до 39 °C , кожа над поражённым суставом приобретает синюшо-багровый окрас.
Межприступная (интервальная) подагра. Без лечения у 62 % пациентов повторный приступ развивается в течение первого года, в течение двух лет – у 78 %. Продолжительность бессимптомного периода со временем сокращается, приступы становятся всё тяжелее, затрагивая новые суставы.
Хронический подагрический артрит. Дальнейшее отложение кристаллов моноурата натрия приводит к развитию хронического болевого синдрома, значительным деформациям суставам и нарушениям их функций, особенно суставов стоп и кистей.
Хроническая тофусная подагра. Характеризуется появлением тофусов — очаговых скоплений кристаллов мочевой кислоты в тканях в виде узлов. Обычно они располагаются подкожно, но иногда образуются в костях и других органах. Тофусы, как правило, безболезненны, кожа над ними может изъязвляться и инфицироваться.
От первой "атаки" болезни до развития хронической подагры проходит в среднем 11,6 лет, темпы развития заболевания зависят от выраженности гиперурикемии.
Приблизительно 20 % пациентов с хронической подагрой страдают от мочекаменной болезни, которая сопровождается болью в поясничной области, отдающей вниз живота, иногда — в половые органы, а также тошнотой и рвотой [22] .
Течение. Симптомы в зависимости от стадии развития подагры
Впервые подагрический приступ настигает пациента без предвестников, как правило, в возрасте от 40 до 50 лет, хотя известны случаи заболевания и в гораздо более молодом возрасте. Острая суставная боль, чаще в плюснефаланговом суставе большого пальца стопы (классический вариант начала), застает человека во второй половине ночи или в ранние утренние часы. Любое движение в суставе или прикосновение вызывает сильнейшую боль.
Нарушение диеты, застолья с алкогольными напитками (алкоголь блокирует почку к выделению мочевой кислоты), хирургические вмешательства, инфекционные заболевания, повышенные нагрузки и травматизация сустава предшествуют возникновению приступа. Пациенты жалуются на покраснение пораженной области, ее припухание, сильную боль, общую слабость и недомогание, повышение температуры тела, потливость, разбитость, подавленность. Также характерными являются острые бурситы (препателлярный или локтевой сумки). [6]
В течение нескольких дней (около недели) приступ самостоятельно проходит. Именно из-за этого подагра часто создаёт видимость доброкачественности: всё проходит (особенно в начале) самостоятельно, и проблема забывается до следующего обострения. На самом деле подагра при таком подходе может привести к разрушению и деформации суставов, хронической болезни почек.
Далее при отсутствии адекватного контроля над заболеванием приступы учащаются, перестают проходить самостоятельно, проходят за больший промежуток времени. Позже человек вообще перестает чувствовать себя здоровым, а находится в состоянии затянувшегося приступа. В результате этого над областью пораженных суставов образуются безболезненные подкожные узелки с крошковидным, творожистым содержимым – тофусы (соли мочевой кислоты беловатого или желтоватого цвета). Излюбленное место расположения тофусов – область суставов кистей и стоп, ахиллово сухожилие, ушные раковины, голеностопные и локтевые суставы. При хронической тофусной подагре происходит разрушение хряща, что грозит деформацией, полным разрушением сустава и его анкилозом (полное заращение и отсутствие движений). Иногда тофусы могут самостоятельно вскрываться, а из них выделяется густое содержимое. [9] [17]
Осложнения подагры
Возможные осложнения:
- образование тофусов;
- формирование деформаций и анкилозов суставов;
- нефролитиаз (камни в почках);
- депрессия как следствие постоянного болевого синдрома;
- статистически значимо при подагре гораздо более часто встречаются сопутствующие заболевания (сахарный диабет, атеросклероз, гипертриглицеридемия — метаболический синдром). [10]
Чем опасна подагра
К серьёзным осложнениям подагры относятся повышение артериального давления и ишемическая болезнь сердца. Гиперурикемия связана с повышенным риском смерти от болезней сердечно-сосудистой системы.
Диагностика подагры
Сбор анамнеза
При подозрении на подагру врач выяснит, что предшествовало приступу. К возможным причинам обострения относятся застолье с употреблением мяса и алкогольных напитков, интенсивная физическая нагрузка или голодание, перенесённое простудное заболевание.
Оценка клинической картины течения болезни
При подагре врач осматривает суставы — для подагрического артрита характерно поражение большого пальца стопы. В этом случае доктор обращает внимание на увеличение объёма сустава, изменение цвета кожи, отсутствие движений в суставе из-за выраженных болей, наличие или отсутствие тофусов.
Острый артрит, болевые ощущения при котором нарастают лавинообразно, появляется отек и покраснение пораженного сустава, является веским поводом подумать о подагре.
Диагностические критерии подагры
Диагностические критерии подагры Wallace (предложены ААР в 1975 году, одобрены ВОЗ в 2002 году):
- наличие кристаллов мочевой кислоты в суставной жидкости;
- наличие тофусов, содержание кристаллов мочевой кислоты в которых подтверждено химически или поляризационной микроскопией;
- наличие 6 из 12 следующих признаков:
- типичная картина острой суставной атаки (один и более раз) в анамнезе;
- признаки воспаления наиболее выражены в первые сутки;
- воспаление одного сустава (моноартрит);
- покраснение кожи над пораженным суставом;
- припухание и боль в первом плюснефаланговом суставе;
- поражение первого плюснефалангового сустава с одной стороны;
- поражение суставов стопы с одной стороны;
- тофусы и образования, напоминающие их;
- лабораторные изменения (повышение уровня мочевой кислоты в крови);
- несимметричный отек суставов;
- кисты под кортикальным слоем кости без эрозий на рентгенографии;
- стерильная синовиальная жидкость. [13]
Исследование синовиальной жидкости
При пункции врач получает синовиальную жидкость, в которой под микроскопом обнаруживаются кристаллы моноурата натрия. Они могут обнаруживаться и в тофусе. Диагноз при этом можно установить со стопроцентной вероятностью.
Микроскопическое исследование кристаллов в суставах
Ураты под микроскопом выглядят как иглообразные кристаллы с одним утонченным концом. В отсутствие поляризационного микроскопа диагноз основывается в основном на типичных клинических проявлениях подагры.
Уровень уратов в сыворотке
Около 30 % пациентов во время острой атаки имеют нормальный уровень мочевой кислоты в сыворотке крови. Высокий уровень мочевой кислоты (> 6,8 мг/дл) подтверждает диагноз, но не является специфичным признаком [22] .
Визуализация
Диагностика хронического подагрического артрита
При хроническом подагрическом артрите у пациентов значительно поражены суставы, присутствуют подкожные или костные тофусы. Для подтверждения диагноза проводят рентгенологическое и ультразвуковое исследование [22] .
Дифференциальная диагностика:
- гнойный артрит;
- болезнь отложения кристаллов пирофосфата кальция дигидрата;
- ревматоидный артрит;
- реактивный артрит;
- псориатический артрит;
- остеоартроз.
Стоит обратить внимание на то, что во время приступа уровень содержания мочевой кислоты в крови может быть нормальным, так как она в этот момент усиленно выводится почками. На ее уровень в крови не следует ориентироваться при постановке диагноза.
Лечение подагры
Можно ли вылечить подагру навсегда
Вылечиться от подагры полностью нельзя, но можно контролировать её развитие и предотвратить обострения.
Нелекарственные методы
- соблюдение диеты;
- ограничение употребления алкоголя;
- уменьшение избыточного веса.
Диета при подагре является довольно строгой, но выполнение диетических рекомендаций является залогом успешного лечения. Продукты, которые богаты пуринами, подлежат исключению или минимизации. Обильное щелочное питье помогает почкам избавиться от избытка мочевой кислоты в крови (почки — единственный орган, выводящий мочевую кислоту).
Начнем с главного источника пуринов — птицы и мяса. Курица — один из самых вредных видов птицы. Курице немного уступают (содержат меньше пуринов) утка и гусь. Индейка замыкает список, обладая самым низким содержанием пуринов среди птицы. Говядина — лидер среди мясных продуктов по содержанию пуринов, далее идут телятина и свинина, баранина.
Что касается рыбы, то самые вредные — лососевые виды, далее шпроты, килька, сардины, треска. Морские обитатели, живущие в раковинах (устрицы), являются самыми богатыми на пурины. Субпродукты также очень вредны (мозги, печень, легкие, почки), так же, как и холодец, мясные бульоны и соусы. Колбасу (любую) стоит полностью исключить из рациона. Не рекомендуются также: грибы и грибные бульоны, бобовые, щавель, яйца, шоколад, дрожжи, рис полированный, инжир, геркулес, капуста цветная, дрожжи. Алкогольные напитки запрещены (особое внимание пиву, вину, шампанскому).
Объем употребляемой за сутки жидкости — 2-2,5 литра. Рекомендовано щелочное питье: щелочная минеральная вода, вода с добавлением лимона, соки.
Теперь о бедных пуринами продуктах — как раз о тех, которые необходимо есть. Ими являются: молоко и молочные, молочнокислые продукты, многие овощи (капуста белокочанная, картофель, огурцы, помидоры, морковь, лук), орехи, фрукты, мучные изделия, крупы, мед, масло сливочное. Отварное мясо и рыбу рекомендуется есть 2-3 раза в неделю. Можно есть сало, так как жир почти не содержит пуринов. Некоторые исследования свидетельствуют, что 1,5 литра кофе в день приравнивается к 100 мг аллопуринола, а таккже известно, что вишня и черешня обладают гипоурикемическим действием. [4] [15]
Лекарственные методы
Лечение подагры противоотечными и обезболивающими препаратами поможет уменьшить симптомы заболевания. Анальгетики при подагре неэффективны.
Как лечить подагру в период обострения:
- колхицин и нестероидные противовоспалительные препараты — это первое, чем стоит лечить приступ подагры. Колхицин является растительным препаратом (производное безвременника). При приеме колхицина довольно часто возникают побочные эффекты (рвота, жидкий стул, сильный дискомфорт в животе, синдром мальабсорбции, геморрагический энтероколит, редко возникает миелосупрессия и гиперкоагуляция), поэтому стоит строго придерживаться рекомендуемых дозировок. Нестероидные противовоспалительные препараты (ацеклофенак, нимесулид, диклофенак, эторикоксиб) стоит принимать в максимальных терапевтических дозировках — меньшие могут быть неэффективны. Рекомендуется учитывать риск развития побочных реакций при их назначении у определённого контингента больных. К сожалению, использование НПВП ограничено вызываемыми ими побочными эффектами, которые включают гастро- и нефропатию, поражение печени и ЦНС, особенно у пожилых. При назначении колхицина надо помнить, что лечение будет более успешным, если его назначить в первые сутки и даже часы после развития приступа. Однократная доза не должна превышать 2 мг, а суммарная 4 мг Высокие дозы колхицина приводят к побочным эффектам( диарея, тошнота, рвота).
- глюкокортикоиды внутрисуставно, внутрь или парентерально, когда противопоказан колхицин, нестероидные противовоспалительные препараты или же лечение ими неэффективно. Эти препараты дают выраженный эффект, но должны быть назначены только врачом, злоупотребление глюкокортикоидами имеет необратимые последствия (развитие сахарного диабета, неконтролируемая артериальная гипертензия и т. д.);
- канакинумаб (Иларис) — моноклональные антитела к интерлейкину-1, используются у пациентов с частыми приступами (более трех приступов за последний год), которые не могут принимать колхицин и НПВП. [12][20]
Лечение хроничекого подагрического артрита
Чтобы успешно лечить хроническую подагру, нужно предупредить образование и растворить уже имеющиеся кристаллы моноурата натрия, а для этого необходимо поддерживать уровень мочевой кислоты ниже 360 мкмоль/л.
Пациенты подлежат диспансерному наблюдению у врача-ревматолога. Врач определяет периодичность контроля анализов, меняет (увеличивает или уменьшает) дозы получаемых препаратов, занимается лечением приступа. Противоподагрические средства принимаются длительное время. Также к лечению сопутствующей патологии могут быть подключены смежные специалисты (кардиолог, эндокринолог, уролог, нефролог). Пациент может быть госпитализирован в ревматологическое отделение при длительном по времени приступе, неэффективном лечении на амбулаторном этапе, а также для подбора постоянной терапии.
Прогноз. Профилактика
Прогноз зависит от своевременности и успешности начатого лечения, приверженности пациента к лечению, соблюдения диетических рекомендаций. По большей части прогноз благоприятный, но он ухудшается при развитии поражения почек, которое может стать даже причиной смерти пациента.
Как предупредить приступы подагры
Строгое соблюдение диеты является основным моментом в профилактике приступов подагры. Необходимо ограничить употребление алкоголя, не принимать некоторые лекарства (мочегонные препараты из группы тиазидов и петлевые мочегонные, неселективные бета-блокаторы, аспирин, никотиновую кислоту, леводопу). Если пациент худеет, то следует опасаться быстрой потери веса. Нужно стараться избегать обезвоживания и тяжелых физических нагрузок, воздействия низких температур. В профилактических целях аллопуринол может быть назначен только пациентам, страдающим онкологическими заболеваниями и получающим химиотерапию. [14]
За дополнение статьи благодарим Ирину Семизарову — ревматолога, научного редактора портала "ПроБолезни".
Анализируя отечественную и зарубежную литературу по проблеме этиологии реактивного артрита, выяснено, что наибольшая роль в качестве триггерных факторов принадлежит инфекциям, передаваемым преимущественно половым путём. Определена распространённость инфекций, передаваемых преимущественно половым путём в мировом масштабе. Выявлена частота встречаемости реактивного артрита в популяции. Показана зависимость роста заболеваемости инфекциями, передаваемыми преимущественно половым путём, от демографических, социальных и поведенческих факторов. Установлено, что одним из наиболее частых и тяжёлых экстрагенитальных осложнений является реактивный артрит, который ассоциируется с антигеном гистосовместимости HLA В27 и относится к группе серонегативных артритов. C. trachomatis рассматривается как основной причинный фактор развития иммунного воспаления в суставах.

1. Агабабова Э. Р. Дифференциальная диагностика серонегативных артритов // Терап. Арх. - 1986. - № 7. - С. 149 - 154.
3. Агабабова Э. Р. Серонегативные спондилоартриты // Руководство по внутренним болезням. Ревматические болезни; под ред. В. А.Насоновой, Н. В.Бунчука. - М.: Медицина, 1997. - С. 305-335.
4. Андерсене Д. П., Милтиньш А. П. Состояние оксиданстной системы при болезни Рейтера / Под ред. И. И. Ильина. - Челябинск, 1990. - С. 22-23.
6. Бакулев А. Л., Рубин В. И., Суворов А. П., Слесаренко Н. А. Болезнь Рейтера. - Саратов: Изд. Сарат. мед. ун-та, 1999. - С.72-80.
7. Белов Б. С., Тарасова Г. М., Солдатова С. И. Применение ровамицина (спирамицина) в комплексной терапии урогенного реактивного артрита // Клин. ревмат. - 1997. - № 1. - С. 33-35.
8. Белькова Ю. А. Дехнич А. В., Козлов Р. С. Реальная практика терапии бактериальных инфекций, передаваемых половым путем, в России: результаты многоцентрового фармакоэпидемиологического исследования // Вестник дерматологии и венерологии. - 2011.- № 1. - С.41-53.
10. Бревертон Д. А. Анкилозирующий спондилоартрит, болезнь Рейтера и родственные заболевания // Клиническая ревматология: Пер. с англ. - Х. Л. Ф. Каррея. - М.: Медицина, 1990. - С.93-120.
11. Глазырина Г. А. Особенности клиники и эпидемиологии болезни Рейтера у детей: Автореф. дис. . канд. мед. наук. - Челябинск, 1995.
12. Дубенский В. В. Болезнь Рейтера (обзор литературы) // Рос. журн. кож. и вен. болезней. - 1999. - № 5. - С. 26-29.
13. Дубенский В. В. Современные клинико-эпидемиологические и иммунологические аспекты болезни Рейтера // Вестн. дерматол. и венерол. - 2003. - № 1. - С. 55-60.
14. Ивашкин В. Т., Положенцев С. Д., Султанов В. К. Актуальные вопросы этиологии и патогенеза болезни Рейтера // Тер. арх. - 1991. - № 3. - С. 162-136.
15. Ильин И. И. Негонококковые уретриты у мужчин. - 3-е изд., перераб. и доп. - М.: Медицина, 1991. - С. 54-60.
16. Казакова Т. В., Рашид М. А., Шостак М. А.,Карпова Н. Ю. Реактивный артрит: клиника, диагностика, лечение // Лечебное дело. - 2010. - №1. - С. 11-22.
17. Киселева Н. М., Шубин С. В. О дифференциальной диагностике хронического урогенного артрита // Терап. арх. - 2000. - № 5. - С.52-55.
18. Ковалев Ю. Н. Роль иммунных нарушений в патогенезе, клиника и патогенетическая терапия болезни Рейтера: Автореф. дис. . д-ра мед. наук. - М., 1987.
20. Ковалев Ю. Н., Молочков В. А., Петрова М. С. Болезнь Рейтера. - М.: ГЭОТАР - Медиа, 2006. - 224 с.
21. Логинова Н. С., Файзулин Л. З., Жданов А. В. и др. Интерфероновый статус больных урогенитальным хламидиозом // Заболевания, передающиеся половым путем. - 1998. - № 6. - С. 19-21.
22. Молочков В. А., Орлова О. Е., Дмитриев Г. А., Брагина Е. Е. Некоторые особенности жизненного цикла хламидий. Атипичные формы существования // Рос. журн. кож. и вен. бол. - 1998. - № 6. - С. 54-58.
23. Насонова В. А. Реактивный артрит / В.А.Насонова, Е. Л. Насонов, Р. Т. Алекперов и др. // Рациональная фармакотерапия ревматических заболеваний / под ред. В. А. Насоновой, Е. Л. Насонова. - М.: Литтерра, 2003. - С. 136-138.
24. Порудоминский И. М. О неспецифических уретритах, эпидидимитах и простатитах// Урология. - 1955. - № 4. - С. 20-27.
26. Хансфилд Х. Заболевания, передающиеся половым путем: Справочник / Под ред. А. А. Кубановой, М. М. Васильева. - М., 2004. - С. 42-47.
27. Хрипунова И. Г., Журбина Н. В. Реактивные артриты. Методические рекомендации. -Ставрополь: ИЗД. СГМА, 2003. - С. 25.
28. Хобейш М. М., Монахов К. Н., Соколовский Е. В. Суставной синдром в практике дерматовенеролога. Нейросифилис. - Санкт-Петербург: СОТИС, 2001. - С. 3.
29. Шерман Ю. Ф., Ворониа Л. Г., Шевлюк Н. Н., Михайлова Е. А., Штиль О. О. Роль гонококковой инфекции и ее ассоциированных форм с другими инфекциями, передаваемыми преимущественно половым путём, в развитии клинико-морфологических изменений шейки матки // Вестник дерматологии и венерологии. - 2012. - № 1. - С. 34-37.
31. Aho К., Ahvonen P., Lassus A. HLA antigen 27 and reactive arthritis // Lancet. - 1973. - Vol. - P. 157.
33. Brewerton D.A., Caffrey M., Nicholls A. et al. Reiter's disease and HLA- 27 //Lancet. - 1973. - Vol.3; 2(7836). - P.996-8.
34. Gotz H., Veldhuijzen I., Ossewaarde J. Chlamydia trachomatis infections in multi-ethnic urban youth: a pilot combining STI health education and outreach testing in Rotterdam, Netherlands // Sex Transm Infect. - 2006. - Vol. 82(2). - P. 97-98.
35. Haibel H., Rudwaleit M., Sieper J. Diagnosis of reactive arthritis // Z Rheumatol. - 2004. -Vol .63(3). - P.211-215.
36. James W. H. Sex ratios and hormones in HLA related rheumatic diseases / W. H. James //Ann. Rheum. Dis. 1991. - Vol. 50, № 6. - P. 401-104.
38. Margo C. M., Crowson A. N., Peeling R. Vasculitis as the basis of cutaneous lesions in Reiters disease // Hum. Pathrol. - 1995. - Vol. 26. - P. 633-638.
39. Rothe M. J., Kerdel F. A. Reiters disiases. In: Demis D. I. ed. Clinical Dermatology. - 24 revision. - Philadelphia; New York: Lippincott-Raven Publischers, 1997; 1-5: 1-13.
40. Sigal L. H. Update on reactive arthritis / L. H. Sigal // Bull. Rheum. Dis. - 2001. - Vol. 50, № 4. - P. 1-4.
41. Sieper J., Kingsley. Recent advaces in the pathogenesis of reactive arthritis // Itnmun. Today. - 1996. - Vо1. 17(4). - P. 160-163.
42. Sieper J, Rudwaleit M, Khan M et al. Concepts and epidemiology of spondylarthritis // Best Pract Res Clin Rheumatol. - 2006. - Vol. 20(3). - P.401-417.
43. Winchester R. Reiters syndrome. In.: Dermatology in General Medicine. Eds. Th. B. Fitzpatrick et al. New York: McGraw Hill. - 1993. - № 14. - Р. 2199-2211.
Среди больных инфекциями, передаваемыми преимущественно половым путём, кроме собственно поражения урогенитальной сферы (уретрит, простатит, цервицит, сальпингит, эндометрит и т.п.), достаточно часто развиваются системные/экстрагенитальные проявления. Одним из наиболее тяжёлых и частых экстрагенитальных осложнений УГИ является реактивный артрит [26,3,11].
Реактивный артрит (РеА) - иммуновоспалительное заболевание суставов, которое возникает в течение одного месяца после перенесённой кишечной или мочеполовой инфекций, ассоциированное с антигенами гистосовместимости HLA B-27 и являющееся системным клиническим проявлением этих инфекций [28]. Частота встречаемости реактивного артрита в популяции составляет 0,1 % [17]. В ревматологических стационарах доля пациентов с реактивным артритом составляет около 10 %, причём хронические его формы сопровождаются значительным нарушением функциональной активности суставов, в силу развития тяжёлых осложнений, нередко (до 42 % случаев) приводящих к инвалидизации [32]. Увеличение роста заболеваемости РеА, преимущественное поражение лиц молодого возраста, частая хронизация патологического процесса, не всегда удовлетворительные результаты лечения определяют медико-социальную значимость данной проблемы. Кроме этого широкое распространение, высокая частота резистентности к терапии, нередкое формирование тяжёлых форм, отсутствие эффективных прогностических критериев раннего диагноза реактивных артритов определяют актуальность изучения данной проблемы [18,3,35].
Различают следующие разновидности реактивного артрита: 1) постэнтероколитический; его триггерными агентами являются серотипы иерсиний, сальмонелл, шигелл, кампилобактера, клостридий; 2) урогенитальный (урогенный), включая болезнь Рейтера; чаще эту форму связывают с хламидиями и уреаплазменной инфекцией. Эта два вида РеА ассоциируются с антигеном гистосовместимости HLA В27 и относятся к группе сеpонегативных спондилоартритов (спондилоартропатий) [29]. Риск развития урогенитального реактивного артрита у мужчин, имеющих HLA В27, в 10 раз выше, чем у лиц без этого антигена. Наличие указанного аномального гена отягощает течение болезни и её прогноз вследствие возникновения тяжёлых клинических симптомов, таких как выраженная лихорадка, быстрая потеря массы тела с последующим переходом в хроническое рецидивирующее течение [21]. Ассоциированность урогенитальных РеА с HLA-антигенами является достоверным фактом, и зачастую ревматологи их называют "болезнями круга В27 антигена" [1,34,38]. Кишечная и урогенитальная инфекции играют триггерную роль в развитии реактивного артрита, они запускают иммунопатологические процессы в суставе. В течение РеА выделяют две стадии: 1) инфекционную, когда формируется очаг инфекционного воспаления в урогенитальном тракте, который служит источником метастатических и токсических поражений суставов и других органов; 2) аутоиммунную, связанную с гиперергической перестройкой организма, когда развиваются реактивные воспаления суставов. Артриты, которые имеют непосредственную связь с инфекционными агентами, могут быть двух видов: 1) артриты, при которых доказан непосредственный контакт с полостью поражённого сустава (инфекционный артрит); 2) артриты, при которых существует связь с предшествовавшей или текущей инфекцией, но жизнеспособные болезнетворные агенты в полости поражения суставов выявить не удаётся (реактивные артриты) [5]. Наиболее тяжёлое течение заболевания, ранняя потеря функциональной активности суставов, быстрые темпы инвалидизации характерны для так называемого синдрома Рейтера, доля которого в структуре урогенных реактивных артритов составляет 30 % [9].
Заболеваемость РеА, связанная с мочеполовыми инфекциями, на 100 тыс. населения составляет 4,6-13 случаев, а с кишечными инфекциями - 5-14 случаев на 100 тыс. населения. Достаточно вариабельны данные показатели по различным регионам [17].
Частота РеА составляет 1-3 % у больных, перенесших хламидийную и 1,5-4 % (до 12 %) - кишечную инфекцию. Хронизация патологического процесса наблюдается в 15-50 % случаев и нередко является причиной длительной нетрудоспособности пациентов [24,37,41]. В общей структуре ревматических болезней на данный момент доля реактивных артритов составляет 5-11 % [7,42,38]. На долю же урогенных реактивных артритов (УРеА) приходится 50-75 %. [9,43]. Вариантом реактивного артрита является синдром или болезнь Рейтера - заболевание, характеризующееся сочетанием поражения мочеполовых органов, воспалением глаз и суставов по типу асимметричного реактивного артрита. Оно, как правило, возникает вследствие полового инфицирования у лиц с генетической предрасположенностью, преимущественно у носителей антигена HLA В27 [21]. В настоящее время большинство исследователей рассматривают C. trachomatis в качестве основного причинного фактора болезни Рейтера [10,13,23]. Частота встречаемости этого возбудителя при данной нозологии колеблется от 30,2 до 100 % [12,13,20,23]. Инфекция, обусловленная C. trachomatis, у лиц с болезнью Рейтера протекает, как правило, без выраженной клинической симптоматики, иногда бессимптомно. Это связано со способностью возбудителя к персистенции [19,23]. В возникновении болезни Рейтера играют роль несколько факторов - инфекционный, генетический, иммунный [6,13,14].
Известно, что хламидии служат основными возбудителями большей части негонококковых уретритов, а болезнь Рейтера наиболее часто развивается у мужчин, страдающих именно этим видом воспалений мочеполовых органов. В связи с этим многие авторы считают, что болезнь Рейтера является осложнением хламидийной инфекции, а хламидии - непосредственной её причиной [1,4,19,6]. В пользу хламидийной этиологии болезни Рейтера говорят следующие факты. Во-первых, закономерное нахождение хламидий в мочеполовых органах у большинства больных с данным заболеванием, не принимавших до обследования противохламидийных препаратов, а также высокая частота выявления у них специфических антител. Во-вторых, хламидийную этиологию подтверждает факт обнаружения некоторыми авторами хламидий или их антигенов непосредственно в суставной жидкости и периартикулярных тканях поражённых суставов, наиболее часто это отмечено в начальной стадии заболевания. В-третьих, о хламидийной этиологии косвенно свидетельствуют положительные результаты применения противохламидийных препаратов в ранних стадиях заболевания до развития иммунокомплексного реактивного воспаления суставов [21], а также возможность предотвращения развития болезни Рейтера у больных хламидийными уретритами при своевременном назначении им специфических препаратов в адекватных дозах [2] и, напротив, регистрация случаев болезни Рейтера у больных негонококковыми уретритами, лечившихся препаратами другой группы [16]. Наконец, хламидийные артриты экспериментально воспроизведены у лабораторных животных. Приведенные выше соображения делают весьма убедительными доводы в пользу хламидийной этиологии болезни Рейтера (или, по крайней мере, в большей части её случаев). Многими авторами болезнь Рейтера безоговорочно относится к осложнениям урогенитального хламидиоза. Около 10 % больных урогенитальным хламидиозом, по данным ВОЗ, могут иметь поражения суставов, глаз и иногда сердца [21].
Кроме хламидийной инфекции роль пускового агента болезни Рейтера некоторые авторы отдают гонококкам, которые с помощью ПЦР обнаруживали в синовиальной жидкости у 9 из 311 больных с этим заболеванием [39]. Однако болезнь Рейтера, как правило, возникает тогда, когда гонококки полностью элиминированы из организма, причём противогонококковая терапия не может предотвратить развития болезни Рейтера, даже если она начата в первые дни после появления симптомов уретрита. С целью дифференциальной диагностики таких случаев от типичного септического гонококкового артрита был предложен термин "постгонорейный артрит". Множественные наблюдения показали, что "постгонорейные артриты" по клиническим проявлениям, течению и лабораторным показателям (в том числе по частоте признаков хламидийной инфекции) ничем не отличаются от обычных форм болезни Рейтера, возникающих после негонококковых уретритов [25].
В последние годы вновь в качестве агента, способного стимулировать развитие болезни Рейтера, стали называть один из видов генитальных микоплазм -U.urealiticum. Гипотеза о причинной роли микоплазм в развитии этого заболевания в прошлом имела отдельных сторонников [21]. Гонококки и микоплазмы у ряда лиц с болезнью Рейтера некоторые авторы рассматривают в качестве факторов, трансформирующих латентную хламидийную инфекцию в клинически выраженное заболевание и способствующих её диссеминации [5].
По мнению многих авторов, болезнь Рейтера рассматривают как мультифакториальное заболевание со сложным патогенезом, в котором инфекционный агент с артрогенными свойствами играет роль только пускового механизма, а затем включаются при наличии определённой предрасположенности аутоиммунные и другие механизмы. При этом болезнь Рейтера может приобретать хроническое рецидивирующее течение, несмотря на элиминацию возбудителя, вследствие эффективной этиотропной терапии [2,21].
Рецензенты:

Разработчик сайтов, журналист, редактор, дизайнер, программист, копирайтер. Стаж работы — 25 лет. Область интересов: новейшие технологии в медицине, медицинский web-контент, профессиональное фото, видео, web-дизайн. Цели: максимально амбициозные.
- Запись опубликована: 27.12.2021
- Reading time: 4 минут чтения
Мочевая кислота — результат трансформации азотистых оснований, в основном выводимый с мочой. Ее концентрация зависит от разницы между количеством, вырабатываемым в организме и выводимым почками. Лишняя мочевая кислота (гиперурикемия) откладывается в виде кристаллов, давая серьезные симптомы.
Анализ на мочевую кислоту в крови или в моче обычно выполняется при симптомах подагры и заболеваний почек. Многих больных, получивших негативный результат, беспокоит вопрос о том, как убрать излишки мочевой кислоты, тем самым уменьшив боль, сопровождающую гиперурикемию.
Что такое мочевая кислота? Откуда она берется в организме?
Мочевая кислота — это конечный и естественный продукт метаболизма пуринов — элемента нуклеиновых кислот (ДНК и РНК) клеток всех организмов. Источники азотистых оснований — внутренний синтез этих соединений и физиологический распад клеток. Некоторые пурины также попадают в организм с продуктами: пивом, красным мясом, копченой рыбой, какао.
Пурины благодаря ферментам деградируют в гепатоцитах печени. Это означает, что конечный продукт их распада должен выводиться, так как больше ни во что не преобразуется. Примерно 70% мочевой кислоты выводится с мочой, фильтруемой через почки, остальное, при участии пищеварительной системы, с калом.
Выведение моч. к-ты затрудняется, например, в случае мочекаменной болезни или подагры. Также это вещество накапливается в больших количествах в крови, в ходе некоторых метаболических заболеваний.
Когда назначаются анализы?
Измерить уровень мочевой кислоты нужно в ряде случаев:
- Подозрение на подагру. Ее симптомы: болезненность, покраснение и отек суставов, особенно воспаление основания сустава большого пальца ноги. Подагра часто вызывает воспаление суставов, особенно первого плюснефалангового сустава.
- Диагностика мочекаменной болезни . Патология связана с выведением большого количества мочевой кислоты. В случае тяжелой почечной колики анализ помогает определить тип мочевых камней у больного. Почечная колика характеризуется сильной болью внизу живота, иррадиирующей вплоть до спины. Также у больных отмечается выраженное уменьшение выделяемой мочи, гематурия или изменение цвета мочи.
- Почечная недостаточность .
- Гестоз у беременных .
Дополнительные (неспецифические) симптомы при повышении мочевой кислоты:
- боль и жжение в области мочевого пузыря;
- Увеличение количества мочи;
- лихорадка;
- боль в животе и поясничной области;
- тошнота и рвота.
Обследование также должно проводиться среди онкологических больных, проходящих химиотерапию и лучевую терапию. Химиотерапия ускоряет разрушение раковых клеток с высвобождением из них пуриновых соединений, впоследствии превращающихся в мочевую кислоту. Также анализы назначаются для контроля за ходом лечения у больных подагрой.
Определение мочевой кислоты в крови и моче. Как подготовиться к исследованию?
Уровень мочевой кислоты может определяться в моче и в сыворотке крови. В случае определения сыворотки венозная кровь берется натощак: желательно выждать 12 часов с момента приема пищи. Важно понимать, что употребление продуктов, богатых пуринами, может фальсифицировать результат, поэтому за двое суток нужно исключить такие продукты из меню.
При подготовке к обследованию нужно избегать физических нагрузок 2-3 дня до анализа. Также нужно ограничить стрессовые факторы. Риск повреждения клеток и временного повышения концентрации мочевой кислоты в крови должен быть сведен к минимуму.
Во время сбора мочи следует придерживаться тех же рекомендаций, что и при подготовке к сывороточному тесту.
Как делают анализ
Измерение концентрации мочевой кислоты заключается в единовременном сборе крови из локтевой вены, с помощью одноразовой иглы и пробирки. Методика проведения теста — спектрофотометрия (колориметрический иммуноферментный метод).
Концентрацию МК в моче можно определить как в одном образце, так и в суточном сборе мочи. Второй метод заключается в сборе всех образцов мочи, сданных в течение 24 часов, в один стерильный сосуд. Затем нужно измерить объем мочи и взять из нее образец, предназначенный для исследования в лаборатории.
Мочевая кислота – нормы для женщин, мужчин и детей
Уровень мочевой кислоты зависит от пола, а дополнительно увеличивается с возрастом, примерно до 70 лет. Анализ результатов испытаний всегда должен основываться на референсных значениях лаборатории, в которой они были выполнены, и находящихся в пределах заданных диапазонов стандартов.
Таблица 1. Средние нормы мочевой кислоты в сыворотке крови (Европа)
| Пол, возраст | Норма мочевой кислоты |
| Мужчины | 300-360 мкмоль/л (5-6 мг/дл) |
| Женщины | 240-300 мкмоль/л (4-5 мг/дл) |
| Дети | 210-240 мкмоль/л (3,5-4 мг/дл) |
Гиперурикемия диагностируется после нескольких определений концентраций выше 420 мкмоль/л (>7 мг/дл). Среднее выведение мочевой кислоты с мочой составляет около 400-650 мг/сут. Верхний предел обычно составляет 800 мг / день (4,8 ммоль / 24 часа).
Приступ подагры может быть у больного с нормальным уровнем мочевой кислоты и наоборот – повышенный уровень мочевой кислоты не всегда дает симптомы подагры. Наиболее частая причина подагры: генетическая склонность к избыточной выработке мочевой кислоты и нарушение выделительной функции почек. Поэтому, перед тестом расскажите врачу о прошлых заболеваниях и о лекарствах, которые вы принимаете.
Низкий и высокий уровень мочевой кислоты — чем это опасно?
Высокий и низкий уровень мочевой кислоты влияет на правильное функционирование организма. МК обладает противоположными эффектами:
- С одной стороны это ненужный продукт метаболических изменений. Поэтому повышение ее концентрации опасно для здоровья. Гиперурикемия приводит к подагре, нефролитиазу и другим заболеваниям почек. Также у людей с повышенной мочевой кислотой часто диагностируются гипотиреоз, гемолитическая анемия и сердечно-сосудистые заболевания, в том числе инфаркт, что говорит о связи этих факторов.
- С другой — мочевая кислота обладает антиоксидантным действием, защищая организм от свободных радикалов и вызванных ими повреждений клеток. Ее дефицит, например, увеличивает риск развития деменции, болезни Паркинсона.
Нельзя самостоятельно интерпретировать результаты анализов. Результат определения мочевой кислоты часто трактуется как вспомогательный к комплексной диагностике.
Расшифровка анализа: высокий уровень мочевой кислоты
Гиперурикемия может быть связана с чрезмерной выработкой МК или ее высвобождением из клеток, например:
- при генетических заболеваниях (болезнь Леша-Нихана, болезнь фон Гирке);
- из-за разрушения клеток в процессе лечения рака, при лучевой терапии или химиотерапии;
- из-за отравления свинцом;
- в случае лейкоза;
- в постменопаузальном периоде.
Гиперурикемия также возникает у людей с больными почками при ацидозе или злоупотреблении алкоголем. Также может повлиять диета с большим количеством белка и физические перегрузки. Ещё повышает уровень мочевой кислоты прием барбитуратов и диуретиков.
Наиболее распространенные симптомы гиперурикемии:
- Почечная колика . Больной чувствует сильную поясничную боль, иррадиирующую в сторону и в нижнюю конечность. Она имеет тенденцию смещаться. Часто боль сопровождается слабостью, лихорадкой и тошнотой;
- Подагра. Сопровождается лихорадкой и слабостью. Это следствие отложения кристаллов моч. к-ты в суставах, в результате чего возникает воспаление суставов.
Расшифровка анализа: низкий уровень мочевой кислоты
Концентрация МК в крови может быть снижена. Однако это не указывает на конкретное заболевание, а скорее возникает как сопутствующий симптом. Снижение может происходить при:
- Болезни Вильсона;
- синдроме Фанкони;
- заболеваниях, связанных с избыточной секрецией гормона роста;
- Синдроме Шварца-Барттера.
Слишком низкий уровень мочевой кислоты также может указывать на продолжающееся воспаление в почках и печени, целиакию, лимфомы и другие виды рака.
Снижают концентрацию препараты, применяемые для лечения гиперурикемии: салицилаты, аллопуринол, пробенецид, эстрогены, кортикотропин, фенотиазины.
Как снизить мочевую кислоту?
Основа лечения гиперурикемии — излечение основного заболевания, так как избыток моч. к-ты может быть результатом врожденных генетических состояний, результатом ожирения, неправильного питания, диабета или обезвоживания.
Чтобы очистить организм от избытка кристаллов мочевой кислоты, нужно увеличить физическую активность и следовать принципам рационального питания.
Диета больных с высоким уровнем мочевой кислоты основывается в первую очередь на употреблении негазированной воды и отказе от крепкого кофе, чая и пива. Также повышают мочевую кислоту в крови напитки, содержащие фруктозу и фруктовые соки. Второй принцип — ограничение пуринов. Это диета, бедная рыбой, красным мясом, бобовыми, грибами.
Количество соли в блюдах следует ограничить, так как избыток натрия тормозит выведение мочевой кислоты с мочой.
Нужно есть больше постного мяса птицы, фруктов и зерновых. Очень хороший эффект дают настои, приготовленные из листьев березы, одуванчика и крапивы.
Назначается фармакотерапия, понижающая мочевую кислоту в крови. Наиболее распространенные лекарства: фебуксостат и аллопуринол. Помимо приема лекарств нужно бросить курить.
Точные рекомендации всегда должны быть согласованы с лечащим врачом (например, урологом, ревматологом), который также принимает решение о необходимости возможной фармакотерапии.
Венерические заболевания, также известные как венерологические инфекции, могут быть вызваны бактериями, вирусами, грибками или паразитами. Заражение может происходить не только во время классического интимного общения, но и при оральном и анальном контактах.
В этой статье мы расскажем о 15 наиболее распространенных венерических заболеваний.
Как происходит заражение
Венерические заболевания — это группа инфекций, которые могут передаваться половым путем: вагинальным, оральным или анальным. В редких случаях заражение происходит при использовании зараженных предметов — мокрых полотенец, губок или интимных принадлежностей.
Факторы, повышающие риск заражения венерическими заболеваниями, включают большое количество сексуальных партнеров, отказ от презервативов и злоупотребление психоактивными веществами, которые усиливают склонность к рискованному сексуальному поведению.

Отказ от презервативов
Доказано, что чаще всего страдают венерическими заболеваниями люди в возрасте от 15 до 24 лет, с низким материальным статусом, проживающие в крупных городских агломерациях, а также мужчины гомосексуальной ориентации, не остающиеся в постоянных отношениях.
Венерические заболевания, вызванные бактериями
Гонорея
Гонорея вызывается грамотрицательными бактериями Neisseria gonorrhea. Заражение почти всегда происходит при половом контакте. Особый случай — когда больная мать заражает ребенка во время родов. Экстрасексуальные инфекции чрезвычайно редки и могут возникать в результате использования инфицированных предметов, например, влажной губки или полотенца (бактерии могут сохраняться на них от 3 до 24 часов).
Гонорея у женщин чаще всего протекает бессимптомно, однако могут возникать гнойные выделения, боли в нижней части живота, жжение во влагалище , нарушения менструального цикла и обильные менструации.

У мужчин заболевание проявляется в виде гнойных выделений из уретры, ощущения жжения и боли при мочеиспускании.
Сифилис
Сифилис вызывается бактерией спирохета. Заражение происходит в основном через половой контакт (вагинальный, оральный, ректальный). Возможно заразиться даже поцелуем, если бактерии присутствуют на слизистой рта человека
У половины людей сифилис не дает никаких симптомов, но даже в скрытой форме он влияет на здоровье и, если его не лечить, повреждает нервную и сердечно-сосудистую системы, кости, суставы, вызывает психические расстройства и слепоту.
Болезнь может привести к появлению симптомов — на первом этапе на половых органах или вульве появляется язва, затем сыпь на ладонях и ступнях ног, которые проходят сами собой. Далее болезнь продолжается скрыто.


Хламидиоз
За развитие хламидиоза ответственна Chlamydia trachomatis. У 50% мужчин и 75% женщин при заражении симптомы отсутствуют, и болезнь диагностируется только тогда, когда начинаются осложнения — эпидидимит у мужчин или воспаление придатков у женщин.
Заражение может происходить не только при половом контакте, но и через поврежденную кожу и слизистые оболочки. Без лечения хламидиоз приводит к проблемам с фертильностью.
Язвы, вызванные хламидией трахоматис
Заболевание, вызванное бактериями Chlamydia trachomatis ранее встречалось в основном в тропических и субтропических странах. Но теперь распространилось и в Европе, в т.ч. в России.
Проявляется в виде язв, везикул или папул на половых органах. Вызывает воспаление лимфатических узлов, боли в суставах, абсцессы.
Венерическая язва
Венерическая язва, также известная как мягкая, чаще встречается у мужчин, чем у женщин. Причиной образования являются бактерии Haemophilus ducreyi. Основной симптом заболевания — болезненное изъязвление на половых органах, которое выглядит как зерно чечевицы с ярко-красной каймой. Болезнь сопровождается опухшими лимфатическими узлами.
Язвенная инфекция в развитой Европе встречается редко, чаще ее диагностируют в развивающихся странах, увы, и в России.
Негонококковый уретрит (НГУ)
Негонококковый уретрит чаще встречается у женщин. Его провоцирует в большинстве случаев бактерия хламидия — Chlamydia trachomatis (30% случаев), реже вагинальные трихомонады Ureaplasma urealyticum или Mycoplasma genitalium.
Симптомы, которые могут возникнуть как у мужчин, так и у женщин, — частые позывы переполненности мочевого пузыр я, боль и жжение при мочеиспускании. Кроме того, у женщин могут возникнуть неприятные выделения из влагалища и гнойные выделения из уретры у мужчин.


Венерические заболевания, вызванные вирусами
СПИД является последней стадией заражения вирусом иммунодефицита человека ( ВИЧ ). На начальном этапе заболевание не имеет симптомов и может оставаться скрытым до 10 лет. Только на поздней стадии СПИД вызывает вспышку таких заболеваний, как пневмония, туберкулез, рак.
Наиболее распространенная причина инфекции — сексуальный контакт. Также заражение может происходить через кровь (например, при использовании нестерильных медицинских инструментов) и во время родов, когда мать заражает новорожденного ребенка.
Люди, имеющие половые контакты с несколькими партнерами, должны регулярно проходить тестирование на ВИЧ, так как отсутствие симптомов может привести к невольному инфицированию других людей.
Генитальный герпес
За развитие генитального герпеса отвечает ВПГ-2. Он изначально проявляется маленькими группами болезненных пузырей, располагающихся вокруг половых органов или заднего прохода. Пузырьки увеличиваются в течение 1-2 недель, а затем лопаются и трансформируются в мелкие язвы.
Лечение состоит из противовирусных пероральных препаратов и смазывания пораженных участков противовоспалительными мазями.

Противовирусные пероральные препараты
Беременным женщинам, являющимся носителями вируса герпеса, показано родоразрешение путем кесарева сечения, чтобы устранить риск заражения новорожденного.
Вирусный гепатит
Заражение гепатитом В происходит главным образом через кровь, но также возможно инфицирование при половом контакте. Опасен не только половой акт, но и прямой контакт со спермой или выделениями из влагалища больного человека.
Инфекция предотвращается (хотя и не на 100%) использованием презервативов.
Генитальные бородавки (ВПЧ)
Генитальные бородавки — это следствие венерического заболевания, вызываемого вирусом папилломы человека (ВПЧ). Инфекция проявляется в форме папул и папилл, расположенных вокруг заднего прохода и половых органов (как снаружи, так и внутри, например, во влагалище).
В более редких случаях кондиломы могут возникать во рту — на языке, на слизистой оболочке глотки, гортани, губах. Нелеченные кондиломы со временем превращаются в похожие на цветную капусту наросты с беловатым оттенком. Папилломы могут перерождаться в рак, так как именно вирус папилломы является основным источником рака шейки матки. У мужчин он вызывает рак полового члена.
Лечение предполагает использование противовирусных мазей, кремов и криотерапию (замораживание). В случае больших поражений необходимо лазерное удаление.
Контагиозный моллюск
Контагиозный моллюск вызывается вирусом оспы Poxviridae. У взрослых он чаще всего передается половым путем, реже при контакте с инфицированными объектами. Характерный симптом этого заболевания — появление твердых, полупрозрачных выпуклостей телесного, жемчужного или желтого цвета, которые заполнены пористым веществом внутри.
У мужчин поражения расположены на половом члене, а у женщин — на лобковых буграх, половых губах, в паху, в округ заднего прохода.

Поражения вокруг заднего прохода
Контагиозный моллюск не опасен и, как правило, вызванные им изменения самопроизвольно исчезают через несколько месяцев. Однако, во избежании осложнений, рекомендуется провести лечение. Гинеколог и уролог выписывают специальные мази и пероральные препараты. Большие поражения иссекаются, лазером или электроножом.
Венерические заболевания, вызванные простейшими и грибами
Трихомониаз
Трихомониаз вызывается простейшими — влагалищной трихомонадой Trichomonas. Основным путем заражения является половой акт, реже контакт с инфицированными объектами (особенно с туалетными принадлежностями, удерживающими влагу, например, полотенца, губки).
Симптомы трихомониаза встречаются в основном у женщин (у мужчин заболевание обычно протекает бессимптомно) и включают желто-зеленые, пенистые выделения из влагалища, зуд и жжение во влагалище, боли в мочеиспускательном канале и сильные позывы в туалет.
Генитальный кандидоз
Кандидоз, или грибковая инфекция половых органов, чаще всего вызывается дрожжами Candida albicans . Более подвержены риску развития заболевания люди, принимающие антибиотики, и те, чья кожа повреждена в результате трения, различных видов травм или контакта с моющими средствами.
У женщин кандидоз вызывает неприятный зуд, жжение и сыроподобные выделения. Заболевание редко поражает мужчин, но когда оно развивается, оно вызывает такие симптомы, как жжение и зуд половых органов, красные пятна и пузырьки на крайней плоти, дискомфорт во время полового акта.
Венерические заболевания, вызванные паразитами
Чесотка в интимных зонах
Чесотка в области интимных органов вызвана внешним паразитом — клещом человеческой чесотки. Первые симптомы заболевания появляются через 1-2 месяца после того, как паразит начинает существовать в организме. К ним относятся, прежде всего, сильный зуд кожи — у мужчин вокруг мошонки и полового члена, у женщин в области половых губ и лобка.

Чесотка в интимной зоне
Паразиты невидимы невооруженным глазом и размножаются, строя в канальцах эпидермиса (чесоточных коридорах), где они откладывают яйца. Лечение чесотки предполагает смазывание зараженных мест специальными препаратами.
Лобковые вши
При заражении вшами, паразитирующими в интимной области, пациентов мучает хронический зуд не только гениталий, но и лобка, живота, паха, бедер. Заражение этим типом вшей обычно происходит во время полового контакта, но паразиты могут также перемещаться в лобковые области от одежды, постельных принадлежностей или полотенец, принадлежащих инфицированному человеку.
Лечение вшей включает использование специальных мазей, лосьонов и шампуней.
Все вышеперечисленные заболевания дают осложнения и очень заразны, поэтому, при появлении любых симптомов, нужно обратиться к гинекологу, урологу или дерматологу, и сдать анализы. Не занимайтесь самолечением, так как симптомы этих инфекций схожи с другими заболеваниями, но лечатся по-разному. Неправильное лечение лишь усугубит симптомы.
Читайте также:

