Помощь при отравлении местными анестетиками
Обновлено: 24.04.2024
Патологическое состояние, обусловленное местным прижигающим, а также общим резорбтивным действием едких химических соединений на организм в результате однократного приема потенциально токсических доз.
Классификация
Диагностика
Диагностические критерии: отравления кислотами
При отравлении кислотами на месте соприкосновения с тканями кислоты вызывают прижигание. Всасывание кислот и продуктов тканевого распада обуславливает общетоксическое действие. Наиболее выражен резорбтивный эффект при отравлениях слабодиссоциирующими органическими кислотами, при отравлениях кислотами с высокой константой диссоциации преобладают симптомы местного поражения.
Различают токсикогенную фазу (патологические реакции в результате специфического действия прижигающего яда на организм), соматогенную (патологические реакции со стороны организма, возникающие преимущественно после удаления или разрушения прижигающего яда).
Клинические проявления: местные, обусловленные химическим ожогом в основном желудочно-кишечного тракта, а также химические ожоги дыхательных путей в результате прямого воздействия паров кислот или их попадания вместе с аспирированными рвотными массами. Химические ожоги характеризуются стадийностью течения.
Первая стадия - острое поражение различной глубины и обширности (первая неделя отравления), коагуляционный некроз 24-48 часов.
Вторая стадия - образование грануляционной ткани (первые две недели), в этой стадии наиболее вероятны перфорации ожоговой поверхности.
Третья стадия - образование рубца и стриктуры. Фиброзная ткань начинает формироваться спустя 2-4 недели.
Общие проявления: обусловленные резорбтивным действием прижигающего яда, его гемолитической способностью, способностью разрушать клеточные мембраны слизистой оболочки желудочно-кишечного тракта, дыхательных путей, а также клеточных мембран сосудистой стенки.
Осложнения: в токсикогенной фазе (1-2 сут.) - гипотензия, экзотоксический шок (выход жидкой части крови во внеклеточное пространство), ранние первичные желудочно-кишечные кровотечения (непосредственное повреждение сосудистой стенки, 1-ые часы отравления), ранние вторичные (1-2 сут., лизис тромбов), перфорация, отек гортани (выброс биологически активных веществ, усугубляющих местный химический отёк), отёк легких (поражение альвеолярно-каппилярной стенки, выброс биологически активных веществ, выход жидкой части крови).
Осложнения в соматогенной фазе (позднее 3-х суток): желудочно-кишечные кровотечения, трахеобронхиты и пневмонии, острая почечно-печеночная недостаточность (острый гемоглобинурийный нефроз), коагулопатии, рубцовые деформации пищевода и желудка, малигнизация рубцово-деформированных стенок пищевода, желудка.
Жалобы и анамнез: тошнота, рвота, жидкий стул, нередко с кровью, боли в горле, по ходу пищевода, эпигастрии, затрудненное дыхание, повышенное слюноотделение, общая слабость, жажда.
Физикальное обследование: психо-моторное возбуждение, экзофтальм, следы ожога на коже подбородка, шеи, гиперемия, отек слизистой ротовой полости, зева, гортани, гиперсаливация, выраженный рвотный рефлекс, бледность, сухость кожных покровов, осиплость голоса, затрудненное дыхание, аускультативно в лёгких ослабленное дыхание, сухие и влажные хрипы, при отеке легких, разнокалиберные хрипы, тахикардия, гипотензия, болезненность в эпигастрии при пальпации, увеличенная печень, положительный симптом Пастернацкого с обеих сторон, гипертермия, жидкий стул возможно с кровью, олигоанурия.
Лабораторные исследования: наличие гемолиза в крови и моче, лейкоцитоз, снижение эритроцитов, гемоглобина, повышение трансаминаз, продуктов азотистого обмена, билирубина, снижение уровня электролитов, признаки гипо- и гиперкоагуляции, наличие белка в моче, свежих и изменённых эритроцитов, повышение лейкоцитов.
Инструментальные исследования
ФГДС
1-10 день: катаральные, катарально-фибринозное воспаление, эрозивные, эрозивно-язвенные поражения ЖКТ, обширные кровоизлияния, кровотечения, язвенно-некротическое поражение.
11-12 день: развитие грануляционной ткани, со 2-4-го месяца с момента отравления - рубцовые деформации грудного отдела, нижней трети пищевода.
Показания для консультации специалистов: консультация хирурга при ранних, поздних кровотечениях, перфорации стенки желудка, пищевода, стриктурах пищевода. Консультация нефролога при острой почечной недостаточности.
Отравление ингаляционными анестетиками и его лечение
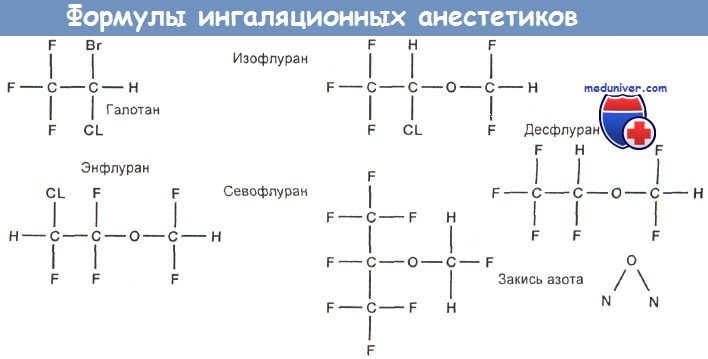
Ингаляционные анестетики широко применяются из-за своей способности быстро индуцировать анестезию, относительной простоты контроля за их действием, а также быстрого и безопасного возвращения пациента к норме. Наиболее популярны закись азота (N2O), галотан, энфлуран, севофлуран и изофлуран. Их анестезирующее действие зависит от парциального давления в головном мозге (Рм), которое коррелирует с парциальным давлением в альвеолах (Рд).
Периодически измеряя (с помощью масс-спектрометрии) и корректируя РА, анестезиолог способен регулировать глубину анестезии, т. е. Рм. Поступление в организм и распределение этих средств зависят от их концентрации во вдыхаемой смеси, от легочной вентиляции, растворимости в крови, сердечного выброса и тканевого поглощения. Во время наркоза формируется нисходящий градиент их концентрации: подаваемый газ — альвеолы — артерии — головной мозг
Структурные формулы ингаляционных анестетиков приведены на рисунке ниже.
Их токсичность скорее всего обусловлена фармакологически активными метаболитами. К другим ее механизмам относятся взаимодействие анестетика с белками и тканями (см. в статье "Закись азота" о витамине В12). Галотан, энфлуран и изофлуран приводили к серьезным и часто летальным передозировкам.
а) Токсичные дозы ингаляционных анестетиков:
- Галотан. Доза галотана 2,5 мл была по ошибке введена внутривенно. Пациент выжил. Прием внутрь 150—200 мл галотана взрослым привел к коме. Пациент выжил. После приема внутрь 250 мл галотана пострадавший в возрасте 48 лет выжил, пробыв в коме 36 ч.
- Изофлуран. Ингаляция 10,2 % изофлурана привела к цианозу и шоку. Пациент выздоровел. Прием внутрь 80 мл изофлурана мужчиной в возрасте 37 лет привел к его смерти.
б) Летальные дозы ингаляционных анестетиков:
- Энфлуран. Ингаляция 250 мл энфлурана привела к смерти женщины в возрасте 29 лет.
- Галотан. Внутривенное введение 3 мл смеси галотана с метогек-ситалом вызвало смерть женщины в возрасте 20 лет от острого отека легких. Прием внутрь 35 мл галотана взрослым завершился летальным исходом.
- Закись азота. Экспозиция к 50—70 % закиси азота в течение 3 ч может снизить активность печеночной метионин-синтазы, приведя к апластической анемии и смерти.
в) Профессиональная ингаляция анесетиков. Опасность энфлурана, галотана и изофлурана для медперсонала, работающего в хорошо вентилируемой операционной, невелика. Сильная профессиональная экспозиция чревата индукцией печеночных микросомных ферментов, метабол изирующих лекарственные средства.
г) Токсикокинетика ингаляционных анестетиков:
- Кардиотоксичность. У взрослых, получивших галотановый наркоз, после введения адреналина (2,0—4,0 мкг/кг в солевом растворе) или 0,5 % лидокаина наблюдалась электрическая нестабильность желудочков. Галотан, вводимый путем инфильтрации детям с уровнем адреналина до 10 мкг/мл, по-видимому, относительно безопасен, если пациент нормо- или гипокапнический и не страдает от врожденного кардиологического заболевания. Похоже, дети менее чувствительны к серьезному аритмогенному действию адреналина на желудочки.
Однако у них возможны предсердные экстрасистолы и тахикардия, что подчеркивает необходимость непрерывного электрокардиографического мониторинга и осторожности при галотановой анестезии с инъекцией адреналина. Закись азота, добавляемая во время стационарной анестезии галотаново-кислородной смесью, может повысить среднее артериальное давление, давление в правом предсердии и системное сосудистое сопротивление. Остановка сердца наблюдалась при использовании галотана с верапамилом и фенфлурамином. Галотан может потенцировать действие нервно-мышечных блокаторов. Экспозиция к трихлорэтану после галотановой анестезии чревата кардиотоксичностью.
- Изофлуран. Изофлуран существенно потенцировал действие атракурия и векурония. Налбуфин снижает потребность в изофлуране. Последний, похоже, ингибирует у человека метаболизацию энфлурана.
- Закись азота. Закись азота может ослабить терапевтическую эффективность и усилить побочные эффекты метотрексата. При введении адреналина с лидокаином пациенту, получающему закись азота, у больного наблюдалась предсердно-желудочковая диссоциация.
д) Ингаляционные анестетики при беременности и лактации:
- Энфлуран. Энфлуран расслабляет мускулатуру матки. Ее реакция на окситоцин сохраняется, если не применять высоких (более 2,5 — 3,0 %) концентраций этого анестетика.
- Галотан. Галотан вызывает зависимое от дозы расслабление маточной мускулатуры как у беременных, так и у небеременных женщин. Во время родов он может привести к атонии матки, сопровождающейся повышенной кро-вопотерей.
- Изофлуран. Изофлуран индуцирует расслабление матки.
- Закись азота. Введение закиси азота во II триместре беременности не оказало отрицательного влияния на плод.
е) Механизм действия ингаляционных анестетиков. Непосредственное действие на дыхательные центры продолговатого мозга на участвующие в дыхании мышцы грудной клетки и диафрагму приводит к зависимому от дозы угнетению дыхания.
ж) Клиника отравления ингаляционными анестетиками:
- Циклопропан. Взрослый человек обнаружен в 1989 г. мертвым после приема внутрь циклопропана. Это первый летальный исход такого рода со времени внедрения циклопропана в клиническую анестезиологическую практику в 1933 г..
- Десфлуран. Как и в случае с изофлураном, применение десфлурана чревато увеличением объема головного мозга или внутричерепного давления. Его использование при нейрохирургии требует особой осторожности.
- Энфлуран. Сердечно-сосудистая система. Энфлуран удлиняет интервал Q—Тс, не влияя на интервалы QRS, P-R и Q-T.
- Печень. Повторная анестезия энфлураном изредка приводит к летальному некрозу печени. Клинические, биохимические и гистологические особенности связанного с этой анестезией гепатита сходны с наблюдаемыми при аналогичной патологии, вызываемой галотаном.
Экспозиция к изофлурану чревата молниеносной гепатотоксической реакцией.
- Галотановый гепатит. Elliott и Strum описали связанный с галотаном гепатит, проявляющийся одним из двух клинических синдромов, чаще всего наблюдаемых у взрослых пациентов. Они развиваются после гладко прошедших анестезии и операции и не демонстрируют явной корреляции со временем применения или дозой вещества. Один из синдромов характеризуется умеренным повышением концентраций аминотрансфераз и в ряде случаев транзиторной желтухой. Ухудшение клинического состояния наблюдается редко. Такой гепатит возможен и во время экспозиции к галотану, а его распространенность достигает 20%.
Второй синдром наблюдается с частотой 1:35 000 пациентов, связан с частым повторным введением вещества через короткие интервалы времени и характеризуется молниеносным развитием печеночной недостаточности с высокой смертностью.
- Нервная система. Продолжительное применение галотана и энфлурана в качестве бронхолитиков при стойком астматическом статусе, по-видимому, индуцировало тетраплегию и сенсорные нарушения у одного взрослого, состояние которого улучшилось после отмены обоих средств. Применение энфлурана чревато припадками без потери сознания.
- Сердечно-сосудистая система. Введение галотана взрослым, вероятно, не оказывает существенного влияния на интервалы P—R и QRS, но увеличивает интервалы Q—Т и Q—Tc.
- Острое отравление. Сильная токсичность галотана при его внутривенном введении (отек легких, припадки) резко контрастирует с почти полным ее отсутствием при ингаляционном использовании данного вещества.
- Десфлуран. Десфлуран, применяемый с искусственной вентиляцией и постоянным РаСО2, вызывает угнетение сердечно-сосудистой функции. Сердечный выброс почти не меняется.
- Изофлуран. Анестезия изофлураном, по-видимому, не ведет к значительному изменению интервалов QRS, P—R и Q—T, но существенно удлиняет интервал Q—Tc. Изредка при этой процедуре наблюдается злокачественная гипертермия.
- Закись азота. Проблемы. Закись азота можно эффективно использовать, только снижая концентрацию подаваемого кислорода. Ее кинетические свойства чреваты раздуванием внутренних газоносных пространств, растяжением кишечника, нарушением условий проведения операции и удлинением госпитализации. Она может угнетать дыхание и кровообращение, а также повышать мышечный тонус, что ведет к увеличению необходимой дозы миорелаксанта. Этот газ поддерживает горение. Он может инактивировать производную В12 составляющую фермента метионин-синтазы. Закись азота участвует в разрушении озонового экрана в верхних слоях атмосферы и формировании парникового эффекта в ее нижних слоях.
- Регулярное применение. Продолжительное использование закиси азота (в течение нескольких суток) чревато апластической анемией, нейронной дегенерацией, мегалобластическими изменениями и летальным исходом.
- Острая экспозиция. Закись азота с минимальной альвеолярной концентрацией 104 %, или 1,04 атм., применяется как вспомогательный анестетик при большинстве операций под наркозом. Анестезия с использованием только N2О в течение 2—4 ч индуцировала у нормальных людей тахипноэ, тахикардию, повышение системного кровяного давления, предсердно-желудочковый узловой ритм, острую сердечнососудистую недостаточность, мидриаз, профузное потоотделение, изредка клонус и опистотонус.
з) Лабораторные исследования при отравлении ингаляционными анестетиками:
- Энфлуран. Высокие уровни неорганического фторида не были токсичными.
- Изофлуран. При анестезии изофлураном гепатотоксичность обычно наблюдается только в условиях тяжелой гипоксии.
- Злоупотребление закисью азота. Неоднократное злоупотребление "веселящим газом" часто индуцирует угнетение костного мозга. Может потребоваться детальное гематологическое обследование, включая определение уровней в крови фолата и витамина В12. Признаки тяжелой недостаточности этих двух веществ после однократного операционного наркоза закисью азота наблюдаются редко.
и) Лечение отравления ингаляционными анестетиками:
- Стабилизация состояния. При обнаружении передозировки ингаляционного анестетика нужно немедленно прекратить его применение, приступить по показаниям к сердечно-легочной реанимации и продуть аппарат для наркоза 100 % кислородом. Необходимы непрерывный кардиомониторинг, кислородотерапия и катетеризация вены. Если пациент не был интубирован, немедленно вводят эндотрахеальную трубку. По показаниям назначают аппаратное дыхание. Проводят анализ газового состава артериальной крови, определяют в крови уровни печеночных ферментов, витамина В12, креатинина и электролитов.
- Неадекватность испарителя. Неправильно подобранный испаритель конкретного вещества, а также последовательное, а не параллельное соединение испарителей создают риск передозировки. Она может произойти случайно при путанице с направлением поворота рукоятки дозирующего устройства ("больше—меньше") или при неадекватной замене одного оборудования другим. Работник операционной, нелегально злоупотребляющий галотаном, иногда сознательно оставляет испаритель включенным, когда в этом нет необходимости. Осведомленность о такого рода необычных причинах неадекватного действия аппаратуры позволяет снизить риск тяжелой передозировки.
- Антидоты. Антидоты для рассмотренных ингаляционных средств не известны.
- Поддерживающая терапия при отравлении ингаляционными анестетиками:
1. При бронхоспазме по показаниям назначают антагонисты b2-адренергических рецепторов (например, сальбутамол), кислород и аппаратное дыхание.
2. Припадки можно купировать внутривенным введением диазепама и фенитоина.
3. Гипоксию облегчают кислородотерапией и искусственной вентиляцией легких с положительным давлением в конце выдоха.
4. Отек легких лечат кислородотерапией, препаратами наперстянки и фуросемидом.
5. Показаны непрерывный кардиомониторинг и серийный анализ газового состава артериальной крови.
6. Средства, угнетающие центральную нервную систему или дыхание, не рекомендуются.
7. Часто бывает необходимо прервать операцию. По соглашению между анестезиологом и хирургом ее можно продолжить после замены данного анестетика на другой. При этом следует тщательно взвесить риск усиления гемодинамической стабильности у пациента, состояние которого уже ухудшилось.
8. Могут потребоваться детальные периодические оценки гематологических параметров, включая исследование костного мозга, клинический анализ крови, определение эритроцитарных индексов, уровней фолата и витамина В12 в крови.
Ретроспективное изучение женщин, работающих ассистентками стоматологов и регулярно контактирующих с высокими уровнями закиси азота, наводит на мысль об удлинении у них времени до зачатия.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Отравление местными анестетиками и его лечение
Передозировка местноанестезирующих средств возможна в результате избыточного введения внутривенного анестетика, случайной спинномозговой, внутриартериальнои или эпидуральной инъекции. К токсическим реакциям относятся сердечно-сосудистый коллапс, угнетение или остановка дыхания, припадки, аритмии и смерть.
Лечение в основном поддерживающее и симптоматическое. Метгемоглобинемию можно лечить метиленовым синим.
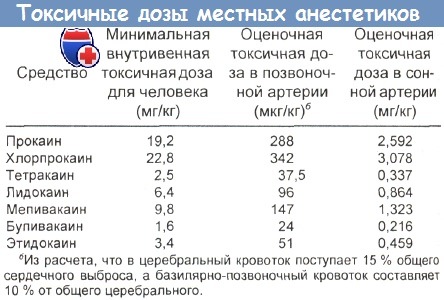
Токсичные дозы местноанестезирующих средств приведены в таблице ниже.
а) Токсикокинетика местных анестетиков:
- Беременность и роженица. При родах все чаще применяется регионарная анестезия. Возможно, роженицы составляют группу повышенного риска с точки зрения интоксикации местноанестезирующими средствами.
К физиологическим изменениям при беременности относятся увеличение сердечного выброса и объема крови, сдавление аорты и полых вен, снижение функциональной остаточной емкости легких, усиление потребления кислорода и уменьшение уровня плазменных белков. Эти факторы могут повысить объем распределения, повлиять на метаболизацию медикаментов и сократить сердечно-легочный "запас прочности" пациентки.
Венозная гиперемия повышает риск случайной внутривенной инъекции, особенно при эпидуральной анестезии. Гипогликемия и относительный плазменный дефицит холинэстеразы, наблюдаемые у беременных, могут предрасполагать к интоксикации в случае применения сложноэфирных медикаментов. Гипомагниемия беременных чревата разобщением калий-натриевого насоса.
- Плод. Местноанестезирующие средства могут понизить симпатический тонус, уменьшить кровяное давление и сердечный выброс у матери, а в результате и перфузию плаценты. Не исключено и их прямое сосудосуживающее действие на нее. Наконец, они могут проникать через плаценту и непосредственно влиять на сердечные и нервные ткани плода.
б) Механизм действия местных анестетиков. Местноанестезирующие средства обратимо блокируют генерирование и проведение импульсов в сенсорных, двигательных и вегетативных нервных волокнах. Блокада периферических нервов обычно прогрессирует в такой последовательности: расширение периферических сосудов и повышение температуры кожи, утрата болевой и температурной чувствительности, утрата проприоцепции, утрата чувствительности к давлению и прикосновению, двигательный паралич.
в) Клиника отравления местными анестетиками:
- Интоксикация местными анестетиками: обычные осложнения. Общими осложнениями при использовании многих местноанестезирующих средств являются интоксикация, неврологические расстройства, неадекватная блокада, полная спинномозговая анестезия и врачебные ошибки.
При рассмотрении проблемы токсичности местных анестетиков полезно воспользоваться мнемонической формулой АИМС: аллергия, идиосинкразия, местно, системно.
Аллергические реакции на местноанестезирующие средства редки и обычно связаны со сложноэфирными соединениями. Идиосинкразия, например вазовагальный криз или истерические реакции, нетипичны и непредсказуемы. Местные эффекты ограничены прилегающими к участку введения тканями, например нервной и мышечной. 2-Хлорпрокаин вызывает венозный тромбоз, когда используется для внутривенной регионарной анестезии.
Случайную субарахноидальную инъекцию больших количеств этого вещества связывали с адгезивным арахноидитом и синдромом конского хвоста. Состав препарата впоследствии изменили. Большинство токсических эффектов местных анестетиков — системные. Чаще всего они возникают из-за случайной внутрисосудистой инъекции медикамента.
Клиническая картина. Наблюдались околоротовое онемение, покалывание, расстройства слуха и зрения, подергивания, большие эпилептические припадки, кома и летальный исход.
- Неврологические осложнения. Стойкое неврологическое расстройство при регионарной анестезии может быть обусловлено травмой, химическим веществом, инфекцией, ишемией или сдавлением, а также быть по происхождению идиопатическим. Снизить частоту токсических реакций помогают предварительная разметка ориентиров карандашом на теле, предупреждение пациента о готовящейся инъекции, беседа с ним и использование игл малого калибра.
- Полная спинномозговая анестезия. Полная спинномозговая анестезия возможна, если большое количество местноанестезирующего средства, предназначенного для эпидурального пространства, достигнет субарахноидального пространства или при использовании избыточных количеств медикамента во время спи-нальной анестезии. Она наблюдается после ретробуль-барной, симпатической блокады и анестезии плечевого сплетения.
Клиническая картина. Быстро развиваются мышечная вялость, апноэ, потеря сознания и сосудистый коллапс.
Врачебные ошибки. К этой категории относятся передозировки, инъекции не того препарата, который нужен, и инъекции в не предназначенные для них места.

г) Системная интоксикация местными анестетиками:
- Сердечно-сосудистая система. Высокие сывороточные уровни местноанестезирующих средств могут ослабить генерирование импульсов в узловой пейсмекерной ткани, нарушить их проведение и уменьшить сократимость миокарда. Некоторые средства способны также вызывать желудочковые аритмии.
Еще большее повышение сывороточного уровня анестетиков чревато сильным расширением сосудов. Угнетение миокарда и расширение периферических сосудов могут привести к сердечно-сосудистому коллапсу.
Многие из пострадавших от таких осложнений — роженицы. Смертность высока. Сердечно-сосудистый коллапс резистентен к традиционным методам реанимации.
Бупивакаин является сильным блокатором натриевых каналов. Он вызывает удлинение интервала QRS в гораздо меньших дозах, чем лидокаин, и медленнее выводится из миокарда. Лидокаин в дозе 1 г внутривенно приводил к апноэ и асистолии.
- Периферические сосуды. Большинство местноанестезирующих средств при токсичных уровнях в сыворотке вызывает расширение сосудов, снижая системное сосудистое сопротивление и венозный возврат.
- Метгемоглобинемия. Прилокаин является производным анилина. Один из его метаболитов, ортотолуидин, способен окислять гемоглобин до метгемоглобина. К этой же химической группе относится лидокаин, также известный как индуктор метгемоглобинемии.
- Сравнительная токсичность. Самые сильные жирорастворимые долгодействующие местные анестетики (бупивакаин и этидокаин), вероятно, более кардиотоксичны, чем менее мощные средства, в частности лидокаин.
- Центральная нервная система: отрицательные эффекты после случайной внутривенной инъекции. Когда местноанестезирующие средства вводят путем внутривенного вливания, возникает довольно типичная картина прогрессирующей симптоматики со стороны центральной нервной системы. В порядке возрастания тяжести проявления интоксикации следующие.
1. Онемение языка и рта. Медикамент покидает сосуды и действует на окончания сенсорных нервов во внесосудистом пространстве.
2. Головокружение.
3. Шум в ушах.
4. Расстройства зрения. Видимые объекты кажутся колеблющимися из стороны в сторону и/или вверх и вниз.
5. Невнятная речь.
6. Мышечные подергивания.
7. Иррациональная беседа.
8. Потеря сознания.
9. Большой эпилептический припадок.
10. Кома.
11. Апноэ.
д) Лабораторные данные отравления местными анестетиками:
- Аналитические методы. Бупивикаин, хлорпрокаин, этидокаин, лидокаин, мепивакаин, прилокаин и прокаин выявляют с помощью газовой хроматографии.
- Уровни в крови:
Бупивакаин. Высокие уровни в крови могут сочетаться с головокружением, звоном в ушах, гипотензией, припадками и желудочковой тахикардией. Токсические реакции на это средство обычно не возникают, если его плазменная концентрация ниже 4 мкг/мл. Однако у женщины в возрасте 28 лет появились судороги при уровне всего 1,1 мкг/мл.
Хлорпрокаин. Через 10 мин после случайной внутривенной инъекции хлорпрокаина мужчине в возрасте 23 лет с массой тела 60 кг плазменная концентрация этого средства составила 17 мкг/мл. Отрицательных реакций не отмечено.
Мепивакаин. Плазменные концентрации мепивакаина 4,4—8,6 мкг/мл после каудального введения в перинатальный период его доз 5,5—9,4 мг/кг сочетались с состоянием тревоги, спутанностью сознания, мышечными подергиваниями, тошнотой и рвотой. Новорожденному с уровнем этого анестетика в крови до 75 мкг/мл потребовались искусственное дыхание и обменное переливание крови.
Симптомы интоксикации исчезли, когда концентрация упала примерно до 8 мкг/мл. Ее токсичный порог в крови для этого средства близок к 6,3 мкг/мл.
Прилокаин. После введения дозы прилокаина 864 мг вскрытие показало его концентрацию в крови 13 мкг/мл, в моче — 69 мкг/мл, а в печени — 49 мг/кг. Этот пациент скончался в кресле дантиста в течение 1 ч.
Прокаин. После внутривенного вливания прокаина в дозах 18— 55 мг/кг отмечались его пиковые плазменные концентрации 21 — 86 мкг/мл. Через 17 — 44 мин эти уровни упали до 1 — 13 мкг/мл. Один взрослый пациент по ошибке получил 4000 мг прокаина. У него наблюдались мидриаз, отсутствие зрачковой реакции на свет, артериальная гипертензия, синусовая тахикардия, расширение и углубление зубца S на электрокардиограмме. Уровень прокаина в крови достигал 96 мкг/мл.
Получив поддерживающее лечение, этот пациент выздоровел. Плазменные концентрации прокаина после внутримышечного введения 4,8 млн ЕД прокаинпенициллина G составляли от 3,6 до 11 мкг/мл.

е) Лечение отравления местными анестетиками:
- Стабилизация состояния. Подготовка к местной анестезии. Должно быть наготове реанимационное оборудование на случай опасных изменений вентиляции и сердечной функции. Непрерывный мониторинг неврологических и кардиологических параметров позволяет быстро выявить случайную внутривенную инъекцию местного анестетика или его повышенный уровень в крови.
При любой анестезии у рожениц рекомендуется мониторинг частоты сердечных сокращений плода. Необходимо проследить, чтобы пациент ничего не получал перед анестезией перорально: это сведет к минимуму риск аспирации, а также обеспечить подачу кислорода через маску. Если ожидается значительное расширение сосудов, следует держать под рукой сосудосуживающие средства.
Нужно проверить, достаточен ли внутрисосудистый объем для адаптации к любому снижению тонуса сосудов. Следует использовать адекватную тест-дозу и минимальные общую дозу и ее концентрацию. С пациентом в сознании нужно постоянно общаться.
- Мнемоническое правило. Для лечения интоксикации местноанестезирующими средствами удобно использовать мнемоническую формулу SAVED:
Slop injection (отмена инъекции);
Airway (дыхательные пути);
Kentilation (вентиляция);
evaluation of circulation (оценка кровообращения);
Drugs (медикаменты).
- Усиление выведения. При передозировке местноанестезирующих средств форсированный диурез, гемодиализ и гемоперфузия не рекомендуются.
- Антидоты. Антидоты для местных анестетиков не известны. Метгемоглобинемию лечат метиленовым синим.
- Поддерживающая терапия при отравлении местными анестетиками:
1. Припадки: большинство припадков, вызываемых местноанестезирующими средствами, излечивается самопроизвольно, если только не было массивной внутривенной передозировки. Поддерживают проходимость дыхательных путей.
Обеспечивают вентиляцию 100 % кислородом. Поддерживают нормальный кислотно-щелочной баланс. Ацидоз снижает связывание анестетика с белками, повышая уровень свободного агента и тем самым его токсичность. Если припадки стойкие, можно использовать тиопентал (50-100 мг), диазепам (10 мг) или мидазолам (2 мг). Если во время припадков необходимо эффективно проводить ручную вентиляцию, может потребоваться введение сукцинилхолина.
2. Гипотензия: сосудосуживающие средства (например, дофамин); инфузионная терапия; адекватное положение тела пациента.
3. Брадикардия: атропин.
4. Желудочковая тахикардия или фибрилляция: электрокардиоверсия; бретилий (5 — 10 мг/кг внутривенно) при индуцированных бупивакаином желудочковых экстрасистолах или тахикардии.
5. Гемодинамическая нестабильность: поднятие ног пациенту; левое смещение матки у роженицы; сердечная реанимация; возможно, прямой массаж сердца или АИК.
6. При полной спинномозговой анестезии требуется поддерживать вентиляцию и кровообращение.
7. При эпидермальном применении бупивакаина его надо вводить медленно, поскольку существует высокий риск случайной инъекции анестетика в вену. Наготове должны быть оборудование, медикаменты и персонал для реанимации.
8. Одному пациенту с индуцированной бупивакаином остановкой сердца помог АИК.
9. Экстракорпоральный насос, экспериментальный метод, опробованный на собаках, возможно, будет полезен при передозировках лидокаина.
10. Предсердно-желудочковая кардиостимуляция оказалась успешной при лечении остановки сердца после случайного введения 2000 мг лидокаина в АИК. Эту процедуру проводили после безрезультатного применения хлорида кальция и изопреналина.
11. Лидокаин: острую лидокаиновую интоксикацию лучше всего лечить неспецифической поддерживающей терапией.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Категории МКБ: Аллергическая крапивница (L50.0), Анафилактический шок, обусловленный патологической реакцией на адекватно назначенное и правильно примененное лекарственное средство (T88.6), Анафилактический шок, связанный с введением сыворотки (T80.5), Ангионевротический отек (T78.3), Генерализованное высыпание на коже, вызванное лекарственными средствами и медикаментами (L27.0), Другая эритема многоформная (L51.8), Лекарственная фотоаллергическая реакция (L56.1), Локализованное высыпание на коже, вызванное лекарственными средствами и медикаментами (L27.1), Небуллезная эритема многоформная (L51.0), Патологическая реакция на лекарственное средство или медикаменты неуточненная (T88.7), Раздражительный контактный дерматит, вызванный лекарственными средствами при их контакте с кожей (L24.4), Токсический эпидермальный некролиз [Лайелла] (L51.2)
Общая информация
Краткое описание
УТВЕРЖДЕНО
Постановление
Министерства здравоохранения
Республики Беларусь
01.06.2 017 № 50
1. Настоящий Клинический протокол устанавливает общие требования к оказанию медицинской помощи пациентам при диагностике и лечении системной токсичности при использовании местных анестетиков для регионарной анестезии при обезболивании родов, при операциях на органах грудной клетки, органах брюшной полости, конечностях и предназначен для врачей-анестезиологов-реаниматологов.
2. Требования настоящего Клинического протокола являются обязательными для юридических лиц и индивидуальных предпринимателей, осуществляющих медицинскую деятельность в порядке, установленном законодательством Республики Беларусь.
4. Показания к лечению:
возникновение реакций системной токсичности местных анестетиков при их использовании при проведении регионарных методов обезболивания.
5. Факторы, повышающие частоту развития реакций системной токсичности местных анестетиков:
беременность;
возраст старше 60 лет;
сердечная недостаточность;
ишемическая болезнь сердца;
заболевания печени;
метаболический или дыхательный ацидоз;
использование жирорастворимых местных анестетиков амидного ряда;
превышение дозы местного анестетика.
6. Рабочее место врача-анестезиолога-реаниматолога, где проводится регионарная анестезия для обезболивания хирургических операций, родов, дополнительно должно быть оснащено укладкой для лечения нарушений ритма, возникающих при системной токсичности местных анестетиков (приложение 2 настоящего Клинического протокола).
Диагностика
7. Диагностика системной токсичности местных анестетиков проводится на основании[1]:
анамнеза (наличие временной связи между введением местного анестетика и развитием симптомов);
жалоб (онемение губ, онемение кожи вокруг рта, парестезии языка, шум в ушах, головокружение, неясность зрения, металлический привкус во рту);
данных физикального обследования (беспокойство, спутанная речь, мышечные подергивания, судороги, нарушение сознания, остановка дыхания);
нарушений со стороны сердечно-сосудистой системы – прогрессирующая гипотензия (систолическое артериальное давление менее 80 мм рт. ст., среднее артериальное давление менее 50 мм рт. ст.), нарушения проводимости (атриовентрикулярная блокада, брадикардия, асистолия), желудочковые аритмии (частая желудочковая экстрасистолия, желудочковая тахикардия, фибрилляция желудочков).
______________________________
1 Необходимо провести дифференциальную диагностику с анафилаксией.
Лечение
8. Лечение при развитии системной токсичности:
прекратить введение местного анестетика;
при сохранении самостоятельного дыхания наладить ингаляцию увлажненного кислорода;
при остановке дыхания обеспечение проходимости дыхательных путей, вентиляция 100 % кислородом;
при проведении искусственной вентиляции легких перейти на вентиляцию 100 % кислородом;
при наличии судорог[2]: введение лекарственных средств: диазепам по 2,5–10 мг в/в или мидазолам по 2,5–5 мг в/в или тиопентал натрия 1–2 мг/кг до достижения эффекта.
______________________________
2 Нельзя использовать пропофол для купирования судорог.
8.1. При неэффективном кровообращении:
проведение сердечно-легочной реанимации согласно протоколам диагностики, анестезии, реанимации и интенсивной терапии критических состояний в стационарных условиях (приложение 1 к приказу Министерства здравоохранения Республики Беларусь от 12.08.2004 № 200);
проведение терапии жировой эмульсией (см. пункт 8.2).
Сердечно-легочная реанимация может проводиться более 30 минут.
8.2. Лечение нарушений ритма:
Основу лечения нарушений ритма составляет введение жировой эмульсии:
ввести внутривенно жировую эмульсию 20 % в дозе 1,5 мл/кг в течение 1 минуты в виде болюсного введения, одновременно начать инфузию жировой эмульсии со скоростью 0,25 мл/кг/мин;
если через 5 минут от начала инфузии эмульсии не восстановилось самостоятельное кровообращение повторить болюсное введение жировой эмульсии в дозе 1,5 мл/кг;
если после трех болюсов жировой эмульсии по 1,5 мл/кг с интервалом в 5 минут не восстановилось самостоятельное кровообращение увеличить скорость инфузии жировой эмульсии до 0,5 мл/кг/мин;
при восстановлении самостоятельного кровообращения инфузию жировой эмульсии продолжить еще минимум 10 мин.
Максимальная доза жировой эмульсии – 10 мл/кг за первые 30 минут.
Алгоритм терапии нарушений ритма жировой эмульсией представлен в приложении 1 настоящего Клинического протокола.
Для лечения нарушений ритма противопоказано использование бета-блокаторов, блокаторов кальциевых каналов, местных анестетиков (лидокаин, прокаинамид), вазопрессина.
9. Пациенты, у которых системное токсическое действие местных анестетиков проявилось в виде нарушений ритма и/или остановки кровообращения, должны быть госпитализированы в отделение интенсивной терапии и реанимации с обязательным проведением непрерывного мониторинга ЭКГ в течение не менее 12 часов.
Алгоритм терапии нарушений ритма, возникающих при системной токсичности местных анестетиков
(Липидное спасение)

Рекомендуемые максимальные дозировки 20 % жировой эмульсии – 10 мл/кг в течение первых 30 мин.
Состав укладки для лечения нарушений ритма, возникающих при системной токсичности местных анестетиков
1. Жировая эмульсия 20 % 500 мл – 1 флакон.
2. Система инфузионно-трансфузионная – 1 шт.
3. Шприц 20 мл – 2 шт.
4. Периферический венозный катетер размером 18G или 20G – 2 шт.
Читайте также:

