Поражение цнс при инфекционных заболеваниях у детей
Обновлено: 24.04.2024
Инфекции центральной нервной системы у детей. Бактериальный менингит - причины
Острые инфекции с поражением ЦНС — наиболее распространенная причина лихорадки с симптомами поражения ЦНС у детей. Практически любой микроорганизм может вызвать инфекционный процесс, специфичность патогенного организма зависит от особенностей его эпидемиологии, а также от возраста и иммунного статуса больного. В целом вирусные инфекции ЦНС встречаются чаще, чем бактериальные, которые в свою очередь более распространены, чем грибковые и паразитарные. Риккетсиозы (например, пятнистая лихорадка Скалистых гор и Ehrlichia) встречаются относительно редко, однако играют важную роль при определенных эпидемиологических обстоятельствах.
Mycoplasma spp. также может вызывать инфекционное поражение ЦНС, однако точный вклад этого возбудителя трудно оценить. Независимо от этиологии заболевания у большинства пациентов с острыми нейроинфекциями клиническая картина сходная. К распространенным симптомам относится головная боль, тошнота, рвота, анорексия, беспокойство и раздражительность; большинство из них неспецифические. Характерные признаки нейроинфекции, кроме лихорадки, включают фотофобию, боль в шее и ригидность затылочных мышц, заторможенность, ступор, кому, судорожные приступы и очаговые неврологические нарушения. Тяжесть и полиморфизм клинических проявлений зависят от специфического патогенного микроорганизма, состояния макроорганизма и локализации поражения в ЦНС. Поражение при нейроинфекциях может быть диффузным или локальным.
Примером диффузного инфекционного поражения служит менингит и энцефалит. При менингите наблюдается первичное поражение менингеальных оболочек, при энцефалите — паренхимы мозга. Поскольку эти анатомические границы часто не разделимы, у многих пациентов сочетаются симптомы поражения менингеальных оболочек и паренхимы мозга; диагностируется менингоэнцефалит. Абсцесс мозга — пример фокального инфекционного поражения ЦНС. Неврологические нарушения при абсцессе мозга определяются его локализацией и распространением. Диагноз диффузной нейроинфекции ставится на основании исследования СМЖ, полученной при ЛП.
Бактериальный менингит — одно из наиболее потенциально опасных заболеваний у детей грудного и более старшего возраста. Это заболевание ассоциируется с высокой частотой осложнений в остром периоде, а также с высоким риском отдаленных неблагоприятных последствий. Этиология и лечение бактериального менингита значительно отличаются в неонатальном периоде (0-28 дней) и у детей более старшего возраста. Тем не менее в неонатальном и постнатальном периодах менингит могут вызывать одни и те же возбудители, особенно у пациентов первых 2 мес. жизни, в том числе Streptococcus группы В, Streptococcus pneumoniae (пневмококк), Neisseria meningitidis (менингококк) и Haemophilus influenzae типа b.
Менингит встречается достаточно часто у младенцев с лихорадочными заболеваниями, его необходимо исключать у пациентов с изменением психического статуса или другими неврологическими нарушениями.

У детей первых 2 мес. жизни с нормальным иммунитетом возбудители менингита зависят от характера материнской флоры и от микроорганизмов, преобладающих в окружающей среде. Наиболее часто в этой возрастной группе менингит вызывают стрептококки группы В и D, грамотрицательные бактерии кишечной группы и hysteria monocytogenes. Кроме того, у детей этого возраста менингит может быть вызван Н. influenzae (типа b и некапсулированными штаммами) и другими патогенными микроорганизмами, которые чаще обнаруживаются у пациентов более старшего возраста.
Бактериальный менингит у детей в возрасте от 2 мес. до 12 лет чаще всего вызывают Streptococcus pneumoniae, Neisseria meningitidis или Haemophilus influenzae типа b. До начала широкого применения вакцины против Haemophilus influenzae типа b практически в 70 % случаев возбудителем бактериального менингита у детей до 5 лет служила Haemophilus influenzae типа b. После введения всеобщей иммунизации против этой бактерии, начиная с 2-месячного возраста, частота этого менингита резко снизилась. Средний возраст дебюта бактериального менингита в США увеличился с 15 мес. в 1986 г. до 25 лет в 1995 г. В настоящее время менингит чаще всего вызывают Streptococcus pneumoniae и Neisseria meningitidis. Однако после того, как в 2000 г. конъюгированная пневмококковая вакцина была разрешена к применению и рекомендована для всеобщей иммунизации начиная с 2-месячного возраста, частота менингита, вызванного этим возбудителем, стала снижаться.
Изменение восприимчивости макроорганизма вследствие анатомических дефектов или иммунодефицита повышает риск менингита, вызванного менее распространенными возбудителями, такими как Pseudomonas aeruginosa, Staphylococcus aureus, коагулазанегативные стафилококки, Salmonella spp., L. monocytogenes.
Основной фактор риска менингита — несформированный иммунитет к специфическому патогенному микроорганизму у детей младшего возраста. Дополнительные факторы риска включают недавнюю колонизацию патогенными бактериями, близкий контакт (например, в семье, детском саду, военных казармах) с людьми с инфекционным процессом, вызванным Haemophilus influenzae типа b и Neisseria meningitidis, большую скученность людей, бедность, негроидную расу и мужской пол. Возбудитель передается, вероятно, при контакте с человеком, служащим источником инфекции, воздушно-капельным путем. Риск менингита повышается у младенцев и детей младшего возраста со скрытой бактериемией, что более выражено в случае менингококковой инфекции (в 85 раз) и Haemophilus influenzae типа b (в 12 раз), чем при пневмококковой инфекции.
Специфическое снижение резистентности к инфекции при внедрении в организм инкапсулированных форм вследствие изменения выработки иммуноглобулинов может служить причиной повышения риска бактериального менингита у уроженцев Америки и эскимосов, в то время как дефекты системы комплемента (С5-С8) ассоциируются с рецидивирующей менингококковой инфекцией, а дефекты пропердиновой системы сочетаются с высоким риском заболеваний, вызванных менингококком, с летальным исходом. Нарушение функции селезенки (серповидноклеточная анемия) или аспления (вследствие травмы, порока развития, при лимфогранулематозе) ассоциируется с повышенным риском сепсиса или менингита, вызванного пневмококком, Haemophilus influenzae типа b (в некоторой степени) и, редко, менингококком. Дефекты системы Т-лимфоцитов (врожденные или приобретенные на фоне химиотерапии, СПИДа или злокачественных новообразований) ассоциируются с повышенным риском инфекционных поражений ЦНС, вызванных L. monocytogenes.
Врожденные или приобретенные дефекты, вызывающие истечение СМЖ, такие как дефекты черепа или лицевого скелета, расположенные по срединной линии (решетчатая пластинка), поражение среднего уха (место прикрепления стремянной кости), фистулы внутреннего уха (овальное окно, внутренний слуховой проход, водопровод улитки), истечение СМЖ через разрыв менингеальных оболочек (вследствие перелома структур основания черепа) в решетчатую пластинку или околоносовые пазухи ассоциируются с повышенным риском пневмококкового менингита. Дермальный синус или менингомиелоцеле в пояснично-крестцовой области связано с бактериальным менингитом, вызванным стафилококком или грамотрицательными бактериями кишечной группы. Инфицирование шунта (после оперативного лечения гидроцефалии) повышает риск менингита, вызванного стафилококками (особенно коагулазанегативными) и другими бактериями, распространенными на кожных покровах.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Медленные инфекции ЦНС — поражения центральной нервной системы вирусными вирионами или инфекционными прионами, возникающие после длительного скрытого (инкубационного) периода. Клинически характеризуются парезами, гиперкинезами, расстройством мозжечковых функций, психическими нарушениями, когнитивным снижением до глубокой деменции. Диагностика осуществляется при помощи неврологического обследования, церебральной томографии, анализа спинномозговой жидкости, определения антивирусных антител в крови. Лечение проводится симптоматическими средствами.
Общие сведения
Понятие медленные инфекции ЦНС включает целый ряд неврологических болезней, обусловленных вирионами (вирусными частицами) и прионами (вирусоподобными белками). Первые данные были опубликованы в 1954 году в Исландии учёным, длительно наблюдавшем неописанные ранее заболевания овец, поражающие ЦНС. Автор дал им название медленные инфекции. В 1957 году появилось описание нового заболевания — куру, распространённого среди жителей Новой Гвинеи. Болезнь полностью соответствовала критериям медленных инфекций и открыла список подобных патологий у человека, который продолжает пополняться. Медленные инфекции ЦНС — редко встречающаяся группа нозологий, точные данные о заболеваемости не собраны. Одни формы распространены повсеместно, другие имеют эндемичный характер.

Причины медленных инфекций ЦНС
Изучение свойств возбудителей позволило установить вирусный характер инфекций. Ранее ошибочно предполагалось, что возбудителями выступают специфические вирусные агенты. В последующем удалось определить два этиологических фактора возникновения патологии: вирусы и прионы.
- Вирусы. В настоящее время опровергнута теория специфической этиологии, подтверждена роль обычных вирусов: полиомавируса, флавивируса, цитомегаловируса, вирусов кори, краснухи, простого герпеса. Медленные инфекционные процессы в ЦНС развиваются вследствие персистирования вируса в организме на протяжении многих лет после перенесённого в типичной форме заболевания. Заражение может происходить воздушно-капельным, алиментарным, парентеральным, трансплацентарным путём.
- Прионы. Являются белками, обладающими некоторыми свойствами вирусов, в отличие от последних не имеют ДНК или РНК. Инфекционные прионы вызывают развитие болезни путём трансформации аналогичных нормальных белков нервных клеток в патологические. Инфицирование происходит при употреблении в пищу недостаточно термически обработанного мяса заражённых животных, трансплантации содержащих патогенные прионы тканей, гемотрансфузиях, нейрохирургических вмешательствах.
Доподлинно неизвестно, что становится причиной многолетнего персистирования вирусов, которые остаются в организме переболевших обычной инфекцией пациентов. Возможными причинами считают дефектное строение вирионов, недостаточность иммунной системы, сопровождающуюся пониженной выработкой антител, активацию пролиферативных процессов внутри поражённых вирусами клеток.
Патогенез
Общей патогенетической характеристикой, объединяющей различные медленные инфекции, выступает длительное скрытое развитие патологии, сопровождающееся накоплением возбудителя в церебральных тканях. После перенесённого вирусного заболевания (чаще внутриутробно или в раннем детстве) возбудители остаются в клетках головного мозга в неактивной форме. Причины и механизмы их активации не установлены. Перейдя в активную фазу, возбудители вызывают постепенное развитие воспалительных изменений в ЦНС.
Попавший в клетку прион взаимодействует с находящимся внутри неё геном, что приводит к синтезу аналогичных прионов вместо нормальных клеточных белков. Продолжительный скрытый период обусловлен временем, требующимся для попадания прионов в головной мозг, длительным процессом внутриклеточного накопления синтезируемых патологических белков. Результатом аномального белкового синтеза являются метаболические изменения, приводящие к гибели нейрона.
Морфологическая картина медленных инфекций достаточно вариабельна. Наиболее часто в тканях ЦНС наблюдается формирование очагов глиоза, демиелинизирующихся участков. При истинно вирусной этиологии процесса типично образование периваскулярных лимфоцитарных инфильтратов, фокусов астроцитоза. Морфологические изменения захватывают различные области мозга, часто носят распространённый характер.
Классификация
Медленные инфекции ЦНС имеют различную клиническую картину, однако отмечаются отдельные особенности течения болезней, связанные с их вирусным или прионным генезом. С учетом этого обстоятельства в неврологии заболевания подразделяются по этиологическому принципу на:
- Вирионные — вызванные типичными вирусами. Сопровождаются выработкой специфичных противовирусных антител. Наиболее распространены подострый склерозирующий панэнцефалит, прогрессирующая мультифокальная лейкоэнцефалопатия, краснушный панэнцефалит.
- Прионные — вызванные белками-прионами. Близкое сходство инфекционных прионов с внутриклеточными белками организма обуславливает практически полное отсутствие иммунного ответа при их внедрении. Большинство случаев составляет болезнь Крейтцфельдта-Якоба. К прионным инфекциям относятся также фатальная семейная инсомния, куру, синдром Герстмана.
Симптомы медленных инфекций ЦНС
Общей чертой заболеваний этой группы является медленное незаметное начало без температурной реакции. Характерен продромальный период, в котором отмечается раздражительность, эмоциональная неуравновешенность, рассеянность больного, лёгкие расстройства координации, шаткость во время ходьбы. Период клинической манифестации отличается постепенным нарастанием симптоматики, длящимся 1-3 недели. Типичны экстрапирамидные и пирамидные нарушения, атаксия, психические расстройства, когнитивное снижение.
Экстрапирамидные симптомы включают гиперкинезы (атетоз, тремор, дистонические синдромы), иногда — брадикинезию, паркинсоническую скованность. Пирамидные двигательные расстройства протекают в виде прогрессирующих геми- и тетрапарезов. Возможно поражение черепных нервов, проявляющееся парезом лицевой мускулатуры, тугоухостью, нарушением зрения, затруднением глотания и пр. Психические отклонения характеризуются эпизодами эйфории, фобий, бреда, спутанного сознания, отрывочных галлюцинаций. Все медленные инфекции сопровождаются постепенным распадом интеллектуальных функций (памяти, мышления, внимания) с исходом в глубокую деменцию. Нарушения речи обусловлены одновременно сенсомоторной афазией и когнитивным дефицитом. В терминальной стадии наблюдается мутизм — речь отсутствует полностью.
Симптоматика каждой отдельной инфекции имеет свои особенности. Для болезни Крейтцфельдта-Якоба, краснушного панэнцефалита характерна мозжечковая атаксия. Отличительным клиническим проявлением фатальной бессонницы выступает инсомния, доводящая пациентов до психического и физического истощения. Базовым симптомом болезни куру является тремор, типична насильственная улыбка. Синдром Герстмана-Штраусслера-Шейнкера протекает с мышечной гипотонией и угнетением сухожильных рефлексов.
Диагностика
Поскольку медленные инфекции — редкие заболевания, диагностировать их непросто. Неспецифическая клиническая симптоматика, трудности выделения вируса-возбудителя, инфекционного приона осложняют диагностику. Диагностический поиск осуществляется в рамках следующих исследований:
- Сбор анамнеза. Большое значение имеет расспрос относительно перенесённых в прошлом (возможно внутриутробно) инфекций, операций с пересадкой тканей. Опрос включает выявление продромальных симптомов, особенностей дебюта патологических проявлений.
- Оценка неврологического статуса.Неврологи исследует двигательную, чувствительную, рефлекторную, когнитивную сферы, координацию. На основании полученных данных формируется картина многоочагового поражения, свидетельствующая о диффузном характере патологических изменений церебральных тканей.
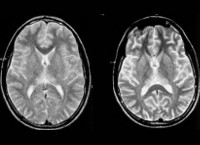
- Нейровизуализация. Проводится при помощи МРТ, КТ, МСКТ головного мозга. Томография определяет мультифокальное поражение мозга в виде демиелинизации, дегенерации, атрофии. Наблюдается расширение желудочков, говорящее о наличии гидроцефалии.
- Исследование цереброспинальной жидкости. Материал получают при люмбальной пункции. Отсутствие воспалительных изменений спинномозговой жидкости позволяет исключить типичные нейроинфекции. Проводятся ПЦР-исследования, направленные на выявление ДНК вероятных возбудителей, анализ на наличие противовирусных антител. В случае вирионного генеза инфекции эти методики дают возможность верифицировать возбудителя у 70-90% больных.
- Анализ крови на антитела. Информативен в случае вирусной этиологии. Осуществляется с определением противокоревых, противокраснушных антител. Диагностически значимы повторные исследования, демонстрирующие нарастание титра в период активации вируса.
- Биопсия мозга. Выполняется при крайней необходимости. Исследование биоптатов позволяет выявить интранейрональные скопления прионов. Однако в ходе биопсии существует вероятность забора участка неизменённых тканей.
При наличии показаний проводятся консультации смежных специалистов: офтальмолога, психиатра, инфекциониста, генетика. Необходима дифференциальная диагностика с энцефалитами, имеющими подострое начало, сосудистой деменцией, хроническими энцефалопатиями, болезнью Альцгеймера.
Лечение медленных инфекций ЦНС
Эффективная терапия не разработана. Предложенные схемы лечения противовирусными фармпрепаратами оказались безрезультатными. Назначается симптоматическая терапия, которая позволяет облегчить состояние пациентов, но не может замедлить прогрессирование патологического процесса. Она включает противоотёчные, нейропротекторные, витаминные, психотропные, противосудорожные средства. Поиск эффективных способов лечения продолжается.
Прогноз и профилактика
Медленные инфекции ЦНС остаются смертельными заболеваниями. Гибель пациентов вследствие тотального поражения мозга происходит в среднем в течение 1-2 лет от момента развития клинических симптомов. Наибольшая продолжительность жизни наблюдается у больных синдромом Герстмана — 3-5 лет. Профилактические мероприятия сводятся к предупреждению распространения вирусных инфекций, поддержанию должного уровня иммунитета. В отношении кори и краснухи возможна специфическая профилактика, которая проводится путём обязательной вакцинации детей соответствующими вакцинами. Способы предупреждения прионных заболеваний не найдены, поскольку отсутствуют методики определения прионов в трансплантируемых тканях, препаратах крови.
Нейроинфекции – группа инфекционных патологий, которые вызываются бактериями, вирусами, грибками или простейшими, характеризуются преимущественной локализацией возбудителя в ЦНС и признаками поражения ее отделов. Клинические проявления представлены менингеальным, интоксикационным, ликвородинамическим синдромами, вегетососудистыми расстройствами. В процессе диагностики используются анамнестические данные, результаты физикального, общеклинического лабораторного, серологического, бактериологического или вирусологического исследования. В ходе лечения назначаются антибиотики или противовирусные препараты, патогенетические и симптоматические средства.
МКБ-10
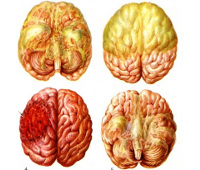
Общие сведения
Нейроинфекции – сравнительно распространенная группа патологий. По данным статистики, инфекционные поражения ЦНС достигают 40% в структуре неврологической заболеваемости. Основную часть составляют бактериальные и вирусные менингиты, распространенность которых в различных географических регионах находится в пределах 5-12 случаев на 100 000 населения в год. Для большинства болезней, входящих в данную группу, характерна осенне-зимняя сезонность. Они могут встречаться среди всех возрастных категорий населения, но основную часть пациентов составляют дети до 10-12 лет и лица, не получившие вакцины согласно календарю прививок.

Причины нейроинфекций
Этиология инфекционного поражения структур центральной нервной системы зависит от вида заболевания. В большинстве эпизодов источником заражения становится больной или здоровый человек-носитель. Способствующими факторами являются постоянный контакт с большим количеством людей, ЧМТ, иммунодефицитные состояния, хронические соматические патологии, беспорядочная половая жизнь. Выделяют следующие механизмы инфицирования:
- Воздушно-капельный. Реализуется при кашле, чихании, разговоре. Характерен для возбудителей бактериальных и вирусных менингитов, энцефалитов, полиомиелита, герпетической инфекции.
- Контактно-бытовой. Подразумевает передачу инфекционного агента при прямом контакте с больным, носителем или инфицированными предметами быта. Это один из путей распространения герпес-вирусов, полиомиелита, сифилиса.
- Фекально-оральный. Тип передачи, при котором возбудитель выделяется вместе с испражнениями, проникает в организм с продуктами питаниями или водой. Может реализовываться при герпес-инфекции, вирусах ЕСНО и Коксаки, ботулизме, полиомиелите.
- Половой. При этом варианте заражение происходит во время полового акта через слизистые оболочки половых путей. Таким способом распространяется ВИЧ-инфекция, сифилис, реже – вирусы-возбудители менингитов, энцефалитов.
Патогенез
Для каждой формы нейроинфекции характерны свои патогенетические особенности, но механизмы развития большинства синдромов и симптомов, как правило, аналогичны при всех вариантах этой группы заболеваний. Инфекционный синдром обуславливают комплексы антиген-антитело и токсины возбудителей, которые оказывают деструктивное воздействие на ЦНС, провоцируя нарушения тонуса сосудов, метаболизма и гемодинамики в целом. Менингеальный синдром развивается при воспалительном поражении мозговых оболочек и повышении внутричерепного давления. Вегетативные расстройства вызываются как прямым контактом инфекционных агентов с центрами автономной нервной системы, так и опосредованным воздействием через внутричерепную гипертензию. Ликвородинамические изменения потенцируются усиленной продукцией спинномозговой жидкости на фоне раздражения сосудистых сплетений и блокадой пахионовых грануляций, усложняющей процесс ее резорбции.
Классификация
Использование систематизации обусловлено необходимостью объединить между собой большое количество разнородных инфекционных патологий с вовлечением нервной системы. В зависимости от характера морфологических изменений, клинических особенностей и конкретного возбудителя в неврологии различают несколько групп поражений ЦНС инфекционного происхождения. Основными вариантами нейроинфекций являются:
1. Энцефалиты. Заболевания с воспалением ткани головного мозга. Наиболее распространенными считаются клещевой, герпетический, ветряночный и краснушный энцефалиты. Проявления зависят от типа возбудителя, могут включать общемозговые, очаговые симптомы, системную интоксикацию разной степени выраженности.
2. Менингиты. Болезни, при которых наблюдается поражение мозговых оболочек. Характеризуются наличием менингеального и интоксикационного синдромов, с учетом особенностей воспалительного процесса подразделяются на:
- Гнойные. Провоцируются бактериями, простейшими или грибами, могут быть первичными либо вторичными. К первичным относятся менингиты, вызванные менингококком, пневмококками, гемофильной палочкой. Вторичные поражения являются осложнением гнойных процессов других локализаций – околоносовых пазух, среднего уха и пр.
- Серозные. Сопровождаются преимущественно лимфоцитарным плеоцитозом. В роли возбудителей выступают туберкулёзная палочка, вирус паротита, энтеровирусы Коксаки и ЕСНО.
3. Полиомиелит. Поражение ЦНС, вызванное РНК-содержащим вирусом полиомиелита. Может протекать в двух формах: непаралитической (менингеальной, абортивной, инаппарантной) и паралитической (спинальной, мостовой, бульбарной, энцефалитической).
4. Абсцесс головного мозга. Представляет собой ограниченное капсулой скопление гнойных масс в тканях мозга. Может иметь отогенное, риногенное, метастатическое или посттравматическое происхождение. Проявляется системной интоксикацией, очаговой неврологической симптоматикой, реже – эпилептическим и гипертензивным синдромами.
5. Опоясывающий лишай. Вариант хронической нейроинфекции, обусловленный герпесвирусом человека III типа – Варицелла-Зостер. Наблюдается персистенция возбудителя в спинномозговых ганглиях с активацией при снижении иммунитета или травмах. К основным симптомам относятся острая боль, герпетические высыпания в области 1-2 дерматомов.
6. Нейросифилис. Инфекционная патология, провоцируемая бледной трепонемой. На ранней стадии поражения ЦНС отмечаются общеинфекционные, общемозговые и очаговые симптомы с нарушением функций II, III, VI, VIII пар черепно-мозговых нервов. На поздних стадиях развивается прогрессирующая деменция, выявляются психические расстройства, инсультоподобная симптоматика.
7. Ботулизм. Инфекционное заболевание, вызываемое Clostridium botulinum и сопровождающееся прерыванием передачи нервных импульсов в холинэргических синапсах. Обнаруживаются признаки поражения двигательных ядер ствола мозга, передних рогов.
8. НейроСПИД. Обусловлено инфицированием вирусом иммунодефицита человека. Зачастую представлено первичными поражениями ЦНС: энцефалопатиями, рецидивирующими ВИЧ-менингитами, вакуолярной миелопатией. Проявления разнообразны, включают парезы, афазии, атаксию, мнестические расстройства, психопатологические нарушения.
Симптомы нейроинфекций
Менингальный синдром возникает при вовлечении в патологический процесс мозговых оболочек, состоит из общемозговой симптоматики, мышечно-тонических и корешковых симптомов. В первую группу входит интенсивная диффузная распирающая головная боль; фотофобия, повышенная чувствительность к звукам и свету, рвота без тошноты, не приносящая облегчения. Зачастую наблюдается нарушение сознания по типу галлюцинаций, бреда, оглушения, сопора. У детей возможны фебрильные судороги. Мышечно-тонические и радикулярные проявления включают в себя ригидность затылочных мышц, симптомы Кернига, Брудзинского, Лессажа, Гордона, Менделя, Бехтерева и др.
Вегетативно-сосудистые расстройства при нейроинфекциях могут носить симпатоадреналовый, вагоинсулярный или смешанный характер. В первом случае обнаруживается учащение сердечного ритма, повышение артериального давления, чрезмерная потливость и жажда, во втором – брадикардия, артериальная гипотония, обильное мочеиспускание. При смешанном варианте симптомы из разных групп сочетаются между собой. Нарушение нормальной циркуляции ликвора может протекать по гипертензивному и гипотензивному типу. Более характерной для нейроинфекций является внутричерепная гипертензия, сопровождающаяся угнетением сознания, судорожными и дислокационными синдромами.
Диагностика
Диагностическая программа при инфекциях ЦНС основывается на анамнезе, физикальном исследовании, общеклинических и специфических лабораторных тестах. Лучевые методы диагностики используются редко, зачастую – с целью дифференциации с объемными поражениями нервной системы. Программа обследования больного может включать следующие процедуры:
- Выяснение анамнеза. При общении с пациентом или его родственниками лечащий инфекционист или невролог осуществляет детализацию имеющихся жалоб, выясняет динамику их развития. Важную роль играет эпидемиологический анамнез – контакт с инфекционными больными или выезд за границу на протяжении последних 21 дней.
- Общий и неврологический статус. При осмотре врач определяет уровень сознания, изучает кожу и слизистые оболочки с целью поиска высыпаний, определяет частоту сердечных сокращений и артериальное давление. При установлении неврологического статуса специалист оценивает тонус затылочных мышц, выявляет специфические симптомы, характерные для различных неврологических синдромов.
- Общеклинические лабораторные тесты. В общем анализе крови помимо повышения СОЭ отмечаются следующие изменения: при бактериальной инфекции – высокий нейтрофильный лейкоцитоз, при вирусной – лейкоцитоз со смещением лейкоцитарной формулы вправо, при ВИЧ-инфекции и тяжелых иммунодефицитах – лейкопения. Показатели биохимического анализа крови зависят от сопутствующих поражений внутренних органов.
- Спинномозговая пункция. При нейроинфекциях существует два основных варианта изменений ликвора (белково-клеточных диссоциаций) – по гнойному и серозному типу. При первом типе СПЖ мутная, имеет определенный окрас (белый, желтоватый), наблюдается нейтрофильный плеоцитоз от 1 000, повышение уровня белка от 1,0 г/л. При серозной форме ликвор прозрачный, опалесцирует, при цитологическом исследовании обнаруживается лимфоцитарный плеоцитоз более 100, уровень белка составляет выше 0,4 г/л.
- Серологическое исследование. Заключается в определении повышенного уровня антител в крови при помощи реакций подавления гемагглютинации, связывания комплемента или нейтрализации. Применяется ИФА, в ходе которого выявляется специфический IgM к возбудителю. Проводится ПЦР для уточнения ДНК или РНК инфекционного агента.
- Вирусологическая или бактериологическая диагностика. Предполагает определение возбудителя заболевания в крови или спинномозговой жидкости пациента путем посева образцов на специфические питательные среды. После идентификации патогенного агента целесообразно уточнение чувствительности к основным антибактериальным препаратам.
Лечение нейроинфекций
Все нейроинфекции являются показанием к госпитализации больного в инфекционный или неврологический стационар. При тяжелом состоянии, необходимости непрерывного контроля жизненно важных функций (дыхание, сердцебиение), пациента транспортируют в отделение ОРИТ. Лечебная программа включает следующие мероприятия:
- Этиотропная терапия. Основной целью является элиминация возбудителя из организма больного. Вначале используются препараты широкого спектра действия. После получения результатов серологического и бактериологического исследований медикаменты заменяют антибактериальными или противовирусными средствами, к которым выявленный возбудитель проявил наибольшую чувствительность.
- Патогенетические препараты. Применяются для борьбы с системной интоксикацией, отеком головного мозга и нарушениями гомеостаза, для коррекции водно-электролитного баланса, десенсибилизации и стимуляции иммунитета. Назначаются плазмозаменители, диуретики, глюкокортикостероиды, антигистаминные средства, интерфероны, донорские и искусственные иммуноглобулины, антикоагулянты.
- Симптоматические средства. К этой категории относятся медикаменты, купирующие отдельные симптомы и улучшающие общее состояние больного: анальгетики, жаропонижающие, противорвотные медикаменты, антиконвульсанты, нейролептики.
- Хирургическое лечение. Характер оперативного вмешательства зависит от обнаруженных изменений. Операция может потребоваться в случае абсцесса, туберкуломы головного мозга, компрессии спинного мозга при туберкулезном спондилите, больших областях некроза при опоясывающем лишае.
Прогноз и профилактика
Исход нейроинфекции определяется типом заболевания, общим состоянием больного, своевременностью и полноценностью лечения. В большинстве случаев вовремя поставленный диагноз и адекватная терапия позволяют сохранить жизнь пациента, минимизировать риск развития осложнений. При некоторых формах нейроинфекций, например – энцефалитах, летальность достигает 50-80%. Специфическая профилактика представлена вакцинами против конкретных возбудителей: вирусов герпеса, ботулизма, клещевого энцефалита, кори, полиомиелита, менингококка и т. д. Неспецифические превентивные мероприятия направлены на укрепление иммунитета, своевременное лечение иммунодефицитных состояний и предотвращение контакта с потенциальными носителями инфекционных заболеваний.
1. Инфекционные поражения головного мозга: учебное пособие/ Гладкий П.А., Сергеева И.Г., Тулупов А.А. – 2015.
Особенности вирусной инфекции нервной системы у детей в зависимости от возбудителя
а) Паралитический полиомиелит. С широким распространением вакцинации случаи полиомиелита стали крайне редкими, и повсеместное уничтожение вируса остается приоритетной задачей ВОЗ. Около 90-95% инфекций полиовируса являются субклиническими, 5% проявляются в виде легкой формы заболевания с фебрилитетом и 1-2% в основном дают симптоматику поражения ЦНС либо менингоэнцефалита, либо полиомиелита.
При полиомиелите в патологический процесс вовлекаются клетки передних рогов, двигательные и чувствительные черепные ядра продолговатого мозга, ретикулярная формация, червь мозжечка и в меньшей степени, таламус и III и V слои моторной зоны коры. Нейроны подвергаются дегенеративным изменениям, сопровождающимся вначале полиморфноядерной реакцией, которая позднее становится мононуклеарной.
Клинические проявления возникают после инкубационного периода, который длится 3-35 дней. Первоначальные симптомы включают головную боль, тошноту и лихорадку, а вслед за ними в течение 2-5 дней менингеальные симптомы раздражения и сильную боль в нижней части спины и конечностях. В серьезных случаях паралич появляется в течение первых двух дней.
Обычный спинальный полиомиелит характеризуется асимметричным вялым параличом, затрагивающим ноги, руки и/или туловище с отсутствием сухожильных рефлексов. Задержку мочи при начале заболевания демонстрируют 20-30% пациентов. Бульбарная форма редко бывает изолированной, распространяясь по меньшей мере на шейный отдел спинного мозга в 90% случаев. Могут поражаться все мышцы, иннервируемые черепными нервами. Кроме того, дыхательная недостаточность и гипертензия может быть результатом повреждения стволовой ретикулярной субстанции. Заболевание может сопровождаться энцефалитическими признаками, но они могут также вызываться и дыхательной недостаточностью из-за паралича диафрагмальных и межреберных мышц.
В анализе СМЖ обнаруживают 30-200 клеток/мм3. Изначально преобладают полиморфноядерные клетки, затем через 5-7 дней сменяющиеся лимфоцитарным плеоцитозом. Содержание белка повышается поздно, достигая максимальных значений примерно на 25 день заболевания.
По данным МРТ описано развитие отека спинного мозга с патологическим сигналом от центральной его части (Kibeetal., 1996). До начала клиники вирус может выделяться из кала и ротоглотки первые 19 дней и до трех месяцев после первых клинических проявлений (в среднем пять недель). При типировании вируса определяют один из трех типов полиовируса. Серологический диагноз ставится на основании повышения титра нейтрализующих или комплемент-связывающих антител.
Прогноз паралитического полиомиелита зависит от степени вовлечения. Восстановление поврежденных мышц часто происходит в течение года и более, но если через месяц мышцы все еще остаются парализованными, то обычно окончательно. Прогрессирующая болезнь моторных нейронов (постполиомиелитный синдром), напоминающий амиотрофический склероз, иногда наблюдается у взрослых через 20 и более лет после острого начала заболевания (Dalakas et al., 1986).
Случаи паралитического полиомиелита, связанного с живой вакциной, могут встречаться у пациентов с иммунодефицитом, получивших вакцину или контактировавших с вирусом (Nkowane et al., 1987; Sen et al., 1989; Groom et al., 1994). При этом возможны атипичные проявления. Поскольку редкие случаи полиомиелита могут также возникать у детей без иммунодефицита после живой вакцины (Dussaix et al., 1987), с уменьшением уровня заболеваемости во всем мире, в большинстве развитых стран сейчас используют убитую инъекционную полиовакцину при плановой вакцинации для предупреждения этого осложнения.
Постановка диагноза не представляет трудностей при условии, если не упускать из вида именно это заболевание. Синдром Гийена-Барре отличается от полиомиелита по характеру начала, симметричности распределения слабости и по данным ликвора. Регистрировались редкие случаи паралитического заболевания, связанного с другими вирусами (Kylleman et al., 1993). Вирус Западного Нила вызывал эпидемии заболеваний, напоминающих паралитический полиомиелит.
Случаи интоксикации химикатами или укусов насекомыми также могут имитировать сходную клиническую картину (Gear, 1984).

б) Энтеровирусы. Первоначальная классификация энтеровирусов, до геномного анализа, была основана на цитопатическом эффекте различных культивируемых клеток и инфицированных животных. Были выделены три типа полиовирусов, 24 коксаки-вируса типа А и 6 коксаки-вирусов типа В вирусов и 34 типа ЕСНО-вирусов. Последующие выделенные энтеровирусы обозначались номером, начиная от энтеровируса 68 без дальнейшего подразделения. Позднее геномный анализ последовательности частично подтвердил первоначальную культуральную классификацию.
Эти вирусы внедряются в организм хозяина через желудочно-кишечный тракт, где реплицируются и вызывают виремию, способную привести к инфекции ЦНС. В большинстве случаев отмечается слабый желудочно-кишечный вирусный продром, а в анамнезе присутствуют данные о наличии у членов семьи схожих симптомов. Большая часть случаев протекает в легкой форме с быстрым выздоровлением. Микроорганизмы можно обнаружить с помощью ПЦР или выделить из ликвора, а также из крови, кала и ротоглотки. При экспресс-диагностике ПЦР результаты можно получить через несколько часов. Инфекция встречается в любом возрасте, включая первые недели жизни (Kaplan et al., 1983).
Энтеровирусы Коксаки В1-5 и Коксаки А7, 9 и 25, ЕСНО-вирусы 4,6,9,11,14,16,18,20 и 30, так же как полиовирусы обычно вызывают асептический менингит. Острый эпидемический конъюнктивит, связанный с энтеровирусом 70, может осложняться менингитом, параличом черепных нервов или поражением конечностей, изолированно или совместно. Характерны сильные боли и фасцикуляции (Wadia et al., 1983; Chopra et al., 1986).
Менингит, вызванный вирусом Коксаки группы А, может сопутствовать или предшествовать герпангине, респираторным инфекциям и паротиту. Среди заболеваний группы В могут встречаться плевродиния (болезнь Борнхольма или эпидемическая миалгия) или диарея. Осложнением менингита могут быть миокардит и энцефалит, особенно у детей раннего возраста (Kaplan et al., 1983). Инфекции ЕСНО-вирусов могут вызывать как спорадические случаи, так и эпидемии. Пятнистопапулезная сыпь особенно характерна при инфекциях вирусов ECHO 4, 9 и 16. Иногда сыпь появляется при Коксаки А9 и А23. Также может быть петехиальной.
В литературе сообщалось о последствиях энтеровирусных менингитов (Kaplan et al., 1983). Вероятней всего, они являются результатом развития энцефалита, сопутствующего менингиту. Они особенно характерны при неонатальном энтеровирусном менингите, который также представлен лихорадкой, плохим аппетитом, диареей, гепатомегалией и сыпью (Huang et al., 2003).
Энтеровирусы также могут быть причиной других проявлений заболеваний ЦНС, включая паралич нижних двигательных нейронов (вирус Коксаки А4, 7, 9, В5, вирус ECHO 70); синдром Гийена-Барре и поперечный миелит (Коксаки А9, В1, 4, ECHO 6, 70); церебральную атаксию (Коксаки А9, 4, 7, В3, 4, ECHO 6, 9, 71); периферический неврит (ECHO 9). Энтеровирусы обычно вызывают самопроходящие заболевания, которые, хотя и связаны с заболеваемостью, редко заканчиваются смертельным исходом. Однако в некоторых более уязвимых группах пациентов (например, у младенцев или детей с иммунодефицитом) энтеровирусы могут вызывать угрожающие жизни инфекции.
Плеконарил — антивирусный препарат, который встраивается в капсид пикорнавирусов, включая энтеровирусы, предупреждая прикрепление вирусов к клеточным рецепторам и высвобождение вирусной РНК в клетку. Клинические испытания плеконарила показали некоторую эффективность у пациентов с тяжелой формой заболевания (Rotbart и Webster, 2001); к сожалению, этот лекарственный препарат не выпускался в промышленном масштабе.
в) Вирус эпидемического паротита. Среди неиммунизированного населения свинка выявляется как наиболее частая причина вирусного асептического менингита. Классическая клиническая картина лептоменингита встречается у 0,5-2% пациентов, больных эпидемическим паротитом. Однако плеоцитоз наблюдался только у 56% таких пациентов с паротитом (Russell и Donald, 1958). Паротит в 30-40% случаев может отсутствовать (Levitt et al, 1970), и в таких случаях диагноз можно получить при ПЦР амплификации вирусного генома в СМЖ или серологическими методами. Симптомы менингита появляются с 8 по 20 день после начала паротита. Часто сопровождаются выраженной лихорадкой.
В ликворе наблюдается лимфоцитарный плеоцитоз, нередко значительный, с сотнями клеток/мм 3 . Содержание глюкозы может быть снижено (Wilfert, 1969). Хотя заболевание обычно протекает в легкой форме, плеоцитоз может присутствовать на протяжении нескольких месяцев с длительным сохранением специфических интратекальных олигоклональных IgG (Vandvik et al., 1978a).

г) Вирусы герпеса. Некоторые представители семейства герпесвирусов могут вызывать лимфоцитарный менингит.
• Вирус простого герпеса. ВПГ 2 типа (Nahmias et al., 1982) чаще отвечающий за болезнь, чем 1 тип, который главным образом вызывает энцефалит. Менингит, вызванный ВПГ-2, может быть проявлением первичной инфекции у сексуально активных подростков. Иногда, легкие случаи ВПГ-1 инфекции могут проявляться только в виде раздражения мозговых оболочек (Whitley et al„ 1982а) с выздоровлением пациентов через 7-14 дней.
• Вирус опоясывающего герпеса. Вирус может вызывать асептический менингит, а также более сложное поражение ЦНС, описанное в следующем разделе. Могут встречаться пре-эруптивные неврологические проявления (Tsolia et al., 1995). В этом исследовании, у двоих детей с энцефалитом сопутствующей патологией была атаксия. Другие очаговые неврологические дефициты, кроме атаксии, развились у семи детей: у троих паралич лицевого нерва, у одного сопровождающая гемиплегия, двое имели парез верхних конечностей, у одного был радикулит, перешедший в парез ноги, и у одного ребенка паралич отводящего нерва. У двоих детей наблюдался изолированный менингит. В этой группе только двое детей переживали длительные последствия: у одного наблюдался стойкий паралич руки, у другого паралич отводящего нерва.
Другие синдромы ЦНС, связанные с вирусом ветряной оспы, включают вирусный миозит, радикулопатию, миелит и отсроченный гемипарез после ветряной оспы (Kamholz и Tremblay, 1985; Ichiyama et al., 1990; Rosenfeld et al., 1993; Herrold и Hahn, 1994; Gilden, 2004; Mariotti et al., 2006). Сообщалось также о поражении базальных ганглиев (Silverstein и Brunberg, 1995) и латеральном медуллярном синдроме (Kovacs et al., 1993). Сосудистые явления ишемического характера, часто поражающие крупные мозговые артерии, нередко отмечаются после ветряной оспы (Amlie-Lefond et al., 1995; Tsolia et al., 1995; Lanthier et al., 2005; Losurdo et al., 2006).
Острые артериопатии, приводящие к ишемическим инсультам, могут быть причиной четверти случаев тромбоза мозговых артерий в детском возрасте; в исследовании Guillot et al. (2005) наиболее вероятным этиологическим фактором в 60% случаев определена ветряная оспа (Guillot et al., 2005). Вероятно, при постинфекционных состояниях действует несколько механизмов, а в некоторых случаях важны воспалительные процессы в стенке артерий, так же как повышенная секреция прокоагулянтов, таких как антикардиолипин (Kurugol et al., 2000, 2001).
Кроме того, иммунная реакция хозяина на вирус ветряной оспы включает образование антител, способные на перекрестную реакцию и инактивацию белка S, важного фактора антикоагуляции хозяина. Это может привести к состоянию гиперкоагуляции и развитию молниеносной пурпуры, также как к ишемическому инсульту после Varicella zoster (Josephson et al., 2001).
• Вирус Эпштейна-Барр (ЭБВ). Большинство инфекций ЭБВ в раннем периоде жизни протекает бессимптомно, неврологические осложнения редки; они могут включать в себя асептический менингит, проявления энцефалита и некоторые другие осложнения ЦНС (Hung et al., 2000). Менингит может предвещать некоторые другие неврологические осложнения, такие как инфекционный полиневрит (синдром Гийена-Барре), энцефаломиелит или поражение черепных нервов (Hausler et al., 2002) или паркинсонизм (Hsieh et al., 2002). Примерно у трети пациентов с инфекционным мононуклеозом при исследовании СМЖ обнаруживают >5 клеток/мм 3 и такие показатели могут сохраняться месяцами, часто после полного клинического выздоровления (Pejme, 1964). Полное выздоровление может откладываться на несколько недель и месяцев.
• Вирус герпеса человека (ВГЧ) 6 и 7. ВГЧ-6 инфекция является причиной внезапной экзантемы (exanthema subitum), и в редких случаях вызывает менингоэнцефалит у здоровых прежде детей (Asano et al., 1992; Jones et al., 1994). Хотя большинство первичных инфекций ВПГ-6 (и тесно связанного ВПГ-7) протекают бессимптомно, оба вируса причастны к более 30% фебрильных судорог, встречающихся в первые два года жизни (Hall et al., 1994; Barone et al., 1995; Ward, 2005).
г) Аденовирусные инфекции нервной системы. Выделено множество типов аденовирусов; большинство вызывает легкие инфекции желудочно-кишечного тракта, дыхательной системы или почек и только в редких случаях они являются причиной синдромов поражения ЦНС. Проявления включают асептический менингит, миелит, подострый очаговый энцефалит, Рейе-подобный синдром и преходящую энцефалопатию (Linssen et al., 1991; Straussberg et al., 2001).
д) Парвовирус В19. Большинство инфекций парвовируса В19 имеют бессимптомное течение, но симптоматическая инфекция у детей обычно проявляется в виде лихорадки и сыпи, а у взрослых могут быть артропатии. Также сообщалось о редких случаях ЦНС инфекции с признаками менингоэнцефалита и определением вирусной ДНК в ликворе (Barah et al., 2001, 2003). Иммунный ответ хозяина к парво В19 в ЦНС считается предположительной причиной воспаления с подтверждением повышенного уровня цитокинов в ликворе, так же как специфического HLA-генома хозяина (Kerr et al., 2002).
е) Вирус лимфоцитарного хориоменингита (вирус ЛХМ). Вирус ЛХМ является человеческим зоонозом, вызываемым распространяемым грызунами ареновирусом, поражающим полевых мышей. Вирус передается человеку после контакта с выделениями зараженных мышей, морских свинок и хомяков. Внутриутробная инфекция у человека может привести к поражению плода (Barton и Mets, 2001; Barton et al., 2002), тогда как постнатальное инфицирование обычно протекает бессимптомно или как простудное заболевание, но может встречаться и синдром вовлечения ЦНС (Barton и Hyndman, 2000).
ж) Другие и неопределенные вирусы. Они, вероятно, являются причиной многих случаев заболеваний — в действительности большинства, в которых не могут быть выделены патогенные микроорганизмы. Понятно, что число возможных вирусных агентов велико, и поскольку заболевание обычно протекает в легкой форме, сложные исследования не проводятся.
Читайте также:

