Пост инфекционный генез головного мозга
Обновлено: 22.04.2024
Виды инфекций головного мозга
Все многообразие нейроинфекций, поражающих головной мозг можно разделить на пять групп:
- бактериальные;
- паразитарные;
- вирусные;
- прионные;
- грибковые.
Бактериальные инфекции
- повреждении костей черепа, с нарушением целостности оболочек мозга;
- заносе возбудителей во время нейрохирургической операции;
- наличии гнойного очага в организме и ослабленный иммунитет.
Однако с другими возбудителями дело обстоит иначе.
Менингококковая инфекция – традиционная нейроинфекция, которая поражает головной мозг. Пик заболеваемости отмечается в осенне- зимний период, когда иммунная система из-за частых переохлаждений человека и нехватки витаминов снижена.
Если иммунная система в норме, то вы ограничитесь обычным назофарингитом, в обратном случае – вероятность заполучить менингит или менингоэнцефалит возрастает.
Симптомы менингококковой инфекции
- лихорадка,
- повышение температуры тела до 39-40° С.
- озноб,
- головная боль
- слабость
- напряжение мышц шеи
- тошнота,
- рвота,
- Выступающая над поверхностью кожи сыпь красно-фиолетового цвета, элементы которой напоминают по форме звезду
- Заболевание начинается очень остро (часто можно указать конкретное время (час), когда человек заболел)
- В течение 24-х часов, пока человек в сознании должно начаться лечение, в противном случае он может впасть в кому.
Микобактерии туберкулеза кроме в всего прочего могут поражать и головной мозг.
Чаще болеют дети, пожилые люди и лица страдающие иммунодефицитом.
После присоединяются неврологические нарушения – парезы и параличи лицевого нерва, глазодвигательной мускулатуры, головокружения. На фоне неврологических расстройств возникают нарушения психики.
Нейросифилис, сейчас почти не встречается, но до открытия пенициллина составлял основу работы неврологов. Нейросифилис бывает нескольких видов:
Неприятной особенностью заболевания является его трудная диагностика.
Вирусные и прионные инфекции
Существует огромное множество вирусов –возбудителей острых энцефалитов (комариный, клещевой, эпидемический), в общем они отличаются переносчиками и географией распространения.
- парезы
- параличи дыхательной мускулатуры
- параличи конечностей,
- параличи лицевой мускулатуры и пр.
Огромную опасность могут составлять бешенство и медленные инфекции, в связи с чем, им уделяется особое внимание.
Бешенство.
Бешенством могут страдать практически все млекопитающие. Источником появления инфекции обычно служат собаки, волки, лисицы и именно через укус зараженных животных к человеку и передается эта опасная инфекция.
Симптомы:
- гидро и аэрофобия
- судороги
- приступы агрессивного поведения.
Экстренная вакцинопрофилактика после укуса – это единственный способ выздороветь, поэтому дожидаться развития первых симптомов заболевания запрещено, поскольку это может говорить только о том, что человека уже не спасти.
Медленные инфекции – вирусные нейроинфекции, которые имеют способность длительное время бессимптомно находиться в нервной ткани человека, с последующим развитием заболевания.
Учеными были выведены четыре главных признака, отличающих медленные инфекции:
- необычно продолжительный (месяцы и годы) инкубационный период;
- медленно прогрессирующий характер течения;
- необычность поражения органов и тканей;
- неизбежность смертельного исхода.
Возбудители вируса - краснуха и корь. По не до конца ясным причинам эти вирусы после перенесенного заболевания могут остаться в клетках головного мозга и через 4 и более лет вызывать заболевание. Оба вируса вызывают панэнцефалит со сходной симптоматикой:
· изменение личности с развитием деменции
· постепенный паралич всей поперечнополосатой мускулатуры.
К огромному сожалению, даже при лечении, последствия у этих нейроинфекций всегда одинаковы – летальный исход.
Существует четыре вида прионных нейроинфекций, и только с одной из них понятен механизм передачи. В некоторых племенах Папуа-Новая Гвинея часто отмечались случаи куру-куру из-за ранее распространенного ритуального каннибализма – поедания мозга родственников. Прионы вызывают спонгиформную энцефалопатию, то есть мозг превращается в подобие губки.
Паразитарные инфекции
Токсоплазмоз – паразитарное заболевание, характеризуется возможностью внутриутробного заражения, поражения нервной системы, глаз, скелетной мускулатуры и мышцы сердца, а также увеличением лимфоузлов, печени и селезенки.
Для возбудителя этого заболевания человек – промежуточный хозяин, а основной – кошки. При нормальном состоянии иммунитета заболевание никак не проявляется, но если человек страдает иммунодефицитом, то могут быть такие варианты заболевания:
- энцефалопатия, с развитием делирия, спутанности сознания вплоть до комы;
- менингоэнцефалит, со всеми своими классическими проявлениями;
- токсоплазменный абсцесс мозга, который проявляется общеинфекционными симптомами, очаговыми нарушениями, в зависимости от расположения, судорогами, нарушением сознания.
Наиболее тяжелые последствия токсоплазмоза – у беременных, так как он вызывает недоразвитие головного мозга плода.
Диагностика
Для того, чтобы диагностировать нейроинфекцию, в том числе головного мозга, используется комплекс мероприятий:
- общий анализ крови и мочи;
- биохимический анализ крови;
- анализ крови на антитела к вирусным, бактериальным и другим агентам;
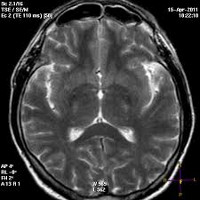
- методы визуализации – МРТ;
Лечение
Несмотря на различие возбудителей, некоторые аспекты лечения совпадают во всех случаях.
Больным обязательно назначают постельный режим (при острых инфекциях), противовоспалительные препараты, детоксикационную терапию.
Меры предосторожности
Не употреблять в пищу сырое или недостаточно термически обработанное мясо, тщательно мыть руки после контакта с кошками.
Энцефалопатия — это обобщающее название разнообразных по своему генезу патологических процессов, основу которых составляет дегенерация нейронов головного мозга вследствие нарушения их метаболизма. Энцефалопатия проявляется полиморфными неврологическими расстройствами, нарушениями в интеллектуально-мнестической и эмоционально-волевой сфере. Диагностический поиск состоит из комплексного неврологического обследования и установления причинной патологии. Лечение энцефалопатии сводится к устранению вызвавшего ее патологического состояния, терапии причинного заболевания и поддержанию оптимального метаболизма церебральных нейронов.
МКБ-10
Общие сведения

Причины энцефалопатии
Перинатальная энцефалопатия
К триггерным факторам, в результате воздействия которых может возникнуть перинатальная энцефалопатия, относятся:
- гипоксия плода;
- внутриутробные инфекции и интоксикации;
- резус-конфликт;
- асфиксия новорожденного;
- родовая травма;
- генетически детерминированные метаболические нарушения и аномалии развития (например, врожденные пороки сердца).
Риск перинатальной патологии возрастает при аномалиях родовой деятельности, крупном плоде, преждевременных родах и недоношенности новорожденного, узком тазе, обвитии пуповиной.
Приобретенная энцефалопатия
Приобретенная форма патологии может развиваться вследствие:
- перенесенной черепно-мозговой травмы;
- воздействия ионизирующего излучения;
- интоксикации нейротропными химическими (этиловым спиртом, свинцом, хлороформом, наркотиками, барбитуратами) и бактериальными (при дифтерии, столбняке, ботулизме и др.) токсинами;
- сосудистых нарушений: атеросклероза, артериальной гипертензии, венозной дисциркуляции, ангиопатии церебральных сосудов при амиломидозе, приводящих к хронической ишемии головного мозга;
- осложнения различных заболеваний внутренних органов: острого панкреатита, острой и хронической почечной недостаточности, цирроза печени и печеночной недостаточности;
- болезней легких, приводящих к расстройству легочной вентиляции (туберкулез легких, абсцесс легкого, бронхоэктатическая болезнь, ТЭЛА). Аналогичный гипоксический генез имеет энцефалопатия, наблюдаемая у ряда пациентов после проведения реанимационных мероприятий;
- метаболических расстройств: энцефалопатия может развиться как при понижении уровня глюкозы (гипогликемии), так и при его повышении (гипергликемии), что часто наблюдается при сахарном диабете. Причиной метаболических церебральных расстройств бывает гиповитаминоз (в первую очередь недостаток витаминов гр. В);
- падения осмотического давления и гипонатриемии, возникших из-за задержки воды при гиперсекреции антидиуретического гормона (при гипотиреозе, надпочечниковой недостаточности, опухолевых процессах и пр.);
- к редко встречающимся относится лейкоэнцефалопатия, имеющая вирусную этиологию и отмечающаяся у иммунокомпрометированных пациентов.
Патогенез
Энцефалопатия любого генеза является диффузным, т. е. затрагивающим различные церебральные структуры, процессом. В ее основе лежит кислородная недостаточность (гипоксия) и обменные нарушения нейронов. Последние могут быть обусловлены самой гипоксией (при дисциркцуляторных и гипоксических энцефалопатиях), дефицитом отдельных метаболитов и воздействием токсинов (при метаболических и токсических энцефалопатиях). Указанные нарушения приводят к дегенерации и гибели церебральных нейронов.
К морфологическим признакам, которыми характеризуется энцефалопатия, относятся: дегенерация и уменьшение количества нейронов в мозговом веществе, а значит его диффузная атрофия; очаги демиелинизации и некроза, а также глиальные разрастания, локализующиеся в белом веществе; микрогеморрагии и отечность церебральных тканей; полнокровие церебральных оболочек. Преимущественная локализация указанных изменений и степень их выраженности может варьировать в зависимости от вида энцефалопатии.
Классификация
В соответствии с этиологическим фактором, энцефалопатия классифицируется на посттравматическую, токсическую, метаболическую, сосудистую (дисциркуляторную), лучевую.
- Посттравматическая энцефалопатия относится к отдаленным последствиям ЧМТ и может развиваться через несколько лет после нее.
- Токсические варианты включают алкогольную энцефалопатию, наблюдающуюся при хроническом алкоголизме, а также церебральные нарушения, возникающие у наркоманов.
- Метаболические варианты: печеночная (портосистемная, билирубиновая), уремическая (азотемическая), диабетическая, панкреатическая, гипогликемическая, гипоксическая, аноксическая энцефалопатии и синдром Гайе-Вернике.
- Дисциркуляторная энцефалопатия подразделяется на атеросклеротическую, гипертоническую, венозную. Отдельной формой гипертонической энцефалопатии выступает болезнь Бинсвангера.
В клинической практике используют градацию энцефалопатии по тяжести, однако это разграничение весьма условно:
- I степень тяжести подразумевает субклиническое течение, т. е. отсутствие проявлений при наличии церебральных изменений, фиксируемых инструментальными методами диагностики. В этой стадии патология может диагностироваться при проведении диспансерного обследования пациентов с хроническими, в первую очередь сосудистыми, заболеваниями.
- II степень тяжести характеризуется наличием легкой или умеренной неврологической симптоматики, зачастую имеющей преходящий характер.
- При III степени наблюдаются тяжелые неврологические расстройства, в большинстве случаев выступающие причиной инвалидизации пациента.
Симптомы энцефалопатии
Более распространена хроническая энцефалопатия, отличающаяся малосимптомным началом и постепенным развитием. Наиболее часто она имеет дисдиркуляторный и посттравматический характер. Острая энцефалопатия характеризуется внезапным дебютом и быстрым усугублением состояния пациента, наличием нарушений сознания. Она может возникнуть при интоксикациях и дисметаболических расстройствах. Примерами являются острая панкреатическая, уремическая, печеночная энцефалопатия, синдром Гайе-Вернике, гипоксическая энцефалопатия при ТЭЛА.
Хроническая энцефалопатия
На ранних стадиях проявляется затруднениями при попытке вспомнить недавние события или недавно полученную информацию, снижением внимательности и умственной работоспособности, утомляемостью, нарушением сна, недостаточной гибкостью при перемене вида деятельности, психоэмоциональной лабильностью. Пациенты могут отмечать повышенную раздражительность, дневную сонливость, шум в голове, головную боль, не имеющую определенной локализации.
Симптомы могут варьировать у разных больных. В неврологическом статусе возможен нистагм, умеренная гиперрефлексия и мышечная гипертония, наличие рефлексов орального автоматизма и стопных знаков, неустойчивость в позе Ромберга, дискоординация, недостаточность ЧМН (понижение зрения, тугоухость, легкий птоз, парез взора), признаки вегетативной дисфункции.
Прогрессирование энцефалопатии сопровождается усугублением симптомов с формированием того или иного четко доминирующего неврологического синдрома: вестибуло-атактического, паркинсонического, гиперкинетического, псевдобульбарного. Нарастание нарушений интеллектуальной и эмоционально-волевой сферы приводит к формированию деменции. Возможны психические расстройства.
Острая энцефалопатия
Дебютирует внезапным психомоторным возбуждением с интенсивной головной болью, зрительными нарушениями, тошнотой и рвотой, шаткостью, в некоторых случаях — онемением языка, дистальных отделов кистей и стоп, психическими расстройствами. Достаточно быстро возбуждение сменяется апатией, зачастую происходит нарушение сознания различной глубины: оглушенность, дезориентация, сопор и кома. Могут наблюдаться различные виды эпиприступов. Острая энцефалопатия относится к ургентным состояниям и без оказания срочной медицинской помощи может привести к смертельному исходу вследствие отека мозга, нарушения функции жизненно важных церебральных центров.
Диагностика
Первичная диагностика энцефалопатии осуществляется неврологом по результатам опроса и неврологического осмотра. Дополнительно проводится комплексное инструментальное неврологическое обследование:
- Электроэнцефалография. ЭЭГ, как правило, выявляет диффузную дезорганизацию биоэлектрической активности мозга с появлением медленных волн. Возможно выявление эпи-активности.
- Эхоэнцефалография. Эхо-ЭГ позволяет оценить внутричерепное давление.
- Сосудистые исследования.Реоэнцефалография или УЗДГ сосудов головы дают информацию о состоянии церебрального кровообращения.
- Томография. Проанализировать степень морфологических изменений можно при помощи МРТ головного мозга. Этот метод также позволяет дифференцировать энцефалопатию от других церебральных заболеваний: болезни Альцгеймера, внутримозговой опухоли, энцефалита, рассеянного энцефаломиелита, инсульта, кортикобазальной дегенерации, болезни Крейтцфельдта — Якоба и пр.
Важнейшее значение в понимании этиологии энцефалопатии имеет сбор анамнеза, обследование соматических органов и консультации смежных специалистов: кардиолога, нефролога, гастроэнтеролога, эндокринолога, пульмонолога, нарколога. По показаниям проводятся гормональные исследования, определение уровня холестерина и сахара крови, анализ мочи, биохимия крови и мочи, УЗИ печени, УЗИ поджелудочной железы, экскреторная урография, УЗИ мочевыделительной системы, КТ почек, рентгенография грудной клетки, КТ легких и т. п.
Лечение энцефалопатии
Острая энцефалопатия является показанием к срочной госпитализации и ургентной терапии. Она может потребовать таких мер, как ИВЛ, гемодиализ, парентеральное питание. В лечении как острой, так и хронической энцефалопатии, ведущее место принадлежит терапии причинного заболевания.
Фармакотерапия
При интоксикациях производится дезинтоксикация, в т. ч. введение инфузионных растворов; при дисметаболических нарушениях — коррекция метаболизма (подбор дозы сахароснижающих препаратов или инсулина, введение р-ра глюкозы, в/в введение тиамина). Осуществляется лечение гепатита, цирроза, панкреатита, нефрита, заболеваний легких, гипертонической болезни, атеросклероза. Рекомендуется соблюдение диеты, соответствующей основной патологии, и режима, адекватного состоянию пациента.
Наличие ишемического компонента в патогенезе энцефалопатии является показанием к назначению сосудистой терапии: пентоксифиллина, тиклопидина, винпоцетина, ницерголина. Атеросклеротическая энцефалопатия требует включения в схему лечения гиполипидемических фармпрепаратов (например, симвастатина, гемфиброзила). Терапия гипертонической энцефалопатии проводится с назначением гипотензивных средств и мониторированием цифр АД.
В обязательном порядке проводится нейропротекторная и метаболическая терапия. В нее входят ноотропы (к-та гопантеновая, пирацетам, пиритинол, луцетам), аминокислоты (глицин, глутаминовая кислота), витамины (В1, В6, С, Е), препараты ГАМК (пикамилон, фенибут). При психических расстройствах необходимы психотропные средства: диазепам, бромиды, дроперидол, фенозепам. При судорогах проводится антиконвульсантная терапия, ноотропы противопоказаны.
Фармакотерапия осуществляется повторными курсами 2-3 раза в год. В качестве вспомогательного лечения используются методы физиотерапии: рефлексотерапия, электрофорез, магнитотерапия.
Хирургическое лечение
Прогноз и профилактика
Во многих случаях прогноз вторичной энцефалопатии определяет то, насколько эффективно можно лечить причинную патологию. Исход терапии также зависит от степени произошедших церебральных изменений. В ряде случаев положительным эффектом считается стабилизация энцефалопатии. При дальнейшем прогрессировании энцефалопатия достигает III степени и приводит к тяжелым неврологическим и эмоционально-психическим нарушениям, инвалидизирующим пациента. В случае перинатальной или острой энцефалопатии исход зависит от массивности и тяжести поражения мозговых тканей. Зачастую острые токсические энцефалопатии сопровождаются глубоким и необратимым поражением мозга.
Профилактика перинатальной энцефалопатии — это вопрос корректного выбора способа родоразрешения, адекватного ведения беременности, соблюдения правил ухода за новорожденным. Профилактика вторичной энцефалопатии заключается в своевременном выявлении и адекватном лечении сосудистых, урологических, гастроэнтерологических заболеваний, легочной патологии, эндокринных и метаболических нарушений. В качестве профилактических мер можно рассматривать правильное питание, активный образ жизни, отказ от курения, наркотиков и алкоголя.

Многие системные инфекции , особенно протекающие достаточно бурно, сопровождаются психическими расстройствами , например, делирием. Другие инфекции проявляют частичный нейротропизм ( инфекционные энцефалиты) , вызывают феномен васкулита , что отражается и на функциональной активности центральной нервной системы ( CNS). Постинфекционные заболевания обычно развиваются на фоне аутоиммунной дисфункции нервной системы. Для некоторых инфекционных агентов , типично развитие хронического активного инфекционного процесса или развитие инсульта , спровоцированного материнской или детской инфекцией. Например, некоторые вирусные инфекции матери , включая краснуху , инфлюэнцу, герпес II типа - HSV-2, повышают риск возникновения психоза у потомства.
Лептоменингит ( менингит) представляют собой воспаление мягкой и арахноидальной оболочек мозга и субарахноидального воспаления , которые могут стать и источником инфекции. Типичными клиническими симптомами менингита являются: головная боль, тошнота, рвота, раздражительность, фотофобия, ригидность мышц шеи , позитивный симптом Kernig ( резистентность при пассивной экстензии колена при согнутом бедре ), шейный симптом Brudzinski , Термин "Менингизм" отражает признаки менингеальной ирритации , особенно резистетность в результате мененгиального растяжения ( ригидность мышц шеи, симптом Kernig ), фотофобия и головная боль. Пахименингит представляет собой изолированное ( локальное) воспаление твердой оболочки и обычно развивается при попадании инфекции внутрь мозга в результате дефекта костей черепа, параназальной синусовой инфекции или краниального остеомиелита. Энцефалит ( церебрит - синоним термина "энцефалит", но обычно используется для характеристики локального бактериального инфекционного проццса с формированием абсцесса) - воспаление паренхимы мозга , сопровождается нарушением его функций , обычно сопровождаясь помрачением сознания в разной степени выраженности, часто судорожными припадками и фокальными неврологическими симптомами. Обычно энцефалит вызывается вирусной инфекцией или может не иметь инфекционного генеза ( острый диссименированный энцефаломиелит). По контрасту , энцефалопатия представляет собой диффузную дисфункцию мозга , развившеюся , например, в результате метаболических нарушений или интоксикации. Субдуральная эмпиема возникает внутри субдурального пространства , между твердой и арахнаидальной оболочками. Вентрикулиты ( эпиндемиты) характеризуют воспаление внутри желудочков мозга, обычно , типичное для менингита. Термин "миелит" обозначает воспаление спинного мозга.
Пиогенные бактериальные менингиты могут возникать спонтанно в вирулентном организме или развиться вследствии нейрохирургической операции , переломе костей черепа ( нарушение естественной защиты). Одна из наиболее распространенных причин пиогенного бактериального менингита стрептококковая пневмония , другой причиной спонтанного менингита являются Neisseria meningitidis , Streptococcus agolactiae, Haemophilus influenzae, Listeria monocytogenes. Типично острое развитие болезни с лихорадкой и признаками менингита , в частности, при Neisseria meningitidis , при этом может развиться системный сепсис или септический шок. К бактериальным инфекциям мозга также относят нейросифилис боррелиоз ( болезнь Лайма) лептоспироз, туберкулез , бруцеллезболезнь Wipple и другие бактериальные инфекции мозга ( тиф, тифоид). Наиболее частые вирусные инфекции : герпетический энцефалит ( вирус простого герпеса, вирус варицелла зостер, человеческий герпесвирус 6 , цитомегаловирус ( CMV) , вирус Эпштейн - Барр . Особое место среди причин вирсуного поражения мозга занимает вирус ВИЧ инфекции и деменция AIDS. К другим вирусным инфекциям способным вызвать инфекционное поражение мозга относят: инфлюэнцу А , бешенство , а к подострым вирусным энцефалитам - подострый склерозирующий панэнцефалит ( SSPE) , прогрессирующую мультифокальную лейкоэнцефалопатию. Протозойные инфекции также способны вызвать энцефалиты : малярия, токсоплазмоз , трипаносомия , аналогично , стоит отметить и грибковые инфекции ( микозы) , эозинофильный менингит и менингоэнцефалит , вызванный гельминтами или макропаразитами. К протеиновым инфекциям относят болезнь Creutzfeld - Jakob и другие прионные болезни.
Аутоиммунные болезни , развившееся после инфекционных заболеваний также способны вызвать энцефалиты ( хорея Sydenham и PANDAS ), летаргический энцефалит постинфекционный энцефаломиелит или острый диссеменирующий энцефаломиелит.

Демиелинизирующие расстройства - заболевания, основным патологическим процессом при которых является демиелинизация - разрушение, потеря миелиновой оболочки нейронов центральной или периферической нервной системы. Повреждение миелиновой оболочки ухудшает проводимость сигналов в пораженных нервах.
Демиелинизирующие заболевания по своему патогенезу чаще всего носят характер аутоиммунных процессов , реже, как проявление генетических заболеваний ( гипотезы о роли генетики и аутоиммунных дефицитах в этиологии демиелинизирующих заболеваний не могут объяснить многие случаи этих расстройств) . Кроме того , эти расстройства могут быть вызваны нейролептиками.
Некоторые демиелинизирующие заболевания могут быть вызваны инфекционными агентами , а некоторые - неизвестными факторами. Органофосфаты - класс химических веществ, которые являются активными ингредиентами инсектицидов, таких, как некоторые " сорняки - убийцы" , препараты для лечения блоху домашних животных и т.д., также демиелинизируют нервы. Дефицит витамина В12 также может привести к демиелинизации.
В отличие от других приматов, люди демонстрируют уникальную картину постпубертатной миелинизации, которая может способствовать развитию психических расстройств и нейродегенеративных заболеваний, возникающих в раннем взрослом возрасте и за его пределами. Продолжительный период кортикального миелинирования у людей предоставляет большую возможность для нарушения процесса миелинизации, в результате чего повышается риск возникновения демиелинизирующего заболевания. Кроме того, было отмечено, что люди имеют значительно больший префронтальный объем белого вещества, чем другие виды приматов, что подразумевает и большую плотность миелина. Таким образом, повышенная плотность миелина у людей в результате длительного процесса миелинирования может повысить риск дегенерации и дисфункции миелина.
Демиелинизацию можно разделить на 2 типа:
- миелинопатия — разрушение уже сформированного миелина из-за причин, связанных с биохимическим дефектом строения миелина, как правило, генетически обусловленным (например, болезнь Канавана, лейкодистрофические заболевания);
- миелинокластия — разрушение нормально синтезированного миелина под влиянием различных воздействий ( интоксикация, аутоиммунный процесс , химические вещества и др.) , как внешних, так и внутренних (например, болезнь Бинсвангера)
Подразделение демиелинизирующих заболеваний на эти две группы условно, так как первые клинические проявления миелинопатий могут быть связаны с воздействием различных внешних факторов, а миелинокластии вероятнее всего развиваются у предрасположенных к ним лиц. Демиелинизирующие заболевания можно также разделить на те, которые затрагивают центральную нервную систему, и те, которые повреждают периферическую нервную систему.
Демиелинизирующие заболевания центральной нервной системы : рассеянный склероз, болезнь Девика, концентрический склероз Бало , воспалительные демиелинизирующие заболевания ( синдром осмотической демиелинизации; миелопатии, например, спинная сухотка, лейкоэнцефалопатии ( ПМЛ) , лейкодистрофии и др.) . Лейкодистрофии , как правило, связаны также с проявлениями оптического неврита и поперечного миелита , которые являются воспалительными состояниями, поскольку воспаление и демиелинизация часто связаны между собой.
В наиболее известном примере, заболевании под названием рассеянный склероз ( воспалительное демиелинизирующее заболевание центральной нервной системы, которое развивается у генетически восприимчивых лиц после воздействия неизвестного экологического триггера (ов), есть веские доказательства того, что собственная иммунная система организма по меньшей мере частично вовлечена здесь в патологический процесс. Известно, что приобретенные клетки иммунной системы ( Т - клетки) , обнаруживаются в месте поражения ; а другие клетки иммунной системы ( макрофаги и , возможно, тучные клетки) также способствуют повреждению миелина. В то же время , рассеянный склероз, не может быть объяснен только аутоиммунным дефицитом, но это заболевание в значительной степени подразумевает влияние ошибочных процессов развития в патогенезе болезни. По большому счету причины рассеянного склроза (MS) неизвестны, но с большой вероятностью связаны с иммунными реакциями против аутоантигенов, в частности миелиновых белков. Наиболее приемлемой гипотезой является та, согласно которой "диалог" ( взаимодействие ) между рецепторами Т-клеток и миелиновыми антигенами приводит к иммунной атаке на комплекс миелин-олигодендроциты. Эти взаимодействия между активными Т-клетками и миелиновыми антигенами вызывают массивный деструктивный воспалительный ответ и способствуют продолжению пролиферации Т и В-клеток , а также активации макрофагов, которые поддерживают секрецию воспалительных медиаторов.
Демиелинизирующие заболевания периферической нервной системы: синдром Гийена - Барре и его хронический аналог хроническая воспалительная демиелинизирующая полинейропатия;, невральная амиотрофия Шарко - Мари - Тута, анти - MAG периферическая нейропатия , болезни связанные с дефицитом меди ( периферическая нейропатия , миелопатия, редко - зрительная нейропатия) , прогрессивная воспалительная нейропатия и др.
Общие клинические признаки демиелинизации как патологического процесса выделить нельзя. Симптомы зависят от очага локализации демиелинизации в центральной или периферической нервной системы. Ниже приведен список наиболее часто встречающихся симптомов демиелинизирующих заболеваний: диплопия ( "двоение в глазах" ) , атаксия, подергивание мышц, диартрия, чувство усталости, односторонний парез , паралич рук , неуклюжесть движений ; окулярный паралич ( паралич черепно - мозговых нервов), нарушение координации мышц, мышечная слабость, потеря ощущений, парестезии, генитальная анестезия, нарушение зрения , очаговые неврологические симптомы, неуверенная походка, спастический парапарез , недержание мочи , проблемы со слухом и речью.
Диагностика демиелинизирующего заболевания периферической нервной системы основывается на результатах электронейромиографии.
Лечение обычно связано с улучшением качества жизни пациента. Это достигается посредством "управления симптомами" или замедления темпа демиелинизации. До сих пор нет терапии, которая специально нацелена на врожденные иммунные клетки при рассеянном склерозе. Ожидаемая продолжительность жизни у пациентов с рассеянным склерозом на 5-10 лет ниже, чем у обычных людей. В настоящее время считается, что N-кадгерин играет роль в процессе миелинизации. Эксперименты показали, что N-кадгерин играет важную роль в создании среды, облегчающей ремиелинизацию. На животных моделях было показано, что существует прямая корреляция между количеством присутствующих миелиновых частиц и наблюдаемой степенью воспаления. Эксперименты также показали, что , что манипулирование уровнями гормонов щитовидной железы можно рассматривать как стратегию для содействия процессам ремиелинизации и предотвращения необратимого повреждения у пациентов с множественным ( рассеянным ) склерозом. Агонисты N-кадгерина идентифицированы и используются для стимуляции роста нейритов и миграции клеток, ключевых аспектов развития роста аксонов и ремиелинизации после травмы или заболевания. Было показано, что интраназальное введение aTf ( apotransferrin ) может защитить миелин и вызвать ремиелинизацию. Большая часть исследований была проведена в 2012 году и представляет собой сравнительно новую информацию о демиелинизирующих заболеваниях и потенциальных методах их лечения.
Читайте также:

