Повышаются ли лимфоциты при туберкулезе
Обновлено: 12.05.2024
Лимфоцитопения (лимфопения) – это снижение уровня лимфоцитов менее 1 800 (18% от общего числа лейкоцитов) в 1 мкл крови. У детей из-за физиологического лимфоцитоза вследствие лейкоцитарного перекреста лимфоцитопенией признан показатель ниже 3 500-4 500. Причиной считаются инфекционные и аутоиммунные заболевания, злокачественные болезни крови. Клиническая картина определяе тся основной патологией. Лимфопения может проявляться гипоплазией миндалин глоточного кольца, активацией оппортунистических инфекций. Концентрация лимфоцитов измеряется в общем анализе крови (ОАК). Для их возврата к нормальным показателям необходимо лечение заболевания, послужившего причиной возникновения лимфоцитопении.
Классификация
Пороговых цифровых значений для разделения лимфоцитопении по степени тяжести не существует, условно выделяют умеренную и тяжелую. По отношению лимфоцитов к другим видам лейкоцитов различают следующие виды лимфоцитопении:
- Относительная. Снижение процентного содержания лимфоцитов в лейкоцитарной формуле меньше 18% при сохранении их нормального количества.
- Абсолютная. Уменьшение количества лимфоцитов в крови ниже 1 800.
Причины лимфоцитопении
Физиологические процессы
Лимфоцитопения не обязательно является признаком какого-либо заболевания. Причиной могут быть различные физиологические состояния, например, продолжительный стресс. При стрессе в кровь выделяются гормоны надпочечников (глюкокортикостероиды), обладающие разрушительным влиянием на лимфоциты. Лимфоцитопения также может наблюдаться при дефиците белка, поэтому нередко встречается при голодании или у людей, придерживающихся вегетарианской либо веганской диеты.
Вирусные инфекции
Под действием некоторых лимфотропных вирусов происходит ускоренная гибель лимфоцитов. Наиболее распространенной и опасной инфекционной причиной лимфоцитопении является вирус иммунодефицита человека (ВИЧ). Он связывается со специальными рецепторами (CD4) на поверхности Т-лимфоцитов (Т-хелперов), проникает внутрь клетки, где активно размножается и приводит к ее гибели. Снижение количества Т-хелперов происходит как за счет прямого повреждающего действия вируса, так и вследствие активации апоптоза (запрограммированной клеточной смерти) и аутоиммунного поражения.
В самом начале инфицирования уровень лимфоцитов может, наоборот, возрастать с развитием лейкоцитоза как иммунная реакция на чужеродный микроорганизм, но затем следует стремительное падение концентрации белых кровяных клеток вплоть до их полного отсутствия, с чем связано развитие синдрома приобретенного иммунодефицита, повышенной восприимчивости организма пациента к различным инфекциям, в том числе оппортунистическим. Лимфоцитопения может начать регрессировать только после длительной антиретровирусной терапии.
Кроме того, разрушению лимфоцитов способствуют следующие вирусные инфекции, при которых лимфоцитопения выражена намного меньше, чем при ВИЧ:
Бактериальные инфекции
Причиной лимфоцитопении также могут стать некоторые бактериальные инфекции – лептоспироз, эрлихиоз, легионеллез. Наибольшую значимость имеет лимфопения при такой распространенной инфекции, как туберкулез (милиарный, диссеминированный). При этом заболевании наблюдается снижение Т-хелперов, Т-супрессоров (CD4, CD8 клеток). Патология встречается при септических состояниях (бактериальном заражении крови). Абсолютная лимфоцитопения свидетельствует о неблагоприятном течении любой бактериальной инфекции. Показатели достаточно быстро приходят в норму после проведения антибактериальной и противотуберкулезной терапии.

Аутоиммунные заболевания
Еще одной причиной лимфоцитопении выступают хронические воспалительные заболевания аутоиммунного характера. В ходе многочисленных исследований было обнаружено два основных патогенетических механизма лимфопении при этих патологиях – выделение антилимфоцитарных антител и снижение экспрессии на мембранах иммунных клеток специальных протеинов (CD55, CD59), защищающих клетки от комплемент-опосредованного цитолиза. Лимфоцитопения обычно умеренная, может коррелировать с тяжестью болезни, регрессирует во время ремиссии или под влиянием патогенетического лечения.
- Заболевания суставов.Ревматоидный артрит.
- Диффузные болезни соединительной ткани (коллагенозы). Системная красная волчанка, синдром Шегрена.
- Системные васкулиты. Гранулематоз с полиангиитом, неспецифический аортоартериит Такаясу.
- Воспалительные заболевания кишечника (ВЗК). Неспецифический язвенный колит, болезнь Крона.
- Рассеянный склероз.
Лимфопролиферативные заболевания
Онкогематологические патологии, такие как лимфогранулематоз (лимфома Ходжкина), Т-В-клеточные лимфомы, лимфосаркомы, тоже могут являться причиной лимфоцитопении. Обычно она развивается на поздних стадиях болезни и считается одним из критериев неблагоприятного исхода. Падение уровня лимфоцитов обусловлено истощением лимфоидной ткани и замещением гемопоэтической ткани атипичными злокачественными клетками.
Редкие причины
- Угнетение лимфоцитообразования: наследственные иммунодефициты (синдром Вискотта-Олдрича, синдром Ди Джорджи), заболевания, сопровождающиеся замещением лимфоидной ткани эпителиоидными гранулемами (саркоидоз, гистиоцитоз Х), воздействие ионизирующего излучения, апластическая анемия.
- Потери лимфы: повреждения крупных лимфатических протоков при травмах и полостных операциях, массивные ожоги, первичная кишечная лимфангиэктазия (болезнь Вальдмана).
- Ускоренное разрушение лимфоцитов: эндокринные расстройства (болезнь и синдром Иценко-Кушинга, сахарный диабет 1 типа), терминальная стадия хронической почечной недостаточности.
- Использование лекарственных препаратов: глюкокортикостероиды, иммуносупрессанты (метотрексат, азатиоприн), моноклональные антитела.
- Заболевания с неизвестным механизмом лимфоцитопении: злокачественные новообразования – рак молочной железы, щитовидной железы, прямой кишки.
Диагностика
Уровень лимфоцитов измеряется при подсчете лейкоцитарной формулы в клиническом анализе крови. Поскольку спектр заболеваний, которые могут быть причиной лимфопении, достаточно широк, при ее обнаружении следует обратиться к врачу для детального обследования. На основании клинических, анамнестических данных специалист составляет программу диагностических исследований, которая включает:
- Лабораторные анализы. Изучается как общее количество, так и процентное соотношение различных видов лейкоцитов. Определяется уровень маркеров воспаления – СОЭ, СРБ. Проверяется наличие аутоантител (АЦЦП, антител к ДНК, к цитоплазме нейтрофилов). При подозрении на сепсис измеряется прокальцитонин, пресепсин. При воспалительных патологиях кишечника в кале повышается содержание фекального кальпротектина. Исследуется концентрация сывороточных иммуноглобулинов (IgG, IgM, IgA).
- Микробиологические исследования. Для подтверждения туберкулеза проводится бактериологический посев и микроскопия мокроты, туберкулинодиагностика (проба Манту, диаскин-тест). Методом иммуноферментного анализа идентифицируются антитела к возбудителям (вирусам, бактериям). Верифицирующим тестом на ВИЧ-инфекцию является обнаружение белков оболочки вируса (gp120, gp41) при иммуноблоттинге.
- Инструментальные исследования. При туберкулезе на рентгенограммах легких отмечается увеличение лимфатических узлов (прикорневых, медиастинальных), инфильтрации верхних долей легких. На снимках суставов при ревматоидном артрите выявляется сужение суставной щели, краевые эрозии, остеопороз. При фиброколоноскопии у больных ВЗК находят гиперемию слизистой оболочки, участки изъязвления. На МРТ головного мозга при рассеянном склерозе видны очаги демиелинизации овальной формы размером 1-2 мм.
- Гистологические исследования. При исследовании материала, полученного путем биопсии лимфатического узла, у больных лимфопролиферативными заболеваниями отмечается диффузная пролиферация лимфоидных клеток, имеющих бластную морфологию, клетки Березовского-Штернберга. При системных васкулитах в биоптате обнаруживают периваскулярную инфильтрацию плазмоцитами, гистиоцитами.

Коррекция
Путей самостоятельного купирования лимфоцитопении не существует. Для нормализации уровня лимфоцитов нужно устранить причину, а именно – проводить лечение основной патологии. Если лимфоцитопения возникла на фоне стресса или дефицита белка в пищевом рационе, лечение не требуется, достаточно откорректировать диету. При стойкой длительной лимфопении необходимо медицинское вмешательство. В зависимости от причины применяются следующие мероприятия:
- Борьба с инфекцией. Для лечения ВИЧ-инфекции назначается антиретровирусная терапия – нуклеозидные ингибиторы обратной транскриптазы, ингибиторы протеазы (саквинавир). При гриппе показан осельтамивир. Для лечения остальных вирусных инфекций не существует этиотропных медикаментов, используются симптоматические методы (жаропонижающие средства, дезинтоксикационная терапия). При неспецифических бактериальных инфекциях рекомендованы антибиотики, при туберкулезе – комбинации противотуберкулезных средств (изониазид, рифампицин).
- Противовоспалительная терапия. Для достижения ремиссии аутоиммунных заболеваний применяются лекарственные препараты, подавляющие процесс воспаления – глюкокортикостероиды, синтетические производные аминохинолина и 5-аминосалициловой кислоты, иммуносупрессанты (метотрексат, циклофосфамид).
- Лечение лимфопролиферативных болезней. При лимфогранулематозе, неходжкинских лимфомах показана полихимиотерапия (винкристин, дакарбазин, этопозид). Эффективно облучение пораженных опухолью лимфатических узлов.
Прогноз
Лимфоцитопения достаточно часто является предиктором неблагоприятного прогноза, сопряжена с повышенным риском инфекционных заболеваний и активацией условно-патогенной микрофлоры. Исход и продолжительность жизни пациентов определяются основной патологией, на фоне которой возникла лимфопения. Наиболее доброкачественной является лимфоцитопения, развившаяся после длительного стресса или при белковом голодании. Наследственные иммунодефицитные состояния и онкогематологические болезни характеризуются большой вероятностью летального исхода в ранние сроки.
1. Лимфопения: основные причины развития/ Ватутин Н.Т., Ещенко Е.В.// Архивъ внутренней медицины. – 2016 - № 2(28).
2. Патофизиология системы крови. Часть II. Нарушения в системе лейкоцитов/ Николаева О.В., Кучерявченко М.А., Шутова Н.А. и др. – 2016.
Кровь при туберкулезе. Гематологические показатели туберкулеза.
В результате интоксикации, изменения реактивности организма и тканевых повреждений у больных туберкулезом наступают различные по характеру сдвиги в кроветворной системе. Существенную роль играют при этом не столько форма, сколько фаза и динамика процесса. При ограниченных и малоактивных его формах количество эритроцитов обычно находится в пределах нормы и отсутствуют признаки анемии. При массивных инфильтратах или творожистой пневмонии, при распространенном казеозном лимфадените, специфическом поражении кишечника, вовлечении в процесс печени, селезенки, костного мозга, а также после больших легочных или послеоперационных кровотечений отмечаются падение количества эритроцитов и изменение их морфологии (олиго- и полихромазия), а иногда мегалобластическая, апластическая или анемия смешанного типа (мегалобластическая и железодефицитная). При этом увеличивается содержание не вполне созревших эритроцитов — ретикулоцитов (свыше 0,5—1 % ) и количество кровяных пластинок (более 250 000—300 000). Подобным образом изменяется и эритропоэтическая функция костного мозга.
Чаще и в большей мере при туберкулезе, но главным образом при выраженных, прогрессирующих и осложненных его формах изменяется лейкограмма. В части случаев может отмечаться умеренный лейкоцитоз (до 10000—15 000 лейкоцитов), реже лейкопения. Так, Е. Л. Кан (1972) наблюдала лейкопению у 20,7% больных с ограниченными и легко протекавшими формами процесса и у 12,5% — при деструктивном и прогрессирующем туберкулезе легких.
Наиболее часто сдвиги наступают в лейкоцитарной формуле. Увеличивается количество нейтрофилов как в абсолютном, так и в относительном выражении за счет палочкоядерных форм (до 15—20%). Одновременно уменьшается содержание лимфоцитов (до 8—15%). При выраженном и затянувшемся инфильтративном процессе и обширном бронхогенном обсеменении появляется патологическая зернистость нейтрофилов. При диссеминации, по наблюдениям Н. Н. Боброва (1950) и Н. А. Шмелева (1959), нарастает моноцитоз (до 10—18%).
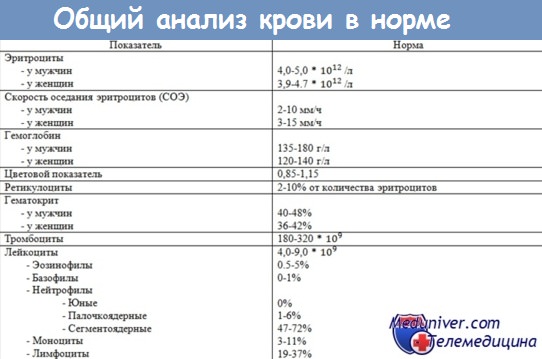
Заслуживает внимания указание на увеличение абсолютного количества базофилов при активном туберкулезном процессе. Тромбоцитарный профиль периферической крови характеризуется увеличением удельного веса форм раздражения и дегенеративных элементов, что обусловлено степенью активности процесса и интоксикации.
Таким образом, отдельные фазы туберкулеза легких характеризуются следующими гематологическими синдромами.
Фаза инфильтрации: умеренный или значительный лейкоцитоз, выраженный сдвиг пейтрофилов влево, нормальное или повышенное содержание нейтрофилов с патологической зернистостью, умеренное или значительное ускорение РОЭ, смещение тромбоцитограммы вправо за счет повышения содержания форм раздражения и дегенеративных элементов.
Фаза распада: небольшой лейкоцитоз или нормальное количество лейкоцитов, увеличение процента нейтрофилов с патологической зернистостью и сдвигом влево, иногда с появлением миелоцитов, уменьшение количества эозинофилов и лимфоцитов, значительное ускорение РОЭ.
Фаза гематогенной диссеминации: нормальное количество лейкоцитов, абсолютный и относительный моноцитоз.
Фаза рассасывания: увеличение количества эозинофилов и лимфоцитов, отсутствие ядерного сдвига влево.
Фаза уплотнения: нормальные показатели гемограммы, иногда лимфоцитоз.
Гемограмма у больных туберкулезом изменяется в процессе лечения. В благоприятных случаях нормализуется количественный и качественный состав кровяных клеток. Такие положительные сдвиги наступают обычно спустя 2—3 мес, т. е. через более длительный срок после исчезновения лихорадки и других симптомов интоксикации. Гематологические сдвиги исчезают тем быстрее, чем успешнее терапевтическое вмешательство, т. е. чем скорее прекращается интоксикация, рассасываются очаги и зоны инфильтрации, закрываются каверны, прекращается бацилловыделение.
Вместе с тем следует иметь в виду воздействие на гемопоэз различных антибактериальных препаратов. Они нередко вызывают эозинофилию, в отдельных случаях — лейкоцитоз, а чаще лейкопению; иногда при этом угнетается образование нейтрофилов вплоть до аграпулоцитоза и может стимулироваться лимфоидно-ретикулярная реакция. Эти изменения наступают в результате аллергизирующего или токсического действия препаратов на костный мозг.
При развитии агранулоцитоза необходимо прекратить прием вызвавшего его медикамента. Аллергизация к препарату определяется лабораторными пробами (тест Шелли, реакция Уанье). Назначение нуклеината натрия или пентоксила, кортикостероидных гормонов, поливитаминов, гемотрансфузии способствует восстановлению костно-мозгового кроветворения.
Таким образом, систематический гематологический контроль и правильный анализ полученных при этом результатов имеют существенное значение для оценки клинического состояния больного, динамики процесса и эффективности применяемого лечения. Гематологические данные приобретают определенное значение и при дифференциальной диагностике туберкулеза и других заболеваний органов дыхания.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Комплексная туберкулинодиагностика. Реакция лейкоцитов на введение туберкулина.
Совместно с Р. А. Иоффе мы в 1959 г. разработали вариант комплексной методики туберкулинодиагностики, который позволяет учесть одновременно очаговую и общую реакцию в виде изменения состава белковых фракций сыворотки крови. У части больных активным туберкулезом через 48 ч после введения 5—20 ТЕ уменьшается уровень альбуминов и увеличивается содержание глобулинов. При этом возможна диссоциация в результатах определения туберкулиновой чувствительности различными способами. Так, у больных с выраженной кожной аллергией белковые фракции сыворотки крови могут не изменяться. Возможно и обратное соотношение. Чаще совпадают общие, очаговые реакции и биохимические сдвиги. Важно, что сдвиги в белковых фракциях крайне редко наступают при неактивных туберкулезных изменениях, неспецифических заболеваниях легких.
Достоверность этой пробы, выпадающей положительной, правда, только у части больных активным туберкулезом, была подтверждена многими исследователями, применившими ее у взрослых и детей при дифференциальной диагностике различных заболеваний органов дыхания, а также при определении активности туберкулеза.
Последующие исследования, проведенные нами совместно с М. Н. Доброхотовой, Р. А. Иоффе и М. 3. Упитером (1967), показали, что при клинической и рентгенологической активности процесса, помимо снижения уровня альбуминов и повышения содержания в сыворотке крови альфа-глобулинов, наступает уменьшение концентрации гликопротеидов в альбуминовой фракции и увеличение их в альфа-глобулиновой фракции. Такие сдвиги отмечались лишь у части больных активным туберкулезом, но они, как правило, отсутствовали при неактивном и излеченном процессе. Между тем при активном туберкулезе после подкожного введения туберкулина не изменяются существенно уровень липопротеидов, содержание сиаловой кислоты, не появляется С-реактивный белок.
Однако указанными тестами не исчерпываются все возможности определения иммунобиологического состояния организма инфицированного или больного туберкулезом человека. В этой области велись и проводятся поиски других способов исследования. Уже давно пытались изучить влияние in vitro туберкулина на клетки периферической крови, селезенки, лимфатических узлов больных, а также инфицированных или здоровых людей и животных (Rich, Lewis, 1932, и др.). При этом было установлено, что в одних случаях происходит разрушение сенсибилизированных клеток, а в других, наоборот, — их бласттрансформация. Этот феномен связан отчасти с повреждением клеток организма в результате их взаимодействия с антигеном, а также с возможностью пассивного переноса аллергии лейкоцитами крови.
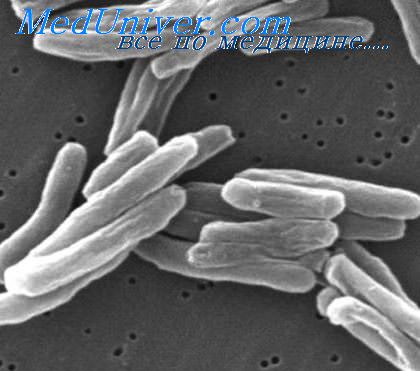
Это обстоятельство побудило нас в 1941 г. изучить в тканевых культурах изменение лейкоцитов крови больных или инфицированных туберкулезом для выявления специфической сенсибилизации организма. При этом мы могли установить, что вскоре после помещения лейкоцитов во флаконы наступает интенсивная миграция главным образом зернистых лейкоцитов. Через 48 ч наряду с зернистыми лейкоцитами, лимфоцитами и моноцитами появляются макрофаги или полибласты Максимова, а иногда и вытянутые фибробластоподобные клетки. Через 3—4 дня зернистые лейкоциты дегенерируют, а количество макрофагов и фибробластоподобных клеток увеличивается. К 5—6-му дню образуются гигантские клетки. После добавления в культуру лейкоцитов микобактерий туберкулеза ускоряется бласттрансформация лейкоцитов больных с благоприятно протекающими формами легочного туберкулеза.
Уже через 24—48 ч в таких случаях, помимо лимфоцитов и моноцитов, можно обнаружить макрофаги, фибробластоподобные и гигантские клетки, которые скопляются вокруг микобактерий, частично подвергающихся фагоцитозу. В дальнейшем образуется синцитиальная ткань, распадающаяся спустя 10—14 дней после начала опыта. При массивной дозе микобактерий туберкулеза происходит замедленное превращение клеточных элементов, которые в дальнейшем быстро разрушаются. У больных с распространенными и неблагоприятно протекающими формами туберкулеза гигантские клетки образуются лишь к 5—6-му дню, а часто уже на 3—4-й День происходит распад клеточных элементов.
Подобные результаты мы получали и в опытах с культурами лейкоцитов в присутствии туберкулина. Установлено, что туберкулин даже в большой концентрации не влияет на развитие лейкоцитов у лиц, не зараженных туберкулезом или клинически здоровых. Но в тех же дозах он вызывает быстрый распад лейкоцитов у больных туберкулезом, в особенности при тяжелых его формах.
Таким образом, изучение клеточных реакций убедило нас в их определенной зависимости от уровня специфической сенсибилизации и реактивности организма. К такому выводу в дальнейшем пришли и другие авторы, пользовавшиеся тем же или разработанными на том же принципе способами исследования. Установлено, например, что микобактерий туберкулеза интенсивно размножаются внутри лейкоцитов здоровых или зараженных вирулентными микобактериями животных. Между тем в тканевых культурах лейкоцитов животных, предварительно вакцинированных БЦЖ, микобактерий не развиваются или размножаются слабо. Выяснилось также, что лейкоциты здоровых животных длительно сохраняются в нормальной плазме в присутствии туберкулина. Между тем лейкоциты туберкулезных животных в тех же условиях разрушаются в течение одного часа. Hall, Scherago (1957) при изучении культуры лейкоцитов от 297 больных туберкулезом и 212 здоровых людей также выявили более высокую сенсибилизацию к туберкулину лейкоцитов больных туберкулезом и здоровых, но инфицированных людей по сравнению с отрицательно реагировавшими на пробу Манту.
В сущности тот же принцип лежит в основе метода, позволяющего определить степень повреждаемости нейтрофилов в присутствии очищенного сухого туберкулина. Если этот показатель (ППН) составляет в норме 0,06—0,09, то при активном туберкулезе он выше в 1,5—3,5 раза.
Для выявления повышенной чувствительности организма и активности туберкулезного процесса исследуют также реакцию торможения миграции лейкоцитов и бласттрансформации лимфоцитов периферической крови in vitro под влиянием туберкулина. Оказывается, что у больных эволютивным и деструктивным туберкулезом замедляется миграция и угнетается иммуноспецифическая бласттрансформация клеточных элементов. Этот феномен не отмечается у здоровых людей. Еще более отчетливо выявляется тот же характер клеточных реакций после подкожного введения туберкулина (20ТЕ). Как показали исследования, проведенные в нашей клинике А. С. Борзенко (1974) на 130 детях и подростках, через 48 ч после впрыскивания туберкулина при активном туберкулезе усиливается торможение миграции лейкоцитов и угнетается бласттрансформация лимфоцитов. Одновременно повышается уровень щелочной фосфатазы нейтрофилов. Эти сдвиги в значительно меньшей степени выражены при излеченном туберкулезе, у инфицированных, но здоровых детей, а также при хронической пневмонии.
По данным автора, эти пробы оказались более чувствительны по сравнению с другими методами туберкулинодиагностики. Тем не менее их диагностическое значение увеличивается при одновременном использовании других туберкулиновых проб, вызывающих, в частности, очаговые реакции, и, конечно, в сочетании с результатами клинико-рентгенологических методов исследования.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Биохимия крови при туберкулезе. Биохимические показатели крови.
Из многих биохимических тестов, широко используемых в настоящее время в клинической практике, определенное значение имеет изучение состава белков крови, которые играют весьма важную роль в физиологических функциях и гомеостазе организма, в состоянии иммунитета, развитии и течении воспалительных реакций и т. д.
Сдвиги в белковом составе крови при туберкулезе зависят не только от его формы, но главным образом от фазы процесса, его осложнений и различных сопутствующих заболеваний. У больных с неактивными специфическими изменениями в легких и других органах в сыворотке крови определяется нормальное содержание общего белка, фибриногена, белковых фракций и гликопротеидов; отсутствует С-реактивный белок, не увеличена РОЭ, нет отклонений в коагуляционных пробах и т. д. При свежих, особенно остро протекающих, формах болезни, а также при обострении и прогрессировании хронического процесса наблюдается диспротеинемия, а иногда и гипопротеинемия, т. е. наступают количественные и качественные изменения в составе белков как проявление неспецифической гуморальной реакции на патологические сдвиги в организме. В таких случаях нарастает РОЭ, изменяются коагуляционные пробы, появляется С-реактивный белок, повышается уровень фибриногена, нарушается количественное соотношение белковых фракций и содержание белково-углеводных соединений (глико- и мукопротеидов, серомукоидов) в сыворотке и плазме крови.
Как показывают многочисленные исследования, в частности проведенные в клинике туберкулеза ЦОЛИУ врачей И. В. Алфимовой (1965), К. В. Бережковой (1955), Л. Н. Бринбауэр (1965), Р. А. Иоффе (1962) и др., эти сдвиги характеризуются уменьшением содержания альбуминов и повышением уровня глобулинов и гликопротеидов. При инфильтративной фазе процесса заметно увеличивается концентрация фракции глобулинов и гликопротеидов, а при фиброзно-кавернозном туберкулезе и эмпиеме плевры значительно нарастает, кроме того, уровень их фракции. При этих формах болезни снижается также концентрация липопротеидов и несколько повышается уровень Р-фракций. Чем острее и неблагоприятнее протекает туберкулез и чем тяжелее его осложнения, например амилоидозом, тем больше содержится в крови связанных с белками гек-соз, гексозаминов, серомукоидов и сиаловой кислоты. По мере затихания болезни протеинограмма постепенно приходит к норме, но медленнее, чем ускоренная РОЭ. Вместе с тем содержание глобулинов и гликопротеидов оказывается нередко повышенным в ранней фазе процесса. По данным Р. А. Иоффе (1962), из 119 больных различными формами туберкулеза легких у 65 при нормальных показателях РОЭ отмечались те или иные сдвиги в белковых фракциях сыворотки крови, главным образом в содержани альбуминов, глобулинов.
В связи с этим исследование белкового профиля важно при определении активности и динамики процесса, а также при оценке эффективности лечения. Оно играет меньшую роль в дифференциальной диагностике туберкулеза и других воспалительных или опухолевых заболеваниях легких, так как и при них имеют место подобные нарушепия белкового состава крови. Тем не менее при некоторых состояниях этот биохимический показатель приобретает известное значение, например в тех случаях, когда туберкулез напоминает по своей клинико-рентгенологической картине рак, саркоидоз, легочные проявления коллагенозов, при которых диспро-теинемия часто имеет более выраженный и своеобразный характер.
Тот же вывод следует сделать, оценивая результаты исследования содержания фибриногена в крови при различных заболеваниях органов дыхания. Как показали наблюдения Л. Н. Бирнбауэр (1965), проведенные в нашей клинике, его уровень обычно находится в пределах нормы при очаговом, инфильтративном и диссеминированном туберкулезе в фазе рассасывания и уплотнения или при стабильных туберкуломах. Он повышается при выраженных инфильтративных и деструктивных изменениях. Концентрация фибриногена, как и других белковых компонентов, повышается при раке, абсцессе, злокачественных опухолях средостения, но не претерпевает существенных сдвигов при саркоидозе, гамартохондроме, ненагноившихся кистах и т. д. Учет этих данных, конечно, в сочетании с основпыми клинико-рентгенологическими признаками важен при дифференциальной диагностике указанных заболеваний.
Из других показателей белкового обмена заслуживают внимания данные о составе свободных и, в частности, незаменимых аминокислот в сыворотке кроЕи. При активных формах туберкулеза легких часто уменьшается содержание цистеина, цистина, орнитина, валина, аргинина, гистидина и т. д. Эти сдвиги нарастают по мере утяжеления болезни и, наоборот, устраняются при ее затихании.
В то же время при изучении экскреции аминокислот с мочой у больных с эволютивными формами туберкулеза отмечается обратное соотношение: повышается суммарное содержание аминокислот и отдельных из заменимых (аспарагиновая кислота, серии, цистеин) и незаменимых ингредиентов (гистидин, аланин, тирозин, треонин, глутаминовая кислота и др.). Эти показатели в той или иной степени также нормализуются при благоприятном течении болезни. Характерно, что у больных саркоидозом органов дыхания даже при II и III стадиях, как показали наши наблюдения, существенные отклонения в аминокислотном составе крови не отмечаются.
Приведенные данные свидетельствуют, таким образом, о целесообразности изучения состояния белкового обмена при туберкулезе, что важно как в прогностическом, так и в диагностическом отношении.
Существенную роль в оценке функционального состояния и органических повреждений печени при туберкулезе и его осложнениях приобретают, как указывалось раньше, биохимические тесты: определение содержания в крови билирубина, альдолазы и активности аминотрансфераз, выделения конго красного, бромсульфалеина, исследование уровня сахара в крови после нагрузки глюкозой или галактозой.
Для выявления нарушений функции почек важно определение содержания остаточного азота в крови, мочевины, креатинина, индикана и т. д. О состоянии коры надпочечников можно судить по содержанию 17-кетостероидов в моче, а также свободных и белковосвязанных 11-оксикортикостероидов. Ценными являются сведения о нарушении обмена некоторых витаминов (тиамин, рибофлавин, пиридоксин, никотиновая кислота и др.), на уровень которых влияют не только туберкулезная интоксикация, но и различные химиопрепараты.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Состояние, когда нейтрофилы понижены, а лимфоциты повышены — лабораторно-диагностический критерий совершенно различных патологических состояний: от острого воспаления до новообразований или туберкулеза. Эти клетки являются разными видами лейкоцитов и выполняют в организме важные функции, защищая его от болезней. Каждые – свою. Чтобы оценить количество всех видов белых клеток, проводят расширенный клинический анализ крови. В его результате указывают общий уровень лейкоцитов и содержание каждой фракции. Определяется т.н.з. лейкоцитарная формула.

Лейкоциты реагируют не на конкретный вид раздражителя, а на сам факт присутствия в организме чужеродных агентов.
Иммунной активностью обладают все клетки лейкоцитарного ряда, но наиболее действенными и функциональными являются нейтрофилы и лимфоциты.
- Нейтрофилы месте с другими клетками-фагоцитами, особыми белковыми соединениями и защитными барьерами тела обеспечивают неспецифическую иммунную защиту. Они активизируются при внедрении микробов в организм, устремляются в очаг поражения, идентифицируют, поглощают и переваривают бактерии, продукты их жизнедеятельности, погибшие и нежизнеспособные клетки. Нейтрофилы продуцируют факторы агрессии, разрушающие микроорганизмы. Жизненный цикл клеток составляет 3-5 дней. Они погибают путем апоптоза — контролируемого физиологического процесса самоуничтожения. Обновление проходит непрерывно. Это позволяет организму ставить настоящий барьер на пути чужеродных агентов. Когда гранулоциты разрушаются, выделяются активные молекулы с выраженной противогрибковой и антибактериальной активностью. Они оказывают антимикробное воздействие, повреждая оболочки и мембраны патогенов. Нейтрофилы практически не участвуют в борьбе с опухолевыми клетками и паразитами.
- B- и Т-лимфоциты обеспечивают клеточную и гуморальную защиту. Они борются с вирусами и грибками, нейтрализуют токсины и продукты распада вредоносных микробов, уничтожают атипичные клетки и структуры с внутриклеточными бактериями. B – лимфоциты дают сигнал остальным иммунокомпетентным клеткам усилить или замедлить свою работу. Лимфоциты распознают антигенные детерминанты на поверхности инфицированных клеток, взаимодействуют с ними, превращаются в плазмоциты и активно продуцируют антитела. Их клеточная жизнедеятельность высока – до 5 лет. Количество лимфоцитов в крови у ребенка намного больше, чем у взрослого. С возрастом концентрация этих клеток постепенно снижается. У мужчин и женщин нет никакой разницы в показателях. При беременности лимфоциты всегда ниже своей нормы.
В ликвидации инфекционно-воспалительных, онкологических, аллергических заболеваний принимают участие и другие типы лейкоцитарных клеток: базофилы, моноциты, эозинофилы. Дисбаланс лейкоцитов возникает под влиянием внешних и внутренних факторов. Низкий уровень нейтрофилов и высокая концентрация лимфоцитов — признак патологии в организме человека. Какой – разберемся далее.
Снижение нейтрофилов – нейтропения
Нейтропения — пониженная концентрация собственнно нейтрофилов и прочих гранулоцитов в крови. Она бывает физиологической и патологической. Физиологическая нейтропения возникает при чрезмерном физическом перенапряжении, во время беременности, после еды или стресса. Подобное состояние обусловлено воздействием различных экзогенных факторов:
- радиационного излучения,
- токсических веществ – ядов и химикатов,
- некоторых лекарств — антибиотиков, иммуносупрессоров, гормонов, цитостатиков.
Физиологическая нейтропения не представляет угрозы для жизни человека и проходит самостоятельно после устранения провоцирующего влияния.

Причиной патологической формы всегда является заболевание. Такая нейтропения требует дополнительного обследования, позволяющего выявить причину нарушения.
Заболевания, при которых понижается уровень нейтрофилов в крови:
- вирусные инфекции — ОРВИ, ветряная оспа, гепатит, краснуха, корь, ВИЧ;
- генерализованное грибковое поражение;
- хроническое воспаление;
- лучевая болезнь;
- гематологические расстройства — агранулоцитоз, анемия;
- наследственные формы циклической и тяжелой врожденной нейтропении;
- гельминтозы и паразитозы;
- злокачественные опухоли костного мозга;
- аллергические реакции – анафилактический шок.
В результате этих патологий костный мозг продуцирует меньшее количество нейтрофилов. Длительно текущий воспалительный процесс истощает организм человека и нарушает его функции. Клетки крови активно погибают, нейтрофильный ряд не успевает восполняться новыми формами. Некоторые лекарственные препараты оказывают прямое угнетающее воздействие на миелопоэз – процесс образования нейтрофилов.
Нейтропения — полиэтиологическое состояние. При постановке диагноза данный показатель редко оценивают изолированно. В гемограмме ключевую роль играет соотношение различных лейкоцитарных фракций.
Таблица: сочетание различных лейкоцитов в норме

Повышение лимфоцитов – лимфоцитоз
Лимфоцитоз – состояние, при котором абсолютное количество лимфоцитов в крови превышает 3,6х10 9 . Уровень нейтрофилов при этом бывает пониженным, а моноцитов повышенным.
Лимфоциты выполняют защитную функцию, уничтожая вирусы, атипичные клетки, патогенные грибки. Когда организм атакуют эти чужеродные агенты, возникает лимфоцитоз. Существуют и иные процессы, при которых в крови повышается концентрация данных иммунных клеток. Повышенный уровень лимфоцитов свидетельствует о начале воспаления в организме. Врач, анализируя сопутствующие проявления, определяет место расположения очага поражения.
Патологии, при которых увеличивается концентрация лимфоцитов в крови:
- вирусные инфекции — ветрянка, корь и краснуха у ребенка, грипп и ОРВИ у взрослого;
- инфекционный мононуклеоз;
- специфическая бактериальная инфекция — туберкулез, сифилис, бруцеллез, дифтерия;
- острый и хронический лимфолейкоз;
- лимфосаркома;
- гипертиреоз;
- аутоиммунные расстройства.
Эти заболевания проявляются лимфоцитозом и нейтропенией. В результате гиперплазии лимфоидной ткани происходит гиперсекреция лимфоцитов, которые усиленно поступают в кровь. Это наблюдается при хронизации процесса, длительном рецидивирующем течении заболевания и при стихании воспаления.
Лимфоцитоз с повышением нейтрофилов наблюдается при гнойном воспалении – сепсисе, перитоните, ангине, пиелонефрите; некротических процессах – инсульте, обморожении, гангрене, обширных ожогах; интоксикации свинцом или спиртом; онкопатологии.
Лимфоцитоз иногда наблюдается у абсолютно здоровых людей. Физиологическая форма возникает при:
- беременности,
- менструации,
- нерациональном питании,
- длительном голодании,
- злоупотреблении алкоголем,
- курении,
- высокой двигательной активности,
- тяжелой работе,
- хронических стрессах,
- общем истощении,
- нарушении правил сдачи крови.
Повышенное содержание лимфоцитов в крови считается временным явлением. Лимфоцитоз возникает после любой операции. Он всегда обнаруживается у лиц, перенесших спленэктомию.
Пониженные нейтрофилы и повышенные лимфоциты одновременно
Лейкоцитарная формула имеет важное значение при постановке диагноза. Именно в лейкограмме чаще всего происходят изменения. При этом общее количество лейкоцитов остается нормальным.
- Вирусные инфекции характеризуются повышением лимфоцитов и понижением нейтрофилов. Абсолютный уровень лейкоцитов в крови не выходит за пределы нормы. Подобные данные лейкограммы указывают на активную борьбу организма с вирусами. Их часто получают на стадии инкубации, когда симптомов заболевания нет, а микробы уже проникли в организм и начали свою жизнедеятельность. Нейтропения и лимфоцитоз наблюдаются у лиц, недавно перенесших ОРВИ. Лимфоциты мигрируют в очаг воспаления, размножаются и дифференцируются для осуществления надежной противомикробной защиты. Необходимо определенное время для нормализации показателей крови. Когда наступает выздоровление, концентрация лейкоцитов восстанавливается.
- Онкологические заболевания характеризуются дисбалансом иммунных клеток, которые образуются и созревают в костном мозге. Опухоли органа нарушают его работу. При этом повышается уровень лимфоцитов и снижается количество нейтрофилов в крови. Апластическия анемия проявляется бледностью, бессилием, головокружение, кровоточивостью. При отсутствии своевременной диагностики и адекватного лечения заболевание переходит в лейкоз. К самым распространенным онкогематологическим болезням относятся хронический лимфоцитарный лейкоз и неходжкинская лимфома. В-лимфоциты скапливаются в костном мозге, лимфоузлах, печени. Эти онкопатологии отличаются медленным течением и специфической симптоматикой.
- Нейтропения с лимфоцитозом наблюдаются и при аллергических реакциях. Такие результаты исследования позволяют докторам определить наличие склонности к аллергии. При этом вместе с лимфоцитами также повышены эозинофилы.
- Много лимфоцитов в крови обнаруживают не только при респираторных инфекциях, но и при туберкулезе, бруцеллезе, брюшном тифе, системной красной волчанке, лимфогранулематозе, почечной патологии.
- Гнойно-деструктивные и сосудистые заболевания также требуют проведения гемотеста, с помощью которого обнаруживают лимфоцитоз и нейтропению. К ним относятся: абсцессы, флегмоны, фурункулы, гангрена, инфаркт, инсульт.
Пониженные нейтрофилы и повышенные лимфоциты в крови — частый признак бактериальной или вирусной инфекции. Обширное заражение сопровождается выходом инфекционного агента в кровоток. Нейтрофилы после взаимодействия с возбудителем быстро погибают, а костный мозг не успевает их продуцировать в достаточном количестве. У больных возникает основные симптомы патологии: лихорадка, озноб, вялость, учащенное сердцебиение, гипергидроз, тахипноэ, гипотензия. При появление признаков интоксикационного синдрома необходимо сразу же обратиться к врачу. Чтобы поставить правильный диагноз и не допустить ошибки, необходимо оценивать количественные показатели клеток крови не изолированно, а в общей совокупности.
У детей пониженные нейтрофилы и повышенные лимфоциты являются вариантом нормы. Подобный перекрест обусловлен не полностью сформированной иммунной системой. Частая причина отклонения – вакцинация. В ответ на чужеродное внедрение организм реагирует выработкой антител — лимфоцитов. При этом гранулоциты не продуцируются в полном объеме.
Диагностика
Лимфоциты и нейтрофилы — клетки крови, выполняющие жизненно важные функции и способные многое сказать о состоянии пациента. Чтобы не пропустить развития серьезных заболеваний, необходимо ежегодно сдавать общий анализ крови. Лейкоциты определяются по специальным стандартным нормативам. Выявленное несоответствие характеризует высокую активность кровяных телец и сигнализирует о начале развития патологических процессов. По результатам исследования можно обнаружить даже скрытые, бессимптомно протекающие, заболевания.

Для анализа необходима капиллярная кровь больного. Сдают ее утром, строго натощак, исключив за несколько дней курение и алкоголь. О приеме жизненно необходимых лекарств следует заранее сообщить лечащему врачу. Пациент перед сбором материала должен быть максимально спокойным в физическом и психологическом отношении. Правильно расшифровать результаты исследования может только специалист. Все показатели гемотеста он оценивает в совокупности. Особого внимания заслуживает лейкоцитарная формула, отражающая соотношение отдельных видов лейкоцитов в процентах и числах. Лейкоцитарный расчет позволяет определить количество белых клеток крови в единице объема. Содержание одних фракций изменяется за счет повышения или понижения других.
Расширенный анализ крови с подсчетом лейкоцитарной формулы обязательно назначают пациентам с:
- острыми инфекционными и воспалительными заболеваниями,
- иммунодефицитными состояниями,
- частыми рецидивами бактериальных и грибковых инфекций,
- беременным женщинам.
Анализируя высокую или низкую долю лейкоцитов, доктор может заподозрить у больного редкое аутоиммунное расстройство, гематологическую болезнь, иммунодефицит. По лейкоцитарной формуле можно сделать вывод о развитии осложнений, о течении патологического процесса и прогнозе заболевания. С помощью результатов лейкограммы врачи дифференцируют вирусные и бактериальные инфекции.
- Вирусное поражение характеризуется повышением лимфоцитов и снижение нейтрофилов.
- Инфекционные заболевания, вызванные бактериями, проявляются сдвигом лейкоцитарной формулы влево — увеличением нейтрофильный лейкоцитов и относительно низким содержанием лимфоцитов.
Лабораторные показатели не позволяют поставить окончательный диагноз имеющейся патологии. Для этого необходимо провести более подробное обследование больного, включающее клинические признаки, анамнестические данные, инструментальные методы и целый перечень анализов биологического материала.
Чтобы определить причину нарушения, доктору необходимо выяснить:
- жалобы больного,
- объективные признаки,
- анамнез,
- наследственность.
Прием некоторых медикаментов может повлиять на количество в крови отдельных фракций лейкоцитов. К ним относятся антибиотики, антигистамины, диуретики, кортикостероиды, антикоагулянты, миорелаксанты. Необходимо сообщить врачу о проведенном лечении. Химиотерапия и радиационная терапия также вызывают повышение в крови доли белых телец. Продолжительное снижение нейтрофилов и повышение лимфоцитов требуют дополнительных обследований – крови на онкомаркеры, томографического, рентгенографического и ультразвукового исследований внутренних органов.
После получения результатов анализов и испытаний доктор ставит окончательный диагноз и составляет лечебный план.
Лечение
Нейтропения и лимфоцитоз — не отдельные заболевания, а симптомы острого или хронического воспалительного процесса. Эти отклонения непросто восстановить. После выяснения причин подобных изменений в гемограмме больным назначается и проводится комплексная терапия. Самолечение категорически запрещено. Оно может оказаться бесполезным и опасным для жизни. Лимфоцитоз при отсутствии сопутствующих симптомов и иных изменений в анализе крови не считается патологическим и не требует лечения. У детей первых лет жизни высокий уровень лимфоцитов и низкий нейтрофилов носит физиологический характер.
После проведения качественной этиотропной терапии показатели общего анализа крови постепенно приходят в норму. Чтобы предупредить повторное понижение нейтрофилов и повышение лимфоцитов, необходимо следить за своим здоровьем, вовремя посещать специалистов-медиков и не заниматься самолечением.
Читайте также:

