Преимущественная морфологическая форма пневмококковой пневмонии
Обновлено: 18.04.2024
Пневмония пневмококковая – это разновидность воспаления легких, встречающаяся чаще всего. Причиной этого заболевания становится Str. pneumoniae. Примерно 5-25% населения, совершенно здорового, – это переносчики пневмококка, по большей части, это касается детей.
Причины возникновения и патогенез заболевания
Пневмококк наиболее часто становится причиной воспаления большей части доли легкого, а также иногда всей доли. Но нередко пневмококк становится первопричиной возникновения очаговой пневмонии.
В медицинской литературе описаны четыре патологоанатомические фазы протекания долевой пневмококковой пневмонии.
1. Фаза прилива, микробного отека, покраснения. Ее характеризует значительное наполнение сосудов кровью, сильная экссудация серозной жидкости. В экссудате определяются пневмококки. Такая фаза длится 12-72 часа.
2. Фаза красного опеченения. Для нее характерно полное заполнение экссудатом альвеол той части легкого, которая поражена болезнью. Причем, в экссудате определяют белки плазмы (фибриноген), а, как следствие диапедеза, увеличено число эритроцитов. Участок легкого, в котором есть воспаление, безвоздушный, плотный, приобретает красноватую окраску и внешне походит на печень. Длительность этого периода 1-3 суток.
3. Фаза серого опеченения. В этой фазе в экссудате из альвеол определяют значительно больше лейкоцитов (по большей части это нейтрофилы), а вот эритроциты значительно уменьшаются в количестве. Легкое, как и раньше, плотное, серовато-желтое на разрезе, очень заметна зернистость легкого. В результате микроскопических анализов определяют увеличение нейтрофильных лейкоцитов и фагоцитированных пневмококков. Эта фаза длится 2-6 суток.
4. Фаза разрешения. В это время в альвеолах неуклонно рассасывается экссудат. Причина этого – воздействие макрофагов и лейкоцитов. Медленно происходит растворение фибрина, легочная ткань перестает быть зернистой. Со временем ткань легкого восстанавливает свою воздушность. Сколько продлится этот период, будет зависеть от того, насколько распространен воспалительный процесс, реактивности организма, а также способов терапии и оттого, насколько лечение интенсивно.
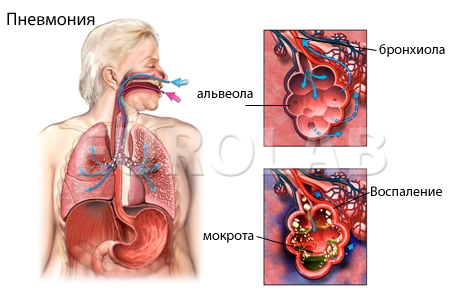
Проявления болезни
Постановка диагноза пневмококковая пневмония
Для долевой пневмококковой пневмонии характерны определенные физикальные проявления, которые прямо обусловлены патоморфологической фазой болезни.
При первой стадии накопления экссудата – это притупленный тимпанический звук выше очага воспаления, удлиненный выдох при жестком дыхании, несильная начальная крепитация. В некоторых случаях слышны оба типа хрипов: влажные и сухие. При второй стадии уплотнения (еще называемой опеченением) сильно увеличивается дрожание голоса, проявляется бронхофония. Во время проведения выстукивания слышится тупой звук, не слышно везикулярное дыхание, крепитации нет, часто слышен шум от трения плевры. На последней стадии неуклонно приходит в норму дрожание голоса, бронхофония прекращается, возникает redux крепитация – звучная, обильная и на большом протяжении). Кроме того, хрипы звучные мелкопузырчатые, а бронхиальное дыхание со временем переходит в жесткое, а потом в везикулярное. Но важно учитывать тот факт, что при пневмококковой пневмонии эти фазы могут не протекать в указанной последовательности, а в отдельных участках легких могут наблюдаться одновременно разные проявления. Если пневмококковая пневмония носит очаговый характер, симптомы намного меньше выражены. Так, в некоторых случаях слышится притупленный перкуторный звук выше очага поражения. А, как следствие сопутствующего очагового бронхита, слышны крепитация и мелкопузырчатые хрипы.
Данные рентгенологии
Во время стадии уплотнения или опеченения определяются самые яркие изменения в ткани легкого. При долевой пневмонии характерно весьма интенсивное затемнение доли легкого. Во время томографического исследования наблюдается воспалительная инфильтрация, а на ее фоне ясно видны бронхи. Этот симптом надежно разграничивает пневмонию и ателектаз легкого. Локальное уплотнение или очаговая тень выявляют очаговую пневмококковую пневмонию.
Лабораторные исследования
Самые явные и показательные изменения в результатах общего анализа крови. Чаще всего сильно проявляется лейкоцитоз – лейкоциты повышаются до 20-30х109/л, определяют, что уровень нейтрофилов намного выше нормы, лейкоцитарная формула очень сдвинута влево (до миелоцитов и промиелоцитов). Во время пика болезни пропадают эозинофилы, намного меньше нормы лимфоцитов и тромбоцитов. Когда приходит завершающая стадия, число лимфоцитов, эозинофилов и тромбоцитов приходит в норму. Очень показательно увеличение СОЭ. Биохимический анализ крови проявляет симптомы воспаления: несколько выше уровень а,- и у-глобулинов, серомукоида, сиаловых кислот, фибрина, гаптоглобина.
Критерии постановки диагноза
Диагноз пневмококковая пневмония ставится, если наличествуют нижеперечисленные признаки.
- Болезнь возникает весьма остро, чувствуется озноб; выражена лихорадка. Пациент испытывает грудные боли, задыхается, сильно кашляет.
- Показательные данные физикального исследования и рентгенологии легких.
- В препаратах мокроты, которые окрашены по Граму, наличествуют грамположительные ланцетовидные диплококки – они создают недлинные цепочки. При этом нужно выявить 10 и более диплококков или типичных пневмококков. Последним доказательством того, что выявленные стрептококки принадлежат к пневмококку является реакция набухания его капсулы. Такая реакция бывает, когда добавляют поливалентную пневмококковую антисыворотку.
- Нарастают титры противопневмококковых антител в парных сыворотках крови пациенте, которые брали в первый день болезни и на 10-14 день.
Терапия пневмококковой пневмонии
Если пневмония протекает легко, позволительно применять бактерицидные антибиотики перорально. Феноксиметилпенициллин, ампициллин (амоксициллин), цефалоспорины первого поколения. Если есть индивидуальная непереносимость вышеуказанных лекарств, назначают эритромицин, в некоторых случаях бисептол или его аналог гросептол. Допустима и терапия с назначением пенициллина. Если диагностирована средняя степень тяжести пневмонии или тяжелое протекание болезни, первостепенно назначение пенициллина. Препарат вводят внутримышечно, по 1-2 млн ЕД через 4 часа. В случае, когда пневмонию осложняют эмпиема плевры, абсцесс легкого, инфекционный эндокардитом, препараты не очень хорошо проникают в ткани. Тогда дозу пенициллина стоит увеличить в два раза. Сейчас признано много штаммов пневмококка, резистентных к пенициллину. Если имеем дело с таким случаем, нужно назначать цефалоспорины, имипенем, ванкомицин.
Средства против кашля
Средства от кашля прописывают пациентам с диагнозом острая пневмония с начала болезни. Чрезмерно кашель несет опасность возникновения пневмоторакса. Все средства от кашля относят к двум категориям: наркотические или ненаркотические. Применение противокашлевых препаратов наркотического характера моет привести к привыканию или к угнетению дыхательного центра. Рекомендованные препараты и дозы:
- Таблетки муколитические – состоят из кодеина 0.02 г; натрия гидрокарбоната 0.2 г; корня солодки 0.2 г; травы термопсиса 0.01 г.
- Кодеина фосфат – принимают 2 - 3 р/день по 0.1 г.
- Кодтерпин – таблетки, которые состоят из кодеина 0.015 г; натрия гидрокарбоната 0.25 г; терпингидрата 0.25 г.
- Метилформин (кодеин) – принимают 2 - 3 р/день по 0.015 г.
- Этилморфин (дионин) – прописывают в таблетках 2 - 3 р/день по 0.01 г.
Врачи считают, что применение ненаркотических препаратов от кашля предпочтительнее, поскольку не приводит к привыканию или к угнетению дыхательного центра. Рекомендованные препараты и дозы:
- Глауцина гидрохлорид – получают из травы мачека желтого, принимают в форме таблеток 2 - 3 р/день по 0.05 г.
- Ледин – произведен из травы багульник, вызывает подавление кашлевого центра, приводит к расширению бронхов, его прописывают в форме таблеток 3 р/день по 0.05 г.
- Битиодин – угнетает действие кашлевых рецепторов на слизистой оболочке дыхательных путей, а также кашлевой центр в продолговатом мозге. Применяют в форме таблеток 3 р/день по 0.01 г . – активное действие против кашля не уступает действию кодеина, он подавляет кашлевой центр в продолговатом мозге, принимают 3 или 4 р/день по 0.1 г .
- Тусупрекс – препарат подаквляет деятельность кашлевого центра, принимается в форме таблеток 3 р/день по 0.01-0.02.
Противовоспалительные препараты пациентам назначают, чтобы уменьшился воспалительный отек и улучшились микроциркуляции. Принимать при значительном повышении температуры тела – 39-40 °С, показаны ацетилсалициловая кислота или парацетамол 2 - 3 р/день по 0.5 г.
Если ярко выражены боли в плевре, целесообразно выписывать метиндол-ретард 1 - 2 р/день по 0.075 г, вольтарен 2 или 3 р/день по 0.025 г, а также иные нестероидные противовоспалительные препараты. Но не забывать, что они влияют на работу иммунной системы, уменьшая способность к фагоцитозу. Поэтому во время острой фазы их применяют короткое время. Если сильны боли в грудной клетке, пациенту рекомендуют принимать анальгин.
Сердечно-сосудистые препараты
- Камфорное масло – важное средство, необходимое в случае острой пневмонии. Камфара тонизирует сердечно-сосудистую и дыхательную системы, усиливает сокращение миокарда, производит отхаркивающий эффект. Препарат оказывает сильное бактерицидное действие. В литературе говорится о свойстве камфары улучшать вентилирование альвеол. Камфара показана к применению, если у пациента пневмония протекает тяжело. Рекомендовано подкожно 3 - 4 р/день по 2-4 мл. Но может иметь побочный эффект – возникновение инфильтратов. – препарат, получаемый соединением сульфокамфорной кислоты с новокаином. 1%-ый раствор вводят внутримышечно, подкожно или внутривенно 2 или 3 раза/день. Достоинством препарата является то, что он имеет важные терапевтические свойства камфары, но не приводит к возникновению инфильтратов. – 25%-ый раствор диэтиламида никотиновой кислоты. Оказывает стимулирующее действие на дыхательный и сосудодвигательный центры. Показан 3 раза/день подкожно, внутримышечно и внутривенно по 2-4 мл, если у пациента диагностировали выраженную артериальную гипотензию или крупозную пневмонию.
Все эти препараты нормализуют движение крови в малом круге кровообращения.
Если очень снижается способность левого желудочка сокращаться, можно рекомендовать сердечные гликозиды, но учитывая чувствительность воспаленного миокарда. Вводить капельно небольшие дозы внутривенно.
ФГБУ "Санкт-Петербургский научно-исследовательский институт фтизиопульмонологии";
Медицинский факультет Санкт-Петербургского университета
Иркутская городская клиническая больница
Пневмококковая (крупозная) пневмония: клинико-морфологические особенности
Журнал: Архив патологии. 2013;75(3): 22‑30
Цинзерлинг В.А., Свистунов В.В. Пневмококковая (крупозная) пневмония: клинико-морфологические особенности. Архив патологии. 2013;75(3):22‑30.
Tsinzerling VA, Svistunov VV. Pneumococcal lobar (croupose) pneumonias: clinical and morphological characteristics. Arkhiv Patologii. 2013;75(3):22‑30. (In Russ.).
ФГБУ "Санкт-Петербургский научно-исследовательский институт фтизиопульмонологии";
Медицинский факультет Санкт-Петербургского университета
Приведены данные о частоте пневмококковых пневмоний, летальности от них и современные представления о свойствах пневмококка. На основании анализа аутопсийного материала по Иркутску и Санкт-Петербургу сделан вывод о том, что крупозная пневмококковая пневмония остается распространенным заболеванием. Летальный исход чаще происходит в первые сутки, высока доля расхождений клинического и патологоанатомического диагнозов. Важнейшими факторами риска являются охлаждение и алкогольная интоксикация. Пневмококк является практически единственным этиологическим фактором крупозной пневмонии даже в тех случаях, когда его не высевают. Среди осложнений важное значение имеют гнойный менингит и менингоэнцефалит, лейкопения. В целом подтверждены представления В.Д. Цинзерлинга о морфогенезе крупозной пневмонии. Показана возможность развития трех вариантов серого опеченения в зависимости от соотношения нейтрофильных лейкоцитов и фибрина. Выявлены частота и клиническая значимость поражений миокарда, почек и других органов.
ФГБУ "Санкт-Петербургский научно-исследовательский институт фтизиопульмонологии";
Медицинский факультет Санкт-Петербургского университета
Иркутская городская клиническая больница
В России, по данным О.В. Зайратьянца и соавт. [3], от острых пневмоний ежегодно умирают около 3000 человек, что составляет 20,1 на 100 000 населения. В Иркутске в 2007 г. смертность от острых пневмоний составила 51, а общая летальность от острых пневмоний — 10,3% [4]. По данным Департамента здравоохранения и социальной помощи населению администрации Иркутска, продолжался неуклонный рост смертности от пневмоний, которая к 2011 г. достигла 59. Среди умерших от заболеваний органов дыхания, по данным вскрытий, КП уверенно занимает 1-е место, составляя на протяжении многих лет в среднем 3—4,5% общего числа аутопсий. По данным В.Д. Цинзерлинга [5, 6], летальность от КП составляла 12—31%. Резкое сокращение числа умерших от этого заболевания отмечалось в 1950—60-е годы, что напрямую связывалось с внедрением в практику антибактериальных препаратов [7]. В 1980—90-е годы появились данные об увеличении числа умерших от КП [8, 9].
Тяжелую интоксикацию, с которой протекает заболевание, объясняют большим числом медиаторов воспаления и цитокинов, продуцируемых в ходе заболевания как ПК, так и самим организмом. После перенесенного заболевания иммунитет становится типоспецифическим и сохраняется в течение 6—12 мес. В настоящее время проводятся исследования по получению оптимальной вакцины.
Зарубежные исследования, посвященные патогенезу ПКИ, довольно многочисленны и проводятся с использованием современных молекулярно-биологических методов исключительно на экспериментальном материале. Показано, что ряд факторов, определяющих особенности макроорганизма, влияет на тяжесть ПКИ. Установлено, что генетическая вариабельность генов TLR2, TLR3, CD14, Fc-gamma RIIA повышает риск развития инвазивного заболевания у инфицированных больных [15]. Выявлено, что выраженное протективное действие против ПК оказывает Il1-β, уровень которого, по крайней мере у мышей, сильно варьирует [16]. Также было показано существенное влияние на течение заболевания галектина-3, члена семейства β-галактозидсвязывающего лектина, который продуцируется альвеолярными макрофагами [17].
Определенную клиническую значимость имеют и результаты исследования in vitro, проведенного J. Wang и соавт. [18], в котором доказано, что морфин резко снижает функции альвеолярных макрофагов в отношении ПК.
Во всех современных источниках показано, что наиболее тяжелое течение ПКИ приобретают у лиц из групп риска. Чаще всего к ним относят детей раннего возраста, стариков, лиц с иммунодефицитом (в том числе СПИДом), а также перенесших вирусные респираторные инфекции. Обычно указывается на преобладание летальных исходов в зимние месяцы. R. Dagan и соавт. [19] опубликовали данные о преобладании числа заболевших КП в социальных группах с низкими материальными доходами. В некоторых источниках [1, 10, 20, 21] особое внимание уделяется бедности, алкоголизму и принадлежности к ряду этнических групп (афроамериканцам, индейцам).
В ряде отечественных источников без ссылок на фактические данные приводятся сведения о полиэтиологичности КП [10]. При этом в качестве возможных, хотя и редких, возбудителей рассматривают стрептококки, кишечную палочку и др. Следует отметить, что В.Д. Цинзерлинг настаивал на выделении только двух этиологических вариантов долевой пневмонии — пневмококковой и довольно редкой клебсиеллезной (так называемой фридлендеровской пневмонии).
Изменения других органов при КП в литературе практически не описаны, кроме общих указаний на возможность дистрофических изменений. Современных зарубежных публикаций, включающих морфологическую характеристику пневмококковых пневмоний, нет. Встречаются только обзоры экспериментальных моделей [11] преимущественно в целях оценки эффективности разных вариантов лечения.
Все изложенное послужило основанием для проведения настоящего исследования летальных исходов от КП с анализом как клинико-эпидемиологических, так и патологоанатомических данных.
Материал и методы
Нами проведен углубленный клинико-морфологический анализ КП по материалам аутопсий по Иркутску за 1999—2011 гг. В ходе детального вскрытия умерших от КП проводили взвешивание органов и микроскопическое исследование материала. Брали материал для бактериологического, бактериоскопического и гистобактериоскопического исследований. Мазки-отпечатки окрашивали метиленовым синим и по Граму. Окрашивание флоры в срезах проводили азуром и эозином. Учитывали клинические и анамнестические сведения.
Цифровой материал обрабатывали методом вариационной статистики с применением критериев достоверности Стьюдента. В ходе исследования использовали материалы отдела статистики Департамента здравоохранения и социальной помощи населению администрации Иркутска [4].
Кроме того, нами проанализированы результаты патологоанатомических вскрытий, проведенных в Санкт-Петербурге в 2011 г. [26]. Для более детальной характеристики КП у умерших в Санкт-Петербурге проведен анализ отчетов патологоанатомического отделения (ПАО) Клинической инфекционной больницы (КИБ) им. С.П. Боткина за 1993—2007 гг. Данная крупная прозектура была взята для анализа в связи с возможностью получения полных достоверных сведений, включая результаты посмертных бактериологических исследований в период, когда в больнице отмечалась очень высокая (до 98%) доля патологоанатомических вскрытий.
Результаты
Общее число аутопсий в Иркутске за этот период составило 9478 случаев, из них умерших от КП было 315 (3,3% общего числа аутопсий). Углубленно проанализированы 152 случая. Мужчины составили 78,3% умерших, женщины — 21,7%, общее число умерших до 60 лет — 61,1%. На весенне-летний период пришлось 58,5% наблюдений, что может быть связано с купанием в холодной воде Байкала. Злоупотребление алкоголем зафиксировано в медицинской документации в 70% случаев. Косвенным морфологическим подтверждением данных анамнеза о злоупотреблении алкоголя явилось обнаружение тотального и крупноочагового жирового гепатоза, который установлен более чем в 80% наблюдений. Связь между эпидемическими периодами по гриппу, острым респираторным вирусным инфекциям и частотой летальных исходов от КП не установлена.
Согласно данным патологоанатомической службы Санкт-Петербурга [26], в 2011 г. в городе от болезней умерли 57 496 человек, из которых патологоанатомами были вскрыты 19 515, судебно-медицинскими экспертами — 16 393 человек. Диагноз КП был поставлен патологоанатомами в 180 случаях, расхождение клинического и патологоанатомического диагноза в стационарах установлено в 13,1% случаев. Подробных сведений о результатах при проведении судебно-медицинских исследований нет.
В ПАО КИБ им. С.П. Боткина за 1993—2007 гг. были вскрыты 269 умерших от КП. Число вскрытий с этим диагнозом существенно варьировало (от 7 случаев в 1996 г. до 33 в 1993 г.) и составляло 3,7—6% от секционного материала больницы. Среди умерших преобладали мужчины (208 человек, 77,3%). Сведения о хроническом алкоголизме имелись в 227 (84,4%) картах стационарного больного.
В половине случаев смерть наступила в первые сутки.
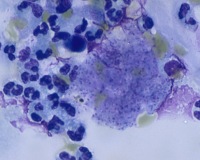
Проведен анализ 152 случаев КП в Иркутске. Высеваемость ПК составила 24%. В то же время при развернутой клинико-морфологической картине КП в 22 (17,9%) случаях флоры при бактериологическом исследовании не выявлено. При бактериоскопическом исследовании во всех случаях обнаружен грамположительный ланцетовидный диплококк, хотя поиск его в ряде случаев был затруднен. Ни в одном из наблюдений прижизненного исследования мокроты на определение микрофлоры не проводилось.
Специально проанализированы 97 случаев с полными клинико-анамнестическими данными. Во всех наблюдениях имелось внезапное начало, фебрильная температура отмечена в 95 случаях. Сосудистая (сердечно-сосудистая) недостаточность клинически выявлена в 87,5% наблюдениях. Летальность в первые сутки составила 55,3%. К 3-м суткам доля умерших составила 79%. В 1-ю неделю КП стала причиной смерти 90,1% пациентов.
В 89,4% случаев КП была долевой, в 15,1% — сублобарной. В 61,2% наблюдений отмечено одностороннее поражение, а в остальных — двустороннее. При одностороннем характере чаще поражалось правое легкое (в 47,7% случаев). Поражение одной доли имело место в 16,4% наблюдений, в остальных случаях поражались несколько долей, а в 13,8% наблюдений КП была тотальной. Отмечено существенное увеличение массы легких, которая при долевых пневмониях превышала 1 кг, при двусторонних составляла около 3 кг, в отдельных случаях достигала 4 кг.
При микроскопическом исследовании установлено несколько вариантов морфологических изменений.
При микробном отеке (1-й тип) наблюдается выраженная гиперемия капилляров, просветы альвеол расширены, заполнены серозной жидкостью, встречаются единичные эритроциты, лейкоциты. При окраске азуром определяется большое количество ланцетовидных диплококков (см. рис. 1, в,г).
Все варианты характеризовались малым или полным отсутствием поражений бронхов.
В 21,7% наблюдений отмечено поражение сосудов в виде флебитов с инфильтрацией стенки сосудов лейкоцитами, в ряде случаев в их просветах визуализировались тромбы. Встречались очаговые некрозы паренхимы, экссудат приобретал гнойный характер (см. рис. 2, в).
КП с абсцедированием отмечена в 30,9% наблюдений. В альвеолах преобладал лейкоцитарный экссудат, фибрин сохранялся в виде мелких депозитов или отсутствовал. Стенки межальвеолярных перегородок были разрушены, видны формирующиеся абсцессы с невыраженной капсулой, гиперемия не наблюдалась (см. рис. 2, г).
Во всех случаях при бактериологическом исследовании высевалась смешанная микробиота, иногда в комбинации с пневмококком.

Следует отметить, что в большинстве наблюдений разная цветовая характеристика и разнообразные микроскопические изменения встречались в одном и том же случае, в кусочках, взятых из разных отделов пораженного легкого, а при двусторонних поражениях — из разных долей. Данные о частоте выявленных нами структурных изменений в зависимости от сроков заболевания представлены в табл. 1. Всего при исследовании 110 случаев, в которых была известна длительность заболевания, установлено 417 типов изменений (в среднем 3,8 варианта морфологической картины на 1 случай).
В табл. 2 представлены сведения о наблюдавшихся нами легочных и внелегочных осложнениях. Среди легочных осложнений отмечена типичная карнификация (см. рис. 2, д). По данным В.Д. Цинзерлинга [5], осложнения в виде менингита имелись в 6% случаев, в нашем исследовании — в 11,2% (рис. 3, а—в). Рисунок 3. Внелегочные поражения при КП. а — вентрикулит с кровоизлиянием в сосудистое сплетение; б — гнойный васкулит сосудов головного мозга; в — гнойный менингит; г — резкое полнокровие сосудов, очаговые кровоизлияния и миоцитолиз в миокарде; д — макроскопические изменения почек: сероватый оттенок расширенного коркового слоя, красно-синюшные пирамидки с подчеркнутыми границами; е — микроскопические изменения почек: малокровие коры, некробиотические изменения нефротелия извитых канальцев; а, б, в, г, е — окраска гематоксилином и эозином. ×100. Гнойные менингиты и менингоэнцефалиты, по материалам КИБ им. С.П. Боткина в Санкт-Петербурге, диагностированы в 25,3% наблюдений. Во многих источниках литературы о них не упоминается. Сведений о частоте других осложнений в литературе мы не встретили.
В 33,5% случаев выявлены изменения миокарда (см. рис. 3, г): микроскопическая картина острой коронарной недостаточности — в 25,6% наблюдений, микроскопическая картина, сходная с ранним инфарктом миокарда, — в 7,9%. В 82% случаев эти изменения были обнаружены у лиц моложе 45 лет при отсутствии атеросклеротических изменений в коронарных артериях.
Бифуркационные лимфатические узлы были резко увеличены в размерах, иногда образуя пакет, темно-серого цвета с красным оттенком. Микроскопически отмечались выраженное полнокровие, кровоизлияния. Краевые синусы были расширены и содержали серозный экссудат.
В надпочечниках (помимо 7 случаев массивных кровоизлияний) отмечались расстройства кровообращения разной степени (от полнокровия до мелких геморрагий).
Бактериологически и бактериоскопически в лимфатических узлах, миокарде, почках и надпочечниках микробиота не обнаруживалась.
Случаев течения заболевания по типу генерализованной ПКИ с проявлениями ДВС-синдрома не выявлено.
В 11,2% наблюдениий в Иркутске и в 3,3% наблюдений в Санкт-Петербурге (особенно в последние годы) в крови отмечалась лейкопения вплоть до агранулоцитоза, расшифровать природу которого не представилось возможным.
Клинико-лабораторные и морфологические признаки вирусных респираторных инфекций и ВИЧ-инфекции документированы в обоих городах в небольшом числе наблюдений.
Представленные сведения и анализ данных литературы свидетельствуют о целесообразности выделения среди внебольничных пневмоний КП, имеющей ряд характерных черт, несмотря на то, что она не указана в Международной классификации болезней 10-го пересмотра. Частота этого заболевания, нередкие ошибки в клинической диагностике и высокая летальность свидетельствуют о необходимости большего внимания к КП со стороны специалистов разных профилей, особенно в России.
Этиология заболевания связана с ПК, в том числе в тех наблюдениях, в которых не высевали данного возбудителя. В пользу этого однозначно свидетельствуют результаты бактериоскопического и гистобактериоскопического исследований. При сочетанных поражениях отрицательный результат мог быть связан с подавлением ПК другой микробиотой. Отрицательные результаты в ряде случаев можно объяснить антибактериальной терапией. Кроме того, следует помнить об уникальной способности ПК к аутолизу.
Основываясь как на собственных фактических материалах, так и на данных современной литературы, можно полностью подтвердить взгляды В.Д. Цинзерлинга на пато- и морфогенез долевой и сублобарной пневмококковой КП. Заболевание начинается с проникновения ПК в нижние отделы респираторного тракта. Этому способствуют дополнительные факторы, важнейшие из которых — охлаждение и алкогольное опьянение, вирусные респираторные инфекции являются факультативным фактором. Весьма вероятна роль особой вирулентности штамма ПК. В просветах альвеол формируется очаг серозного воспаления, который по порам Кона начинает быстро распространяться и за короткий период может охватить всю долю. Под воздействием аутолизина происходит распад ПК с выделением большого количества медиаторов воспаления и цитокинов, обеспечивающих системный воспалительный ответ с яркими клиническими проявлениями (лихорадкой, ознобом и др.) Гиалуронидаза и нейраминидаза, способные разрушать основное вещество соединительной ткани, обеспечивают адгезию и колонизацию ПК на первых этапах. Пневмолизин, высвобождающийся при распаде ПК, оказывает прямое токсическое действие на капилляры, резко увеличивая их проницаемость. Аналогичным действием обладают продукты распада капсульного вещества. Среди них — производные пептидогликана, оказывающие мембранолитическое действие на альвеолы и эндотелий капилляров, а также перекись водорода, которая также резко повышает проницаемость сосудистой стенки. При этом сосудистая стенка может пропускать не только фибрин, но и эритроциты. Пневмолизин также оказывает и выраженное хемотаксическое действие на лейкоциты и моноциты. Такой механизм объясняет быстроту и выраженность сосудистых реакций, а также выход фибрина и эритроцитов в альвеолярные пространства. Именно скорость распространения и захват больших пространств легочной паренхимы в короткие сроки явились ключевыми факторами для включения в патогенез этого заболевания аллергических механизмов [22, 24]. N. Engleberg и соавт. [1] подчеркивают, что КП нельзя рассматривать как заболевание, в основе которого лежат аллергические механизмы. Предшествующая сенсибилизация, напротив, способствует быстрому распознаванию ПК, что и обеспечивает более эффективный фагоцитоз. В настоящее время можно выделить 5 вариантов экссудативной реакции, следующей за серозным отеком. Достоверно судить о причинах развития тех или иных изменений не представляется возможным. Отсутствует строгая зависимость между длительностью заболевания и определенной морфологической картиной. В некоторых случаях воспалительный процесс захватывает не всю, но бóльшую часть доли. Результаты проведенного нами клинико-морфологического анализа свидетельствуют о принципиальном сходстве долевых и сублобарных КП.
Среди легочных и внелегочных осложнений КП наиболее важными являются изменения в миокарде, встретившиеся в 33,5% случаев, которые могут иметь решающее значение в танатогенезе и являться непосредственной причиной смерти. Причины изменений в сердечной мышце, вероятно, связаны с циркуляцией в крови большого числа медиаторов воспаления и цитокинов, продуцируемых как самим ПК, так и макроорганизмом. В клинической практике могут иметь значение изменения, обнаруженные в почках у 42,8% умерших. Обнаруженная морфологическая картина острой почечной недостаточности коррелировала с клиническими проявлениями в виде олигоурии и азотемии, выявленных при жизни у 21% пациентов. Важное значение имеют и вторичные пневмококковые гнойные менингиты и менингоэнцефалиты, частота которых может достигать 25,3%.
ФГБУ "Санкт-Петербургский научно-исследовательский институт фтизиопульмонологии";
Медицинский факультет Санкт-Петербургского университета
Иркутская городская клиническая больница
Пневмококковая (крупозная) пневмония: клинико-морфологические особенности
Журнал: Архив патологии. 2013;75(3): 22‑30
Цинзерлинг В.А., Свистунов В.В. Пневмококковая (крупозная) пневмония: клинико-морфологические особенности. Архив патологии. 2013;75(3):22‑30.
Tsinzerling VA, Svistunov VV. Pneumococcal lobar (croupose) pneumonias: clinical and morphological characteristics. Arkhiv Patologii. 2013;75(3):22‑30. (In Russ.).
ФГБУ "Санкт-Петербургский научно-исследовательский институт фтизиопульмонологии";
Медицинский факультет Санкт-Петербургского университета
Приведены данные о частоте пневмококковых пневмоний, летальности от них и современные представления о свойствах пневмококка. На основании анализа аутопсийного материала по Иркутску и Санкт-Петербургу сделан вывод о том, что крупозная пневмококковая пневмония остается распространенным заболеванием. Летальный исход чаще происходит в первые сутки, высока доля расхождений клинического и патологоанатомического диагнозов. Важнейшими факторами риска являются охлаждение и алкогольная интоксикация. Пневмококк является практически единственным этиологическим фактором крупозной пневмонии даже в тех случаях, когда его не высевают. Среди осложнений важное значение имеют гнойный менингит и менингоэнцефалит, лейкопения. В целом подтверждены представления В.Д. Цинзерлинга о морфогенезе крупозной пневмонии. Показана возможность развития трех вариантов серого опеченения в зависимости от соотношения нейтрофильных лейкоцитов и фибрина. Выявлены частота и клиническая значимость поражений миокарда, почек и других органов.
ФГБУ "Санкт-Петербургский научно-исследовательский институт фтизиопульмонологии";
Медицинский факультет Санкт-Петербургского университета
Иркутская городская клиническая больница
В России, по данным О.В. Зайратьянца и соавт. [3], от острых пневмоний ежегодно умирают около 3000 человек, что составляет 20,1 на 100 000 населения. В Иркутске в 2007 г. смертность от острых пневмоний составила 51, а общая летальность от острых пневмоний — 10,3% [4]. По данным Департамента здравоохранения и социальной помощи населению администрации Иркутска, продолжался неуклонный рост смертности от пневмоний, которая к 2011 г. достигла 59. Среди умерших от заболеваний органов дыхания, по данным вскрытий, КП уверенно занимает 1-е место, составляя на протяжении многих лет в среднем 3—4,5% общего числа аутопсий. По данным В.Д. Цинзерлинга [5, 6], летальность от КП составляла 12—31%. Резкое сокращение числа умерших от этого заболевания отмечалось в 1950—60-е годы, что напрямую связывалось с внедрением в практику антибактериальных препаратов [7]. В 1980—90-е годы появились данные об увеличении числа умерших от КП [8, 9].
Тяжелую интоксикацию, с которой протекает заболевание, объясняют большим числом медиаторов воспаления и цитокинов, продуцируемых в ходе заболевания как ПК, так и самим организмом. После перенесенного заболевания иммунитет становится типоспецифическим и сохраняется в течение 6—12 мес. В настоящее время проводятся исследования по получению оптимальной вакцины.
Зарубежные исследования, посвященные патогенезу ПКИ, довольно многочисленны и проводятся с использованием современных молекулярно-биологических методов исключительно на экспериментальном материале. Показано, что ряд факторов, определяющих особенности макроорганизма, влияет на тяжесть ПКИ. Установлено, что генетическая вариабельность генов TLR2, TLR3, CD14, Fc-gamma RIIA повышает риск развития инвазивного заболевания у инфицированных больных [15]. Выявлено, что выраженное протективное действие против ПК оказывает Il1-β, уровень которого, по крайней мере у мышей, сильно варьирует [16]. Также было показано существенное влияние на течение заболевания галектина-3, члена семейства β-галактозидсвязывающего лектина, который продуцируется альвеолярными макрофагами [17].
Определенную клиническую значимость имеют и результаты исследования in vitro, проведенного J. Wang и соавт. [18], в котором доказано, что морфин резко снижает функции альвеолярных макрофагов в отношении ПК.
Во всех современных источниках показано, что наиболее тяжелое течение ПКИ приобретают у лиц из групп риска. Чаще всего к ним относят детей раннего возраста, стариков, лиц с иммунодефицитом (в том числе СПИДом), а также перенесших вирусные респираторные инфекции. Обычно указывается на преобладание летальных исходов в зимние месяцы. R. Dagan и соавт. [19] опубликовали данные о преобладании числа заболевших КП в социальных группах с низкими материальными доходами. В некоторых источниках [1, 10, 20, 21] особое внимание уделяется бедности, алкоголизму и принадлежности к ряду этнических групп (афроамериканцам, индейцам).
В ряде отечественных источников без ссылок на фактические данные приводятся сведения о полиэтиологичности КП [10]. При этом в качестве возможных, хотя и редких, возбудителей рассматривают стрептококки, кишечную палочку и др. Следует отметить, что В.Д. Цинзерлинг настаивал на выделении только двух этиологических вариантов долевой пневмонии — пневмококковой и довольно редкой клебсиеллезной (так называемой фридлендеровской пневмонии).
Изменения других органов при КП в литературе практически не описаны, кроме общих указаний на возможность дистрофических изменений. Современных зарубежных публикаций, включающих морфологическую характеристику пневмококковых пневмоний, нет. Встречаются только обзоры экспериментальных моделей [11] преимущественно в целях оценки эффективности разных вариантов лечения.
Все изложенное послужило основанием для проведения настоящего исследования летальных исходов от КП с анализом как клинико-эпидемиологических, так и патологоанатомических данных.
Материал и методы
Нами проведен углубленный клинико-морфологический анализ КП по материалам аутопсий по Иркутску за 1999—2011 гг. В ходе детального вскрытия умерших от КП проводили взвешивание органов и микроскопическое исследование материала. Брали материал для бактериологического, бактериоскопического и гистобактериоскопического исследований. Мазки-отпечатки окрашивали метиленовым синим и по Граму. Окрашивание флоры в срезах проводили азуром и эозином. Учитывали клинические и анамнестические сведения.
Цифровой материал обрабатывали методом вариационной статистики с применением критериев достоверности Стьюдента. В ходе исследования использовали материалы отдела статистики Департамента здравоохранения и социальной помощи населению администрации Иркутска [4].
Кроме того, нами проанализированы результаты патологоанатомических вскрытий, проведенных в Санкт-Петербурге в 2011 г. [26]. Для более детальной характеристики КП у умерших в Санкт-Петербурге проведен анализ отчетов патологоанатомического отделения (ПАО) Клинической инфекционной больницы (КИБ) им. С.П. Боткина за 1993—2007 гг. Данная крупная прозектура была взята для анализа в связи с возможностью получения полных достоверных сведений, включая результаты посмертных бактериологических исследований в период, когда в больнице отмечалась очень высокая (до 98%) доля патологоанатомических вскрытий.
Результаты
Общее число аутопсий в Иркутске за этот период составило 9478 случаев, из них умерших от КП было 315 (3,3% общего числа аутопсий). Углубленно проанализированы 152 случая. Мужчины составили 78,3% умерших, женщины — 21,7%, общее число умерших до 60 лет — 61,1%. На весенне-летний период пришлось 58,5% наблюдений, что может быть связано с купанием в холодной воде Байкала. Злоупотребление алкоголем зафиксировано в медицинской документации в 70% случаев. Косвенным морфологическим подтверждением данных анамнеза о злоупотреблении алкоголя явилось обнаружение тотального и крупноочагового жирового гепатоза, который установлен более чем в 80% наблюдений. Связь между эпидемическими периодами по гриппу, острым респираторным вирусным инфекциям и частотой летальных исходов от КП не установлена.
Согласно данным патологоанатомической службы Санкт-Петербурга [26], в 2011 г. в городе от болезней умерли 57 496 человек, из которых патологоанатомами были вскрыты 19 515, судебно-медицинскими экспертами — 16 393 человек. Диагноз КП был поставлен патологоанатомами в 180 случаях, расхождение клинического и патологоанатомического диагноза в стационарах установлено в 13,1% случаев. Подробных сведений о результатах при проведении судебно-медицинских исследований нет.
В ПАО КИБ им. С.П. Боткина за 1993—2007 гг. были вскрыты 269 умерших от КП. Число вскрытий с этим диагнозом существенно варьировало (от 7 случаев в 1996 г. до 33 в 1993 г.) и составляло 3,7—6% от секционного материала больницы. Среди умерших преобладали мужчины (208 человек, 77,3%). Сведения о хроническом алкоголизме имелись в 227 (84,4%) картах стационарного больного.
В половине случаев смерть наступила в первые сутки.
Проведен анализ 152 случаев КП в Иркутске. Высеваемость ПК составила 24%. В то же время при развернутой клинико-морфологической картине КП в 22 (17,9%) случаях флоры при бактериологическом исследовании не выявлено. При бактериоскопическом исследовании во всех случаях обнаружен грамположительный ланцетовидный диплококк, хотя поиск его в ряде случаев был затруднен. Ни в одном из наблюдений прижизненного исследования мокроты на определение микрофлоры не проводилось.
Специально проанализированы 97 случаев с полными клинико-анамнестическими данными. Во всех наблюдениях имелось внезапное начало, фебрильная температура отмечена в 95 случаях. Сосудистая (сердечно-сосудистая) недостаточность клинически выявлена в 87,5% наблюдениях. Летальность в первые сутки составила 55,3%. К 3-м суткам доля умерших составила 79%. В 1-ю неделю КП стала причиной смерти 90,1% пациентов.
В 89,4% случаев КП была долевой, в 15,1% — сублобарной. В 61,2% наблюдений отмечено одностороннее поражение, а в остальных — двустороннее. При одностороннем характере чаще поражалось правое легкое (в 47,7% случаев). Поражение одной доли имело место в 16,4% наблюдений, в остальных случаях поражались несколько долей, а в 13,8% наблюдений КП была тотальной. Отмечено существенное увеличение массы легких, которая при долевых пневмониях превышала 1 кг, при двусторонних составляла около 3 кг, в отдельных случаях достигала 4 кг.
При микроскопическом исследовании установлено несколько вариантов морфологических изменений.
При микробном отеке (1-й тип) наблюдается выраженная гиперемия капилляров, просветы альвеол расширены, заполнены серозной жидкостью, встречаются единичные эритроциты, лейкоциты. При окраске азуром определяется большое количество ланцетовидных диплококков (см. рис. 1, в,г).
Все варианты характеризовались малым или полным отсутствием поражений бронхов.
В 21,7% наблюдений отмечено поражение сосудов в виде флебитов с инфильтрацией стенки сосудов лейкоцитами, в ряде случаев в их просветах визуализировались тромбы. Встречались очаговые некрозы паренхимы, экссудат приобретал гнойный характер (см. рис. 2, в).
КП с абсцедированием отмечена в 30,9% наблюдений. В альвеолах преобладал лейкоцитарный экссудат, фибрин сохранялся в виде мелких депозитов или отсутствовал. Стенки межальвеолярных перегородок были разрушены, видны формирующиеся абсцессы с невыраженной капсулой, гиперемия не наблюдалась (см. рис. 2, г).
Во всех случаях при бактериологическом исследовании высевалась смешанная микробиота, иногда в комбинации с пневмококком.

Следует отметить, что в большинстве наблюдений разная цветовая характеристика и разнообразные микроскопические изменения встречались в одном и том же случае, в кусочках, взятых из разных отделов пораженного легкого, а при двусторонних поражениях — из разных долей. Данные о частоте выявленных нами структурных изменений в зависимости от сроков заболевания представлены в табл. 1. Всего при исследовании 110 случаев, в которых была известна длительность заболевания, установлено 417 типов изменений (в среднем 3,8 варианта морфологической картины на 1 случай).
В табл. 2 представлены сведения о наблюдавшихся нами легочных и внелегочных осложнениях. Среди легочных осложнений отмечена типичная карнификация (см. рис. 2, д). По данным В.Д. Цинзерлинга [5], осложнения в виде менингита имелись в 6% случаев, в нашем исследовании — в 11,2% (рис. 3, а—в). Рисунок 3. Внелегочные поражения при КП. а — вентрикулит с кровоизлиянием в сосудистое сплетение; б — гнойный васкулит сосудов головного мозга; в — гнойный менингит; г — резкое полнокровие сосудов, очаговые кровоизлияния и миоцитолиз в миокарде; д — макроскопические изменения почек: сероватый оттенок расширенного коркового слоя, красно-синюшные пирамидки с подчеркнутыми границами; е — микроскопические изменения почек: малокровие коры, некробиотические изменения нефротелия извитых канальцев; а, б, в, г, е — окраска гематоксилином и эозином. ×100. Гнойные менингиты и менингоэнцефалиты, по материалам КИБ им. С.П. Боткина в Санкт-Петербурге, диагностированы в 25,3% наблюдений. Во многих источниках литературы о них не упоминается. Сведений о частоте других осложнений в литературе мы не встретили.
В 33,5% случаев выявлены изменения миокарда (см. рис. 3, г): микроскопическая картина острой коронарной недостаточности — в 25,6% наблюдений, микроскопическая картина, сходная с ранним инфарктом миокарда, — в 7,9%. В 82% случаев эти изменения были обнаружены у лиц моложе 45 лет при отсутствии атеросклеротических изменений в коронарных артериях.
Бифуркационные лимфатические узлы были резко увеличены в размерах, иногда образуя пакет, темно-серого цвета с красным оттенком. Микроскопически отмечались выраженное полнокровие, кровоизлияния. Краевые синусы были расширены и содержали серозный экссудат.
В надпочечниках (помимо 7 случаев массивных кровоизлияний) отмечались расстройства кровообращения разной степени (от полнокровия до мелких геморрагий).
Бактериологически и бактериоскопически в лимфатических узлах, миокарде, почках и надпочечниках микробиота не обнаруживалась.
Случаев течения заболевания по типу генерализованной ПКИ с проявлениями ДВС-синдрома не выявлено.
В 11,2% наблюдениий в Иркутске и в 3,3% наблюдений в Санкт-Петербурге (особенно в последние годы) в крови отмечалась лейкопения вплоть до агранулоцитоза, расшифровать природу которого не представилось возможным.
Клинико-лабораторные и морфологические признаки вирусных респираторных инфекций и ВИЧ-инфекции документированы в обоих городах в небольшом числе наблюдений.
Представленные сведения и анализ данных литературы свидетельствуют о целесообразности выделения среди внебольничных пневмоний КП, имеющей ряд характерных черт, несмотря на то, что она не указана в Международной классификации болезней 10-го пересмотра. Частота этого заболевания, нередкие ошибки в клинической диагностике и высокая летальность свидетельствуют о необходимости большего внимания к КП со стороны специалистов разных профилей, особенно в России.
Этиология заболевания связана с ПК, в том числе в тех наблюдениях, в которых не высевали данного возбудителя. В пользу этого однозначно свидетельствуют результаты бактериоскопического и гистобактериоскопического исследований. При сочетанных поражениях отрицательный результат мог быть связан с подавлением ПК другой микробиотой. Отрицательные результаты в ряде случаев можно объяснить антибактериальной терапией. Кроме того, следует помнить об уникальной способности ПК к аутолизу.
Основываясь как на собственных фактических материалах, так и на данных современной литературы, можно полностью подтвердить взгляды В.Д. Цинзерлинга на пато- и морфогенез долевой и сублобарной пневмококковой КП. Заболевание начинается с проникновения ПК в нижние отделы респираторного тракта. Этому способствуют дополнительные факторы, важнейшие из которых — охлаждение и алкогольное опьянение, вирусные респираторные инфекции являются факультативным фактором. Весьма вероятна роль особой вирулентности штамма ПК. В просветах альвеол формируется очаг серозного воспаления, который по порам Кона начинает быстро распространяться и за короткий период может охватить всю долю. Под воздействием аутолизина происходит распад ПК с выделением большого количества медиаторов воспаления и цитокинов, обеспечивающих системный воспалительный ответ с яркими клиническими проявлениями (лихорадкой, ознобом и др.) Гиалуронидаза и нейраминидаза, способные разрушать основное вещество соединительной ткани, обеспечивают адгезию и колонизацию ПК на первых этапах. Пневмолизин, высвобождающийся при распаде ПК, оказывает прямое токсическое действие на капилляры, резко увеличивая их проницаемость. Аналогичным действием обладают продукты распада капсульного вещества. Среди них — производные пептидогликана, оказывающие мембранолитическое действие на альвеолы и эндотелий капилляров, а также перекись водорода, которая также резко повышает проницаемость сосудистой стенки. При этом сосудистая стенка может пропускать не только фибрин, но и эритроциты. Пневмолизин также оказывает и выраженное хемотаксическое действие на лейкоциты и моноциты. Такой механизм объясняет быстроту и выраженность сосудистых реакций, а также выход фибрина и эритроцитов в альвеолярные пространства. Именно скорость распространения и захват больших пространств легочной паренхимы в короткие сроки явились ключевыми факторами для включения в патогенез этого заболевания аллергических механизмов [22, 24]. N. Engleberg и соавт. [1] подчеркивают, что КП нельзя рассматривать как заболевание, в основе которого лежат аллергические механизмы. Предшествующая сенсибилизация, напротив, способствует быстрому распознаванию ПК, что и обеспечивает более эффективный фагоцитоз. В настоящее время можно выделить 5 вариантов экссудативной реакции, следующей за серозным отеком. Достоверно судить о причинах развития тех или иных изменений не представляется возможным. Отсутствует строгая зависимость между длительностью заболевания и определенной морфологической картиной. В некоторых случаях воспалительный процесс захватывает не всю, но бóльшую часть доли. Результаты проведенного нами клинико-морфологического анализа свидетельствуют о принципиальном сходстве долевых и сублобарных КП.
Среди легочных и внелегочных осложнений КП наиболее важными являются изменения в миокарде, встретившиеся в 33,5% случаев, которые могут иметь решающее значение в танатогенезе и являться непосредственной причиной смерти. Причины изменений в сердечной мышце, вероятно, связаны с циркуляцией в крови большого числа медиаторов воспаления и цитокинов, продуцируемых как самим ПК, так и макроорганизмом. В клинической практике могут иметь значение изменения, обнаруженные в почках у 42,8% умерших. Обнаруженная морфологическая картина острой почечной недостаточности коррелировала с клиническими проявлениями в виде олигоурии и азотемии, выявленных при жизни у 21% пациентов. Важное значение имеют и вторичные пневмококковые гнойные менингиты и менингоэнцефалиты, частота которых может достигать 25,3%.
Пневмоцистная пневмония – это тяжелая форма интерстициального легочного воспаления, вызываемая пневмоцистами и развивающаяся на фоне выраженных иммунодефицитных состояний. Клиническое течение характеризуется нарастающей одышкой, непродуктивным кашлем, фебрильной лихорадкой, болями в груди, развитием сердечно-легочной недостаточности. Диагноз ставится на основании рентгенологических признаков, состояния иммунного статуса, лабораторной идентификации патогена в крови, БАЛ, мокроте, биоптате (ПЦР, серологические тесты, РНИФ). Для этиотропной терапии используются сульфаниламидные, противопротозойные, иммуномодулирующие средства.
МКБ-10


Общие сведения
Пневмоцистная пневмония (ПП) относится к оппортунистическим инфекциям, поражающим лиц с иммунодефицитом и иммуносупрессией. При этом большинство людей с нормальным уровнем иммунитета переносит пневмоцистную инфекцию в виде ОРВИ. Антитела к возбудителю имеют около 90% взрослого населения, около 10% являются бессимптомными носителями пневмоцист – именно они представляют наибольшую угрозу для иммунокомпрометированных пациентов. Пневмоцистная пневмония является самой тяжелой клинической формой пневмоцистоза.

Причины
Характеристика возбудителя
Pneumocystis jirovecii – микроорганизм, вызывающий пневмоцистную пневмонию и другие виды пневмоцистоза у человека. До недавнего времени пневмоцисты считались простейшими, однако в 1988 г. на основании ряда характерных генетических, морфологических и биохимических признаков были отнесены к грибам семейства актиномицетов. Пневмоцисты обладают тропизмом к легочной ткани, весь их жизненный цикл протекает внутри альвеол и проходит 4 стадии:
- Трофозоит. Представляет собой вегетативную стадию P. Jirovecii. Имеет амебоидную форму, диаметр 1-5 мкм, одно ядро и тонкую двухслойную мембрану. Прикрепляется к альвеолоцитам, где увеличивается в размерах и делится.
- Прециста. Имеет овальную форму, диаметр 5 мкм. В ранней стадии содержит одно ядро, окруженное митохондриями, на поздней – 2-6 ядер с мембранами.
- Циста. Зрелая циста округлой формы, с 3-слойной стенкой, диаметром 7-8 мкм. Внутри цисты содержится четное количество (обычно 8 шт.) внутрицистных телец ‒ спорозоитов.
- Спорозоит. При разрыве зрелых цист из них высвобождаются спорозоиты, часть которых обладает одинарным набором хромосом (являются гаплоидными). Сливаясь, они вновь образуют трофозоиты, и жизненный цикл патогена повторяется.
В описанном цикле различают две фазы: неполовую, или асексуальную (деление трофозоита), и половую, или сексуальную (спорозоит-трофозоит-прециста-циста).
Пути передачи
Источниками P. jirovecii являются носители (бессимптомные или больные ОРЗ) и больные пневмоцистной инфекцией. В 30% случаев выявляется вовлеченность в эпидемический процесс медицинских работников. При кашле и чихании носители выделяют мелкодисперсный аэрозоль, содержащий патогены. Заражение восприимчивого макроорганизма происходит при вдыхании контаминированного воздуха (воздушно-капельным, воздушно-пылевым путем). Воротами для входящей инфекции служат дыхательные пути. Редко реализуется трансплацентарный путь передачи.
Характерны внутрисемейные и внутрибольничные эпидемические вспышки пневмоцистной пневмонии. Последние чаще происходят в отделениях недоношенных, домах престарелых, инфекционных стационарах. Пик детской заболеваемости пневмоцистной пневмонией приходится на конец лета – начало осени, взрослые болеют круглогодично.
Группы риска
Пневмоцисты являются типичными оппортунистами, поскольку вызывают манифестную инфекцию только при выраженном дефиците клеточного и гуморального иммунитета у определенного контингента пациентов. К группам риска по заболеваемости пневмоцистной пневмонией относятся:
- ВИЧ-инфицированные и больные СПИДом;
- пациенты с ЦМВ-инфекцией;
- недоношенные дети и младенцы с ЗВУР;
- дети, страдающие гипотрофией, рахитом;
- больные, получающие иммуносупрессивную терапию (по поводу лейкозов, миеломной болезни, других видов рака, трансплантации органов, коллагенозов);
- пациенты с первичными иммунодефицитами, болезнями крови (анемией, полицитемией), туберкулезом, патологией почек.

Патогенез
Пневмоцисты присутствуют в дыхательных путях здоровых людей, но вызывают пневмоцистную пневмонию только у лиц с нарушением гуморального и клеточного звена иммунитета. Экспериментально доказано, что ведущую роль в механизме пневмоцистоза играет снижение Т-хелперов (критическим является снижение СД4+ лимфоцитов ˂300-200 клеток/мкл), увеличение количества цитотоксических лимфоцитов СД8+.
P. Jirovecii с помощью особых выростов – филоподий – прикрепляется к альвеолоцитам первого порядка и альвеолярным макрофагам. Клеточной адгезии также способствуют гликопротеины пневмоцистов, которые взаимодействуют с фосфолипидами, апопротеинами, мукополисахаридами, сурфактантом альвеолярного эпителия. В условиях иммунокомпрометации цисты размножаются, используя сурфактант-ассоциированные белки, выделяют токсические метаболиты.
Происходит разрушение альвеолоцитов, заполнение альвеол пенистым экссудатом, содержащим большое количество пневмоцист на разных стадиях развития, воспалительные клетки, детрит. Интерстициальная ткань инфильтрируется плазматическими клетками. Развивается интерстициальная плазмоклеточная пневмония. Межальвеолярные перегородки гипертрофируются, что приводит к резкому снижению диффузии газов (альвеолярно-капиллярный блок), формированию дыхательной недостаточности и тяжелой гипоксии.
Классификация
В соответствии с патоморфологическими критериями в современной пульмонологии выделяют три стадии пневмоцистной пневмонии:
- I стадия. Происходит прикрепление пневмоцист к альвеолярной стенке. Воспалительная реакция и клинические проявления отсутствуют.
- II стадия. Отмечается десквамация альвеолоцитов, увеличение числа возбудителей в форме цист в макрофагах. В эту стадию появляются начальные клинические проявления пневмоцистной пневмонии.
- III стадия. Развивается альвеолит, плазмоцитарная инфильтрация интерстиция, гигантские скопления пневмоцист в макрофагах и альвеолах. Соответствует разгару заболевания.
Этапы развития пневмоцистной пневмонии:
- отечная фаза ‒ длится 7-10 дней, характеризуется нарастанием симптоматики;
- ателектатическая фаза ‒ продолжается в течение 4-х недель, сопровождается выраженной легочной недостаточностью;
- эмфизематозная фаза – имеет различную длительность, знаменуется обратным развитием симптоматики.
Симптомы пневмоцистной пневмонии
Инкубационный период вариабелен – от 7-10 дней до 2-4 недель (у больных СПИДом – до 10 недель). В отечную стадию клинические признаки пневмоцистной пневмонии легко спутать с обычной респираторной инфекцией. Симптомы нарастают постепенно: вначале беспокоит слабость, недомогание, субфебрилитет. Затем появляется одышка при умеренной нагрузке, боли в грудной клетке, сухой кашель.
В ателектатической стадии лихорадка принимает фебрильный характер, усиливается интоксикационный синдром (отсутствие аппетита, снижение веса, потливость по ночам). Кашель становится коклюшеподобным, постоянным, особенно беспокоит в ночное время суток. Одышка до 30-50 дыхательных движений в минуту выражена в покое. Отмечаются бледность кожных покровов с носогубным цианозом, тахикардия. В этот период пациент может погибнуть от сердечно-легочной недостаточности (СЛН).
У выживших пациентов наступает эмфизематозная стадия. Температура тела снижается, дыхательные расстройства исчезают. В исходе пневмоцистной пневмонии формируется эмфизема легких, легочное сердце. Пневмоцистная пневмония часто протекает в ассоциации с туберкулезом легких.
Четкая стадийность при пневмоцистозе прослеживается в основном у детей раннего возраста. У ВИЧ-инфицированных болезнь имеет стертое затяжное течение, у ВИЧ-негативных лиц с иммунодефицитом – более активное, с быстрым нарастанием СЛН.
Осложнения
Типичными осложнениями, развивающимися в разгар болезни, являются пневмоторакс, подкожная эмфизема, пневмомедиастинум, возникающие вследствие разрыва мелких кистозных образований. Возможно развитие абсцедирующей пневмонии. Эти состояния еще более усугубляют дыхательную недостаточность, повышают летальность. При значительном подавлении иммунитета может произойти генерализация пневмоцистной инфекции с мультиорганным поражением печени, селезенки, ЖКТ, щитовидной железы, органов зрения и слуха, лимфоузлов, костного мозга.

Диагностика
Из-за неспецифичности и стертости симптоматики существенной проблемой является гиподиагностика пневмоцистной пневмонии. Иногда патология диагностируется только посмертно. Все больные с подозрением на ПП должны быть в срочном порядке проконсультированы врачом-пульмонологом, инфекционистом. При выставлении диагноза опираются на следующие данные:
Дифференциальная диагностика
Комплексное клинико-лабораторное, рентгенологическое и бронхологическое обследование позволяет отличить пневмоцистную пневмонию от других поражений легких:
- легочного кандидоза;
- криптококковой пневмонии;
- цитомегаловирусной пневмонии;
- микоплазменной пневмонии;
- хламидийной пневмонии;
- туберкулеза легких;
- респираторного криптоспоридиоза;
- саркомы Капоши;
- бактериальной пневмонии.
Лечение пневмоцистной пневмонии
Стандартные антибактериальные средства при ПП неэффективны. В настоящее время препаратами первой линии считаются комбинированные сульфаниламиды, оказывающие противомикробное, бактерицидное и противопротозойное действие. Могут назначаться как перорально, так и внутривенно. Курс лечения составляет 1-3 недели.
При выраженных токсических эффектах и резистентности подбираются другие антибиотики, активные в отношении пневмоцист (линкозамиды, противолепрозные, противомалярийные, антипротозойные препараты). Из-за массовой гибели патогенов в первые дни терапии состояние пациентов с пневмоцистной пневмонией может ухудшиться, в связи с чем целесообразно назначение кортикостероидов.
Прогноз и профилактика
Смертность от пневмоцистной пневмонии достигает 50% среди недоношенных детей, 25-40% ‒ среди больных СПИДом. У 10-30% иммунокомпрометированных пациентов через несколько месяцев после излечения возникают рецидивы ПП. При отсутствии лечения летальность 100%.
Профилактическая работа реализуется в двух направлениях: эпидемиологическом и медикаментозном. Первый аспект предполагает широкое тестирование на пневмоцистную инфекцию представителей групп риска: пациентов с ВИЧ, онкопатологией, иммунодефицитами, недоношенных детей, сотрудников роддомов и стационаров. Второе направление – это фармакопрофилактика пневмоцистной пневмонии у лиц с количеством СД4+ клеток ˂200. Она заключается в приеме сульфаниламидов в профилактических дозах длительными курсами.
1. Пневмоцистная пневмония. Этиология, патогенез, клиника, дифференциальная диагностика, лечение (лекция)/ Боровицкий В.С.// Проблемы медицинской микологии. – 2012.
2. Пневмоцистная пневмония: исторические, эпидемиологические, клинико-морфологические аспекты/ Марковский В. Д., Плитень О. Н., Мирошниченко М. С., Мирошниченко А. А.// Annals of Mechnikov Institute, - 2012. - №3.
3. Особенности пневмоцистной пневмонии у ВИЧ-инфицированных лиц/ Пузырёва Л.В., Сафонов А.Д., Мордык А.В.// Медицинский вестник Северного Кавказа. – 2016. – Т.11, №3.
4. Пневмоцистоз. Современное состояние проблемы/ Каражас Н.В.// Альманах клинической медицины. – 2010.
Читайте также:

