Препаратов которые могут усилить симптомы дигиталисной интоксикации
Обновлено: 23.04.2024
Лечение отравления дигоксином (дигиталисом)
а) Стабилизация состояния. Предположительная схема лечения при интоксикации наперстянкой низкого, среднего и повышенного риска представлена ниже.
Лечение интоксикации дигиталисом:
I. Пациенты пониженного риска:
Электрокардиографические показания нарушений ритма отсутствуют
Сывороточные уровни дигоксина несколько повышены В анамнезе нет тяжелых сердечных заболеваний Функция левого желудочка хорошая
Дигоксин применяется в случае неосложненной фибрилляции предсердий
- Лечение:
Лечение амбулаторное
Прием дигиталиса временно прекращают
Повторить ЭКГ: обратить внимание на последствия отмены дигиталиса
II. Пациенты из группы среднего риска:
ЭКГ выявляет токсическое воздействие на сердце у пациентов без опасных для жизни осложнений
- Лечение:
Наблюдать в контролируемых условиях Установить концентрации калия и магния
Если концентрации калия или магния в крови значительно снижены, назначить курс заместительной терапии
Возмещение калия может обострить предсердно-желудочковую блокаду
Гиперкальциемия (подобно гипокалиемии и гипомагниемии) увеличивает желудочковый автоматизм
Избегать применения антиаритмических средств, если только нет гемодинамически значимой аритмии или эктопии высокой степени
III. Пациенты из группы повышенного риска:
Сывороточные уровни калия очень высоки
Наблюдаются опасные для жизни аритмии
- Лечение:
Доставить пациента в отделение интенсивной терапии коронарных больных
Опорожнить желудок не позднее чем через 6—8 ч после перорального приема
Медленно вводить активированный уголь
Анионообменные смолы могут сократить период полужизни дигитоксина в желудочно-кишечном тракте
Применять атропин в случаях выраженной синусовой брадикардии, прекращения активности синусно-предсердногоузла и блокады сердца II или III степени
В случае гемодинамической нестабильности и если пациенту не помогает атропин, ввести временный водитель ритма
Использовать дигоксинспецифические Fab-фрагменты

б) Очистка пищеварительного тракта. Показано, что холестирамин при пероральном приеме по 12—16 мг в день стимулирует удаление дигоксина, вероятно, посредством прерывания энтерогепатической рециркуляции дигоксина.
Как показало рандомизированное исследование по предупреждению абсорбции дигоксина, активированный уголь (могут потребоваться повторные дозы) более эффективен, чем холестирамин и холестирол. У 94-летнего пациента холестирамин и холестирол предположительно вызвали прерывание энтерогепатической рециркуляции дигоксина.
в) Антидоты дигоксина (дигиталиса). Если вводятся выделенные из организма овец дигоксинспецифические антитела, необходимо:
1) на протяжении первых нескольких часов контролировать показатели, свидетельствующие о возможном развитии гипокалиемии;
2) наблюдать за признаками застойной сердечной недостаточности, развивающейся вследствие утраты инотропии, индуцированной дигиталисом; и
3) контролировать аллергические реакции, особенно у пациентов с аллергией на овечьи белки и у пациентов, которым ранее вводили дигиталисиммунные Fab.
Показания. Фрагменты Fab нейтрализуют также отравление ланатозидом С4 и просцилларидином и сциллирозидом, а также отравление другими гликозидами, обнаруженными в листьях Nerium oleander.
Фрагменты Fab следует применять для лечения в случаях отравления наперстянкой грудных детей и детей младшего возраста без сердечных заболеваний, проглотивших более 0,3 мг/кг препарата; для лечения тех, у кого есть заболевание сердца или у которых концентрация сывороточного дигоксина выше 0,5 нг/мл; тех, кому угрожают аритмии, гемодинамическая неустойчивость или быстро прогрессирующая интоксикация.
Предпочтительно раннее применение Fab-терапии, до применения кардиостимуляции или лечения антиаритмическими средствами. После Fab-терапии необходимо тщательно контролировать состояние пациентов, так как может потребоваться вторая доза — в случае рецидива интоксикации или отсутствия положительных результатов. Подростки более чувствительны к наперстянке, и для них Fab-терапия может потребоваться при более низких концентрациях дигоксина в плазме.
Общие показания к применению Fab-терапии следующие:
• Надвигающаяся остановка сердца, остановка сердца или шок либо быстрое прогрессирование клинических показателей (прогрессирующее притупление чувствительности, усиление дефектов проведения, быстрый подъем уровня сывороточного калия при наличии в анамнезе отравления дигиталисом).
• Гиперкалиемия при отравлении дигиталисом (Fab-терапия быстро снимает гиперкалиемию).
• Уровень сывороточного дигоксина в устойчивом состоянии, превышающий 10 нг/мл через 6—8 ч после проглатывания у взрослых, или уровень сывороточного дигоксина, превышающий 5 нг/мл у детей. (Лечение должно основываться на симптомах, а не только на данных о концентрации дигоксина в сыворотке.)
• Гемодинамически неустойчивые, опасные для жизни аритмии (например, фибрилляция желудочков, желудочковая тахикардия, предсердная тахикардия, предсердно-желудочковая блокада разной степени, ускоренный узловой ритм, дефекты проведения).
• Проглатывание более 10 мг (40 таблеток по 0,25 мг) взрослыми или 4 мг (16 таблеток по 0,25 мг или > 0,3 мг/кг) детьми или более низких доз подростками (0,2 мг/кг).
• Брадикардия или блокада сердца III степени, не поддающаяся лечению атропином.
Fab-терапия показана для лечения отравлений дигиталисом у грудных младенцев и детей младшего возраста, которые проглотили 0,3 мг дигоксина на 1 кг массы тела, у лиц с заболеванием сердца или у пациентов с сывороточной концентрацией дигоксина, превышающей 6,4 нмоль/л (>5,0 нг/мл) в фазе элиминации, а также у лиц с опасной для жизни аритмией, гемодинамической неустойчивостью, гиперкалиемией выше 6 мэкв/л или с быстро прогрессирующей интоксикацией.
Fab-терапия может быть эффективна в случаях некардиологических проявлений интоксикации дигиталисом, например при остром психозе "дигиталисный делирий", который характеризуется сильным возбуждением, бредовым мышлением, агрессивным поведением и даже может привести к смерти.
Подростки, более чувствительные к токсическому действию дигоксина по сравнению с детьми, могут нуждаться в Fab-терапии после приема более низких доз препарата.
Лечение Fab-фрагментами должно основываться на симптомах и признаках, а не только на величинах концентрации дигоксина в сыворотке.
Пациенты с ранее имевшейся острой или хронической почечной недостаточностью в большей степени подвержены риску тяжелой интоксикации дигиталисом.
Fab-терапия эффективна при интоксикации дигитоксином и при отравлении препаратами из олеандра.
Неэффективное применение. Несмотря на то что дигок-синспецифические Fab-фрагменты эффективны против действия сердечных гликозидов, выделенных из таких растений, как олеандр, наперстянка и майский ландыш, он не оказал быстрого лечебного воздействия на ребенка, который отравился, съев ягоды физалиса (yew berries).
Физалис содержит токсин, сердечный гликозид, отличный от сердечных гликозидов, содержащихся в олеандре, наперстянке и ландыше, — он не вызывает гиперкалие-мии, и его прием не сопровождается появлением в сыворотке измеримых концентраций дигоксина. Очень маленькой дозы Fab (20 мг) было достаточно, чтобы связать всего 0,03 мг дигоксина. Была также применена кардиостимуляция, и ребенок выздоровел.
Дозировка. Taboulet и соавт. установили, что если первоначальное введение 800 мг Fab не приводит к снятию индуцированных дигоксином аритмий, следует попытаться ввести дополнительную дозу 500 мг [10]. При хронических передозировках обычно адекватна средняя доза 80— 160 мг Fab. Экстраполяция этого расчета, произведенного для дигитоксина, на дигоксин должна осуществляться с осторожностью.

Расчет нагрузки гликозида на организм с учетом проглоченного количества:
Проглоченное количество (мг) х биодоступность дигоксина (60 %) или биодоступность дигитоксина (100%).
С учетом концентрации гликозида в сыворотке:
Концентрация гликозида в сыворотке (нг/мл) х объем распределения (Vd) х масса (кг), где Vd — 5,6 л/кг для дигоксина и 0,56 л/кг для дигитоксина.
Fab-фрагменты можно также приобрести в Европе (Digidot Boehringer — Ingelheim). Во Франции одна ампула Fab-фрагментов содержит 80 мг Fab и нейтрализует 1 мг дигоксина или дигитоксина. Когда нет данных о проглоченном количестве или о концентрации гликозида в моче, вводят 10 ампул, и еще 10 ампул должны храниться на случай необходимости. В Германии Fab-фрагменты вводятся в ударной дозе 80—160 мг, и затем в течение 7—24 ч производится вливание 320 мг.
В случаях массивных дигитоксиновых интоксикаций могут потребоваться длительные и повторяющиеся внутривенные вливания Fab.
Передозировка дигоксина: расчет дозы фрагментов Fab. Если количество и тип дигоксина неизвестны:
- Суммарная нагрузка на организм = проглоченное количество (мг) х 0,8 а .
- Суммарная нагрузка на организм/0,6 b мг = число необходимых ампул.
Если известна устойчивая концентрация дигоксина (или дигитоксина) в сыворотке:
- Суммарная нагрузка на организм = концентрация дигоксина или дигитоксина в сыворотке (нг/мл) х Vd c х масса (кг)/1000.
- Суммарная нагрузка на организм/0,6 мг = число необходимых ампул Fab.
а Этот коэффициент соответствует 80 % биодоступности таблеток. Коэффициент 1,0 может быть использован для эликсира дигоксина или капсул дигитоксина.
b 0,6 мг нейтрализуется каждой ампулой (40 мг) Fab-фрагментов.
c Vd = 5,6 л/кг для дигоксина, 0,56 л/кг для дигитоксина.
d Расчет эквимолярной дозы Fab: (Молекулярная масса Fab = 50 000/Молекулярная маса дигоксина = 781) = 64 х нагрузка на организм (мг) = доза Fab-фрагментов (мг)
Погрешность расчета: острые передозировки. Если расчет количества ампул, требующихся в случае острой передозировки дигоксина, основывается на концентрации дигоксина в сыворотке, это может привести к ошибочному определению числа необходимых ампул Fab. Использование в расчетах сывороточной концентрации дигоксина основано на допущении, что суммарная нагрузка дигиталиса на организм — величина стационарная.
Состояние пациента с острой интоксикацией не является стационарным по меньшей мере в течение 6 ч. При тяжелом отравлении дигоксином потери дигоксина вследствие рвоты, промывания желудка, приема активированного угля и метаболических процессов могут привести к тому, что в систему кровообращения поступит менее 60 % проглоченной дозы. Heath утверждает, что для 75 % пациентов достаточно 10 ампул (400 мг).
Может потребоваться даже меньшая доза, поскольку полная стехиометриче-ская эквивалентность не всегда обязательна для получения удовлетворительной клинической реакции на ранней фазе (фазе распределения) острого отравления. В первые часы объем распределения может быть меньше. Начальная доза 6—8 мг/кг Fab-фрагментов, повторяемая в случае необходимости через 30—60 мин, может быть достаточной. Для подтверждения этих данных необходимы дальнейшие исследования.

u) Поддерживающая терапия:
- Хроническая токсичность. До того как будут получены дигоксинспецифичные Fab-фрагменты, в качестве временного антиаритмического средства можно использовать магний. На фоне дигоксиновой интоксикации магний обнаруживает значительную антиаритмическую активность. При лечении индуцированной дигоксином фибрилляции желудочков внутривенно вводимый магний может оказаться спасительным вспомогательным средством.
При назначении лечения пациентам с признаками или симптомами интоксикации дигитоксином следует руководствоваться конкретными проявлениями токсического действия. Лечение может включать использование водителя ритма или введение калия, антиаритмических средств, Fab-фрагментов или, возможно, многократное введение пероральных доз активированного угля. Для клинически стабильных пациентов, у которых в результате приема дигоксина повышаются концентрации дигоксина в сыворотке, но при этом отсутствуют признаки и симптомы токсического действия дигоксина, по-видимому, невелик риск развития тяжелой интоксикации дигитоксином и они не нуждаются в каком-либо лечении, а только в прекращении приема дигоксина.
Интоксикация дигоксином у взрослых пациентов:
1. Вводить внутривенно 2 г сульфата магния (10%) в течение 2 мин.
2. Вводить дополнительно 1—2 г/ч.
3. Каждые 2 ч определять концентрацию магния в сыворотке. Поддерживать концентрацию магния на уровне 4—5 мэкв/л.
4. Контролировать показатели, позволяющие предотвратить нервно-мышечную дисфункцию, дыхательную недостаточность или и то и другое.
5. Подавление глубоких сухожильных рефлексов или дыхания является показанием к немедленному прекращению инфузии сульфата магния и повторному определению содержания магния в сыворотке.
6. Вводить Fab-фрагменты в соответствии с вышеприведенным описанием.
Желудочковые аритмии. Taboulet и соавт. считают, что стимуляцию желудочков (ее трудно осуществлять, она может повысить риск летального исхода) следует назначать пациентам, не поддающимся лечению Fab-фрагментами. Желудочковые аритмии, индуцированные дигиталисной интоксикацией, очень чувствительны к магниевой терапии. Магний может снять желудочковую аритмию у пациентов как с нормальным уровнем магния, так и с гипомагниемией и может быть использован в тех случаях, когда возможна задержка поступления дигоксиновых антител.
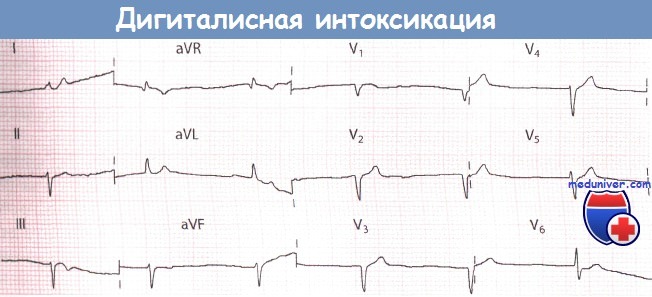
Ритм из АВ-соединения у пациента, получавшего дигоксин по поводу фибрилляции предсердий (ФП).
Содержание дигоксина в плазме крови 5,9 нмоль/л.
Гиперкалиемия. Гиперкалиемия (>6 мэкв/л) ингибирует нагнетание Na+-, К+-АТФазы при острой интоксикации дигоксином. Наличие гиперкалиемии отмечается в 50 % случаев летального исхода в отсутствие Fab-терапии. Концентрациям калия в крови, превышающим 7 мэкв/л, сопутствуют электрокардиографические изменения пиков зубцов Т, уменьшение сегмента ST, широкий QRS и удлиненный интервал Р— R.
Лечение гиперкалиемии при передозировках (>6 мэкв/л) дигиталиса должно включать следующие мероприятия.
1. Вводить внутривенно 5—10 % глюкозу 0,5 г/кг, бикарбонат натрия — 1 мэкв/кг и внутривенно инсулин — 0,1 г/кг на каждые 200—400 мг/кг глюкозы.
2. Избегать применения кальция.
3. В тяжелых случаях вводить с удерживающей клизмой натрий-полистиролсульфонат — 0,5 г/кг перорально (25 % на сорбите или Кайэксалате). Кайэксалатная клизма действует в течение 30 мин, и ее можно повторять каждые 4 ч, если предыдущие дозы не были удалены.
4. Гемодиализ целесообразен в случаях тяжелой или упорной гиперкалиемии или при почечной недостаточности.
Если введение Fab-фрагментов и глюкозы, инсулина и бикарбоната осуществляется одновременно, это может привести к тяжелой гипокалиемии.
Госпитализация:
1. Признать наличие острого отравления, если сывороточный уровень дигоксина превышает 2 нг/мл или если нарушения проведения или аритмии выявляются в первые 6 ч.
2. В случаях хронической интоксикации обычно необходима госпитализация для контроля аритмий и коррекции предрасполагающих факторов.
3. Дигоксинспецифичные Fab-фрагменты препятствуют проведению клинического иммуноанализа дигиталиса, и поэтому подобные сывороточные тесты ненадежны в течение по меньшей мере 5—7 дней после введения Fab.
4. Пациенты со стабильным состоянием здоровья, у которых в результате приема дигоксина концентрации последнего в сыворотке повышены, по-видимому, в меньшей степени подвержены риску развития тяжелой интоксикации дигоксином и нуждаются не в лечении, а только в прекращении приема дигоксина.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Отравление сердечными гликозидами — это острая лекарственная интоксикация, спровоцированная минимум двукратным превышением дозы препарата. Основные клинические проявления включают брадикардию, экстрасистолию, снижение сократительной способности миокарда, тошноту, слабость, изменение цветоощущения, абдоминальные и кардиальные боли, диарею. Диагностируется по данным, полученным при сборе анамнеза, информации, предоставленной родственниками пострадавшего, результатам лабораторного и аппаратного обследования. Основные направления терапии: удаление яда из желудка, антидоты, коррекция водно-электролитных нарушений, симптоматическое лечение.
МКБ-10
Общие сведения

Причины
Основная причина — прием средства без учета факторов, требующих снижения дозировки. Лекарство накапливается в плазме и тканях, что приводит к развитию токсического эффекта. Явление встречается у больных с клиренсом креатинина менее 50-80 мл/минуту, хронической сердечной недостаточностью. Риск передозировки повышен у пациентов школьного возраста (сложно подобрать дозу и режим терапии). Другие ситуации, провоцирующие отравление:
Патогенез
СГ на 60% угнетают активность мембранной Na + /K + -АТФазы, тем самым нарушая процесс поляризации и реполяризации миокарда. Часть отсутствующих ионов калия замещается ионами водорода, что способствует развитию внутриклеточного ацидоза и внеклеточного алкалоза. Снижается сократительная способность сердца, возникает гипосистолия. АТФаза проводящей системы более чем вдвое чувствительна к влиянию сердечных гликозидов по сравнению с аналогичным энзимом в миокарде. Поэтому на фоне дигиталисного поражения выражены блокады внутрисердечной передачи импульса.
Помимо прямого кардиотоксического эффекта средство действует на ЦНС. Под его влиянием нарушается функция нейромедиаторов. Возникают зрительные и психические нарушения. Поражение периферической нервной системы характеризуется усилением возбудимости блуждающего нерва, это становится причиной резкой брадикардии. Развивается гиперкалиемия, обусловленная ухудшением возврата ионов калия в клетки скелетной мускулатуры. Она дополнительно провоцирует ослабление сердечного ритма и гемодинамики.
Классификация
Деление производится с учетом вида использованного препарата (короткого, среднего, длительного действия), механизма отравления (суицидальное, случайное, ятрогенное), наличия осложнений (осложненное, неосложненное), набора выпитых медикаментов (моноинтоксикация сердечными гликозидами, сочетанное отравление комплексом лекарств), фазы (токсикогенная, соматогенная). В клинической практике чаще используют вариант классификации, основанный на степени тяжести экзотоксикоза:
- Легкое. Возникает, если дозировка средства была превышена в 2-2,5 раза. Симптоматика выражена умеренно, отмечается АВ-блокада I степени, не несущая угрозы жизни пострадавшего. Значимые неврологические нарушения отсутствуют. Встречается у пациентов, ошибочно принявших повышенную дозу лекарства.
- Средней тяжести. Состояние значительно ухудшается. Есть признаки поражения центральных и периферических нервных структур. Блокада проводимости достигает II степени (чаще Мобитц I). Происходит нарушение гемодинамики. Патология встречается у людей, получающих дигоксин на фоне почечной недостаточности, детей, случайно выпивших таблетки.
- Тяжелое. Все симптомы выражены максимально. Внутрисердечная блокада может быть субтотальной или тотальной. Отмечается диссоциация в работе желудочков и предсердий. Общее состояние нарушено значительно. Смерть часто наступает в течение первых 6-24 часов с момента приема токсиканта. Наблюдается преимущественно при попытках суицида.
Симптомы
Тяжесть отравления сердечными гликозидами напрямую зависит от дозы, принятой пострадавшим. Легкие интоксикации характеризуются тошнотой, диплопией, изменением цветоощущения по типу красок Ван Гога. Возникают жалобы на жидкий стул, неприятное чувство в области сердца, слабость. При осмотре живот мягкий, незначительно болезненный в зоне проекции тонкого кишечника. АД сохранено, пульс нормального напряжения и наполнения, кожа умеренно влажная, обычной окраски. Общее периферическое сосудистое сопротивление увеличено.
При среднетяжелых экзотоксикозах на первый план выходят неврологические, психические нарушения. Отмечается головная боль, дезориентация в пространстве и времени, галлюцинации. Присутствуют все симптомы, свойственные легкой степени. Определяется выраженный гипергидроз, бледность кожи. Пульс становится более редким, однако не достигает критических значений. Артериальное давление умеренно снижается. Больной жалуется на страх смерти, ощущение перебоев в работе сердца.
Тяжелые интоксикации сопровождаются картиной кардиологических нарушений. Клинические признаки, свойственные менее выраженным отравлениям, многократно усиливаются. Диагностируется брадикардия, резкое снижение показателей АД, симптомы нарушения мозгового кровотока (головокружение, угнетение сознания, кома). Пациент покрыт липким холодным потом, периферические вены спадаются, выявляется акроцианоз. При поражении дыхательного центра продолговатого мозга возникает респираторная недостаточность.
Осложнения
Распространенное осложнение – тотальная AВ-блокада встречается в 25-30% случаев тяжелого дигиталисного поражения. При этом работа верхней и нижней части сердца становится нескоординированной, что делает невозможным поддержание приемлемых гемодинамических показателей. Желудочки сокращаются с частотой 20-45 ударов/минуту за счет активизации эктопических очагов. Существует высокий риск фибрилляции и асистолии. АВ-блокада тотального типа требует пребывания больного в условиях кардиологической реанимации и установки кардиостимулятора.
У 3-5% пострадавших развивается аритмогенное шоковое состояние, которое проявляется централизацией кровообращения, комой, патологическим типом дыхания. У 5-7% пациентов наблюдаются приступы Морганьи-Адамса-Стокса. При длительном и значительном снижении перфузии крови в мозге на соматогенном этапе могут выявляться признаки повреждения коры, сопровождающиеся нарушением мыслительных способностей, поведения и памяти, головными болями. Обнаруживается в 1-2% случаев.
Диагностика
Диагноз выставляется врачом бригады скорой медицинской помощи, подтверждается в условиях стационара, куда будет доставлен пациент. Дифференциация проводится с отравлением ФОС, другими антиаритмическими препаратами, героином. Требуется консультация врача-кардиолога, терапевта, гастроэнтеролога, невролога. Непосредственным ведением пострадавшего обычно занимается реаниматолог. Обследование проводится с применением следующих методов:
- Физикальное. Артериальное давление сохранено или снижено. При тяжелых процессах этот показатель может достигать 70/40 мм рт. ст. и ниже. Пульс реже 60-70 уд/мин, иногда определяется тахикардия. Присутствуют клинические признаки дигиталисной интоксикации. При аускультации сердца выявляются перебои, глухость тонов.
- Лабораторное. Плазменная концентрация токсиканта — 3-10 нг/мл. Содержание калия выше 5,3 ммоль/л. Присутствуют явления ацидоза, pH ниже 7,3. Возможен рост показателей креатинина и мочевины, увеличение активности микросомальных ферментов печени. При нарушении дыхания отмечается рост парциального давления углекислого газа, снижение оксигенации крови.
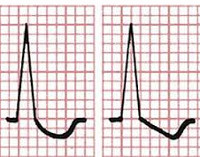
- Аппаратное. Основной метод аппаратной диагностики — электрокардиография. У пациентов со здоровым сердцем под влиянием СГ происходит депрессия сегмента ST в форме ковша. При наличии предшествующих поражений миокарда отмечается его резкий дугообразный подъем. Могут присутствовать другие патологические явления: выпадение QRS, двухфазность зубца P, экстрасистолы.
Лечение отравления сердечными гликозидами
Острое отравление всегда требует госпитализации пострадавшего. Это обусловлено высоким риском летальных осложнений. Больные с тяжелой интоксикацией и выраженными клиническими проявлениями нуждаются в реанимационном пособии. Легкие экзотоксикозы могут быть купированы в условиях терапевтического или токсикологического отделения общего профиля. Терапия направлена на удаление невсосавшегося и всосавшегося яда, усиление естественной экскреции, связывание токсиканта антидотами, коррекцию электролитных нарушений.
Первая помощь
Независимо от времени, прошедшего с приема отравляющего вещества, проводится зондовое промывание желудка. Для этого используют чистую воду, объем которой может достигать 10-15 литров на 1 процедуру. После полного очищения вводят взвесь измельченного активированного угля, что помогает связать как невсосавшуюся часть препарата, так и токсикант, циркулирующий в энтерогепатическом цикле. Доза сорбента рассчитывается по формуле 1 г/кг веса. При наличии выраженной аритмии манипуляцию не проводят.
На догоспитальном этапе пациенту может быть назначен дифенин, который обладает антиаритмическим влиянием, не замедляя атриовентрикулярную проводимость. Брадикардию купируют с помощью атропина. Требуется инфузионная и симптоматическая терапия. При необходимости пациента переводят на ИВЛ, начинают вливание прессорных аминов. Доза последних подбирается эмпирически путем медленного титрования под контролем АД. Фибрилляция предсердий — показание для начала сердечно-легочной реанимации.
Консервативное лечение
В качестве противоядия больной получает унитиол 5% по 1 мл на 10 кг массы. Первые 3-е суток требуется три внутримышечных инъекции ежедневно, далее – 1-2 введения. Общий курс — 7-10 дней. Используется натрия цитрат или трилон Б. Для устранения гиперкалиемии необходима инфузия глюкозы с инсулином и магния сульфатом. Смесь способствует поступлению K + в клетки. Сходным действием обладает натрия гидрокарбонат. Применяют солевые слабительные, петлевые диуретики. Последние нужно использовать с осторожностью. Помимо калия они выводят из организма магний, способствуют развитию гипотонии.
При выраженном урежении ЧСС пациенту вводится атропин, на фоне экстрасистолии целесообразно внутривенное вливание лидокаина. Для вытеснения СГ из тканей показан дифенин. Существует неподтвержденное мнение ряда ученых, что этот препарат улучшает результаты экстракорпорального очищения. Эффективный метод — вливание фрагментов антител к СГ, позволяющий быстро восстановить сердечный ритм, устранить явления интоксикации. Дозу лекарства подбирают по количеству принятого отравляющего вещества.
Реанимационное пособие
Больного подключают к анестезиологическому монитору для постоянного контроля коронарного ритма. Форсированный диурез и гемодиализ как средство активной экскреции токсиканта считаются малоэффективными, однако могут применяться в составе восстановительного комплекса. Фармакологическая терапия не отличается от вышеописанной. Работу сердца при значительных блокадах проводимости обеспечивают с помощью внешнего или эндокардиального стимулятора. Может потребоваться ИВЛ, установка центрального венозного катетера, электроимпульсное воздействие.
Прогноз и профилактика
Отравление сердечными гликозидами имеет положительный прогноз при средней и малой тяжести интоксикации. К числу неблагоприятных прогностических факторов относится резистентная к введению глюкозо-инсулиновой смеси гиперкалиемия, блокада проводимости II-III степени, хроническая сердечная недостаточность. Наибольшее количество смертей происходит в первые 24 часа со времени появления симптомов экзотоксикоза. Общая летальность, по данным различных источников, составляет 2-10%. 85% погибших — люди, совершившие попытку суицида.
Профилактика медикаментозных отравлений заключается в тщательном контроле над лекарственными препаратами. Медикаменты должны храниться там, куда не имеют доступа дети, старики и больные с психическими отклонениями. Пациенты пожилого возраста, получающие лечение сердечными гликозидами, обязаны иметь таблетницу, которая позволяет предотвратить повторный прием средства. Люди, страдающие депрессией и имеющие суицидальные наклонности, нуждаются в постоянном контроле родственников.
3. Руководство по скорой медицинской помощи/ Хубутия М.Ш., Верткин А.Л., Багненко С.Ф., Мирошниченко А.Г. — 2007.
Ключевые слова: сердечные гликозиды, дигоксин, побочные эффекты, интоксикация, аритмия, Fab-фрагменты.
Для цитирования: Дядык А.И., Куглер Т.Е., Здиховская И.И., Ракитская И.В. Дигиталисная интоксикация: диагностика, лечебная тактика и профилактика. РМЖ. 2021;1:29-33.
Digitalis intoxication: diagnosis, management strategy, and prevention
A.I. Dyadyk , T.E. Kugler, I.I. Zdikhovskaya, I.V. Rakitskaya
M. Gorkiy Donetsk National Medical University, Donetsk, DPR
Current guidelines recommend prescribing cardiac glycosides with caution. However, considering their pharmacological properties and narrow therapeutic index, the rate of incorrect use of cardiac glycosides in clinical practice is still high. Digitalis toxicity develops at various serum concentrations of digoxin (generally, at concentrations > 2.0 ng/ml). Preventive strategies for digitalis toxicity should be based on both serum digoxin concentrations and its risk factors. Optimal doses of cardiac glycosides should be selected based on patient’s age, comorbidities, renal functions, and drug interactions. A wide spectrum of cardiac and non-cardiac manifestations of digitalis toxicity significantly hampers its diagnosis. The most common symptoms are irregular heartbeat and conduction abnormalities, nausea, vomiting, weakness, dizziness, headache, psychic disorders, and vision loss. The management strategy for digitalis toxicity is based on the severity of clinical signs. Severe life-threatening arrhythmias are a reason to prescribe anti-digoxin antibodies (Fab-fragments), which are, unfortunately, not readily available in Russian clinical practice.
Keywords: cardiac glycosides, digoxin, adverse effects, digitalis toxicity, arrhythmia, Fab-fragments.
For citation: Dyadyk A.I., Kugler T.E., Zdikhovskaya I.I., Rakitskaya I.V. et al. Digitalis intoxication: diagnosis, management strategy, and prevention. RMJ. 2021;1:29–33.

Памяти нашего Учителя
Введение
Сердечные гликозиды (СГ) продолжают широко применяться в клинической практике. В настоящее время в кардиологии в основном используется дигоксин, обладающий доказанной клинической эффективностью. В крупномасштабных рандомизированных контролируемых исследованиях последних лет (SENIORS [1], ROCKET-AF [2], ARISTOTLE AF NOAC [3]) приблизительно 30–40% пациентов с хронической сердечной недостаточностью (ХСН) и/или фибрилляцией предсердий (ФП) получали СГ в различных режимах терапии. Положительный эффект дигоксина может быть в большей степени связан с увеличением сократимости спиральных волокон миокарда, определяющих активную позднюю фазу опорожнения левого желудочка (ЛЖ) и активную раннюю фазу диастолического наполнения, чем со снижением ЧСС (особенно при синусовом ритме) [4].
Согласно рекомендациям Российского кардиологического общества (РКО) по диагностике и лечению острой декомпенсированной сердечной недостаточности и ХСН [1] дигоксин может применятьсяу больных ХСН с синусовым ритмом, несмотря на лечение ингибиторами ангионтензинпревращающего фермента,β-блокаторами и антагонистами альдостерона, для снижения риска госпитализации как по поводу как сердечной недостаточности, так и других причин (класс рекомендаций — IIb, уровень доказательности — B). Назначение дигоксина должно быть рассмотрено у больных ХСН II–IV функционального класса, с ФВ ЛЖ
Факторы риска развития дигиталисной интоксикации
Клиническая эффективность и безопасность дигоксина определяются рядом фармакокинетических параметров, включающих абсорбцию, распределение по органам и тканям и элиминацию путем биотрансформации и экскреции [23–25]. При одинаковых режимах дозирования дигоксина изменение сывороточной концентрации может наблюдаться у пожилых пациентов, при сниженной функции почек, сердечно-сосудистой патологии, электролитных нарушениях, одновременном приеме с некоторыми лекарственными препаратами. Отмечена повышенная чувствительность миокарда к токсическим эффектам СГ у больных с хроническим обструктивным заболеванием легких, особенно при развитии правожелудочковой сердечной недостаточности, гипоксемии и гиперкапнии. Сывороточные концентрации дигоксина снижаются при гипертиреозе и повышаются при гипотиреозе [16, 26–29].
Особенности фармакокинетики дигоксина
С целью профилактики ДтИ следует учитывать особенности фармакокинетики дигоксина при различных клинических ситуациях [28, 29]. Так, с возрастом наблюдается снижение скорости клубочковой фильтрации (СКФ), уменьшается скелетная мышечная масса, являющаяся основным депо СГ, что приводит к уменьшению объема распределения, а следовательно, к более высоким плазменным концентрациям [16]. Наличие коморбидности и полипрагмазии определяет необходимость снижения дозировок дигоксина у лиц пожилого возраста — обычно до 0,125 мг.
Фармакокинетика дигоксина существенно не меняется у больных гепатитами, циррозом печени и тучных больных в связи с низкой концентрацией в жировой ткани. Следовательно, при ожирении дозы дигоксина должны рассчитываться не на общую массу тела, а на мышечную [25, 30].
Взаимодействие с лекарственными препаратами
Представлены убедительные доказательства изменения плазменных концентраций дигоксина при комбинированном применении с другими лекарственными препаратами [26, 27, 29]. Снижение абсорбции дигоксина происходит при одновременном приеме с антацидами, холестирамином, сорбентами, метоклопрамидом, сульфасалазином, препаратами цитотоксического действия.
Повышение концентрации дигоксина в плазме происходит при назначении противоаритмических препаратов (хинидин, амиодарон, пропафенон, новокаинамид, верапамил), препаратов с холинергическими свойствами (атропин, метацин), ингибиторов ангиотензинпревращающего фермента. Применение нестероидных противовоспалительных препаратов сопряжено с риском снижения СКФ, что приводит к уменьшению почечной экскреции дигоксина на 20–30%, а следовательно, к повышению его плазменного уровня [26, 29, 31].
Комбинированное применение дигоксина с диуретиками повышает риск развития ДтИ вследствие присущих им побочных эффектов: гипокалиемии, гипомагниемии (петлевые и тиазидные диуретики), гиперкалиемии (калийсберегающие диуретики), гиперкальциемии (тиазидные диуретики), метаболического алкалоза (петлевые и тиазидные диуретики). В связи с этим у больных, получающих дигоксин и диуретическую терапию, необходимо контролировать плазменные уровни электролитов и электрокардиографические показатели [25–27].
Электролитные нарушения
С нарушениями баланса ионов К + , Na + , Mg 2+ и Са 2+ связано как изменение эффективности СГ, так и развитие ДтИ. Среди этих нарушений важное место занимают нарушения гомеостаза К + . В эксперименте и клинических исследованиях показано повышение риска развития ДтИ при гипокалиемии. Этот феномен обусловлен целым рядом факторов, включая снижение связывания CГ с Na + -К + -АТФазой сарколеммы, снижение содержания Na + -К + -АТФазных единиц в скелетной мускулатуре, непосредственное влияние гипокалиемии на формирование эктопических очагов в миокарде и нарушение проводимости. Электрофизиологические механизмы, обусловленные гипокалиемией, способствуют увеличению токсических эффектов СГ и существенно повышают риск развития аритмий [16].
В отличие от гипокалиемии, гиперкалиемия не ассоциируется с увеличением риска развития ДтИ. Повышение концентрации экстрацеллюлярного К + ведет к структурным изменениям Na + -К + -АТФазы, нарушающим связь с ней СГ. Кроме того, при гиперкалиемии наблюдается стимуляция активности Na + -К + -АТФазы. Повышение плазменных уровней К + (более 5,5 мэкв/л) стимулирует деполяризацию проводящей ткани сердца (особенно атриовентрикулярных соединений), результатом чего может быть снижение проводимости и развитие атриовентрикулярных блокад [26–28].
Ионам Са 2+ отводится важная роль в развитии ДтИ. Одним из факторов риска ДтИ является увеличение внутриклеточного Na + , что модифицирует Na + -Са 2+ обмен, в результате чего повышается внутриклеточное содержание Са 2+ , ведущее к замедлению процессов проведения [12]. Сказанное выше аргументирует необходимость определения плазменных уровней электролитов при использовании дигоксина [32].
Клинические проявления дигиталисной интоксикации
Широкий спектр проявлений ДтИ, как кардиальных, так и некардиальных, существенно затрудняет ее диагностику. По данным G. Ordog et al. (1987) [33], своевременная диагностика ДтИ осуществляется приблизительно в 20% случаев.
По результатам исследования М. Böhn et al. (1998) [34], при ДтИ кардиальные проявления имеют место в 67–80% случаев, желудочно-кишечные — в 20–25% случаев, неврологические — в 5–10% случаев. Нарушения сердечного ритма и проводимости нередко могут быть первыми (а иногда и единственными) проявлениями ДтИ.
I. See et al. (2014) [19] опубликовали детальный анализ данных 5165 больных, госпитализированных в отделения интенсивной терапии с 2005 по 2010 г. в США в связи с побочными эффектами лекарственных препаратов. Среди них был выявлен 441 случай ДтИ. Большинство составили женщины (67,8% [95% ДИ 62,9–72,6%]), лица ≥70 лет (79,1% [95% ДИ 73,5–84,7%]). Диагноз ДтИ был установлен в 5,9% случаев (95% ДИ 4,0–7,9%) госпитализаций пациентов ≥85 лет. Уровень сывороточной концентрации дигоксина ≥2,0 нг/мл имел место в 95,8% случаев. Эти данные дают реальное представление о частоте и тяжести ДтИ, ее структуре и факторах риска развития в клинической практике (табл. 1).
![Таблица 1. Частота клинических проявлений дигиталисной интоксикации [19]](https://www.rmj.ru/upload/medialibrary/69d/29-1.jpg)
Кардиальные симптомы
Токсическое влияние СГ на кардиальные электрофизиологические процессы — наиболее частое и серьезное проявление ДтИ. Практически все летальные случаи ДтИ обусловлены тяжелыми нарушениями ритма и проводимости, которые не носят специфический характер, в связи с чем установление их этиологии нередко представляет существенные трудности.
Аритмогенные эффекты СГ являются комплексными и недостаточно изученными. К механизмам их развития относят постдеполяризационные потенциалы, усиленную диастолическую реполяризацию и механизмы re-entry. Важное место также отводится внутриклеточной перегрузке Са 2+ [16, 18].
В зависимости от генеза выделяют две группы аритмий, развивающихся при ДтИ [25, 26]:
аритмии, обусловленные преимущественно повышением парасимпатической активности (синусовая брадикардия, синоатриальные и атриовентрикулярные блокады, узловой ритм, а также частота желудочковых комплексов менее 50 в минуту при ФП);
аритмии, обусловленные повышением эктопической активности (предсердная и желудочковая экстрасистолия, узловая тахикардия, желудочковая тахикардия и фибрилляция желудочков).
В ряде случаев усиленная эктопия сочетается с повышенным вагусным тонусом, что проявляется предсердной тахикардией с атриовентрикулярной блокадой или атриовентрикулярной тахикардией с атриовентрикулярной блокадой. Сочетание пароксизмальной предсердной тахикардии с атриовентрикулярной блокадой 2:1 считается классическим типом аритмии при ДтИ [19, 26, 35].
Наиболее частым проявлением ДтИ является развитие желудочковой эктопии, что проявляется полиморфной желудочковой экстрасистолией как с фиксированными, так и с разными интервалами сцепления. Желудочковая экстрасистолия часто носит характер бигеминии. Проявлениями ДтИ также могут быть пробежки желудочковой тахикардии (3 и более последовательных желудочковых комплекса). Характерной считается ее редкая форма — двунаправленная (или бифасцикулярная) желудочковая тахикардия. При ДтИ возможно также развитие фибрилляции желудочков [34, 35].
Некардиальные симптомы
Некардиальные симптомы ДтИ многообразны и неспецифичны, плохо коррелируют с сывороточными уровнями дигоксина и обычно не носят жизнеопасный характер. Среди них превалируют симптомы со стороны ЖКТ, ЦНС и зрительного аппарата [19, 26–28]. Аллергические реакции (кожная сыпь, эозинофилия, лихорадка) при приеме СГ наблюдаются редко.
Частыми и нередко ранними проявлениями ДтИ (до 80% случаев) являются анорексия, тошнота и рвота, имеющие центральное происхождение. Довольно часто наблюдается абдоминальная боль и диарея. Практически у всех больных с ДтИ развивается слабость, недомогание, снижение толерантности к физической нагрузке и головная боль. В 2/3 случаев наблюдаются различные психические нарушения, включающие раздражительность, нервозность, спутанность сознания, реже — дезориентацию, галлюцинации и психоз [17, 29, 31]. Нарушения зрения включают изменение цветовосприятия, ретробульбарный неврит и глазной паралич [37].
Лечебная тактика при дигиталисной интоксикации
Характер лечебных мероприятий при ДтИ и их эффективность определяются целым рядом факторов, включающих своевременную диагностику, установление тяжести состояния, суммарного количества принятого препарата и времени приема последней дозы, наличие нарушений электролитного баланса, функции почек, а также взаимодействия СГ с другими лекарственными препаратами [38–41]. Так, при ДтИ, проявляющейся синусовой брадикардией, атриовентрикулярной блокадой 1-й степени, редкими желудочковыми или предсердными экстрасистолами, достаточно временно отменить СГ, проводить мониторинг ЭКГ и АД. В последующем необходим подбор адекватных дозировок дигоксина для предотвращения повторных эпизодов ДтИ [41, 42].
В то же время серьезные жизнеопасные нарушения сердечного ритма и проводимости требуют немедленного проведения лечебных мероприятий. Так, при выраженной синусовой брадикардии, брадиаритмии при ФП или атриовентрикулярной блокаде 2-й степени применение атропина нередко обеспечивает хороший клинический эффект. При отсутствии эффекта от атропина, а также в случаях более тяжелой дисфункции синусового узла с атриовентрикулярной блокадой 3-й степени необходима установка кардио-стимулятора. Это может быть как временной мерой — в период острой борьбы с опасными для жизни нарушениями сердечного ритма, так и постоянной мерой — при сохраняющейся высокой степени блокады [16, 18, 29].
Развитие тяжелых жизнеопасных аритмий служит основанием для назначения специальных антидигоксиновых фрагментов антител (Fab-фрагментов). До назначения Fab-фрагментов или в ходе их применения необходимо срочное проведение других лечебных мероприятий, включающих коррекцию калиевого и/или магниевого гомеостаза и/или назначение противоаритмических препаратов (новокаинамид, пропафенон, лидокаин, амиодарон) [38, 39, 43].
Fab-фрагменты связываются с внутрисосудистым дигоксином, а также с дигоксином, находящимся в интерстициальном пространстве, куда он поступает путем диффузии. В результате этого происходит снижение концентрации свободного дигоксина во внеклеточном пространстве почти до нулевых уровней. Устанавливаемый при этом концентрационный градиент способствует выходу дигоксина из тканей и быстрому соединению с Fab-фрагментами. Благодаря этому наблюдается заметное повышение суммарной концентрации внеклеточного дигоксина, являющегося фармакологически неактивным, т. к. он находится в связанном состоянии с Fab-фрагментами. Связанный с Fab-фрагментами дигоксин элиминируется преимущественно почками. Таким образом, Fab-фрагменты антидигоксиновых антител быстро и эффективно устраняют проявления ДтИ [21, 39, 43]. По мнению E. Antman et al. (1990) [44], продолжение дигиталисной терапии возможно через 7 дней после устранения ДтИ и коррекции дозировок дигоксина. Гемодиализ и перитонеальный диализ не способны существенно элиминировать дигоксин из организма, т. к. он находится в связанном состоянии в различных (прежде всего в мышечных) тканях [45].
Заключение
Подходы к снижению частоты развития и тяжести клинических проявлений ДтИ должны базироваться на комплексе факторов, включающих знание фармакологических характеристик СГ, показаний и противопоказаний к их применению. Быстрая дигитализация должна применяться только в случаях развития жизнеопасных суправентрикулярных аритмий, когда использование других лекарственных средств противопоказано или неэффективно [46]. Кроме того, важное место в профилактике ДтИ отводится определению сывороточных концентраций дигоксина. Клиницистам следует рассматривать применение дигоксина с концентрацией в плазме не более 1,1 нг/мл (0,25 мг/сут и менее). Выбор дозы дигоксина должен осуществляться с учетом факторов риска развития ДтИ, т. е. особенностей кардиальной патологии, возраста, мышечной и жировой массы тела больного, сопутствующих заболеваний, состояния функции почек, а также возможного взаимодействия с другими лекарственными препаратами.
Ключевые слова: ингибиторы протонной помпы, инструкции по применению, побочные эффекты, эрадикация, Helicobacter pilori.
S.V. Plyusnin
Non-State Educational Private Institution Of Additional Professional Education
"Medical Dental Institute", Moscow, Russian Federation
Proton pump inhibitors (PPIs) are drugs that block H + -K + -ATPase on the apical membrane of the gastric parietal cells. Due to this pharmacological effect, it is possible to achieve inhibition of hydrochloric acid and its secretion formation. To date, 6 PPIs (under an international nonproprietary name) have been registered in the Russian Federation. PPIs, having proven efficacy and safety in many clinical studies, have several patterns reflected in their patient information leaflet. The attending physician should pay attention to these patterns before starting PPIs therapy. The author considers the characteristics of pharmacokinetics, pharmacodynamics of various PPIs, as well as the issues concerning efficacy and safety of use. The lecture also discusses the adverse events of PPIs, including rare ones, such as mental disorders (hallucinations), bronchospasm, subacute cutaneous lupus erythematosus. The author focuses on the metabolism peculiarities of various PPIs and the possibility of adverse drug interactions. It is especially important to consider the PPIs administration in the treatment of elderly and senile patients, patients with liver failure, during the eradication of Helicobacter pylori.
Keywords: proton pump inhibitors, patient information leaflet, adverse events, eradication, Helicobacter pylori.

Введение
Особенности ИПП
Побочные эффекты ИПП
При проведении опроса среди членов Российской гастроэнтерологической ассоциации было установлено, что наиболее часто врачи назначают следующие ИПП: Омез ® , Нексиум ® , Нольпаза ® , Разо ® , Париет®. Предпочтения разделились примерно по 20%, но следует учесть, что Разо ® и Париет® — это рабепразол. Почему именно рабепразолу были отданы предпочтения врачей? Рассмотрим возможные побочные эффекты указанных препаратов, которые отражены в инструкции по медицинскому применению (ИМП) (табл. 1) [1, 4–7].
Побочные эффекты со стороны желудочно-кишечного тракта (ЖКТ), такие как боль в животе, диарея, метеоризм, запор, сухость во рту, отмечены в ИМП всех обсуждаемых ИПП (см. табл. 1). Но есть и отличия: например, стоматит и кандидоз ЖКТ указаны среди побочных эффектов препаратов Нексиум ® и Омез ® , а микроскопический колит — побочный эффект препаратов Нольпаза® и Нексиум®.
Применение Разо и Париета не вызывает нарушения зрения, которое отмечено в инструкциях препаратов Нольпаза ® , Нексиум ® и Омез ® (см. табл. 1). Именно из-за возникающей нечеткости зрения, а также из-за головокружения при приеме ряда ИПП пациентам следует соблюдать осторожность при управлении транспортными средствами, занятиях потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Говоря о более редких побочных эффектах ИПП, следует отметить психические нарушения. За более чем 30-летнюю практику я дважды сталкивался с возникновением галлюцинаций на фоне приема ингибиторов секреции соляной кислоты. Описание развития психических нарушений при приеме ИПП (омепразол, пантопразол) встречается в литературе [8, 9]. Опасность их кроется именно в их редкости при общей безопасности ИПП. При приеме рабепразола нарушений писхики не описано (среди побочных эффектов в инструкциях по применению указанных препаратов не отмечена ни депрессия, ни бессонница, ни агрессивное поведение, ни галлюцинации). Также к редким побочным эффектам ИПП относится бронхоспазм, который, согласно ИМП, возникает при приеме препаратов Омез ® и Нексиум ® и не отмечен в ИМП препаратов Нольпаза ® , Разо ® и Париет® (см. табл. 1).
Известно, что применение препарата Нольпаза ® (см. табл. 1) может вызывать подострую кожную красную волчанку (ПККВ). В ИМП отмечено, что в случае возникновения очагов поражения кожи, особенно на участках, подвергшихся воздействию солнечных лучей, а также при наличии артралгии, пациент должен незамедлительно обратиться за медицинской помощью. ПККВ вследствие предшествующей терапии ИПП может увеличить риск развития ПККВ при последующей терапии другими ИПП. Упоминаний о возникновении ПККВ при применении препаратов Омез ® , Нексиум ® , Разо ® и Париет® в инструкциях указанных препаратов нет. Но возможность появления алопеции и фотосенсибилизации зафиксирована у препаратов Нексиум ® и Омез ® [1].
Для большинства ИПП беременность и лактация являются противопоказаниями для применения (см. табл. 1), однако в ИМП препарата Омез ® указано, что результаты эпидемиологических исследований свидетельствуют об отсутствии клинически значимого негативного влияния омепразола на беременность и состояние здоровья плода или новорожденного. Омепразол проникает в материнское молоко, однако при применении препарата в терапевтических дозах негативного влияния на ребенка не ожидается.
Из ИПП, применяемых при почечной, печеночной недостаточности и у пожилых пациентов наибольшую безопасность продемонстрировал рабепразол (табл. 2). Так, в ИМП препаратов Разо ® и Париет® отмечено, что пациенты с хроническим компенсированным циррозом печени хорошо переносят рабепразол в дозе даже 20 мг 1 р/сут, хотя терапевтическая доза рабепразола составляет 10 мг/сут (самая низкая терапевтическая доза из всех ИПП).
Минимум побочных эффектов при использовании рабепразола обусловлен его фармакокинетическими особенностями. Рабепразол метаболизируется двумя путями: значительная часть принятой дозы рабепразола метаболизируется системно неферментативным путем с образованием тиоэфирных производных, а меньшая часть дозы подвергается метаболизму в печени посредством цитохрома Р450 (cytochrome P450, CYP) с образованием сульфонового и десметилового производных [3]. Например, при приеме эзомепразола рекомендуется контролировать международное нормализованное отношение (МНО) в начале и по окончании совместного применения эзомепразола и варфарина или других производных кумарина. Рабепразол, согласно результатам исследований с участием здоровых добровольцев, не вступает в фармакокинетические и клинически значимые взаимодействия с лекарственными веществами, которые метаболизируются системой CYР (варфарин, фенитоин, теофиллин и диазепам) [1].
Потенциал кислотосупрессии ИПП
J. Kirchheimer et al. [2] проанализировали данные 57 исследований и установили, что на основании результатов 24-часового изменения внутрижелудочного pH ИПП располагались в следующем порядке по возрастанию кислотосупрессии: пантопразол, лансопразол, омепразол, эзомепразол и рабепразол. Имея максимальный потенциал кислотосупрессии, чем достигается снижение фактора агрессии, рабепразол может усиливать факторы защиты при кислотозависимых заболеваниях. В доклинических исследованиях рабепразола, омепразола и лансопразола было показано, что только рабепразол усиливает выработку муцина. Рабепразол показал одинаковое позитивное действие на факторы защиты и у животных, и у человека. У 21 здорового добровольца в двойном слепом исследовании изучено влияние рабепразола на содержание муцина, слизи в желудочном соке и на вязкость желудочного сока. Содержание слизи при введении рабепразола достоверно увеличивалось как при стимулированном пентагастрином введении (3,36±0,39 против 1,50±0,32 мг/мл, p<0,001), так и при базальном состоянии (3,31±0,38 против 2,28±0,36 мг/мл, p<0,01). Содержание муцина при приеме рабепразола было в 2,6 раза выше (0,96±0,08 против 0,36±0,06 мг/мл, p<0,0001) при стимуляции и на 41% (0,82±0,09 против 0,58±0,09 мг/мл, p<0,05) выше в базальных условиях. Вязкость желудочного сока при введении рабепразола также была достоверно выше как в стимулированных (p<0,01), так и в базальных (p<0,05) условиях [10]. После введения рабепразола достоверно увеличивалась и концентрация пищеводного муцина [11]. Усиление секреции пищеводного муцина, основного защитного компонента пищеводного преэпителиального барьера, при введении рабепразола может трансформироваться в эзофагопротекторный потенциал у пациентов с рефлюкс-эзофагитом.
Эрадикация Helicobacter pylori
Показания и дозировки
Интересным в ИМП обсуждаемых ИПП представляется показание к эрадикации Helicobacter pylori (H. pylori) см. табл. 2). Самой радикальной в этом случае выглядит ИМП препарата Нольпаза ® , а самыми консервативными — ИМП препаратов Нексиум ® и Париет®. В работе A. Petrillo et al. [12] указано, что эпидемиологические данные свидетельствуют о том, что связанный с H. pylori атрофический гастрит может быть защитным фактором в отношении пищевода Барретта и, следовательно, узловых аденокарцином и аденокарцином пищевода. С учетом этих данных позиция препаратов Нексиум ® и Париет® выглядит более предпочтительной. В данной работе отмечено, что заболеваемость дистальными опухолями желудка, связанными с питанием и H. pylori, снизилась, а частота рака гастроэзофагеального соединения и пищевода стремительно увеличивается [9]. И здесь уместно сказать о том, что в большинстве ИМП обсуждаемых препаратов отсутствует такое показание к эрадикации, как инфицированность H. pylori. Среди показаний к эрадикации H. pylori представлены или только язвенная болезнь желудка и двенадцатиперстной кишки, или язвенная болезнь желудка и хронический гастрит, который, в отличие от функциональной диспепсии, может быть диагностирован лишь при гистологическом исследовании биоптата. Очень актуальным в этой части представляется ИМП препарата Нексиум ® , в которой имеются отдельные указания для эрадикации H. pylori при язвенной болезни желудка и язвенной болезни двенадцатиперстной кишки (лечение язвы двенадцатиперстной кишки, ассоциированной с H. pylori и профилактика рецидивов пептической язвы, ассоциированной с H. pylori). Дозы ИПП, применяемых для эрадикации H. pylori, и длительность самой эрадикационной терапии, указанные в ИМП обсуждаемых препаратов, представлены в таблице 2.
Практически ни одна из ИМП не укладывается в привычную для сознания врача схему эрадикационной терапии, либо длительность терапии кажется не такой, о которой обычно говорят на лекциях (для препаратов Нексиум ® и Париет® указанная продолжительность терапии ограничена одной неделей), либо комбинация антибиотиков исключает квадротерапию. Так, Нексиум ® однозначно рекомендуется комбинировать только с кларитромицином и амоксициллином [1]. Рекомендации по сочетанию ИПП с антибиотиками обоснованы тем, что у пациентов, получавших лечение метронидазолом в комбинации с другими антибиотиками, наблюдались случаи развития печеночной недостаточности, потребовавшей проведения трансплантации печени. При назначении метронидазола следует тщательно взвешивать показания для длительного приема данного лекарственного средства и при отсутствии строгих показаний избегать его длительного применения. При приеме тетрациклина, который тоже может входить в схемы эрадикационной терапии, со стороны пищеварительной системы, кроме рвоты, диареи, тошноты, эзофагита и гастрита, возможно развитие изъязвлений желудка и двенадцатиперстной кишки, гепатотоксическое действие, панкреатит, энтероколит.
Юридические аспекты
На сегодня понятно, что взаимодействие H. pylori с организмом человека сложное, в некоторой степени индивидуальное и до конца не изученное. Врач должен знать, что колонизация H. pylori снижает риск заболеваний пищевода (в том числе злокачественных) [12–14], бронхиальной астмы и атопии, а также, возможно, ожирения и сахарного диабета, и учитывать это при назначении лечения [15].
Клинические рекомендации
Мы уже обсудили выше, какой рекомендацией будут пользоваться все врачи при эрадикации H. pylori. Следующей клинической рекомендацией воспользуются не все, но большинство врачей: всем пациентам с язвенной болезнью с положительными результатами тестирования на инфекцию H. рylori с целью профилактики последующих рецидивов язвенной болезни рекомендуется проведение эрадикационной терапии (уровень убедительности рекомендаций B, уровень достоверности доказательств 2) [16].
Заключение
Сведения об авторе:
Плюснин Сергей Вениаминович — д.м.н., профессор, заслуженный врач Российской Федерации, заведующий кафедрой терапии Ночу Дпо "Медицинский Стоматологический Институт"; 127253, Россия, г. Москва, ул. Псковская, д. 9, к. 1; ORCID iD 0000-0002-4885-8976.
Прозрачность финансовой деятельности: автор не имеет финансовой заинтересованности в представленных материалах или методах.
Конфликт интересов отсутствует.
Статья поступила 07.07.2021.
Поступила после рецензирования 30.07.2021.
Принята в печать 24.08.2021.
About the author:
Sergey V. Plyusnin — Dr. Sc. (Med.), Professor, Honored Doctor of the Russian Federation, Head of the Department of Therapy, Non-State Educational Private Institution Of Additional Professional Education "Medical Dental Institute"; 9/1, Pskovskaya str., Moscow, 127253, Russian Federation; ORCID iD 0000-0002-4885-8976.
There is no conflict of interests.
Received 07.07.2021.
Revised 30.07.2021.
Accepted 24.08.2021.
Читайте также:

