Препараты для уменьшения интоксикации при раке
Обновлено: 19.04.2024
Опухолевая интоксикация констатирует отравление организма продуктами жизнедеятельности злокачественной опухоли. Патологическое состояние не удостоилось отдельного места в классификациях, но его не минует ни один пациент с генерализованным процессом, эпизоды возможны и во время лекарственного лечения.
Причины опухолевой интоксикации
Главная причина — наличие клеток, выделяющих биологически активные вещества. Некоторые новообразования вырабатывают вредные субстанции, но после удаления первичной опухоли все признаки отравления бесследно исчезают. Такого рода интоксикация возникает ещё до обнаружения опухоли, так бывает при аденокарциноме легкого, когда вырабатываемые клетками вещества вызывают боли в суставах, при злокачественных лимфомах токсины инициируют слабость с потливостью и высокой температурой.
Интенсивность проявлений зависит от биологических особенностей клеток и их общей массы, при прогрессировании с увеличением объема опухоли усиливаются и симптомы хронического отравления. Особенно выраженные признаки наблюдаются при распаде опухоли, аналогичное по проявлениям, но гораздо более тяжелое состояние может развиться при массированной гибели злокачественных клеток в результате химиотерапии. При лечении высокочувствительных к цитостатикам новообразований лимфатической ткани и крови проводится профилактика синдрома лизиса опухоли.
Симптомы интоксикации характерны для множественных метастазов в костях, когда к токсичным клеточным продуктам присоединяется негативное действие выходящего из распадающейся костной ткани кальция — гиперкальциемия.

Симптомы опухолевой интоксикации
Интоксикация — это отравление, но не острое, а хроническое, то есть признаки его нарастают постепенно. Исключение составляет только синдром лизиса опухоли во время химиотерапии, когда клинические проявления нарастают стремительно вплоть до острой почечной недостаточности.
Типичны для интоксикации слабость и быстрая утомляемость, доводящие пациента до постоянного пребывания в постели. Возможно повышение температуры — от субфебрилитета при генерализованном процессе до 40°С при распаде крупного опухолевого конгломерата с образованием некротической полости диаметром в несколько сантиметров.
У всех пациентов изменяется цвет кожи — от бледного до землистого, всё индивидуально, но заметно окружающим. Присоединяется небольшая отечность поверхностных тканей — пастозность, повышается потливость, особенно ночная.
Продукты ракового метаболизма циркулируют в крови, оседая в органах и нарушая их функционирование. Повреждение сердечно-сосудистой системы проявляется изменением ритма сердца и учащением дыхания, нервной системы — депрессией с дневной сонливостью при нарушениях ночного сна. Почечные канальцы забиваются продуктами метаболизма, снижая выделительную функцию.
Частично токсичные продукты выводятся слизистой оболочкой желудочно-кишечного тракта, что приводит к её сухости и, как следствие, нарушению аппетита. Печень активно борется с токсинами, но и она перестает справляться, изменяя содержание в плазме микроэлементов и вязкость крови. При тяжелой опухолевой интоксикации постоянная тошнота сменяется не приносящей облегчения рвотой.
Диагностика и лечение опухолевой интоксикации
В первую очередь об интоксикационном синдроме свидетельствует совокупность жалоб пациента и его внешний вид, начиная с нездоровой окраски кожи.
В общем анализе крови интоксикацию заметить непросто, но в биохимическом может повыситься концентрация печеночных трансаминаз, креатинина, мочевой кислоты, калия и фосфатов.
Стимуляция аппетита заключается не только в приеме противорвотных и даче стимуляторов аппетита, необходима тщательная коррекция микроэлементов и макронутриентов — белков, жиров и углеводов. Недостаточно вызвать аппетит, надо предоставить питание, не усугубляющее опухолевую интоксикацию и помогающее восстановлению.
Длительность и интенсивность медикаментозной терапии зависит от степени выраженности интоксикации. В тяжелых случаях может потребоваться гемосорбция — очищение крови специальной аппаратной системой, или только очищение плазмы при плазмаферезе.
Адекватная терапия опухолевой интоксикации не только улучшит состояние пациента, но и увеличит продолжительность его жизни, сделав её качественней и спокойнее.
Не всегда при злокачественном заболевании возможно остановить протекание болезни, но необходимо стремиться сделать жизнь онкобольного достойной. В нашей клинике помогают всем онкологическим пациентам и в любой период развития опухоли.

Раковая интоксикация (эндотоксикоз) – это патологический процесс, который развивается в организме онкологического больного в результате распада злокачественной опухоли. Состояние характерно для поздних стадий рака. Вызвать опухолевую интоксикацию может и активная противораковая терапия.
К характерным признакам эндотоксемии (отравления организма продуктами опухолевого распада) относятся тошнота, рвота, утомляемость, слабость, снижение веса, сухость слизистых, боли в суставах, психические нарушения и др. Опухолевая интоксикация, клинические проявления которой имеют интенсивную симптоматику, приводит к системным нарушениям в виде почечной и печеночной недостаточности. Возникает риск развития инфекционных осложнений и сепсиса.
Если проигнорировать симптомы интоксикации и не принять меры по их устранению, пациент быстро теряет силы и вес, развивается кахексия. Далее человек впадает в состояние комы, из которого его вывести практически невозможно. Принимать лечебные меры нужно незамедлительно при появлении первых подозрений на раковую интоксикацию.

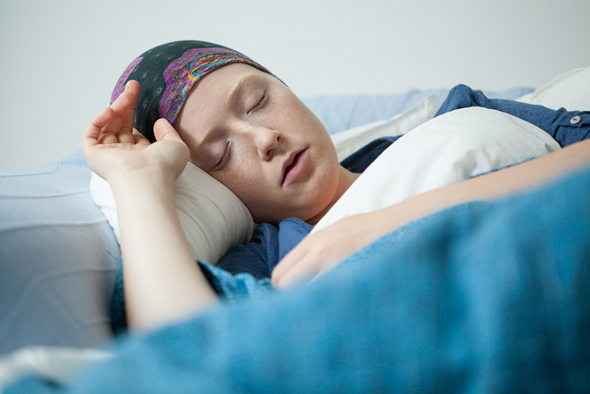
Причины опухолевой интоксикации
Отличительной особенностью раковых заболеваний является быстрый и неконтролируемый рост злокачественного образования, клетки которого продуцируют токсины. Сосуды, обеспечивающие кровоснабжение опухоли, растут медленнее, чем сама опухоль.
Способность раковых клеток выживать в условиях гипоксии, несколько затягивает процесс. Но гибель клеток все же происходит. Их огромное количество распадается и попадает в кровоток. Большая концентрация в крови погибших клеток вызывает интоксикацию. Зараженная кровь продолжает циркулировать по всему организму, затрагивая все органы. Это приводит к необратимому процессу и системным нарушениям.
В патогенезе раковой интоксикации:
- повышение уровня мочевой кислоты;
- увеличение числа ионов калия;
- рост процентного соотношения фосфатов;
- снижение концентрации кальция.
Рассмотренные вещества образуются при отмирании тканей злокачественного образования и проникают в кровоток. Этот процесс приводит к осложнениям из-за нарастающего обезвоживания организма. Отмечается перевозбуждение организма вследствие снижения уровня ионов кальция на фоне излишней концентрации фосфатов. Из-за повышенного содержания кальция происходит негативное воздействие на функционирование миокарда, что проявляется аритмией.
Синдром опухолевой интоксикации характерен для более обширных новообразований. Гибель большого количества раковых клеток – основная причина распада опухоли и отравления организма. На степень развития интоксикационного процесса влияет природная специфика атипичных клеток и их общее количество.
Яркие признаки отравления организма при распаде раковых клеток часто наблюдаются в результате проведения интенсивного химиотерапевтического лечения. При проведении химио- или лучевой терапии речь идет о массовой гибели раковых клеток. В дальнейшем продукты распада попадают в кровь и вызывают интоксикационное воздействие на организм больного. Вещества, которые находятся в составе препаратов, используемых при химиотерапии, плохо выводятся из организма и имеют свойство накапливаться. Опухолевая интоксикация проявляется яркой выраженностью уже в первые дни химиотерапевтических процедур.
Существует ряд факторов, которые усложняют и усугубляют течение интоксикационного процесса:
- возраст и общее состояние пациента;
- наличие сопутствующих заболеваний;
- интенсивность процесса распада;
- кровопотери в результате оперативного вмешательства.
Прогноз жизни при раковой интоксикации на последних стадиях является неблагоприятным. Летальный исход возможен при внутреннем кровотечении, истощении и тромбозе. Огромный риск смерти при раковой интоксикации возникает при почечной недостаточности, нарушении сердечной деятельности, а также при поражении органов метастазами.
Симптомы раковой интоксикации
Симптомы опухолевой интоксикации характеризуются постепенным проявлением. Исключением является развитие синдрома лизиса опухоли после проведения химиотерапии. Быстрый рост симптоматики требует моментального реагирования, имеется риск развития острой стадии почечной недостаточности.
Типичные симптомы раковой интоксикации:
- Слабость и усталость. Появляются даже при незначительных физических нагрузках. Пациент большую часть времени проводит в постели.
- Повышение субфебрильной температуры. Образование некротической полости и распад большей части опухолевого конгломерата (может сопровождаться повышением температуры до 400C).
- Изменение цвета кожи. Сначала становится бледной, затем появляется землистый оттенок. Бледность может быть причиной развития анемии, в результате нарушения работы почек и эндокринной системы.
- Нарушение сердечной деятельности. Меняется ритм сердечных сокращений, учащается дыхание.
- Повреждение нервной системы. Ночной сон нарушается, появляется дневная сонливость с признаками депрессии. Характерны периодические приступы мигрени и головокружения.
- Нарушение функции почек. Продукты метаболизма блокируют почечные канальцы, в результате снижается мочевыделительная функция. Большая концентрация мочевины в крови проявляется зудом и образованием на теле пятен, похожих на синяки.
Опухолевая интоксикация проявляется повышенной потливостью и отечностью. Постоянное ощущение тошноты, не проходит даже после рвоты. Нарушается функция печени, что приводит к уменьшению сопротивляемости токсинам и изменению вязкости крови.
Диагностика и лечение опухолевой интоксикации
На первом этапе диагностических мероприятий проводится осмотр больного и оценка симптомов раковой интоксикации и прогноза для жизни. Далее назначаются анализы крови на биохимию и дополнительные инструментальные исследования. Важную роль здесь играет определение основной причины, повлекшей развитие симптоматики. Если наблюдается характерная для опухолевой интоксикации картина клинических проявлений, назначается комплексное исследование.
Основные диагностические мероприятия при раковой интоксикации:
- общий анализ мочи и крови;
- анализ крови на биохимию;
- кровь на онкомаркеры;
- сцинтиграфия костного аппарата;
- осмотр гинеколога (для женщин);
- рентген грудной клетки;
- УЗИ брюшной полости и органов малого таза.
План проводимых исследований имеет индивидуальный подход. Для определения степени тяжести опухолевой интоксикации при диагностированном раке используется перечень стандартных анализов.
Однозначное определение эндогенной или раковой интоксикации дать сложно. Это связано с тем, что интоксикация при почечной недостаточности имеет определенную схожесть с эндотоксикозом. Многие промежуточные метаболиты, которые оказывают токсическое действие, до сих пор не идентифицированы. В качестве неспецифического маркера используется высокий уровень олигопептидов. Без тщательного исследования и коррекции раковой интоксикации адекватное лечение не может быть проведено, поэтому и полного излечения быть не может.
Лечение раковой интоксикации
При интенсивном росте опухолевого очага признаки интоксикации могут наблюдаться на более ранних стадиях. Поэтому онкологи заранее назначают пациенту мероприятия для предупреждения или облегчения интоксикационного синдрома. Все известные процедуры (гемодиализ, экстракорпоральная гемосорбция и др.) имеют недостаточный уровень эффективности и кратковременный результат.
Для улучшения показателей проводимого лечения при раковой интоксикации используется комплексный подход:
- углеродные волокнистые и гранулированные энтеросорбенты;
- экстракорпоральная гемосорбция (при химиотерапии).
Полученный результат является кратковременным, но мощным. Энтеросорбция гранулированными или волокнистыми сорбентами позволяет добиться медленного, но существенного снижения уровня эндотоксемии. При проведении многочисленных исследований удалось установить, что энтеросорбенты при пероральном приеме дают длительный и выраженный детоксицирующий эффект. Это именно то, что нужно при хронической раковой интоксикации.
Терапевтические мероприятия направлены на устранение симптоматики и восстановление функций поврежденных органов и систем. Тяжелая опухолевая интоксикация предусматривает применение плазмафереза или гемодиализа.
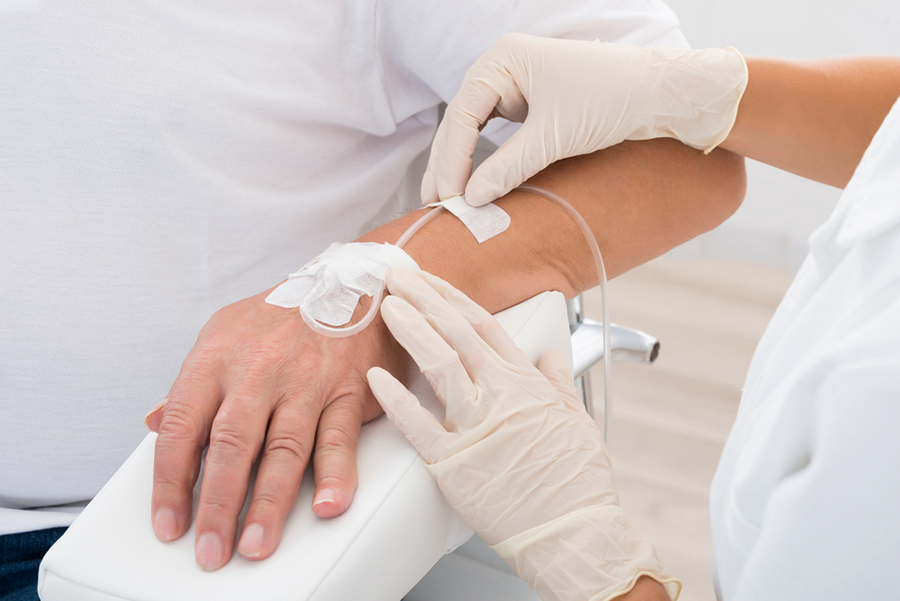
Основные направления лечения больных с опухолевой интоксикацией:
- Рвотная симптоматика устраняется противорвотными средствами (метоклопрамид, домперидон).
- При запорах назначаются слабительные препараты (бисакодил, макрогол).
- Широко используются сорбенты, зарекомендовавшие себя, как средство для детоксикации. Они обладают свойством связывать токсины, и с каловыми массами выводят их из организма.
- Проводится дезинтоксицирование организма введением большого количества жидкости, с последующим ускоренным ее выведением.
- Пациентам с низким уровнем гемоглобина назначаются железосодержащие препараты, в виде капельниц или инъекций (эритропоэтин).
- При наличии психических расстройств пациентам назначаются седативные средства, при депрессивных состояниях – антидепрессанты и транквилизаторы.
В соответствии с показателями долголетней практики, у большей части пациентов с эндотоксикозом происходит развитие сердечной или почечной недостаточности. Эти патологии в большинстве случаях являются причиной скоропостижной смерти больного. При принятии неотложной онкологической помощи такой исход удается предотвратить. Лечебная программа, направленная на устранение выраженной симптоматики, позволяет улучшить состояние больного, повысить качество и продолжительность жизни. Основным путем улучшения прогноза жизни при раковой интоксикации является усиление ранней диагностики злокачественного процесса с помощью проведения профилактических программ в практику здравоохранения (поезд здоровья, онкопатруль и др.).
Режим питания при раковой интоксикации предусматривает употребление еды небольшими порциями. При этом между приемами пищи интервалы должны быть небольшими. В рацион следует ввести самые необходимые для жизнеобеспечения минералы и микроэлементы. Ни в коем случае нельзя допустить обезвоживания. Известно, что жидкость выводит токсины. При невозможности приема пищи, ее вводят парентерально. Ежедневный рацион должен включать продукты, насыщенные витаминами и минералами. Обязательное составляющее – белок, углеводы и жиры. Рекомендована умеренная физическая активность. Для лежачих больных необходим массаж.
Раковая интоксикация – патологическое состояние, обусловленное распространенным онкологическим процессом и распадом злокачественной опухоли. Возникает на поздних стадиях онкологического заболевания. Может провоцироваться активной противораковой терапией. Проявляется слабостью, утомляемостью, бледностью кожи, сухостью слизистых, тошнотой, рвотой, потерей веса и аппетита, потливостью, гипертермией, костно-суставными болями, нарушениями сна, психическими расстройствами, анемией и снижением иммунитета. Диагноз выставляется на основании анамнеза, клинической симптоматики, результатов анализов и инструментальных исследований. Лечение симптоматическое.
Общие сведения
Раковая интоксикация – комплекс расстройств, возникающих у онкологических больных при отравлении организма продуктами распада злокачественной опухоли. Выявляется преимущественно на терминальных стадиях заболевания, рассматривается как одна из основных причин гибели пациентов. Кроме того, раковая интоксикация часто наблюдается при проведении химиотерапии, является закономерным следствием активного противоракового лечения, вызывающего разрушение опухоли.
Раковая интоксикация может провоцировать нарушения деятельности различных органов и систем, в том числе – почечную и печеночную недостаточность, сепсис и другие тяжелые инфекционные осложнения, что обуславливает важность продуманного подбора дозировок и видов лекарственных препаратов с учетом общего состояния больного, а также наличия тех или иных хронических заболеваний. Лечение осуществляют специалисты в области онкологии.

Причины раковой интоксикации
Одной из отличительных особенностей злокачественной опухоли является ее способность к быстрому неконтролируемому росту. Как правило, темпы роста сосудов, обеспечивающих кровоснабжение новообразования, отстают от скорости роста опухолевой ткани. Злокачественные клетки достаточно устойчивы к гипоксии и могут некоторое время существовать в условиях недостаточного кровоснабжения, однако рано или поздно умирают. Обычно этот процесс наблюдается при опухолях достаточно большого размера. Массовая гибель клеток становится причиной распада новообразования и вызывает раковую интоксикацию.
В организм попадает большое количество продуктов распада, которые провоцируют расстройства всех видов обмена веществ и нарушения деятельности различных органов и систем. Раковая интоксикация становится причиной повышения уровня мочевины. Кристаллы мочевины оседают в почечных канальцах, вызывая развитие почечной недостаточности, которая еще больше усугубляет обменные нарушения. Из-за увеличения количества фосфатов возникает дефицит ионов кальция, следствием которого становятся нарушения работы нервной системы. Повышение уровня кальция негативно влияет на работу сердца. У пациентов с раковой интоксикацией возникают аритмии, в тяжелых случаях возможно прекращение сердечной деятельности. Увеличение количества свободных радикалов стимулирует распад эритроцитов и развитие анемии.
Проявления раковой интоксикации весьма вариабельны. Формирование клинической картины определяется тяжестью состояния пациента, скоростью разрушения новообразования, количеством токсических веществ, попадающих в основной кровоток, особенностями локализации и течения онкологического процесса, масштабом хирургического вмешательства, наличием и объемом кровопотери (как возникшей в ходе операции и послеоперационном периоде, так и связанной с распадом опухоли), присоединением воспалительных осложнений, дозой химиопрепарата и другими факторами.
Симптомы раковой интоксикации
Наиболее постоянными признаками раковой интоксикации являются прогрессирующая слабость и беспричинная утомляемость. Наблюдаются характерные изменения внешнего вида: дефицит массы тела (в тяжелых случаях – вплоть до кахексии), бледный, землистый или желтоватый оттенок кожи, сухость кожи и слизистых оболочек. Возможен цианоз дистальных отделов конечностей. У больных с нарушениями функции печени выявляется иктеричность склер. Пациенты с раковой интоксикацией предъявляют жалобы на усиленное потоотделение. Как правило, потливость более выражена в ночное время.
В ходе опроса врач устанавливает, что резкое снижение веса произошло в течение короткого промежутка времени и сопровождалось нарушениями аппетита: отвращением к еде (особенно – к мясным продуктам), извращением вкуса и т. д. Кроме того, при раковой интоксикации наблюдаются диспепсические расстройства: тошнота, рвота и нарушения стула. Возможны запоры, поносы или чередование запоров и поносов. Отмечается длительное повышение температуры до субфебрильных (при некоторых заболеваниях – до фебрильных) цифр. Возникают боли в костях и суставах.
Больные с раковой интоксикацией могут сообщать о периодических мигренях и приступах головокружения. Расспрос пациентов и их родственников позволяет выявить изменения психического и эмоционального статуса. Могут наблюдаться апатия, раздражительность и эмоциональная лабильность. Раковая интоксикация нередко сопровождается депрессивными расстройствами. Возможны нарушения сна: бессонница, поверхностный сон, трудности при засыпании, ночные и ранние пробуждения. Часто обнаруживаются нарушения сердечного ритма. При раковой интоксикации существует высокая вероятность развития тромбозов и склонность к возникновению инфекционных осложнений. В анализе крови обнаруживаются признаки анемии (обычно – умеренной нормохромной).
Диагностика раковой интоксикации
Диагноз выставляется с учетом анамнеза, жалоб, данных объективного осмотра и результатов дополнительных исследований. Решающую роль в определении причины раковой интоксикации играет выявление основной патологии. При характерной клинической картине и отсутствии установленного диагноза онкологического заболевания пациентам с подозрением на раковую интоксикацию назначают комплексное обследование, которое включает в себя общие анализы крови и мочи, биохимический анализ крови, анализ крови на онкомаркеры, рентгенографию грудной клетки, сцинтиграфию костей скелета, УЗИ брюшной полости, УЗИ малого таза, гинекологический осмотр и другие исследования. План обследования определяется индивидуально.
При уже диагностированном онкологическом заболевании требуется оценка выраженности раковой интоксикации для определения тактики лечения (составления плана химиотерапии, принятия решения об оперативном вмешательстве, подбора симптоматических препаратов и т. д.). Для оценки тяжести раковой интоксикации используются стандартные показатели крови: уровень мочевины, креатинина и С-реактивного белка, реактивный ответ нейтрофилов, лейкоцитарный индекс интоксикации и т. д. Наряду с перечисленными показателями могут потребоваться данные о состоянии различных органов и систем больного с раковой интоксикацией, полученные при проведении ЭКГ, анализов мочи, анализов крови на гормоны и других исследований.
Лечение раковой интоксикации
Лечение симптоматическое, включает в себя мероприятия по детоксикации, устранению или смягчению клинических проявлений и коррекции нарушений деятельности различных органов и систем. Осуществляют энтеросорбцию, гемосорбцию и аппликационную сорбцию. Пациентам выписывают сорбенты для приема внутрь. При тяжелой раковой интоксикации применяют гемодиализ или плазмаферез. При наличии открытых ран в области распада опухоли проводят перевязки с сорбентами местного действия.
При рвоте больным с раковой интоксикацией назначают противорвотные средства (домперидон, метоклопрамид), при запорах – слабительные для перорального приема и ректальные свечи (макрогол, препараты сены, бисакодил, касторовое масло и пр.). При анемии используют препараты железа внутрь и парентерально, применяют эритропоэтин. Выбор медикаментов при раковой интоксикации, сопровождающейся психическими расстройствами, зависит от вида и тяжести расстройств. При эмоциональной лабильности назначают мягкие седативные средства, при нарушениях сна – снотворные, при депрессии – транквилизаторы и антидепрессанты.
Прогноз определяется причинами раковой интоксикации, тяжестью основного процесса, возрастом и общим состоянием больного, наличием и тяжестью сопутствующей соматической патологии. Состояния, возникающие при распаде крупных распространенных опухолей в запущенных стадиях заболевания, являются прогностически неблагоприятными. Больные с раковой интоксикацией погибают от кровотечений, нарушений деятельности органов, пораженных первичной опухолью или гематогенными метастазами, а также от истощения, инфекционных осложнений, почечной недостаточности, тромбозов, нарушений сердечной деятельности или полиорганной недостаточности, обусловленной обменными расстройствами и ослаблением организма. При раковой интоксикации, возникшей в процессе химиотерапии, прогноз может быть благоприятным. При приеме химиопрепаратов это – временное состояние, являющееся частью лечебного процесса.

Лейкопения – состояние, при котором уровень лейкоцитов в крови ниже 4000 в 1 мкл. Спровоцировать его развитие могут различные факторы: патогенные агенты, воспалительные процессы, аутоиммунные заболевания, генетические нарушения и многое другое. Проявляется лейкопения в виде повышенной восприимчивости организма к инфекциям. При соблюдении мер безопасности и рекомендаций врача обычно протекает бессимптомно. Выявить лейкопению удастся по анализу капиллярной или венозной крови.
Разновидности лейкопений
Даже у абсолютно здоровых людей может быть лейкопения. Статистика ВОЗ называет, что около 3% населения имеют пониженный уровень лейкоцитов в крови. По происхождению это заболевание бывает 2 видов:
- Первичное. В таком случае болезнь носит наследственный характер. Она развивается из-за генетических детерминированных нарушений, из-за которых в костном мозге не созревает достаточное количество лейкоцитов;
- Вторичное. Это приобретенная лейкопения. Она возникает из-за влияния патологических факторов, таких как облучение или длительный прием лекарственных препаратов.
Также лейкопению принято различать по механизму развития. Болезнь развивается из-за:
- Нарушения поступления лейкоцитов из костного мозга;
- Неправильного перераспределения лейкоцитов;
- Сокращения времени пребывания лейкоцитов в крови.
Лейкоциты состоят из нескольких типов клеток. При диагностике болезни нужно определять, какого именно фрагмента в крови недостаточно. В зависимости от типа недостающих клеток, существуют следующие формы лейкопений:
- Нейтропения – снижение уровня нейтрофилов;
- Лимфопения – недостаток уровня лимфоцитов;
- Эозинопения – концентрация эозинофилов не достигает 1%;
- Моноцитопения – показатель моноцитов ниже 2%;
- Агранулоцитоз – полное или почти полное отсутствие нейтрофилов в крови.


Основные симптомы лейкопении
При незначительном снижении уровня лейкоцитов выявить лейкопению удастся только при помощи клинического анализа крови. Болезнь не будет проявлять себя явными признаками. Если же отклонение от нормы значительное, пациенты могут жаловаться на следующие симптомы:
- Повышение температуры тела до 37,5-38 градусов;
- Постоянное ощущение усталости, общую слабость;
- Головную боль, головокружение;
- Ощущение нехватки воздуха;
- Боли в животе, расстройство пищеварения;
- Ломоту в костях, суставах.
Пациенты с лейкопенией склонны к различным инфекционным процессам. Это происходит из-за снижения иммунных способностей организма. Первыми поражаются слизистые оболочки ротовой полости, так как в них изначально присутствует мощная бактериальная флора. У пациента развивается язвенно-некротический стоматит.
Затем поражается мочеполовая система. Больные жалуются на учащенное болезненное мочеиспускание, ощущение неполного опорожнения мочевого пузыря. У женщин наблюдаются проблемы с менструацией: она становится нерегулярной, удлиненной. Наибольшую опасность представляет некротическая энтеропатия – тяжелое поражение кишечника.
Самым грозным осложнением лейкопении является сепсис. Это – генерализованное воспаление на фоне локальной инфекции. В таком случае вероятность смертельного исхода высока.
Лейкопения – это рак?
Особую опасность представляет ситуация, когда снижение лейкоцитов сопровождается появлением синяков по всему телу, повышением температуры тела, быстрой утомляемостью, многочисленными кожными высыпаниями. В таком случае нужно пройти комплексную диагностику и обратиться к врачу.
Лейкопения является одним из симптомов рака крови. Это опасное заболевание, главная коварность которого – отсутствие опухоли, которую нужно удалять. Именно поэтому лейкопения требует обязательного диагностического обследования, ведь онкология, выявленная на начальных стадиях, хорошо поддается лечению.
Причины возникновения лейкопений
Спровоцировать развитие лейкопении способно множество факторов. Очень важно определить точную причину этого нарушения, ведь от нее будет зависеть и тактика лечения. Причиной снижения лейкоцитов в крови человека могут стать следующие факторы:
- Патологии клеток крови и костного мозга: апластическая анемия, миелофиброз, миелодиспластические синдромы, гиперспленизм, миелопролиферативный синдром;
- Наследственные заболевания: миелокатексис, синдром Костмана;
- Инфекции: туберкулез, ВИЧ, СПИД, различные вирусные заражения;
- Аутоиммунные патологии: системная красная волчанка, полиневрит, ревматоидный артрит;
- Авитаминоз: недостаток витаминов группы В, меди, цинка, других минералов. Обычно происходит из-за несбалансированного питания;
- Прием некоторых лекарственных препаратов: Интерферона, Клозапина, Миноциклина, Циклоспорина, некоторых антибактериальных средств;
- Саркоидоз: заболевание, при котором наблюдается слишком бурная реакция иммунитета;
- Онкология: при раке происходит снижение концентрации белых кровяных клеток из-за повреждения костного мозга. Подобный клинический признак наблюдается и у пациентов после лучевой либо химиотерапии, пересадки костного мозга.
Диагностика лейкопении
Определить лейкопению можно при помощи общего анализа крови. Именно он показывает концентрацию лейкоцитов в крови. Дополнительно проводят исследование крови с дифференциацией лейкоцитов: исследование помогает определить, каких именно белых кровяных клеток недостаточно. Этот анализ позволяет обозначить круг возможных причин лейкопении. Также диагностика лейкопений включает:
- Гемограмму – определяет абсолютное количество эритроцитов, лейкоцитов, тромбоцитов, показывает процентное соотношение различных видов белых клеток;
- Иммунологический анализ крови – выявляет антигранулоцитарные и антинуклеарные иммуноглобулины;
- Биохимический анализ крови – отражает количество фолатов, витамина В12, печеночных трансаминаз, билирубина в крови;
- Цитологическое исследование – направлено на определение конкретного типа лейкопений, устанавливает механизм ее развития;
- Анализ крови на гепатиты, ревматоидный фактор.
Может потребоваться проведение и других исследований. Они нужны для определения причины лейкопении. Через некоторое время после первого обследования назначаются повторные анализы – это необходимо для получения достоверного результата.
Методы лечения
При первых признаках инфекции пациентам с лейкопенией назначают антибактериальные препараты. Первоначально применяются антибиотики широкого спектра действия. Когда будут готовы результаты о чувствительности микроорганизмов, подбирается подходящая терапия. Если состояние пациента улучшается в течение 72 часов, то схема лечения подобрана эффективно. Препараты продолжают принимать в течение недели или до полного исчезновения симптомов в той же дозировке.
Отсутствие эффекта от лечения говорит об антибиотикорезистентности, когда микроорганизмы устойчивы к действующим веществам препарата, или наличии двух и более инфекций. Если у пациента нет признаков заражения, но уровень лейкоцитов значительно снижен, проводится профилактическая терапия антибиотиками. При грибковых инфекциях показаны противогрибковые препараты.
Для лечения лейкопении также назначают колониестимулирующие факторы – факторы роста. Они заставляют красный костный мозг активнее продуцировать новые кровяные клетки. Используются препараты 2 видов:
- G-CSF – гранулоцитарные колониестимулирующие факторы. Способствуют быстрому росту нейтрофилов;
- GM-CSF – гранулоцитарно-макрофагальные колониестимулирующие факторы. Вызывают ускоренную выработку гранулоцитов и макрофагов.
В качестве поддерживающей терапии назначаются глюкокортикостероиды, анаболические стероиды, витаминные комплексы. Они не помогают вырабатывать лейкоциты, но препятствуют их стремительному разрушению.
При развитии тяжелого инфекционного процесса (сепсиса, пневмонии, некротической энтеропатии) и при отсутствии эффекта от антибиотиков проводится переливание лейкоцитарной массы. Если лейкопения возникла на фоне лучевой либо химиотерапии, необходимо пересмотреть используемую схему терапии или заменить отдельные препараты.
Трансплантация костного мозга при лейкопении
В редких случаях лейкопения обусловлена низким уровнем агранулоцитов в крови. В таком случае медикаментозная терапия неэффективна. Химиотерапия, которая необходима для лечения онкологии, разрушает собственный костный мозг. Для терапии лейкопении такого типа проводится трансплантация костного мозга – пересадка части стволовых клеток. Именно они и будут вырабатывать новые лейкоциты.
При низком уровне лейкоцитов также проводится переливание лейкоцитарной массы. Обычно процедура назначается пациентам с системной вирусной инфекцией при отсутствии эффекта от антибиотиков. Однако при локальном бактериологическом воспалении или же инфицировании вирусом переливание лейкоцитарной массы не дает никакого результата.
Прогноз и профилактика
Смертность от лейкопении на фоне лучевой или химиотерапии составляет 4-6%. Если болезнь не вызвана лечением онкологии, то показатель колеблется на уровне 5-10%. Еще 20 лет назад это значение достигало 20%. Снижения данного параметра удалось добиться за счет разработки адекватной антибактериальной терапии, грамотного ухода за больным, применения КСФ.
Высокая смертность наблюдается у пожилых пациентов, у людей с почечной и печеночной недостаточностями, если лейкопения осложнилась септическим шоком либо бактериемией. Специфической профилактики лейкопении не существует. Врачи дают следующие обязательные к выполнению рекомендации:
- Каждую неделю сдавайте анализ крови;
- Пропивайте витаминные комплексы;
- Минимизируйте стрессы и переживания;
- Носите защитную маску в общественных местах;
- Соблюдайте правила личной гигиены, ежедневно принимайте душ;
- Не контактируйте с домашними животными, их фекалиями;
- Откажитесь от бритья, маникюра (всего, из-за чего можно пораниться);
- Откажитесь от работ с почвой;
- Правильно и полноценно питайтесь;
- Откажитесь от вредных привычек;
- Строго соблюдайте протокол химиотерапии.
Лейкопения – опасное состояние. Оно требует обязательного соблюдения всех рекомендаций врача. Игнорирование этих правил часто приводит к смертельным осложнениям. Если вы проходите химиотерапию, нужно быть максимально внимательным к своему здоровью. Контролировать течение лейкопении и подобрать эффективное лечение вам помогут в медицинском центре Медскан. Опытные врачи смогут разработать индивидуальную схему терапии, которая снизит риск развития каких-либо осложнений.
Распад опухоли — это закономерное следствие слишком активного роста ракового узла по периферии или осложнение избыточно высокой реакции распространённого злокачественного процесса на химиотерапию.
Не каждому пациенту доводится столкнуться с тяжелой проблемой распада ракового процесса, но при любой интенсивности клинических проявлений инициируемое распадом злокачественной опухоли состояние непосредственно угрожает жизни и радикально меняет терапевтическую стратегию.

Распад опухоли: что это такое?
Распад — это разрушение злокачественного новообразования, казалось бы, что именно к распаду необходимо стремиться в процессе противоопухолевой терапии. В действительности при химиотерапии происходит уничтожение раковых клеток, только убийство органичное и не массовое, а единичных клеток и небольших клеточных колоний — без гибели большого массива ткани с выбросами в кровь из распадающихся клеток токсичного содержимого.
Под действием химиотерапии клетки рака приходят не к распаду, а к процессу апоптоза — программной смерти. Останки раковых клеток активно утилизируются фагоцитами и уносятся прочь от материнского образования, а на месте погибших возникает нормальная рубцовая ткань, очень часто визуально не определяющаяся.
Регрессия злокачественного новообразования в форме апоптоза происходит медленно, если наблюдать за новообразованием с перерывами в несколько дней, то заметно, как по периферии раковый узел замещается совершенно нормальной тканью и сжимается в размере.
При распаде раковый конгломерат не замещается здоровыми клетками соединительной ткани, мертвые клеточные пласты формируются в очаг некроза, отграничивающийся от остальной раковой опухоли мощным воспалительным валом. Внутри злокачественного новообразования некроз не способен организоваться и заместиться рубцом, он только увеличивается, захватывая новые участки ракового узла, походя разрушая опухолевую сосудистую сеть. Из мертвого очага в кровь поступают продукты клеточного гниения, вызывая интоксикацию.
Массированный выброс клеточного субстрата становится причиной тяжелейшей интоксикации, способной привести к смерти.
Причины распада злокачественной опухоли
Инициируют распад ракового образования всего только две причины: сама жизнедеятельность клеток злокачественной опухоли и химиотерапия.
Первая причина спонтанного — самопроизвольного распада характерна для солидных новообразований, то есть рака, сарком, злокачественных опухолей головного мозга и меланомы. Вторая причина распада типична для онкогематологических заболеваний — лейкозов и лимфом, при онкологических процессах встречается чрезвычайно редко.

Второй вариант распада, типичный для онкогематологических заболеваний, можно констатировать по клиническим симптомам тяжелейшей интоксикации с осложнениями — тумор-лизис-синдрому (СОЛ) и биохимическим анализам крови, где резко повышена концентрация мочевой кислоты, калия и фосфора, но существенно снижен кальций. Конкретная побудительная причина для развития СОЛ — обширное злокачественное поражение с очень высокой чувствительностью к химиотерапии.
При онкологических процессах — раках, саркомах, меланоме реакция на цитостатики преимущественно умеренная и не столь стремительная, поэтому СОЛ принципиально возможен только в исключительных случаях мелкоклеточного, недифференцированного или анаплазированного злокачественного процесса.
Симптомы распада злокачественной опухоли
Клиническим итогом спонтанного распада раковой опухоли становится хроническая интоксикация, нередко сочетающаяся с симптомами генерализованного воспаления вследствие образования гнойного очага. Симптомы разнообразны, но у большинства отмечается прогрессивно нарастающая слабость, повышение температуры от субфебрильной до лихорадки, сердцебиение и даже аритмии, изменение сознания — оглушенность, нарушение аппетита и быстрая потеря веса.
Локальные проявления спонтанного разрушения раковой опухоли определяются её локализацией:
- рак молочной железы, меланома и карцинома кожи, опухоли ротовой полости — гнойная, обильно секретирующая открытая язва с грубыми подрытыми краями, часто источающая гнилостный запах;
- распадающаяся карцинома легкого — при прободении некротической полости в крупный бронх возникает приступообразный кашель с гнойной мокротой, нередко с прожилками крови, иногда случается обильное легочное кровотечение;
- разрушение новообразования органов желудочно-кишечного тракта — развитие локального перитонита при прободении ракового конгломерата в брюшную полость, кровотечение с чёрным стулом и рвотой кофейной гущей;
- распадающаяся карцинома матки — интенсивные боли внизу живота, нарушение мочеиспускания и дефекации при образование гнойных свищей.
Синдром опухолевого лизиса при лейкозах и лимфомах потенциально смертельное состояние, приводящее:
- в первую, очередь к осаждению кристаллов мочевой кислоты в почечных канальцах с выключением функции и острой почечной недостаточностью;
- дополнительно повреждает почки быстрое закисление крови — лактатацидоз;
- снижение уровня кальция и повышение фосфатов инициирует судорожный синдром, дополняемый неврологическими проявлениями вследствие выброса цитокинов;
- повышения калия негативно отражается на сердечной деятельности;
- выброс биологически-активных веществ из клеток приводит к повышению проницаемости мелких кровеносных сосудов, что снижает уровень белков и натрия крови, уменьшает объем циркулирующей плазмы, клинические проявляется падением давления и усугублением поражения почек;
- обширные и глубокие нарушения метаболизма во всех системах органов с исходом в полиорганную недостаточность.
Лечение распада опухоли
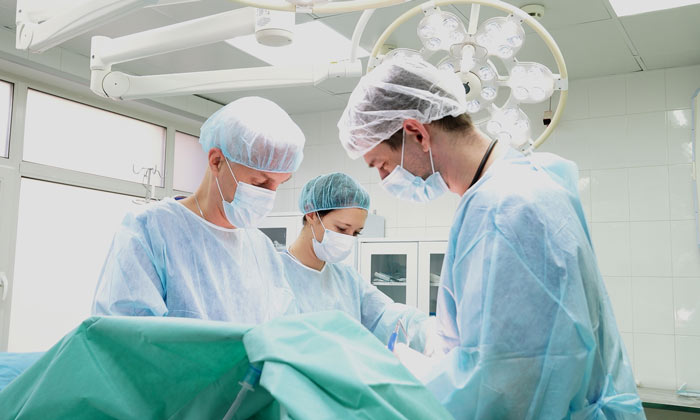
Формально при распадающейся опухоли невозможна радикальная операция, зачастую заболевание считается неоперабельным, но химиотерапия и облучение исключаются из программы, потому что способны усугубить некроз. Отчаянное положение пациента и вероятность массированного кровотечения из изъеденного раком крупного сосуда оправдывает выполнение паллиативной операции, основная цель которой — удаление очага хронического воспаления и интоксикации.
Синдром лизиса опухоли лечится многочасовыми капельными вливаниями при усиленном диурезе — выведении мочи, связыванием мочевой кислоты специальными лекарствами. Одновременно поддерживается работа сердечно-сосудистой системы, купируется интоксикация и воспаление. При развитии острой почечной недостаточности проводится гемодиализ.
Синдром лизиса опухоли сложно лечить, но можно предотвратить или хотя бы уменьшить его проявления. Профилактика начинается за несколько дней до курса химиотерапии и продолжается не менее трёх суток после завершения цикла. Кроме специальных препаратов, выводящих мочевую кислоту, назначаются продолжительные капельницы, вводятся недостающие микроэлементы, а избыточные выводятся или связываются другими лекарствами.
Профилактика лизиса опухоли стала стандартом лечения онкогематологических больных, чего нельзя сказать об онкологических пациентах с распадающимися злокачественными процессами, которым очень сложно найти хирурга, готового выполнить паллиативную операцию. Во вмешательстве по санитарным показаниям отказывают из-за сложности выхаживания тяжелого больного после обширного хирургического вмешательства. В нашей клинике никому не отказывают в помощи.
Читайте также:

