При цитомегаловирусе может быть эпилепсия или нет
Обновлено: 18.04.2024
Цитомегаловирусная инфекция (ЦМВИ) – вирусное инфекционное заболевание, вызываемое цитомегаловирусом (ЦМВ). ЦМВ - это разновидность вируса герпеса человека, герпесвирус 5-го типа, который относится к семейству Herpesviridae, подсемейству β-герпесвирусов.
Источником инфекции является человек, зараженный цитомегаловирусом. Наличие в крови специфических антител в абсолютном большинстве случаев означает присутствие в организме самого вируса. У 20–30% здоровых беременных ЦМВ присутствует в слюне, 3-10% - в моче, 5-20% - в цервикальном канале или вагинальном секрете. Вирус обнаруживают в грудном молоке 20-60% серопозитивных матерей. Установлена значительная частота выявления (до 35%) и длительность присутствия (в среднем, до 22 месяцев) ЦМВ в сперме. Кровь около 1% доноров содержит ЦМВ.
Для ЦМВ характерен широкий спектр путей передачи – воздушно-капельный, контактный (при сексуальных и бытовых контактах), внутриутробный, пероральный, парентеральный, через компоненты крови при переливании крови, а также при пересадке органов.
Группу наибольшего риска по отношению к ЦМВИ составляют лица с искусственной или естественной иммуносупрессией (т.е. люди с угнетенным иммунитетом): реципиенты органов и тканей, ВИЧ-инфицированные, онкологические больные, пациенты, перенесшие тяжелые хирургические операции; а также беременные женщины.
Выделяют два периода жизни человека, наиболее уязвимые для инфицирования ЦМВ. Первый достигается к трехлетнему возрасту, при этом заражение происходит контактно-бытовым путем. Дети младшего возраста заражаются друг от друга в домах ребенка, детских садах; вирус передается от матери к ребенку и от инфицированного ребенка матери. Заражение происходит при непосредственном контакте с источником инфекции или опосредованно через контаминированную вирусом посуду, зубные щетки, игрушки.
Другим критическим периодом заражения ЦМВ является возраст 16–30 лет, который является периодом половой зрелости и половой активности В данной группе лиц передача вируса осуществляется главным образом при близком контакте через поцелуи и половым путем, причем как при гетеро- , так и гомосексуальных контактах.
Беременным принадлежит значительная роль в эпидемиологии ЦМВИ, которая обнаруживается у них в 2 раза чаще, чем краснуха. Частота обнаружения ЦМВ в цервикальном канале, вагинальном секрете здоровых беременных составляет от 2-8% до 18–20%. ЦМВ обладает высокой способностью проникать от женщины к плоду. Наличие ЦМВ в генитальном тракте у беременных может служить причиной заражения ребенка во время родов. Риск интранатального инфицирования ребенка при наличии вируса в генитальном тракте матери составляет 50–57%.
Серьезной проблемой является заражение цитомегаловирусом реципиентов крови, являющееся одним из путей передачи инфекции. В случае, если доноры не обследуются на ЦМВИ, гемотрансфузии и парентеральные манипуляции могут приводить к заражению ЦМВ. Переливание цельной крови и ее компонентов, содержащих лейкоциты, ведет к передаче вируса с частотой 0.14 – 10 на 100 доз. Риск инфицирования ЦМВ с каждой гемотрансфузией возрастает на 5–12%.
Еще более сложные проблемы связаны с трансплантацией органов, поскольку фактором передачи инфекции может быть не только перелитая кровь, но и пересаженный орган.
Выявлена зависимость между частотой распространенности ЦМВ среди населения, с одной стороны, и условиями и уровнем жизни, с другой. Так, антитела к цитомегаловирусу класса IgG выявляются чаще среди жителей городов, что обусловлено более высокой плотностью населения и большей долей лиц с иммунодепрессией среди городских жителей, а также среди населения с низким уровнем жизни. У последних в 40–60% случаев до 5 лет происходит инфицирование цитомегаловирусом, а к 15–19 годам уже у 50–88% обнаруживаются антитела к ЦМВ.
Цитомегаловирусный энцефалит является редким проявлением цигомегалии и характеризуется тяжелым поражением мозга с высокой летальностью и инвалидизацией.
Что провоцирует / Причины Цитомегаловирусного энцефалита:
Возбудитель (Cytomegalovirus hominis) относится к вирусам герпеса (семейство Herpesviridae). Диаметр вириона около 180 нм, вирус содержит ДНК, при развитии вируса в ядрах инфицированных клеток образуются включения. Может развиваться на культурах фибробластов человека. Под воздействием вируса нормальные клетки превращаются в цитомегалические, диаметр которых достигает 25-40 мкм. В культуре тканей не выявлено существенных нарушений хромосомного аппарата. Возможность онкогенного действия вируса окончательно не изучена. Имеются антигенные различия между отдельными штаммами вируса. Обладает свойствами, общими для всех вирусов группы герпеса.
Частота цитомегаловирусного энцефалита у детей составляет 2-3% среди других форм острых энцефалитов.
Патогенез (что происходит?) во время Цитомегаловирусного энцефалита:
В зависимости от путей передачи воротами инфекции могут служить слизистые оболочки верхних отделов респираторного тракта, органов пищеварения и половых органов. Каких-либо изменений на месте ворот инфекции не отмечается. Не сказывается характер инфицирования и на клинических проявлениях болезни. Вирус имеет тропизм к ткани слюнных желез и при локализованных формах обнаруживается только в этих железах.
Вирус персистирует в организме пожизненно. В ответ на первичное внедрение развивается иммунная перестройка организма. Переход латентной цитомегаловирусной инфекции в клинически выраженные формы обычно провоцируется какими-либо ослабляющими факторами, например, интеркуррентными заболеваниями, назначением цитостатиков и других иммунодепрессантов. В последние годы особенно актуальной стала проблема обострения цитомегаловирусной инфекции у ВИЧ-инфицированных лиц.
У беременных с латентной цитомегаловирусной инфекцией плод поражается далеко не всегда. Необходимым условием для этого является обострение у матери латентной инфекции с развитием вирусемии с последующим заражением плода. Вероятность заражения плода будет значительно выше при инфицировании матери во время беременности. Во время фазы вирусемии при отсутствии антител у матери (а, следовательно, у плода) передача инфекции плоду осуществляется значительно легче, чем в иммунном организме ранее инфицированной матери.
Симптомы Цитомегаловирусного энцефалита:
Цитомегаловирусный энцефалит зачастую не имеет четкого начала. Дети становятся беспокойными, плохо спят, отказываются от еды, часто срыгивают, теряют массу тела. Типичны гипертензионно-гидроцефальный синдром или гидроцефалия с выбуханием и напряжением родничка, расхождением черепных швов, увеличением окружности головы. Повышается мышечный тонус, отмечаются тремор конечностей, сухожильная гиперрефлексия, клонусы стоп. Возможно развитие центральных парезов и параличей, чаще по гемитипу. Периодически могут наблюдаться генерализованные клонико-тонические судороги. Ребенок значительно отстает в психическом развитии или теряет уже приобретенные умственные и двигательные навыки. Изменения цереброспинальной жидкости (увеличение содержания белка, умеренный лимфоцитарный или смешанный плеоцитоз) бывают лишь в начальном периоде болезни. Характерна генерализация процесса с гепатолиенальным синдромом, почечной недостаточностью. На этом фоне присоединяется бактериальная инфекция. Больные умирают в течение 1-2 лет.
Диагностика Цитомегаловирусного энцефалита:
Клиническая диагностика генерализованных форм ЦМВ-инфекции представляет значительные трудности, т.к. клиническая картина ее полиморфна, часто не имеет специфических проявлений и протекает под маской других заболеваний
Лабораторная диагностика ЦМВ-инфекции:
– определение методом ИФА специфических антител класса IgG
– определение методом ИФА специфических антител класса IgM
– цитологические исследования (анализ на клетки –цитомегалы)
– определение методом ПЦР ДНК ЦМВ в разных биосубстратах (плазма крови, моча, ликвор, слеза, слюна, амниотическая жидкость и др.)
– МРТ выявляет перивентрикулярные сливные очаги с усилением контраста.
– ПЦР на цитомегаловирус в СМЖ обладает чувствительностью >80% и специфичностью 90%.
– Выделить культуру ЦМВ из СМЖ обычно не удается.
Лечение Цитомегаловирусного энцефалита:
Этиотропного лечения нет. Противогерпетические препараты (ацикловир, видарабин), успешно применяемые при других болезнях, при цитомегалии оказались неэффективными. Имеются данные, что препарат Cymeven (ganciclovir sodium) оказывает некоторый эффект при цитомегаловирусной инфекции, однако требуется дальнейшее его изучение, тем более, что он вызывает побочные реакции (гранулоцитопению и др.). При приобретенной цитомегаловирусной инфекции беременных основной задачей является предупреждение генерализации инфекции и внутриутробного заражения плода. С этой целью проводят десенсибилизацию и общеукрепляющую терапию. Рекомендуется также введение нормального человеческого иммуноглобулина, содержащего специфические антитела, вводят его внутримышечно по 6-12 мл с интервалами 2-3 нед в течение первых 3 мес беременности. При трансплантации почки профилактический эффект оказывало введение альфа-интерферона.
Профилактика Цитомегаловирусного энцефалита:
Специфическая профилактика не разработана. При переливании крови новорожденным, а также лицам с ослабленным иммунитетом следует использовать кровь от доноров, у которых отсутствуют антитела против цитомегаловирусов. Мероприятия в очаге не проводятся.
К каким докторам следует обращаться если у Вас Цитомегаловирусный энцефалит:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Цитомегаловирусного энцефалита, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Цитомегаловирусная инфекция у детей (ЦМВИ) – типичный представитель оппортунистических инфекционных заболеваний, клинически проявляющихся только на фоне иммунодефицитных состояний.
Цитомегалия — это вирусное заболевание, которое проявляется множеством симптомов, которые возникаюь из-за образования гигантских клеток с типичными внутриядерными и цитоплазматическими включениями в слюнных железах, висцеральных органах и центральной нервной системе.
Цитомегаловирусная инфекция, согласно международной классификации, бывает таких видов:
- цитомегаловирусный панкреатит
- цитомегаловирусный гепатит
- цитомегаловирусная пневмония
- другие цитомегаловирусньте болезни
- неуточненная цитомегаловирусная болезнь.
Также существует врожденная цитомегаловирусная инфекция и цитомегаловирусный мононуклеоз.
Цитомегалия бывает врожденной или приобретенной. При врожденной могут быть поражены многие органы и системы ребенка, такую форму болезни называют генерализированной.
Приобретенная цитомегалия у детей раннего возраст протекает по типу мононуклеозоподобного синдрома. В некоторых случаях вирус преимущественно поражает желудочно-кишечный тракт, легкие, печень. Или же болезнь может принять генерализированную форму. Обе формы (врожденная и приобретенная) могут проходить бессимптомно. Согласно классификации по признаку течения, цитомегалия бывает острой и хронической.
Что провоцирует / Причины Цитомегаловирусной инфекции у детей:
Возбудитель – ДНК-содержащий вирус семейства Herpes-viriae – Cytomegalovirus hominis. Источником цитомегаловирусной инфекции у детей является мать. Механизмы передачи: вертикальный и интранатальный.
Пути передачи – гематогенный (трансплацентарный), восходящий, контактный, аспирационный (при заглатывании инфицированных околоплодных вод). У детей первого года жизни возможно инфицирование через грудное молоко. Дети раннего возраста могут инфицироваться контактно-бытовым, воздушно-капельным, трансфузионным путем.
Эпидемиологические особенности ЦМВИ (широкое распространение цитомегаловируса в человеческой популяции, различные механизмы и пути передачи, преобладание субклинических форм инфекции), а также особенности иммунитета у беременных и плода способствуют повышенному риску внутриутробного инфицирования вирусом цитомегалии.

У больных цитомегаловирусной инфекцией клетки, зараженные вирусом, обнаруживают в осадке мочи, слюне, спинномозговой жидкости и пораженных органах. Вирус сохраняет жизнедеятельность в среде, имеющей комнатную температуру. Он имеет чувствительность к дезинфицирующим средствам и эфиру. Вирус устойчив к антибиотикам.
Патогенез (что происходит?) во время Цитомегаловирусной инфекции у детей:
У новорожденных детей встречается в 0,2-2,5% случаев. Клинические формы врожденной цитомегаловирусной инфекции у детей: бессимптомная, генерализованная. У 80% детей, перенесших генерализованную ЦМВИ, в дальнейшем отмечается неврологическая симптоматика, у 17% детей при бессимптомном течении заболевания отмечается минимальная мозговая дисфункция, задержка развития, неврозоподобные расстройства.
Скорость репликации и инфицирования дочерними вирусами незараженных клеток зависит от функционального состояния иммунной системы. Неспецифические факторы иммунитета – система интерферона, комплемента, естественные киллеры – на первых этапах инфекционного процесса замедляют скорость распространения возбудителя, а в дальнейшем потенцируют активность специфического иммунитета и препятствуют инфицированию непораженных клеток. Однако наиболее действенной защитой от ЦМВИ является создание специфического иммунитета (образование специфических антител и специфических Т-лимфоцитов). Специфическая иммунная защита может формироваться только в том случае, если вирусы расположены и неклеточно. Внутриклеточное расположение вируса защищает его от иммунного воздействия.
Клинические проявления: риск инфицирования плода, тяжесть заболевания новорожденного ребенка и дальнейший прогноз при внутриутробной ЦМВИ зависят от характера течения инфекционного процесса у матери в период беременности. Если женщина, не имеющая иммунитета к вирусу цитомегалии, впервые инфицируется им в период беременности, то это приводит к развитию у нее первичной ЦМВИ. Частота передачи цитомегаловируса при первичной инфекции от серонегативной беременной плоду составляет от 30 до 50%. Следует отметить, что в большинстве случаев отмечается бессимптомное течение инфекции у женщин. При вторичной цитомегаловирусной инфекции риск внутриутробного инфицирования плода значительно ниже (2%).
Симптомы Цитомегаловирусной инфекции у детей:
Клинические проявления внутриутробной ЦМВИ:
- петехиальная сыпь (мелкие кожные кровоизлияния) – 60-80%
- тромбоцитопеническая пурпура – 76%;
- желтуха – 67%;
- гепатоспленомегалия – 60%;
- микроцефалия – 53%;
- гипотрофия – 50%;
- недоношенность – 34%;
- гепатит – 20%;
- энцефалит –15%;
- хориоретинит – 12%.
Клиническая картина приобретенной цитомегалии. Инкубационный период может длиться минимум 15 дней, максимум 3 месяца. Всё это время ребенок является носителем инфекции.
При приобретенной цитомегалии ребенок заражается от матери или медперсоналав роддоме в том случае, если данные взрослые – носители вируса. Если малышу делают переливание плазмы/крови от доноров, и кровь недостаточно проверена, возможно заражение.
Болезнь может проявиться в изолированном поражении слюнных желез, либо инфекция поражает, помимо слюнных желез, еще и висцеральные органы. Приобретенная цитомегалия редко бывает генерализированной. У ребенка постепенно повышается температура. Среди симптомов отмечают такие: боли в горле, увеличение шейных лимфатических узлов, печени и селезенки. Могут быть головные боли, боли в животе, анорексия, ощущение слабости в теле.
Слизиста оболочка ротоглотки чуть красновата, можно наблюдать увеличение небных миндалин.
В других случаях могут проявляться симптомы интерстициальной пневмонии, такие как цианоз, одышка и пр. Не исключены желудочно-кишечные расстройства, проявляющиеся в учащении стула и рвоте. Может наблюдаться также нарушение печеночных функций, например, потемнение мочи, желтуха и т. д., а также изменения в мочи.
Болезнь длится долго. Температура может ежедневно повышаться до уровня 39—40 ˚ С. Ребенок во время подъемов температуры ощущает озноб, что может длиться от 2 до 4 недель, редко – более длительный срок.
Если заражение возникло вследствие переливания крови, через 5-6 недель после процедуры возникает цитомегаловирусный мононуклеозоподобный синдром.
Генерализированная форма приобретенной цитомегаловирусной инфекции отличается тем, что вирус постепенно поражает многие органы и системы в организме ребенка. Лихорадка длительная, проявляется общеинфекционный токсикоз. Вирус поражает легкие, что приводит к интерстициальной пневмонии. Поражение желудочно-кишечного тракта проявляется в повторяющихся приступах рвоты и жидком многократном стуле. Вирус при генерализированной форме поражает сердечно-сосудистую систему. Фиксируются явления паренхиматозного гепатита, энцефалита. Течение генерализированной формы длительное.
Диагностика Цитомегаловирусной инфекции у детей:
Чтобы диагностировать наличие цитомегаловирусной инфекции у детей проводиться лабороторное исследование крови на специфические антитела к цитомегаловирусу – иммуноглобулинов М и G.
Обнаружение иммуноглобулинов М может указывать на первичное заражение цитомегаловирусами либо на реактивацию хронической цитомегаловирусной инфекции. Высокие титры IgМ у беременных могут способствовать инфицированию плода. Повышение IgМ определяется в крови через 4-7 недель после заражения вирусом и наблюдается в течение16-20 недель.
Повышенные иммуноглобулины G развиваются в период снижения активности цитомегаловирусной инфекции. Их наличие в крови указывает на цитомегаловирус в организме, но не показывает активности инфекционного процесса.
С помощью ПЦР-диагностики определяется ДНК цитомегаловируса в клетках крови и слизистых – соскобы из уретры и цервикального канала, мокроты, слюна и т.д. Эффективным способом диагностики является проведение количественной ПЦР, которая показывает активность цитомегаловируса и вызываемого им инфекционного процесса. Диагноз ставится, когда выделение цитомегаловируса в забранном материале пошается.
Зависимо от того, какой орган пострадал от инфекции, пациент проходит осмотр гинеколога, гастроэнтеролога, андролога или других докторов. Дополнительно может назначаться проведение УЗИ органов брюшной полости, гастроскопия, кольпоскопия, МРТ головного мозга и другое.
Лечение Цитомегаловирусной инфекции у детей:
В настоящее время существует два основных направления терапии и профилактики вирусных инфекций. Это виростатические препараты и специфические иммуноглобулины. Эти два вида терапии имеют принципиальные отличия в механизме противовирусного действия.
Ганцикловир назначают внутрь во время еды, а также вводят внутривенно. Биоусвоение из желудочно-кишечного тракта равно 15-20%, тем не менее этого достаточно для оказания эффекта. У препарата высокая активность и он обладает способностью избирательно накапливаться в клетках, инфицированных вирусом, но не в интактных клетках. Его концентрация в инфицированных клетках может в 30-120 раз быть больше, чем в плазме крови. Это важное обстоятельство объясняет большую широту терапевтического действия данного препарата по сравнению с другими и меньшую опасность осложнений. Связывание с белками плазмы крови всего 9-30%, поэтому препарат хорошо проникает в различные ткани и жидкости (включая ликвор). Большая часть препарата (80-90%) в неизмененном виде и в виде метаболита 9-карбоксиметоксиметилгуанина выводится почками. Период полувыведения примерно 3,3 ч, однако при почечной недостаточности он может увеличиваться до 20 ч, поэтому необходимо корректировать дозирование. Так, при скорости клубочковой фильтрации (СКФ) менее 70 мл/мин — дозу препарата снижают в 2 раза; при СКФ менее 50 мл/мин – дозу уменьшают еще на треть; при СКФ менее 25 мл/мин еще на '/2 и при СКФ менее 10 мл/мин – в 3 раза.
Нежелательные эффекты ганцикловира: гематотоксичность (нейтро-, лейко-, тромбоцитопения); энцефалопатические реакции; иммунодепрессия; повреждение репродуктивной функции у мужчин и женщин; мутагенное, тератогенное и канцерогенное действие.
Фоскарнет (фосфоноформат) вводят внутривенно. Период его полувыведения от 2 до 4 ч. Экскретируется в неизмененном виде почками. Фоскарнет может вызывать костномозговую депрессию, иммунодепрессию, нарушения функции печени и почек; он обладает тератогенным, мутагенным и канцерогенным свойством.
При использовании ганцикловира и фоскарнета необходимо каждые 2 дня анализ крови. При выраженной нейтропении (меньше 500/мкл) и тромбоцитопении (менее 25 000/мкл) препараты срочно отменяют.
Ганцикловир и фоскарнет являются цитостатиками, поэтому при лечении ЦМВИ их иногда комбинируют с иммуностимуляторами или с интерфероногенами (например, с циклофероном и др.), а также со стимуляторами кроветворения (например, с филграстимом и др.) и с иммуноглобулинами (цитотект).
Цитотект – иммуноглобулин с повышенным содержанием специфических антител к цитомегаловирусу. Его применяют как средство заместительной терапии.
Индивидуальная непереносимость препарата проявляется головной болью, тошнотой, головокружением, рвотой, диареей, тахикардией, цианозом, одышкой, гипертермией, ознобом, повышенным потоотделением, болью в спине, миалгией. Перечисленные симптомы могут появиться уже через 30 мин после начала инфузии и наблюдаться в течение первых суток. Тяжелая анафилактическая реакция может наблюдаться у больных с отсутствием или выраженным дефицитом IgA, что примерно в 30% случаев связано с наличием у них антител против названного иммуноглобулина. Когда такие больные получают иммуноглобулиновый препарат, у них образуются макромолекулярный комплекс IgA – анти-IgA, приводящий к анафилаксии. Целесообразно у всех больных определять IgA в сыворотке крови перед введением цитотекта.
Профилактика Цитомегаловирусной инфекции у детей:
К методам профилактики принадлежат неспецифические: соблюдение личной гигиены, к специфическим относятся медикаментозный метод препаратами – ганцикловир, ацикловир, фоскарнет.
Чтобы исключить возможность инфицирования цитомегаловирусом пациентов при пересадке органов и тканей необходимо проводить тщательный подбор доноров и контроль донорского материала на наличие цитомегаловирусной инфекции.
Особую опасность цитомегаловирусная инфекция представляет для беременных женщин, так как может спровоцировать выкидыш, мертворождение или вызвать тяжелые врожденные уродства у ребенка. Поэтому цитомегаловирус, наряду с токсоплазмозом, герпесом и краснухой принадлежит к числу инфекций, обследоваться на которые женщины должны еще на этапе планирования беременности.
К каким докторам следует обращаться если у Вас Цитомегаловирусная инфекция у детей:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Цитомегаловирусной инфекции у детей, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Что такое юношеская миоклоническая эпилепсия? Причины возникновения, диагностику и методы лечения разберем в статье доктора Агранович А. О., эпилептолога со стажем в 12 лет.
Над статьей доктора Агранович А. О. работали литературный редактор Вера Васина , научный редактор Татьяна Гаврилова (Уханова) и шеф-редактор Маргарита Тихонова
Определение болезни. Причины заболевания
Юношеской миоклонической эпилепсией (синдромом Янца) называют эпилептический синдром, который проявляется внезапными подёргиваниями в мышцах — миоклоническими приступами (от греч. "myos" — мышца, "klonos" — беспорядочное движение). Заболевание обычно развивается в подростковом возрасте.
Подёргивания в первую очередь возникают в мышцах верхнего плечевого пояса и рук. Сначала пациенты не обращают на них внимания, но со временем эпизоды возникают всё чаще и ухудшают качество жизни. Например, во время приступов из рук могут выпадать предметы. В дальнейшем появляются подёргивания ног, из-за которых человек может упасть.
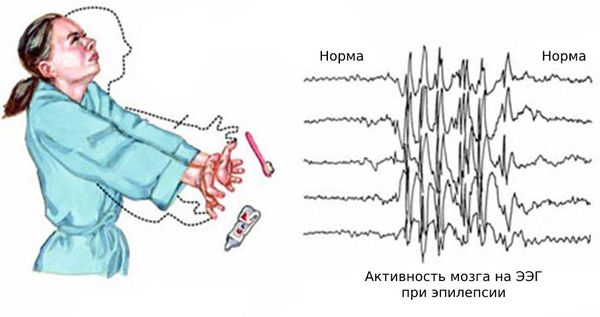
Нередко к этим эпизодам присоединяются генерализованные судорожные приступы — судороги возникают по всему телу и пациент теряет сознание. Также возникают абсансы — бессудорожные приступы с отключением сознания и амнезией на этот период. Как правило, частота генерализованных приступов невысокая: от одного за всю жизнь до раза в месяц. Подёргивания обычно случаются утром после пробуждения. Ярким провоцирующим фактором может стать недосыпание или вынужденное пробуждение. Также в трети случаев отмечается фотосенситивность — чувствительность к ритмическим вспышкам света.
Распространённость
Юношеская миоклоническая эпилепсия составляет 5–10 % среди всех эпилепсий и чуть больше четверти среди генетических генерализованных эпилепсий [5] . Заболевание проявляется в возрасте от 7 до 21 года, чаще в 11–15 лет, и более распространено среди женщин (61 %) [2] .
Причины заболевания
По классификации Международной противоэпилептической лиги за 2017 год, юношеская миоклоническая эпилепсия относится к генетическим болезням [1] . Заболевание имеет полигенное наследование, то есть контролируется двумя или более генами. Его развитие связано с локусами (участками ДНК): 6p11-12 (EJM1), 15q14 (EJM2), 6р21 (EJM3), 5q12-q14 (EJM4), 5q34-q35 (EJM5), 2q22-q23 (EJM6), 1p36 (EJM7), 3q26 (EJM8), 2q33-q36 (EJM9). Выделить ген, сильнее всего влияющий на развитие заболевание, пока не удалось [3] [4] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы юношеской миоклонической эпилепсии
Основным симптомом заболевания являются миоклонические вздрагивания (миоклонии) — патологические непроизвольные сокращения мышц или их групп [7] . Во время приступа пациенты испытывают ощущение, похожее на лёгкий удар током. В ответ на него возникают молниеносные движения в мышцах: от лёгкого подёргивания кончиков пальцев до патологического вздрагивания всего тела, которое может привести к падению.
Чаще всего подёргивания возникают в верхнем плечевом поясе: мышцах рук и плеч с обоих сторон. Из-за этого пациенты нередко выпускают предметы из рук, например разбивают кружки и роняют зубные щётки. Однако возможны различные вариации миоклоний.
Приступы учащаются в утренние часы, особенно при недосыпе или вынужденном пробуждении.
В 90 % случаев, помимо миоклонических эпизодов, отмечаются и генерализованные судорожные приступы [6] . После серии вздрагиваний в патологический процесс часто вовлекаются обе стороны тела.
Генерализованный тонико-клонический приступ — состояние, при котором полностью отключается сознание. Приступ начинается с тонической фазы: напряжения в мышцах и специфического вскрикивания или хрипения. Руки полусогнуты и приподняты вверх или прижаты к телу. В этот момент из-за спазма дыхательной мускулатуры меняется цвет лица: оно синеет или сереет.
Далее развивается клоническая фаза, которая проявляется ритмичными подёргиваниями в конечностях. Она завершается полным мышечным расслаблением.
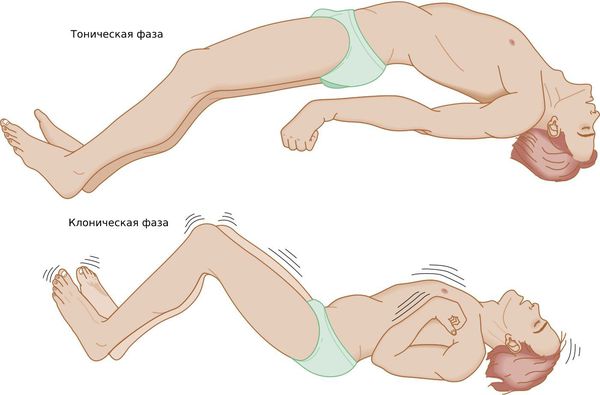
Третий вид эпилептических приступов при юношеской миоклонической эпилепсии — это абсансы [8] . Во время эпизода больной застывает, его взгляд устремлён в одну точку, сознание отключено. Состояние длится до 15 секунд и часто воспринимается окружающими как задумчивость. Сами пациенты могут не замечать эти приступы или воспринимать их как "провалы в памяти".
Патогенез юношеской миоклонической эпилепсии
Мозг человека состоит из двух основных типов клеток: нейронов и глии. Нейроны — это электрически возбудимые клетки, которые обрабатывают, хранят и передают информацию с помощью электрических и химических сигналов. Глиальные клетки играют в этом процессе вспомогательную роль.
Нейроны могут соединяться друг с другом и образовывать нервные сети. В пределах одного нейрона и его отростков информация передаётся в виде электрического возбуждения. В синапсе (месте контакта между нервными клетками) оно приводит к выделению различных химических веществ — нейромедиаторов.
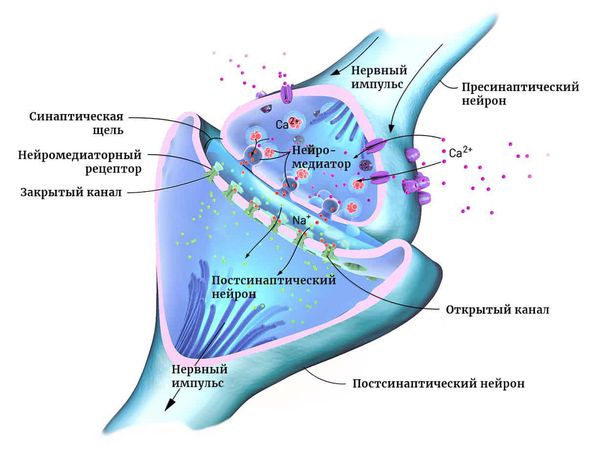
Нейромедиатор взаимодействует с рецепторами на мембране следующего нейрона. В результате в нём возникает электрическое возбуждение. Или не возникает — это зависит от конкретного нейромедиатора, активного в данный момент.
Чтобы заряд менялся в сторону возбуждения, в клетку должны поступать положительно и отрицательно заряженные ионы. Они проходят через ионные каналы в её мембране. Ионными каналами называют белки, образующие п о́ ру для обмена клетки с окружающей средой ионами K+, Na+ и другими [9] .
В нервных сетях между возбуждением и торможением работы нейронов поддерживается постоянный баланс. При сдвиге равновесия в сторону возбуждения происходит эпилептический приступ.
К юношеской миоклонической эпилепсии приводят мутации в генах ионных каналов. Однако выявлены нарушения и в других генах, также влияющих на процессы возбуждения в головном мозге [4] .
Классификация и стадии развития юношеской миоклонической эпилепсии
В Международной классификации болезней (МКБ-10) юношеская миоклоническая эпилепсия шифруется кодом G40.3 [10] .
В 2017 году Международная лига борьбы с эпилепсией (ILAE) обновила классификацию заболевания, выделив четыре уровня диагностики:
1. Определить тип приступа: фокальный (возникающий из одного очага), генерализованный и с неизвестным началом. Миоклонические, тонико-клонические приступы и абсансы относятся к генерализованным приступам.
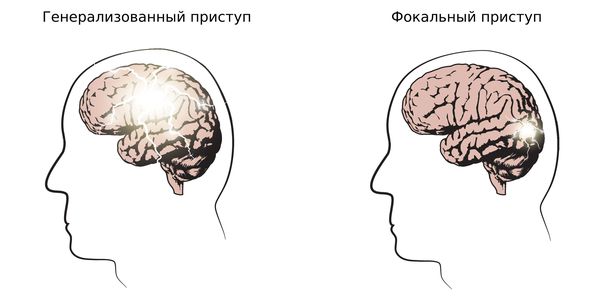
2. Установить тип эпилепсии: фокальная, генерализованная, сочетанная (фокальная + генерализованная) и неизвестная. Юношеская миоклоническая эпилепсия относится к генерализованной эпилепсии.
3. Определить эпилептический синдром. Юношеская миоклоническая эпилепсия как раз и является синдромом. Синдром включает типы приступов, возраст дебюта заболевания, характерные изменения на ЭЭГ, провоцирующие факторы и зачастую прогноз заболевания. Все эти факторы определяют лечебную тактику [11] .
4. Выявить причины заболевания: генетические, структурные, метаболические, иммунные, инфекционные и с неизвестной этиологией. Юношеская миоклоническая эпилепсия в большинстве случаев вызвана генетическими факторами.
Классификация юношеской миоклонической эпилепсии проводится в зависимости от течения заболевания. Главный критерий — это наличие миоклонических приступов. Также выделяют варианты течения с добавлением генерализованных судорожных приступов и/или абсансов.
Осложнения юношеской миоклонической эпилепсии
Пациенты часто не обращают внимания на патологические сокращения мышц, поэтому к неврологу и эпилептологу больной зачастую обращается после появления генерализованных тонико-клонических приступов. В результате противоэпилептические препараты назначают с опозданием. На фоне этого приступы могут учащаться и угрожать здоровью и жизни пациента травмами и утоплениями.
Серьёзным осложнением эпилепсии, в том числе и юношеской миоклонической эпилепсии, является внезапная смерть (SUDEP — Sudden Unexpected Death EPilepsy). Среди людей, страдающих эпилепсией, риск внезапной смерти в 20 раз выше, чем среди населения в целом [12] .
Точные причины SUDEP не установлены. Предполагается, что гибель пациентов связана с нарушением дыхания и развитием аритмии после приступа. Вероятность внезапной смерти при эпилепсии повышается при наличии генерализованных тонико-клонических приступов. Также важно, когда заболевание проявилось и сколько оно длится [12] .
При наличии дневных генерализованных приступов в течение предыдущего года риск развития SUDEP возрастает в 27 раз, ночных — в 15 раз. Проживание в одиночестве повышает риск внезапной смерти в 5 раз. Также SUDEP чаще встречается при злоупотреблении психоактивными веществами и алкоголем [13] .
Снизить риск внезапной смерти при эпилепсии можно, если придерживаться назначенного лечения: не пропускать приём противоэпилептических препаратов, не менять самостоятельно его частоту и дозировку [14] [15] .
Диагностика юношеской миоклонической эпилепсии
Основной диагностический критерий заболевания — это наличие миоклонических приступов.
Сбор анамнеза
На приёме врач спрашивает о необычных внезапных состояниях:
- вздрагиваниях в теле;
- дежавю — состоянии, при котором человек ощущает, что когда-то уже был в подобной ситуации или месте;
- потере сознания и т. д.
Пациенты могут не обращать внимания на такие симптомы и считать их своей особенностью. Абсансы и генерализованные тонико-клонические приступы с потерей сознания, особенно во сне, они могут и вовсе забывать. Поэтому при сборе анамнеза важно выяснить обстоятельства приступа не только у самих пациентов, но и у родственников и очевидцев.
Электроэнцефалограмма (ЭЭГ)
Основным способом диагностики эпилепсии является электроэнцефалограмма — метод исследования, при котором регистрируется суммарная электрическая активность клеток коры головного мозга.
Сейчас диагноз "эпилепсия" устанавливают с помощью длительного видео-ЭЭГ мониторинга — электроэнцефалограмма записывается параллельно с одной или несколькими видеокамерами, датчиком ЭКГ и при необходимости дополнительным контролем мышечной активности, частоты и глубины дыхания.
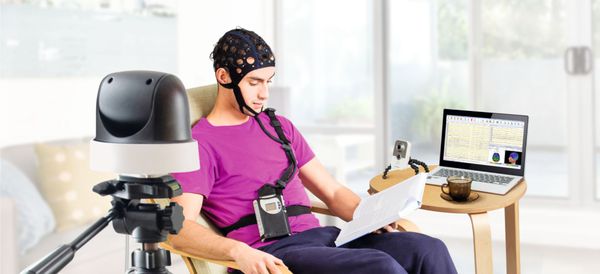
Основной фон биоэлектрической активности при юношеской миоклонической эпилепсии, как правило, соответствует возрастной норме. Патологическая активность проявляется короткими и генерализованными разрядами полиспайков (островолновых комплексов), которые регистрируются при миоклонических вздрагиваниях и полипик-волновыми комплексами между приступами.
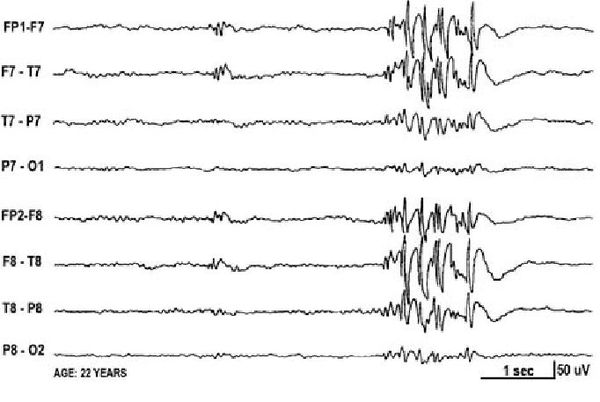
При заболевании часто встречается феномен фотосенситивности. Для её выявления во время ЭЭГ пациента просят закрыть глаза и проводят ритмичную фотостимуляцию с частотой около 15 Гц [16] .
Эпилептическая фотосенситивность — это предрасположенность к приступам под влиянием света. Может протекать бессимптомно или проявляться эпилептическими приступами под воздействием провоцирующих факторов: видеоигр, работы за компьютером, просмотра телевизора, мигающего освещения в ночных клубах и света природного происхождения.
На МРТ патологические изменения в головном мозге при юношеской миоклонической эпилепсии не выявляются [17] .
Интеллект и неврологический статус при заболевании находятся в норме. Выражена эмоциональная неустойчивость и признаки невротического развития личности: резкая смена настроения, вспыльчивость и повышенная тревожность
Лечение юношеской миоклонической эпилепсии
Образ жизни
При эпилепсии следует соблюдать режим сна и бодрствования, исключить алкоголь и избегать резких вспышек света. Также нужно по возможности уменьшить стрессы, переживания и тревоги [20] .
Антиэпилептические препараты
Приём антиэпилептических препаратов (АЭП) позволяет устранить до 90 % приступов. Монотерапия (лечение одним препаратом) при юношеской миоклонической эпилепсии применяется в 79 % случаев, дуотерапия (двумя препаратами) — 17 %, политерапия (несколькими препаратами) — 4 % [16] .
Прекращать приём лекарств рекомендуется не ранее чем через пять лет полной клинико-нейрофизиологической ремиссии. Но даже спустя 4–7 лет ремиссии рецидивы после отмены терапии возникают у 70 % больных. Поэтому пациентам с юношеской миоклонической эпилепсией может быть рекомендован пожизненный приём АЭП [21] .

Ранее лидерами в лечении юношеской миоклонической эпилепсии являлись препараты вальпроевой кислоты. Они эффективны для прекращения приступов, но вызывают много побочных эффектов:
Также выявлено, что они обладают повышенным тератогенным эффектом по сравнению с другими АЭП. Тератогенное действие — это нарушение эмбрионального развития ребёнка при приёме препаратов матерью. Поэтому назначение вальпроатов, в особенности у молодых женщин, ограничено [18] .
В настоящее время препаратом выбора стартовой терапии является "Леветирацетам". Он хорошо переносится и эффективно устраняет все три вида приступов, в том числе сопровождающихся фотосенситивностью [19] .
Также используется препарат "Ламотриджин". Он эффективно подавляет генерализованные тонико-клонические судороги и абсансы, но в половине случаев способствует учащению миоклоний. Его применение в монотерапии у пациентов с частыми миоклоническими приступами ограничено, но лекарство можно использовать в комбинированной терапии [21] .
Помимо перечисленных препаратов, могут применяться "Топирамат", "Зонисамид", "Перампанел" и "Фенобарбитал".
Чтобы избежать учащения приступов и усиления симптомов, важно ограничить приём "Карбамазепина", "Окскарбазепина", "Фенитоина", "Габапентина" и "Вигабатрина". Эти лекарства могут повышать гипервозбудимость мембраны клеток головного мозга, что приводит к обострению состояния [21] .
Прогноз. Профилактика
Прогноз определяется индивидуально в зависимости от частоты приступов, эффективности АЭП, возраста начала заболевания и т. д. Лечение часто не помогает пациентами с тремя видами приступов [21] .
Без приёма противоэпилептических препаратов (АЭП) приступы могут сохраняться всю жизнь. Их частота, как правило, снижается только после 40 лет [20] .
Эффективность АЭП в предотвращении приступов достигает 90 %. При отмене терапии часто возникают рецидивы, поэтому потребуется длительный приём препаратов, иногда пожизненный.
Качество жизни значительно ухудшается при частых миоклонических и генерализованных тонико-клонических приступах, при которых пациенты рискуют получить травмы.
Профилактика
Особое внимание стоит уделить образу и режиму жизни пациента. Самыми мощными провоцирующими факторами являются недосыпание и злоупотребление алкоголем. А учитывая, что дебют заболевания приходится на подростковый возраст, молодые люди часто нарушают эти рекомендации, особенно в студенческие годы.
Пациент, у которого выявили фотосенситивность, предрасположен к приступам под воздействием мерцающего света. Поэтому им необходимо ограничить просмотр телевизора и работу за компьютером, исключить видеоигры и избегать посещения ночных клубов.
У всех пациентов с эпилепсией имеются определённые социальные ограничения: они не могут работать в некоторых сферах, водить автомобиль и нести военную службу. Все они определяются индивидуально соответствующими комиссиями.
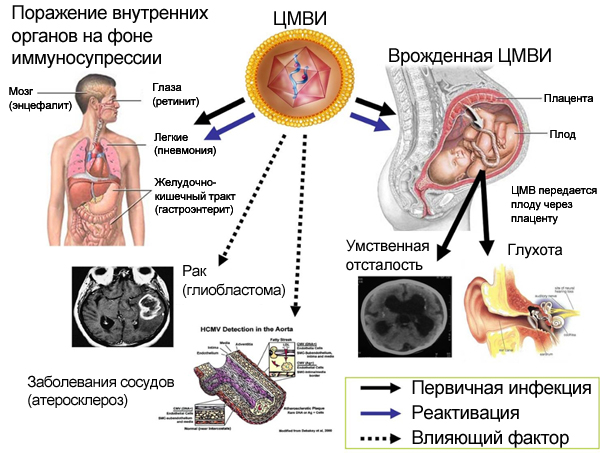
Генерализованная форма ЦМВИ (цитомегалии, цитомегаловирусной инфекции), как правило, возникает на фоне какого-либо другого заболевания, резко снижающего иммунитет (лейкозы, злокачественные опухоли, СПИД), или после тяжелых хирургических операций. Следствием цитомегалии в этом случае могут быть воспаление надпочечников, селезенки, поджелудочной железы, почек и других внутренних органов. ЦМВИ также может проявляться в виде гепатита. Доказано, что до 30% гепатитов неясной этиологии обусловлены поражением печени герпесвирусами, а именно цитомегаловирусом или вирусом простого герпеса.
Как сопутствующие явления возникают пневмонии, поражения сосудов глаза, стенок кишечника, головного мозга и периферических нервов. В составе крови уменьшается количество тромбоцитов. Кроме основного заболевания и ЦМВИ, ухудшение состояния больного может вызвать наслаивающаяся септическая бактериальная инфекция.
По статистике Всемирной Организации Здравоохранения генерализованная форма цитомегалии является причиной наибольшего количества летальных случаев в мире после гриппа и ОРВИ.
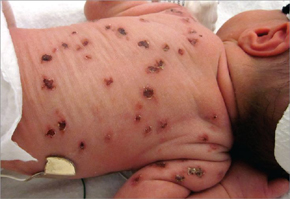
Внутриутробная ЦМВИ считается наиболее опасной, так как может вызвать серьезные поражения плода вплоть до его гибели или привести к рождению детей с тяжелыми неврологическими расстройствами, патологией зрительного и слухового нервов, различными соматическими повреждениями. Характер поражения зависит от сроков инфицирования плода ЦМВ. На ранних сроках (4–6 недель беременности) возможна его гибель или самопроизвольный выкидыш. При инфицировании цитомегаловирусом (ЦМВ) в поздние сроки беременности прогноз более благоприятен. Инфицирование ЦМВ плода во второй половине беременности может не приводить к клинически выраженной патологии при рождении, но быть причиной развития заболевания в первые недели - месяцы жизни ребенка.
Инфицирование в первые 3 месяца гестации может привести к тератогенному действию на плод, а в более поздние сроки – к врожденной цитомегалии, не сопровождающейся пороками развития. У части детей внутриутробное инфицирование ЦМВ проявляется лишь к 5–7 годам в виде нарушения зрения, ухудшения слуха, судорожных расстройств, или задержки физического и умственного развития.
В связи с этим крайне важно обследование женщин на ранних сроках беременности (оптимально – при ее планировании) с целью установления иммунного статуса в отношении ЦМВИ и выявления группы риска, требующей более серьезного и регулярного обследования вплоть до родов.
Возможность онкогенного действия вируса окончательно не изучена. Полагают, что выделение вируса цитомегалии из опухоли больных саркомой Капоши, карциномы простаты, злокачественной лимфомы, рака шейки матки, аденокарциномы толстой кишки и др. является косвенным свидетельством этиологической роли отдельных штаммов ЦМВ человека в развитии онкологических заболеваний.
Цитомегаловирусная инфекция наиболее часто поражает реципиентов трансплантируемых органов. У 38–96% пациентов после трансплантации встречается активная форма ЦМВИ, при которой каждый орган может быть вовлечен в инфекционный процесс. Клинически выраженная ЦМВИ – одно из серьезных инфекционных осложнений при трансплантации солидных органов и костного мозга, являясь одной из частых причин длительной госпитализации больных и их смерти.
Имеются данные, подтвержденные при экспериментальной инфекции у животных, что у больных, перенесших пересадку сердца, ЦМВИ является одной из причин атеросклероза. Доказано, что сосудистые поражения почечного трансплантанта с дисфункцией почки обусловлены ЦМВИ.
Период максимального риска инфицирования приходится на 1–4-й мес. после трансплантации. Максимальный риск заболевания выше при первичном инфицировании. При первичном инфицировании заболевание протекает более тяжело, чем при активизации латентной ЦМВИ.
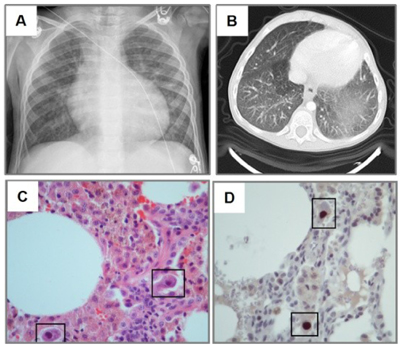
Основными проявлениями ЦМВИ у больных после трансплантации органов является гепатит, пневмония, ретинит, тяжелые поражения желудочно-кишечного тракта, лейкопения. Присоединение бактериальной, грибковой или протейной инфекции на фоне ЦМВИ могут приводить к угрожающим жизни последствиям. Так, у пациентов после трансплантации костного мозга самым тяжелым осложнением считается интерстициальная пневмония, которая диагностируется в 15–20% случаев. У 80–90% больных пневмония заканчивается летальным исходом.
Читайте также:

