При дисбактериозе кишечника повышенная кислотность
Обновлено: 19.04.2024
Главной опасностью увеличения секреторной функции желудка, является развитие воспалительного процесса в слизистой оболочке органа, с последующим её повреждением и развитием структурных дефектов. Изменение pН желудочной среды всегда сопровождается клинической симптоматикой, выраженность которой зависит от тяжести воспалительного процесса и характера структурно-функциональных нарушений.
Общая информация
В 80% случаев, причиной развития воспалительного процесса с повышенной кислотностью желудка, является микроорганизм Хеликобактер Пилори, которая нарушает естественные защитные свойства желудка и приводит к повреждению эпителия органа. Гастрит с повышенной кислотностью может развиваться у людей независимо от возраста, в том числе у детей.
К другим факторам, предрасполагающим к развитию данного состояния, можно отнести:
- Регулярное воздействие стресса на организм.
- Нерациональное питание, преобладание в рационе жареной и жирной пищи, а также блюд, приготовленных во фритюре.
- Злоупотребление так называемыми перекусами.
- Длительное или бесконтрольное использование препаратов из группы нестероидных противовоспалительных средств. Частое употребление слишком горячей или слишком холодной пищи. Кроме того, высокая предрасположенность к развитию гиперацидного гастрита имеется у людей с заболеваниями щитовидной железы, сахарным диабетом и подагрой.
Чем опасна повышенная кислотность
Желудочный сок содержит соляную кислоту, которая необходима для расщепления компонентов пищи. Для того чтобы кислотная среда не повреждала стенки желудка, вырабатывается защитная слизь. При повышенной кислотности желудка наблюдается разрушение слизистого защитного слоя, с последующим формированием воспалительного процесса, образованием эрозий и язв.
Клинические симптомы
Воспалительное поражение органа с увеличением секреции желудочного сока чаще обостряется в период межсезонья, в осенние или весенние месяцы. К симптомам повышенной кислотности желудка можно отнести:
- Тянущая или схваткообразная боль в подложечной области, которая чаще усиливается после приема пищи. При остром течении воспалительного процесса, боль может сопровождаться рвотой, которая приносит временное облегчение.
- Изжога, которая вызвана забросом кислотного содержимого желудка в пищевод. . . или диареи.
К другим симптомам повышенной кислотности желудка при гастрите относится слабость, головокружение, повышенная потливость, избыточное газообразование в кишечнике (метеоризм), усиленное слюноотделение, повышение или снижение аппетита, появление белого или серого налёта на поверхности языка. Пониженная кислотность желудка сопровождается такими симптомами, как уменьшение аппетита, ощущение тяжести в эпигастрии, отрыжка тухлым.
Диагностика
Одним из ключевых методов как определить кислотность желудка, является проведение дыхательного уреазного теста на выявление бактерии Хеликобактер Пилори. Также, выполняется ПЦР и ИФА исследования, направленные на выявление антител к данному микроорганизму. К другим обязательным методам исследования при подозрении на гастрит с повышенной кислотностью, относят:
- Эндоскопическое исследование желудка (гастроскопия).С помощью данного метода оценивается состояние желудка, пищевода и двенадцатиперстной кишки. При необходимости, во время обследования, ведется забор фрагментов слизистой оболочки (биопсия).
- Внутрижелудочная pН-метрия. Для проведения исследования используется pН-метрический трансназальный зонд, который соединён с автономным регистрирующим блоком. Если показатели pН желудочного содержимого составляют менее 1,5 единиц, то диагноз гиперацидного гастрита подтверждается.
В качестве вспомогательных методов обследования может быть назначено ультразвуковое исследование органов брюшной полости.
Лечение
Информацию о том, как снизить кислотность желудка необходимо получить у врача гастроэнтеролога. Любые варианты самолечения в домашних условиях с использованием подручных средств, являются не только малоэффективными, но и могут привести к развитию осложнений. При симптомах гастрита с повышенной кислотностью, диета и лечение предусматривает исключение из рациона жареной и жирной пищи, копченостей, фаст-фуда, алкоголя, мясных, рыбных и овощных консервов, специй, приправ, соусов. Питаться следует дробно, небольшими порциями, 4-5 раз в день. Блюда необходимо готовить преимущественно на пару или путем отваривания. При повышенной кислотности желудка назначается диета № 1 по Певзнеру.
При симптомах гастрита с пониженной кислотностью, лечение и диета включают рецепты блюд, стимулирующих кислотообразующую функцию желудка.
Для лечения повышенной кислотности желудка, традиционная медицина использует такие группы фармацевтических средств:
- Антибактериальные препараты, которые эффективны при гиперацидном гастрите, спровоцированном бактерией Хеликобактер Пилори.
- Обволакивающие средства.
- Ингибиторы протонной помпы.
- Антациды.
- Н2 гистаминовые блокаторы.
- Препараты висмута.
Для поддержания нормальной кислотности желудочного сока, важно сохранять баланс нормальной желудочной микрофлоры. С этой целью, рекомендовано использовать метапребиотики, которые содержат натуральный питательный субстрат для желудочных и кишечных бактерий. Метапребиотик Стимбифид Плюс помогает не только восстановить баланс нормальной желудочной и кишечной микробиоты, но и способствует эрадикации (уничтожению) Хеликобактер Пилори. Также, компоненты метапребиотика ускоряют процесс восстановления желудочного эпителия.
Профилактика
Уменьшить до минимума вероятность развития гиперацидного гастрита можно только при условии соблюдения профилактических мер. Если у человека имеется склонность к избыточной секреции желудочного сока, то ему необходимо придерживаться диетических рекомендаций, не злоупотреблять жареной и жирной пищей, отказаться от употребления алкоголя и фаст-фуда. Незаменимым помощником в сохранении здоровья желудка, является метапребиотик Стимбифид Плюс, который нормализует баланс желудочной микрофлоры и защищает эпителий органа от агрессивного воздействия соляной кислоты.
Известно, что в кишечнике здорового человека обитает более 300 видов различных микроорганизмов: бифидобактерии, лактобактерии, непатогенная кишечная палочка и многие другие. Численность этой популяции различается в различных отделах желудочно-кишечного т
Нарушение микробного равновесия в кишечнике называется дисбактериозом, или дисбиозом, кишечника. Основными причинами дисбактериоза кишечника являются различные заболевания ЖКТ, особенно связанные с нарушением кишечного всасывания, нерациональное питание, антибиотикотерапия (в наибольшей степени — в первые дни жизни) [5, 10].
Дисбактериоз — это не только количественное и качественное изменение кишечной микрофлоры. Согласно отраслевому стандарту, под дисбактериозом кишечника понимают клинико-лабораторный синдром, возникающий при ряде заболеваний и клинических ситуаций и характеризующийся:
- симптомами поражения кишечника;
- изменением качественного и/или количественного состава нормальной микрофлоры;
- транслокацией различных микроорганизмов в несвойственные биотопы;
- избыточным ростом микрофлоры.
В норме избыточному росту бактерий в тонкой кишке препятствуют:
- нормальная секреция соляной кислоты (предотвращает размножение бактерий в верхних отделах ЖКТ);
- илеоцекальный клапан (предупреждает поступление бактерий из толстой кишки в тонкую);
- нормальная пропульсивная моторика тонкой кишки (препятствует застою кишечного содержимого) [4].
Ведущая роль в формировании дисбактериоза принадлежит нарушению популяционного уровня бифидо- и лактобактерий. Условно-патогенные бактерии, колонизирующие слизистую оболочку кишечника, вызывают нарушение всасывания углеводов, жирных кислот, аминокислот, азота, витаминов, конкурируют с микроорганизмами полезной флоры за участие в ферментации и усвоении питательных веществ, поступающих с пищей. Продукты метаболизма (индол, скатол, сероводород и др.) и токсины, продуцируемые условно-патогенными бактериями, снижают детоксикационную способность печени, усугубляют симптомы интоксикации, подавляют регенерацию слизистой оболочки, способствуют образованию опухолей, угнетают перистальтику и обусловливают развитие диспепсического синдрома [4, 8, 9].
Микрофлора при дисбиозе не способна выполнять в полном объеме физиологические функции, присущие нормальной микрофлоре, и прежде всего противостоять колонизации кишечника экзогенными патогенными микроорганизмами.
Факторы, ведущие к нарушению нормальной флоры кишечника, многочисленны. Дисбактериоз формируется у большинства больных с острыми кишечными инфекциями, вследствие влияния патогенных микроорганизмов на нормальную флору и экологию кишечника, применения антибактериальных препаратов (антибиотиков и сульфаниламидов), подавляющих не только патогенную, но и нормальную микрофлору кишечника [1, 11]. Развитию дисбактериоза способствуют аллергия, воспалительные заболевания пищеварительного тракта (заболевания желудка, протекающие с ахлоргидрией, кишечника, поджелудочной железы, печени, резекция желудка и тонкой кишки, нарушение перистальтики, в частности стаз в толстом кишечнике), стрессы, нерациональное питание и терапия, эндокринные нарушения, ионизирующая радиация. Причинами дисбактериоза могут быть также болезни почек, В12- и фолиеводефицитная анемия, злокачественные новообразования. Дисбактериозы и вторичные иммунодефицитные состояния формируются в условиях возрастающего вредного воздействия окружающей среды на организм человека.
Важно, что дисбактериоз кишечника всегда является вторичным состоянием и, следовательно, требуется поиск первопричины. В свою очередь, дисбактериоз кишечника существенно меняет состав внутренней среды кишки, нарушая пищеварительные процессы, что оказывает повреждающее действие на кишечную стенку. Таким образом, дисбактериоз кишечника нельзя считать безобидным состоянием: он требует к себе пристального внимания [4].
Дисбактериоз кишечника может быть явным (декомпенсированным) и скрытым (компенсированным). Явный дисбактериоз кишечника, как правило, сопровождается нарушениями стула — диареей или запорами. Заподозрить скрытый дисбактериоз кишечника можно у пациента с каким-либо заболеванием ЖКТ, угнетенным состоянием иммунной системы (например, с частыми простудными, инфекционными заболеваниями), а также у больных, получающих массивные курсы антибактериальной терапии.
Устранение дисбактериоза кишечника должно начинаться с лечения первопричины, т. е. того заболевания или состояния, которое вызвало нарушение микробного состава в кишечнике, а также с коррекции питания: в рацион, если позволяет состояние пациента, следует включать достаточное количество пищевых волокон и кисломолочных продуктов. Диета должна быть полноценной по калорийности и содержанию основных ингредиентов. Желательно составить рацион так, чтобы в него входили (конечно, с учетом возраста и состояния больного) изделия из ржи, кукурузы, гречихи, проса, капуста, морковь, кабачки, томаты, огурцы, свежие фрукты, соки без консервантов, орехи, кисломолочные продукты, содержащие живые бифидобактерии и лактобактерии и бифидогенные факторы. В этих продуктах содержатся компоненты питания, обеспечивающие нормальный рост и жизнедеятельность микроорганизмов кишечника, которые называются пребиотиками. Что касается детей первого полугодия жизни, для них крайне важно полноценное грудное вскармливание. При невозможности его обеспечения следует применять адаптированные молочные смеси, содержащие пребиотики [3, 6]. Необходимо также своевременное введение в питание продуктов растительного происхождения.
Этих мер может оказаться достаточно для ликвидации кишечного дисбактериоза, но в ряде случаев приходится назначать специфическую медикаментозную терапию.
В настоящее время для коррекции дисбактериоза наиболее широко применяются препараты, содержащие живые микроорганизмы, положительно влияющие на состав кишечного микробиоценоза, так называемые пробиотики. Собственно probiosis означает сообщество двух организмов, способствующее жизнедеятельности обоих партнеров, probiotic — организм, участвующий в симбиозе. Согласно классическому определению, пробиотики — это живые микроорганизмы, которые благоприятно влияют на здоровье человека, нормализуя его кишечную микрофлору. Пробиотики широко используются в качестве пищевых добавок, в йогуртах и других молочных продуктах, а также в составе лекарственных препаратов. Микроорганизмы, входящие в состав пробиотиков, должны быть непатогенными, нетоксигенными и сохранять жизнеспособность при длительном хранении [9]. Различают следующие основные группы пробиотиков [4]:
- препараты, содержащие живые микроорганизмы и структурные компоненты;
- препараты, содержащие комплекс живых микроорганизмов, их структурных компонентов и метаболитов в различных сочетаниях;
- препараты на основе живых генноинженерных штаммов микроорганизмов;
- продукты функционального питания, способные восстанавливать микробную экологию организма хозяина.
С этой целью могут применяться препараты, содержащие микроорганизмы — обычные обитатели кишечника, в том числе бифидо- и лактобактерии, а также микроорганизмы, которые в норме в кишечнике человека не обитают (например, Bacillus cereus IP 5832 или Saccharomyces boulardii). Эти препараты могут быть монокомпонентными, т. е. включать только один вид микроорганизмов, или многокомпонентными. Доказано, что положительный эффект на кишечную микрофлору оказывают следующие микроорганизмы: Lactobacillus (L.) acidophilus, L. GG, L. fermentum, Strepto- (Entero-)coccus faecium SF68, Streptococcus (S.) termophilus, Bifidobacterium (B.) bifidum. В связи с этим для коррекции дисбактериоза кишечника наиболее целесообразно использовать многокомпонентные лекарственные средства, содержащие вышеперечисленные микроорганизмы. Эти препараты обычно назначаются курсами, длительностью не менее 1 мес.
Современные бактерийные препараты (бифидумбактерин, лактобактерин, линекс и др.) относятся к категории биотерапевтических, т. е. лечебных препаратов. Механизм действия биотерапевтических препаратов обусловлен наличием у микроорганизмов, входящих в их состав, ряда функциональных свойств: способности выживать в кислой среде, эффективно прикрепляться к эпителиоцитам слизистой стенки кишки и колонизировать ее, продуцировать антимикробные вещества, вызывать стимуляцию иммунной системы, предупреждать избыточный рост и размножение патогенных микробов и восстанавливать нормальную микрофлору кишечника [4].
Продвигаясь по пищеварительному тракту, микроорганизмы сохраняют свою жизнеспособность и обеспечивают временное полезное воздействие на микрофлору кишечника, модифицируя ее состав и метаболическую активность. Пробиотики могут включаться в питание в качестве диетических добавок в виде лиофилизированных порошков, содержащих бифидобактерии, лактобактерии и их комбинации [3].
Эффективность пробиотиков зависит от многих факторов: их состава, состояния микрофлоры организма человека, образа жизни и др. Наиболее часто назначаются и наиболее хорошо изучены пробиотики, изготовленные на основе бифидобактерий и лактобактерий.
Пробиотики должны соответствовать следующим требованиям:
- оказывать положительное действие на организм хозяина;
- не вызывать побочных эффектов при длительном применении;
- обладать колонизационным потенциалом, т. е. сохраняться в пищеварительном тракте до достижения максимального положительного эффекта (быть устойчивыми к низкой кислотности, желчным кислотам, антимикробным токсинам и ферментам, продуцируемым патогенной микрофлорой);
- обладать стабильной клинической эффективностью, простотой технологии получения [4].
Известно, что соляная кислота и пепсин желудка являются довольно серьезным препятствием для продвижения микроорганизмов. Однако значительная часть бифидо- и лактобактерий, принимаемых перорально, успешно преодолевают этот барьер и в конечном итоге оказываются в толстой кишке. Всего при пероральном приеме сквозь весь пищеварительный тракт проходит от 20 до 40% бифидо- и лактобактерий. Выживаемость бактерий в ЖКТ повышается при одновременном приеме пищи, которая не только снижает кислотность желудочного содержимого и играет роль своеобразного буфера, но и создает благоприятные условия для питания микроорганизмов, выполняя пребиотическую функцию. Несмотря на то, что после приема бактерии обнаруживаются в стуле от 1 до 3 нед, колонизирующая способность бифидо- и лактобактерий в кишечнике невысока. Поэтому для обеспечения постоянного присутствия микроорганизмов в микрофлоре кишечника и достижения стойкого положительного эффекта от применения бифидо- и лактобактерий, содержащие их препараты должны приниматься непрерывно в течение длительного времени и в значительном количестве [3, 9].
Результаты многочисленных исследований подтверждают, что инфекции пищеварительного тракта могут быть предотвращены или излечены при применении бифидо- и лактобактерий. Наибольшие данные накоплены по терапии молочнокислыми бактериями ротавирусных гастроэнтеритов. L. acidophilus быстро устраняет диарею. Этот же штамм показывает высокую эффективность против грибка Candida albicans. Продолжительность диареи, обусловленной вирусной инфекцией, у детей достоверно сокращается после приема L. GG. Также показано угнетающее действие L. acidophilus на сальмонеллы. Подтверждено действие бифидо- и лактобактерий при диарее путешественников [2].
Бифидо- и лактобактерии, применяемые в составе пробиотиков, обеспечивают стабилизацию микрофлоры организма человека, восстанавливают ее нарушенный баланс, а также целостность эпителиальных клеточных образований и стимулируют иммунологические функции слизистой оболочки пищеварительного тракта. Энтерококки и коли-бактерии в большей степени обладают иммуномодулирующим воздействием.
Под синбиотиками понимают комбинацию пробиотиков и пребиотиков, которая оказывает положительный эффект на здоровье организма-хозяина, способствуя выживаемости и колонизирующей способности в кишечнике живых бактериальных добавок и избирательно стимулируя рост и активацию метаболизма лакто- и бифидобактерий.
Особую группу составляют препараты, содержащие метаболиты микроорганизмов (дисахариды, органические кислоты) и другие стимуляторы размножения нормальной микрофлоры, к которым относятся парааминометилбензойная кислота (памба, амбен), хилак форте и др.
Важно, что пробиотики назначают не в качестве заместительной терапии, а как средства, обеспечивающие условия для восстановления нормальной микрофлоры. Для лечения дисбактериоза кишечника применяют многочисленные пробиотические препараты.
В последнее время большой интерес вызывают синбиотики, представляющие собой рациональную комбинацию пробиотиков, микробных метаболитов и пребиотиков, которая оказывает положительный эффект на здоровье организма-хозяина, способствуя выживаемости и приживляемости в кишечнике живых бактериальных добавок и избирательно стимулируя рост и активацию метаболизма лакто- и бифидобактерий (нормофлорин-Л, нормофлорин-Б, нормофлорин-Д, гастрофарм, биофлор и др.).
Препараты бифидобактерий — наиболее многочисленная группа пробиотических препаратов, содержащих различные штаммы бифидобактерий (как представителей нормальной микрофлоры кишечника, так и синтетические штаммы). Препараты бифидобактерий применяются для лечения и профилактики дисбиозов, некоторые (бифидумбактерин форте и др.) при лечении антибактериальными препаратами для профилактики антибиотикассоциированного дисбиоза и пр. Бифидобактерии не оказывают токсического действия на организм ребенка, поэтому бифидопрепараты практически не имеют противопоказаний.
Препараты лактобактерий. Действующим началом этих пробиотиков являются живые лактобактерии. Корригирующую терапию лактосодержащими пробиотиками можно назначать совместно или последовательно в течение 2–3 сут после лечения специфическими бактериофагами, предназначенными для элиминации условно-патогенных бактерий, или с химиотерапевтическими препаратами направленного действия.
Нецелесообразно назначать лактосодержащие препараты при средних, выраженных и затяжных формах кандидамикозов, так как продуцируемые лактобактериями кислоты способствуют увеличению количественного состава грибов рода Candida [3].
Колисодержащие препараты изготовлены на основе живых бактерий Escherichia coli штамма М-17, которые обладают антагонистической активностью, иммунокорригирующим действием, оказывают местное и системное протективное действие.
Препараты, содержащие культуры бактерий, обладающих антагонистической активностью. Лечебное действие препаратов из непатогенных представителей рода Bacillus (споробактерин жидкий, бактиспорин, биоспорин, бактисубтил) и лечебных дрожжей Saccharomyces Boulardii (энтерол) обусловлено их выраженными антагонистическими свойствами против широкого спектра патогенных и условно-патогенных микроорганизмов. Эти пробиотики синтезируют комплекс ферментов, стимулирующих пищеварение. Имеются разные точки зрения на применение бактерийных препаратов, содержащих аэробные спорообразующие бактерии. Существуют указания на то, что искусственное введение в кишечник этих бактерий в больших количествах и излишнее размножение бацилл в нехарактерном для них микробиотопе, сопровождающееся распространением бацилл за пределы кишечника, может ухудшить состояние пациента. Поэтому эти препараты рекомендуется назначать кратковременно с последующим применением бифидо- и лактосодержащих пробиотиков.
Дрожжевые грибы Saccharomyces Boulardii принадлежат к высшим одноклеточным организмам — эукариотам. Их генетической природной особенностью является устойчивость к действию всех групп антибиотиков, сульфаниламидов и других антимикробных средств. В то же время они чувствительны к фунгицидным средствам. В настоящее время колонии Saccharomyces Boulardii выращивают на стандартных средах, затем они подвергаются ферментной обработке, лиофилизируются и хранятся в виде порошка. Лиофилизированные дрожжевые клетки оживают в среде желудка, а также в аэробных условиях кишечника.
Комплекс пробиотиков и их метаболитов. Несмотря на довольно широкое использование, бактериальные препараты на основе живых микроорганизмов не всегда оказываются высокоэффективными. Возможно, это связано с быстрой элиминацией вводимых в агрессивную среду штаммов, из-за высокой толерантности иммунной системы к собственной микрофлоре. Высокая себестоимость также ограничивает их применение. Решение проблем коррекции дисбактериозов может заключаться в разработке и во внедрении в клиническую практику принципиально новых препаратов, созданных на основе компонентов микробных клеток или их метаболитов. Такие препараты реализуют свое положительное влияние на физиологические функции и биохимические реакции организма хозяина, либо непосредственно вмешиваясь в метаболическую активность клеток соответствующих органов и тканей, либо опосредованно — через регуляцию функционирования биопленок на слизистых макроорганизма.
Таким образом, коррекция дисбактериоза как у детей, так и у взрослых представляется многогранной проблемой, которая требует учета как первопричины ее возникновения, так и множества сопутствующих факторов. Тем не менее в настоящее время разработаны и внедрены в повседневную практику эффективные средства коррекции состава кишечной микрофлоры, а врач, руководствуясь своими знаниями и опытом, может определить комбинацию, наиболее целесообразную для каждого конкретного пациента.
Литература
С. В. Бельмер, доктор медицинских наук
А. В. Малкоч, кандидат медицинских наук
РГМУ, Москва
Заболевания органов пищеварительной системы во многом связаны с особенностями пищевого поведения. Отсутствие режима питания, неадекватные диеты, агрессивная пища, голодание наряду с перееданием - все это приводит к неблагоприятным последствиям. В группе особого риска пациенты с осложненным гастроэнтерологическим анамнезом, лица, употребляющие алкогольные напитки, курильщики. К лечению расстройств пищевого поведения подключаются психотерапевты, гастроэнтерологи, терапевты, диетологи.
Под агрессивной пищей понимают консервацию, копчености, пряности, соленья, маринады. В этот список входят промышленные соусы, сдоба, жирное мясо, фастфуд и другие. Неправильное питание и неумеренность в еде приводят к заболеваниям органов ЖКТ, снижению функции желудка и кишечника, общесоматические расстройства.
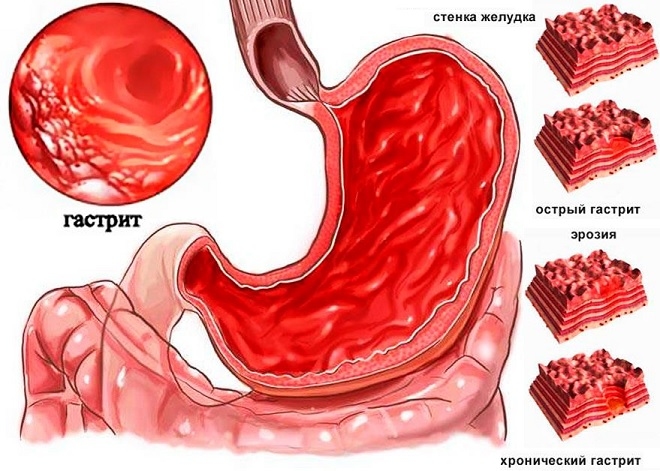
Хронический гастрит
Хронический гастрит развивается, преимущественно, при отсутствии пищевой дисциплины. Половина населения планеты страдают от гастрита. Важное клиническое значение имеет кислотность желудочного сока и уровень его секреции. При пониженной секреции патология сопровождается снижением аппетита, горечью во рту, позывами к рвоте сразу после приема пищи (чаще всего после переедания). При повышенной секреции болезнь характеризуется болью и дискомфортом в эпигастрии, тошнотой, болевым синдромом в области поджелудочной железы.
Лечение комплексное, включает коррекцию образа жизни, питания. С целью симптоматической терапии назначают антацидные, обволакивающие препараты, обезболивающие. Важно не заниматься самолечением, а пройти обследовать и подобрать индивидуальную схему терапии с учетом клинического анамнеза больного.
Гастрит часто осложняется язвенной болезнью, профузными кровотечениями или геморрагическим шоком при эрозивном поражении. При флегмонозном гастрите есть вероятность перфорации стенок органа, деформации желудка, образования свищевых ходов. При недостатке фактора Касла у 90% всех больных хроническим гастритом развивается мегалобластная анемия. При длительном течении патологического процесса есть риск озлокачествления слизистого эпителия и образования аденокарциномы.
Кишечный дисбактериоз
Дисбактериоз кишечника или кишечный симбиоз - патологическое состояние микрофлоры кишечника, обусловленное с нарушением видового состава бактерий. При дисбактериозе условно-патогенная микрофлора меняет численный состав в сторону патогенной, что сопровождается диареей, метеоризмом, отделением зловонных газов, снижением аппетита, зудом в анусе из-за частых дефекаций. Нередко при дисбактериозе в каловых массах появляется скрытая кровь (выявляется лабораторно), кровяные прожилки, которые можно рассмотреть. Появление симптома требует срочной коррекции, чтобы исключить развитие более серьезных осложнений.
С целью лечения назначают бифидобактерии, кисломолочные продукты, лактобактерии. Спустя 1-2 недели стул восстанавливается, состояние нормализуется. Коррегируют и питание. Легкие формы дисбактериоза можно вылечить питанием: кисломолочными продуктами, сбалансированным рационом, обогащением питания клетчаткой, свежими овощами, фруктами.
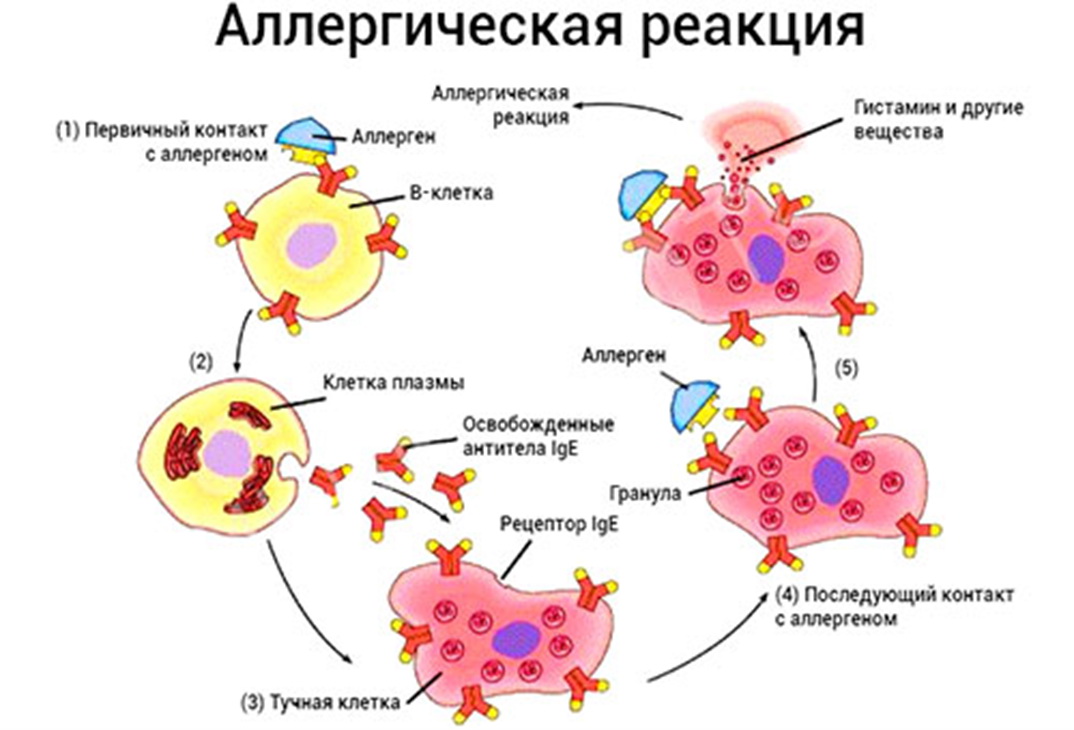
Аллергические реакции
Аллергией на пищу страдают более 12% взрослых и почти 35-40% детей. Увеличение статистики связано с ухудшением экологической ситуации, употреблением в пищу консервации, красителей, стабилизаторов, эмульгаторов. Аллергические реакции встречаются при употреблении промышленных продуктов питания. При отягощенном аллергоанамнезе следует уделить внимание качеству и видовому составу пищи. Чаще всего аллергия развивается на клубнику, томаты, цитрусовые, цельное молоко, какао и шоколад.
Головные боли
Частые головные боли, в том числе мигренеподобные, развиваются в результате негативного воздействия пищи. Одним из провокаторов головной боли является тирамин, который содержится в сырах и кисломолочной продукции, слабосоленой, соленой и маринованной рыбе, шоколаде, копченом мясе, колбасных продуктов.
Вызвать головную боль может и глютамат натрия - усилитель вкуса, который входит в соевый соус и блюда китайской, японской кухни. Если головные боли возникают сразу или через некоторое время после приема пищи, то можно подозревать некоторые пищевые ингредиенты.
Появление признаков пищевых расстройств и симптомов заболеваний органов ЖКТ требует обращения к доктору гастроэнтерологу. В нашей клинике А2МЕД в Симферополе пациенты могут пройти полный комплекс обследований, получить консультацию опытного диетолога. Коррекция рациона и навык правильного выбора еды для всей семьи - залог здоровья на долгие годы.
ОПТИМАЛЬНАЯ КИСЛОТНОСТЬ ДЛЯ РОСТА И РАЗВИТИЯ ПОЛЕЗНОЙ МИКРОФЛОРЫ и УГНЕТЕНИЯ УСЛОВНО-ПАТОГЕННОЙ
Кислотность (лат. aciditas) — характеристика активности ионов водорода в растворах и жидкостях.
Водородный показатель pH
В растворах неорганические вещества: соли, кислоты и щелочи разделяются на составляющие их ионы. При этом ионы водорода H + являются носителями кислотных свойств, а ионы OH − – носителями щелочных свойств. В сильно разбавленных растворах кислотные и щелочные свойства зависят от концентраций ионов H + и OH − . В обычных растворах кислотные и щелочные свойства зависят от активностей ионов аН и аOН, то есть от тех же концентраций, но с поправкой на коэффициент активности γ, который определяется экспериментально. Для водных растворов действует уравнение равновесия: аН × аOН = К w, где К w – константа, ионное произведение воды (К w = 10 −14 при температуре воды 22 °C). Из этого уравнения следует, что активность ионов водорода H + и активность ионов OH − связаны между собой. Датским биохимиком С.П.Л. Серенсеном в 1909 году был предложен водородный показать рН, равный по определению десятичному логарифму активности водородных ионов, взятому с минусом:
рН = — lg (аН).
Т.е. водородный показатель pH показывает концентрацию свободных ионов водорода в воде. Водородный показатель pH - это отрицательный десятичный логарифм концентрации ионов водорода в воде. Исходя из того, что в нейтральной среде аН = аOН и из выполнения равенства для чистой воды при 22 °С: аН × аOН = Кw = 10 −14 , получаем, что кислотность чистой воды при 22 °С (то есть нейтральная кислотность) = 7 ед. pH.
Растворы и жидкости в отношении их кислотности считаются:
• нейтральными при рН = 7
• кислыми при pH < 7
• щелочными при рН > 7
Большинство микроорганизмов развивается при нейтральной или слабощелочной реакции среды. Есть среди бактерий кислотоустойчивые, например, молочнокислые, и некоторые уксуснокислые бактерии.
При подкислении среды до рН 4 развитие большинства бактерий практически прекращается. К колебаниям рН в пределах от 6 до 9 бактерии сравнительно малочувствительны.
Пропионовокислые бактерии растут в пределах температуры - (15-40) 0 С, хотя есть данные, что рост происходит при более низкой температуре (до минус 100 0 С).
Оптимальная температура развития классических пропионовокислых бактерий - (30±1) 0 С. (для бифидобактерий 37°С)
Оптимальная величина рН роста пропионовокислых бактерий - 6,5-7,0, максимальная - 8,0, минимальная - 4,5.
Например, исследованные штаммы пропионовокислых бактерий Propionibacterium freudenreichii subsp freudereichii АС-2500, P. cyclohexanicum Kusano АС-2259, P. freudenreichii subsp. shemanii AC–2503, P. cyclohexa-nicum Kusano АС-2260, P. freudenreichii subsp. shermanii – КМ 186. проявили устойчивость к высокой концентрации желчи (40%), NaCl (6%) и развивались в среде с низким рН (4,5), что указывает на высокую выживаемость данных культур в неблагоприятных условиях ЖКТ человека.
Кислотность… Некоторые заблуждения
Когда говорят о кислотности кого-либо органа, важно при этом понимать, что часто в различных частях органа кислотность может значительно отличаться. Кислотность содержимого в просвете органа и кислотность на поверхности слизистой оболочки органа также часто бывает не одинаковой. Для слизистой оболочки тела желудка характерно, что кислотность на поверхности слизи, обращенной в просвет желудка кислотность 1,2–1,5 рН, а на стороне слизи, обращённой к эпителию — нейтральная (7,0 рН).
Кислотность в желудке. Повышенная и пониженная кислотность

Максимальная теоретически возможная кислотность в желудке 0,86 рН, что соответствует кислотопродукции 160 ммоль/л. Минимальная теоретически возможная кислотность в желудке 8,3 рН, что соответствует кислотности насыщенного раствора ионов HCO3 - . Нормальная кислотность в просвете тела желудка натощак 1,5–2,0 рН. Кислотность на поверхности эпителиального слоя, обращённого в просвет желудка 1,5–2,0 рН. Кислотность в глубине эпителиального слоя желудка около 7,0 рН. Нормальная кислотность в антруме желудка 1,3–7,4 рН.
Кислотность в кишечнике
Нормальная кислотность в луковице двенадцатиперстной кишки 5,6–7,9 рН. Кислотность в тощей и подвздошной кишках нейтральная или слабощелочная и находится в пределах от 7 до 8 рН. Кислотность сока тонкой кишки 7,2–7,5 рН. При усилении секреции достигает 8,6 рН. Кислотность секрета дуоденальных желез — от рН от 7 до 8 рН.
Кислотность сока толстой кишки 8,5–9,0 рН.
Кислотность кала
Кислотность кала здорового человека, питающегося смешанной пищей обусловлена жизнедеятельность микрофлоры толстой кишки и равна 6,8–7,6 рН. Нормальной считается кислотность кала в диапазоне от 6,0 до 8,0 рН. Кислотность мекония (первородного кала новорожденных) — около 6 рН. Отклонения от нормы при кислотности кала:
- резко-кислая (рН менее 5,5) бывает при бродильной диспепсии
- кислая (рН от 5,5 до 6,7) может быть из-за нарушения всасывания в тонкой кишке жирных кислот
- щелочная (рН от 8,0 до 8,5) может быть из-за гниения белков пищи, не переваренных в желудке и тонкой кишке и воспалительного экссудата в результате активации гнилостной микрофлоры и образования аммиака и других щёлочных компонентов в толстой кишке
- резкощелочная (рН более 8,5) бывает при гнилостной диспепсии (колите)
Таблица 1. Величины кислотности некоторых распространенных продуктов и чистой воды при разной температуре
Читайте также:


