При гангренозной пиодермии назначаются
Обновлено: 23.04.2024
Гангренозная пиодермия встречается редко, поражаются в равной степени и мужчины, и женщины. Пик заболеваемости приходится на возраст 25-54 года. Хотя и редко, заболевание может встречаться у детей.
Точные этиология и патогенез большей частью неизвестны, но предполагают, что заболевание представляет собой проявление измененной иммунологической реактивности, о чем свидетельствуют многочисленные гуморальные и клеточно-опосредуемые нарушения, которые наблюдаются в связи с гангренозной пиодермией.
Патогенетический ответ, проявляющийся возникновением очагов заболевания в местах травмы, представляет собой измененный и неконтролируемый воспалительный процесс, который наблюдается у пациентов с нарушениями иммунной реактивности.Гангренозная пиодермия - это нейтрофильный дерматоз, гистологическим признаком которого является интенсивный дермальный нейтрофильный инфильтрат без первичного васкулита.
Клинически гангренозная пиодермия разделяется на четыре формы.
- язвенная
- пустулезная
- буллезная
- вегетативная (поверхностная гранулематозная пиодермия)
Язвенная гангренозная пиодермия
Пустулезная гангренозная пиодермия
Буллезная гангренозная пиодермия
Вегетативная гангренозная пиодерия
Системные заболевания, которые могут ассоциироваться с гангренозной пиодермией
Особенно важно исключить различные инфекции, которые имитируют болезнь, поскольку они могут ухудшиться, если начинают иммуносупрессивную терапию по поводу предположительного диагноза гангренозной пиодермии
- Воспалительное заболевание кишечника. Гангренозная пиодермия наблюдается при язвенном колите и болезни Крона с равной частотой (1, 5-5%) и может предшествовать, протекать одновременно с этими заболеваниями или следовать за ним. Заболевание имеет обычно язвенную или пустулезную форму.
- Артрит. 37% случаев язвенной формы связаны с артритом. Это обычно серонегативный моноартрит крупных суставови реже, артриты при воспалительных заболеваниях кишечника, ревматоидный артрит, синдром Фелти, остеоартрит и сакроилеит.
- Иммунологическое заболевание: врожденная и приобретенная гипогаммаглобулинемия, избирательная недостаточность IgA, синдром гипоиммуноглобулинемии Е, иммуносупрессия.
- Моноклональная гаммапатия. Наблюдается в 10% случаев, обычно при язвенной форме. Обычно связана с секрецией IgA.
- Злокачественное заболевание. Наблюдается в 7% случаев, обычно при буллезной форме. Наиболее часто гангренозная пиодермия ассоциируется с гематологическими злокачественными процессами - лейкемией (острой миелоидной лейкемией, хронической миелоидной лейкемией), множественной IgA-миеломой и макроглобулинемией Вальденстрема, истинной красной полицитемией и другими (миелофиброзом, ходжкинской и неходжкинской лимфомами, кожной Т-клеточной лимфомой), а также с солидными опухолями (редко) - карциноидом, раком кишечника, мочевого пузыря, простаты, молочной железы, бронхов или яичников.
- Другие заболевания: хронический активный гепатит, заболевание щитовидной железы и, возможно, его лечение пропил- тиоурацилом, аутоиммунная гемолитическая анемия, хроническое обструктивное заболевание легких, гнойный гидраденит, конглобатное акне, саркоидоз, атрофический гастрит, сахарный диабет, системная красная волчанка (СКВ) и болезнь Такаясу.
Диагноз основывается главным образом на клинических признаках, поскольку патогномоничные гистопатологические характеристики и специфические серологические и гематологические маркеры отсутствуют.Диагноз является диагнозом исключения, и большинство исследований проводится, чтобы исключить другие состояния, которые могут клинически напоминать гаргренозную пиодермию.
Диагностические критерии
К основным диагностическим критериям относятся:
- возникновение болезненных язвенных дефектов вслед за незначительными травмами
- сильные болевые ощущения в зоне поражения, которые не зависят от глубины поражения
- отсутствие роста патологической флоры при бактериологическом исследовании.
К дополнительным критериям относятся:
- характерные патоморфологические изменения в краевой зоне очага (обильная нейтрофильная инфильтрация с явлениями васкулита, отложение иммуноглобулина G и комплемента в сосудах дермы);
- частые ассоциации с такими заболеваниями, как язвенный колит, болезнь Крона, ревматоидный артрит, болезни крови
- положительный тест на патергию (25-50%)
- отсутствие или слабо-выраженный эффект от традиционного лечения язв;
- активная положительная динамика на фоне системной иммуносупрессивной терапии
Гистологическое исследование
Ведущим гистологическим признаком является наличие нейтрофильных дермальных абсцессов в сочетании с другими характеристиками, которые зависят от клинического типа заболевания:
- изъязвлением эпидермиса, фолликулярным / перифолликулярным и лимфоцитарным васкулитом на периферии при язвенной форме;
- субкорнеальными пустулами и субэпидермальным отеком при пустулезной форме;
- субэпидермальным пузырем при буллезной форме;
- псевдоэпителиоматозной гиперплазией, синусными пучками и палисадной гранулематозной реакцией при вегетативной форме.
Исключение имитирующих заболеваний
Исследования для исключения состояний, имитирующих заболевание, включают:
- биопсию кожи с окрашиванием препаратов гематоксилином и эозином, культуральное исследование микроорганизмов (бактерий, грибов и микобактерий), а также прямую иммунофлуоресценцию для исключения васкулита;
- анализы крови: йодид и бромид; кальций и фосфат; антитела люпусного антикоагулянта/антикардиолипина; антинейтрофильное цитоплазматическое антитело (С и перинуклеарное антинейтрофильное цитоплазматическое антитело (Р-АНЦА)); серологическое исследование на сифилис.
Диагностика ассоциированных заболеваний
Исследования для диагностики ассоциированного системного заболевания включают:
- гастроинтестинальные исследования: бариевая клизма, проктосигмоидоскопия/колоноскопия;
- гематологические тесты: полный анализ крови, электрофорез сывороточного белка;белок Бенс-Джонса в моче; биопсия костного мозга; компьютерная томография грудной клетки/ брюшной полости/ малого таза и биопсия лимфатического узла;
- другие тесты: рентгенологическое исследование суставов, ревматоидный фактор, антинуклеарное антитело; у-глобулин и ВИЧ.
Ряд состояний клинически имитируют заболевание и тем самым значительно осложняют установление диагноза. Дифференциальный диагноз гангренозной пиодермии включает:
- Инфекционные: бактерии туберкулезные и атипичные микобактерии, третичный гуммозный сифилис, синергическая гангрена, бластомикозоподобная пиодермия
- Глубокие грибковые инфекции, амебиаз
- Вирусные инфекции - хроническая инфекция вирусом ветряной оспы у пациентов с иммунодефицитом
- Неинфекционные
- системный васкулит
- антифосфолипидный синдром
- некротизирующий арахнидизм (укус паука)
- Опухоли
- первичные злокачественные опухоли кожи
- метастазы
- Лекарства / токсины
- галогенодерматоз - йодиды или бромиды
- колониестимулирующий фактор гранулоцитов (G-CSF)
- изотретиноин
- Травма - включая механические дерматозы
- Кальцифилаксия
- Профилактика и лечение вторичных раневых инфекций, а именно: ежедневная очистка раны стерильными солевыми и антисептическими растворами, . герметичные гидроколлоидные повязки, которые защищают рану и обеспечивают кислотную среду, препятствующую росту микробов, постоянное наблюдение за раной для исключения инфекции путем взятия культуры жидкости с поверхности раны и немедленное применение местных и системных антибиотиков при первом признаке инфекции.
- Санация дна раны: агрессивная хирургическая санация противопоказана из-за патергической реакции. Поэтому необходима мягкая санация, которую обычно проводят влажными солевыми компрессами, 0, 5% нитратом серебра, жидкостью Бурова, раствором перманганата калия, а также с помощью гидромассажа, гидроколлоидных повязок или гидроактивных гелей.
- Содействие реэпителизапии и закрытию раны: кроме предохранения раны от инфекции, можно также попытаться стимулировать реэпителизацию раны, повышая уровни факторов роста на ее поверхности. Этого можно добиться с помощью герметичных гидроколлоидных повязок, которые концентрируют факторы роста на поверхности раны, а также выращенных в культуре аутотрансплантатов кератиноцитов и расщепленного кожного трансплантата при одновременной специфической иммунотерапии и, кроме того, применением местных препаратов с факторами роста.
В недавнем исследовании сообщалось, что использование полученной с помощью методов биотехнологии кожи в качестве вспомогательного мероприятия в ходе иммуносупрессивной терапии циклоспорином ускоряло заживление и уменьшало боль в случае быстро расширяющейся язвы голени. В течение 2 нед. язва зажила на 30-40%, а 100% реэпителизация была достигнута за 6 нед. - Кортикостероиды.Кортикостероиды действуют благодаря своим противовоспалительным и иммуносупрессивным свойствам, но одно из исследований предполагает, что кортикостероиды при этом заболевании могут восстанавливать функцию моноцитов. Кортикостероиды назначаются различными способами, все эти способы можно использовать при всех формах.
- Агенты, ингибирующие функцию нейтрофилов.Антинейтрофильные препараты оказывают благотворное действие , исходя из того факта, что заболевание преимущественно характеризуется нейтрофильным дермальным инфильтратом. Основным показанием для этих препаратов является их применение для экономии стероидов или дополнительно к стероиду, когда последний дает лишь частичный ответ, а также при неагрессивном распространенном заболевании и при неэффективности местной терапии.
- Иммуносупрессоры и иммуномодуляторы.Механизм действия этих препаратов связан с коррекцией или изменением иммунологических дефектов, присущих заболеванию. Иммуносупрессоры и иммуномодуляторы назначаются в качестве вспомогательной или альтернативной терапии, когда системные кортикостероиды оказываются неэффективными, или в качестве терапии первой линии вместе с системными стероидами при агрессивном заболевании.
- Хромогликат натрия.Этот препарат помогает, если его применять в форме 1-4% раствора 3 раза в день в качестве монотерапии локального заболевания либо в качестве вспомогательной терапии при распространенном заболевании.
- Талидомид.Препарат назначают в дозе 150-400 мг/день. Основные побочные действия - тератогенность и невропатия.
- Йодид калия.Йодид калия назначают в дозе 300 мг 2 или 3 раза в день. Основные побочные действия - металлический привкус во рту, артралгия, иногда возможно возникновение нейтрофильного дерматоза.
- Замещение плазмы.Замещение плазмы проводят 3 раза в неделю, общее число процедур - 4-27. Основными побочными эффектами являются нарушение жидкостного и электролитического баланса, тенденция к кровотечениям и инфекции.
- Внутривенный иммуноглобулин G.Внутривенный иммуноглобулин G назначают в дозе 0, 4 г/день в течение 5 дней, а затем через 2 нед. в дозе 0, 1 г/день в течение 2 дней. Основные побочные действия - высокая стоимость лечения, головная боль и повышенная частота инфекций.
- 5-аминосалициловая кислота.Препарат эффективен при местном ежедневном применении на очаги поражения в форме 10% крема. Механизм действия сводится, вероятно, к супрессии подвижности лейкоцитов и цитотоксичности.
- Никотиновая камедь.Эффект ремиссии замечают при дозе 6 г/день.
- Азотистый иприт.Эффективен при применении в виде 20% раствора.
- Цитозина арабинозид и даунорубицин
- Микофенолата мофетил
- Лечение китайскими травами.Применяют внутрь мультигликозид Tripterygium wiifordii.
- Классическую(язвенную) гангренозную пиодермию, которая характеризуется глубокими язвами фиолетового оттенка с краями, нависающими над поверхностью дефекта кожи. Патология сочетается с системными процессами в кишечнике, суставах, лёгочной ткани. В эту группу входят пиостоматит, пиогенное гангренозное поражение половых органов, периорбитальных тканей, слизистых верхних дыхательных путей.
- Атипичнуюгангренозную пиодермию, состоящую из буллёзной и пустулёзной разновидности. Данная форма заболевания сопутствует бластным лейкозам или миелопролиферативным заболеваниям, характеризуется пузырными или гнойчиковыми высыпаниями на отёчной кайме по периферии язвы с локализацией на лице и конечностях.
- Посттравматическую гангренозную пиодермию, возникающую на фоне патергии.
- Фагеденическую гангренозную пиодермию, эндемичную для тропиков и субтропиков, отличительной чертой которой является множественность и прочное спаивание с подлежащими тканями.
- Злокачественную поверхностную гранулематозную гангренозную пиодермию, сопровождающую системные патологии и злокачественные опухоли.
Общие терапевтические рекомендации
Уход за раной
Базовой целью ухода за раной является создание идеальных условий для содействия ее реэпителизации и закрытию, а специфическая терапия применяется для контроля воспаления, которое приводит к изъязвлению. Проводятся следующие мероприятия.
Купирование боли
Очаги при гангренозной пиодермии очень болезненные и, хотя специфическая терапия ослабляет боль, чаще все-таки нужны немедленные мероприятия по купированию боли. К ним обычно относятся поэтапное применение анальгетиков (парацетамола, нестероидных противовоспалительных препаратов, опиоидов и их комбинаций), а также специфическая гипербарическая оксигенация и, возможно, ципрогептадин.
Рекомендуемые методы терапии
Поскольку ГП является иммунологическим расстройством, специфическая терапия выключает главным образом вещества, которые подавляют или модулируют иммунную систему. Рекомендуются кортикостероиды, вещества, ингибирующие активность нейтрофилов, иммуносупрессоры и иммуномодуляторы.
Альтернативные и экспериментальные методы лечения
Хирургия
Пациентам с нестабильным состоянием и многочисленными, не поддающимися лечению медицинскими проблемами может быть показано хирургическое лечение ГП из-за наличия сопутствующих, угрожающих жизни заболеваний. В современной литературе указывается, что хирургическое лечение ГП может быть адекватным и при других особых обстоятельствах. Хирургическое лечение, включая ампутацию, может играть определенную роль в терапии ГП. Однако необходимы дальнейшие исследования для точного определения обстоятельств и индивидуальных факторов, которые являются адекватными показаниями для такой хирургии.
Гангренозная пиодермия – вторичный дерматоз с деструкцией кожи и омертвением подлежащих тканей, сопровождающий системные патологии. Клинически проявляется высыпанием булл с серозным, гнойным или геморрагическим содержимым, которые вскрываются, образуя расширяющиеся по периферии розовые язвы размером с ладонь с рваными краями и пиогенным отделяемым. Появление язв сопровождается продромой. Диагностируют гангренозную пиодермию на основании системной патологии в анамнезе и типичной кожной симптоматики – пиогенных язв. Для исключения других дерматозов выполняют комплекс лабораторных исследований. Осуществляют лечение первичной патологии, параллельно назначают кортикостероиды и антибиотики внутрь, наружно применяют турбулентные ванны, влажные антисептические повязки.
Общие сведения
Гангренозная пиодермия – тяжёлый прогрессирующий некроз кожи, возникающий на фоне системной патологии и характеризующийся образованием глубоких язв с гнойно-некротическим отделяемым. Гангренозная пиодермия является редким заболеванием, ежегодно диагностируется у 1-3 из 100 000 человек. Чаще всего кожная патология сопровождает воспалительные заболевания пищеварительной системы (30%), патергию (30%), артриты, опухоли, лейкозы. От 25% до 50% случаев гангренозной пиодермии имеют идиопатический характер. Первые описания гангренозной фагеденической язвы принадлежат французскому дерматологу Луи Броку, исследовавшему данную патологию в начале ХХ столетия. Современное представление о нозологии ввели в дерматологию американские специалисты А. Бранстинг, В. Хокерман и П. O'Лейри в 1930 году.
Гангренозная пиодермия имеет и другие названия: геометрический фагеденизм, язвенный дерматит, серпингинирующая и гангренозно-язвенная вегетирующая пиодермия. Суть названий патологии связана с основным клиническим симптомом заболевания – прогрессирующей гнойно-некротической язвой. Фагеденическая форма заболевания встречается исключительно в тропических и субтропических странах обоих полушарий, там, где климат сырой и жаркий. Другие формы неэндемичны. Патологический процесс возникает в любом возрасте, пик заболеваемости приходится на 20-40 лет, дети болеют редко. Отмечается незначительное преобладание пациентов женского пола. Актуальность проблемы связана с серьёзными трофическими нарушениями, которые существенно снижают качество жизни пациентов.

Причины гангренозной пиодермии
Этиология и патогенез патологического процесса точно не установлены. В ряде случаев имеет значение наследственная предрасположенность. Гангренозная пиодермия в качестве симптомокомплекса входит в состав редких генетически детерминированных синдромов PAPA (гнойный артрит, гангренозная пиодермия, гангренозные акне), PASH (гангренозная пиодермия, акне, гнойный гидраденит) и PASS (гнойный артрит, гангренозная пиодермия, акне, гнойный гидраденит). Причиной перечисленных синдромов являются мутации гена PSTPI1/CD2BP1, расположенного в хромосоме 15q. Патологии наследуются по аутосомно-доминантному механизму.
Существует также иммунная теория развития гангренозной пиодермии. Согласно данной теории патологический процесс возникает на фоне изменённой чувствительности дермы к эндогенным и экзогенным агентам. Длительно существующие хронические соматические заболевания вызывают изменения клеточного и гуморального иммунитета за счёт нарушения нейроэндокринной регуляции, обменных процессов, трофики тканей. Начинается аберрантная иммунная реакция, в которой задействованы Т-лимфоциты и цитокины. Клетки иммунной системы Т-хелперы вырабатывают антитела – реагины, создающие основу сенсибилизации кожи. Одновременно Т-супрессоры пытаются подавить эти реакции, в результате развивается нестандартный иммунный ответ в виде некротической деструкции соединительной ткани.
Процесс формирования язвы при гангренозной пиодермии проходит три стадии. На стадии иммунных реакций происходит накопление специфических для определённого вида антигена антител. При этом иммунные лимфоциты и антитела класса Е из крови переходят в ткани кожи, сенсибилизируя её. На второй (патохимической) стадии заболевания повторное попадание чужеродного антигена вызывает активацию протеолитических ферментов клеток и тканей с нарушением их функций. Эпидермальные клетки начинают вырабатывать биологически активные вещества, провоцирующие воспаление. На третьей (патофизиологической) стадии возникает специфический ответ кожи на внедрение патологического антигена в виде дегрануляции клеток, разрушения сосудов, нарушения трофики и локальной деструкции ткани. Глубина деструкции зависит от количества патогенного антигена и степени устойчивости иммунной системы.
Классификация
В современной дерматологии принято различать несколько разновидностей патологического процесса. Выделяют:
Симптомы гангренозной пиодермии
Изменения на поверхности дермы дебютируют фурункулоподобными элементами с прозрачным или геморрагическим содержимым на фоне гиперемии. Поверхность кожи в местах высыпаний при гангренозной пиодермии инфильтрируется, затем некротизируется с формированием увеличивающейся вглубь и вширь язвы полициклической формы, достигающей размеров ладони взрослого человека. На пике своего развития очаг поражения представляет собой сплошную язвенную поверхность с валикообразными краями и оборками из остатков эпидермиса. Язва ливидного цвета с приподнятыми краями и широкой полосой гиперемии по периметру наполнена гноем, сгустками крови, остатками эпидермиса и бактериями, источает зловоние. Дно дефекта кожи бугристое, покрыто яркими грануляциями. Исход гангренозной пиодермии – реэпителизация с краёв дефекта в рубец.
Субъективное состояние нарушается мало, образование язвы сопровождается болезненностью, в период обострений появляются продромальные явления, присоединяются артралгии, миалгии. Гангренозная пиодермия начинается остро, но довольно быстро хронизируется, обладает волнообразным течением с частыми рецидивами. В 50% локализацией патологического процесса является голень, как правило, очаг единичный. Фагеденические язвы чаще множественные, возникают преимущественно на половых органах. Отличительной особенностью этой формы гангренозной пиодермии является быстрое формирование язвы, покрытой дифтероидным налётом серого цвета и плотно спаянной с подлежащими тканями. Валик вокруг дефекта кожи имеет заостренные края и чрезвычайно плотную консистенцию. Образование дефекта тканей сопровождается полиневритами и лимфангоитами.
Диагностика
Клинический диагноз ставится дерматологом на основании анамнеза, специфической симптоматики и консультаций узких специалистов, поскольку гангренозная пиодермия является междисциплинарным заболеванием. Гистология очага поражения не показательна, но в сложных случаях полезна. Выявляется тромбоз сосудов, гранулематозные инфильтраты, островки деструкции в эпидермисе и дерме. Дополнительно проводят электрофорез сывороточного белка, исключают микотическую природу язвы, берут кровь на RW. Дифференцируют гангренозную пиодермию с язвенным туберкулёзом кожи, третичным сифилисом, глубокими дерматомикозами, вегетирующей язвенной пиодермией, карбункулом, гранулематозом Вегенера, панникулитом, амёбиазом, бромодермой, гангреной, вегетирующей пузырчаткой, микобактериальной и клостридиальной инфекцией, трофическими нарушениями, пустулёзным псориазом.
Лечение гангренозной пиодермии
Терапию гангренозной пиодермии начинают с коррекции соматической патологии у профильных специалистов, поскольку кожный патологический процесс без этого плохо поддаётся терапии. Целью дерматологического лечения является снятие воспалительных проявлений, болезненных ощущений, восстановление кожных покровов. Для этого проводят курсы гормонотерапии и антибиотикотерапии. В тяжёлых случаях подключают цитостатики, иммуносупрессоры, калия иодид, внутривенно вводят иммуноглобулин. Показан плазмаферез. Наружно при гангренозной пиодермии очищают поверхность дефекта кожи с помощью вибрационно-турбулентных ванн, антисептических растворов. Применяют влажно-высыхающие повязки с растворами серебра, гормональные препараты. С учётом патергии стараются избегать хирургических манипуляций. Прогноз гангренозной пиодермии определяется первичной патологией, вызвавшей язву.
Пиодермии объединяют в себе гнойно-воспалительные кожные болезни, причиной которых является гноеродная микрофлора – пиококки, стафилококки и стрептококки. Примерно треть всех кожных заболеваний составляют различные пиодермии; первичные пиодермии возникают при поражении здоровой кожи, а вторичные являются осложнением заболеваний, при которых возможны повреждения кожи из-за зуда. Пиодермиями осложняется чесотка, экзема, а так же сахарный диабет и хроническая почечная недостаточность. Если пиодермия протекает с вовлечением глубоких слоев кожи, то после нее остаются стойкие рубцовые и пигментные изменения.
МКБ-10



Общие сведения
Пиодермии объединяют в себе гнойно-воспалительные кожные болезни, причиной которых является гноеродная микрофлора – пиококки, стафилококки и стрептококки. Примерно треть всех кожных заболеваний составляют различные пиодермии; первичные пиодермии возникают при поражении здоровой кожи, а вторичные являются осложнением заболеваний, при которых возможны повреждения кожи из-за зуда. Пиодермиями осложняется чесотка, экзема, а так же сахарный диабет и хроническая почечная недостаточность.
При неосложненных пиодермиях поражения кожи неглубокие и после выздоровления кожный покров полностью восстанавливается; если пиодермии принимают хроническое или затяжное течение, в процесс вовлекаются глубокие слои кожи, то остаются рубцы и пигментные пятна.
Причины пиодермий
На коже человека постоянно присутствует большое количество микроорганизмов, какие-то из них являются нормальной микрофлорой кожи, какие-то сапрофитной и транзиторной микрофлорой, которая при снижении защитных функций кожи способна вызывать пиодермии. В результате жизнедеятельности микроорганизмы выделяют ферменты, эндо- и экзотоксины, что и вызывает местную реакцию в виде пиодермий.
В патогенезе пиодермий важное место занимают условия труда и особенности кожи человека, возраст и состояние иммунной системы; снижение иммунологической реактивности человека и несоблюдение личной гигиены увеличивает вероятность возникновения пиодермий. В большинстве случаев пиодермии вызывает сапрофитная микрофлора, а потому пациенты не представляют опасности для окружающих.
Микротравмы, стрессовые ситуации, перегревание или переохлаждения являются факторами, которые снижают защитные функции кожи и повышают вероятность пиодермий; в группу риска попадают люди, страдающие сахарным диабетом, патологиями пищеварительной системы, нарушениями функции кроветворения и витаминного баланса, ожирение и истощение также угнетают местный иммунитет.
Кожа, склонная к выработке излишнего количества кожного сала, что случается при нарушениях ЦНС, наиболее уязвима для пиококков, так как изменение химического состава кожного сала снижает стерилизационные свойства кожи. Изменение гормонального фона или прием корткостероидов приводят к общим заболеваниям, которые являются предрасполагающими к пиодермиям.
Классификация пиодермий

Пиодермии классифицируют в зависимости от глубины и тяжести поражения, а так же в зависимости от возбудителя. Поверхностные пиодермии проявляющиеся остиофолликулитами, сикозами кожи – это чаще всего стафилодермии. Поверхностные стрептодермии и смешанные пиодермии клинически проявляются в виде импетиго вульгарного.
Глубокие стафилодермии проявляются в виде глубоких фолликулитов, гидраденитов, фурункулеза и карбункулеза. Глубокие воспаления кожи стрептококковой инфекцией заканчиваются язвенными поражениями кожи, протекающими по типу эктимы вульгарной. Язвенно-вегетатирующие хронические формы глубоких пиодермий чаще всего вызываются смешанной микрофлорой.
Лечение пиодермии

Лечением пиодермии занимается дерматолог. При пиодермиях волосы в очаге инфекции и вокруг него состригают, но не бреют, чтобы не допустить обсеменения патогенной микрофлорой участки здоровой кожи; если пиодермия носит генерализованный характер, то запрещаются водные процедуры, в том числе и мытье. Контакт с водой крайне не желателен, особенно в острой фазе заболевания.
Кожу вокруг пораженного участка обрабатывают спиртовыми растворами анилиновых красителей и дезинфектантами, хороший эффект оказывает салициловая кислота и раствор перманганата калия. Несмотря на то, что контакт с водой запрещен, ежедневно нужно тщательно мыть руки и обрабатывать ногти 2% раствором йода, чтобы предотвратить распространение инфекции, а также протирать здоровую кожу влажной губкой.
Питание в период лечения должно быть сбалансированным, лучше перейти на молочно-растительную диету, полностью исключить из меню экстрактивные вещества и алкоголь, ограничить употребление соли и простых углеводов. Если пациент ослаблен, имеет сопутствующие заболевания или пиодермия принимает затяжной или хронический характер течения, при присоединении симптомов интоксикации, медикаментозное лечение пиодермии целесообразно проводить антибактериальными препаратами. Перед назначением антибиотика проводят бакпосев отделяемого или соскоба, определяют возбудителя и его чувствительность к препаратам. Антибиотики пенициллинового ряда практически не назначают из-за их низкой эффективности, макролиды и тетрациклины дают хороший терапевтический эффект, но эритромицин и тетрациклин нежелательно применять для лечения детей и беременных.
Лечение комбинированными антибактериальными препаратами и цефалоспоринами (цефотаксим и др) назначают при инфицировании смешанной микрофлорой, так как эти препараты обладают широким спектром действия и устойчивы к изменчивости бактерий. Курс и дозировка препаратов назначаются индивидуально, исходя из тяжести течения пиодермий, обычно прием антибиотиков не должен быть меньше недели. Сульфаниламидные препараты менее эффективны при пиодермиях, но если у пациента непереносимость антибиотиков, то назначают сульфаметоксазол+триметоприм, сульфомонометоксин в нужных дозировках.
Активная специфическая иммунотерапия в сочетании с антибиотикотерапией и местным лечением дает хорошие результаты, особенно при хронических и вялотекущих процессах. Подкожное введение анатоксинов, специфических антигенов, стафилопротектинов два раза в неделю проводят в условиях поликлиники или в стационаре, если пациент находится на госпитальном лечении.
Для стимуляции неспецифического иммунитета прибегают к аутогемотрансфузии, переливанию компонентов крови, ультрафиолетовому облучению крови (УФОК); такие препараты как метилурацил, настойка лимонника и экстракт элеутерококка тоже стимулируют иммунную систему. Если имеются иммунные нарушения, то лечение пиодермий целесообразно проводить с назначением иммуностимуляторов группы препаратов тимуса; препаратов гамма-глобулинов и стимуляторов выработки интерферона. Витаминотерапия показана при всех видах пиодермий.
Профилактика пиодермий
Профилактика как для лиц, у которых нет в анамнезе гнойничковых заболеваний, так и для лиц с рецидивами пиодермий в анамнезе, заключается в соблюдении правил личной гигиены, в организации предупреждающих мер в быту и на производстве. Соблюдение санитарно-технических и санитарно-гигиенических норм на производстве существенно снижают заболеваемость пиодермиями в отдельно взятом учреждении. Кроме того своевременная обработка травм и микротравм позволяет исключить дальнейшее инфицирование ран и развитие пиодермий.
Регулярные профилактические медицинские осмотры с целью выявления хронических заболеваний пищеварительной системы, ЛОР-органов позволяют назначить лечение и не допустить развитие вторичных пиодермий. Для больных сахарным диабетом профилактика пиодермий заключается в более тщательном уходе за кожей, в своевременном ее увлажнении, чтобы не допускать мацерации и образования микротравм, так как при сахарном диабете даже небольшая царапина зачастую становится причиной обширных и глубоких пиодермий.
Брок впервые описал пиодермию в 1916 году (1). В 1930 году Бранстинг, Гекерман и О'Лири ввели термин "пиодермия" в клинике Майо (Рочестер, штат Миннесота) и первоначально считали, что это заболевание инфекционной этиологии (1).
Сейчас, более 80 лет спустя, точная этиология неизвестна, но она не считается инфекционной и остается проблемой в плане диагностики и лечения. Само название добавляет путаницы, потому что заболевание не является ни гангренозным, ни инфекционным.
Очень немногие специалисты встречаются с данным заболеванием регулярно, и все же многие столкнутся по крайней мере с 1 случаем в какой-то момент своей профессиональной деятельности.
Постановка диагноза является решающим первым шагом, потому что, если заболевание имеется, но не распознано, результаты лечения могут быть неблагоприятными. В случаях пиодермии обычные методы лечения, такие как санация, могут ускорить патологический процесс и создать порочный круг, что приведёт к увеличению размера очагов.
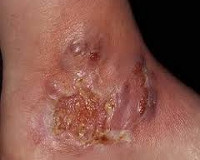
Например, в случае 1 показан пациент с послеоперационной пиодермией, возникшей за ухом, у которого было несколько операций на ухе, носу и глотке в университетской больнице. Даже после того, как очаг явно прогрессировал после каждого вмешательства, пиодермия не была диагностирована, как видно из случая 1 (рисунки 1A-1C).
Диагноз
История. Наиболее распространенной историей заболевания для пациентов с пиодермией является небольшое повреждение, которое, как правило, является укусом или царапиной, которые быстро увеличились в размерах, или после медицинской процедуры, такой как хирургическое вмешательство, или даже после такой, казалось бы, безопасной манипуляции, как пункционная биопсия, как в случае 2 (рисунок 2) и случае 3 (рисунок 3A-3D).
Популяционные особенности пациентов. У некоторых пациентов с пиодермией обнаруживаются воспалительные заболевания, такие как воспалительное заболевание кишечника ( IBD ) (т. е. болезнь Крона или язвенный колит) или другие заболевания, такие как волчанка, лейкемия или заболевания печени.
Процент пациентов с пиодермией, у которых также есть IBD , первоначально указывался на уровне около 50%, но в последующих обзорах отмечалось меньшее количество пациентов с пиодермией с сопутствующим IBD (2).
Было дано несколько объяснений этому очевидному увеличению доли изолированной пиодермии с течением времени, например, многие из первоначальных серий наблюдений были из специализированных клиник, специализирующихся на IBD , или в связи с тем, что клиницисты со временем стали более достоверно диагностировать пиодермию (2).
Клиника. Высыпания при пиодермии могут возникать de novo или после незначительной травмы, укуса или хирургического вмешательства (3). Перистомальная пиодермия по сути является послеоперационным осложнением, которое было описано в 1984 году (4).
Перистомальная пиодермия особенно часто встречается у пациентов с IBD после операции и формирования стомы. В то время как перистомальная пиодермия может быть легче диагностирована из-за ее расположения, она может быть неправильно диагностирована из-за раздражения перевязочным материалом или присоединения инфекции.
Неперистомальная пиодермия может присутствовать на любом участке тела, и случай 4 (рисунки 4A-4C) показывает случай пиодермии, проявляющейся на руках.
Хотя существуют и другие, как правило, травматические или инфекционные причины высыпаний на руках, всякий раз, когда на руках появляются необычные высыпания, особенно если имеется несколько видов элементов, это должно требовать дифференцировки с пиодермией.
Проявления и результаты культурального исследования высыпаний. Классическим признаком пиодермии является плотной консистенции язва с голубовато-фиолетовыми краями (рисунки 4A, 4C). Определенного гистологического признака нет, но гистологические изменения, подтверждающие диагноз, - это нейтрофильная инфильтрация дермы и эпидермиса.
Несмотря на то, что в ранах часто имеются значительные количества фрагментов лейкоцитов, которые выглядят как гной в местах подрыва краёв язвы, культуральное исследование чаще всего не выявляло роста патогенной флоры по данным автора.
Положительные культуры, безусловно, не исключают пиодермию; однако очаги пиодермии могут быть колонизированы или инфицированы и иметь положительные культуры, особенно если они длительное время не заживали.
Роль биопсии. Биопсия используется при подозрении на пиодермию, чтобы исключить другие причины образования язв. Weenig и соавт. (5) описали частоту ошибочных диагнозов около 10% в своей серии наблюдений в клинике Майо и по данным обзора литературы (5).
Они пришли к выводу, что биопсия всегда оправдана, потому что лечение пиодермии часто заставляет пациента проходить курс терапии системными стероидами. Они классифицировали случаи других заболеваний, которые были ошибочно диагностированы как пиодермия, по следующим группам: сосудистые поражения, васкулиты, злокачественный процесс, первичная инфекция, лекарственное или экзогенное повреждение тканей и другие воспалительные заболевания.
Уиниг и соавторы (5) также отметили, что язвы в результате венозного застоя являются наиболее распространенными язвами нижних конечностей, но обычно не похожи на пиодермию.
Язвы в результате венозного застоя, как правило, не столь болезненны и сопровождаются отложением гемосидерина. Язвы при васкулите бывает трудно отличить от пиодермии, и они также часто реагируют на стероиды. Кроме того, они отметили, что антифосфолипидный синдром является “весьма проблематичным симулятором пиодермии” из-за его клиники и реакции на стероиды, но волчаночный антикоагулянт почти всегда был положительным при антифосфолипидном синдроме и язвах.
Случай 5. В этом случае представлен пациент с васкулитом вследствие антифосфолипидного синдрома, который может быть схож с проявлениями пиодермии. Проявления болезненной язвы несколько схожа с пиодермией, но пурпура была более распространена (по крайней мере, во время обострения васкулита), что обычно наблюдается при пиодермии.
Дозу преднизолона пришлось увеличить, когда произошло обострение васкулита, и был отмечен периферический фиолетовый ореол. Васкулит похож на пиодермию по своей реакции на стероиды, а также по потенциальному эффекту использования человеческого аллотрансплантата (рисунки 5A-5E).
Роль биопсии. Клиническое обследование, а не биопсия позволяет поставить диагноз пиодермии, поэтому на практике врачи не считают биопсию обязательной при диагностике и лечении каждого случая пиодермии, но, безусловно, ее следует применять шире.
Решения о том, когда проводить биопсию, принимаются в каждом конкретном случае. В таблице 1 перечислены факторы, учитываемые при принятии решения о проведении биопсии (таблица 1).
Одна из причин, по которой клиницисты могут не решаться проводить биопсию поражений, относящихся к пиодермии, заключается в том, чтобы избежать возможности усугубления патологического процесса.
По опыту автора, этого риска можно избежать, если пациент будет принимать системные стероиды, начиная с дня проведения биопсии и продолжая до тех пор, пока не будет исключена пиодермия.
Медикаментозное лечение пиодермии
Когда следует госпитализировать? Пациентам с быстро прогрессирующими поражениями и/или обширными поражениями или при отсутствии эффекта от амбулаторного лечения следует рассмотреть возможность госпитализации.
Госпитализация рекомендована для обеспечения тщательного наблюдения, внутривенного введения антибиотиков, лечения высыпаний и проявлений боли, а также многопрофильной помощи.
Затруднения в диагнозе и лечении. Поскольку пиодермия может быть диагностирована методом исключения, существуют трудности в диагностике, что требует тщательного наблюдения и интенсивной терапии. В течение этого времени диагноз пиодермии будет устанавливаться на основе клинической картины, результатах стероидной терапии и полученных результатах культурального исследования и/или биопсии.
Может рассматриваться наличие или отсутствие системного заболевания, и также назначаются соответствующие тестирования. Как подчеркивают Гавлик и соавт. (6), системные стероиды следует начинать, как только диагноз пиодермии считается вероятным, также за состоянием пациента необходимо внимательно наблюдать.
Во время первоначального лечения необходимо внимательно наблюдать за реакцией пациента на стероиды, пока не будут получены результаты биопсии, посевов и/или других тестов (6).
Этот критический период неопределенности особенно неудобен для клиницистов, потому что атипичные и некротизирующие инфекции могут иметь сходство с пиодермией, и стероиды, подходящие для начального лечения пиодермии, могут усугубить эти состояния.
Местными признаками того, что процесс действительно является пиодермией, реагирующей на стероиды, будет уменьшение боли, отсутствие новых высыпаний и уменьшение ореолов вокруг существующих поражений в течение 24-48 часов.
Если местные симптомы сохраняются, необходима оценка общей картины, включая жизненно важные показатели и результаты лабораторных исследований; если это выявляет ухудшение клинической ситуации, стероиды необходимо отменить или уменьшить дозу.
Дозировка системных стероидов. Протокол лечения автора статьи состоял в том, чтобы начинать лечение большинства госпитализированных тяжелых потенциальных случаев пиодермии с приема 100 мг (ежедневно в разовой дозе) внутривенного метилпреднизолона в течение нескольких дней, затем снизить дозу до 60-80 мг/сут в течение нескольких дней, прежде чем перейти на пероральный преднизолон в дозе 40-60 мг/сут и уменьшать дозу по мере переносимости. Эта дозировка стероидов аналогична рекомендациям других отчетов (7, 8).
Автор предпочитает назначать начальные дозы внутривенно, а не перорально для госпитализированных пациентов, главным образом для ускорения поступления и избежания любых нарушений всасывания, поскольку у некоторых пациентов могут быть IBD . И наоборот, для менее тяжелых проявлений, которые лечатся амбулаторно, целесообразно пероральное введение.
Обзор случаев и данные таблицы 5 в серии наблюдений Холта (8) особенно интересны: для достижения ремиссии чаще всего требовалось 60-100 мг/сут, и дозы чуть ниже этого уровня во многих случаях были неэффективными.
Следовательно, важно подчеркнуть, что лечение пиодермии не должно быть ограниченным — дозировка стероидов должна быть адекватной (автор предлагает 80-100 мг/сут), потому что при отсутствии хорошего клинического ответа более вероятно, что это не пиодермия, а пациент был недостаточно обследован.
Что касается процесса снижения дозы, то в практике автора и других исследователей было отмечено, что снижение более чем на 10-20 мг/сут каждую неделю может привести к обострениям или рецидивам (2, 3).
Также рекомендуется лечение обострений преднизолоном или метилпреднизолоном в дозе 1-2 мг/кг/сут. Для пациентов со средней массой тела или менее дозы будут сходны с дозировками, указанными выше (9, 10).
Большинство источников рекомендуют вводить суточную дозу в виде 1 дозы, но также было описано разделение доз (9). Неизвестно, полезна ли корректировка веса, но для пациентов, со значительно превышающей или ниже среднего массой тела, представляется разумным рассмотреть возможность дозирования в зависимости от веса.
Джонсон и Лазарус (11) описали другой режим, называемый пульс-терапией, который они определили, как “использование однократных или многократных ежедневных вливаний супрафармакологических доз метилпреднизолона”.
Опыт этого автора и многих других, начиная с исследования Джонсона и Лазаруса, показал, что в большинстве случаев метилпреднизолон или преднизолон в дозе 100-120 мг в день вызывают ремиссию пиодермии (2, 8). В практике автора клиницисты называют суточные дозы внутривенного метилпреднизолона в диапазоне 100 мг/сут “мини-пульс-терапией”.
Медикаментозное лечение хронической пиодермии
Большинство пациентов в практике автора в конечном итоге были полностью избавлены от необходимости применять стероиды, но примерно у половины из них были рецидивы, которые требовали повторного введения или увеличения доз стероидов при сих снижении, по крайней мере, в течение короткого периода времени (случай 3, рисунки 3A-3D).
В других сериях наблюдений описаны рецидивы примерно в одной трети случаев (9). Для пациентов, которые не могут прекратить прием стероидов из-за развития рецидива, могут быть рассмотрены стероидосберегающие средства, такие как циклоспорин, такролимус, инфликсимаб, дапсон и сульфасалазин, среди прочих (7, 9, 10, 12-16).
Информативная сводная таблица с дозами системных терапевтических средств для лечения пиодермии представлена в обзорах Каллена и Джексона (12), а также Воллина (15).
Направление к ревматологу или другому специалисту, имеющему опыт применения иммуносупрессивной терапии, может быть показано пациентам, которых проблематично вести без стероидов.
Местное стероидное лечение очагов пиодермии
Небольшие очаги пиодермии, которые быстро не прогрессируют, могут реагировать на местные стероиды, и автор с некоторым успехом использовал этот подход для перистомальных локализаций (14). Внутриочаговое введение стероидов также было описано, но у автора нет опыта использования этой техники (7).
Перевязка и хирургическое лечение. Мягкие повязки и предотвращение чрезмерных травм и раздражений лучше всего подходят для ухода за очагами пиодермии. Были проведены исследования по использованию многих типов повязок, в том числе с использованием пены, гидроколлоидов и сульфадиазина серебра (17).
Были достигнуты особенно хорошие результаты при использовании пенных повязок, содержащих анилиновые красители, метиленовый синий и кристаллический фиолетовый (пена Hydrofera Blue, Hollister Wound Care, Либертивилл, Иллинойс), и об этом также сообщалось в литературе (18). Возможно, анилиновые красители подавляют воспаление, хотя это не доказано.
Хирургическое лечение пиодермии. При обширных поражениях с некрозом или без него может потребоваться хирургическое лечение для обработки и/или достижения закрытия дефекта.
Обзор более старой литературы может легко создать впечатление, что диагноз пиодермии абсолютно исключает хирургическое вмешательство. Тей и его коллеги в работе “Острая гангренозная пиодермия не требует хирургического лечения” (19) не оставили сомнений в том, как они относились к оперативному лечению пиодермии. Они описали, как регулярная обработка поражения на пальце ухудшила ситуацию, но это был случай нераспознанной пиодермии, и стероидное лечение не применялось (19).
Аналогичным образом, Хикман и Лазарус (2) заявили, что из-за патогенности “попытки пересадки чрезвычайно опасны, поскольку трансплантаты редко приживаются, и на донорских участках могут развиться новые язвы. Ампутации следует избегать, так как в культе может возникнуть гангренозная пиодермия” (2).
Как показывает опыт автора и более поздние данные литературы, хотя всегда следует помнить о возможной реакции патергии, на самом деле это не исключает операции по удалению или пересадке кожи, если пациент принимает стероиды.
В настоящее время известны многочисленные примеры хирургических вмешательств, приводящих к пиодермии (6, 20, 21).
В статье Гавлика 1998 года “Гангренозная пиодермия молочной железы: последовательная пересадка” представлен случай пиодермии в молочной железе 15-летней девочки, которой была проведена первоначальная аллотрансплантация кожи от донора человека для лечения боли и очагов с последующей аутотрансплантацией (6).
Они отметили, что в некоторых случаях аутотрансплантация даст гораздо лучший косметический результат, чем заживление только вторичным натяжением. Этот опыт предшествовал аналогичному результату в случае 6 настоящей статьи (рисунок 6).
Аллотрансплантат используется не только для контроля боли и стабилизации раневого процесса, но, если он успешно применён, это показатель того, что аутотрансплантация сможет быть эффективной.
Одного аллотрансплантата может быть достаточно, чтобы помочь закрыть небольшие очаги, но поскольку он обычно в конечном итоге отторгается, аутотрансплантация остается наиболее функциональным и косметически приемлемым вариантом для больших ран.
Размер ран после очистки будет определять, как закрыть дефект: относительно небольшие раны могут эпителизироваться; раны среднего размера хорошо сочетаются с человеческим аллотрансплантатом; и очень большие раны могут потребовать аутотрансплантации.
Случай 6 был крайним случаем, который демонстрирует несколько важных хирургических принципов ведения ран. Этому пациенту потребовалось несколько операций, которые были благополучно завершены без реакции патергии.
Образовавшийся в результате большой дефект обнажил кость и сухожилия, и первоначально аллотрансплантация использовалась для определения того, будет ли в ране успешно функционировать трансплантат, тем самым избегая донорского участка, если взятая для пересадки кожа будет отторгнута.
Как только аллотрансплантат был взят, пациента направили в операционную за взятием аутотрансплантата из области бедра, который в конечном итоге закрыл большую часть раны, и не было никаких проблем с заживлением большого донорского участка.
Вывод
Диагностика пиодермии имеет первостепенное значение. Госпитализация эффективна в случаях тяжёлых поражений. Биопсия не поставит диагноз, но может быть использована для исключения других причин, и её выполнение следует проводить при применении стероидных препаратов, чтобы предотвратить патергию, когда возможно наличие пиодермии. Когда вероятно наличие пиодермии, врачи должны быть готовы назначить стероиды и выдержать критический период.
Afsaneh A., French L., Davis M, Brassard A, Kirsner R. Pyoderma Gangrenosum: An Update on Pathophysiology, Diagnosis and Treatment.
Гангренозная пиодермия: обновление по патофизиологии, диагностике и лечению
Алави А , Университет Торонто (Канада), Ларс Э., Университет Цюриха (Швейцария), Дэвис М., клиника Майо в Рочестере (США), Брассард А., Университет Альберты (Канада), Кирснер Р., Университет Майами (США)
Гангренозная пиодермия: обновление по патофизиологии, диагностике и лечению
Патофизиология
Патофизиология гангренозной пиодермии остается непонятной. Она представляет собой сложную реакцию с несколькими путями развития или сочетанием различных признаков, которые создают гетерогенное представление о болезни. Сообщалось о дисрегуляции врожденной иммунной системы, а также об аномальных хемотаксисе, миграции нейтрофилов, фагоцитозе, бактерицидной способности и аномальной функции нейтрофилов у пациентов с гангренозной пиодермией. Факторы, способствующие клиническим проявлениям гангренозной пиодермии, включают дисфункцию нейтрофилов, генетические мутации и аномальное воспаление.
Нейтрофильная дисфункции
Гангренозная пиодермия считается одним из редких нейтрофильных дерматозов, типичным для асептической нейтрофильной инфильтрации и системного воспаления. Она также связана с другими нейтрофильными или воспалительными расстройствами, такими как воспалительные заболевания кишечника, ревматоидный артрит, серонегативный артрит, аутоиммунный гепатит и гематологические расстройства, включая парапротеинемию, моноклональную гаммапатию, обычно связанную с секрецией IgA и нейтрофильные злокачественные новообразования, такие как острый миелолейкоз. Гангренозная пиодермия была описана при нейтропении и при дефиците адгезии лейкоцитов 1 типа.
Генетическое влияние
Существуют определенные генетические сходства между воспалительным заболеванием кишечника и гангренозной пиодермией. При обоих заболеваниях наблюдаются повышенные уровни медиаторов миграции нейтрофилов (LociIL-8RA), белка, содержащего PR-домен, и тканевого ингибитора металлопротеиназы 3, которые связаны с развитием аутоиммунных заболеваний. Инфламасомы являются полипротеиновыми олигомерами, часто экспрессируемыми в миелоидных клетках и кератиноцитах. Они могут быть вовлечены в процессы активации полиморфноядерных нейтрофилов (PMN), как показано в случаях, связанных с мутацией гена PSTPI1/СВ2ВР1, расположенного на хромосоме 15q. Значение генетической предрасположенности к гангренозной пиодермии лучше всего иллюстрируется тем, что гангренозная пиодермия в качестве симптомокомплекса входит в состав редких генетически детерминированных синдромов PAPA (гнойный артрит, гангренозная пиодермия, гангренозные акне), PASH (гангренозная пиодермия, акне, гнойный гидраденит) и PASS (гнойный артрит, гангренозная пиодермия, акне, гнойный гидраденит). Причиной перечисленных синдромов являются мутации гена PSTPI1/CD2BP1, расположенного в хромосоме 15q. Патологии наследуются по аутосомно-доминантному механизму. Мутированный ген PSTPIP1 приводит к множеству эффектов, таких как снижение ингибирования воспаления с активацией каспазы 1, увеличение продукции IL-1B и IL-18, что приводит к нейтрофильной инфильтрации, связанной с вышеупомянутыми синдромами.
Воспаление
При гангренозной пиодермии были обнаружены повышенные уровни воспалительных медиаторов, что указывает на патологический воспалительный процесс. Гистологические особенности включают зрелые, нормальные нейтрофилы в дерме, но различные исследования показали, что они функционально ненормальны, в то время как у некоторых пациентов они показали повышенную экспрессию интегрина или нарушение его регуляции. Сообщается, что вовлечение Т-клеток и макрофагов происходит на раневых краях язв гангренозной пиодермии, где обнаруживаются повышенные уровни CD3 + Т-клеток, а также CD163 + макрофагов. IL-8, также известный как хемотаксический фактор нейтрофилов, обнаружен в раневом слое. Таким образом, Т-клетки и макрофаги, вероятно, играют ключевую роль в патогенезе болезни через аномальную передачу сигналов цитокинам. Кроме того, Caproni и др. обнаружено повышение Th - 17 в поражениях гангренозной пиодермии и предложены анти-IL-17 в качестве альтернативного лечения. Существует также отчетливая аномалия в экспрессии хемокинов периферической крови, поддерживающих поляризацию лимфоцитов. Экспрессия провоспалительных цитокинов, IL1β и его рецептор, а также IL-8, Fas, FasL, CD40, CD40L, CXCL 1/2/3, CXCL 16 были значительно увеличены при гангренозной пиодермии. IL-23, цитокин, который играет важную роль в стимулировании IL-17-опосредованного нейтрофильного воспаления, в последнее время, как было показано, повышается в зависимости от экспрессии гена и уровня белка в поражениях гангренозной пиодермии. Повышенные уровни IL-23 обнаруживаются при воспалительном заболевании кишечника и псориазе, что наблюдается и при рефрактерной гангренозной пиодермии.
Клинические проявления
Ассоциированные заболевания и внекожные проявления
Дифференциальная диагностика
Никаких специфических серологических маркеров для подтверждения гангренозной пиодермии не существует, а гистопатология неспецифична и варьирует в зависимости от подтипа и стадии гангренозной пиодермии. Поэтому в дифференциальном диагнозе гангренозной пиодермии существует множество недостатков, что объясняет сложность ее диагностики. При дифдиагностике гангренозной пиодермии важно исключение всех возможных диагнозов. Ahronowitz и др. считают, что минимальная оценка должна включать полный анамнез, физикальное обследование, биопсию кожи (биопсия кожи должна включать активную границу язвы и проникать глубоко в подкожную ткань). Рекомендуется также культуральное исследование тканей для исключения бактериальных, атипичных микобактериальных и глубоких грибковых инфекций, однако общепринятого диагностического критерия для гангренозной пиодермии не существует. В недавнем исследовании, проведенном в Германии, эритематозная активная граница, быстрое распространение границ поражения и исключение других диагнозов были наиболее важными диагностическими ориентирами для гангренозной пиодермии.
Предлагаемые диагностические критерии
Надежные диагностические критерии для гангренозной пиодермии все еще отсутствуют. Используя опросник у 57 пациентов с гангренозной пиодермией, исследователи из Германии предложили несколько потенциальных диагностических критериев, таких как гиперемия по краям очагов, быстрое прогрессирование, исключение соответствующих дифференциальных диагнозов и быстрое реагирование на иммунодепрессивное лечение. Гангренозная пиодермия представляет собой нейтрофильный дерматоз, характеризующийся нейтрофильной дисфункцией, генетическим влиянием и сильной связью с другими воспалительными или неопластическими заболеваниями, прежде всего с воспалительным заболеванием кишечника, артритом и гематологическими расстройствами. В основе патогенеза гангренозной пиодермии, воспалительного заболевания кишечника и псориаза могут лежать общие провоспалительные пути и / или молекулы.
Лечение
Гангренозная пиодермия является сложной задачей как для диагностики, так и для лечения, а лечение направлено на уменьшение связанного с ним воспаления, которое приводит к изъязвлению. Выбор лечения зависит от множества факторов, в том числе от локализации, количества, размера очагов, наличия внекожных проявлений, наличия ассоциированных заболеваний, стоимости и побочных эффектов лечения, а также сопутствующих заболеваний и предпочтений пациента. Выявление и лечение основных заболеваний, таких как воспалительное заболевание кишечника или артрит, является важным аспектом в лечении, хотя прямая связь между серьезностью связанных заболеваний и гангренозной пиодермией является предметом обсуждения. В большинстве случаев гангренозная пиодермия ограничена 1-3 очагами поражения с вовлечением менее чем 5% поверхности тела. Оптимальное лечение может включать в себя клинически значимые для гангренозной пиодермии аспекты: исключение триггеров, адекватное лечение раны, адекватное купирование боли и топическую, системную и таргетную иммуномодулирующую терапию. Терапия первой линии включает системные кортикостероиды в высоких дозах, в то время как ингибиторы циклоспорина и TNF оказались полезными в качестве терапии второй и третьей линии, но не всегда успешны. Для достижения контроля над ограниченным заболеванием, могут быть достаточными топическая и пероральная терапия без необходимости системной терапии. Уход за ранами является неотъемлемой частью лечения. Для содействия заживлению необходимы повязки и контроль отечности конечностей при компрессионной терапии (при отсутствии значительной артериальной недостаточности). Кроме того, необходим контроль за болевым синдромом. Язвы при гангренозной пиодермии могут быть одними из наиболее болезненных язв, которые лечат дерматологи. Неадекватное лечение боли может привести к стрессу, тревоге и депрессии, что может отрицательно сказаться на качестве жизни и замедляет или препятствует заживлению. Для устранения боли могут быть назначены топические анальгетики, а также системные ацетаминофен, нестероидные противовоспалительные препараты (НПВП) и опиаты. Основные принципы надлежащего ухода за раной включают адекватное, но щадящее очищение с использованием антибактериальных средств и поддержание оптимальной влажности в ране (не слишком сухой или слишком влажной). Очистка раны является частью стандартного ухода, но консервативная обработка (ферментативная, аутолитическая или хирургическая) для удаления нежизнеспособных тканей, в то время как она может уменьшить инфицированность и запах, должна выполняться осторожно. Следует избегать агрессивной хирургической обработки и использования сильных адгезивов.
Топические и дерматологические процедуры
Системные методы лечения
Используются системные кортикостероиды, которые считаются терапией первой линии при прогрессирующей, тяжелой или обезображивающей болезни либо в виде перорального преднизона (0,5-1 мг / кг / день), либо внутривенной пульс-терапии кортикостероидами (1000 мг / сут). Эффект можно увидеть в течение 2-3 дней. Неблагоприятные последствия, возникающие при длительном применении кортикостероидов (в том числе остеопороз, увеличение веса, глаукома, катаракта, гипергликемия, диабет, синдром Кушинга, иммуносупрессия, надпочечниковая недостаточность, кортикостероидный психоз и др.) должны контролироваться и часто ограничивают длительное использование системных кортикостероидов.
Циклоспорин (2,5-5 мг / кг / день) часто используется в качестве лечения второй линии и может быть эффективным, особенно в случаях, устойчивых к кортикостероидам. Ormerod и др. провели исследование, сравнивающее пероральный преднизолон 0,75 мг / кг / день с циклоспорином 4 мг / кг / день, до максимальной дозы 75 и 400 мг / день, соответственно, у 121 пациента с гангренозной пиодермией. Обе группы показали тот же результат: 47% пациентов как в группе циклоспорина, так и в группе преднизолона, достигли полной эпителизации очагов. Однако рецидив наблюдался у 8 (30%) пациентов, пролеченных циклоспорином и у 7 (28%) получавших преднизолон.
В 1997 году Reynoso-von Drat пролечил 9 пациентов с гангренозной пиодермией внутривенным циклофосфамидом из расчета 500 мг / м 2 площади тела 1 раз в месяц до 6 доз на курс или до 3 доз при заживлении язв или при отсутствии эффекта. 7 пациентов достигли полной ремиссии. Сообщалось также об успешном использовании других системных иммунодепрессантов, включая метотрексат, микофенолят-мофетил, сульфасалазин и азатиоприн. Однако, их эффективность не доказана в контролируемых испытаниях. Использование таргетных методов лечения, таких как биологические препараты, расширило терапевтические возможности при гангренозной пиодермии. В этом обзоре мы фокусируемся на ценности биологических препаратов и лучших доступных результатах, подтверждающих их эффективность при гангренозной пиодермия.
Роль биологических препаратов
Таргетная терапия повышает эффективность лечения многих дерматозов, включая псориаз и суппуративный гидраденит. Сообщается, что гангренозная пиодермия улучшается при использовании биологической терапии, особенно препаратов - антагонистов TNF и IL-1β. Активация врожденной иммунной системы играет существенную роль в патогенезе гангренозной пиодермии. Высокие уровни IL-8 и TNFα связаны с нейтрофильной инфильтрацией, характерной для гангренозной пиодермии. Недавние исследования профиля экспрессии цитокинов в пораженной коже при гангренозной пиодермии продемонстрировали суперэкспрессию IL-1β, потенциального провоспалительного цитокина. Кроме того, несколько синдромов, связанных с гангренозной пиодермией, помогли пролить свет на патогенез болезни. При синдроме PAPA мутации в гене PSTPIP1 приводят к активации комплекса цитозольного мультимерного воспалительного белка, и последующему созреванию воспалительных цитокинов IL-1β и IL-18. Ряд малых серий описывает использование антагонистов ФНО при гангренозной пиодермии (этанерцепт, адалимумаб, инфликсимаб). Единственное рандомизированное контролируемое исследование, в котором применялся инфликсимаб, продемонстрировало преимущества, но этого уровня доказательств не существует для других антагонистов ФНО
Антагонисты фактора некроза опухоли (ФНО)
За исключением этанерцепта гангренозная пиодермия часто улучшается при лечении антагонистами ФНО, которые эффективны при лечении сопутствующего воспалительного заболевания кишечника. Наиболее изученными антагонистами ФНО являются:
Инфликсимаб - химерное моноклональное антитело против ФНО, оказывает влияние на аневрические регуляторные Т-клетки, восстанавливая их способность ингибировать продукцию цитокинов.В РКИ (рандомизированное контролируемое исследование) под руководством Бруклина и др. 30 пациентов с гангренозной пиодермией были рандомизированы для приема инфликсимаба или плацебо. В группе инфликсимаба наблюдалось уменьшение размера язв, сокращение сроков заживления ран, улучшение качества жизни и ремиссия болезни по сравнению с плацебо. Положительный клинический ответ на инфликсимаб в дозе 5 мг / кг, вводимый внутривенно в течение 6 недель, отмечался у 69% пациентов против 21% в контрольной группе. Хотя на сегодняшний день это единственное РКИ гангренозной пиодермии, его размер выборки невелик, и результаты этого небольшого РКИ должны быть подтверждены в более крупных испытаниях. Результаты небольших ретроспективных исследований и отчетов о случаях показали благоприятные результаты.
Адалимумаб. В нескольких исследованиях изучалось лечение в общей сложности 9 пациентов с гангренозной пиодермией с использованием адалимумаба. Все пациенты положительно ответили на терапию уменьшением размеров язв, а 5 пациентов достигли полной ремиссии. Patel и др. предположили, что адалимумаб является оптимальным лечением терапевтически стойкой гангренозной пиодермии. Эти данные свидетельствуют о том, что адалимумаб (40 мг каждые 2 недели) может быть полезен для лечения гангренозной пиодермии, поскольку использование при других заболеваниях указывает на его хороший профиль безопасности. Количество случаев ограничено, и требуется больше клинических доказательств.
Этанерцепт - может быть полезен при лечении рефрактерных случаев гангренозной пиодермии но, по-видимому, обладает меньшей эффективностью по сравнению с инфликсимабом в лечении гангренозной пиодермии, протекающей на фоне активной болезни Крона. Сообщалось об 11 пациентах с гангренозной пиодермией, получавших этанерцепт, из которых полной ремиссии достигли 8 пациентов.
Анти-интерлейкин (IL) -12 / IL23.
Устекинумаб - является единственным ингибитором IL-23, который, как сообщается, улучшает гангренозную пиодермию. 2 пациента с гангренозной пиодермией успешно лечились с помощью устекинумаба. Однако, необходимо больше исследований для определения эффективности этого агента при лечении гангренозной пиодермии.
Антагонисты IL-1. Роль антагонистов IL-1 в управлении гангренозной пиодермии является многообещающей, но ограничена нехваткой доказательств.
Канакинумаб (Canakinumab) - является человеческим анти-IL-1β моноклональным антителом (без перекрестной реактивности против других членов семейства IL-1). Он одобрен для использования в связанных с криопирином периодических синдромах (CAPS) и также используется для лечения аутовоспалительных синдромов, связанных с повышенным уровнем каспазы-1. В недавнем исследовании Kolios и др. наблюдали 5 пациентов с рефрактерной к кортикостероидам гангренозной пиодермией, которым Канакинумаб вводился подкожно в разовой дозе 150 мг в 1 и 14 дни и в дозе 150-300 мг на 28 день. У 4 из 5 пациентов наблюдалось уменьшение размеров раны, улучшение Врачебной глобальной оценки (PGA) и улучшение индекса качества жизни (DLQI).
Анакинра - является рекомбинантной, негликозилированной формой антагониста рецептора IL-1, используемого для лечения ревматоидного артрита и криопиринопатий. Опубликованы 3 исследования пациентов с гангренозной пиодермией с или без ассоциированного заболевания, получавших лечение анакинрой. В своем обзоре Липскер и Ленорманд предположили, что Анакинра может быть менее эффективной при лечении гангренозной пиодермии, чем при лечении ревматоидного артрита или криопиринопатий.
Гевокизумаб. В качестве антагониста IL-1β гевокизумаб показал эффективность у пациентов с болезнью Бехчета, пустулезным псориазом и синдромом PAPA, но не сообщалось о лечении гангренозной пиодермии или гангренозной пиодермии, связанной с другими воспалительными состояниями, такими как воспалительное заболевание кишечника. Сообщалось о доказательном исследовании у 6 пациентов с гангренозной пиодермией, из которых значительное улучшение на 28 день было отмечено у 5 пациентов.
Другие биологические препараты:
Тоцилизумаб (Tocilizumab, анти-IL-6), Бродалумаб (анти-IL-17), Икзекизумаб (анти-IL-17) по мнению экспертов обладают высоким потенциалом, который предстоит доказать в будущих исследованиях.
Выводы
Гангренозная пиодермия - редкое заболевание, которое остается сложным с диагностической и терапевтической точек зрения. Диагноз осложняется отсутствием серологических и гистологических маркеров и обилием клинически сходных заболеваний. Текущие исследования показывают, что дисфункция нейтрофилов, воспаление и генетика играют определенную роль в прогрессировании заболевания. Полностью понимание патофизиологических механизмов остается проблемой, и, возможно, в результате этого подходы к лечению отличаются от пациента к пациенту и даже в разное время у одного и того же пациента. Цели лечения - контролировать воспаление и оптимизировать заживление ран. При этом все пациенты должны быть проинформированы о важности профилактики язв, необходимости избегать травм и, если возможно, хирургических вмешательств, а также об оптимальном лечении любого системного заболевания. Для лечения нет золотого стандарта. Для локализованной гангренозной пиодермии часто применяются топические и вводимые интрафокально кортикостероиды. Для более тяжелых или резистентных случаев можно использовать системное лечение, такое как системные кортикостероиды и иммунодепрессанты, такие как циклоспорин. Теоретически, таргетные биологические методы лечения могут давать преимущества в лечении гангренозной пиодермии, но данные ограничены. Среди таргетных биологических методов лечения на сегодняшний день наиболее сильные доказательства использования при гангренозной пиодермии имеются в отношении инфликсимаба, но адалимумаб и этанерцепт также могут принести пользу. Антагонисты IL-1 и антагонисты IL-12/23 представляют собой другие теоретически возможные методы лечения. Для более эффективного определения эффективности биологических препаратов при гангренозной пиодермии необходимы дополнительные клинические испытания.
Читайте также:

