При описторхозе могут быть диффузные изменения печени
Обновлено: 10.05.2024
Описторхоз — природно-очаговый зооантропоноз. Возбудителями описторхоза являются гельминты, относящиеся к типу Plathelmintes, классу Trematoda, семейству Opisthorchidae, видам Opisthorchis (Distomum) felineus (двуустка кошачья) и Opisthorchis viverrini. Самый крупный и напряженный очаг описторхоза в мире — Обь-Иртышский, охватывающий 10 краев и областей России и Казахстана. Инвазирование населения в Западной Сибири Opisthorchis felineus достигает 51,82%, в отдельных районах — свыше 95%. Течение описторхоза может быть острым и хроническим. Клиническая картина инфекции зависит от количества возбудителей, при небольшом количестве паразитов заболевание может протекать умеренно или бессимптомно, что может привести к пропущенному или позднему диагнозу. Фактически эти паразиты не могут размножаться в организме человека, и поэтому интенсивность инвазии с высокой частотой вспышек может быть достигнута только путем повторного потребления зараженной рыбы. Важность своевременного диагноза заключается в том, что нелеченная описторхозная инвазия может привести к тяжелым осложнениям, таким как цирроз печени, гепатоцеллюлярная карцинома и др. В статье описываются случай цирроза печени описторхозной этиологии, тактика лечения этого грозного осложнения и результаты дегельминтизации. Обсуждается проблема отсутствия противоописторхозного препарата в России, и предлагаются альтернативные способы решения этой проблемы.
Ключевые слова: описторхоз, Opisthorchis felineus, цирроз печени, празиквантел, албендазол.
Для цитирования: Плотникова Е.Ю., Баранова Е.Н. Проблемы лечения описторхозной инвазии. РМЖ. Медицинское обозрение. 2018;26(3):53-56.
Plotnikova E.Yu., Baranova Е.N.
Kemerovo State Medical University Ministry
Opisthorchiasis is a natural focal zooanthroponosis. Opisthorchiasis is caused by helminths related to the Plathelmintes type, the Trematoda class, the Opisthorchidae family, Opisthorchis felineus and Opisthorchis viverrini species. The largest and most tense center of opisthorchosis in the world is Ob-Irtysh region, covering 10 districts and regions of Russia and Kazakhstan. Invasive population of Opisthorchis felineus in Western Siberia reaches 51.82%, in some areas over 95%. The course of opisthorchiasis can be acute and chronic. The clinical picture of the infection depends on the number of pathogens, with a small number of parasites the disease can be mild or asymptomatic, which can lead to a missed or late diagnosis. In fact, these parasites can not reproduce in the human body, and therefore the intensity of infestation with a high frequency of outbreaks can only be achieved by re-consuming the infected fish. Timely diagnosing is very important because the untreated opisthorchiasis invasion can lead to serious complications, such as liver cirrhosis, hepatocellular carcinoma and others. The article describes the case of liver cirrhosis of opisthorchiasis etiology, tactics of treatment of this severe complication and the results of dehelminthization. The problems of the absence of an anti-opisthorchiasis drug in Russia are discussed and alternative ways of solving this problem are proposed.
Key words: opisthorchiasis, Opisthorchis felineus, liver cirrhosis, Praziquantel, Albendazole.
For citation: Plotnikova E.Yu., Baranova Е.N. Problems of treatment of opisthorchiasis // RMJ. Medical Review. 2018. № 3. P. 53–56.
В статье описывается случай цирроза печени описторхозной этиологии, тактика лечения этого грозного осложнения и результаты дегельминтизации. Обсуждается проблема отсутствия противоописторхозного препарата в России, и предлагаются альтернативные способы решения этой проблемы.
Введение
Патогенез описторхоза
В патогенезе описторхоза, как и многих других гельминтозов, прослеживаются 2 фазы: ранняя и поздняя. Ранняя фаза, или острый описторхоз, длится от нескольких дней до 4–8 нед. и более и связана с проникновением личинок (эксцистированных метацеркариев) паразита в гепатобилиарную систему и поджелудочную железу. В ранней стадии болезни ведущим патогенетическим фактором является развитие общей аллергической реакции и органных поражений в ответ на воздействие ферментов и продуктов метаболизма паразита. В их основе лежат клеточная пролиферация с выделением клетками эндогенных факторов воспаления в коже, слизистых оболочках дыхательных путей, пищеварительных органов, нарушение микроциркуляции, грануломатоз. При массивной инвазии это приводит к развитию эрозивно-язвенного гастрита, аллергического гепатита, пневмонии, миокардита, энцефалопатии. Клинические проявления острой стадии болезни зависят и от индивидуальной реактивности, наклонности к аллергическим реакциям. У коренных жителей высокоэндемичных очагов описторхоза вследствие ранних повторных заражений и развития толерантности к сенсибилизирующему действию антигенов паразита острая стадия болезни клинически реализуется редко [8].
Поздняя (хроническая) фаза, или хронический описторхоз, продолжается многие годы. В патогенезе хронической фазы описторхоза большую роль играют повторные заражения с обострением воспалительного процесса, фиброзом билиарных путей, поджелудочной железы, дистрофией паренхимы печени, ДЖВП, холестазом. Описторхозный холангиогепатит, не осложненный бактериальной инфекцией желчных путей, алкогольной интоксикацией желчных путей, перенесением вирусных гепатитов, протекает обычно доброкачественно. Однако хронический воспалительный процесс в билиарных путях является одним из факторов, способствующих развитию холангиокарциномы у населения территорий, гиперэндемичных по описторхозу. Развитию хронического гастродуоденита, панкреатита, холепатии способствует нарушение гормональной регуляции пищеварения — снижение продукции гастрина, секретина, глюкагона. Описторхоз отягощает язвенную болезнь желудка и двенадцатиперстной кишки, способствует развитию хронической пневмонии, хронического астмоидного бронхита, что обусловлено иммуносупрессивным воздействием инвазии [9].
Клиническая картина описторхоза
Лечение
Клинический случай
Заключение
Паразитарные заболевания печени – группа разнородных болезней, вызываемых паразитами и гельминтами. Самые распространенные паразитозы печени: аскаридоз, эхинококкоз, амебиаз, описторхоз и др. К общим симптомам относят истощение, дистрофические изменения кожи и волос, повышенную утомляемость, нарушения сна, неприятный запах изо рта. В диагностике используют дуоденальное зондирование, исследование дуоденального содержимого, анализ кала на яйца гельминтов, УЗИ, КТ, сцинтиграфию печени. Лечение консервативное, заключающееся в назначении антипаразитарного препарата (специфического либо широкого спектра действия), либо оперативное.
Общие сведения
Паразитарные заболевания печени вызываются протозоозами и глистными инвазиями. Всемирная организация здравоохранения считает, что не менее 25% населения Земли заражено теми или иными паразитами. Паразитозы и гельминтозы занимают четвертое место среди заболеваний, приносящих наибольший вред здоровью человека. На данный момент не существует исследований, которые бы отражали истинную заболеваемость паразитарными болезнями и гельминтозами в России. По мнению экспертов в области инфекционных заболеваний и гастроэнтерологии, паразитарные инвазии могут быть выявлены не менее чем у двадцати миллионов россиян. Учитывая тот факт, что паразиты и глисты могут персистировать в организме долгие годы, заболевание нередко накладывает отпечаток на всю жизнь: вызывает задержку роста и развития в детском возрасте, ухудшает умственные способности школьников, провоцирует снижение работоспособности и активности взрослого населения.
Причины паразитарных заболеваний печени
Все паразитарные заболевания печени возникают либо при протозойном инфицировании, либо в результате глистной инвазии. Поражение печени в этой ситуации выступает одним из проявлений генерализованной инфекции. Среди протозойных инфекций печень чаще всего поражается при токсоплазмозе, амебиазе, лейшманиозе, малярии. Гельминтозы представлены нематодозами, цестодозами, трематодозами. Нематодозы вызываются круглыми червями (аскаридоз, стронгилоидоз, токсокароз, трихинеллез); трематодозы – сосальщиками (фасциолез, клонорхоз, описторхоз); цестодозы – ленточными глистами (альвеококкоз, эхинококкоз).
Разнообразие клинических проявлений паразитарных заболеваний печени обусловлены не только видом паразита либо гельминта, но и их жизненным циклом, местом внедрения в организм, локализацией различных жизненных форм, реакцией иммунитета на возбудителя.
Сосальщики обычно локализуются в желчевыводящих протоках, желчном пузыре. Присосками сосальщиков повреждается эпителий протоков, в которых образуются кисты, воспалительная реакция, формируется холангит и холестаз. При фасциолезе личинки с током крови проникают в ткань печени, затем мигрируют в желчевыводящие пути и там превращаются в половозрелого паразита. В дальнейшем гельминты повреждают ткань печени, формируя микроскопические гнойники в паренхиме и желчных ходах. Схожий патогенез заболевания имеет и аскаридоз.
При эхинококкозе и амебиазе в печени формируются объемные образования. Шистосомозы приводят к фиброзированию паренхимы печени. Заражение малярийным плазмодием, трипаносомами, шистосомами приводит к значительному увеличению размеров печени, воспалительному процессу, печеночной недостаточности.
Главную роль в поражении печеночной паренхимы играют патологические иммунные реакции. Паразиты и гельминты выделяют антигены, которые провоцируют избыточные иммунные реакции, приводящие к значительному поражению клеток и микрососудов печени. Личинки и взрослые особи глистов, находящиеся в ткани печени, выделяют ряд ферментов, повреждающих гепатоциты и стимулирующих синтез фибрина. Хроническое персистирование паразитов рано или поздно приводит к фиброзированию печени, хронической печеночной недостаточности. Ниже рассмотрены основные виды паразитарных заболеваний печени, встречающиеся в России.
Виды паразитарных заболеваний печени
Эхинококкоз печени
Эхинококкоз занимает ведущее место среди всех паразитарных заболеваний печени. В подавляющем большинстве случаев поражается правая половина печени, практически у половины пациентов эхинококковых кист несколько. У людей эхинококкоз печени может быть гидатидным (личиночная стадия, кистозная форма, человек является промежуточным хозяином) и альвеококковым. Основным хозяином являются псовые, в организме которых эхинококк созревает, а его терминальные членики с огромным количеством яиц попадают в окружающую среду, вызывая заражение человека фекально-оральным либо контактным путем. Попадая в желудок, оболочка яиц растворяется и гельминты проникают через стенку желудка или кишечника в кровь. С током крови возбудители мигрируют в печень, а затем и в другие органы, формируя в них кисты (изначально – около 1 мм диаметром). Эхинококковая киста печени имеет две оболочки, внутренняя продуцирует жидкую составляющую кисты, образует дочерние пузыри. Наружная оболочка может кальцифицироваться, содержимое ее может нагнаиваться. Кисты огромных размеров сдавливают паренхиму печени и сосуды, желчевыводящие пути.
Гидатидный эхинококкоз. В первые годы после заражения эхинококкоз может никак не проявляться. Первые клинические проявления обычно возникают по достижению кистой больших размеров – боли в правом боку, тошнота и рвота, слабость, исхудание, хроническая диарея, аллергические высыпания на коже, ломкость волос. Размеры печени увеличиваются, при поверхностном расположении кисты ее можно даже пропальпировать. Желтуха развивается только при сдавлении кистой протоков печени. Возможен прорыв кистозного образования в брюшную или грудную полость, сопровождающийся сильной болью, анафилактическим шоком (реакция на всасывание содержимого кисты). Нагнаивание содержимого кисты сопровождается болезненностью печени, лихорадкой, ухудшением общего состояния.
Диагностика эхинококкоза включает сбор анамнеза (контакт с собакой), пальпацию печени и выявление эхинококковой кисты. Специфическим методом диагностики является реакция Казони (положительна в 85% случаев), латекс-агглютинации (90%). Визуализировать паразита помогут УЗИ печени и желчного пузыря, ангиография чревного ствола, МРТ печени и желчевыводящих путей, статическая сцинтиграфия печени, диагностическая лапароскопия.
Лечение только оперативное. Производится иссечение эхинококковых кист печени, предварительно в кисту вводят формалин и отсасывают ее содержимое. Полость кисты ушивают наглухо. В последующем может сформироваться непаразитарная киста, гнойник. При маленьких размерах и краевом положении кисты возможна резекция печени вместе с кистой.
Альвеолярный эхинококкоз. Является более редкой формой паразитарного заболевания печени, вызываемого эхинококком. Возбудитель альвеококкоза отличается своей личиночной стадией. Заражение происходит при обработке шкур основного хозяина (лисы и др.), употреблении зараженных продуктов. Особенностью альвеококкоза является образование множества мелких кист, которые инфильтрируют паренхиму печени, плотно прилегая друг к другу и образуя опухолевидный узел в ткани печени. Пузырьки паразита способны прорастать в паренхиму печени, сосуды, желчные пути, соседние органы. В центре очага альвеококкоза формируется некроз, в дальнейшем альвеококковый очаг может обызвествляться. Дифференцировать заболевание следует с раком печени, циррозом печени.
Клиническая картина альвеококкоза сходна с гидатидной формой заболевания, однако имеет большую частоту механической желтухи. Лечение альвеококкоза печени имеет определенные особенности. Проведение операции затруднено инфильтративным ростом паразитов, прорастанием сосудов, желчных путей, круглой связки печени. Обычно операция назначается при значительном поражении печени, нагноении и прорыве кист. Чаще всего производится частичная резекция печени, оставшиеся кисты обрабатываются химиопрепаратами или формалином, подвергаются криодеструкции.
Аскаридоз печени и желчных путей
На сегодняшний день аскаридоз печени встречается достаточно редко. Человек заражается при употреблении в пищу зараженных яйцами аскарид продуктов. Попадая в кишечник, возбудители через кишечную стенку проникают в кровеносное русло, с током крови попадают в печень. В печени из-за персистирования паразитов формируются некрозы, микроабсцессы. В дальнейшем возбудители могут мигрировать по организму, попадая в другие органы и системы, а в кишечнике превращаясь в половозрелые формы.
Основными проявлениями аскаридоза являются холангиты, холестаз, абсцессы печени. Специфических симптомов аскаридоза не существует. Диагноз аскаридоза печени устанавливается на основании обнаружения аскарид и их яиц в рвотных массах, кале; также возможна визуализация гельминтов при УЗИ, КТ печени.
Лечение аскаридоза желчевыводящих путей только хирургическое. Применение противоаскаридозных средств при закупорке желчных путей противопоказано, так как приводит к кратковременной активизации паразитов и их дальнейшему проникновению в желчные пути и паренхиму печени. Для уточнения степени поражения протоков во время операции проводят РХПГ. Для профилактики персистирования аскаридоза, образования конкрементов желательно провести холецистэктомию. В послеоперационном периоде по дренажам вводят антиаскаридозные препараты для уничтожения оставшихся гельминтов.
Описторхоз печени
Данное паразитарное заболевание печени встречается достаточно редко, заражение человека происходит через сырую рыбу, зараженные водоемы. Размножение гельминта в желчных путях приводит к их расширению. Ткань печени становится очень плотной, расширенные внутрипеченочные протоки видны сквозь капсулу печени. Персистирование инвазии приводит к утолщению стенок желчных путей, формированию грубых рубцовых изменений вокруг них, которые напоминают цирроз печени, часто приводят к перфорации желчных протоков и перитониту. Закупорка желчных ходов благоприятствует застою и воспалительным изменениям в них. У пациентов с описторхозом часто в будущем развивает рак печени.
Описторхоз, как и другие паразитарные заболевания печени, не имеет специфической клиники. Частыми проявлениями являются увеличение и уплотнение печени, боли в правом подреберье, жидкий стул. В случае присоединения инфекции пациента беспокоят лихорадка, озноб, липкий пот.
Диагноз ставится на основании выявления особей и яиц гельминтов в кале и дуоденальном соке, полученном при зондировании. Лечение описторхоза печени хирургическое, заключается в дренировании протоков, введении антипаразитарных препаратов в дренажи.
Амебиаз печени
Заболевание часто встречается в тропических странах. Характеризуется преимущественным поражением толстого кишечника, диссеминацией возбудителя в паренхиматозные органы. Цисты амеб попадают в организм человека с зараженной водой, фруктами и овощами, зеленью.
Амебы вызывают образование язв в кишечнике, через которые возбудители попадают в кровоток, а затем в печень, приводя к формированию абсцессов печени примерно в 10% случаев. Особенность амебных абсцессов в том, что они не имеют капсулы, содержат в себе расплавленные ткани, кофейного цвета гной. Состояние пациентов обычно очень тяжелое, печень увеличена и болезненна. Кожные покровы иктерично-серые, сухие.
В диагностике абсцесса печени используют УЗИ гепатобилиарной системы, сцинтиграфию печени, КТ, пункционную биопсию печени (с целью выявления амеб). Лечение амебиаза обычно комплексное: антиамебные, антибактериальные и дезинтоксикационные препараты. Хирургическое лечение проводится при неэффективности консервативных мероприятий, возникновении осложнений.
Прогноз и профилактика паразитарных заболеваний печени
Прогноз при паразитарных заболеваниях печени зависит от многих факторов: длительности паразитарной инвазии, обширности поражения печени, наличия осложнений. При длительном течении паразитарного поражения печени с формированием фиброза, развитием печеночной недостаточности прогноз неблагоприятный.
Профилактика всех паразитарных заболеваний печени заключается в соблюдении правил личной гигиены (мыть руки после контакта с животными, пить только кипяченую воду, тщательно мыть овощи и фрукты перед употреблением в пищу, проводить термическую обработку мяса и рыбы), контроле за состоянием водоемов, из которых производится забор питьевой воды.
Описторхоз – гельминтное заболевание, вызываемое плоскими паразитическими червями класса сосальщиков и протекающее с поражением гепатопанкреатобилиарной системы. Течение описторхоза характеризуется лихорадкой, болями в животе, нарушением аппетита, кожными высыпаниями, желтухой, гепатоспленомегалией, диспепсией, астматическим бронхитом, астеновегетативным синдромом. Диагностика описторхоза основывается на обнаружении яиц описторхисов в дуоденальном содержимом и в кале, результатах серологических реакций, данных биохимического анализа крови, инструментальных исследований (УЗИ, холецистохолангиографии, КТ). Для терапии описторхоза используются противогельминтные (празиквантел, азинокс), желчегонные и ферментные препараты.
МКБ-10
Общие сведения
Описторхоз – внекишечный гельминтоз из группы трематодозов, возбудители которого паразитируют в желчных протоках печени и поджелудочной железе, вызывая полиморфные клинические проявления. Наиболее напряженный очаг описторхоза расположен на территории Западной Сибири, в низовьях р. Иртыш и среднем течении Оби, где инвазированность местного населения приближается к 80-90%. Кроме этого, эндемичными по описторхозу районами служат бассейны рек Волга, Кама, Днепр, Дон, Енисей и др., главным образом, связанные с рыбным промыслом и рыбопереработкой. Наибольшая заболеваемость регистрируется среди лиц в возрасте от 15 до 50 лет, преимущественно мужчин. Опасность описторхоза заключается в том, что при длительном течении он повышает риск развития рака печени и рака поджелудочной железы.

Причины описторхоза
Описторхоз вызывают два вида гельминтов-сосальщиков: Opisthorchis felineus и Opisthorchis viverrini. На территории России распространен возбудитель О. felineus – сибирская или кошачья двуустка. Это плоский гельминт длиной 4–20 мм, шириной 1–4 мм, имеющий ланцетовидное тело, снабженное ротовой и брюшной присосками. Описторхоз, вызываемый O. viverrini встречается в странах Юго-Восточной Азии.
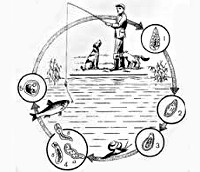
Развитие описторхисов происходит с трехкратной сменой хозяев: первым промежуточным хозяином выступают моллюски, вторым промежуточным - пресноводные рыбы семейства карповых (лещ, сазан, линь, елец, язь, плотва и др.) и окончательным - млекопитающие (кошка, собака, лисица, выдра, песец, соболь, человек), питающиеся рыбой. Окончательные хозяева выделяют яйца с личинками во внешнюю среду вместе с фекалиями. Попав в водоем, яйца заглатываются пресноводными моллюсками рода Codiella, в организме которых претерпевают изменения: сначала из яйца выходит мирацидий, который последовательно превращается в спороцисту, редию и церкария. Хвостатая личинка (церкарий) выходит из тела моллюска и в водоеме прикрепляется к телу карповых рыб, внедряется в соединительную и мышечную ткань, где инцистируется, превращаясь в метацеркарий. Находясь в теле рыб, через 6 недель личинки становятся инвазионными, т. е. приобретают способность вызывать описторхоз у окончательных хозяев.
Заражение человека и животных происходит при употреблении инвазированной, плохо обработанной (сырой, малосольной) рыбы. В ЖКТ окончательного хозяина под действием дуоденального сока капсула и оболочки личинок растворяются, в результате чего метацеркарии мигрируют в общий желчный проток, внутрипеченочные желчные протоки, а также в протоки поджелудочной железы. В гепатопанкреатобилиарной системе через 3–4 недели метацеркарий превращается в зрелого описторхиса, способного продуцировать яйца. Полный цикл развития гельминта от стадии яйца до половозрелой особи длится 4–4,5 месяца. Инвазированность человека описторхисами может варьировать от нескольких единиц до десятков тысяч. В организме окончательного хозяина кошачья двуустка может паразитировать 20-25 лет.
Патогенез описторхоза
Характер и выраженность патологических процессов, характеризующих течение описторхоза, зависят от массивности и длительности инвазии, состояния иммунной системы. В зависимости от этих факторов течение описторхоза может быть стертым или манифестным; легким, среднетяжелым и тяжелым. В патогенезе описторхоза выделяют раннюю (острую) и позднюю (хроническую) стадии.
В острой стадии гельминтоза доминируют токсико-аллергические реакции, развивающиеся в ответ на действие метаболитов паразитов на организм хозяина. Они сопровождаются повышением проницаемости сосудистой стенки, периваскулярным отеком и эозинофильной инфильтрацией стромы различных органов, образованием некротических очагов в паренхиме печени. Повреждение сосальщиками эпителия желчных протоков вызывает гиперплазию бокаловидных клеток, кистозное расширение мелких желчных ходов. При хроническом описторхозе в стенках желчных протоков развивается вялотекущее воспаление, выявляется разрастание соединительной ткани, нередко возникает закупорка гельминтами мелких желчных протоков. Данные процессы приводят к развитию вторичного бактериального холангита, дискинезии желчевыводящих путей, образованию желчных камней, в тяжелых случаях – к циррозу печени и портальной гипертензии. Поражения поджелудочной железы при описторхозе определяются, главным образом, отеком железы и нарушением оттока панкреатического секрета, что сопровождается кистевидным расширением канальцев, пролиферативным каналикулитом и фиброзом органа.
Симптомы описторхоза
Острая фаза описторхоза манифестирует через 2-4 недели после заражения. Легкая форма гельминтоза начинается с внезапного скачка температуры тела до 38°С и последующего сохранения субфебрилитета в течение в течение 1-2-х недель. В это время пациенты испытывают слабость, боли в животе, отмечают неустойчивый характер стула. В периферической крови при легком течении описторхоза выявляется умеренный лейкоцитоз и эозинофилия до 15 - 20%.
Среднетяжелая форма описторхоза протекает с лихорадкой (до 39°С и выше), которая длится около 3-х недель. Характерны миалгии и артралгии, уртикарные кожные высыпания, катар верхних дыхательных путей, увеличение печени и селезенки, рвота, диарея, астматический бронхит. Нарастают лейкоцитоз, эозинофилия до 25 - 60%, повышается СОЭ.
Тяжелые формы острого описторхоза развиваются у 10 - 20% больных и могут протекать по тифоподобному, гастроэнтероколитическому, гепатохолангитическому и респираторному вариантам. Симптоматика тифоподобного варианта описторхоза включает высокую лихорадку, озноб, лимфаденит, полиморфную кожную сыпь, диспепсию. В клинике преобладают явления интоксикации и аллергизации; возможно токсико-аллергическое поражение ЦНС или миокарда. При гастроэнтероколитической форме описторхоза развивается клиническая и патоморфологическая картина гастрита (катарального, эрозивного), гастродуоденита, язвы желудка и двенадцатиперстной кишки, энтероколита. Данные состояния сопровождаются снижением аппетита, тошнотой, болями в эпигастрии и правом подреберье, диареей. В течении гепатохолангитического варианта острого описторхоза превалируют желтуха, гепатоспленомегалия, абдоминальный синдром по типу печеночной колики или опоясывающего характера. Патологические синдромы могут включать в себя гепатит, холангит, холецистит, панкреатит. При вовлечении органов дыхания (респираторном варианте описторхоза) развивается трахеит, астмоидный бронхит, пневмония, плеврит, лихорадка.
Хронический описторхоз чаще всего протекает по типу дискинезии желчных путей, холангиогепатита, холангиохолецистита, желчнокаменной болезни, хронического панкреатита, гастрита, дуоденита. Имеют место признаки астеновегетативного синдрома: слабость, утомляемость, раздражительность, эмоциональная неустойчивость, головная боль, нарушение сна, повышенное потоотделение. Могут развиваться дистрофические изменения миокарда, проявляющиеся болями за грудиной, тахикардией, артериальной гипотонией. Длительное течение хронического описторхоза может осложниться циррозом печени, гнойным холангитом, флегмоной желчного пузыря, желчным перитонитом, первичным раком печени и поджелудочной железы.
Диагностика описторхоза
При проведении диагностики описторхоза учитываются эпидемиологические сведения, указывающие на пребывание пациента в эндемичных очагах, употребление в пищу свежезамороженной, малосоленой, недостаточно термически обработанной рыбы. Характерно изменение биохимических проб печени и ферментов поджелудочной железы - повышение билирубина, трансаминаз, амилазы и липазы. Данные инструментальных исследований (ФГДС, УЗИ гепатодуоденальной зоны и поджелудочной железы, холецистография, КТ, МРТ печени и желчевыводящих путей) обнаруживают признаки гастродуоденита, дискинезии желчевыводящих путей, холецистита, холангита, гепатита, панкреатита.
В целях паразитологического подтверждения описторхоза проводится микроскопическое исследование дуоденального содержимого и кала, в которых обнаруживаются яйца кошачьей двуустки. Для повышения вероятности обнаружения яиц гельминта перед проведением дуоденального зондирования и копроовоскопии целесообразно назначать пациенту тюбажи по Демьянову и желчегонные препараты. Выявить противоописторхозные антитела в сыворотке крови позволяет иммуноферментный анализ. Ввиду полиморфизма клинических симптомов течение острого описторхоза может напоминать вирусный гепатит, пищевую токсикоинфекцию, заболевания тифопаратифозной группы, миграционную фазу аскаридоза и анкилостомидоза.
Лечение описторхоза
Лечение описторхоза осуществляется поэтапно. На первом этапе назначается подготовительная терапия, включающая желчегонные и спазмолитические препараты, блокаторы Н1-гистаминовых рецепторов; по показаниям – короткие курсы антибиотиков. Кроме медикаментозной терапии, проводится физиотерапевтическое лечение (электрофорез сернокислой магнезии, магнитотерапия, микроволновая терапия). Целью подготовительного этапа служит нормализация желчевыделения и оттока желчи, купирование воспалительного процесса в ЖКТ и желчевыводящих путях.
В рамках основного этапа лечения описторхоза назначается противогельминтная химиотерапия. Наибольшую эффективность в уничтожении паразитов доказали празиквантел и его аналоги. После проведения дегельминтизации для эвакуации описторхисов с желчью проводится слепое зондирование, импульсная магнитотерапия, электростимуляция диафрагмального нерва. В случае выраженного токсико-аллергического синдрома требуется назначение антигистаминных препаратов, глюкокортикоидов, инфузионной терапии. Контроль эффективности противопаразитарного лечения предполагает проведение трехкратного исследования фекалий и дуоденального содержимого.
Заключительный этап курса лечения описторхоза направлен на выведение продуктов распада паразитов и восстановления биоценоза кишечника. С этой целью проводятся тюбажи с ксилитом, сорбитом, минеральной водой; назначаются желчегонные и ферментные препараты, гепатопротекторы, сорбенты, пре- и пробиотики.
Прогноз и профилактика описторхоза
При легких и среднетяжелых формах описторхоза прогноз обычно благоприятный, хотя возможны случаи повторной гельминтной инвазии. При возникновении гнойного холецистита и перитонита исход зависит от полноты и скорости оказания хирургической помощи. Прогностически неблагоприятно развитие острой печеночной недостаточности, рака печени, поджелудочной железы или холангиокарциномы.
Действия по предотвращению заражения описторхозом включают лечебно-профилактическую работу (выявление и дегельминтизацию инвазированных), эпидемиологические мероприятия (защиту водоемов от загрязнения фекалиями человека и животных, соблюдение технологии обработки и приготовления рыбы, уничтожение моллюсков), санитарно-просветительную работу (информирование населения).
Что такое жировой гепатоз, неалкогольная жировая болезнь печени (НАЖБП)? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Неалкогольная жировая болезнь печени / НАЖБП (стеатоз печении или жировой гепатоз, неалкогольный стеатогепатит) — это неинфекционное структурное заболевание печени, характеризующееся изменением ткани паренхимы печени вследствие заполнения клеток печени (гепатоцитов) жиром (стеатоз печени), которое развивается из-за нарушения структуры мембран гепатоцитов, замедления и нарушения обменных и окислительных процессов внутри клетки печени.
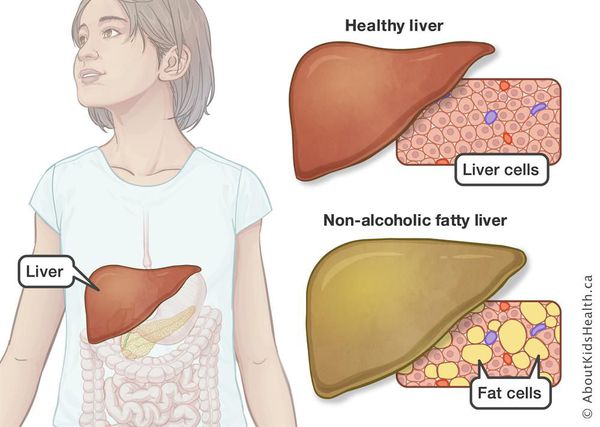
Все эти изменения неуклонно приводят к:
- разрушению клеток печени (неалкогольный стеатогепатит);
- накоплению жировой и формированию фиброзной ткани, что вызывает уже необратимые, структурные (морфологические) изменения паренхимы печени;
- изменению биохимического состава крови;
- развитию метаболического синдрома (гипертоническая болезнь, ожирение, сахарный диабет);
- в конечном итоге, циррозу.
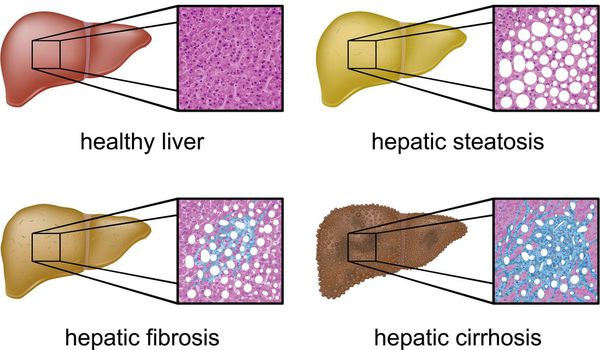
Метаболический синдром — широко распространённое состояние, характеризующееся снижением биологического действия инсулина (инсулинорезистентность), нарушением углеводного обмена (сахарный диабет II типа), ожирением центрального типа с дисбалансом фракций жира (липопротеинов плазмы и триглицеридов) и артериальной гипертензией. [2] [3] [4]
В большинстве случаев НАЖБП развивается после 30 лет. [7]
Факторами риска данного заболевания являются:
- малоподвижный образ жизни (гиподинамия);
- неправильное питание, переедание;
- длительный приём лекарственных препаратов;
- избыточная масса тела и висцеральное ожирение;
- вредные привычки.
Основными причинам развития НАЖБП являются: [11]
- гормональные нарушения;
- нарушение жирового обмена (дисбаланс липопротеидов плазмы);
- нарушение углеводного обмена (сахарный диабет);
- артериальная гипертензия;
- ночная гипоксемия (синдром обструктивного апноэ сна).
При наличии гипертонической болезни, ожирения, сахарного диабета, регулярном приёме лекарств или в случае присутствия двух состояний из вышеперечисленных вероятность наличия НАЖБП достигает 90 %. [3]
Ожирение определяется по формуле вычисления индекса массы тела (ИМТ): ИМТ = вес (кг) : (рост (м)) 2 . Если человек, например, весит 90 кг, а его рост — 167 см, то его ИМТ = 90 : (1,67х1,67) = 32,3. Этот результат говорит об ожирении I степени.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
У большинства больных данное заболевание на ранних стадиях протекает бессимптомно — в этом и заключается большая опасность.
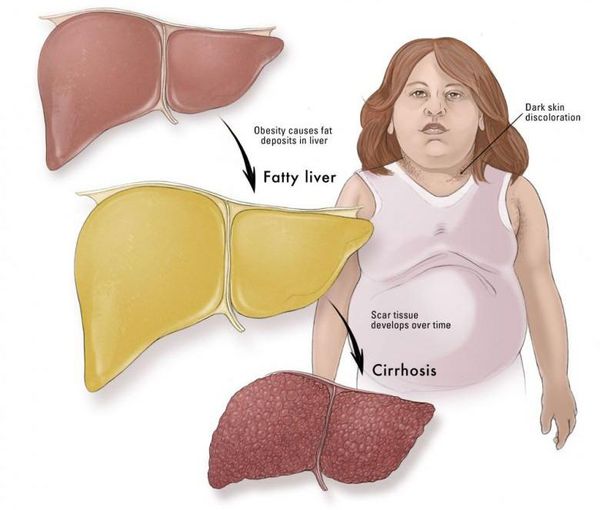
Часто НАЖБП сопутствуют заболевания желчного пузыря: хронический холецистит, желчнокаменная болезнь. Реже, в запущенных случаях, возникают признаки портальной гипертензии: увеличение селезёнки, варикозное расширение вен пищевода и асцит (скопление жидкости в брюшной полости). Как правило, данные симптомы наблюдаются на стадии цирроза печени. [7]
Патогенез жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
К накоплению холестерина, а именно липидов (жироподобных органических соединений) в печени, приводят, прежде всего, следующие факторы:
- избыточное поступление свободных жирных кислот (FFA) в печень;
- усиленный синтез свободных жирных кислот печени;
- пониженный уровень бета-окисления свободных жирных кислот;
- снижение синтеза или секреции липопротеинов очень высокой плотности. [7]
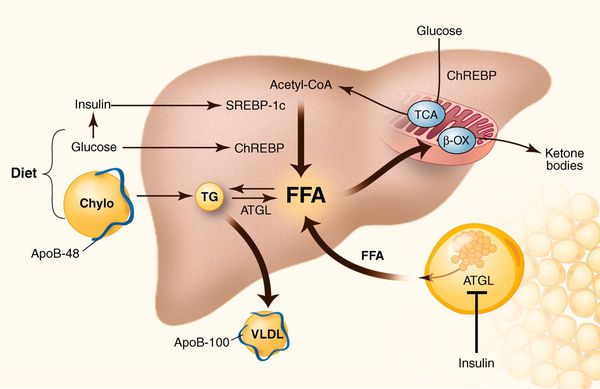
У пациентов с ожирением в ткани печени повышенно содержание свободных жирных кислот, что и может быть причиной нарушения функций печени, так как жирные кислоты химически активны и могут привести к повреждению биологических мембран гепатоцитов, образуя в них ворота для поступления в клетку эндогенного жира, в частности липидов (преимущественно низкой и очень низкой плотности), а транспортом является сложный эфир — триглицерид. [2]
Таким образом, гепатоциты заполняться жиром, и клетка становиться функционально неактивной, раздувается и увеличивается в размерах. При поражении более миллиона клеток макроскопически печень увеличивается в размерах, в участках жировой инфильтрации ткань печени становиться плотнее, и данные участки печени не выполняют своих функций либо выполняют их с существенными дефектами.
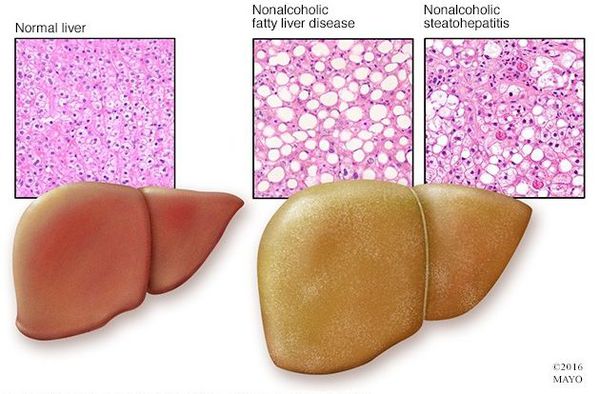
Перекисное окисление липидов в печени приводит к синтезу токсичных промежуточных продуктов, которые могут запускать процесс апоптоза (запрограммированной гибели) клетки, что может вызывать воспалительные процессы в печени и сформировать фиброз. [2]
Также важное патогенетическое значение в формировании НАЖБП имеет индукция цитохрома P-450 2E1 (CYP2E1), который может индуцироваться как кетонами, так и диетой с высоким содержанием жиров и низким содержанием углеводов. [7] CYP2E1 генерирует токсические свободные радикалы, приводящие к повреждению печени и последующему фиброзу.
Кроме того, патогенетическое значение в формировании НАЖБП имеет эндотоксин-опосредованное повреждение, которое, в свою очередь, усиливает выработку провоспалительных цитокинов (ФНО-α, ИЛ-6 и ИЛ-8), приводящих к нарушению целостности мембран гепатоцитов и даже к их некрозу [9] , а также к развитию воспалительной клеточной инфильтрации как в портальных трактах, так и в дольках печени, что приводит к стеатогепатиту.
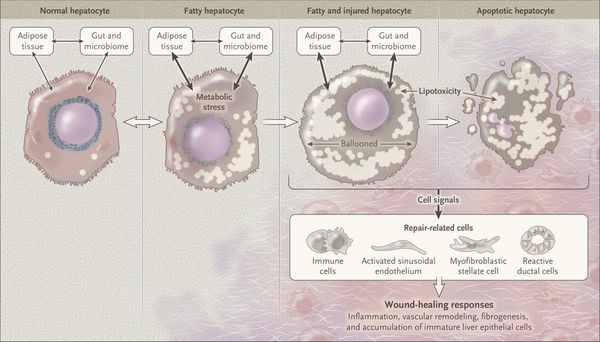
Продукты перекисного окисления липидов, некрозы гепатоцитов, ФНО и ИЛ-6 активируют стеллатные (Ito) клетки, вызывающие повреждение гепатоцитов и формирование фиброзных изменений.
Классификация и стадии развития жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
В настоящий момент общепринятой классификации НАЖБП не существует, однако ряд авторов выделяет стадии течения заболевания и степени неалкогольного стеатогепатита (НАСГ).
Оценка стеатоза печени и гистологической активности НАЖБП по системе E.M. Brunt: [9] [10] [11]
- I степень (мягкий НАСГ) — стеатоз крупнокапельный, не более 33-66% поражённых гепацитов;
- II степень (умеренный НАСГ) — крупно- и мелкокапельный, от 33% до 66% поражённых гепацитов;
- III степень (тяжелый НАСГ) — крупно- и мелкокапельный, больше 60% поражённых гепацитов.
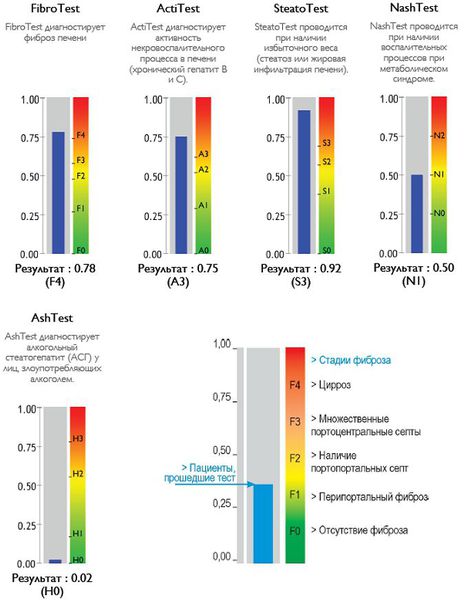
Также можно условно разделить степени стеатоза, фиброза и некроза по результату теста ФиброМакс — степени выраженности жировой инфильтрации:
- S1 (до 33% жировой инфильтрации);
- S2 ( 33-60% жировой инфильтрации)
- S3 (более 60% жировой инфильтрации)
- F1,F2, F3, цирроз.
Осложнения жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
Наиболее частые осложнения НАЖБП — это гепатит, замещение нормальной паренхиматозной ткани печени фиброзной — функционально нерабочей тканью с формированием в конечном итоге цирроза печени.
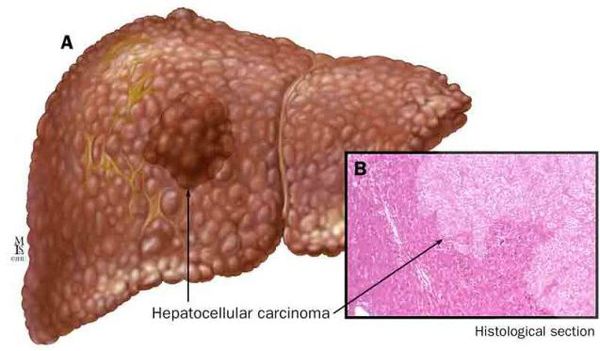
К более редкому осложнению, но всё же встречающемуся, можно отнести рак печени — гепатоцеллюлярную карциному. [9] Чаще всего она встречается на этапе цирроза печени и, как правило, ассоциируется с вирусными гепатитами.
Диагностика жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
В диагностике НАЖБП используются лабораторные и инструментальные методы исследования.
В первую очередь оценивается состояние печени на предмет воспалительных изменений, инфекционных, аутоиммунных и генетических заболеваний (в том числе болезней накопления) с помощью общеклинических, биохимических и специальных тестов. [7]
Далее проводится оценка выполняемых печенью функций (метаболическая/обменная, пищеварительная, детоксикационная) по способности выработки определённых белков, характеристикам жиров и углеводов. Детоксикационная функция печени оценивается преимущественно при помощи С13-метацетинового теста и некоторых биохимических тестов.
Кода первые два этапа завершены, исследуется структурное состояние печени при помощи УЗИ [4] , МСКТ, МРТ и эластометрии (FibroScan), при необходимости исследуется морфологическое состояние — биопсия печени. [3]
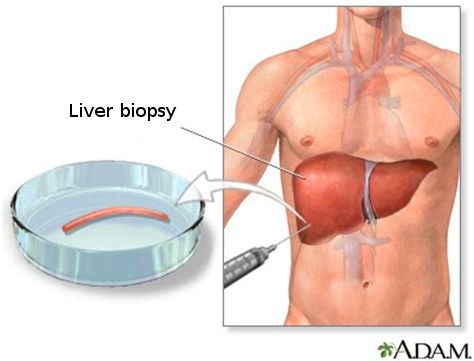
С помощью эластометрии исследуется эластичность мягких тканей. Злокачественные опухоли отличаются от доброкачетсвенных повышенной плотностью, неэластичностью, они с трудом поддаются компрессии. На мониторе FibroScan более плотные ткани окрашены в голубой и синий цвет, жировая ткань — жёлто-красный, а соединительная ткань — зелёный. Высокая специфичность метода позволяет избежать необоснованных биопсий.
После проведённой диагностики, устанавливается окончательный диагноз и проводится соответствующее лечение.
Лечение жирового гепатоза, неалкогольной жировой болезни печени (НАЖБП)
С учётом механизма развития заболевания разработаны схемы курсового лечения НАЖБП, направленные на восстановление структуры клеточных мембран, обменных и окислительных процессов внутри клеток печени на молекулярном уровне, очистку печени от внутриклеточного и висцерального жира, который затрудняет её работу.
В процессе лечения производится:
- коррекция углеводного, жирового (липидного) обмена веществ;
- нормализация процессов окисления в клетке;
- влияние на основные факторы риска;
- снижение массы тела;
- улучшение структуры печени на обратимых стадиях.
После лечения наступает заметное улучшение дезинтоксикационной (защитной), пищеварительной и метаболической функции печени, пациенты теряют в весе, улучшается общее самочувствие, повышается умственная и физическая работоспособность.
Курсовые программы лечения занимают от трёх до шести месяцев и подбираются в зависимости от степени выраженности метаболических нарушений. К ним относятся:
Программы включают в себя предварительное обследование, постановку диагноза и медикаментозное лечение, которое состоит из двух этапов:
- инфузионная терапия с пролонгацией приёма препаратов внутрь, подбор диеты и физической активности;
- сдача контрольных анализов и оценка результатов.
Прогноз. Профилактика
На ранних стадиях заболевания прогноз благоприятный.
Профилактика НАЖБП предполагает правильное питание, активный образ жизни и регулярную календарную диспансеризацию.
К правильному питанию можно отнести включение в свой рацион питания омега-3 полиненасыщенных жирных кислот, коротких углеводов, ограничение потребления приправ, очень жирной и жаренной пищи. Разнообразие рациона питания также является ключевым моментом полноценного питания. Показано потребление продуктов, богатых растительной клетчаткой.
Для активного образа жизни достаточно ходить пешком от 8 000 до 15 000 шагов в сутки и уделять три часа в неделю физическим упражнениям.
В отношении календарной диспансеризации следует ежегодно выполнять УЗИ органов брюшной полости и оценивать уровень своих печёночных ферментов (АЛТ, АСТ, общий билирубин), особенно при приёме каких-либо лекарственных препаратов на постоянной основе.
Что такое цирроз печени? Причины возникновения, диагностику и методы лечения разберем в статье доктора Васильева Романа Владимировича, гастроэнтеролога со стажем в 15 лет.
Над статьей доктора Васильева Романа Владимировича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Цирроз печени (ЦП) — это хроническое дегенеративное заболевание печени, связанное с диффузным патологическим процессом, при котором нормальные клетки печени повреждаются, а затем замещаются рубцовой тканью, образуя избыточный фиброз и структурно-анатомические регенераторные узлы.
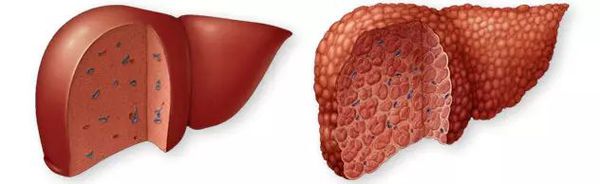
Этиология
По этиологическим характеристикам можно выделить:
- распространённые формы ЦП;
- редкие формы ЦП.
К распространённым относят вирусные (В, С, D), алкогольные и метаболические формы цирроза печени.
Редкими формами ЦП являются:
- аутоиммунные, лекарственные, токсические, первичные и вторичные билиарные циррозы;
- генетически обусловленные патологии — гемохроматоз (нарушение обмена железа), болезнь Вильсона — Коновалова, дефицит белка альфа-1-антитрипсина, гликогеноз IV типа (недостаток ферментов), галактоземия, наследственная тирозинемия и непереносимость фруктозы;
- нарушение венозного оттока из печени — венокклюзионные формы ЦП (болезнь Бадда — Киари);
- тяжёлая правожелудочковая сердечная недостаточность;
- флебопортальные циррозы (типа Банти).
Пути заражения
Заразиться циррозом печени нельзя. Однако, если он вызван вирусным гепатитом, то возбудитель может передаться через кровь, при половых контактах и от матери к ребёнку.
Основную роль в возникновении и развитии вирусного ЦП играют симптомные, малосимптомные и бессимптомные формы острого вирусного гепатита В, С, а также одновременное заболевание гепатитами В и D с последующим переходом в активный хронический вирусный гепатит. У большинства больных интервал между острым гепатитом С и клинически выраженными проявлениями ЦП превышает 30 лет. Только у мужчин, употребляющих более 50 г спирта в день, выраженные формы ЦП возникают через 13-15 лет.
Наиболее частыми причинами смерти больных ЦП является:
- большая печёночная недостаточность;
- кровотечение из варикозно расширенных вен пищевода;
- первичный рак печени;
- иммунопротективная недостаточность, влекущая за собой активизацию инфекционных (микробных) процессов, в первую очередь спонтанного бактериального перитонита и пневмонии, а также возникновение оксидативного стресса.
У больных в терминальной (заключительной) фазе заболеваний печени в основном наблюдаются декомпенсированные формы цирроза печени: асцит, варикозное расширение вен пищевода и желудка, энцефалопатия и желтуха.
Особенности цирроза печени у детей
Заболевание у детей встречается крайне редко и обычно связано:
- с аутоиммунным поражением печени;
- кардиогенными заболеваниями — лёгочной гипертензией и хронической сердечной недостаточностью;
- болезнью Бадда — Киари;
- врождёнными болезнями накопления — наследственным гемохроматозом, лизосомальными болезнями накопления, болезнью Вильсона — Коновалова;
- флебопортальным циррозом (типа Банти).
Прогноз у таких детей неблагоприятный, чаще всего они погибают, так как не успевают попасть к гепатологу и выяснить диагноз. Также они обычно страдают от множества сопутствующих болезней, в том числе от основного заболевания, ставшего причиной цирроза.
Проявления заболевания у детей и взрослых схожи. Единственный эффективный метод лечения цирроза у детей — это пересадка печени. Поэтому крайне важно вовремя диагностировать заболевание и встать в очередь на пересадку печени.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы цирроза печени
Цирроз печени в течение длительного времени может протекать латентно, т. е. бессимптомно.
Клиническая картина ЦП зависит от его формы и течения, активности основного заболевания, а также наличия или отсутствия печёночно-клеточной недостаточности, синдрома портальной гипертензии, холестаза и внепечёночных проявлений.
Основные общие симптомы, которые чаще всего встречаются при ЦП:
- повышенная утомляемость;
- похудение;
- нарушения сознания и поведения;
- ухудшение аппетита и чувство дискомфорта в животе;
- пожелтение кожи, белковых оболочек глаз и слизистой;
- осветление или обесцвечивание кала;
- потемнение мочи;
- болевые ощущения в животе;
- отёки;
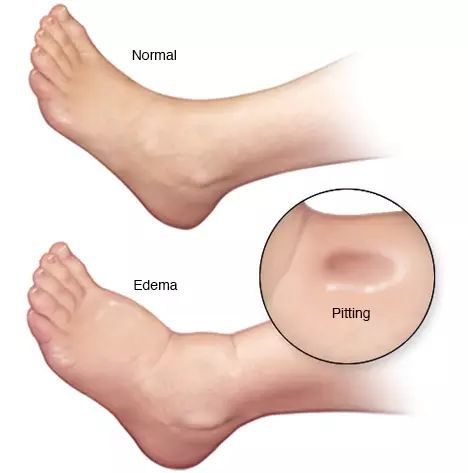
- асцит (скопление жидкости в брюшной полости);
- кровотечения из носа, желудочно-кишечного тракта, дёсен или геморроидальных узлов, а также подкожные кровоизлияния;
- часто возникающие бактериальные инфекции (например, органов дыхания);
- снижение полового влечения;
- кожный зуд.
Симптомы распространённых форм ЦП
При высокоактивном ЦП, кроме общей утомляемости, осветления стула и потемнения мочи, может возникать тупая боль в правом подреберье и вздутие живота.
Во время осмотра часто выявляют:
- субиктеричность (желтушность) склер;
- расширение вен брюшной стенки, напоминающее голову медузы;
- венозный шум при выслушивании в эпигастральной области живота (шум Крювелье — Баумгартена);
- серо-коричневатый цвет шеи;
- гинекомастию (увеличение грудных желёз);
- гипогонадизм (у мужчин);
- контрактуру Дюпюитрена (укорочение сухожилий ладоней).
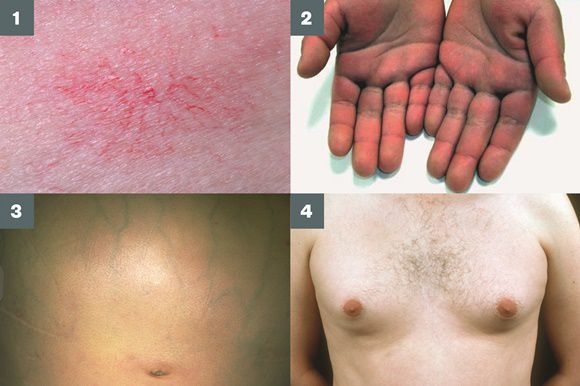
Три последних признака цирроза печени зачастую наблюдаются при алкогольных ЦП.
В области грудной клетки в 50-80% случаев наблюдаются телеангиэктазии кожи (расширения мелких сосудов), чаще при алкогольных ЦП. Пальпаторно печень отчётлива уплотнена, имеет неровный нижний край. Размеры печени различны — от значительного увеличения до уменьшения.
Часто при пальпации выявляется умеренно увеличенная селезёнка, причём её край может выступать из-под рёберной дуги на 1-3 см.
При развитии ЦП появляются симптомы белково-энергетической недостаточности, асцит, отёки, а также печёночный запах при тяжёлой печёночной недостаточности.
Симптомы при малоактивных и начальных стадиях ЦП
Данные формы ЦП зачастую протекают бессимптомно и выявляются в ходе периодических медицинских осмотров, диспансеризации, а также как случайная находка при обследовании пациента со смежной патологией или внепечёночными проявлениями.
При малоактивном ЦП, как правило, не возникают жалобы, связанные с печенью. Во время активного расспроса можно выявить весеннее снижение работоспособности, частые болезни, после которых возможны кровоточивость дёсен и потемнение мочи. Такие пациенты хуже, чем раньше, переносят длительные физические и нервно-психические нагрузки.
Желтухи и выраженного увеличения билирубина, за исключением периода интеркурентного острого гепатита, нет. Неяркая телеангиоэктазия кожи (сосудистые звёздочки) в области грудной клетки наблюдаются у 40-60% людей с ЦП.
Телеангиоэктазии кожи, плотная печень с фестончатым краем и умеренно увеличенная селезёнка — ценная клинико-диагностическая триада, которая с вероятностью 80-90% свидетельствует о ЦП или далеко зашедшем активном хроническом гепатите.
Патогенез цирроза печени
В основе патофизиологии цирроза лежит повреждение и некроз паренхимы (основной ткани) печени с деструкцией и гибелью гепатоцитов (клеток печени), а также системное поражение интерстициальной ткани.
При всех формах ЦП нарушается иммунологическое равновесие организма, преобладающими становятся аутоиммунные процессы: иммунная система человека принимает собственные клетки печени за чужеродные и повреждает их. В конечном итоге, это приводит к разрушению гепатоцитов и структуры печени в целом. Однако при этом каждая форма ЦП имеет свои патогенетические особенности:
- при вирусных гепатитах повреждающим агентом является сама вирусная частица, которая, размножаясь в клетке, разрушает её, вызывая цитолиз;
- при алкогольном ЦП прямое токсическое воздействие на мембраны гепатоцитов оказывает ацетальдегид с развитием алкогольной жировой болезни печени и алкогольного стеатогепатита;
- при метаболическом ЦП ведущую роль в патогенезе играет ожирение и сахарный диабет через стадию неалкогольного стеатогепатита с инсулинорезистентностью и последующей запрограммированной гибелью клеток печени.
В основе патогенеза более редких причин цирроза печени лежат ещё более частные механизмы развития повреждения и разрушения гепатоцитов и структуры печени:
- нарушение обмена и накопления железа при гемохроматозе;
- накопление меди при болезни Вильсона — Коновалова;
- окклюзия в системе воротной вены при гепатопортальном склерозе.
Цирроз формируется на протяжении многих лет. С течением времени происходят изменения генетического аппарата клеток печени, в результате чего появляются новые патологические клетки. Этот процесс в печени является иммуновоспалительным, он поддерживается чужеродными агентами, в роли которых могут выступать разные субстраты:
- вирус гепатита В;
- алкогольный гиалин;
- денатурированные белки;
- некоторые лекарственные средства;
- медьбелковые и железобелковые комплексы (ферритин).
В итоге повреждения паренхимы печени развивается гепатоцеллюлярная (печёночно-клеточная) недостаточность за счёт диффузного фиброза и трансформации ткани печени в анормальные узлы-регенераты. [3] [4] [5]
Классификация и стадии развития цирроза печени
В 1974 году на съезде гепатологов в Акапулько (Мексика) была принята единая морфологическая классификация, которую позже уточнили и несколько доработали эксперты ВОЗ. В настоящее время она является общепринятой.
Читайте также:

