При помощи чего вычисляется эозинофилов при токсокарозе
Обновлено: 24.04.2024
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут бы
Токсокароз — паразитарное заболевание, вызываемое миграцией личинок аскарид животных семейства псовых (T. canis ). Характеризуется длительным рецидивирующим течением и полиорганными поражениями иммунологической природы. Возбудителями токсокароза могут быть также личинки других аскарид — кошки (T. mystax), коровы, буйвола, (T. vitulorum). Однако роль этих возбудителей в патологии человека практически не изучена
Половозрелые формы T. canis — крупные раздельнополые черви длиной 4 — 18 см локализуются в желудке и тонком кишечнике животных (собак). Интенсивность инвазии у собак может быть очень высокой, особенно у молодых животных. Средняя продолжительность жизни половозрелых особей составляет 4 месяца, максимальная — 6 месяцев. Самка паразита за сутки откладывает более 200 тыс. яиц. В 1 г фекалий может содержаться 10 000—15 000 яиц, так что в почву попадают миллионы яиц, обусловливая тем самым высокий риск заражения токсокарозом.
 |
Яйца токсокар округлой формы, крупнее яиц аскариды (65—75 мкм). Наружная оболочка яйца толстая, плотная, мелкобугристая. Внутри яйца располагается темный бластомер.
Цикл развития возбудителя следующий. Выделившиеся яйца токсокар попадают в почву, где, в зависимости от влажности и температуры почвы, созревают за 5—36 суток, становясь инвазионными. Инвазионность яиц сохраняется в почве длительное время, в компосте — несколько лет.
Жизненный цикл токсокары сложный. Выделяют основной цикл и два варианта вспомогательных. Основной цикл происходит по схеме: окончательный хозяин (псовые) — почва — окончательный хозяин (псовые). Передача инвазии осуществляется геооральным путем. Вспомогательный цикл (вариант 1) идет трансплацентарно, в этом случае паразит в личиночной стадии переходит от беременной самки к плоду, в организме которого совершает полную миграцию, достигая в кишечнике щенка половозрелой стадии. Инвазированный щенок становится функционально полноценным окончательным хозяином, источником инвазии.
Вспомогательный цикл (вариант 2) осуществляется по цепи: окончательный хозяин (псовые) — почва — паратенический хозяин. Паратеническим (резервуарным) хозяином могут быть грызуны, свиньи, овцы, птицы, земляные черви. Человек также выступает в роли паратенического хозяина, но не включается в цикл передачи инвазии, являясь для паразита биологическим тупиком. Дальнейшее развитие возбудителя происходит при условии, что паратенический хозяин будет съеден собакой или другим окончательным хозяином. Механизм передачи инвазии при этом варианте — геооральный — ксенотрофный.
В зависимости от возраста хозяина реализуются разные пути миграции личинок токсокар. У молодых животных (щенков до 5 недель) почти все личинки совершают полную миграцию с достижением половозрелых форм в кишечнике и выделением яиц во внешнюю среду. В организме взрослых животных большая часть личинок мигрирует в соматические ткани, где сохраняет жизнеспособность несколько лет. В период беременности и лактации у беременных сук возобновляется миграция личинок. Мигрирующие личинки через плаценту попадают в организм плода. Личинки остаются в печени пренатально инвазированных щенков до рождения, а после рождения личинки из печени мигрируют в легкие, трахею, глотку, пищевод и попадают в желудочно-кишечный тракт, где через 3—4 недели достигают половозрелой стадии и начинают выделять во внешнюю среду яйца. Кормящие суки могут передавать щенкам инвазию также через молоко.
У человека цикл развития возбудителя, его миграция осуществляется следующим образом. Из яиц токсокар, попавших в рот, затем в желудок и тонкий кишечник выходят личинки, которые через слизистую оболочку проникают в кровеносные сосуды и через систему воротной вены мигрируют в печень, где часть из них оседает, инцистируется или окружается воспалительными инфильтратами, образуя гранулемы. Часть личинок по системе печеночных вен проходит фильтр печени, попадает в правое сердце и через легочную артерию — в капиллярную сеть легких. В легких часть личинок также задерживается, а часть, пройдя фильтр легких, по большому кругу кровообращения заносится в различные органы, оседая в них. Личинки токсокар могут локализоваться в различных органах и тканях — почках, мышцах, щитовидной железе, головном мозге и др. В тканях личинки сохраняют жизнеспособность многие годы и периодически, под влиянием различных факторов, возобновляют миграцию, обусловливая рецидивы заболевания.
- Географическое распространение и эпидемиология
Токсокароз — широко распространенная инвазия, она регистрируется во многих странах. Показатели пораженности плотоядных являются высокими во всех странах мира. Средняя пораженность собак кишечным токсокарозом, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах у части животных достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз. Распространенность инвазии в различных регионах точно неизвестна, поскольку токсокароз не подлежит обязательной регистрации. Совершенно очевидно, что токсокароз имеет широкую геграфию распространения, и число больных значительно выше официально регистрируемых.
| Токсокароз широко распространен и регистрируется во многих странах. Средняя пораженность кишечным токсокарозом собак, обследованных на различных континентах, составляет свыше 15%, но в некоторых регионах достигает 93%. По данным сероэпидемиологических исследований, от 2 до 14% обследованных практически здоровых лиц в различных очагах токсокароза имеют положительные иммунологические реакции на токсокароз |
- Патогенез и патологическая анатомия
Патогенез токсокароза сложный и определяется комплексом механизмов в системе паразит — хозяин. В период миграции личинки травмируют кровеносные сосуды и ткани, вызывая геморрагии, некроз, воспалительные изменения. Ведущая роль принадлежит иммунологическим реакциям организма в ответ на инвазию. Экскреторно-секреторные антигены личинок оказывают сенсибилизирующее действие с развитием реакций немедленного и замедленного типов. При разрушении личинок в организм человека попадают соматические антигены личинок. Аллергические реакции проявляются отеками, кожной эритемой, увеличением резистентности дыхательных путей к вдыхаемому воздуху, что клинически выражается развитием приступов удушья. В аллергических реакциях принимают участие тучные клетки, базофилы, нейтрофилы, но основную роль играют эозинофилы. Пролиферация эозинофилов регулируется Т-лимфоцитами при участии медиаторов воспалительных реакций, выделяемых сенсибилизированными лимфоцитами, нейтрофилами, базофилами. Образующиеся иммунные комплексы привлекают в очаг поражения эозинофилы. Вокруг личинок токсокар кумулируются сенсибилизированные Т-лимфоциты, привлекаются макрофаги и другие клетки — формируется паразитарная гранулома.
Патоморфологическим субстратом токсокароза является выраженное в различной степени гранулематозное поражение тканей. При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими. При токсокарозе находят многочисленные гранулемы в печени, легких, поджелудочной железе, миокарде, лимфатических узлах, головном мозге и других органах.
Наиболее характерным лабораторным показателем является повышенное содержание эозинофилов в периферической крови. Относительный уровень эозинофилии может колебаться в широких пределах, достигая в ряде случаев 70 — 80% и более. Повышается содержание лейкоцитов (от 20х109 до 30х109 на 1 л). При исследовании пунктата костного мозга выявляется гиперплазия зрелых эозинофилов. У детей нередко отмечается умеренная анемия. Некоторые исследователи отмечают прямую корреляцию между тяжестью клинических проявлений инвазии и уровнем эозинофилии и гиперлейкоцитоза периферической крови. Характерным лабораторным признаком является также ускорение СОЭ, гипергаммаглобулинемия. В случаях поражения печени наблюдается повышение билирубина, гиперферментемия.
В хронической стадии болезни острые клинические и лабораторные признаки затухают. Наиболее стабильным лабораторным показателем остается гиперэозинофилия периферической крови.
Выделяют субклиническое, легкое, среднетяжелое и тяжелое течение токсокароза. Возможна так называемая бессимптомная эозинофилия крови, когда явные клинические проявления инвазии отсутствуют, но наряду с гиперэозинофилией выявляются антитела к антигенам T.canis.
Одной из наиболее серьезных проблем, связанных с токсокарозом, является его взаимосвязь с бронхиальной астмой. При сероэпидемиологических исследованиях установлено, что у больных бронхиальной астмой нередко обнаруживаются антитела к антигенам T.canis классов Ig G и Ig E. В зависимости от остроты паразитарного процесса, его длительности и длительности клинических проявлений бронхиальной астмы преобладает тот или другой класс иммуноглобулинов. Имеются клинические наблюдения, свидетельствующие об улучшении течения бронхиальной астмы или выздоровлении после ликвидации токсокарозной инвазии.
Паразитологический диагноз устанавливается редко и только по наличию в тканях характерных гранулем и личинок и их идентификации при исследовании биопсийного и секционного материала. Это возможно при пункционной биопсии печени, легких, оперативном вмешательстве. Обычно диагноз токсокароза устанавливается на основании данных эпидемиологического анамнеза, клинической симптоматики и гематологических проявлений. Используют также иммунологические реакции, позволяющие выявлять антитела к антигенам токсокар. Обычно применяют ИФА с секреторно-экскреторным антигеном личинок токсокар второго возраста. В настоящее время в России выпускается коммерческий диагностикум. Диагностическим титром считают титр антител 1:400 и выше (в ИФА). Титр антител 1:400 свидетельствует об инвазированности, но не болезни. Титр антител 1:800 и выше свидетельствует о заболевании токсокарозом. Практика показывает, что прямая корреляция между уровнем антител и тяжестью клинических проявлений токсокароза существует не всегда. Не всегда имеется и корреляция между уровнем антител и гиперэозинофилии крови.
При постановке диагноза и определении показаний к специфической терапии следует учитывать, что токсокароз протекает циклически с рецидивами и ремиссиями, в связи с чем возможны значительные колебания клинических, гематологических и иммунологических показателей у одного и того же больного.
М. И. Алексеева и соавт. (1984) разработали алгоритм диагностики токсокароза, основанный на оценках в баллах значимости клинических симптомов и сопоставлении клинико-эпидемиологических и лабораторных показателей. Этот метод может быть перспективен при проведении массовых обследований населения.
Дифференциальный диагноз проводят с миграционной стадией других гельминтозов (аскаридоз, описторхоз), стронгилоидозом, эозинофильной гранулемой, лимфогранулематозом, эозинофильным васкулитом, метастазирующей аденомой поджелудочной железы, гипернефромой и другими заболеваниями, сопровождающимися повышенным содержанием эозинофилов в периферической крови. Следует иметь в виду, что у больных с системными лимфопролиферативными заболеваниями и серьезными нарушениями в системе иммунитета иммунологические реакции могут быть ложно положительными. В этих случаях необходим тщательный анализ клинической картины заболевания.
| При интенсивной инвазии развиваются тяжелые гранулематозные поражения многих органов и систем, которые при повторных заражениях могут стать хроническими |
Глазной токсокароз. Патогенез этой формы токсокароза до конца не ясен. Существует гипотеза об избирательном поражении глаз у лиц с инвазией низкой интенсивности, при которой не развивается достаточно выраженная иммунная реакция организма из-за слабого антигенного воздействия небольшого числа поступивших в организм личинок токсокар.
Эта форма токсокароза чаще наблюдается у детей и подростков, хотя описаны случаи заболевания и у взрослых.
Для токсокароза характерно одностороннее поражение глаз. Патологический процесс развивается в сетчатке, поражается хрусталик, иногда параорбитальная клетчатка. В тканях глаза формируется воспалительная реакция гранулематозного характера. Патологический процесс часто принимают за ретинобластому, проводят энуклеацию глаза. При морфологическом исследовании обнаруживают эозинофильные гранулемы, иногда — личинки токсокар.
Клинически поражение глаз протекает как хронический эндофтальмит, хориоретинит, иридоциклит, кератит, папиллит. Глазной токсокароз — одна из частых причин потери зрения.
Диагностика глазного токсокароза сложна. Количество эозинофилов обычно нормальное или незначительно повышено. Специфические антитела не выявляются или выявляются в низких титрах.
Разработано недостаточно. Применяют противонематодозные препараты — тиабендазол (минтезол), мебендазол (вермокс), медамин, диэтилкарбамазин. Эти препараты эффективны в отношении мигрирующих личинок и недостаточно эффективны в отношении тканевых форм, находящихся в гранулемах внутренних органов.
Минтезол (тиабендазол) назначают в дозах 25—50 мг/кг массы тела в сутки в три приема в течение 5—10 дней. Побочные явления возникают часто и проявляются тошнотой, головной болью, болями в животе, чувством отвращения к препарату (в настоящее время препарат в аптечную сеть России не поступает).
Вермокс (мебендазол) назначают по 200 —300 мг в сутки в течение 1—4 недель. Побочные реакции обычно не наблюдаются.
 |
Медамин применяют в дозе 10 мг/кг массы тела в сутки повторными циклами по 10 — 14 дней.
Диэтилкарбамазин назначают в дозах 2 — 6 мг/кг массы тела в сутки в течение 2 — 4 недель. (В настоящее время препарат в России не производится, не закупается за рубежом. — Прим. ред.)
Альбендазол назначают в дозе 10 мг/кг массы тела в сутки в два приема (утро — вечер) в течение 7 — 14 дней. В процессе лечения необходим контроль анализа крови (возможность развития агранулоцитоза) и уровня аминотрансфераз (гепатотоксическое действие препарата). Небольшое повышение уровня аминотрансфераз не является показанием к отмене препарата. В случае нарастающей гиперферментемии и угрозы развития токсического гепатита требуется отмена препарата.
Критерии эффективности лечения: улучшение общего состояния, постепенная регрессия клинических симптомов, снижение уровня эозинофилии и титров специфических антител. Следует отметить, что клинический эффект лечения опережает положительную динамику гематологических и иммунологических изменений. При рецидивах клинической симптоматики, стойкой эозинофилии и положительных иммунологических реакциях проводят повторные курсы лечения.
Прогноз для жизни благоприятный, однако при массивной инвазии и тяжелых полиорганных поражениях, особенно у лиц с нарушениями иммунитета, возможен летальный исход.
Включает соблюдение личной гигиены, обучение детей санитарным навыкам.
Важным профилактическим мероприятием является своевременное обследование и дегельминтизация собак. Наиболее эффективно преимагинальное лечение щенков в возрасте 4 — 5 недель, а также беременных сук. Для лечения собак используют противонематодозные препараты. Необходимо ограничение численности безнадзорных собак, оборудование специальных площадок для выгула собак.
Следует улучшить санитарно-просветительскую работу среди населения, давать информацию о возможных источниках инвазии и путях ее передачи. Особого внимания требуют лица, по роду деятельности имеющие контакты с источниками инвазии (ветеринарные работники, собаководы, землекопы и другие).
В последние годы на территории РФ, в том числе и в Астраханской области, отмечается увеличение числа случаев заражения человека различными инфекционными заболеваниями, как эндемичными, так и неэндемичными для данной территории. К эндемичным относят такие инфекции, как крымская геморрагическая лихорадка, астраханская риккетсиозная лихорадка, коксиеллез (лихорадка Ку) и многие другие [1, 2].
В мире более 2 млрд человек заражены гельминтами. По официальной статистике ВОЗ, причиной более 16 млн из 50 млн летальных исходов, которые ежегодно регистрируют в мире, являются паразитарные и инфекционные заболевания. В последнее время повсеместно увеличивается количество гельминтозов, которые раньше были редким явлением и регистрировались в спорадических случаях [3].
Несмотря на то, что санитарно-эпидемиологическая обстановка в целом по РФ в последние годы характеризуется как стабильная (не считая пандемии новой коронавирусной инфекции), паразитарные болезни продолжают занимать одно из ведущих мест в структуре инфекционной заболеваемости. Ежегодно в стране регистрируются сотни тысяч новых случаев паразитарных болезней. В их структуре особая роль принадлежит так называемым тканевым (ларвальным) гельминтозам, среди которых токсокароз до настоящего времени остается недостаточно изученным и трудно верифицируемым гельминтозом человека. Токсокароз является одним из наиболее часто встречающихся зоонозных гельминтозов в мире. В настоящее время он приобрел устойчивую социально-экономическую значимость и в нашей стране. С начала официальной регистрации (1991 г.) отмечен значительный рост уровня заболеваемости токсокарозом населения РФ, который колебался от 0,03 в 1991 г. до 1,72 на 100 тыс. населения в 2015 г. [4].
С точки зрения зоонозных инвазий, токсокароз является наиболее распространенным и важным для общественного здравоохранения паразитарным заболеванием [6]. Территории юга России характеризуются своеобразными природно-климатическими, экогеографическими и социально-экономическими условиями, определяющими поддержание активности очагов токсокароза. Высокая степень обсемененности яйцами Toxocara canis фекалий собак, значительная численность и плотность последних на селитебных территориях, контаминация почвы, сточных вод канализации и осадков, а также высокая доля жизнеспособных яиц Toxocara canis в объектах окружающей среды создают благоприятные условия для реализации путей передачи и широкого распространения инвазии на юге России [7].
Токсокароз характеризуется тяжелым, длительным и рецидивирующим течением, полиморфизмом клинических проявлений, обусловленных миграцией личинок токсокар в различные органы и ткани. Рост числа бродячих собак в городах, их высокая пораженность токсокарами, интенсивность экскреции яиц половозрелыми гельминтами, обитающими в кишечнике животных, устойчивость яиц во внешней среде являются определяющими факторами распространения инвазии среди людей [8].
Токсокароз – одна из наиболее часто регистрируемых зоонозных гельминтозных инвазий в мире с более высокой распространенностью в тропических регионах и среди сельского населения. Это вызвано личиночной стадией аскарид Toxocara canis, обыкновенного круглого червя собак, и, вероятно, также личиночной стадией Toxocara cati, аскариды кошек. Клинический спектр токсокароза у людей варьирует от бессимптомного течения до тяжелого повреждения органа, вызванного миграцией личинок в основные органы (висцеральная мигрирующая личинка) [9, 10].
Гельминтозы собак причиняют значительный экономический ущерб животноводству и представляют серьезную опасность для здоровья населения [11].
Токсокароз – зоонозное паразитарное заболевание, которое характеризуется попаданием (иначе – миграцией) и ходом вредоносной жизнедеятельности личинок круглых червей (токсокар) в организме человека с частотным поражением внутренних органов или систем. Человек заражается токсокарами при проглатывании яиц паразита вместе с пищей или водой, которые загрязнены испражнениями собак, либо при непосредственном контакте с инвазированными собаками. Опасность болезни усугубляется и тем, что самка токсокары способна за одни сутки отложить около 200 000 яиц. С кровотоком они попадают в ткани и органы носителя, а за сутки число отложенных яиц измеряется уже миллионами. При этом чаще всего заболевают именно дети 1-4 лет.
Протекает заболевание с аллергическими симптомами (зудящие высыпания, лихорадка, гепатоспленомегалия, бронхопневмония, приступы мучительного кашля, удушье, одутловатость лица, образование в органах гранулем, которые содержат личинки токсокар). Встречается токсокарозный офтальмит, при котором поражается задний сегмент глаза (хориоретинит), а также возникает кератит. Глазной токсокароз опасен необратимыми повреждениями глаз (абсцессы, мигрирующие личинки в стекловидном теле, потеря зрения). Болезнь может протекать от нескольких месяцев до нескольких лет. Актуальность исследования и лечения токсокароза связана с тем, что в наше время в связи с экономическими и политическими кризисами в разных странах планеты снижается уровень жизни людей, ухудшаются бытовые условия существования, не соблюдаются санитарно-гигиенические нормы. Токсокароз широко распространен в ряде регионов и стран, например, в Африке, Юго-Восточной Азии. Встречается он и в России, США, Европе. Болезнь в основном распространяется среди бродячих собак и кошек, которые являются пожизненными носителями личинок и выделяют в жилых массивах яйца гельминтов вместе с фекалиями. Показатель средней инфицированности среди собак и кошек – около 16%, но в ряде случаев может достигать и 90% [12, 13].
Токсокароз, вызванный инфицированием личинками Toxocara canis и, в меньшей степени, Toxocara cati и другими видами аскарид, проявляется у человека в виде ряда клинических синдромов. К ним относятся мигрирующие висцеральные и глазные личинки, нейротоксокароз и скрытый или общий токсокароз. Исследования по серологической распространенности показали, что это забытое заболевание особенно распространено среди детей из социально-экономически неблагополучных групп населения как в тропиках, так и в субтропиках, а также в промышленно развитых странах [14].
Увеличение популяций людей и собак, перемещение населения и изменение климата будут способствовать увеличению значимости этого зооноза [14].
Заражению токсокарами подвержены как домашние, так и дикие животные, выступающие чаще всего в качестве окончательных хозяев с различными путями передачи [15].
Паразитические нематоды из рода Toxocara являются социально-экономически важными зоонозными инвазиями. Эти паразиты обычно напрямую передаются человеку-хозяину фекально-оральным путем и могут вызывать токсокароз и связанные с ним осложнения, включая аллергические и неврологические расстройства [16].
В ряде субъектов РФ токсокароз практически не регистрируется на протяжении нескольких лет. Это связано не с благополучной санитарно-эпидемиологической обстановкой, а скорее с неудовлетворительной клинической и лабораторной диагностикой этой инвазии. Подтверждением тому служат многочисленные серо-эпидемиологические исследования населения, по результатам которых доля серопозитивных лиц колеб-лется от 5% до 46%. Широкое распространение токсокароза среди населения во многом зависит от проблемы несоблюдения правил содержания домашних собак, наличия большого количества бродячих животных, отсутствия мер по систематической контролируемой дезинвазии их экскрементов. В некоторых субъектах РФ пораженность собак токсокарозом составляет до 40% в городской и 80-100% в сельской местностях. Данные многочисленных санитарно-паразитологических исследований показывают, что контаминация почвы яйцами токсокар колеблется от 1-3% до 50-60% в разных регионах России, интенсивность загрязнения составляет от 1 до 10 яиц на 100 г почвы [4].
Возбудители токсокароза собак и кошек – Toxocara canis и Toxocara mistax способны в миграционной (ларвальной) стадии длительно паразитировать у человека, вызывая повреждение тканей внутренних органов и сенсибилизацию организма продуктами обмена личинок. Проблема токсокароза обусловлена, с одной стороны, высоким уровнем инвазированности собак, что связано с универсальным механизмом передачи возбудителя, с другой стороны – ростом численности собак и кошек, несоблюдением правил их содержания, отсутствием действенных мер по их дегельминтизации и дезинвазии почвы, что способствует широкой циркуляции возбудителя в природной среде [17].
По данным серологических и эпидемиологических исследований, от 1,5% до 14% обследованных практически здоровых людей имеют положительные иммунологические реакции на токсокароз. Человек способен заражаться круглогодично при попадании инвазионных яиц токсокар в кишечник через загрязненные яйцами почву, воду, продукты питания и руки. Возможно заражение человека через шерсть. Сам человек не является источником инвазии при токсокарозе, так как в его организме токсокары паразитируют в личиночной стадии, а не в половозрелой. В организме человека личинка возбудителя токсокароза способна выживать до 10 лет. Токсокароз протекает в острой, хронической и латентной форме. При латентном характере течения симптоматика отсутствует, а выявление гельминтоза возможно только по данным лабораторных анализов. Наиболее характерным лабораторным показателем является лейкемоидная реакция по эозинофильному типу с повышением эозинофилов от 30% до 90%. О заболевании свидетельствуют наличие клинических проявлений и титр специфических антител 1:800 и выше. Титр антител ниже 1:800 свидетельствует о носительстве, а титры 1:400 – о глазном токсокарозе при наличии патологического процесса в глазах [18].
Наиболее высокие уровни заболеваемости населения токсокарами отмечены в Уральском и Сибирском федеральных округах. Заболеваемость токсокарозом в целом по Южному федеральному округу ниже по сравнению с таковой в РФ, несмотря на высокую обсемененность возбудителем данного гельминтоза объектов среды обитания человека, значительную пораженность токсокарозом собак в округе (до 30%) и высокую серопревалентность населения (до 39%) [19].
Целью данного исследования было провести ретроспективный анализ заболеваемости населения Астраханской области токсокарами за 2012-2019 гг.
Материалы и методы исследования
Работа проводилась на базах кафедры инфекционных болезней и эпидемиологии ФГБОУ ВО Астраханский ГМУ Минздрава России, лаборатории бактериологических и паразитологических исследований и эпидемиологического отдела ФБУЗ ЦГиЭ в Астраханской области.
Всего за анализируемый период было изучено и обработано 48 эпидемиологических карт лиц, инвазированных токсокарами. Наибольшее число случаев токсокароза у людей зафиксировано в 2013 и 2017 гг., составив 20,8% (n = 10) и 25,0% (n = 12) соответственно (рис. 1).
Статистическая обработка результатов проводилась при помощи программы Microsoft Office Exel и BioStat Professional 5.8.4. Определяли процентное выражение ряда данных (%).
Результаты исследования
В большинстве случаев паразит регистрировался у женщин – 54,2% (n = 26).
Доля взрослых, которые были инвазированы токсокарами, составила 81,2% (n = 39), в том числе работающие граждане – 69,2% (n = 27), пенсионеры – 20,5% (n = 8) и безработные – 10,3% (n = 4).
Чаще всего токсокароз регистрировался у проживавших в городской местности – 70,8% (n = 34) (рис. 2).
Из городских районов наиболее часто токсокароз выявлялся у жителей Трусовского – 38,2% (n = 13) и Ленинского – 32,4% (n = 11) районов. Доля паразитарной контаминации населения, проживавшего в Кировском и Советском районах Астрахани, незначительна – 20,6% (n = 7) и 8,8% (n = 3) соответственно.
Больше всего зараженных токсокарами было среди жителей Икрянинского, Камызякского и Наримановского районов Астраханской области – 35,7% (n = 5), 28,6% (n = 4) и 21,4% (n = 3) соответственно. Спорадические случаи отмечались в Приволжском и Володарском районах области – по 7,1% (по n = 1) (рис. 3).
Предположить наличие данного заболевания и в дальнейшем провести соответствующие диагностические исследования заставили жалобы пациентов, выявленные при проведении ежегодных медицинских осмотров в 83,3% (n = 40) случаев, а также при непосредственном обращении за первичной медико-санитарной помощью в различные лечебно-профилактические учреждения Астрахани и ее области – 14,6% (n = 7), и у одного пациента (2,1%), проходившего как контактное лицо с заболевшим токсокарозом членом семьи.
В большинстве случаев паразитоз протекал в виде различных клинических проявлений и симптомов – 60,4% (n = 29) (табл. 1).
Так, из приведенной выше таблицы видно, что большая часть пациентов предъявляла жалобы на боль в области живота – 37,9% (n = 11), в том числе на боль в эпигастральной области – 27,6% (n = 8) и в правом подреберье – 10,3% (n = 3), общую слабость – 34,5% (n = 10) и кашель – 31,0% (n = 9).
Также отмечались жалобы на боль в суставах верхних конечностей – 10,3% (n = 3), частую утомляемость – 13,8% (n = 4), аллергический насморк, тошноту и незначительное повышение температуры – по 3,4% (по n = 3), отсутствие аппетита – 6,9% (n = 2). В редких случаях пациенты предъявляли жалобы на вздутие живота, крапивницу, чувство удушья в ночное время, незначительное снижение веса и расслоение ногтей – по 3,4% (по n = 1).
Почти у половины больных – 39,6% (n = 19) наблюдалось бессимптомное течение токсокароза. Собранный эпидемиологический анамнез показал, что большая часть инвазированных – 91,7% (n = 44) не соблюдала правила личной гигиены (употребляли в пищу грязные немытые фрукты и овощи – 89,6% (n = 43), не мыли руки перед едой – 16,7% (n = 8), контактировали с недегельминтизированными животными – 58,4% (n = 28): собаками – 43,8% (n = 21), в том числе домашними – 90,5% (n = 19), кошками – 14,6% (n = 7), в том числе домашними – 85,7% (n = 6). Склонность к геофагии (поеданию почвы) отмечалась у 68,8% (n = 33) инвазированных. А привычка грызть ногти на руках и ногах (онихофагия) зафиксирована у 18,8% (n = 9) детей.
Продолжительность заболевания от появления первых клинических признаков до установления окончательного диагноза составляла от нескольких дней до 2 лет (табл. 2).
Чаще всего длительность клинического течения составляла несколько дней – 29,2% (n = 14). В редких случаях длительность заболевания составляла 2 недели и 1 месяц – 14,6% (n = 7) и 18,8% (n = 9) соответственно.
После установления окончательного диагноза все пациенты проходили курс химиотерапии препаратом албендазол (10 мг/кг/сутки от 7 до 14 дней) в сочетании с антигистаминными и симптоматическими средствами.
После окончания курса лечения проводился контроль его эффективности (все пациенты были обследованы методом ИФА, табл. 3).
Как видно из приведенной выше таблицы, после курса химиотерапии титр антител стал снижаться: через 3 месяца после лечения он уменьшился незначительно только у двух пациентов – 4,2%. Спустя еще 3 месяца (6 месяцев после курса лечения) титр антител снизился до нулевых цифр почти у половины больных – 45,8% (n = 22). А еще через 6 месяцев (12 месяцев после окончания химиотерапии) титр антител снизился до нуля у всех пациентов.
Клинически висцеральный токсокароз проявляется поражением внутренних органов с различными аллергическими проявлениями. У наших пациентов отмечались общая слабость – 34,5%, боль в эпигастральной области – 27,6% и кашель – 31,0%. В редких случаях больные жаловались на утомляемость – 13,8%, боль в области правого подреберья и в суставах верхних конечностей, повышение температуры до субфебрильных цифр и аллергический насморк – по 10,3%, а также отсутствие аппетита – 6,9%, крапивницу, чувство удушья ночью, снижение веса, расслоение ногтей и вздутие живота – по 3,4%.
В то же время зарубежные авторы [20] отмечают, что, по их наблюдениям, при висцеральном токсокарозе чаще отмечались головная боль и продолжительный кашель – по 33,0%, гепатомегалия, головокружение, боли в животе и кожный зуд – от 20,0% до 10,0%. В редких случаях наблюдались астения и потеря веса.
Если рассматривать симптоматику токсокароза, выявленную российскими авторами [8], то она напоминает симптомы, обнаруженные нами.
Недостатком нашего исследования явилась невозможность наблюдения за лицами с токсокарозом, связанным с другими паразитозами.
Выводы
- Высокий уровень зараженности жителей Ленинского и Трусовского районов Астрахани связан с высокой плотностью населения и преобладанием домовладений частного сектора, в котором находятся домашние животные (кошки и собаки).
- Предположительно основными причинами заражения человека токсокарами стали несоблюдение правил личной гигиены, употребление в пищу плохо вымытых фруктов и овощей, контакт с животными и геофагия.
- Ведущую роль в диагностике токсокароза человека играет серологическое исследование – ИФА с титрованием.
- Титр антител к антигенам токсокар выше разведения 1:800 свидетельствует о заболевании обследуемого висцеральным токсокарозом.
- Снижение титра антител до нулевых значений после курса химиотерапии свидетельствует об эффективности лечения пациентов на 100%.
КОНФЛИКТ ИНТЕРЕСОВ. Авторы статьи подтвердили отсутствие конфликта интересов, о котором необходимо сообщить.
CONFLICT OF INTERESTS. Not declared.
Литература/References
1 ФГБОУ ВО Астраханский ГМУ Минздрава России; 414000, Россия, Астрахань, ул. Бакинская, 121
2 ГБУЗ АО КРД им. Ю. А. Пасхаловой; 414024, Россия, Астрахань, ул. Ахшарумова, 82
3 ГБУЗ АО ДГП № 3; 414041, Россия, Астрахань, ул. Куликова, 61
4 ФБУЗ ЦГиЭ в Астраханской области; 414057, Россия, Астрахань, ул. Н. Островского, 138
Сведения об авторах:
Information about the authors:
Toxocara canis — глист, не характерный для человека, но от этого не менее опасный. Взрослые особи паразитируют у собак и других псовых, а вот личинки настолько вредят своему случайному хозяину, что иногда несут угрозу для его жизни. У взрослых токсокароз — явление редкое, чего нельзя сказать о детях, которые чаще контактируют с почвой и домашними животными. Рассмотрим формы гельминтоза, симптоматику, лечение народными средствами и аптечными препаратами, меры профилактики и возможные осложнения.

Что такое токсокароз
Токсокароз — это заболевание с разнообразной симптоматикой, тяжёлым хроническим течением, иммунносупрессирующим эффектом и полиорганным поражением.
Возбудитель является раздельнополым гельминтом, представителем типа круглых червей (нематод). Похож на аскариду, но отличается широкими боковыми крыльями на головной части. Женские особи длиной до 18 см, мужские не более 10 см. Самки чрезвычайно плодовиты, в сутки каждая откладывает до 200 тысяч яиц. Из-за собак ими обсеменены детские площадки, придомовые участки, скверы и парки.
Живут гельминты от 4 до 6 месяцев. Яйца токсокар достигают инвазионной стадии, спустя 6—36 дней. В помещении не погибают в течение года. Во время внутриутробного развития и в период лактации токсокарами заражаются все щенки.
У личинок паразитов высокая антигенная чужеродность. Они вызывают аллергические реакции общего и местного характера. Формирование многочисленных эозинофильных гранулём сопровождается механическим и токсическим воздействием на ряд органов:
- Лимфоузлы.
- Скелетная мускулатура.
- Щитовидная и поджелудочная железы.
- Лёгкие.
- Почки.
- Миокард.
- Печень.
Реже личинки поражают головной мозг и глаза. Остаются жизнеспособными на протяжении нескольких лет. При активизации некоторой их части возобновляются миграционные процессы. Остальные покрываются фиброзной капсулой и со временем саморазрушаются.
Случаи повторного заражения приводят к увеличению численности гранулём и токсокароз переходит в более длительную и тяжёлую форму. Миграция личинок может растянуться на месяцы. В этот период они успевают травмировать капиллярную сеть, провоцировать геморрагии, воспаление и некроз тканей.
Методы заражения
Человек становится хозяином нематод при общении с собаками, на шерсти которых много яиц. Заразиться можно также через воду или почву с фекалиями псовых.
В пищеварительном канале оболочка растворяется, и выходят личинки. Оказавшись в организме человека, они кровью разносятся по всем его тканям. Для токсокар наступает экологический тупик, так как на этом дальнейшее их развитие заканчивается. В группу риска входят представители следующих специальностей:
- Ветеринары.
- Шофёры.
- Охотники.
- Фермеры.
- Хозяева приусадебных или дачных участков.
Пик заражений — тёплое время года, когда температура и влажность способствуют быстрому созреванию личинок, а взрослые и дети чаще контактируют с землёй.
Формы заболевания
У человека симптомы токсокароза зависят от его течения, которое может быть лёгким или тяжёлым, острым или хроническим продолжительностью от 0,5 до 2 лет.
Симптоматика токсокароза
Способность поражать многие органы лежит в основе классификации, согласно которой различают три формы токсокароза.
Висцеральный

Паразит на ноге под кожей у человека
Вид, который развивается при масштабном заражении. В 60% случаев больной страдает от рецидивирующей лихорадки. Возможно поражение лёгких с цианозом, одышкой, приступообразным кашлем с астматическим компонентом. У лиц с наследственной предрасположенностью к аллергии на коже появляются:
- Экземы.
- Дерматиты.
- Крапивница.
- Отёк Квинке.
Покраснения и сопровождающий их зуд перемещаются вместе с мигрирующими личинками. А также каждый четвёртый заражённый токсокарами страдает от поноса, тошноты, рвоты, вздутия кишечника. Возможно увеличение размеров селезёнки, печени, развитие желтухи, панкреатита. Эозинофильные гранулёмы поражают мышцы, суставы, почки, миокард.
Неврологическая форма
Разновидность гельминтоза, которая развивается при проникновении паразитов в центральную нервную систему. При этом человека мучают упорные головные боли, беспокоят проблемы с речью и концентрацией внимания.
Глазной токсокароз

Так выглядит паразит в глазе у человека
Форма заболевания, при которой в заражении участвует небольшое число личинок. Из-за минимального антигенного воздействия глистов аллергическая реакция не развивается, гранулёмы не образуются, число эозинофилов тоже остаётся в пределах нормы. При этом паразиты токсокары свободно перемещаются по кровяному руслу и беспрепятственно оказываются в зрительном анализаторе с преимущественным поражением одного глаза. Такое состояние продолжается несколько месяцев. При этом возможны:
- Гнойное воспаление оболочек глазного яблока.
- Нарушения в работе сосудистого слоя.
- Периодически возникающие отёки.
- Односторонняя слепота из-за проблем со зрительным нервом.
- Кератит.
- Помутнение, изъязвления роговицы глаза.
Эозинофильная гранулёма образуется в районе сетчатки. Как следствие, зрение снижается, в ряде случаев полностью пропадает.
Точная диагностика, к какому врачу обратиться
Многочисленные и разнообразные признаки гельминтоза затрудняют процесс идентификации возбудителя. Токсокароз вызывает изменение ряда показателей крови:
- Повышенный уровень эозинофилов (до 30—90%).
- Лейкоцитоз.
- Высокое содержание гамма-глобулинов, обеспечивающих гуморальный иммунитет.
- Ускорение СОЭ.
- Превышение нормы печёночных проб и билирубина.
Высокочувствительный и специфичный иммуноферментный анализ позволяет выяснить форму, а также тяжесть течения заболевания. Данные представлены в таблице.
| Титры специфических антител | Возможный диагноз |
| 1:100 (200) | Инкапсулированные личинки. Лечение неэффективное. |
| 1:200(400) | Носительство. |
| Выше 1:400 | Активная форма гельминтоза. |
| От 1:800 | Висцеральный токсокароз, требующий немедленной терапии. |
В случае продолжительного течения глистной инвазии и проявлении глазной формы поражения возможны ложноположительные результаты иммунологического анализа. Эффективна также биопсия с определением гранулём и личинок глистов.
Трудно диагностировать глазную форму, так как число эозинофилов остаётся в пределах нормы, а специфических антител недостаточно или их нет. При этом для обнаружения личинок токсокары врач проводит офтальмологическое обследование.
Лечение токсокароза
Для гельминтоза характерно циклическое течение со сменой периодов ремиссии и обострений. Схема терапии зависит от формы заболевания. Использование противопаразитарных препаратов эффективно в период миграции личинок, слабее против гранулём и совсем бесполезно при инкапсулировании паразитов.
Обязательным элементом комплексного подхода является проведение симптоматического лечения, так как под ударом глистов оказываются многие системы органов:
- Гепатопротекторы показаны при нарушении работы печени.
- Антибиотики, отхаркивающие составы, бронхолитики при поражении дыхательной системы.
- Антигистамины при развитии аллергических реакций.
- Для мощного противовоспалительного эффекта показан приём нестероидных составов.
- Глюкокортикоиды помогают при тяжёлом течении токсокароза с поражением головного мозга, сердца, лёгких.
Об эффективности антигельминтной терапии судят по следующим признакам:
- Низкие титры антител.
- Снижение уровня эозинофилов.
- Постепенная нормализация гемато- и иммунологических показателей.
- Исчезновение симптомов гельминтоза.
- Улучшение общего состояния.
При глазной форме показаны субконъюнктивальные инъекции Депо-медрола. При необходимости применяют микрохирургические методы, удаляющие гранулёмы внутри зрительного анализатора. Для разрушения личинок используют лазерокоагуляцию.
В течение полугода после выздоровления пациенты остаются под диспансерным наблюдением. Врачебный осмотр и обследование проводятся 1 раз в 2 месяца. Больных снимают с учёта, если результаты двух ИФА, проведённых с интервалом в 90 дней, окажутся отрицательными.
Медикаменты, курс лечения
В терапии токсокароза применяются следующие антигельминтные средства:
- Саноксал, Немозол с альбендазолом в качестве действующего вещества (ДВ). Продолжительность лечения составляет 1—2 недели. Возможны побочные эффекты при массовой гибели личинок. Во избежание аллергии врач назначает параллельный приём антигистаминов. Один раз в неделю пациент сдаёт печёночные пробы и кровь для общего анализа.
- Вермокс, Вормин с мебендазолом (ДВ). Препараты отличаются хорошей переносимостью. Не оказывают побочного действия. Показаны даже детям от 2 лет. Схема лечения для взрослых: 300 мг за 2 приёма. Курс от 10 до 14 дней с повтором через 2 недели.
Лечение может повторяться до пяти раз, если имеют место:
- Стойкая эозинофилия.
- Высокий титр специфических антител.
- Рецидивы гельминтоза.
Врач исходит из индивидуальных особенностей каждого пациента, учитывает результаты лабораторных анализов и клинические данные, так как единая схема лечения токсокароза не разработана.
Народные средства

Нетрадиционные методы терапии применяются после подтверждения диагноза и консультации врача. Иногда они единственно возможный вариант, позволяющий избавить от паразитов детей и беременных женщин. При отсутствии результатов, резком ухудшении состояния больного, выраженной аллергической реакции понадобится срочное обращение в медицинское учреждение.
К эффективным рецептам народной медицины относятся:
- Отвар коры ясеня, обладающий противогельминтным, антимикробным действием. Требует осторожного применения.
- Полынь и пижма — растения, содержащие натуральные горечи и обладающие желчегонными свойствами. Для отвара берут 2 ст. л. измельчённых листьев одного из растений, заливают 250 мл кипятка, после настаивания процеживают. Схема приёма настоя пижмы: 4 раза по 2 ч. л. Курс лечения — 4 дня. Отвар полыни можно пить на протяжении 2 недель 3 раза в сутки до еды.
- Настой из листьев заячьей капусты или кислицы обыкновенной. Готовится из 1 ст. л. растительного сырья и стакана кипятка. Спустя 2 часа состав можно принимать по 2 ст. л. Курс лечения 7 дней с повтором через неделю.
- Отвар девясила помогает при различных видах глистных инвазий. Готовится из горсти измельчённой зелёной массы и 250 мл горячей воды. Настаивать ночь. Пить в течение недели по 2 ст. л. 4 раза в день. Курс повторять до полного выздоровления.
- Сырые тыквенные семена (4 ст. л.) съедать натощак, затем принимать слабительное.
- Спиртовая настойка лука. Настаивать 9 дней. Пить 2 раза по 15 мл.
- Десять зубчиков свежего чеснока в сутки.
Для клизм готовят:
- Настой, включающий золототысячник, облепиху, шалфей (по 4 ст. л.), залить 1 л кипячёной воды. Выдержать ночь, после использовать для очистки кишечника от глистов.
- Средство из 1 ст. л. пижмы и 250 мл кипятка.
- Отвар из головки чеснока и стакана молока. Использовать сразу после остывания.
Длительное применение клизм противопоказано из-за негативного влияния на перистальтику кишечника, состояние слизистых оболочек. Частота процедур: максимум 1 раз в неделю.
Лечение детей
Терапия токсокароза подразумевает приём антигельминтных препаратов, таких как Вермокс. Многие противопаразитарные составы обладают побочным действием, поэтому принимаются под наблюдением врача. Он же назначает гепатопротекторы, а также составы, нормализующие баланс полезных бактерий.
Лечение токсокароза у детей может растянуться на длительный срок, иногда на 3 года и включать до 5—6 курсов антигельминтной терапии. Увеличивать дозировки категорически запрещено, поэтому приходится удлинять сроки воздействия лекарств. В течение последующих после выздоровления 3 лет проводится контроль эффективности проведённых терапевтических мероприятий.
Профилактика
Предотвратить гельминтоз можно, выполняя ряд рекомендаций общегигиенического характера:
- Тщательное мытьё рук перед едой, а также зелени, овощей, фруктов.
- Обучение детей правилам личной гигиены.
- Постоянная борьба с тараканами, переносящими яйца паразитов.
- Регулярная (не менее 2 раз в год) дегельминтизация собак.
- Учёт численности беспризорных животных.
Защита детских площадок, а также скверов от паразитов выгуливанием домашних питомцев в специальных отведённых для этой цели местах.
Возможные осложнения
Глазной токсокароз приводит к следующим последствиям:
- Катаракта.
- Фиброз.
- Отслоение сетчатой оболочки.
- Белый зрачок.
- Косоглазие.
В тяжёлых случаях неврологической формы возможны:
- Приступы эпилепсии.
- Психические расстройства.
- Параличи, парезы.
Заключение врача
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Эозинофилия: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Эозинофилия – это состояние, при котором отмечается повышение уровня эозинофилов в крови. Эозинофилы представляют собой один из видов белых клеток крови – лейкоцитов, образуются в костном мозге, откуда попадают в кровоток. Повышение их количества отмечается при паразитарных и аллергических заболеваниях, туберкулезе, инфекционных процессах и некоторых других состояниях и заболеваниях, требующих полноценного обследования и специфической терапии.
Разновидности эозинофилии
По количеству клеток в единице крови различают следующие эозинофилии:
- легкая, когда содержание эозинофилов составляет от 500 до 1500 в микролитре крови;
- умеренная, когда содержание эозинофилов составляет от 1500 до 5000 в микролитре крови;
- выраженная, когда содержание эозинофилов составляет более 5000 в микролитре крови.
- первичную, или клональную эозинофилию, которая наблюдается при патологиях крови;
- вторичную, или реактивную эозинофилию, которая развивается как ответная реакция на аллергены, паразитарные инвазии и т.д.
- идиопатическую, или транзиторную эозинофилию, причины которой выяснить не удается.
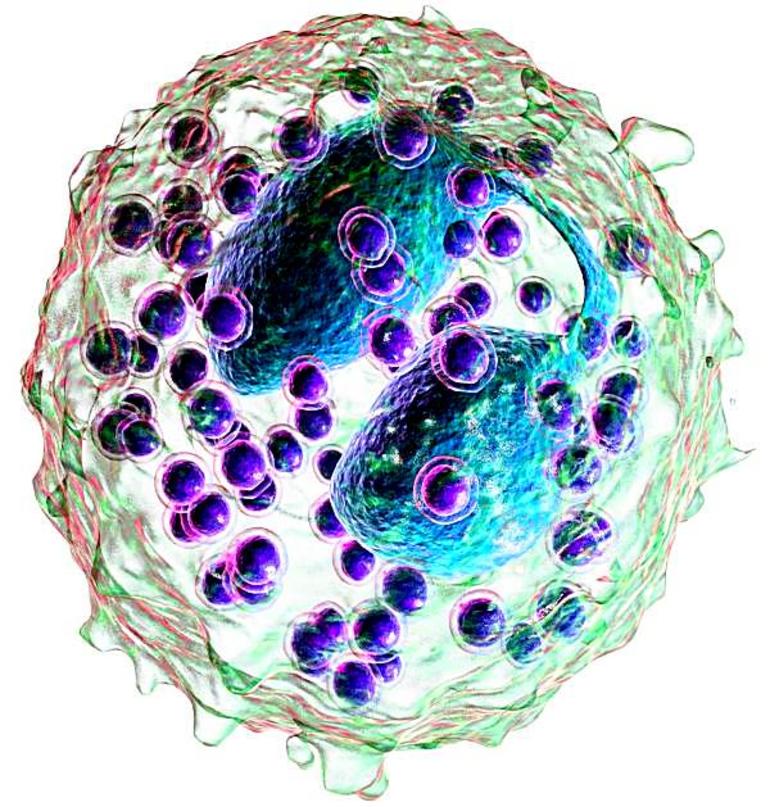
В наибольшей степени эозинофилы задействованы в иммунном ответе с выраженным аллергическим компонентом.
Аллергическая реакция является одной из форм ответа организма на проникновение извне чужеродных агентов (аллергенов).
Аллергеном может стать практически любое вещество, однако чаще в роли аллергена выступают белки. При первом попадании аллергена в организм клетки лимфоциты начинают вырабатывать особый вид антител IgE, играющих ключевую роль в развитии аллергической реакции при повторном контакте организма с данным аллергеном. Антитела активируют эозинофилы, приводя к их повышенному содержанию в крови.
Заболевания, при которых повышаются эозинофилы крови
Эозинофилия является характерным проявлением аллергических заболеваний и состояний, таких как:
- аллергический ринит и конъюнктивит;
- атопический дерматит;
- бронхиальная астма;
- пищевая аллергия и др.
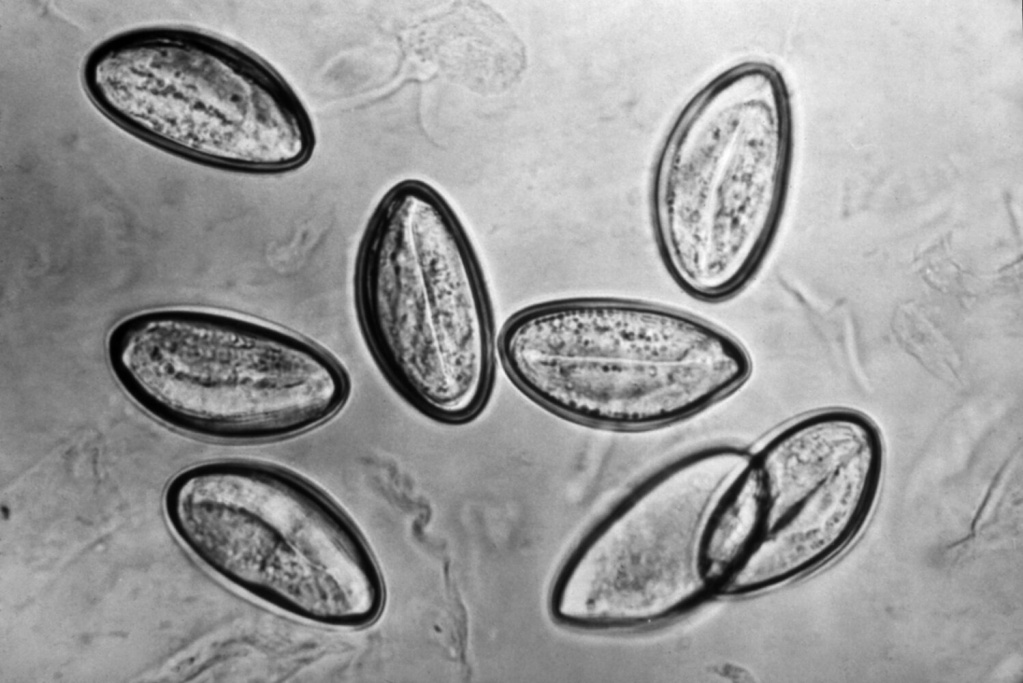
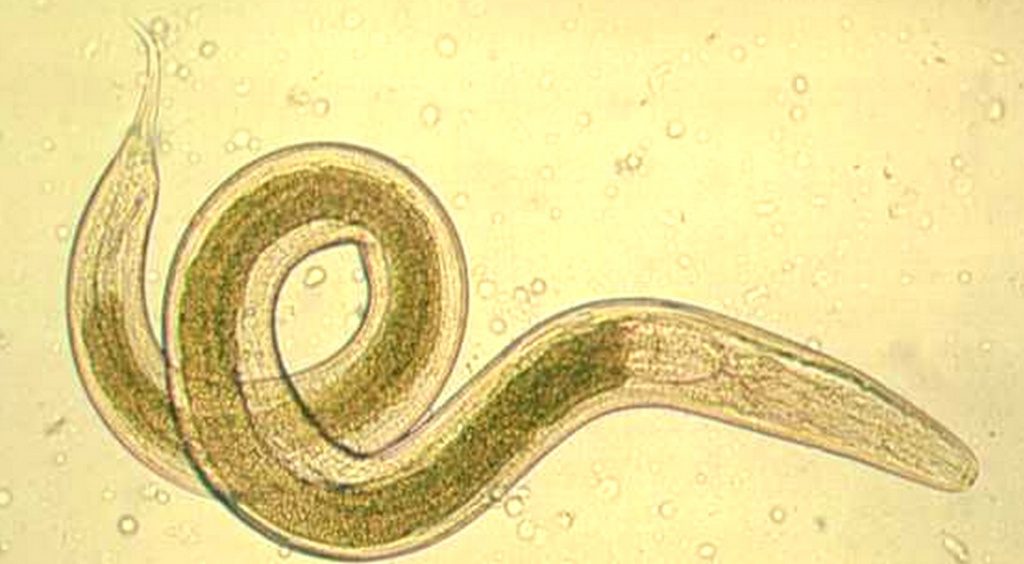
С одной стороны, эозинофилы обладают противопаразитарной активностью, за счет способности выделять эозинофильный катионный белок и активные формы кислорода, которые губительны для гельминтов. С другой стороны, продукты метаболизма гельминтов вызывают реакцию гиперчувствительности, для которой свойственны симптомы аллергии.
Следующая группа заболеваний, протекающих с повышением количества эозинофилов, - ревматологические патологии, или системные воспалительные заболевания соединительной ткани. Данные заболевания в абсолютном большинстве случаев являются аутоиммунными.
В основе аутоиммунных процессов лежит нарушение распознавания клетками иммунной системы собственных тканей, в результате чего они воспринимаются как чужеродные. Против них начинают вырабатываться антитела, и запускается воспалительный процесс.
Одним из аутоиммунных заболеваний, для которого характерна эозинофилия, является разновидность васкулита (воспаления сосудов) – эозинофильный гранулематоз с полиангиитом, или синдром Черджа–Стросса (воспаление мелких и средних кровеносных сосудов).
Эозинофилия может свидетельствовать о наличии в организме злокачественного процесса. Это связано с тем, что клетки злокачественных опухолей вырабатывают, среди прочего, вещества, стимулирующие образование эозинофилов. Так, эозинофилия является частым симптомом хронического миелолейкоза.
К каким врачам обращаться при эозинофилии
Эозинофилия не является самостоятельным заболеванием, но может быть признаком аллергических, аутоиммунных, инфекционных патологий.
Поэтому сначала можно обратиться к терапевту (врачу общей практики) или педиатру , если пациентом является ребенок. Зачастую данных, собранных в процессе опроса и клинического осмотра пациента, может оказаться достаточно для направления на прием к узкопрофильному специалисту. Так, при впервые выявленном аллергическом заболевании требуется консультация аллерголога-иммунолога, при гельминтозе - врача-инфекциониста, а при подозрении на аутоиммунный процесс – ревматолога.
Диагностика и обследование при эозинофилии
После тщательного сбора анамнеза и выявления ключевых фактов развития заболевания назначают лабораторные обследования.
Клинический анализ крови с определением лейкоцитарной формулы необходим для определения количества эозинофилов. В данном исследовании важно провести микроскопию мазка, которая позволяет не только достоверно подсчитать количество эозинофилов, но и выявить наличие в крови специфических клеток, характерных, например, для лейкоза и некоторых аутоиммунных заболеваний.
Синонимы: Общий анализ крови (ОАК); Гемограмма; КАК; Развернутый анализ крови. Full blood count; FBC; Complete Blood Count (CBC); Hemogram; CBC with White Blood Cell Differential Count; Peripheral Blood Smear; Blood Film Examination; Complete blood count (CBC) with differential white blood cell coun.
Читайте также:

