При развитии дыхательной недостаточности при сепсисе проводится
Обновлено: 25.04.2024
Сепсис. Первая помощь при сепсисе.
1. Клинические проявления сепсиса часто бывают очень неспецифичны, и поэтому для правильной диагностики необходимо в критических ситуациях не забывать о возможности развития септического состояния. Нарушения психики и гипервентиляция с дыхательным алкалозом являются важными признаками сепсиса, так как они появляются самыми первыми, часто до возникновения лихорадки и озноба. Лихорадка развивается не всегда; до 15% больных с сепсисом имеют нормальную или пониженную температуру. Если ранее была проведена катетеризация центральных сосудов для мониторинга гемодинамических показателей, ранними признаками септического состояния могут быть увеличение сердечного выброса, увеличение содержания кислорода в смешанной венозной крови либо снижение периферического сосудистого сопротивления.
При наличии кожных проявлений септического состояния следует выполнить скарификацию, окраску мазка по Граму и бактериологическое исследование; обнаружение возбудителя в мазке подтверждает диагноз сепсиса и помогает выбрать нужный антибиотик. Лейкоцитоз, если он имеется, может отражать динамику процесса, однако количество лейкоцитов при сепсисе нередко бывает нормальным или даже сниженным.
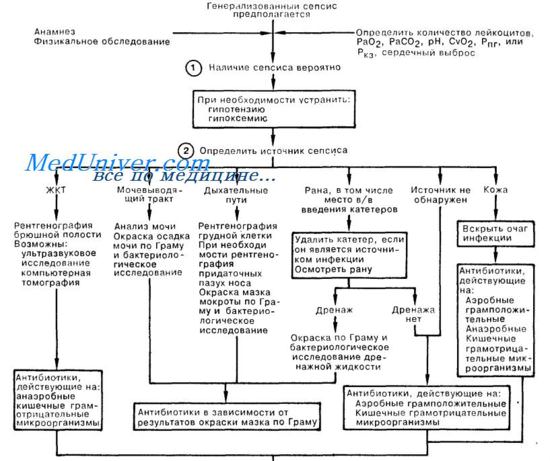
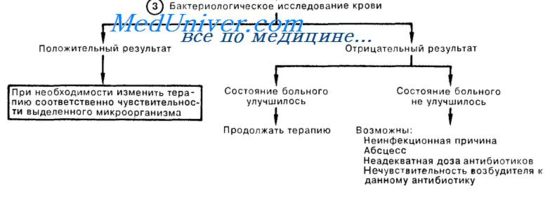
2. Выбор препарата для начальной антибиотикотерапии во многом зависит от локализации источника септицемии. Если источник удается обнаружить, а в дальнейшем удалить или дренировать (например, в/в катетер, хирургическая рана, абсцесс), результаты лечения улучшаются. Перед началом антибиотикотерапии забирают две пробы крови для бактериологического исследования; НЕ следует откладывать лечение для того, чтобы получить несколько гемокультур в течение большого промежутка времени. Приводящая к сепсису инфекция мочевых путей или дыхательного тракта обычно имеет выраженную клиническую картину, а возбудитель окрашивается по Граму. Нозокомиальный синусит у больных с установленным назотрахеальным воздуховодом или назогастральным зондом часто не учитываются в качестве возможной причины лихорадки и сепсиса в ОИТ. Инфекция операционной раны и флебит часто не зависят от наличия дренажа; лечение должно быть направлено против наиболее вероятных возбудителей — золотистого стафилококка и кишечных грамотрицательных микроорганизмов.
Абдоминальные инфекционные процессы обычно вызываются анаэробами (в том числе Bacteroides fragilis), а также грамотрицательными микроорганизмами (например, Е. coli, Klebsiella sp., Proteus sp.). Декубитальные язвы обычно инфицируются несколькими возбудителями, в том числе золотистым стафилококком, анаэробами, а также грамотрицательными палочками. У 25% больных с сепсисом не удается обнаружить источник инфекции; в этой ситуации показано назначение антибиотиков с широким спектром действия с активностью против как грамположительных, так и грамотрицательных микроорганизмов. Не могут считаться однозначными рекомендации вводить однократно большие дозы кортикостероидов (3 мг/кг дексаметазона или 30 мг/кг метилпреднизолона). Исследуется эффективность антагониста опиатов—налоксона для купирования шока.
3. При получении положительной гемокультуры обычно имеется возможность изменить терапию с учетом чувствительности изолированного микроорганизма. Если источник инфекции таков, что часто сопровождается полимикробной бактериемией (например, ЖКТ), следует продолжать введение препаратов широкого спектра действия. Если до начала анти-биотикотерапии было произведено лишь одно бактериологическое исследование крови, имеется примерно 20% вероятность ложноотрица-тельного результата вследствие перемежающегося характера бактериемии. Отрицательные результаты бактериологических исследований у больного с сепсисом могут отражать лишь эффективность начатой антибиотикотерапии и не должны приводить к немедленному отказу от проводимого лечения. При отсутствии положительной динамики в ответ на терапию показано дальнейшее исследование.
Мониторинг жизненно важных функций при сепсисе. Поддержание адекватного газообмена при сепсисе.
Больные с тяжелым сепсисом или септическим шоком должны быть транспортированы в ОРИТ, так как они нуждаются не только в проведении интенсивной терапии, но и динамическом мониторинге нарушенных витальных функций. Объем мониторинга зависит от возможностей ЛПУ и, как правило, включает неинвазивное определение систолического, диастолического, среднего артериального давления, ЧСС, пульса, частоты дыхания, сатурации крови, температуры тела.
Обеспечение надежного сосудистого доступа, достигаемое катетеризацией подключичной вены, непременно должно сопровождаться оценкой ЦВД, забором крови для посева на гемокультуру и лабораторных исследован™, включающих определение уровней гемоглобина, эритроцитов, лейкоцитов с подсчетом ЛИИ, гематокрита, общего белка и его фракций, глюкозы, трансаминаз, билирубина, азотемии. Обязательным являются также исследования состояния гомеостаза (коагуло-грамма), кислотно-основного равновесия, оценка уровня содержания электролитов в крови.
Мониторинг показателей центральной гемодинамики достигается выполнением интегральной реографии тела по М. И. Тищенко или катетеризацией легочной артерии катетером Свана-Ганца, что позволяет у больного с септическим шоком в динамике оценивать ударный объем и расчетным путем определять сердечный выброс (СВ), сердечньш индекс (СИ), общее периферическое сопротивление сосудов (ОПСС) и другие показатели, давление заклинивания легочных капилляров (ДЗЛК), О ЦК, оксигенацию смешанной венозной крови (Sv02).
Контроль темпа диуреза осуществляется путем установки в мочевом пузыре катетера Фолея.
Поддержание адекватного газообмена
Адекватная и своевременная респираторная поддержка - один из основополагающих компонентов терапии сепсиса и септического шока, позволяющий наряду с поддержанием кислородного транспорта и снижением работы дыхания, уменьшить скорость реакции цитокинового каскада.
Проведение оксигенотерапии требует тщательной санации трахеобронхиального дерева и обеспечения проходимости дыхательных путей. Если после эвакуации мокроты из трахеобронхиального дерева и устранения бронхообструкции признаки ОДН сохраняются, то это указывает на паренхиматозный характер ОДН и диктует необходимость дополнительных лечебных мероприятий.
Оксигенотерапия начинается с ингаляции увлажненного кислорода через носовые катетеры или лицевую маску, что позволяет довести Fi02 до 0,4-0,6.
Ингаляция 100% кислорода может осуществляться только непродолжительное время, так как высокие концентрации кислорода за счет токсического действия способствуют развитию респираторного дистресс-синдрома.
Нарушение сознания у больного, выраженное тахипноэ (более 40 в минуту) с участием вспомогательной мускулатуры, патологические ритмы дыхания являются показанием для интубации трахеи и перевода больного на управляемую ИВЛ. Клинические показания к переводу на ИВЛ должны быть дополнены инструментальными, к которым относятся рост Р(А-а)02 выше 350 мм рт. ст., уменьшение Ра02 ниже 70 мм рт. ст., снижение отношения Pa02/Fi02 менее 180 мм рт. ст., увеличение РаС02 более 50 мм рт. ст., полученные на фоне ингаляции 100% кислорода.
Следует обратить внимание на важность инструментальных показаний к ИВЛ у больных с септическим шоком, так как респираторная поддержка должна начинаться как можно раньше, до клинических проявлений нарушения равновесия между состоянием легочного газообмена и компенсаторными возможностями /организма, нарушение которых ведет к значительному ухудшению транспорта и потребления кислорода.
ИВЛ у больных септическим шоком проводится в режиме PEEP до 5-7 см H2О, Vt = 6,0-7,5 мл/кг и частотой дыхания до 16 в минуту. В случае развития респираторного дистресс-синдрома ИВЛ осуществляется в режиме "защиты легких": Vt = 4-6 мл/кг, PEEP - 10-15 см Н2О, Ppeak -менее 35 см Н2О, FiO2 менее 0,65, частота дыхания - 18 в минуту с тем, чтобы поддерживать РаС>2 на уровне не менее 80 мм рт. ст. и Sp02 не менее 90% Синхронизация больного с респиратором достигается внутривенным введением оксибутарата натрия в дозе 100-120 мг/кг.
Нормализацию кислородного потока в организме больного необходимо сочетать со снижением повреждающего Действия тканевой гипоксии. С этой целью используются антигипоксанты, которые либо снижают потребление кислорода, либо улучшают его утилизацию. Дозировки антигипоксантов представлены в таблице.
На адекватность респираторной поддержки у больных с септическим шоком указывает стабилизация пороговых значений кислородного потока в организме: SpO2 не менее 90%, доставка кислорода на уровне 570-600 мл/мин, потребление кислорода на уровне 170— 180 мл/мин при среднем артериальном давлении более 70-75 мм рт. ст., а также энергетическая стабилизация клеток организма, оцениваемая по снижению уровней лактата (до 2,0 ммоль/л), глюкозы (5,5-7,0 ммоль/л) и пирувата (до 30-40 Ед/л).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Септический шок – это тяжелое патологическое состояние, возникающее при массивном поступлении в кровь бактериальных эндотоксинов. Сопровождается тканевой гипоперфузией, критическим снижением артериального давления и симптомами полиорганной недостаточности. Диагноз ставится на основании общей клинической картины, сочетающей в себе признаки поражения легких, сердечно-сосудистой системы (ССС), печени и почек, централизации кровообращения. Лечение: массивная антибиотикотерапия, инфузия коллоидных и кристаллоидных растворов, поддержание деятельности ССС за счёт введения вазопрессоров, коррекция респираторных нарушений путем ИВЛ.
МКБ-10
Общие сведения
Септический шок (СШ) также называют инфекционно-токсическим (ИТШ). Как самостоятельная нозологическая единица патология впервые была описана в XIX веке, однако полноценное изучение с разработкой специфических противошоковых мер началось не более 25 лет назад. Может возникать при любом инфекционном процессе. Наиболее часто встречается у пациентов хирургических отделений, при менингококковой септицемии, брюшном тифе, сальмонеллезе и чуме. Распространен в странах, где диагностируется наибольшее количество бактериальных и паразитарных заболеваний (Африка, Афганистан, Индонезия). Ежегодно от ИТШ погибает более 500 тысяч человек по всему миру.

Причины
В абсолютном большинстве случаев патология развивается на фоне ослабления иммунных реакций. Это происходит у пациентов, страдающих хроническими тяжелыми заболеваниями, а также у людей пожилого возраста. В силу физиологических особенностей сепсис чаще диагностируется у мужчин. Список самых распространенных заболеваний, при которых могут возникать явления ИТШ, включает в себя:
- Очаги гнойной инфекции. Признаки системной воспалительной реакции и связанных с ней нарушений в работе внутренних органов отмечаются при наличии объемных абсцессов или флегмоны мягких тканей. Риск генерализованного токсического ответа повышается при длительном течении болезни, отсутствии адекватной антибактериальной терапии и возрасте пациента старше 60 лет.
- Длительное пребывание в ОРИТ. Госпитализация в отделение реанимации и интенсивной терапии всегда сопряжена с риском возникновения сепсиса и инфекционного шока. Это обусловлено постоянным контактом с резистентной к антибактериальным препаратам микрофлорой, ослаблением защитных сил организма в результате тяжёлой болезни, наличием множественных ворот инфекции: катетеров, желудочных зондов, дренажных трубок.
- Раны. Нарушения целостности кожных покровов, в том числе возникшие во время операции, существенно повышают риски инфицирования высококонтагиозной флорой. ИТШ начинается у больных с загрязненными ранами, не получивших своевременной помощи. Травматизация тканей в ходе оперативного вмешательства становится причиной генерализованной инфекции только при несоблюдении правил асептики и антисептики. В большинстве случаев септический шок возникает у пациентов, перенесших манипуляции на желудке и поджелудочной железе. Еще одна распространенная причина – разлитой перитонит.
- Приём иммунодепрессантов. Лекарственные средства, угнетающие иммунитет (меркаптопурин, кризанол), используются для подавления реакции отторжения после трансплантации органов. В меньшей степени уровень собственной защиты снижается при употреблении химиотерапевтических средств – цитостатиков, предназначенных для лечения онкологических заболеваний (доксорубицина, фторурацила).
- СПИД.ВИЧ-инфекция в стадии СПИДа приводит к развитию нетипичного сепсиса, спровоцированного не бактериальный культурой, а грибком рода Candida. Клинические проявления болезни характеризуется малой степенью выраженности. Отсутствие адекватного иммунного ответа позволяет патогенной флоре свободно размножаться.
Возбудитель сепсиса – грамположительные (стрептококки, стафилококки, энтерококки) и грамотрицательные (Enterobacter cloacae, Clostridium pneumoniae) бактерии. Во многих случаях культуры нечувствительны к антибиотикам, что затрудняет лечение пациентов. Септический шок вирусного происхождения в настоящее время вызывает споры специалистов. Одни представители научного мира утверждают, что вирусы неспособны стать причиной патологии, другие – что внеклеточная форма жизни может спровоцировать системную воспалительную реакцию, являющуюся патогенетической основой ИТШ.
Патогенез
В основе симптомов лежит неконтролируемое распространение медиаторов воспаления из патологического очага. При этом происходит активация макрофагов, лимфоцитов и нейтрофилов. Возникает синдром системного воспалительного ответа. На фоне этого снижается периферический сосудистый тонус, объем циркулирующей крови падает за счет повышения проницаемости сосудов и застоя жидкости в микроциркуляторном русле. Дальнейшие изменения обусловлены резким уменьшением перфузии. Недостаточное кровоснабжение становится причиной гипоксии, ишемии внутренних органов и нарушения их функции. Наиболее чувствителен головной мозг. Кроме того, ухудшается функциональная активность легких, почек и печени.
Помимо СВР в формировании септического шока важную роль играет эндогенная интоксикация. В связи со снижением работоспособности экскреторных систем в крови накапливаются продукты нормального обмена веществ: креатинин, мочевина, лактат, гуанин и пируват. Во внутренних средах повышается концентрация промежуточных результатов окисления липидов (скатол, альдегиды, кетоны) и бактериальных эндотоксинов. Всё это вызывает тяжелые изменения гомеостаза, расстройства кислотно-щелочного баланса, нарушения в работе рецепторных систем.
Классификация
Симптомы септического шока
90% случаев СШ сопровождается дыхательной недостаточностью различной степени тяжести. Пациенты с декомпенсированным и терминальным течением болезни нуждаются в аппаратной респираторной поддержке. Печень и селезенка увеличены, уплотнены, их функция нарушена. Может отмечаться атония кишечника, метеоризм, стул с примесью слизи, крови и гноя. На поздних стадиях возникают симптомы диссеминированного внутрисосудистого свертывания: петехиальная сыпь, внутреннее и наружное кровотечения.
Осложнения
Септический шок приводит к ряду тяжелых осложнений. Наиболее распространённым из них считается полиорганная недостаточность, при которой нарушается функция двух и более систем. В первую очередь страдает ЦНС, легкие, почки и сердце. Несколько реже встречается поражение печени, кишечника и селезенки. Летальность среди пациентов с ПОН достигает 60%. Часть из них погибает на 3-5 сутки после выведения из критического состояния. Это обусловлено органическими изменениями во внутренних структурах.
Еще одним распространенным последствием ИТШ являются кровотечения. При формировании внутримозговых гематом у пациента развивается клиника острого геморрагического инсульта. Скопление экстравазата в других органах может приводить к их сдавлению. Уменьшение объема крови в сосудистом русле потенцирует более значимое снижение артериального давления. ДВС на фоне инфекционно-токсического шока становится причиной гибели пациента в 40-45% случаев. Вторичное поражение органов, спровоцированное микротромбозами, возникающими на начальном этапе формирования коагулопатии, отмечается практически у 100% больных.
Диагностика
- Осмотр и физикальное исследование. Реализуется непосредственно лечащим врачом. Специалист обнаруживает характерные клинические признаки шокового состояния. Для этого проводится тонометрия, визуальная оценка цвета кожных покровов, особенностей дыхательных движений, подсчет пульса и ЧДД, аускультация сердца и легких. При подозрении на наличие осложнений необходима оценка неврологического статуса на предмет симптоматики кровоизлияния в мозг.
- Аппаратное исследование. Имеет вспомогательное значение. Пациенту показан контроль состояния с использованием анестезиологического монитора. На экран устройства выводится информация о величине артериального давления, частоте сердечных сокращений, степени насыщения крови кислородом (при легочной недостаточности SpO2<90%) и коронарном ритме. На фоне нарушений дыхания и токсического поражения миокарда может отмечаться тахикардия, аритмия и блокады внутрисердечной проводимости.
- Лабораторное исследование. Позволяет выявить имеющиеся нарушения гомеостаза, сбои в работе внутренних органов. У пациентов с шоком септического происхождения обнаруживается повышенный уровень креатинина (> 0,177 ммоль/л), билирубина (>34,2 мкмоль/л), лактата (>2 ммоль/л). О нарушении коагуляции свидетельствует тромбоцитопения (
Лечение септического шока
Пациентам показана интенсивная терапия. Лечение проводят в отделениях ОРИТ с использованием методов аппаратной и медикаментозной поддержки. Лечащий врач – реаниматолог. Может потребоваться консультация инфекциониста, кардиолога, гастроэнтеролога и других специалистов. Требуется перевод больного на искусственную вентиляцию лёгких, круглосуточное наблюдение среднего медицинского персонала, парентеральное кормление. Смеси и продукты, предназначенные для введения в желудок, не используются. Все методы воздействия условно делятся на патогенетические и симптоматические:
- Патогенетическое лечение. При подозрении на наличие сепсиса больному назначают антибиотики. Схема должна включать в себя 2-3 препарата различных групп, обладающих широким спектром действия. Подбор медикамента на начальном этапе проводят эмпирическим путем, в соответствии с предполагаемой чувствительностью возбудителя. Одновременно с этим производят забор крови на стерильность и восприимчивость к антибиотикам. Результат анализа готовится в течение 10 дней. Если к этому времени подобрать эффективную лекарственную схему не удалось, следует использовать данные исследования.
- Симптоматическое лечение. Подбирается с учетом имеющейся клинической картины. Обычно больные получают массивную инфузионную терапию, глюкокортикостероиды, инотропные средства, антиагреганты или гемостатики (в зависимости от состояния свертывающей системы крови). При тяжелом течении болезни используют препараты крови: свежезамороженную плазму, альбумин, иммуноглобулины. Если пациент находится в сознании, показано введение анальгетических и седативных лекарств.
Прогноз и профилактика
Септический шок имеет неблагоприятный прогноз для жизни. При субкомпенсированном течении погибает около 40% больных. Декомпенсированная и терминальная разновидности оканчиваются гибелью 60% пациентов. При отсутствии своевременной медицинской помощи смертность достигает 95-100%. Часть больных умирает через несколько дней после устранения патологического состояния. Профилактика ИТШ заключается в своевременном купировании очагов инфекции, грамотном подборе антибиотикотерапии у хирургических больных, соблюдении антисептических требований в отделениях, занимающихся инвазивным манипуляциями, поддержке адекватного иммунного статуса у представителей ВИЧ-инфицированной прослойки населения.
2. Тактика ведения пациентов с сепсисом и септическим шоком в многопрофильном стационаре/ Сапичева Ю.Ю., Лихванцев В.В. – 2015.
Дыхательная недостаточность — это патологический синдром, сопровождающий ряд заболеваний, в основе которого лежит нарушение газообмена в легких. Основу клинической картины составляют признаки гипоксемии и гиперкапнии (цианоз, тахикардия, нарушения сна и памяти), синдром утомления дыхательной мускулатуры и одышка. ДН диагностируется на основании клинических данных, подтвержденных показателями газового состава крови, ФВД. Лечение включает устранение причины ДН, кислородную поддержку, при необходимости - ИВЛ.
МКБ-10
Общие сведения
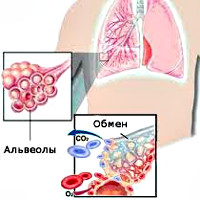
Внешнее дыхание поддерживает непрерывный газообмен в организме: поступление атмосферного кислорода и удаление углекислого газа. Любое нарушение функции внешнего дыхания приводит к нарушению газообмена между альвеолярным воздухом в легких и газовым составом крови. В результате этих нарушений в крови нарастает содержание углекислоты и уменьшается содержание кислорода, что ведет к кислородному голоданию, в первую очередь, жизненноважных органов – сердца и головного мозга.
При дыхательной недостаточности (ДН) не обеспечивается необходимый газовый состав крови, либо он поддерживается за счет перенапряжения компенсаторных возможностей системы внешнего дыхания. Угрожающее для организма состояние развивается при дыхательной недостаточности, характеризующейся снижением парциального давления кислорода в артериальной крови менее 60 мм рт. ст., а также повышением парциального давления углекислоты более 45 мм рт. ст.

Причины
Дыхательная недостаточность может развиваться при различных острых и хронических воспалительных заболеваниях, повреждениях, опухолевых поражениях органов дыхания; при патологии со стороны дыхательной мускулатуры и сердца; при состояниях, приводящих к ограничению подвижности грудной клетки. К нарушению легочной вентиляции и развитию дыхательной недостаточности могут приводить:
- Обструктивные нарушения. Дыхательная недостаточность по обструктивному типу наблюдается при затруднении прохождения воздуха по воздухоносным путям – трахее и бронхам вследствие бронхоспазма, воспаления бронхов (бронхита), попадания инородных тел, стриктуры (сужения) трахеи и бронхов, сдавления бронхов и трахеи опухолью и т. д.
- Рестриктивные нарушения. Дыхательная недостаточность по рестриктивному (ограничительному) типу характеризуется ограничением способности легочной ткани к расширению и спаданию и встречается при экссудативном плеврите, пневмотораксе, пневмосклерозе, спаечном процессе в плевральной полости, ограниченной подвижности реберного каркаса, кифосколиозе и т. д.
- Гемодинамические нарушения. Причиной развития гемодинамической дыхательной недостаточности могут служить циркуляторные расстройства (например, тромбоэмболия), ведущие к невозможности вентиляции блокируемого участка легкого. К развитию дыхательной недостаточности по гемодинамическому типу также приводит право-левое шунтирование крови через открытое овальное окно при пороке сердца. При этом происходит смешение венозной и оксигенированной артериальной крови.
Классификация
Дыхательная недостаточность классифицируется по ряду признаков:
1. По патогенезу (механизму возникновения):
- паренхиматозная (гипоксемическая, дыхательная или легочная недостаточность I типа). Для дыхательной недостаточности по паренхиматозному типу характерно понижение содержания и парциального давления кислорода в артериальной крови (гипоксемия), трудно корригируемое кислородной терапией. Наиболее частыми причинами данного типа дыхательной недостаточности служат пневмонии, респираторный дистресс-синдром (шоковое легкое), кардиогенный отек легких.
- вентиляционная ("насосная", гиперкапническая или дыхательная недостаточность II типа). Ведущим проявлением дыхательной недостаточности по вентиляционному типу служит повышение содержания и парциального давления углекислоты в артериальной крови (гиперкапния). В крови также присутствует гипоксемия, однако она хорошо поддается кислородотерапии. Развитие вентиляционной дыхательной недостаточности наблюдается при слабости дыхательной мускулатуры, механических дефектах мышечного и реберного каркаса грудной клетки, нарушении регуляторных функций дыхательного центра.
2. По этиологии (причинам):
- обструктивная. При этом типе страдают функциональные возможности аппарата внешнего дыхания: затрудняется полный вдох и особенно выдох, ограничивается частота дыхания.
- рестриктивная (или ограничительная). ДН развивается из-за ограничения максимально возможной глубины вдоха.
- комбинированная (смешанная). ДН по комбинированному (смешанному) типу сочетает признаки обструктивного и рестриктивного типов с преобладанием одного из них и развивается при длительном течении сердечно-легочных заболеваний.
- гемодинамическая. ДН развивается на фоне отсутствия кровотока или неадекватной оксигенации части легкого.
- диффузная. Дыхательная недостаточность по диффузному типу развивается при нарушении проникновения газов через капиллярно-альвеолярную мембрану легких при ее патологическом утолщении.
3. По скорости нарастания признаков:
- Острая дыхательная недостаточность развивается стремительно, за несколько часов или минут, как правило, сопровождается гемодинамическими нарушениями и представляет опасность для жизни пациентов (требуется экстренное проведение реанимационных мероприятий и интенсивной терапии). Развитие острой дыхательной недостаточности может наблюдаться у пациентов, страдающих хронической формой ДН при ее обострении или декомпенсации.
- Хроническая дыхательная недостаточность может нарастатьна протяжении нескольких месяцев и лет, нередко исподволь, с постепенным нарастанием симптомов, также может быть следствием неполного восстановления после острой ДН.
4. По показателям газового состава крови:
- компенсированная (газовый состав крови нормальный);
- декомпенсированная (наличие гипоксемии или гиперкапнии артериальной крови).
5. По степени выраженности симптомов ДН:
- ДН I степени – характеризуется одышкой при умеренных или значительных нагрузках;
- ДН II степени – одышка наблюдается при незначительных нагрузках, отмечается задействованность компенсаторных механизмов в покое;
- ДН III степени – проявляется одышкой и цианозом в покое, гипоксемией.
Симптомы дыхательной недостаточности
Признаки ДН зависят от причин ее возникновения, типа и тяжести. Классическими признаками дыхательной недостаточности служат:
Гипоксемия клинически проявляется цианозом (синюшностью), степень которого выражает тяжесть дыхательной недостаточности и наблюдается при снижении парциального давления кислорода (РаО2) в артериальной крови ниже 60 мм рт. ст. Для гипоксемии характерны также нарушения гемодинамики, выражающиеся в тахикардии и умеренной артериальной гипотонии. При понижении РаО2 в артериальной крови до 55 мм рт. ст. наблюдаются нарушения памяти на происходящие события, а при снижении РаО2 до 30 мм рт. ст. пациент теряет сознание. Хроническая гипоксемия проявляется легочной гипертензией.
Проявлениями гиперкапнии служат тахикардия, нарушения сна (бессонница ночью и сонливость днем), тошнота, головные боли. Быстрое нарастание в артериальной крови парциального давления углекислоты (РаСО2) может привести к состоянию гиперкапнической комы, связанной с усилением мозгового кровотока, повышением внутричерепного давления и развитием отека головного мозга. Синдром слабости и утомления дыхательных мышц характеризуется увеличением частоты дыхания (ЧД) и активным вовлечением в процесс дыхания вспомогательной мускулатуры (мышц верхних дыхательных путей, мышц шеи, брюшных мышц).
- синдром слабости и утомления дыхательной мускулатуры
ЧД более 25 в мин. может служить начальным признаком утомления дыхательной мускулатуры. Урежение ЧД менее 12 в мин. может предвещать остановку дыхания. Крайним вариантом синдрома слабости и утомления дыхательной мускулатуры служит парадоксальное дыхание.
Одышка субъективно ощущается пациентами как нехватка воздуха при чрезмерных дыхательных усилиях. Одышка при дыхательной недостаточности может наблюдаться как при физическом напряжении, так и в спокойном состоянии. В поздних стадиях хронической дыхательной недостаточности с присоединением явлений сердечной недостаточности у пациентов могут появляться отеки.
Осложнения
Дыхательная недостаточность является неотложным, угрожающим для здоровья и жизни состоянием. При неоказании своевременного реанимационного пособия острая дыхательная недостаточность может привести к гибели пациента. Длительное течение и прогрессирование хронической дыхательной недостаточности приводит к развитию правожелудочковой сердечной недостаточности в результате дефицита снабжения сердечной мышцы кислородом и ее постоянных перегрузок. Альвеолярная гипоксия и неадекватная вентиляция легких при дыхательной недостаточности вызывает развитие легочной гипертензии. Гипертрофия правого желудочка и дальнейшее снижение его сократительной функции ведут к развитию легочного сердца, проявляющегося в застое кровообращения в сосудах большого круга.
Диагностика
На начальном диагностическом этапе тщательно собирается анамнез жизни и сопутствующих заболеваний с целью выявления возможных причин развития дыхательной недостаточности. При осмотре пациента обращается внимание на наличие цианоза кожных покровов, подсчитывается частота дыхательных движений, оценивается задействованность в дыхании вспомогательных групп мышц.
В дальнейшем проводятся функциональные пробы для исследования функции внешнего дыхания (спирометрия, пикфлоуметрия), позволяющая провести оценку вентиляционной способности легких. При этом измеряется жизненная емкость легких, минутный объем дыхания, скорость движения воздуха по различным отделам дыхательных путей при форсированном дыхании и т. д.
Обязательным диагностическим тестом при диагностике дыхательной недостаточности является лабораторный анализ газового состава крови, позволяющий определить степень насыщения артериальной крови кислородом и углекислым газом (PаО2 и PаСО2) и кислотно-щелочное состояние (КОС крови). При проведении рентгенографии легких выявляются поражения грудной клетки и паренхимы легких, сосудов, бронхов.
Лечение дыхательной недостаточности
Лечение пациентов с дыхательной недостаточностью предусматривает:
- восстановление и поддержание оптимальной для жизнеобеспечения вентиляции легких и оксигенации крови;
- лечение заболеваний, явившихся первопричиной развития дыхательной недостаточности (пневмонии, экссудативного плеврита, пневмоторакса, хронических воспалительных процессов в бронхах и легочной ткани и т. д.).
При выраженных признаках гипоксии в первую очередь проводится оксигенотерапия (кислородная терапия). Кислородные ингаляции подаются в концентрациях, обеспечивающих поддержание PаО2 = 55— 60 мм рт. ст., при тщательном мониторинге рН и PаСО2 крови, состояния пациента. При самостоятельном дыхании пациента кислород подается масочно или через носовой катетер, при коматозном состоянии проводится интубация и поддерживающая искусственная вентиляция легких.
Наряду с оксигнотерапией проводятся мероприятия, направленные на улучшение дренажной функции бронхов: назначаются антибактериальные препараты, бронхолитики, муколитики, массаж грудной клетки, ультразвуковые ингаляции, лечебная физкультура, проводится активная аспирация секрета бронхов через эндобронхоскоп. При дыхательной недостаточности, осложненной легочным сердцем, назначаются диуретики. Дальнейшее лечение дыхательной недостаточности направлено на устранение вызвавших ее причин.
Прогноз и профилактика
Дыхательная недостаточность является грозным осложнением многих заболеваний и нередко приводит к летальному исходу. При хронических обструктивных заболеваниях легких дыхательная недостаточность развивается у 30% пациентов.Прогностически неблагоприятно проявление дыхательной недостаточности у пациентов с прогрессирующими нейромышечными заболеваниями (БАС, миотония и др.). Без соответствующей терапии летальный исход может наступить в течение одного года.
При всех прочих патологиях, приводящих к развитию дыхательной недостаточности, прогноз разный, однако невозможно отрицать, что ДН является фактором, сокращающим продолжительность жизни пациентов. Предупреждение развития дыхательной недостаточности предусматривает исключение патогенетических и этиологических факторов риска.
1. Интенсивная терапия заболеваний, сопровождающихся острой дыхательной недостаточностью: методические рекомендации/ Прасмыцкий О.Т., Ржеутская Р.Е. – 2001.
3. Дыхательная недостаточность с преимущественным нарушением бронхо-легочных механизмов/ Чеснокова Н.П., Брилль Г.Е., Моррисон В.В., Полутова Н.В.// Научное обозрение. Медицинские науки. – 2017 - №2.
4. Формирование дыхательной недостаточности при хронических обструктивных заболеваниях легких, пути и возможности лечения больных: Автореферат диссертации/ Игнатьев В. А. – 1993.
Читайте также:

