Профилактика инфекционного эндокардита у детей что это
Обновлено: 18.04.2024
Главная → Статьи доктору → Кардиология → Профилактика инфекционного эндокардита у детей. Ситуация и современные протоколы.
Несмотря на лечение антибиотиками и успехи хирургии сердца, инфекционный эндокардит остается серьезной патологией, потенциально летальной, частота которого может возрастать в связи с улучшением выживаемости пациентов носителей врожденных кардиопатий. Частота составляет 1,35 случая на 1000 населения в год, она несколько больше среди детей носителей сложных пороков сердца; она составляет от 0,95 до 1,65 в год в случаях врожденных некорригированных ВПС и снижается до 0,2 в год после коррекции. Общая смертность составляет от 11 до 27% в зависимости от серий. Его тяжесть, так же как и затраты на лечение, значительны, начиная с диагностики и терапии (протезирование клапанов бывает необходимым в 25% случаев, внутривенная антибиотикотерапия минимум 4 недели), оправдывает проведение тщательной профилактики.
Экспериментальные модели
Рекомендации по антибиотикопрофилактике инфекционного эндокардита всегда являются объектом тщательного рассмотрения. В то же время не существует ни одного контролированного проспективного, которое трудно реализуемо по этическим причинам. Исследования касающиеся частоты инфекционного эндокардита у леченных не леченных пациентов дают различные результаты, возможно по причине разницы антибиотических протоколов. Хотя экспериментальные модели осуществимы у крыс. Риск бактериального вмешательства кажется зависит от объема введенной бактериальной массы, вирулентности вида и основного состояния (кардиопатия sous-jacent, иммуносупрессия). Локальная бактериальная продлиферация начинается на 2 часу после бактериемии.
Эффективность антибиотикопрофилактики связана с бактерицидным действием повышенным уровнем в сыворотке на момент бактериемии и в течение 6 часов после нее, что позволяет разом элиминировать микроорганизмы циркулирующие в крови и микроорганизмы, фиксированные на клапанах. Чем больше инокулировано бактерий, тем более длительной должна быть высокая ингибирующая концентрация антибиотика.
Также в зависимости от типа процедуры связанной с риском бактериемии, профилактика должна проводится или одной единственной дозой или многими дозами. И наконец, максимальный пик в сыворотке должен достигаться на 2 час после бактериемии, необходимо вводить антибиотик незадолго до geste, на практике за час до.
Основное заболевание и факторы риска
Инфекционный эндокардит может развиться на фоне известной кардиjпатии, но также и на фоне небольшой нераспознанной кардиопатии и на здоровом сердце.
Таблица 1. Врожденные кардиопатии и риск инфекционного эндокардита
Высокий риск
Умеренный риск
Небольшой риск
Не цианогенные кардиопатии
(CIV, CAP, CAV)
Обструктивные миокардиопатии с IM
Интракардиальный инородный материал для окклюзии (CAP, CIA)
Пролапс митрального клапана без недостаточности
Оперированные лево-правосторонние шунты
CAP- проходимый артериальный проток; CAV - атриовентрикулярный проток; CIA - межпредсердная коммуникация; CIV - межжелудочковая коммуникация; EI - инфекционный эндокардит; IM - недостаточность митрального клапана; RAA - острый суставной ревматизм
Известная патология сердца
Риск бактериального пораждения различен в зависимости от аномалии сердца. Обычно он более значителен в случае поражения с током крови с высокой скоростью или в присутствии ин-тракардиальная материала.
Кардиопатии с высоким риском
Антецедент инфекционного эндокардита вызывает риск рецидива значительно более высокий (50%) и оправдывает хирургическую коррекцию кардиопатии, если это возможно, после излечения эпизода инфекции.
Клапанный протез какой бы не была его локализация, прежде всего механический, а также как любой другой интракардиальный материал (анастомотические трубки системо-пульмональные, клапанные трубки) являются точками притяжения инфекции.
Среди врожденных кардиопатий сложные кардиопатии с хроническим цианозом, прежде всего, в случае предшествующего паллиативного хирургического вмешательства, представляют собой более благоприятную среду. Максимальная частота наблюдается при тетральгии Фалло, но мероприятия по профилактике должны также тщательно проводится и в случае цианогенных сложных кардиопатий, не поддающихся коррекции, и при синдроме Eisenmenger, для которых риск не может быть уменьшен проведением коррекционной хируругии. Кроме того, интракардиальный шунт справа-налево исключает пульмональную бактериальную фильтрацию бактерий и предрасполагает к церебральным метастазам и абсцессам мозга.
Среди врожденных патологий клапанов митрального и/или аортального аортальное сужение кажется представляет больший риск (тем более значительный, чем более выражен стеноз); обычно аортальный клапан поражается более часто, чем митральный клапан.
Ревматические вальвулопатии стали редки во Франции и не составляют более чем 10% случаев инфекционного эндокардита. Все вальвулопатии поражаются (митральные или аортальные, стенозирующие или связанные с недостаточностью).
Недавнее хирургическое вмешательство на сердце (менее чем 2 месяца назад) также представляет собой значительный риск.
Кардиопатии с умеренным риском
Врожденные кардиопати не связанные с цианозом менее часто являются причиной. Межжелудочковая коммуникация наиболее часто поражаемая среди кардиопатий с лево-правосторонним шунтом, затем следует проходимый артериальный канал и атривентрикулярный канал.
Пролапс митрального клапана связан с умеренным риском когда он сопровождается недоста-точностью митрального клапана также как и гипертрофическая обструктивная гипертрофия. Риск связанный с пролапсусом митрального клапана связан с его частотой и прежде всего из-за недиагносцирования среди общей популяции.
Соврменные методы интервенционной катетеризации создали новую группу риска, как таковая кардиопатий корригированных эндолюминально с применением окллюзирующего интракарди-ального материала (артериального протока, межпредсердной коммуникации).
Кардиопатии с небольшим или нулевым риском
Риск раценивается как нулевой при межпредсердных коммуникациях, стенозе легочного клапна, лево-прово шунтах оперированных без остаточного шунта, пролапсусе митрального клапана без недостаточности его и дилатирующей миокардиопатии. В то же время наличие бляшки закрытия шунта (межжелудочковой коммуникации или межпредсердной) требуют проведения антибактериальной профилактики.
Вмешательство на сердце или наличие интракардиального пайсмейкера являются чрезвычайно редкими причинами.
Нераспознанная патология сердца
Некоторые асимптоматические субъекты являются носителями не прошедшего экспертизы шума, который может быть связан с небольшой аномалией сердца: небольшим стенозом пульмонального клапана, аортальной бикуспидией, маленькой межжелудочковой коммуникацией, пролапсом митрального клапана с его недостаточностью. Наличие шума не не сотвествующего критериям типичных разнообразий анорганического шума требует однако провдения исследования для исключения риска бактериальной контаминации.
Частота инфекционного эндокардита вариирует с возрастом создавая более высокий риск у детей в возрасте до 2 лет, в частности у недоношенных с нозокомикальными заболеваниями.
Развитию инфекционного эндокардита благоприятствует состояние подавления иммунитета (пациенты получающие иммуносупрессоры, с различными иммунными дефицитами, аспленией).
Развитию инфекционного эндокардита правого сердца благоприятствует наличие центрального венозного катетера, вентрикулоатриальное отведение при гидроцефалии и атриовенозная фистула (диализ) и у подростков токсикомания.
Существует не малый процент (10%) инфекционных эндокардитом развившихся на здоровом сердце в контексте нозокомикальной инфекции с введением центрального катетера.
Эволюция этиологий: собственный опыт
Сравнение этиологий инфекционных эндокардитов 70 и 80 лет нашего личного опыта показывает персистенцию явного преобладания бактериальных поражений при врожденных кардиопатиях, в основном это межжелудочковые коммуникации, тетрада Fallot и сложные кардиопатии. В любом случае 80 годы были отмечены с одной стороны значительным снижением инфекционных эндокардитов на фоне тетрады Fallot в связи с ранней хирургическойц коррекцией и, с другой стороны, увеличением инфекционных эндокардитов в связи с улучшением выживаемости этих пациентов.
Дентарные входные ворота
Все виды лечения зубов могут оказаться причиной если они вызывают кровоточивость из десен, основным риском является удаление зубов. Выпадение молочных зубов не представляет значительного риска. Различные патологии зубов часто недиагносцированные и пренебрегаемые в частности девитализированных зубов (кариес, парадонтальная и периапикальная инфекция, пульпиты, абсцессы) также могут оказаться причиной. Важно отметить, что патология десен представляет собой риск аналогичный зубной; ортодонтные аппараты, источники повторных ранений десен также могут оказаться причиной.
Амигдалиты, синуситы, отиты и мастоидиты являются потенциальными входными воротами и должны систематически лечиться антибиотиками направленных против стерптококков у субъектов с повышенным риском. Профилактические предостаорожности также обязательны в случае хирургического вмешательства на инфицированном органе: амигадлектомия, аденоидектомия, парацентез. То же самое относится и к эндоскопическим процедурам уха-горла-носа способным вызвать ранение слизистой (биопсии).
Установка транстимпанического дренажа не требует профилактических мероприятий так как осуществляется только при отсутствии развивающейся инфекции.
Кожные входные ворота
Кожные поражения вероятно остаются наиболее часто нераспознаваемыми причинами. Основными поражениями связанными с риском это : панарции, импетиго, инфицированные акне и все ранки даже поверхностные не леченные.
Другие входные ворота
Причины пищеварительные и урологические более редки у ребенка чем у взрослого: острая инфекция, эндоскопическая процедура, хирургическое вмешательство. Интервенционная катетеризация сердца с установкой внутрисердечного материала для окклюзии персистирующего артериального протока или межпредсердной коммуникации, а также центральные катетеры являются факторами риска; и наоборот, редко причиной является сердечный pacemaker.
Диагностические критерии инфекционного эндокардита
Крупные критерии
Типичные микроорганизмы для инфекционного эндокардита (Streptococcus viridans, Staphylococcus, Enterococcus)
Персистирующая бактериемия: две гемокультуры полученные с интервалом более 12 часов или три гемокультуры (или больше) полученные по меньшей мере с 1 часовым интервалом
Признаки эндокардиального поражения
Изменения или появления шума
Эхокардиографические признаки: вегетации на клапанах или протезах клапанов, абсцессы, недавнее dehiscence протеза.
Малые критерии
Фон : кардиопатии или внутривенный катетер
Лихорадка : больше 38оС
Васкулярные феномены: системные артериальные эмболии, септический инфоркт легких, микотьические аневризмы, кровоизлияние в мозг или в коньюнктивы, поражение Janeway.
Иммунологические фоеномены: гломерулонефрит, faux pnaris d’Osler, ретинальные узелки Roth, ревматоидный фактор.
Микробиологические: положительная гемокультура не соотвествующая крупному критерию или серологическое подтверждение развивающиейся инфекции соотвествующей эндокардиальному поражению.
Эхографические: поражения соотвествующеие инфекционному эндокардиту, но не соотвествующие крупному критерию.
Диагноз инфекционного эндокардита может иметь место при наличии двух крупных критериев и трех малых критериев или пяти малых критериев.
Причинные микроорганизмы
Гемокультуры оказываются положительными в 80-90% случаев, но в 10-20% случаях инфекционного эндокардита гемокультуры остаются негативными и причинный микроорганизм неизвестен., иногда вследствие предшествующей плохо адаптированной антибиотикотерапии (табл. II).
Инфекционный эндокардит вызванный золотистым стафиллококком особенно тяжел по причине вирулетности микроорганизма, который быстро вызывает обширные и разрушительные пораже-ния,несмотря на даптированную антибиотикотерапию, со значительным риском эмболизации; поражение клапанных протезов является официальным показанием для хирургического вмеша-тельства. Прогноз инфекционных эндокардитов вызванных стафилококками резистентными или чувствительными к метицеллину идентичен. Тяжесть этих поражений стафилококками оправдывает строгое наблюдение и проведение эффективного лечения кожных поражений.
Они являются причиной 10% случаев. Это микрорганизмы происходящие из пищеварительного тракта часто резистентные к пенициллину, к цефалоспринам и иногда к гликопептидам (ванкомицину, тейкопланину); некоторые мультирезистеные штаммы ставят сложные терапевтические задачи.
Причинные микроорганизмы прежде всего это Streptococcus mutans, Enterococcus faecalis et Enterococcus faecium.
Друге многочисленные виды встречаются значительно реже : пневмококки, Haemophilus influenzae, грам-отрицательные бациллы использующие в качестве входных ворот пищевариетльный или моевой тракты, грибковые инфекции (Candida, Aspergillus) по происхождению нозокомикальные прогноз при которых весьма неблагоприятен несмотря на ранее хирургическое лечение совместно с антифунгальной терапией.
Профилактическое лечение
Профилактика проводится всем пациентам со значительным риском оказавшихся в ситуации потенциального риска. Назначаемые антибиотики имеют антистрептококковую направленностью Важно указать, что пенициллинотерапия длинными курсами применяемая для предупреждения рецидивов ревматизма или при асплении не эффективна в отношении резистентных стрептококков и, что обычные мероприятия антибиотикопрофилактики в этих случаях должны прово-диться с применением различных антибиотиков отличающихся от пенициллина G.
Антибиопрофилактика
В табл. III представлены протоколы применяемые в обычной практике во Франции в случае лечения зубов или отоларингологических, урологических гастроэнтерологических вмешательствах. В случаях проведения эндоскопии применяются протоколы соотвествующие таковым при лечении зубов под местной анестезией.
Таблица III. Антибиотикопрофилактика инфекционного эндокардита. По материалам конференции консенсуса по профилактике инфекционного эндокардита. Paris, 27 марта 1992 г.
Антибиотик
Дозиролвание и путь введения за час предшествующий мероприяютию
Дозировка 6 часов спустя
Лечение зубов и действия на VAS
Отсутствие аллергии на b-лактамы
Аллергия на b-лактамы
Однократный прием 75 mg/kg per os
Однократный прием 15 mg/kg per os
Однократный прием 25 mg/kg per os
Лечение зубов и воздействия на VAS (AG)
Отсутствие аллергии на b-лактамы
Аллергия на b-лактамы
20 mg/kg (max 1 g) во внутривенной перфузиии (>60 min)
Пока еще по получен сертификат применения у детей
Без второй дозы
При вмешательствах на мочевых или пищеварительном трактах
Отсутствие аллергии на b-лактамы
1,5 mg/kg (max : 80 mg) IV
Аллергия на b-лактамы
20 mg/kg (max 1 g) в перфузиии IV (>60 min)
Отсуствтвует сертификат применение у детей
1,5 mg/kg (max 80 mg) IV
Без второй дозы
VAS - верхние дыхательный пути; AG - общая анестезия; IV - внутривенно; max - максимальная доза
Другие случаи
Инфекции отоларингологические предпочтительнее лечить амоксициллином а кожные инфекции антибиотиками имеющими антистафилококковвую направленность.
Сердечная хирургия является объектом системной профилактики в течение 48 часов с использованием комбинации антистафилококкового беталактама и аминогликозида.
Интревенционной катетеризации с окклюзие артериального канала с помощью coils предшествует профилактика преимущественно цефалоспорином.
Другие профилактические мероприятия
Эффективная профилактика инфекционного эндокардита предполагает просветительскую информацию и обучение семьи, самого ребенка если он достаточно большой, а также врача и лечащего дентиста.
Тщательная буккодентарная гигиена имеет весьма большое значение так как некоторые инфекционные эндокардиты являются следствием гингивопародонтальной инфекции вызывающей спонтанную бактериемию; она состоит из необходимости чистить зубы щеткой несколько раз в день, поступление фтора, умеренном потреблении сахара и осмотра зубов систематически по меньшей мере один раз в год.
Особые случаи вмешательства на зубах
Только лечение поверхностного кариеса и пломбирование пульпированных зубов не исключает антибиотикопрофилактики. Пульпопатии, парадонтопатии и травматизация требуют экстракции. Также не рекомендуется проводить девитализации зубов, также как установку протезов на депульпированные зубы, имплантацию и проведение пародонтальных операций. И наконец, ортодонтные аппараты не следует применять в случаях кардиопатии с высоким риском, особенно при цианогенной врожденной кардиопатии.
Заключение
Инфекционный эндокардит это серьезная патология, потенциально летальная. Эволюция последних лет происходит в направлении увеличения бактериального поражения врожденных кардиопатий и прогрессирования нозокомикальных стафилококковых инфекций, с сомнительным прогнозом и резистентными микроорганизмами. Необходимо проведение тщательной профилактики. Субъекты с наиболее высокми риском это дети носители цианогенных врожденных кардиомиопатий, вальвулопатий митроаортальных, внутрикардиальных протезов или с неоперированными межжелудочковыми коммуникациями.
Основной риск приходится на лечение зубов, но не следует недооценивать и входных ворот со стороны кожи или уха-горла-носа. Снижение частоты инфекционного эндокардита у детей требует тщательной профилактики, информированности всех участвующих во вмешательствах, оптимизации терапевтических протоколов и постоянной бдительности.
Инфекционный эндокардит у детей: признаки, диагностика
У всех детей в любом возрасте с врождённым пороком сердца (за исключением вторичных ДМПП), в том числе у новорождённых, имеется риск инфекционного эндокардита. Риск является наиболее высоким, когда имеется турбулентное направление потока крови, как при ДМЖП, коарктации аорты и ОАП или если при хирургическом лечении был установлен протезирующий материал.
Он может быть сложен для диагностики, однако должен быть заподозрен у любого ребёнка или взрослого с продолжительной лихорадкой, недомоганием, повышением СОЭ, необъяснимой анемией или гематурией. Не стоит надеяться на наличие классических периферических симптомов инфекционного эндокардита.
• Изменяющиеся сердечные симптомы.
• Спленомегалия.
• Неврологические признаки инфаркта головного мозга.
• Инфаркты сетчатки.
• Артрит / артралгия.
• Гематурия (микроскопическая).
Диагностика инфекционного эндокардита у детей
Необходимо произвести посев на наличие культур крови до начала антибиотикотерапии. Детальная перекрёстная ЭхоКГ может подтвердить диагноз путём выявления вегетации, однако никогда не исключает его. Вегетации состоят из фибрина и тромбоцитов и содержат инфекционные организмы. Реактанты острой фазы повышаются и могут оказать помощь для мониторинга ответа на терапию.
Наиболее распространённым причинным организмом является а-гемолитический стрептококк (Streptococcus viridans). Бактериальный эндокардит обычно лечится высокими дозами пенициллина в комбинации с аминогликозидами, назначаемыми на 6 нед в виде внутривенных инъекций с контролем плазменного уровня антибиотиков, которые должны убить микроорганизмы.
Если имеется инфицирование протезного материала, например протезированных клапанов, заплат ДМЖП или шунтов, имеется меньше шансов для полной эрадикации и может потребоваться хирургическое удаление.
Профилактика инфекционного эндокардита у детей
Наиболее важным фактором профилактики эндокардита является хорошая гигиена полости рта, за которой необходимо следить всем детям с врождёнными пороками сердца. Антибиотикопрофилактика необходима при:
• лечении зубов, даже незначительном;
• хирургическом вмешательстве, которое, вероятно, будет связано с бактериемией (например, аппендэктомия, хирургическое лечение ЛОР-патологии).
Профилактика антибиотиками бактериального эндокардита должна проводиться у всех детей с врождёнными пороками сердца (за исключением вторичного ДМПП) перед экстракцией зубов или любой операцией с вероятностью сепсиса.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Эндокардит: причины, диагностика, лечение, профилактика
Поражение сердечных клапанов обычно происходит при транзиторной (преходящей) бактериемии. Наиболее высокий риск развития заболевания отмечают при врождённой патологии клапанов и их повреждении в результате различных причин.
Причиной могут быть микроорганизмы из ротовой полости, мочевыводящих путей, а также попадающие в кровоток при неправильном внутривенном введении лекарств или колонизации микроорганизмами внутрисосудистых устройств.
При аускультации выслушивают непостоянные сердечные шумы. На более поздних стадиях заболевания возможно развитие септической эмболии, часто приводящей к инсульту. Если эндокардит обусловлен чрезвычайно вирулентными штаммами (например, Staphylococcus aureus), то болезнь быстро прогрессирует и симптомы острого сепсиса превалируют в клинической картине заболевания.
Диагностика эндокардита. Диагностика основана на выявлении соответствующих данных клинической картины, инструментального и лабораторного обследования (критерии Дьюка) (Duke criteria).

Большие критерии Дьюка включают выделение из крови (гемокультура) микроорганизмов, чаще всего связанных (характерных) с развитием эндокардита (например, зеленящих стрептококков); выделение (неоднократно) из крови любых других микроорганизмов; выявление, по данным эхонарднографии, очевидных признаков поражения эндокарда и появление изменений клапанной регургитации.
Малые критерии Дьюка: выявление предрасполагающих факторов, лихорадка >38 °С, иммунологические признаки (септический инфаркт лёгких и др.) и другие патологические изменения, выявленные при эхокардиографии, данные микробиологического обследования больного, не связанные с большими критериями Дьюка.
Диагноз эндокардита устанавливают при наличии двух основных критериев или одного основного и трёх второстепенных.
Осложнения эндокардита. Прогрессирующее заболевание приводит к образованию прикорневого абсцесса аорты. При разрушении клапана быстро возникает сердечная декомпенсация и тяжёлая сердечная недостаточность. Результатом септической эмболии может быть поражение сосудов конечностей или инсульт. Нефрит — вторичное заболевание, возникающее в результате отложения иммунных комплексов в почечной ткани.
На фоне развивающегося сепсиса или при бесконтрольном применении нефротоксичных антибиотиков (аминогликозидов) отмечают быстрое прогрессирование поражения органа.
Обследование при эндокардите. Эхокардиография (трансторакальная, чреспищеводная — более чувствительная) позволяет обнаружить патологическое разрастание (вегетации) ткани клапана. На рентгенограмме грудной клетки отмечают очевидные признаки сердечной недостаточности. Для бактериологического исследования необходимо отобрать три образца крови с промежутком в один час (на высоте лихорадки). Антибиотикотерапию, если это возможно, следует начинать после получения результатов посевов крови.
В сыворотке крови возможно определение Coxiella и Chlamydia psittaci (например, с помощью полимеразной цепной реакции).
Лечение эндокардита. Идеально антибиотики не должны назначаться, пока не выделен микроорганизм (не выявлен этиологический фактор) и не определена его чувствительность к спектру антибиотиков. Прогноз эмпирической терапии эндокардита при отрицательных результатах микробиологического обследования хуже, чем, когда установлен возбудитель. Помощь в определении исходов заболевания оказывает мониторинг лабораторных показателей воспалительных реакций организма больного (С-реактивный белок др.).
Лечение должно быть основано на результатах определения чувствительности микроорганизмов к антибиотикам, минимальной подавляющей концентрации препарата и минимальной бактерицидной концентрации. При назначении гентамицина необходимо контролировать его содержание в крови, так как пациенты с эндокардитом очень чувствительны к токсическому действию этого препарата (ухудшение функции почек). В зависимости от показателя минимальной бактерицидной концентрации лечение продолжают в течение 2—6 нед.
Типичная схема комплексной терапии обычно включает бензилпенициллин и гентамицин для эрадикации зеленящих стрептококков, флуклоксациллин и гентамицин — для борьбы со стафилококками (ванкомицин и гентамицин — для пациентов с аллергией на препараты пенициллинового ряда). Кроме того, в каждой стране существуют свои рекомендации по лечению эндокардита.
Хирургическое вмешательство может потребоваться для устранения гемодинамических последствий эндокардита (особенно если инфекция вызвана S. aureus и другими микроорганизмами с высокой степенью патогенности), а также при отсутствии эффекта антибактериальной терапии.
Профилактика эндокардита. Для профилактики эндокардита у пациентов с клапанными пороками, которым предстоят различные манипуляции, способствующие повышению риска развития бактериемии (стоматологические операции, другие хирургические вмешательства), применяют антибиотики. При бактериурии выбор антимикробного препарата зависит от чувствительности выделенного микроорганизма. При проведении процедур, требующих общего наркоза, её начинают осуществлять при помощи лекарственных средств, принимаемых внутрь.
Кроме того, существует ряд профилактических схем в разных странах (при аллергии на препараты пенициллинового ряда, протезировании клапанов сердца и др.).
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
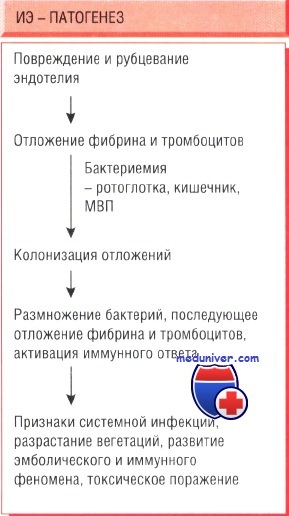
Инфекционный эндокардит (ИЭ) – тяжелое инфекционное (чаще бактериальное) системное заболевание с первоначальным поражением клапанов сердца и пристеночного эндокарда, которое сопровождается бактериемией, деструкцией клапанов, эмболическим, тромбогеморрагическим, иммунокомплексным поражением внутренних органов и без лечения приводит к смерти.
Литература
1. Демин А.А., Скопин И.И., Соболева М.К. и др. Инфекционный эндокардит: новые стандарты диагностики и лечения // Клин. Медицина.– 2003.– N.6.– C. 68–71.
2. Соболева М.К. Инфекционный эндокардит у детей и подростков. Кардиология и ревматология детского возраста. Практическое руководство по детским болезням. М. Медпрактика. Т.III. С. 264–278
3. Соболева М.К. , Соболева Е.Г., Веселова Е.А., Скоблякова М.Е. Инфекционный эндокардит у детей и подростков– инъекционных наркоманов // Педиатрия.– 2003.– N6. – C.43–51.
4. Тюрин В.П. Инфекционные эндокардиты. М.: 2002 – 224 С.
5. Asperberro F., Begnette M., Oberhansli I et al. Fungal endocarditis in critically ill children // Eur. J.Pediatr.– 1999.– V.158. – N.1– P. 275–280.
6. Bitar F.F., Jawdi R.A., Dbaibo G.S. et al. Paediatric infective endocarditis: 19– years experience at a tertiare care hospital in a developing country // Acta Pediatr. – 2000.– V.89.– N.4.– P. 427–430.
7. Cabell C.H., Jollis J.G. Peterson G.E. Changing patient characterictics and the effectson mortality on infective endocarditis // Arch. Intern, Med.– 2002. – V. 162.– N. 1.– P. 90–94.
8.Dajani A.S., Taubert K.A., Wilson W. et al. Prevention of bacterial endocarditis: recommendations of American Heart Association. JAMA 1997; 277: 1794–1801.
9. Donal E., Coisne D., Valy Y. et al. Miocardial infarction caused by septic embolism during mitral endocarditis // Arch. Mal. Coeur. Vaiss. – 1999.– V.92.– N.3.– P. 253–257.
10. Durack D.T., Lukes A.S., Bright D.K. The Duke endocarditis service. New criteria for diagnisis of infective endocarditis: Utilization of specific echocardiografic findings // Am.J. Med.– 1994.– V. 96.– N.3.– P. 200–209.
11. Ferrieri P., Gewitz M.H., Gerber M.A. Unique Features of Infective Endocarditis in Childhood // Circulation.– 2002.– V.105.– N.24.– P.2115–2126.
12. Hoen B., Alla F., Selton – Suty C. et al. Changing profile of infective endocarditis. Results of a 1 –year syrvey in France // JAMA .– 2002.– V.228.– N.1.– P. 75–81.
13. Li J.S., Sexton D.J., Mick N et al. Proposed modification to the DUKE criteria for the diagnosis of infective endocarditis // Clin. Infect. Dis. – 2000– V. 30 (4).– P. 633–638.
14. Still T.L., LiPuma J.J. Endocarditis in children. In: D. Kaye, ed. Infective endocarditis. 2nd ed. NY, Raven Press,1992: 313–327.
15. William C.R. Epidemiology and Pathology of Infective Endocarditis // ACC Scientific Session 2000.– March 15.

По данным литературы заболеваемость ИЭ у взрослых составляет 1,7–6,5:100.000 населения в год, у подростков — более низкая, и составляет 3,0–4,3:1 млн. населения в год [3]. В то же время по данным, поступающим из крупных медицинских центров Европы и США, удельный вес ИЭ среди детей и подростков в специализированных стационарах постепенно нарастает, что связывают с увеличением числа операций на сердце при врожденных пороках, постоянным расширением спектра инвазивных диагностических и лечебных медицинских манипуляций, а также распространением внутривенной наркомании [4]. При этом мальчики заболевают эндокардитом в 2–3 раза чаще, чем девочки. Среди всех случаев эндокардита инфекционный генез составляет 25–40 %.
При современном ИЭ у детей и подростков наблюдается тенденция к учащению поражения митрального и трикуспидального клапанов, а также клапанов легочной артерии как в отдельности, так и в виде многоклапанного процесса. [2].
Несмотря на то, что в настоящее время подробно изучен патогенез всех типов инфекционного эндокардита (ИЭ), включая острый (ОИЭ) и подострый инфекционный эндокардит (ПИЭ), многие врачи не имеют четких представлений об использовании антибиотиков для профилактики ИЭ [1, 4]. Очень часто пренебрегаются фундаментальные принципы первичной антибиотикопрофилактики.
Целью исследования явилось изучениеклинических, лабораторных и инструментальных методов исследования, инфекционного эндокардита у детей в современных условиях.
Материалы иметоды исследования. Исследование проводилось при кафедре Госпитальной педиатрии № 2 на базе клиники ТашПМИ. В исследование были включены 8 детей с установленным диагнозом инфекционный эндокардит, находившихся на лечении с 2013 по 2016гг, и проведён ретроспективный анализ 12 историй болезни детей с диагнозом инфекционный эндокардит за период с 2010 по 2016гг.
Всем детям проводился комплекс клинико-лабораторных исследований включающий в себя посев крови на стерильность, при анализе результатов которого определились нижеследующие результаты.
Результаты иих обсуждение. Наиболее опасным возбудителем ИЭ является S. Aureus — именно с этим патогенном ассоциирован высокий риск летального исхода и инвалидизации. В последние годы его роль как лидирующего возбудителя ИЭ в отдельных регионах возрастает: этот микроорганизм является возбудителем ИЭ не менее чем в 40 % случаев. S. epidermidis встречается реже в 5 раз, чем S. aureus. Положительная гемокультура у больных с инфекционным эндокардитом выявлена в 40 %, из них: грам (+) флора в 69,6 %, грам (-) флора в 26,8 %, грибы рода Кандида в 3 %. Клинико-лабораторные септические и иммунокомплексные проявления при ИЭ, вызванные золотистым стафилококком и зеленящим стрептококком, предопределяют прогноз заболевания и ассоциируются с острым и подострым вариантами ИЭ. При ИЭ, вызванном грам (-) флорой, наблюдается высокий процент тромбоэмболических осложнений (33,3 %) и иммунокомплексных изменений (нефрит, полиартрит, геморрагический васкулит), которые ассоциируются с затяжным вариантом заболевания.
У 12 детей инфекционный эндокардит развился на фоне ВПС, при этом у 50 % отмечалисьпороками Фалло, ДМЖП у 25 %, аотральный стеноз отмечался у 8 % исследуемых. Наименьший риск ИЭ имеют пациенты с дефектом межпредсердной перегородки, открытым артериальным протоком.
Выявлены клинико-лабораторные особенности вторичного ИЭ: на фоне ВПС отмечался в 60 %, при врожденных пороках сердца: у половины больных ИЭ проявлялся гломерулонефритом, у трети — миокардитом, у четверти больных — суставным синдромом, на фоне ревматизма ИЭ определился в 33 % случаях и проявлялся наличием в 50 % постоянной формы фибрилляции предсердий, в 30 % — тромбоэмболических осложнений.
При ИЭ на фоне дисплазии соединительной ткани при пролапсе митрального клапана (ПМК) проявлялся в основном иммунокомплексными поражениями, а при двустворчатом аортальном клапане — умеренным септическим синдромом. Факторами риска неблагоприятного прогноза развития вторичного ИЭ являются: при ревматизме — митрально-аортальные пороки сердца, фибрилляция предсердий; врожденных пороках сердца — пороки сердца синего типа, возникновение ИЭ после перенесенных реконструктивных операций.
У 8 % исследованных имеются признаки ПМК — состояние, которое иногда является основанием для профилактического назначения антибиотиков. Несмотря на то, что в целом пациенты с ПМК не относятся к группе повышенного риска, ИЭ развивается у них в 5–10 раз чаще, чем в общей популяции. Пациенты, страдающие ПМК с регургитацией, нуждаются в проведении антибиотикопрофилактики. У 3 % пациентов с регургитацией и/или утолщением передней створки митрального клапана в конечном итоге развивается инфекционный эндокардит.
При клиническом исследовании особое внимание уделяется не только однократно фиксируемой аускультативной картине, но и ее динамике. В частности, в дебюте поражения первоначально не измененного аортального клапана может быть выслушан систолический шум по левому краю грудины, вероятно, обусловленный стенозированием устья аорты за счет вегетаций на полулунных клапанах. В дальнейшем появляется нежный протодиастолический шум в V точке с усилением при наклоне тела больного вперед; по мере усугубления клапанной деструкции интенсивность и продолжительность шума нарастает, отмечается ослабление II тона на аорте и снижение диастолического артериального давления.
При лечении инфекционного эндокардита назначение антибиотиков позволяет достигнуть стерилизации вегетаций в более чем 90 % случаев при ПИЭ и в 70 % при ОИЭ. Тем не менее, у 15–25 % пациентов, в конце концов, возникает необходимость в хирургической коррекции повреждённых клапанов сердца. Эти цифры значительно выше (70 %) при ИЭ у пациентов с искусственными клапанами сердца. Помимо этого, необходимо помнить об угрозе нарастания ИЭ, вызванных энтерококками, устойчивыми к антибиотикам, и метициллинорезистентыми S.aureus (MRSA). Очевидно, что гораздо легче предупредить развитие инфекции эндокарда, чем иметь дело с ранними и поздними осложнениями инфекционного эндокардита.
Заключение. Проведена углубленная оценка инфекционного эндокардита с клинико-лабораторных позиций на фоне ревматизма, врожденных пороков сердца, ИБС, дисплазии соединительной ткани сердца и выявлены факторы риска неблагоприятного прогноза. В настоящее время только 15–25 % случаев ИЭ возникают вторично, после проведения инвазивных процедур. Лишь у 50 % этих пациентов в анамнезе имеются указания на изменения со стороны клапанов сердца, что могло бы служить основанием для назначения антибиотиков с профилактической целью.
Таким образом, такое тяжелое, потенциально летальное заболевание должно быть курабельным. Для этого необходимы его раннее распознавание и активное, часто агрессивное лечение в соответствии с отечественными и международными рекомендациями.
- Гендлин Г. Е., Сторожаков Г. И., Прокофьева Е. В. и др. Предикторы отдаленного прогноза при протезировании клапанов у больных с ревматическим митральным пороком / сборник материалов IV Всероссийского съезда трансплантологов памяти академика В. И. Шумакова, 2008. — С. 53–54.
- Мелехов А. В., Гендлин Г. Е., Сторожаков Г. И. Эндокардит внутривенных наркоманов. // Росс. мед. журн. — 2007: выпуск: 42–45. 3.
- Соболева М. К., Белов Б. С. Инфекционный эндокардит у детей. РМЖ. 2006. — том 14. — № 8. — С. 630–636.
- Mylonakis E., Calderwood S. B. Infective endocarditis in adults // N. Engl. J. Med.- 2001.- Vol. 345.- P. 1318–1330.
Основные термины (генерируются автоматически): инфекционный эндокардит, врожденный порок сердца, MRSA, митральный клапан, назначение антибиотиков, пациент, ребенок, фон ВПС, фон ревматизма.
Читайте также:

