Профилактика инфекционных осложнений офтальмология
Обновлено: 18.04.2024
Оценена эффективность препарата Вигамокс® (моксифлоксацин) для профилактики инфекционных воспалительных осложнений у 809 больных с возрастными и осложненными катарактами после факоэмульсификации. Хорошая переносимость препарата и неосложненное течение послеоперационного периода позволяют рекомендовать Вигамокс® для профилактики бактериальных инфекций при хирургии катаракты.
- КЛЮЧЕВЫЕ СЛОВА: факоэмульсификация катаракты, фторхинолоны, Вигамокс, эндофтальмит, имплантация интраокулярных линз
Оценена эффективность препарата Вигамокс® (моксифлоксацин) для профилактики инфекционных воспалительных осложнений у 809 больных с возрастными и осложненными катарактами после факоэмульсификации. Хорошая переносимость препарата и неосложненное течение послеоперационного периода позволяют рекомендовать Вигамокс® для профилактики бактериальных инфекций при хирургии катаракты.
Рис. 2. Первый день после факоэмульсификации катаракты на фоне оперированной глаукомы, отек роговицы в области послеоперационного разреза
Однако, несмотря на успехи отечественной и зарубежной фармакотерапии, проблема пред- и послеоперационного ведения, а также профилактики инфекционных и воспалительных осложнений остается актуальной.
К наиболее тяжелому осложнению в хирургии катаракты относится развитие инфекционного воспалительного процесса – эндофтальмита, который встречается в 2–5 случаях на 1000 операций [1, 3, 4, 5]. В ходе многочисленных исследований доказано, что развитие эндофтальмита в хирургии катаракты, как правило, вызывают экзогенные факторы, обусловленные наличием потенциальных возбудителей инфекции век и конъюнктивальной полости
[6, 7]. Именно поэтому главное в профилактике эндофтальмитов – сократить численность бактериальной микрофлоры на поверхности глазного яблока [8, 9–11].
Большинство применяемых в офтальмологии антибиотиков имеют доказанную эффективность в отношении сокращения численности бактериальной флоры на поверхности глазного яблока [8, 12]. В настоящее время используются различные группы антимикробных препаратов: пенициллины, цефалоспорины, гликопептиды, аминогликозиды, макролиды, тетрациклины, сульфонамиды, триметоприм, пептидные антибиотики, хлорамфеникол. Однако надо иметь в виду, что антимикробную терапию затрудняет появление устойчивых форм микроорганизмов, развитие аллергии, присоединение грибковой инфекции [8, 13]. Все это требует использования препаратов, не только обладающих широким и мощным спектром действия, но и создающих высокую концентрацию в очаге воспаления при местном применении.
Названным требованиям в наибольшей степени удовлетворяют фторхинолоны – группа лекарственных средств с выраженной противомикробной активностью. По широте спектра противомикробного действия, активности и показаниям к применению они действительно близки к антибиотикам, но отличаются от них химической структурой и происхождением. Данные препараты являются производными налидиксовой кислоты, которая была синтезирована в 1962 г. и использовалась для лечения малярии. В результате различных модификаций были разработаны фторхинолоны широкого спектра действия, эффективные против грамотрицательных и грамположительных бактерий. Это фторхинолоны II поколения – ципрофлоксацин, офлоксацин, норфлоксацин и др. Широкое распространение названной группы лекарственных веществ позволило оптимизировать подготовку больных перед экстракцией катаракты [13, 14]. Тем не менее на протяжении последних десятилетий резистентность различных классов микроорганизмов к фторхинолонам прежних поколений возрастает из-за широкого системного применения при лечении общих заболеваний [3, 4, 7].
Таким образом, появление новых фторхинолонов – III и IV поколений – было продиктовано объективными причинами. Мишенью современных фторхинолонов служат бактериальные ферменты ДНК-гираза (тетрамер, состоящий из двух А- и двух В- полипептидных субъединиц) и топоизомераза 4 (тетрамер, состоящий из двух С- и двух Е-субъединиц). Эти ферменты отвечают за репликацию, генетическую рекомбинацию и восстановление ДНК большинства грамположительных, грамотрицательных и атипичных бактерий, а также ингибируют их рост от 2 до 6 часов после воздействия [15]. Кроме того, современные фторхинолоны обладают оптимизированной фармакокинетикой и высокой проникающей способностью во влагу передней камеры глаза [15, 16–19]. Такие свойства позволили Европейскому обществу катарактальных и рефракционных хирургов (European Society of Cataract and Refractive Surgeons, ESCRS) включить современные фторхинолоны в схему профилактики инфекционных осложнений при факоэмульсификации катаракты [5, 20].
Одним из препаратов фторхинолонового ряда IV поколения является Вигамокс ® (моксифлоксацин) (компания Alcon). Антибиотик обладает широким спектром антибактериального действия в отношении большинства инфекционных агентов, высокой проникающей способностью во все структуры глаза [16–19, 21].
Цель нашего исследования – оценить эффективность моксифлоксацина (препарата Вигамокс ® ) для профилактики инфекционных воспалительных осложнений в собственной практике при факоэмульсификации катаракты.
Материалы и методы
В течение 2011–2012 гг. под наблюдением находилось 809 пациентов с возрастными (226) и осложненными (583) катарактами.
Средний возраст больных – 67,7 ± 0,6 (от 19 до 87) года, средняя острота зрения без коррекции – 0,343 ± 0,07 (от 0,01 до 0,8) единиц, средний уровень внутриглазного давления – 18,7 ± 0,07 (от 14 до 22) мм рт. ст.
В структуру сопутствующей патологии у пациентов с осложненными катарактами входили глаукома различной стадии (у 149 пациентов – 18,4% случаев), в том числе ранее оперированная (у 91), псевдоэксфолиативный синдром (128–15,8%), дистрофия роговицы (47–5,8%), заболевания сетчатки и зрительного нерва (161–19,9%), травма (19–2,3%), увеит (13–1,6%), нарушения рефракции (66 пациентов – 8,2%). Большинство больных (633 пациента – 78,2% случаев) имели сопутствующие общие заболевания в стадии ремиссии: сахарный диабет обоих типов, бронхиальную астму, хронический бронхит, хронический синусит, заболевания почек и суставов, гипертоническую болезнь и др.
Факоэмульсификация катаракты с имплантацией ИОЛ выполнена всем 809 больным амбулаторно без осложнений на факоэмульсификаторе Infiniti Vision System компании Alcon по технологии Ozil IP через роговичный тоннель длиной 2,2 мм. Использовалась методика Phaco chop.
Операционное поле больного обрабатывали 5%-ным раствором повидон-йода (Бетадином) и 0,05%-ным раствором хлоргексидина, конъюнктивальную полость – 0,05%-ным раствором антисептика Витабакта, специальными стерильными салфетками ограничивали операционное поле с изоляцией ресниц.
Для профилактики инфекционного воспаления применяли следующую схему лечения: за 2 дня до операции всем больным назначали закапывание в конъюнктивальную полость 0,5%-ного раствора антибиотика Вигамокс ® 4 раза в день. Непосредственно перед операцией (за 60 и 30 минут) и сразу после нее проводили инстилляции антибиотика. В послеоперационном периоде после факоэмульсификации катаракты с имплантацией ИОЛ к фторхинолону Вигамокс ® , который назначался в течение недели 4 раза в день, добавляли стероидные противовоспалительные средства (0,1%-ный раствор дексаметазона) в течение 2 недель и нестероидные противовоспалительные препараты (0,1%-ный раствор индометацина) 4 раза в день в течение месяца.
Пациенты находились под офтальмологическим контролем в 1-й, 3-й, 7-й дни и через четыре недели после операции. Оценивались клиническое течение послеоперационного периода и субъективные ощущения больных на фоне инстилляций препарата Вигамокс ® до и после операции.
Клинически течение раннего послеоперационного периода у большинства больных проходило ареактивно (рис. 1). Анализ результатов измерения внутриглазного давления, остроты зрения, данных биомикроскопии не выявил никаких патологических изменений, связанных с местным офтальмологическим применением раствора Вигамокс ® . При этом в большинстве случаев отсутствовала перикорнеальная инъекция глазного яблока при всех типах операций (таблица). Отмечались прозрачность роговицы или ее легкий отек в области операционного разреза (рис. 2).
После факоэмульсификации катаракты влага передней камеры в 97,3% случаев была прозрачной и лишь в 2,7% отмечался феномен Тиндаля 1–2-й степени (рис. 3).
На фоне более интенсивных инстилляций Вигамокса (до 6–8 раз в день), глюкокортикостероидов, нестероидных противовоспалительных препаратов и мидриатиков воспалительную реакцию удалось купировать в течение 2–3 дней.
Анализ результатов не выявил каких-либо изменений или выраженных признаков раздражения глаз, связанных с лечением, ни до, ни после операции. Субъективно большинство больных хорошо переносили препарат, и только в единичных случаях еще на дооперационном этапе отмечались кратковременные умеренные боли или жжение при закапывании препарата Вигамокс ® .
Зрительные функции после операции улучшились у всех пациентов. Максимальная корригированная острота зрения 0,4–1,0 в первый послеоперационный день была достигнута в 88,4% случаев (715 больных). Послеоперационная острота зрения менее 0,4, как правило, имела место при патологии сетчатки и зрительного нерва.
На сегодняшний день подавляющее большинство диагностических, лечебных и хирургических манипуляций в офтальмологии проводятся в амбулаторных условиях, поэтому к профилактике и лечению бактериальных инфекций глаз предъявляются повышенные требования [7, 20].
По данным многочисленных исследований, основной причиной воспалительных осложнений при факоэмульсификации катаракты является проникновение микроорганизмов из конъюнктивальной полости или наружных источников – инструментов, расходных материалов, ИОЛ [1, 3, 8]. Цель профилактического применения антибактериальных средств – максимально снизить бактериальную интервенцию во время операции и в ближайший послеоперационный период (через края раны).
В последние годы антибактериальные препараты фторхинолонового ряда обычно используются в катарактальной и рефракционной хирургии в виде инстилляций [6, 8, 10, 22]. Основными аргументами в пользу их широкого использования с целью профилактики послеоперационных осложнений в офтальмохирургии являются доказанная активность в отношении грамположительных и грамотрицательных бактерий, а также высокая проникающая способность во влагу передней камеры [6, 15, 16, 21]. Так, многоцентровое исследование показало, что после назначения фторхинолонов до операции достоверно снижался уровень микроорганизмов в конъюнктивальной полости и, как следствие, уменьшалось число эндофтальмитов после операций по поводу катаракты [5, 20]. Предложенная ESCRS схема профилактики инфекционных осложнений с включением фторхинолонов была также использована в нашей клинической практике у 809 больных с возрастными и осложненными катарактами до, во время и после факоэмульсификации. Отмечалась хорошая переносимость и высокая эффективность фторхинолонов в профилактике воспалительных осложнений [10, 11].
Фторхинолоны IV поколения, в частности моксифлоксацин (Вигамокс ® ), внедренный в офтальмологическую клиническую практику в 2011 г., сегодня занимают первую линию антимикробной обороны в офтальмохирургии благодаря широкому спектру действия, хорошей переносимости и минимальному токсическому воздействию на глаза [9, 12, 16–19].
В собственной практике в качестве предоперационной подготовки Вигамокс ® назначали, как правило, за 2 дня до операции и применяли в течение 1 недели после нее. Препарат оказывал щадящее воздействие на поверхность глаза. Большинство пациентов отмечали хорошую субъективную переносимость, отсутствие жжения и затуманивания зрения при инстилляциях. Низкая токсичность препарата обусловлена его высокой растворимостью при нейтральном уровне рН среды. Клинически у большинства больных отсутствовали инъекция глазного яблока и отек роговицы, лишь в 2,7% случаев имела место реакция глаза (ирит) на операционную травму в виде феномена Тиндаля 1–2-й степени.
Современные фторхинолоны, в частности препарат Вигамокс ® (моксифлоксацин), с широким спектром действия, хорошей переносимостью и минимальным токсическим действием на глаза, применяемые в клинической практике в комплексе с антисептическими мероприятиями, обеспечивают достаточный уровень микробиологической эрадикации возбудителей и эффективны для профилактики инфекционных осложнений в хирургии катаракты.
Антибактериальная профилактика инфекции глаза после травмы
Среди антибактериальных лекарственных средств, использующихся при профилактике и лечении внутриглазных инфекционных поражений, ведущее место продолжают занимать различные антибиотики. Однако в связи с появлением в последние годы большого числа антибиотикорезистентных штаммов микроорганизмов, некоторые антибиотики, широко известные в медицине, утрачивают свое практическое значение. Число устойчивых штаммов бактерия продолжает расти.
Следовательно, применение данных лекарственных средств в клинической офтальмологии должно осуществляться под строгим контролем чувствительности к ним микроорганизмов. Но общепринятые методы бактериологического исследования, направленного на определение чувствительности возбудителя инфекции к антибиотикам, требуют, как известно, продолжительного времени (нескольких суток). Эффективность же профилактики внутриглазных инфекционных поражений в значительной степени зависит от того, насколько рано применяются соответствующие антибактериальные препараты.
В данных обстоятельствах с целью профилактики инфекционных осложнений после проникающих ранений глаза офтальмологи вынуждены прибегать к использованию антибиотиков без строгого учета чувствительности к ним микроорганизмов, внедрившихся в полость глазного яблока. Это, естественно, отрицательно сказывается на эффективности профилактики внутриглазной инфекции.
При всех прободных ранениях глаза до получения результатов бактериологического исследования чувствительности к антибиотикам выделенных микроорганизмов необходимо применение с целью профилактики внутриглазной инфекции антибактериальных препаратов, обладающих широким спектром действия. Наиболее эффективными из них являются препараты, относящиеся к группе амиyогликозидов, например, гентамицин. Гентамиции выпускается отечественной промышленностью, обладает широким спектром действия, подавляя рост большинства грамположитнльных и грамотрицательных микроорганизмов, в том числе синегнойной палочки.
Как современный высокоактивный антибиотик, гентамиции в качестве одного из основных антибактериальных лекарственных средств был включен в разработанную нами систему профилактики посттравматической бактериальной инфекции (Южаков А. М.) и широко применяется в настоящее время.
В эксперименте при изучении вопроса о влиянии сроков профилактического применения антибактериальных препаратов на частоту возникновения внутриглазной инфекции установлено, что инъекции антибиотиков (например, пенициллина, мономицина) или нитрофуранов (фуракрилина) в стекловидное тело предупреждали развитие инфекционного процесса во всех случаях, если препараты вводились в первые 3-6 ч после интравитреального заражения глаза культурой вирулентного стафилококка.
Если же указанные препараты вводились через более продолжительное время, то профилактический аффект резко снижался (Джалиашнили О. А., Корнилова А. Ф., Майчук Ю. Ф.).
По данным А. А. Куглеева, П. И. Лебехова, среди пострадавших с проникающими ранениями глаза, у которых применение антибиотиков было начато в течение первых суток после травмы, развитие эндофтальмита имело место в 6,6% случаев, тогда как при более поздней антибиотикотерапии внутриглазная инфекция была отмечена почти в 7 раз чаще (43,2%). Даже применением нескольких антибиотиков часто не удается купировать инфекционный процесс, если пострадавший с проникающим ранением глазного яблока направляется к окулисту для оказания помощи не в первые 6 ч после травмы (Кроль А. Г, Каган Л. Е.). По мнению А. Ф. Корниловой и соавт., на частоту развития внутриглазного гнойного процесса, главным образом, оказывает влияние не хирургическая обработка раны, которая определяется размерами последней, а сроки проведения профилактической антибактериальной терапии.
Все эти данные, как и многочисленные сведения других авторов, свидетельствуют о необходимости самого раннего применения антибактериальных препаратов для профилактики инфекции глаза после его проникающего ранения.
Концентрация антибактериального препарата в тканях глаза находится в прямой зависимости от метода его введения. По данным литературы, при профилактике внутриглазной посттравматической инфекции целесообразно сочетание общего назначения антибиотиков с их местным применением. Анализ материала архива Московского научно-исследовательского института глазных болезней им. Гельмгольца подтверждает эффективность такого сочетания.
Известно, что при общей антибиотикотерапии лишь незначительное количество лекарственного вещества проникает в полость глазного яблока. Кроме того, в случаях общего назначения антибиотиков необходимо иметь в виду возможность их токсического действия на внутренние органы, развития аллергической или даже анафилактической реакции со стороны организма. По мнению большинства офтальмологов, методы местного применения антибиотиков, как обеспечивающие наибольшее накопление препарата в тканях глазного яблока, имеют наиболее важное значение.
С учетом данного обстоятельства, мы сочли возможным при разработке собственной эффективной системы профилактики внутриглазной посттравматической инфекции отказаться от общего назначения антибиотиков, уделив основное внимание рациональному выбору местного способа применения гентамицина (как показано выше, наиболее эффективного и доступного в настоящее время антибиотика) в зависимости от клинической картины прободной травмы глаза. Эффективность антибактериального действия антибиотика на микроорганизмы, занесенные в глазное яблоко при его проникающем ранении, определяется, как известно, чувствительностью бактерий к применяемому препарату и концентрацией последнего во внутриглазных жидкостях.
Содержание антибиотика в полости глаза должно быть обеспечено на уровне, соответствующем подавляющей концентрации препарата в отношении потенциального возбудителя внутриглазной инфекции.
Приведенные выше исследования по фармакокинетике гентамицина показали, что подконъюнктивальное введение позволяет обеспечить концентрацию препарата во влаге передней камеры глаза на достаточно высоком терапевтическом уровне. Минимальная подавляющая концентрация (МПК) гентамицина в отношении различных штаммов стафилококка, кишечной и синегнойной палочки, вызывающих наиболее опасные и тяжело протекающие инфекционные поражения глаза, находятся в довольно больших пределах: для Staphylococcus aureas МПК гентамицина составляет 0,1-16 мкг/мл, для Escherichia coli — 2-10 мкг/мл, для Pseudomonas aeruginosa — 2-16 мкг/мл. Для наиболее чувствительных штаммов указанных микроорганизмов МПК гентамицина составляет 0,03; 0,2 и 0,1 мкг/мл соответственно.
Однако исследование лекарственной чувствительности микроорганизмов и определение соответствующей МПК антибактериального препарата требуют значительного времени (несколько суток). Кроме того, как показали результаты проведенных нами исследований по изучению микрофлоры при проникающих ранениях глазного яблока, более чем в половине случаев прободных травм глаза выявляется микрофлора, имеющая смешанный характер.
В этой связи при осуществлении профилактики внутриглазной посттравматической инфекции приходится ориентироваться на средний уровень подавляющей концентрации препарата. Концентрация гентамицина на среднем уровне 4 мкг/мл является активной одновременно в отношении большинства штаммов микроорганизмов. Сопоставление данной концентрации с полученными результатами исследований по изучению фармакокинетики гентамицина во влаге передней камеры и в стекловидном теле позволило определить рациональный выбор метода и режима введения данного антибиотика, обеспечивающих оптимальное терапевтическое воздействие препарата на внутриглазную микрофлору при ее локализации в переднем или заднем отделах глазного яблока.
Проведенное нами исследование фармакокинетики гентамицина показало, что из исследованных методов его введения в принятых клинических дозах наибольшее практическое значение при воздействии на внутриглазную микрофлору имеют инъекции данного препарата под конъюнктиву и в стекловидное тело. Оптимальные терапевтические концентрации антибиотика (активные в отношении большинства штаммов микроорганизмов) в случаях введения гентамицина иод конъюнктиву наблюдались, в основном, во влаге передней камеры глаза.
Содержание антибиотика в камерной влаге достигало оптимального терапевтического уровня достаточно быстро после подконъюнктивального введения 20 мг гентамицина — через 3 ч после инъекции. При этом было показано, что для поддержания концентрации препарата на терапевтическом уровне необходимы повторные введения антибиотика не менее 2 инъекций в сутки.
В стекловидном теле концентрации антибиотика, являющиеся подавляющими в отношении большинства штаммов микроорганизмов, были получены лишь при интравитреальных инъекциях гентамицина. Высокое содержание антибиотика в стекловидном теле наблюдалось в первый же час с момента интравитреального введения гентамицина в доле 0,4 мг. При данном методе введения препарата его концентрация в стекловидном теле сохранялась на оптимальном терапевтическом уровне в течение длительного времени (не менее 4 сут с момента инъекции).
Содержание гентамицина во влаге передней камеры при его интравитреальном введении было значительно ниже, чем в стекловидном теле, но все же достигало уровня, соответствующего подавляющей концентрации препарата в отношении большинства штаммов микроорганизмов. Однако эта концентрация наблюдалась лишь через 9-12 ч с момента инъекции антибиотика. Спустя 24 ч после интравитреалыюго введения препарат обнаруживался в камерной влаге в концентрациях, являющихся активными только в отношении наиболее чувствительных к гентамицину штаммов микроорганизмов.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Профилактика посттравматической инфекции глаза
По материалам отдела травматологии, реконструктивной и пластической хирургии и глазного протезирования Московского научно-исследовательского института глазных болезней им. Гельмгольца за последние 20 лет была подтверждена чрезвычайно важная роль ранней хирургической обработки прободной раны глаза в профилактике посттравматической внутриглазной инфекции. Как показали клинические наблюдения, при первичной хирургической обработке проникающих ран глазного яблока, выполненной в первые сутки после травмы, инфекционные осложнения развились у 3,2% пострадавших. Если же хирургическую обработку производили на вторые сутки и позже после ранения, частота развития внутриглазной инфекции резко увеличивалась, составляя 21% и более.
Подобная закономерность отмечена и многими другими офтальмологами. Так, Я. К. Варшавский отмечает, что частота обнаружения клинических признаков инфекции зависит от сроков госпитализации после проникающего ранения глазного яблока: если госпитализация пострадавшего осуществлялась в первый день после травмы, инфекция глаза развивалась в 1,7% случаев, на второй день — в 28,5%, после четвертого дня — в 50% случаев. По данным В. И. Поспелова и соавт., при оказании квалифицированной офтальмологической помощи пострадавшим с ранениями глазного яблока в первые 6 ч, первые сутки, 2-3 суток после травмы частота развития гнойной инфекции составляла 7,2; 18,2 и 24,9% соответственно.
На большую роль ранней хирургической обработки в предотвращении внутриглазной инфекции после прободной травмы глаза указывают многие авторы. Так, опыт оказания медицинской помощи в Афганистане показал, что gри первичной хирургической обработке прободных ранений глаза, проведенной позднее 12 ч с момента ранения, риск развития эндофтальмита увеличивается в 10 раз, а наиболее благоприятных результатов удается достигнуть при условии обработки ранений в течение первых 3 ч с момента получения ранения.
По мнению большинства современных авторов, на частоту развития внутриглазного гнойного процесса в основном оказывает влияние не хирургическая обработка раны, которая определяется размером последней и характером повреждения структур глаза, а сроки проведения профилактической антибактериальной терапии.
Установлено, что клиническая форма развития внутриглазной инфекции в виде гнойного иридоциклита или эндофтальмита зависит от зоны проникающего ранения глазного яблока, внедрения инородного тела и его локализации (Южаков А. М.). Одним из факторов, способствующих распространению инфекции из переднего на задний отдел глаза, является повреждение хрусталика или цинновой связки, выполняющих, как известно, в нормальных условиях роль естественного анатомического барьера между передним и задним отделами глазного яблока. С другой стороны, известно, что набухающие массы поврежденного хрусталика отягощают течение внутриглазного инфекционного процесса и являются, кроме того, достаточно благоприятной средой для роста микроорганизмов.
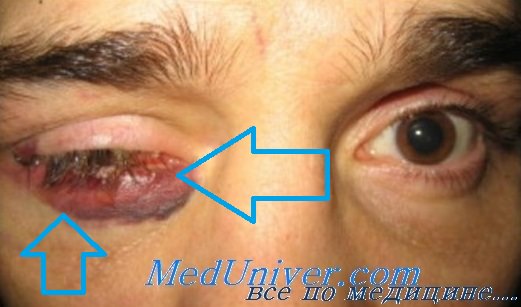
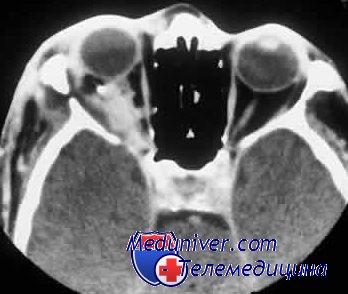
Проведенные в отделе травматологии Московского научно-исследовательского института глазных болезней им. Гельмгольца исследования показали, что если прободная травма глазного яблока не сопровождается внедрением в глаз инородного тела, то в случаях локализации раны в зоне роговицы инфекция чаще всего протекает в виде иридоциклита. При ранениях в роговично-склеральной зоне частота гнойного иридоциклита и эпдофтальмита примерно одинакова. При проникающих ранениях склеры более 8 мм от лимба инфекция, как правило, протекает в виде эндофтальмита.
Анализ случаев внутриглазных инфекционных осложнений после прободных травм, сопровождающихся внедрением в глаз осколка при его локализации в цилиарyом теле, стекловидном теле, во внутренних оболочках глазного яблока, показал, что инфекционный процесс независимо от зоны ранения у большинства больных протекает в виде эндофтальмита. Если осколок, внедрившийся в глаз в результате ранения роговицы, локализуется в передней камере, то инфекция в большинстве случаев протекает в виде гнойного иридоциклита. При локализации инородного тела в хрусталике инфекция чаще всего протекает в виде эпдофтальмита.
Следовательно, профилактика внутриглазных инфекционных осложнений после проникающих ранений глазного яблока в зоне роговицы без внедрения или с внедрением в глаз инородного тела с его локализацией в передней камере при сохранности хрусталика, особенно его задней капсулы и цинновой связки, должна быть направлена, главным образом, на предупреждение гнойного иридоциклита.
При ранениях роговицы без внедрения в глаз инородного тела, но сопровождающихся повреждением хрусталика с разрывом задней капсулы или повреждением цинновой связки, необходима профилактика внутриглазной инфекции как переднего, так и заднего отделов глазного яблока. В случаях прободных травм, не сопровождающихся внедрением в глаз инородного тела, при локализации раны в роговично-склеральной зоне профилактика инфекции также должна быть направлена на предупреждение одновременно иридоциклита и эпдофтальмита. При проникающих ранениях глазного яблока в области склеры (более 8 мм от лимба) в основном необходима профилактика внутриглазной инфекции заднего отдела глаза.
В случаях прободных травм, сопровождающихся внедрением в глаз осколка с его локализацией в хрусталике, цилиарном теле, стекловидном теле, а также во внутренних оболочках глазного яблока, независимо от зоны ранения необходима профилактика эндофтальмита как наиболее часто наблюдающейся клинической формы внутриглазной инфекции при таких травмах.
Таким образом, каждый случай проникающего ранения глазного яблока при осуществлении соответствующей профилактики внутриглазных инфекционных осложнений требует к себе дифференцированного подхода в зависимости от клинической картины травмы. При одних прободных травмах глаза необходимо создание терапевтической концентрации антибактериального лекарственного вещества преимущественно или во влаге передней камеры, или в стекловидном теле, при других — во внутриглазных жидкостях как переднего, так и заднего отделов глазного яблока одновременно.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Частота инфекционных осложнений операций на глазах
По данным М. Л. Цитовского, Н. А. Плетневой, Н. И. Артемьева и Ф. X. Капкаевой, М. Г. Рабинович и др., внутриглазной гнойный процесс осложняет экстракцию катаракты в 0,2-2% случаев. По наблюдениям зарубежных авторов (Bonamour, Royer, Mangieracine, Allen, Sloene), частота внутриглазной инфекции после данной операции колеблется в пределах от 0,08 до 0,5%. Peyman et al. сообщают о более высокой частоте этого осложнения после экстракции катаракты (3-6%), что авторы связывают с условиями проведения оперативного вмешательства в сельских глазных амбулаториях.
Внутриглазные гнойные процессы возникают также после антиглаукоматозных операций фистулизирующего типа. При этом инфекция может развиться как в первые дни послеоперационного периода, так и спустя много лет после хирургического вмешательства. По данным Е. А. Буйвида, А. Л. Канкрова, В. П. Одинцова, Е. Н. Киселевой и др., поздняя гнойная инфекция после операции трепанации склеры по Элиоту наблюдалась в среднем в 2,27% случаев.
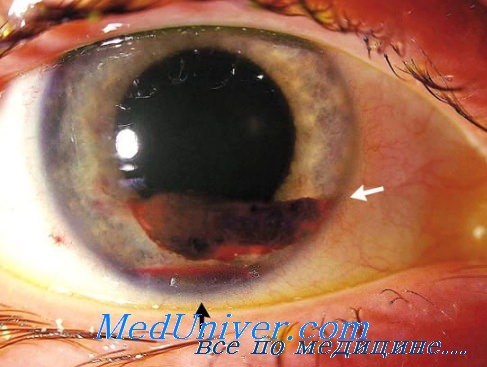
По материалам клиники глазных болезней 1 ММИ им. И. М. Сеченова, внутриглазная инфекция после иридосклерэктомии в модификации А. И. Покровского отмечена в 0,4% случаев (Гринберг Э. М.). Sloene et al. наблюдали развитие бактериального эндофтальмита после антиглаукоматозных операций фильтрующего типа у 1-18% больных. Фактором, способствующим развитию поздней внутриглазной инфекции после хирургических вмешательств данного вида, является образование тонкостенной кистевидной фильтрационной подушечки, через которую возможно внедрение в полость глаза микроорганизмов (Гринберг Э. М., Ершкович И. Г., Kanski и др.).
По данным Abel, Binder, Bellows, частота развития внутриглазной инфекции после различных хирургических вмешательств, сопровождающихся вскрытием полости глазного яблока, составляет в среднем 0,3%. При этом гибель глаза наступает в 66% случаев внутриглазного инфекционного поражения.
Однако исходы послеоперационных гнойных процессов так же тяжелы, как и в случаях инфицированных прободных травм глазного яблока. В результате внутриглазного инфекционного процесса слепота и гибель глаза при них наступают в 53,4-89,4% случаев.
Как видно из приведенного выше материала, профилактика и лечение внутриглазной инфекции после проникающих ранений глазного яблока и различных хирургических вмешательств, сопровождающихся вскрытием глазной полости, продолжают оставаться актуальной проблемой клинической офтальмологии.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
На основании собственного опыта проведения кераторефракционных операций у 274 больных с аномалиями рефракции авторы разработали схему профилактики инфекционных осложнений: за день до операции – инстилляции 0,5%-ного раствора антибиотика моксифлоксацин (Вигамокс®) в дозе 1–2 капли 4 раза в день; за 60 и 30 минут перед операцией и сразу после нее – инстилляции моксифлоксацина; в поcлеоперационном периоде – инстилляции моксифлоксацина 4 раза в день в течение 7 дней. Хорошая переносимость и высокая эффективность препарата Вигамокс® позволяют рекомендовать его в качестве монотерапии в профилактике воспалительных осложнений при кераторефракционных операциях.
- КЛЮЧЕВЫЕ СЛОВА: кераторефракционные операции, Вигамокс, фторхинолоны
На основании собственного опыта проведения кераторефракционных операций у 274 больных с аномалиями рефракции авторы разработали схему профилактики инфекционных осложнений: за день до операции – инстилляции 0,5%-ного раствора антибиотика моксифлоксацин (Вигамокс®) в дозе 1–2 капли 4 раза в день; за 60 и 30 минут перед операцией и сразу после нее – инстилляции моксифлоксацина; в поcлеоперационном периоде – инстилляции моксифлоксацина 4 раза в день в течение 7 дней. Хорошая переносимость и высокая эффективность препарата Вигамокс® позволяют рекомендовать его в качестве монотерапии в профилактике воспалительных осложнений при кераторефракционных операциях.
Рис. 1. Состояние роговицы на первый день после операции, проведенной по технологии а) ReLEx, б) Femto-LASIK, в) LASIK
На сегодняшний день среди антибактериальных препаратов для профилактики внутриглазных инфекций в офтальмохирургии предпочтение отдано фторхинолонам, которые имеют широкий спектр активности в отношении грамположительных и грамотрицательных бактерий. Европейское общество катарактальных и рефракционных хирургов (European Society of Cataract and Refractive Surgeons, ESCRS) рекомендовало схему применения фторхинолонов для профилактики послеоперационных инфекционных осложнений при кераторефракционной хирургии [1, 2].
Однако на протяжении последних десятилетий наблюдается рост резистентности различных классов микроорганизмов к фторхинолонам прежних поколений из-за их широкого системного применения при лечении общих заболеваний [2, 3]. В связи с этим появление нового, четвертого, поколения фторхинолонов, одним из представителей которых является препарат моксифлоксацин (Вигамокс ® , компания Аlcon), продиктовано объективными причинами.
Целью исследования явилась оценка эффективности препарата Вигамокс ® (моксифлоксацин) в качестве монотерапии для профилактики инфекционных воспалительных осложнений в кераторефракционной хирургии.
Материалы и методы
В течение 2010–2012 гг. под наблюдением находились 274 пациента (522 глаза), которым выполнены кераторефракционные операции по разным технологиям – топографический LASIK (Laser-Assisted in Situ Keratomileusis – лазерный кератомилез) (134 глаза), топографический Femto-LASIK (229 глаз), внутрироговичная фемтосекундная коррекция ReLEx (159 глаз) (табл. 1).
В группе, в которую вошли 134 больных после топографического LASIK, возраст пациентов в среднем составил 26,7 ± 0,6 (от 19 до 38) года, средняя острота зрения без коррекции – 0,143 ± 0,07 (от 0,01 до 0,2), средний уровень внутриглазного давления – 18,7 ± 0,07 (от 14 до 22) мм рт. ст. (табл. 2).
У 104 (38,2%) пациентов, которым выполнена периферическая профилактическая, ограничительная лазеркоагуляция сетчатки, диагностирована периферическая хориоретинальная дистрофия сетчатки (в структуре сопутствующей патологии).
Рефракционные операции выполнялись по технологии LASIK с помощью микрокератома Zyoptix (фирма Bausch & Lomb) и на эксимерном лазере MEL 80 с CRS-Master (Atlas) (фирма Carl Zeiss). С 2011 г. с появлением фемтосекундного лазера VisuMax (фирма Carl Zeiss) перешли на технологии Femto-LASIK и ReLEx (полностью фемтосекундная операция для устранения миопии без использования эксимерного лазера).
Операционное поле больного обрабатывали 5%-ным раствором повидон-йода (Бетадин) и 0,05%-ным раствором хлоргексидина, конъюнктивальную полость – 0,05%-ным раствором антисептика пиклосидин (Витабакт), специальными стерильными салфетками ограничивали операционное поле с изоляцией ресниц.
С целью профилактики инфекционного воспаления за день до операции всем больным назначались закапывания в конъюнктивальную полость 0,5%-ного раствора антибиотика Вигамокс® по 1–2 капли 4 раза в день. Препарат представляет собой изотонический раствор, содержащий борную кислоту, натрия хлорид и 0,5%-ный раствор моксифлоксацина с рН 6,8. Антибиотик оказывает широкое антибактериальное действие в отношении большинства инфекционных агентов, обладает высокой проникающей способностью во все структуры глазного яблока [4]. Непосредственно перед операцией (за 60 и 30 минут) и сразу после нее продолжали инстилляции антибиотика. В послеоперационном периоде использовали следующую схему инстилляций препарата Вигамокс ® : 4 раза в день в течение 7 дней. Таким образом, препарат Вигамокс® использовали в качестве монотерапии.
Пациенты находились под офтальмологическим контролем в первый, третий, седьмой день и через четыре недели после проведения операции. Оценивались субъективные ощущения больных на фоне инстилляций препарата Вигамокс ® – до операции и после нее – и клиническое течение послеоперационного периода. Анализ результатов не выявил каких-либо изменений или выраженных признаков раздражения глаз, связанных с лечением, как до операции, так и после нее. Субъективно большинство больных хорошо переносили препарат, и только в единичных случаях (2,3%) отмечались умеренные боли или жжение при закапывании препарата Вигамокс ® (табл. 3).
Клинически течение раннего послеоперационного периода во всех группах проходило ареактивно (рис. 1 А, Б, В). Анализ результатов внутриглазного давления, остроты зрения, данных биомикроскопии не выявил никаких патологических изменений, связанных с местным применением препарата. В группах после операций Femto-LASIK и ReLEx практически отсутствовала перикорнеальная инъекция глазного яблока, роговица сохраняла прозрачность после операции по технологии Femto-LASIK у 95,6% пациентов, а после операции по технологии ReLEx – в 98,1% случаев. Полученные результаты достигались за счет высокой точности и деликатности процедуры (табл. 4 А, Б). Для сравнения: в группе после механического LASIK отмечался легкий отек в области начала формирования роговичного разреза в 14,9% случаев и самого клапана в 2,9% случаев, реакцию удалось купировать в течение 2–3 дней после добавления стероидных инстилляций (рис. 2).
Зрительные функции после операции улучшились у всех пациентов. Максимальная некорригированная острота зрения 0,8–1,0 в первый послеоперационный день достигнута в 94,9% (260 больных) случаев после всех видов рефракционных операций. Острота зрения менее 0,8 обусловлена амблиопией.
На сегодняшний день подавляющее большинство диагностических, лечебных и хирургических манипуляций в офтальмологии проводятся в амбулаторных условиях, поэтому к профилактике и лечению бактериальных инфекций глаз предъявляются повышенные требования [5, 6].
По данным многочисленных исследований, наиболее частой причиной воспалительных осложнений в офтальмохирургии является проникновение микроорганизмов из конъюнктивальной полости или из наружных источников – инструментов, расходных материалов [1, 7, 8]. Задачей применения антибактериальных средств для профилактики воспаления является максимальная возможность снижения бактериальной интервенции во время проведения операции и через края раны в ближайший послеоперационный период.
Доказанную эффективность в отношении сокращения бактериальной флоры на поверхности конъюнктивы имеют большинство применяемых в офтальмохирургии антибиотиков, которые до настоящего времени довольно часто применяются в виде подконъюнктивальных инъекций в конце операции. Однако данный метод, по нашему мнению, необоснован, поскольку однократное использование антибиотика не может создать его оптимальную концентрацию во внутриглазных структурах, адекватную для профилактики инфекционных осложнений в офтальмохирургии.
В последние годы антибактериальные препараты фторхинолонового ряда чаще всего используются в катарактальной и рефракционной хирургии в виде инстилляций [5, 4, 9]. Основными аргументами для их широкого использования с целью профилактики послеоперационных осложнений в офтальмохирургии являются доказанная активность в отношении как грамположительных, так и грамотрицательных бактерий, а также высокая проникающая способность во влагу передней камеры [1, 5, 10]. Так, многоцентровое исследование показало, что назначение фторхинолонов до операции достоверно снижает уровень микроорганизмов в конъюнктивальной полости и, как следствие, приводит к уменьшению числа послеоперационных осложнений. Предложенная Европейским обществом катарактальных и рефракционных хирургов (ESCRS) схема профилактики инфекционных осложнений с включением фторхинолонов была также использована в нашей клинической практике у 274 больных с аномалиями рефракции до, во время и после проведения кераторефракционных операций. Полученные данные позволяют говорить о хорошей переносимости и высокой эффективности препарата Вигамокс ® в качестве монотерапии в профилактике воспалительных осложнений [2, 9, 11].
Внедренные в клиническую практику в 2011 г. фторхинолоны четвертого поколения (в частности, моксифлоксацин – Вигамокс ® ) заняли в настоящее время первую линию антимикробной обороны в офтальмохирургии благодаря широкому спектру действия, хорошей переносимости и минимальному токсическому воздействию на глаза [4, 6].
Настоящая работа показывает хорошую переносимость препарата Вигамокс ® , отсутствие субъективных жалоб во время инстилляций и неосложненное течение послеоперационного периода при кераторефракционной хирургии, что позволяет рекомендовать применение препарата в большинстве случаев в виде монотерапии для профилактики бактериальной инфекции при всех типах кераторефракционных операций.
Читайте также:

