Профилактика инфекционных заболеваний в лаборатории
Обновлено: 23.04.2024
Лабораторные исследования при инфекционных заболеваниях. Методы
Отбор проб для анализа при инфекционных заболеваниях. Для микробиологического исследования может быть отобрана любая ткань или физиологическая жидкость организма.
Выделение чистой культуры способствует увеличению количества бактерий и их точной идентификации. Для этого используют питательные среды. Если в образце присутствует нормальная микрофлора, то применяют избирательные (селективные) среды, позволяющие создать условия, неблагоприятные для роста непатогенных микроорганизмов и способствующие росту патогенной микрофлоры.
Для получения точных результатов следует выбрать оптимальный метод отбора проб и подойти к этому процессу с должной аккуратностью. При несоблюдении правил асептики контаминация проб крови микроорганизмами извне может привести к назначению неправильного лечения.
Большинство бактерий не способны существовать вне организма хозяина: облигатные анаэробы погибают под действием кислорода воздуха, а некоторые возбудители очень чувствительны к высыханию (Neisseria gonorrhoeae). Именно поэтому анализируемые образцы сразу после отбора должны быть помещены на подходящие среды или посеяны на среды для транспортировки.
Лабораторные методы исследования при инфекционных заболеваниях
Образцы могут быть проанализированы невооружённым глазом (например, для определения взрослых гельминтов в фекалиях или крови в мокроте). Микроскопия — быстрый и недорогой метод исследования, но требует высокого технического мастерства, характеризуется низкой чувствительностью: для точного определения необходимо присутствие большого количества возбудителей.
Кроме того, очень часто условно-патогенные микроорганизмы принимают за патогенные, что связано с недостаточной специфичностью метода.
Для определения возбудителя могут быть использованы различные красители (например, аурамин или окрашивание по Цилю—Нильсену для идентификации микобактерий). Уротропиновый серебряный окрашивает хитин клеточной стенки грибов и Pneumocystis jiroveci. Краситель Гимза применяют для окрашивания возбудителей малярии, лейшманий и других паразитов.
В основе иммунофлюоресцентного метода лежит применение специфических антител, помеченных флюоресцентными маркёрами. Микроскопию осуществляют в ультрафиолетовом свете, при этом возбудитель и связанные с ним антитела светятся ярко-зелёным цветом.
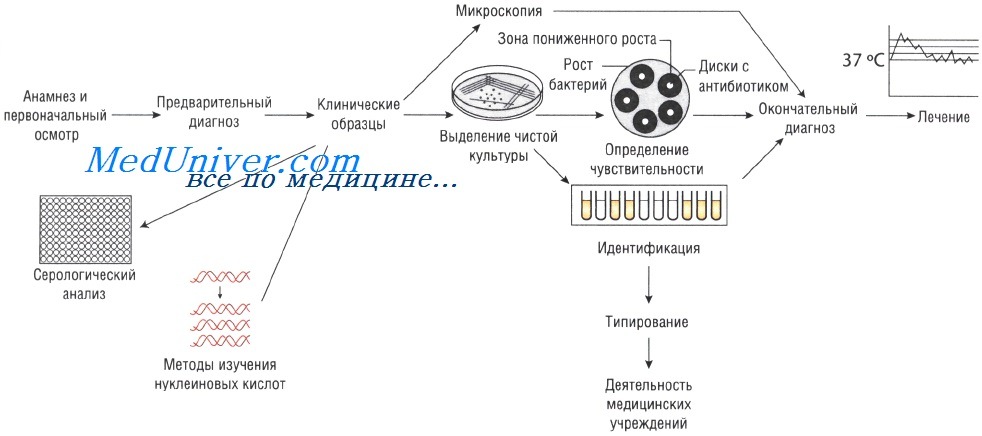
Лабораторные исследования при инфекционных заболеваниях
Выделение чистой культуры возбудителя при инфекционных заболеваниях
Иногда, даже при выраженных клинических симптомах, возбудитель может присутствовать в очаге инфекции в количестве, недостаточном для микроскопического определения. В этом случае выделение чистой культуры позволяет увеличить численность микроорганизмов в исследуемом субстрате.
Существует два способа выращивания микроорганизмов: на жидких (увеличивается количество возбудителей) и твёрдых (исследуют отдельные колонии, в том числе и на чувствительность к антибиотикам) питательных средах. Большинство возбудителей инфекций человека достаточно требовательны к условиям культивирования. Именно поэтому питательные среды для их выращивания должны содержать белки, сахарозу и нуклеиновые кислоты (присутствующие в крови и сыворотке).
Кроме того, необходимо поддерживать соответствующий газовый состав: для культивирования анаэробов необходимо отсутствие кислорода, в то время как для облигатных аэробов (Bordetella pertussis) — наоборот. Оптимальная температура выращивания большинства патогенных микроорганизмов составляет 37 °С; культивирование некоторых фибов осуществляют при 30 С.
Идентификация возбудителя инфекционного заболевания
Симптомы заболеваний зависят от вида возбудителей, вызвавших их. Именно поэтому идентификация микроорганизма позволяет предположить клиническую картину вызываемого им заболевания (например, симптомы инфекции, вызванной Vibrio cholerae, отличны от таковых при заражении Shigella sonnei). Большое значение имеет выделение Neisseria meningitidis именно из спинномозговой жидкости. Идентификация микроорганизмов основана на:
• изучении морфологических свойств их колоний в агаре;
• различной окраске по Граму;
• способности возбудителей к образованию спор;
• изучении биохимических свойств (каталазный или коагулазный тесты).
Точное определение штамма обычно зависит от результатов биохимического анализа (например, уреазный тест) или обнаружения продуктов жизнедеятельности бактерий (индол). Возбудителей, которые не могут быть выращены на питательных средах, идентифицируют при помощи молекулярно-генетического метода ДНК и секвенирования (например, Trophyrema whippelii).

Определение чувствительности возбудителя инфекционного заболевания к антибиотикам
Если для эрадикации микроорганизмов достаточно стандартной дозы антимикробного препарата, то их считают чувствительными, если необходимо увеличение дозы лекарственного средства — относительно устойчивыми. Абсолютно устойчивыми (резистентными) называют возбудителей, в отношении которых антибиотикотерапия неэффективна. Существует широкий спектр различных методов определения чувствительности к антимикробным препаратам.
Методы Британской ассоциации антимикробной химиотерапии (British Society of Antimicrobial Chemotherapy — BSAQ и Института клинических лабораторных стандартов (Clinical Laboratory Standards Institute — С LSI) основаны на определении диаметра зоны слабого роста микроорганизмов на твёрдой питательной среде при применении антимикробного препарата.
Минимальную подавляющую концентрацию антибиотика измеряют с помощью Е-теста, растворения препарата в питательном бульоне или нанесения его на плотный агар. В последнем случае на засеянный исследуемыми микроорганизмами агар наносят бумажные диски, пропитанные различными антибиотиками (метод бумажных дисков).
Уровень чувствительности зависит от диаметра зоны пониженного роста бактерий. Однако тестирование in vitro предоставляет лишь приблизительные данные, так как в клинической практике многое зависит от состояния больного.

Серологический анализ при инфекционном заболевании
Различные виды инфекций можно идентифицировать с помощью определения иммунного ответа, возникающего при внедрении возбудителя. Для этого существует большое количество различных методов: реакция агглютинации (РА), реакция связывания комплемента (РСК), реакция нейтрализации (РН) и иммуноферментный анализ (ИФА). Диагноз устанавливают на основании:
• определения уровня антител (IgM) в ответ на попадание в организм чужеродного белка (антигена);
• определения антигена.
Молекулярный анализ при инфекционном заболевании
Южный блоттинг и метод гибридизации нуклеиновых кислот. Методы основаны на связывании меченой ДНК с анализируемым образцом, при условии, что он имеет определённую последовательность аминокислот. Связанный комплекс определяют по активности метки. Это достаточно быстрый и надёжный способ, который, тем не менее, уступает по чувствительности молекулярно-генетическим методам.

Метод молекулярно-генетический (NAAT)
Для диагностики инфекционных заболеваний используют несколько молекулярно-генетических методов. Механизм выделения патогенной ДНК или РНК в количестве, достаточном для постановки диагноза, для каждого метода индивидуален. Так, при молекулярно-генетическом методе ДНК возбудителя разделяют на отдельные цепи, затем синтезируют праймеры для связывания с целевыми последовательностями. Образование новой ДНК катализирует полимераза.
Основное преимущество — достижение результата даже при наличии всего лишь одной копии ДНК. Благодаря автоматизированным системам и большому выбору специальных наборов эти методы стали доступны большинству диагностических лабораторий. Новые аппараты способны выдавать результат в режиме реального времени. Генетические методы позволяют идентифицировать микроорганизмы, выращивание которых отличается сложностью или сопряжено с риском для человека (например, Mycobacterium tuberculosis и Chlamydia trachomatis).
Кроме того, их можно использовать для определения генов, кодирующих устойчивость к действию антибиотиков (например, мутационный ген rpoВ, обеспечивающий устойчивость М. tuberculosis к рифампицину). Это позволяет заранее выбрать альтернативный путь лечения инфекционных заболеваний.
Иногда необходимо проводить типирование микроорганизмов в случае их распространения в больницах или в окружающей (внебольничной) среде.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
УТВЕРЖДЕНА
Минздравом СССР
17 января 1991 года
ИНСТРУКЦИЯ
по мерам профилактики распространения инфекционных
заболеваний при работе в клинико-диагностических лабораториях
лечебно-профилактических учреждений
Общие положения
С целью профилактики инфицирования медицинского персонала лечебно-профилактических учреждений особое значение имеет выполнение требований противоэпидемического режима.
Ответственность за организацию и соблюдение противоэпидемического режима при работе с потенциально опасным материалом возлагается на руководителя клинико-диагностической лаборатории (КДЛ).
Инструктаж среднего и младшего медицинского персонала проводится ответственным за технику безопасности не реже одного раза в квартал.
Инструкция составлена в соответствии с ГОСТом 42-21-2-85 "Стерилизация и дезинфекция изделий медицинского назначения. Методы, средства и режимы", а также приказом Минздрава СССР (1989 год) "О мерах по снижению заболеваемости вирусным гепатитом в стране".
I. Основные правила работы в КДЛ
Медицинскому персоналу КДЛ следует избегать контактов кожи и слизистых оболочек с кровью и другими биологическими жидкостями, для чего необходимо:
1. Работать в медицинских халатах, шапочках, сменной обуви, а при угрозе забрызгивания кровью или другими биологическими жидкостями - в масках, очках, клеенчатом фартуке.
2. Работать с исследуемым материалом в резиновых перчатках, все повреждения кожи на руках должны быть закрыты лейкопластырем или напальчником. Избегать уколов и порезов.
3. Проводить разборку, мойку, прополаскивание лабораторного инструментария, посуды после предварительной дезинфекции в резиновых перчатках.
4. В случае загрязнения кожных покровов кровью или другими биологическими жидкостями следует немедленно обработать их в течение 2 мин тампоном, обильно смоченным 70% спиртом, вымыть под проточной водой с мылом и вытереть индивидуальным тампоном. При загрязнении перчаток кровью их протирают тампоном, смоченным 3% раствором хлорамина, 6% раствором перекиси водорода.
При подозрении на попадание крови на слизистые оболочки их немедленно обрабатывают струей воды, 1% раствором протаргола; рот и горло прополаскивают 70% спиртом, или 1% раствором борной кислоты, или 0,05% раствором перманганата калия.
5. Запрещается есть, пить, курить и пользоваться косметикой на рабочем месте.
6. Запрещается пипетирование крови ртом; следует использовать автоматические пипетки, а при их отсутствии - резиновые груши.
7. Поверхность рабочих столов в конце каждого рабочего дня подвергается дезинфекции, а в случае загрязнения биологическим материалом - немедленно.
II.Способы взятия крови
Взятие крови следует проводить в резиновых перчатках, соблюдая правила асептики, обрабатывая перчатки 70% спиртом перед каждым взятием. Перед проколом кожу пальца обследуемого обрабатывают стерильным тампоном (шариком из ваты), смоченным 70% спиртом.
После взятия крови к раневой поверхности прикладывают новый стерильный тампон, смоченный 70% спиртом. Извлекать скарификаторы следует только с помощью пинцета, хранящегося в растворе дезинфекционного средства.
Стерильные тампоны хранятся в упаковке из бумаги, указанной в ГОСТе 42-21-2-85, в количестве не более 20 штук. Стерильные лабораторные инструменты хранятся в той же упаковке, в которой проводилась их стерилизация. Существует несколько вариантов взятия крови для гематологического исследования.
I вариант. После прокола пальца несколько капель крови (не менее 3-4), спускают на индивидуальное предметное (часовое) стекло, перемешивают и используют для работы.
II вариант. Кровь набирают в индивидуальные стерильные, предварительно выверенные капилляры объемом 20 мкл и капилляры Панченко непосредственно с поверхности кожи проколотого индивидуальным копьем пальца пациента.
III вариант. Кровь в количестве 40 мкл набирают стерильным индивидуальным капилляром Панченко, предварительно смоченным цитратом в соотношении цитрата и крови 1: 4 по объему.
IV вариант. После прокола кожи пальца 6-8 капель крови спускают в пластиковую пробирку, в которую предварительно внесено небольшое (на кончике глазной лопаточки) количество трилона Б.
Пробирку с кровью тщательно перемешивают, вращая ее между ладонями. Разлив крови пипетками по пробиркам осуществляется в лаборатории.
Приготовление моющего раствора
Количество компонентов для приготовления 1 л моющего р-ра
Моющее средство "Биолот", г
При механизированной очистке (струйный метод)
Вода питьевая, мл
Моющее средство "Биолот", г
Вода питьевая, мл
При ручной очистке
Раствор перекиси водорода:
При механизированной очистке (струйный метод, использование ультразвука) и ручной очистке
Моющее средство "Прогресс", "Айна", "Астра", "Лотос", "Лотос-автомат", "Маричка", г
При механизированной очистке с использованием ультразвука
Вода питьевая, мл (см3)
Примечание. При использовании моющего средства, содержащего 0,5% перекиси водорода и 0,5% синтетического моющего средства "Лотос" и "Лотос-автомат", применяют ингибитор коррозии - 0,14% олеат натрия (1,4 г на 1 л раствора). В скобках указано количество питьевой воды в мл.
Предстерилизационная очистка (ручной способ)
Процесс при проведении очистки
Время выдержки, мин
Замачивание в моющем растворе при полном погружении изделия при применении моющего средства "Биолот"
Бачок, ванна, раковина
То же при применении моющего средства "Прогресс", "Астра", "Лотос", "Лотос-автомат", "Айна", "Маричка"
Мойка каждого изделия в моющем растворе при помощи ерша и ватно-марлевого тампона
Ополаскивание проточной водой:
- при применении моющего средства "Биолот"
Ванна, раковина с устройством для струйной подачи
- при применении моющего средства "Маричка", "Прогресс"
- при применении средств "Астра", Лотос", "Айна", "Лотос-автомат"
Ополаскивание дистиллированной водой
Сушка горячим воздухом
До полного исчезновения влаги
1. Температура раствора в процессе мойки не поддерживается.
2. Моющий раствор перекиси водорода с синтетическими моющими средствами, в том числе "Лотос", "Лотос-автомат", с ингибитором коррозии можно использовать в течение суток с момента изготовления, если цвет раствора не изменился. Неизмененный раствор можно подогревать до 6 раз, в процессе подогрева концентрация перекиси водорода существенно не изменяется.
3. Раствор моющего средства "Биолот", применяемый как при ручном, так и при механическом способе, используется однократно, так как при повторном использовании фермент, входящий в состав моющего средства, разрушается в процессе очистки.
III. Дезинфекция лабораторного инструментария, посуды,
спецодежды, биоматериала, оборудования
Лабораторные инструменты, иглы, капилляры, предметные стекла, пробирки, меланжеры, счетные камеры, кюветы фотоэлектроколориметра, пипетки, наконечники, резиновые груши, баллоны и т.д., посуда после каждого использования должны подвергаться дезинфекции.
1. Использованные изделия промывают в емкости с водой. Промывные воды обеззараживают кипячением в течение 30 мин или засыпают сухой хлорной известью, известью белильной термостойкой, нейтральным гипохлоритом кальция (НГК) в соотношении 200 г на 1 л, перемешивают и обеззараживают в течение 60 мин. Промытые изделия кипятят в закрытой емкости в воде в течение 30 мин или в 2% растворе соды в течение 15 мин. (В случае кипячения изделий в 2% растворе соды дальнейшая предстерилизационная очистка не проводится.)
2. Лабораторные инструменты могут быть обеззаражены погружением в раствор с дезинфицирующим раствором.
В качестве дезинфицирующих используются следующие растворы: 3% раствор хлорамин, 6% перекись водорода, 6% перекись водорода с 0,5% моющего средства ("Прогресс", "Астра". "Айна", "Лотос", "Лотос-автомат"), 4% формалин, 0,5% НГК, 0,5% сульфохлорантин; время обеззараживания 60 мин.
Дезинфицирующие растворы используются однократно.
Емкости для проведения дезинфекции должны быть четко маркированы, иметь крышки.
При дезинфекции изделий, имеющих внутренние каналы, растворы дезинфекционного средства в объеме 5-10 мл пропускают через канал с помощью груши для удаления остатков крови, сыворотки и пр., после чего изделия полностью погружают в дезинфицирующий раствор во вторую емкость.
При погружении инструментов в горизонтальном положении полости каждого инструмента должны быть заполнены дезинфицирующим раствором.
3. Каждая партия сухих хлорсодержащих дезинфектантов перед использованием должна подвергаться контролю на содержание активного хлора.
4. Посуду, соприкасающуюся с кровью или сывороткой и не предназначенную для последующего контакта с обследуемым, после дезинфекции промывают проточной водой для полного удаления дезинфектанта и проводят необходимую технологическую обработку.
5. Блоки кювет анализатора ФП, кюветы измерительной аппаратуры, пластиковые пробирки и т.д. обеззараживают только 6% раствором перекиси водорода и промывают проточной водой.
6. С предметных стекол с фиксированным и окрашенным мазком крови после проведения микроскопии удаляют остатки иммерсионного масла, стекла кипятят в мыльном растворе не менее 15 мин до полного отхождения краски, затем промывают проточной водой, подсушивают на воздухе и протирают.
7. Остатки крови, мочи, спинномозговой жидкости и т.д., пробы, содержащие разведенную сыворотку без добавления кислот, щелочей сливают в специальную тару и обеззараживают сухой хлорной известью, известью белильной термостойкой, НГК в соотношении 1:5 в течение 1 часа. При удалении сгустков следует предварительно отделить материал металлическим шпателем, который затем обеззараживают. Посуду из-под мочи, кала обрабатывают по описанной выше методике, но ее можно не подвергать стерилизации.
8. При загрязнении кровью или секретами мебели, инвентаря, приборов их следует немедленно дважды протереть ветошью, ватными или марлевыми тампонами, обильно смоченными дезинфицирующими растворами.
Использованную ветошь сбрасывают в специально выделенную емкость с дезинфицирующим раствором, маркированную "Для дезинфекции использованной ветоши".
9. При загрязнении кровью или секретами спецодежды ее снимают, предварительно обработав дезинфицирующим раствором участок загрязнения.
Стирка спецодежды на дому категорически запрещается. Смена спецодежды должна осуществляться не менее 2 раз в неделю.
10. Перчатки после окончания работы обеззараживают погружением в 3% раствор хлорамина или 6% раствор перекиси водорода на 1 час или кипячением в течение 30 мин.
11. Одноразовый инструментарий (плашки, наконечники, автоматические пипетки и т.д.) обеззараживают и утилизируют в паровом стерилизаторе при 2,0 кг/2 (132° С) в течение 60 мин.
IV. Предстерилизационная очистка
После дезинфекции лабораторный инструментарий, соприкасающийся с раневой поверхностью или слизистыми оболочками обследуемого, подлежит обязательной предстерилизационной очистке и стерилизации.
от 22 мая 2020 года N 15
(с изменениями на 4 февраля 2022 года)
(редакция, действующая с 5 марта 2022 года)
Документ с изменениями, внесенными:
1. Утвердить санитарно-эпидемиологические правила СП 3.1.3597-20 "Профилактика новой коронавирусной инфекции (COVID-19)" (приложение).
2. Настоящее постановление действует до 1 января 2024 г.
в Министерстве юстиции
26 мая 2020 года,
регистрационный N 58465
Приложение
УТВЕРЖДЕНЫ
постановлением Главного
государственного санитарного врача
Российской Федерации
от 22 мая 2020 года N 15
Санитарно-эпидемиологические правила СП 3.1.3597-20 "Профилактика новой коронавирусной инфекции (COVID-19)"
(с изменениями на 4 февраля 2022 года)
I. Общие положения
1.1. Настоящие санитарно-эпидемиологические правила (далее - санитарные правила) устанавливают требования к комплексу организационных, профилактических, санитарно-противоэпидемических мероприятий, проведение которых обеспечивает предупреждение возникновения и распространения случаев заболевания новой коронавирусной инфекцией (COVID-19) на территории Российской Федерации.
1.2. Новая коронавирусная инфекция (COVID-19) (далее - COVID-19) является острым респираторным заболеванием, вызванным новым коронавирусом (SARS-CoV-2). Вирус SARS-CoV-2 в соответствии с санитарным законодательством Российской Федерации отнесен ко II группе патогенности.
II. Мероприятия, направленные на предупреждение распространения COVID-19
2.1. Мероприятия, направленные на предупреждение распространения COVID-19, включают:
- лабораторный мониторинг (слежение за циркуляцией и распространением возбудителя);
- мониторинг напряженности иммунитета среди переболевших лиц, среди групп риска и среди всего населения;
- сбор и анализ полученной информации;
- оценку эффективности проводимых мероприятий
- гигиеническое воспитание населения.
2.2. В целях принятия решений, направленных на предупреждение распространения COVID-19, разработки санитарно-противоэпидемических (профилактических) мероприятий, направленных на снижение рисков распространения COVID-19 и предотвращение формирования очагов с множественными случаями заболеваний, проводятся:
- постоянная и динамическая оценка масштабов, характера распространенности и социально-экономической значимости инфекции, в том числе с учетом тяжести течения заболеваний;
- выявление тенденций эпидемического процесса;
- выявление высокого уровня заболеваемости и риска инфицирования населения в субъектах Российской Федерации, населенных пунктах, организациях и в связи с деятельностью индивидуальных предпринимателей;
- изучение популяционного иммунитета у населения с учетом проявлений эпидемического процесса;
- выявление лиц, наиболее подверженных риску развития заболевания;
- выявление причин и условий, определяющих уровень и структуру заболеваемости COVID-19;
- контроль и обоснованная оценка масштабов, качества и эффективности осуществляемых профилактических и противоэпидемических мероприятий для их корректировки, планирование последовательности и сроков их реализации;
- изучение и оценка результатов иммунизации населения (после ведения специфической профилактики);
- изучение эффективности средств специфической, неспецифической и экстренной профилактики, применяемой в эпидемических очагах COVID-19;
- прогнозирование развития эпидемиологической ситуации.
2.3. Гигиеническое воспитание населения как метод профилактики COVID-19 включает:
- представление населению подробной информации о COVID-19, основных симптомах заболевания и мерах профилактики с использованием средств массовой информации, листовок, плакатов бюллетеней, проведение индивидуальной беседы с пациентом и другие;
- разъяснение правил ношения масок для защиты органов дыхания, применение дезинфицирующих средства, включая индивидуальные антисептические средства;
- разъяснение необходимости соблюдения социальной дистанции (1,5 м - 2 м от человека) в период подъема заболеваемости;
- доведение до организованных коллективов взрослых и детей правил организации деятельности в период подъема заболеваемости COVID-19.
2.4. Гигиеническое воспитание населения проводится органами исполнительной власти субъектов Российской Федерации, работниками медицинских организаций при методической поддержке специалистов органов и организаций, входящих в систему федерального государственного санитарно-эпидемиологического надзора.
2.5. Иностранные граждане при наличии иммунного ответа (антител IgG (S-белок) к возбудителю COVID-19, выявленного по результатам лабораторных исследований, проведенных на территории Российской Федерации и переданных в федеральную государственную информационную систему "Единый портал государственных и муниципальных услуг (функций)" в соответствии с постановлением Правительства Российской Федерации от 27.03.2021 N 452 "Об обеспечении уведомления физических лиц о результатах исследований на наличие возбудителя новой коронавирусной инфекции (COVID-19) с использованием федеральной государственной информационной системы "Единый портал государственных и муниципальных услуг (функций)" и обмена информацией о результатах таких исследований" (Собрание законодательства Российской Федерации, 2021, N 14, ст.2330; Официальный интернет-портал правовой информации (www.pravo.gov.ru), 2022, 26 января, N 0001202201260032) (далее - постановление N 452), вправе оформить Справку о наличии иммунного ответа (антител) к возбудителю COVID-19 (далее - Справка) с использованием федеральной государственной информационной системы "Единый портал государственных и муниципальных услуг (функций)". Рекомендуемый образец Справки приведен в приложении к санитарным правилам.
2.6. Для оформления Справки иностранный гражданин сдает тест на антитела IgG (S-белок) в организации, осуществляющей исследования на наличие антител к возбудителю новой коронавирусной инфекции (COVID-19), подключенной к системе федерального бюджетного учреждения науки "Центральный научно-исследовательский институт эпидемиологии" Федеральной службы по надзору в сфере защиты прав потребителей и благополучия человека (пункт 2 постановления N 452), с указанием:
фамилии, имени, отчества (при наличии);
номера документа, удостоверяющего личность иностранного гражданина, или свидетельства о рождении иностранного гражданина;
адреса электронной почты (при наличии).
2.7. Иностранный гражданин с использованием федеральной государственной информационной системы "Единый портал государственных и муниципальных услуг (функций)" на специализированной странице вводит следующие идентифицирующие сведения для формирования Справки:
номер документа, удостоверяющего личность иностранного гражданина, или свидетельства о рождении иностранного гражданина;
номер заказа проведенного лабораторного исследования, который получен в организации, осуществляющей исследования на наличие антител к возбудителю новой коронавирусной инфекции (COVID-19).
2.8. Справка автоматически формируется в федеральной государственной информационной системе "Единый портал государственных и муниципальных услуг (функций)" на русском и английском языке с возможностью ее направления на электронную почту иностранного гражданина либо ее выгрузки в формате PDF.
III. Лабораторная диагностика и регистрация случаев COVID-19
3.1. В целях оперативной организации проведения исследований и противоэпидемических мероприятий лабораторное обследование лиц в условиях распространения COVID-19 проводится исходя из следующих приоритетов:
3.1.1. К приоритету 1-го уровня относится проведение лабораторных исследований и противоэпидемических мероприятий в отношении:
- лиц, прибывших на территорию Российской Федерации с наличием симптомов инфекционного заболевания (или при появлении симптомов в течение периода медицинского наблюдения);
- лиц с диагнозом "внебольничная пневмония", "острая респираторная вирусная инфекция" и "грипп";
- работников медицинских организаций, имеющих риск инфицирования при профессиональной деятельности при появлении симптомов, не исключающих COVID-19;
- лиц, при появлении респираторных симптомов, находящихся в интернатах, детских домах, детских лагерях, пансионатах для пожилых и других стационарных организациях социального обслуживания, учреждениях уголовно-исполнительной системы;
- лиц, поступающих в стационар медицинской организации для оказания им медицинской помощи в экстренной или неотложной форме, в организации социального обслуживания для детей и взрослых.
3.1.2. К приоритету 2-го уровня относится проведение лабораторных исследований и противоэпидемических мероприятий в отношении:
- лиц старше 65-ти лет, обратившихся за медицинской помощью с респираторными симптомами;
- работников медицинских организаций, имеющих риск инфицирования при профессиональной деятельности (лабораторные исследования проводятся 1 раз в неделю до появления иммуноглобулина G (далее - IgG);
- работников стационарных организаций социального обслуживания населения, учреждений уголовно-исполнительной системы при вахтовом методе работы до начала работы в организации с целью предупреждения заноса COVID-19.
3.1.3. К приоритету 3-го уровня относится проведение лабораторных исследований и противоэпидемических мероприятий в отношении детей из организованных коллективов при возникновении 3-х и более случаев заболеваний, не исключающих COVID-19 (обследуются как при вспышечной заболеваемости).
3.2. Первичные исследования без выделения возбудителя проводятся лабораториями, имеющими санитарно-эпидемиологическое заключение на работу с возбудителями инфекционных болезней человека III-IV группы патогенности. К работе по проведению исследований допускаются специалисты, давшие письменное согласие и прошедшие подготовку/инструктаж по вопросам обеспечения требований биологической безопасности.
Отбор и транспортировка биологического материала для лабораторных исследований проводятся в соответствии с требованиями законодательства Российской Федерации в отношении возбудителей инфекционных заболеваний человека I-II группы патогенности.
Срок выполнения лабораторного исследования на COVID-19 не должен превышать 24 часов с момента поступления биологического материала в лабораторию до получения его результата лицом, в отношении которого проведено соответствующее исследование.
Время доставки материала для исследования на COVID-19 в лабораторию не должно превышать 24 часов с момента его отбора.
от 22 августа 2014 года N 50
(с изменениями на 29 декабря 2015 года)
____________________________________________________________________
Утратило силу с 1 сентября 2021 года на основании
постановления Главного государственного санитарного врача
Российской Федерации от 28 января 2021 года N 4
____________________________________________________________________
Документ с изменениями, внесенными:
Срок действия соответствующего пункта в указанном Перечне - до 1 сентября 2021 года.
Дополнительно см. ярлык "Примечания".
- Примечание изготовителя базы данных.
В соответствии с Федеральным законом от 30.03.99 N 52-ФЗ "О санитарно-эпидемиологическом благополучии населения" (Собрание законодательства Российской Федерации, 1999, N 14, ст.1650; 2002, N 1 (ч.1), ст.2; 2003, N 2, ст.167; N 27 (ч.1), ст.2700; 2004, N 35, ст.3607; 2005, N 19, ст.1752; 2006, N 1, ст.10; N 52 (ч.1), ст.5498; 2007 N 1 (ч.1), ст.21, ст.29; N 27, ст.3213; N 46, ст.5554; N 49, ст.6070; 2008, N 24, ст.2801; N 29 (ч.1), ст.3418; N 30 (ч.2), ст.3616; N 44, ст.4984; N 52 (ч.1), ст.6223; 2009, N 1, ст.17; 2010, N 40 ст.4969; 2011, N 1, ст.6; N 30 (ч.1), ст.4563, ст.4590, ст.4591, ст.4596; N 50, ст.7359; 2012, N 24, ст.3069; N 26, ст.3446; 2013, N 27, ст.3477; N 30 (ч.1), ст.4079; N 48, ст.6165; 2014, N 26 (ч.1), ст.3366, ст.3377 и постановлением Правительства Российской Федерации от 24.07.2000 N 554 "Об утверждении Положения о государственной санитарно-эпидемиологической службе Российской Федерации и Положения о государственном санитарно-эпидемиологическом нормировании" (Собрание законодательства Российской Федерации, 2000, N 31, ст.3295; 2004, N 8, ст.663; N 47, ст.4666; 2005, N 39, ст.3953)
1. Утвердить санитарно-эпидемиологические правила и нормативы СанПиН 3.2.3215-14 "Профилактика паразитарных болезней на территории Российской Федерации" (приложение).
в Министерстве юстиции
12 ноября 2014 года,
регистрационный N 34659
Профилактика паразитарных болезней на территории Российской Федерации
Санитарно-эпидемиологические правила и нормативы СанПиН 3.2.3215-14
(с изменениями на 29 декабря 2015 года)
В настоящих Санитарно-эпидемиологических правилх и нормативах учтены:
I. Область применения
1.1. Настоящие санитарно-эпидемиологические правила и нормативы (далее - санитарные правила) разработаны в соответствии с законодательством Российской Федерации.
1.2. Санитарные правила устанавливают требования к комплексу организационных, санитарно-противоэпидемических (профилактических) мероприятий, проведение которых направлено на предупреждение возникновения и распространения паразитарных заболеваний.
1.3. Соблюдение санитарно-эпидемиологических правил является обязательным на всей территории Российской Федерации для государственных органов, органов государственной власти субъектов Российской Федерации, муниципальных образований, должностных лиц государственных органов, должностных лиц органов государственной власти субъектов Российской Федерации, должностных лиц органов местного самоуправления, граждан, индивидуальных предпринимателей и юридических лиц.
1.4. Контроль за выполнением настоящих санитарных правил проводится органами, уполномоченными осуществлять федеральный государственный санитарно-эпидемиологический надзор в соответствии с законодательством Российской Федерации.
II. Общие положения
2.1. В целях предупреждения возникновения и распространения паразитарных болезней должны своевременно и в полном объеме проводиться предусмотренные санитарными правилами и иными нормативными правовыми актами Российской Федерации санитарно-противоэпидемические (профилактические) мероприятия, в том числе мероприятия по осуществлению производственного контроля, по проведению медицинских осмотров, гигиеническому воспитанию и обучению населения.
2.2. Санитарная охрана территории Российской Федерации по предупреждению завоза паразитарных болезней из других стран осуществляется в соответствии с законодательством Российской Федерации.
III. Мероприятия по обеспечению федерального государственного санитарно-эпидемиологического надзора
3.1. Мероприятия по обеспечению федерального государственного санитарно-эпидемиологического надзора (далее - эпидемиологический надзор) за паразитарными болезнями включают непрерывное наблюдение должностными лицами уполномоченными осуществлять федеральный государственный санитарно-эпидемиологический надзор за эпидемическим процессом с целью оценки ситуации в популяции людей и в объектах окружающей среды, разработку и корректировку санитарно-противоэпидемических (профилактических) мероприятий, обеспечивающих предупреждение возникновения, распространения паразитарных болезней среди населения и формирование эпидемических очагов с групповой заболеваемостью.
3.2. Мероприятия эпидемиологического надзора за паразитарными болезнями включают:
- постоянную оценку масштабов, характера распространенности и социально-экономической значимости паразитарных болезней;
- выявление тенденций эпидемического процесса;
- выявление регионов, областей, населенных пунктов с высоким уровнем заболеваемости и риском заражения;
- выявление причин и условий, определяющих уровень и структуру заболеваемости паразитарными болезнями на территории; контроль и обоснованную оценку масштабов их распространенности;
- оценку качества и эффективности осуществляемых профилактических и противоэпидемических мероприятий;
- планирование последовательности мероприятий и сроков их реализации;
- разработку прогнозов эпидемиологической ситуации.
3.3. Основным инструментом эпидемиологического надзора является эпидемиологическая диагностика.
Эпидемиологическая диагностика осуществляется помощью ретроспективного и оперативного эпидемиологического анализа заболеваемости.
3.4. Многолетний ретроспективный эпидемиологический анализ проводится не менее чем за последние 5 лет и предусматривает:
- анализ многолетней динамики заболеваемости (пораженности);
- анализ заболеваемости по территориям;
- анализ заболеваемости по возрастным группам, полу, контингентам населения;
- анализ эпидемических очагов паразитарных болезней по конкретным нозологическим формам;
- анализ по факторам риска с учетом источников и факторов передачи паразитоза;
- анализ лабораторной диагностики паразитозов;
- выводы и предложения по разработке профилактических мероприятий.
Ретроспективный эпидемиологический анализ заболеваемости паразитозами должен проводиться ежегодно.
3.5. Оперативный эпидемиологический анализ проводится в условии эпидемического подъема заболеваемости или регистрации эпидемических очагов групповой заболеваемости. Эпидемиологический анализ включает постоянное наблюдение за динамикой заболеваемости с учетом определенного этиологического агента, оценку санитарно-эпидемиологической ситуации, формулирование предварительного и окончательного эпидемиологического диагноза с установлением причин и условий подъема заболеваемости или формирования эпидемического очага.
3.6. По эпидемическим показаниям (внепланово) должностными лицами, уполномоченными осуществлять федеральный государственный санитарно-эпидемиологический надзор, принимается решение о кратности и объеме лабораторных исследований почвы, сточных вод и их осадков, вод поверхностных водоёмов, которые используются для целей рекреации и в качестве источников хозяйственно-питьевого водоснабжения, вод плавательных бассейнов, питьевой воды на различных этапах водоподготовки.
IV. Выявление, регистрация и учет паразитарных болезней
4.1. Выявление больных и лиц с подозрением на паразитозы осуществляется медицинскими организациями при всех видах оказания медицинской помощи.
Обследованию на гельминтозы и кишечные протозоозы подлежат: дети, посещающие детские дошкольные образовательные организации; персонал детских дошкольных образовательных организаций; школьники младших классов, дети, подростки, декретированные и приравненные к ним группы населения при диспансеризации и профилактических осмотрах; дети, подростки по эпидемическим показаниям; дети и подростки, оформляющиеся в детские дошкольные и другие образовательные организации, приюты, дома ребенка, детские дома, школы-интернаты, на санаторно-курортное лечение, в оздоровительные организации, в детские отделения больниц; дети всех возрастов детских организаций закрытого типа и круглогодичного пребывания, больные детских и взрослых поликлиник и больниц, лица, общавшиеся с больными.
4.2. Отбор биологических проб для исследования на паразитозы проводится медицинскими работниками медицинских организаций, образовательных и иных организаций.
4.3. Доставка биологического материала в лабораторию производится в герметичных контейнерах, обеспечивающих его сохранность и безопасность транспортировки.
4.4. Лабораторные исследования на выявление возбудителей паразитозов осуществляют организации и индивидуальные предприниматели, имеющие лицензию на выполнение работ с микроорганизмами III-IV групп патогенности.
4.5. Организация и проведение плановых обследований детей, посещающих дошкольные, школьные образовательные организации и другие детские организации, обеспечивается руководителями таких организаций.
4.6. В целях ежегодного планового обследования детей на паразитозы руководителями образовательных организаций совместно с медицинскими организациями (государственной, муниципальной и частной системы здравоохранения) разрабатывается график отбора и доставки проб биологического материала на исследование.
4.7. О каждом случае паразитозов медицинские работники медицинских организаций (государственной, муниципальной и частной системы здравоохранения) в течение 12 часов направляют экстренное извещение в территориальный орган федерального органа исполнительной власти, уполномоченного осуществлять федеральный государственный санитарно-эпидемиологический надзор.
4.8. При выявлении лиц, пораженных паразитозами, должностными лицами уполномоченными осуществлять федеральный государственный санитарно-эпидемиологический надзор проводится эпидемиологическое расследование с заполнением карты эпидемиологического расследования случая паразитарного заболевания.
4.9. В случае изменения или уточнения диагноза медицинские работники медицинских организаций сообщают по телефону, а затем в течение 12 часов направляют экстренное извещение в письменной форме об изменении или уточнении диагноза в территориальный орган федерального органа исполнительной власти, уполномоченного осуществлять федеральный государственный санитарно-эпидемиологический надзор.
4.10. Каждый случай паразитарных заболеваний подлежит регистрации и учету в журнале учета инфекционных заболеваний по месту их выявления.
4.11. Инвазированные подлежат лечению в амбулаторных или стационарных условиях на основании их информированного добровольного согласия и с учетом права на отказ от медицинского вмешательства.
4.12. В целях активного выявления и предупреждения распространения паразитарных болезней проводятся плановые профилактические обследования должностных лиц и работников организаций, деятельность которых связана с производством, хранением, транспортировкой и реализацией пищевых продуктов и питьевой воды, воспитанием и обучением детей, коммунальным и бытовым обслуживанием населения (далее - декретированные группы населения).
4.13. При угрозе возникновения и распространения паразитарных заболеваний должностные лица, уполномоченные осуществлять федеральный государственный санитарно-эпидемиологический надзор, выдают гражданам и юридическим лицам предписания о проведении дополнительных санитарно-противоэпидемических мероприятий, в том числе в рамках лабораторного обследования и медицинского наблюдения и выполнения работ по дезинфекции, дезинвазии, дезинсекции и дератизации.
4.14. Организация и проведение плановых и по эпидемическим показаниям обследований декретированных групп населения на наличие паразитарных болезней обеспечивается руководителями организаций и индивидуальными предпринимателями по месту их работу.
4.15. Все выявленные инвазированные лица обеспечиваются диспансерным наблюдением в соответствующих медицинских организациях.
4.16. На каждого инвазированного заполняется форма диспансерного наблюдения.
4.17. Снятие с диспансерного учёта осуществляется после проведения лечения и получения отрицательных результатов лабораторного исследования биологического материала.
4.18. Ответственность за полноту, достоверность и своевременность регистрации и учета случаев паразитозов, а также оперативное и полное информирование о них несет руководитель медицинской организации по месту выявления больного.
V. Требования к мероприятиям по профилактике отдельных групп паразитарных болезней
5. Мероприятия по профилактике малярии.
5.1. Сбор и анализ данных о местных или завозных случаях малярии осуществляется медицинскими организациями и органами, уполномоченными осуществлять санитарно-эпидемиологический надзор.
Рекомендуемая инструкция разработана сотрудниками кафедры клинической лабораторной диагностики ЦОЛИУ врачей (зав. Кафедрой профессор В.Т. Морозова, ассистент Е.О. Смолиговец) совместно с отделом очаговой дезинфекции дезинфекционной станции ГУЗМ (Гвелесиани Г.А., Смирнова В.В.).
В рецензировании принимали участие заведующий специализированной научно-исследовательской лабораторией эпидемиологии и профилактики СПИД к.м.н. Покровский В.В., заведующая Всесоюзным научно-методическим и контрольным центром по лабораторному делу д.м.н. Делекторская Л.Н., зам. Начальника госпиталя им. Бурденко Н.Н. по медицинской части Ивлиев А.С., главный специалист по лабораторной службе Москвы к.м.н. Каплан Б.С., главный специалист по лабораторной службе МЗ РСФСР Розенталь В.М. Москва, 1991
С целью профилактики инфицирования медицинского персонала лечебно-профилактических учреждений особое значение имеет выполнение требований противоэпидемического режима.
Сотрудники клинико-диагностических лабораторий подвергаются риску заражения СПИД, вирусным гепатитом, кишечными инфекциями и другими инфекционными заболеваниями. При этом следует иметь в виду, что в качестве главного фактора распространения выше названных заболеваний выступает кровь, мокрота, сперма, моча и другие секреты и экскреты организма человека. В клинико-диагностических лабораториях кровь и биологические жидкости должны считаться потенциально инфицированными.
Ответственность за организацию и соблюдение противоэпидемического режима при работе с потенциально опасным материалом возлагается на руководителя клинико-диагностической лаборатории.
Инструктаж среднего и младшего медицинского персонала проводится ответственным за технику безопасности не реже одного раза в квартал.
Инструкция составлена в соответствии с ОСТ 42-21-2-85 "Стерилизация и дезинфекция изделий медицинского назначения. Методы, средства и режимы", а также приказом № 408 от 12 июля 1989 г. "О мерах по снижению заболеваемости вирусным гепатитом в стране".
Инструкция предназначена для медперсонала клинико-диагностических лабораторий. Контроль за выполнением инструкции осуществляют специалисты санитарно-эпидемиологических и дезинфекционных станций.
Медицинскому персоналу клинико-диагностических лабораторий следует избегать контакта кожи и слизистых оболочек с кровью и другими биологическими жидкостями, для чего необходимо:
Работать в медицинских халатах, шапочках, сменной обуви, а при угрозе забразгивания кровью или другими биологическими жидкостями, в масках, очках, клеенчатых фартуках.
Работать с исследуемым материалом в резиновых перчатках, все повреждения кожи на руках должны быть закрыты лейкопластырем или напальчником. Избегать уколов и порезов.
Проводить разборку, мойку, прополаскивание лабораторного инструментария, посуды после предварительной дезинфекции в резиновых перчатках.
В случае загрязнения кожных покровов кровью или другими биологическими жидкостями следует немедленно обработать их в течение 2-х минут тампоном, обильно смоченным 70 0 спиртом, вымыть под проточной водой с мылом и вытереть индивидуальным полотенцем. При загрязнении перчаток кровью их протирают тампоном, смоченным 3% раствором хлорамина, 6% раствором перекиси водорода.
При подозрении попадания крови на слизистые оболочки, их немедленно обрабатывают струей воды, 1% раствором борной кислоты или вводят несколько капель азотнокислого серебра; нос обрабатывают 1% раствором протаргола; рот и горло прополаскивают 70 0 спиртом или 1% раствором борной кислоты или 0,05% раствором марганцево-кислого калия.
Запрещается пипетирование крови ртом; следует использовать автоматические пипетки, а при их отсутствии – "груши".
Поверхность рабочих столов в конце каждого рабочего дня, а в случае загрязнения биологическим материалом немедленно, подвергается дезинфекции.
Взятие крови следует проводить в резиновых перчатках, соблюдая правила асептики, обрабатывая перчатки 70 0 спиртом перед каждым взятием. Перед проколом кожа пальца обследуемого обрабатывается стерильным тампоном (шариком из ваты), смоченным 70 0 спиртом. После взятия крови к раневой поверхности прикладывается новый стерильный тампон, смоченный 70 0 спиртом.
Стерильные тампоны хранятся в упаковке из бумаги, указанной в ОСТ 42-21-2-85, в количестве не более 20 штук.
Стерильные лабораторные инструменты хранятся в той же упаковке, в которой проводилась их стерилизация.
После прокола пальца несколько капель крови (не менее 3-4) спускают на индивидуальное предметное (часовое) стекло, перемешивают и используют для работы.
Кровь набирается в индивидуальные, стерильные, предварительно выверенные капилляры объёмом 20 мкл и капилляра Панченко непосредственно с поверхности кожи проколотого индивидуальным копьём пальца пациента.
Кровь в количестве 40 мкл набирают стерильным индивидуальным капилляром Панченко, предварительно смоченным цитратом в соотношении цитрата и крови 1:4 по объёму.
После прокола кожи пальца, 6-8 капель крови спускают в пластиковую пробирку, в которую предварительно внесено небольшое (на кончике глазной лопаточки) количество трилона Б. Пробирку с кровью тщательно перемешивают, вращая её между ладонями. Разлив крови пипетками по пробиркам осуществляется в лаборатории.
Лабораторные инструменты, иглы, капилляры, предметные стекла, пробирки, меланжеры, счетные камеры, кюветы фотоэлектрометра, пипетки, наконечники, резиновые груши, баллоны и т.д., посуда после каждого использования должны подвергаться дезинфекции.
Использованные изделия промываются в ёмкости с водой. Промывные воды обеззараживаются кипячением в течение 30 минут или засыпают сухой хлорной известью, известью белильной термостойкой, нейтральным гипохлоритом кальция (НГК) в соотношении 200 г на 1 л воды, перемешивают и обеззараживают в течение 60 минут. Промытые изделия кипят в закрытой емкости в воде в течение 30 минут, или в 2% растворе соды, дальнейшая предстерилизационная очистка не проводится.
6% раствор перекиси водорода с 0,5% моющего средства ("Прогресс", "Астра", "Айна", "Лотос", "Лотос-автомат")
При дезинфекции изделий, имеющих внутренние каналы, растворы дезинфицирующего средства в объёме 5-10 мл пропускают через канал с помощью груши для удаления остатков крови, сыворотки и др., после чего изделия полностью погружают в дезинфицирующий раствор во вторую ёмкость.
При погружении инструментов в горизонтальном положении полости каждого инструмента должны быть заполнены дезинфицирующим раствором.
Каждая партия сухих хлорсодержащих дезинфектантов перед использованием должна подвергаться контролю на содержание активного хлора.
Посуда, соприкасающаяся с кровью или сывороткой и не предназначенная для последующего контакта с обследуемым после дезинфекции промывается под проточной водой для полного удаления дезинфектанта и проходит необходимую технологическую обработку.
Ёмкости кювет-анализатора ФП, кюветы измерительной аппаратуры, пластиковые пробирки и т.д. обеззараживаются только 6% раствором перекиси водорода и промываются проточной водой.
С предметных стёкол с фиксированным и окрашенным мазком крови после проведения микроскопии удаляются остатки иммерсионного масла, стёкла кипятятся в мыльном растворе не менее 15 минут до полного отхождения краски, затем промываются под проточной водой, подсушиваются на воздухе и протираются.
Остатки крови, мочи, спинномозговой жидкости и т.п., пробы, содержащие разведенную сыворотку без добавления кислот, щелочей сливают в специальную тару и обеззараживают сухой хлорной известью, известью белильной термостойкой, нейтральным гипохлоритом кальция в соотношении 1:5 в течение часа. При удалении сгустков следует предварительно отделить материал металлическим шпателем, который затем обеззараживается. Посуда из-под мочи, кала обрабатывается по описанной выше методике, но может не подвергаться стерилизации.
При загрязнении кровью или секретами мебели, инвентаря, приборов их следует немедленно дважды протереть ветошью, ватными или марлевыми тампонами, обильно смоченными дезинфицирующими растворами.
Использованную ветошь сбрасывают в специально выделенную ёмкость с дезраствором, маркированную: "Для дезинфекции использованной ветоши".
При загрязнении кровью или секретами спец. одежды, её снимают, предварительно обработав дезраствором участок загрязнения.
Стирка спецодежды на дому категорически запрещается. Смена спецодежды должна осуществляться не менее 2 раз в неделю.
Перчатки после окончания работы обеззараживаются погружением в 3% раствор хлорамина или 6% раствор перекиси водорода на 1 час или кипячением в течение 30 минут.
Одноразовый инструментарий (плашки, наконечники автоматических пипеток и т.д.) обеззараживаются и утилизируются в паровом стерилизаторе при 2,0 кг/см 2 (132 0 С) – 60 минут.
После дезинфекции лабораторный инструментарий, соприкасающийся с раневой поверхностью или слизистыми оболочками обследуемого подлежит обязательной предстерилизационной очистке и стерилизации. Предстерилизационную очистку проводят с применением моющих растворов.
Качество предстерилизационной очистки изделий оценивают на наличие крови путём постановки бензидиновой или амидопириновой проб; на наличие остаточных количеств щелочных компонентов моющего средства ставится фенолфталеиновая проба.
Самоконтроль в клинико-диагностических лабораториях проводится ежедневно, контролю подвергают не менее 1% от одновременно обработанных изделий одного наименования, но не менее 3-5 единиц.
При положительной пробе на кровь или моющее средство всю группу контролируемых изделий подвергают повторной обработке до получения отрицательных результатов.
V . После дезинфекции и предстерилизационной очистки проводят стерилизацию игл, шприцев, пробирок, пипеток, стеклянных палочек, стекол, меланжеров и т.д. (режимы и условия стерилизации указаны в таблицах 3-5).
Влажная уборка помещений должна осуществляться не менее одного раза в сутки, а при необходимости чаще с применением моющих средств и дезинфекции.
Один раз в месяц в помещениях, где проводится работа с кровью, сывороткой делают генеральную уборку с использованием 3% раствора хлорамина, хлорной извести, извести белильной термостойкой.
Во время генеральной уборки тщательно моются стены, оборудование, мебель, проводится очистка полов от наслоений, пятен и т.д.
При транспортировке биоматериал помещают в пробирки, закрывающиеся резиновыми пробками, сопроводительную документацию – в упаковку, исключающую возможность её загрязнения биоматериалом. Бланки направлений помещать в пробирку с кровью запрещается.
Транспортировка биоматериала осуществляются в закрытых контейнерах, подвергающихся дезинфекционной обработке.
При открывании пробок бутылок, флаконов, пробирок с кровью, плазмой или другими секретами следует не допускать разбрызгивания содержимого.
При хранении потенциально инфицированного материала в холодильнике необходимо поместить биоматериал в полиэтиленовый пакет.
В случае подтверждения зараженности биоматериала размораживание холодильника совмещают с его дезинфекцией.
При аварии (разбрызгивании зараженного материала и т.д.) помещение, где произошла авария, тщательно дезинфицируют.
Если авария произошла на центрифуге, то дезинфекционные мероприятия начинают проводить не ранее, чем через 30-40 минут, т.е. после осаждения аэрозоли.
Все случаи аварий и принятые в связи с этим меры подлежат обязательной регистрации во внутрибольничном журнале по технике безопасности.
Читайте также:

