Протейная инфекция сельскохозяйственных животных
Обновлено: 19.04.2024
Концентрация на ограниченной территории большого количества одновидового, одновозрастного чувствительного к инфекции молодняка обусловливает быстрый охват болезнью больших групп животных со сложной этиологией, неясно выраженными симптомокомплексами.
Высокая заболеваемость молодняка приводит к вынужденному убою и гибели значительного числа животных, недополучению живой массы, что тормозит развитие животноводства. Поэтому так важно своевременно выявить закономерности возникновения и развития инфекций, проводить раннюю диагностику в хозяйствах-поставщиках, разрабатывать и внедрять экспресс-методы групповой диагностики респираторных и желудочно-кишечных заболеваний, определяющих специфичность мер борьбы и их эффективность.
Значительные трудности возникают при организации и проведении профилактических и лечебных мероприятий, что объясняется отсутствием эффективных специфических препаратов для борьбы с рядом инфекционных болезней молодняка сельскохозяйственных животных (телят, поросят, ягнят, жеребят, крольчат и др.), а также трудоемкостью одновременных массовых обработок животных традиционными индивидуальными методами.
Для проведения эффективных мероприятий по предупреждению заболеваний сельскохозяйственных животных и оказанию заболевшим своевременной помощи ветеринарным специалистам необходимо все время быть в курсе современных достижений науки и передовой практики по всем вопросам лечебной и профилактической работы.
В данной книге приводятся сведения отечественных и зарубежных исследователей, а также авторский материал по эпизоотологии наиболее распространенных респираторных и желудочно-кишечных болезней телят, поросят, ягнят и жеребят, описаны клиническая картина, патологоанатомические изменения, новые методы диагностики болезней. Рекомендованы наиболее эффективные методы серопрофилактики, лечения и ликвидации респираторных и желудочно-кишечных болезней молодняка животных.
Проблема сохранности молодняка до сих пор остается актуальной, несмотря на применение различных схем вакцинации и витаминотерапии. Из официальных данных видно, что уровень сохранности молодняка довольно низок. Это связано с нарушениями в кормлении, приводящими к гиповитаминозам и гипотрофии, с наличием персистирующих бактериальных и вирусных инфекций, со вторичными иммунодефицитами и другими факторами.
БАКТЕРИАЛЬНЫЕ БОЛЕЗНИ
ПУПОЧНЫЙ СЕПСИС (ОМФАЛОФЛЕБИТ)
Пупочный сепсис (Sepsis umbilici, омфалофлебит omphalophlebitis) — инфекционная болезнь новорожденных животных, протекающая по типу раневой инфекции и возникающая при попадании условно-патогенной микрофлоры через пупочный канатик (бактерии, кокки, бациллы) в организм. Попадание в открытую рану микробов приводит к быстрому развитию септицемии.
Распространена болезнь во всех странах. Наличие ее — показатель низкой санитарной культуры персонала, ухаживающего за новорожденными, плохая организация работы зоотехников и ветеринарных специалистов, не обеспечивающих правильную подготовку животных к родам. Омфалофлебит может появиться в любом хозяйстве без заноса возбудителя инфекции извне.
Болезнь регистрируют чаще у телят и поросят 1—10-дневного возраста.
Патогенез. Поврежденная ткань культи пупочного канатика — благоприятная среда для размножения микрофлоры. Микрофлора по кровеносным сосудам пупочного канатика проникает в организм новорожденного. После проникновения микробов у основания культи пупочного канатика развивается воспалительный отек с образованием гнойных тромбов в венах. Отсюда значительная часть микробов попадает в кровоток, обусловливая тем самым быстрое развитие сепсиса.
Болеют слабые телята. Больные с фекалиями, мочой, выделениями из воспалительной культи пупочного канатика инфицируют пассажированными микробами помещение (подстилку, пол, стены). По мере пассажирования вирулентность микроорганизмов нарастает, поэтому заболевают даже крепкие, хорошо развитые животные.
Клинические признаки. Течение болезни может быть сверхострым, острым, подострым и хроническим.
Сверхострое течение наблюдают в первые 24 ч жизни животного, клинические признаки, кроме воспаления пуповины, развиться не успевают.
Острое течение проявляется угнетением, отказом от корма, повышением температуры на 0,5—1,5 "С. В области пуповины — горячий и болезненный отек тестоватой консистенции. У поросят отмечают покраснение пуповины и прилежащей брюшной стенки, в начале болезни — запор, а затем учащенную дефекацию, гибель. Если болезнь затягивается на 3—4 сут, признаки диареи выражены сильнее. Периодически наблюдается мышечная дрожь. Культя пупочного канатика при этом влажная, утолщенная, горячая, из нее выделяется воспалительный экссудат.
Хроническое течение выявляют у телят более старшего возраста (3—6 дней) при уже подсохшем канатике. Процесс развивается медленно, первые клинические признаки слабо выражены: плохой аппетит, слабое угнетение, повышение температуры тела. Позднее поражаются суставы и легкие: животные передвигаются с трудом, выявляют болезненность и опухание суставов, кашель, серозно-катаральные истечения из носа, учащенное дыхание, хрипы при аускультации.
Патологоанатомические изменения. Кожа и слизистые оболочки бледные, серо-белого цвета, суховатые. В случае септической формы при вскрытии находят общесептические процессы с развитием в пуповине воспалительных изменений серозно-геморрагического или гнойно-некротического типа. Развивается серозно-фибриноз-ный перитонит с массивным наложением фибрина на серозных покровах брюшной полости, вокруг пупочной вены и артерий. Стенки сосудов утолщены, отечны, снаружи красного цвета, в просвете сосудов видны различной длины тромбы с зонами гнойного расплавления. Поверхностные паховые лимфоузлы увеличены, гиперемированы, отечны, на разрезе темно-вишневого цвета. Селезенка слегка увеличена, полнокровна. Печень — дряблая, с очаговыми некрозами. В суставах — признаки серозно-фибриноз-ного воспаления.
Местный воспалительный процесс выражается признаками воспаления пупочного канатика.
Диагноз. Его ставят с учетом анамнестических данных о течении родов, клинических и патологоанатомических признаков; диагностическим тестом можно считать изменения в области пупочного канатика.
Дифференциальный диагноз. Пупочный сепсис необходимо отличать от диспепсии, анаэробной дизентерии, энте-робактериальных инфекций. Окончательный диагноз подтверждают лабораторными бактериологическими исследованиями.
Лечение. Используют антибактериальные средства. Наиболее эффективно введение половины дозы антибиотика парентерально и половины — методом обкалывания области пуповины.
Эффективны тетрациклин в дозе 20мг/кг массы животного 4 раза в день внутримышечно, бициллин-3 и -5—20 тыс. ЕД/кг (бициллин-3 инъецируют 1 раз в 4—6 дней, а бициллин-5 — 1 раз в 10—15 дней), эритромицин внутримышечно. Для внутримышечного введения готовят раствор эритромицина на этиловом спирте из расчета 5—8 тыс. ЕД/кг массы животного. Сначала препарат растворяют в 2—Зсм 3 спирта, а затем добавляют 4—6 см 3 1%-ного раствора новокаина. Раствор вводят 2 раза в день.
Мономицин или мицерин вводят внутримышечно по 15— 20 тыс. ЕД/кг массы животного 2—3 раза в день. Оримицин инъецируют внутримышечно, подкожно или внутрибрюшинно из расчета 4—10 мг/кг массы животного 2 раза в сутки в течение 5— 7 дней. Эффективно парентеральное применение сарафлоксацина ежедневно в течение 3 дней в дозе 10 мг/кг. Используют и другие антибиотики широкого спектра действия: препараты группы энрофлоксацина, ципрофлоксацина, офлоксацина, цефаллоспорины. При необходимости назначают симптоматическое лечение.
Профилактика. Для того чтобы снизить заболеваемость и гибель молодняка от пупочного сепсиса, следует роды принимать в строго санированных помещениях, соблюдая при этом правила гигиены. Норматив микробного загрязнения в родильном отделении скотоводческих ферм составляет не более 50 тыс. микробных тел в 1 м 3 воздуха помещения.
Сразу после рождения животное необходимо обтереть сухим стерильным полотенцем. Если не произошел самопроизвольный обрыв, необходимо обрезать пупочный канатик (оставляя культю у телят и жеребят длиной 7—8 см, а у поросят, ягнят и козлят 3—5 см), затем стерильными руками или пинцетом выдавить вартонов студень (желеобразная соединительнотканная прослойка пупочного канатика) и обработать культю классическими антисептическими препаратами: 5%-ным спиртовым раствором иода, 96%-ным этиловым спиртом, 2%-ным раствором перексида водорода, 1%-ным спиртовым раствором бриллиантового зеленого, 2%-ным раствором диоксидина или хлоргексидина.
Протейная инфекция (Contagiu protealis) — факторная энтеро-бактериальная болезнь молодняка животных, в том числе птиц, характеризующаяся нарушением пищеварения.
Возбудитель. Болезнь вызывают кишечные бактерии из семейства Enterobacteriaceae. Род Proteus характеризуют полиморфность палочек (1—3x0,4—0,8 мкм), грамнегативность, отсутствие образования спор и капсул, подвижность за счет перитрихиальных жгутиков.
На кровяном агаре некоторые штаммы протея при росте могут вызвать гемолиз. На агаре Плоскирева протей образует крупные (2—8 мм) колонии с перламутровым оттенком. Для выделения чистой культуры посев проводят в конденсационную жидкость скошенного агара.
Палочки протея образуют уреазу, сероводород, редуцируют нитраты, гидролизуют желатин, ферментируют глюкозу с выделением кислоты и газа, оксидазоотрицательны, каталазоположи-тельны. Способность к дезаминированию фенилаланина — один из основных признаков энтеробактерий рода Proteus и фенотипи-чески близких к ним морганелл и провиденций, позволяющих дифференцировать их от остальных энтеробактерий.
Антигенная структура протеев включает термостабильный соматический О-антиген (известно около 50 соматических антигенов) и термолабильный жгутиковый Н-антиген (таких открыто 19), серологическая принадлежность к которым определяется имеющимися коммерческими иммунными сыворотками.
Род Proteus включает четыре вида: P. vulgaris, P. mirabilis, P. morganil и P. retigeri. В этиопатогенезе кишечных расстройств у молодняка участвуют в основном P. vulgaris и P. mirabilis. Эти виды протея — наиболее часто выделяемые у животных, в том числе птиц, а также у людей и с объектов окружающей среды. Дифференцирующие признаки P. vulgaris — индолообразование и ферментация мальтозы с образованием кислоты, P. mirabilis — положительный тест с орнитиндекарбоксилазой и ферментация ксилозы с образованием кислоты.
Из лабораторных животных к парентеральному введению протея чувствительны белые мыши, кролики, морские свинки.
Возбудитель протейной инфекции устойчив к воздействию неблагоприятных факторов среды, резистентен к фенолу, пероксиду водорода, этакридину в стандартных концентрациях. На объектах внешней среды, в почве, воде, навозе сохраняется несколько мес, температура 60 °С его инактивирует не менее чем за 1 ч, 90 °С — за 5 мин.
Эпизоотологические данные. Протей относится к группе сапрофитных микроорганизмов желудочно-кишечного тракта животных. Удельный вес протейных бактерий относительно микроорганизмов других родов в тонком кишечнике здорового молодняка сельскохозяйственных животных— 1,1 %. Развитие инфекционного заболевания — протейной диареи — во многом зависит от санитарной культуры, условий кормления, зоогигиенических параметров содержания животных, иммунного статуса.
Являясь слабовирулентными, протейные палочки становятся причиной болезни ослабленного молодняка, наиболее подверженного стрессам, находящегося в иммунодепрессивном состоянии. Кроме того, протейные инфекции часто развиваются вторично при дисбактериозах неспецифического характера (диспепсия, гастроэнтериты) и при вирусной инфекции (ротавирусной диарее, корона-, парво-, аденовирусной и других инфекциях). Пассажи-руясь через ослабленных животных, возбудитель накапливает вирулентность и выделяется в больших количествах с фекальными массами больных животных. Это служит причиной заражения молодняка остального поголовья.
Палочки протея выделяют из ран, среднего уха при отитах, смывов с глазного яблока при керато-конъюнктивальных поражениях, дерматитных и язвенных поражений межпальцевых пространств, ногтевого ложа, носового хода животных практически всех видов, в том числе птиц, а также человека. В чистой культуре возбудителя почти всегда получают из мочи. Выделение бактерий Proteus из влагалища при метритах и вагинитах, молочной железы при маститах у самок не исключает вертикальный путь передачи инфекта.
Вспышки протейной инфекции преимущественно спорадические, в случае эпизоотии протей, как правило, играет сопряженную роль вторичной инфекции при смешанном (ассоциативном) инфекционном поражении. Основной путь передачи возбудителя инфекции — алиментарный. Восприимчивые животные — преимущественно телята первых трех недель жизни, поросята до 2-месячного возраста. У ягнят, жеребят, козлят и молодняка животных других видов болезнь в кишечной форме отмечали редко, чаще единичные случаи. Протей может быть причиной пищевых токсикоинфекций человека.
Летальность при протейной инфекции среди молодняка крупного рогатого скота и свиней колеблется в пределах 5—18 %.
Патогенез. Он свойственен факторным энтеробактериозам. При благоприятных факторах для развития бактерий (низкая резистентность организма, высокая доза попадания вирулентных протеев, дисбалансы рациона, низкое качество кормов, приводящие к нарушению рН кишечной среды, низкой активности ферментов, накоплению недоокисленных продуктов, развитию процессов гнилостного распада и токсинообразования) и ослаблении местного иммунитета в желудочно-кишечном тракте начинают усиленно размножаться грамотрицательные палочки протея и других энтеробактерий, угнетая размножение бифидо- и лакто-бактерий. Быстрый рост и заполнение кишечника токсижюбразу-ющими палочками протея приводит к усилению перистальтики раздраженной слизистой кишечника, увеличению выделения аде-нилатциклазы, приводящему к переходу воды из организма в просвет кишечника. Развивается диарея и явления дегидратации. Воздействие токсинов приводит к выраженному угнетению, потере аппетита.
Клинические признаки. Различают острое, под острое и хроническое течение.
При остром течении протейной инфекции инкубационный период составляет от двух до нескольких суток. Болезнь проявляется у молодняка всех видов животных лихорадкой (часто невысокой), угнетением, анорексией. Развивается диарея серо-коричневого цвета с зеленоватым оттенком, у телят профи-лакторного периода — желтого цвета с кисловатым и гнилостным запахом.
На 3—4-е сутки отмечают западение глаз, потерю эластичности кожи, слабость конечностей, одышку и тахикардию. Поражаются органы мочевыделительной системы: развивается болезненность паховой области, возможны странгурия и тенезмы, в моче — много слизи, белка, эпителиального детрита.
На 4—5-е сутки вероятна гибель животных.
Подострое течение болезни сопровождается менее выраженными признаками общего угнетения и слабости. Диарея не профузна, лихорадка не характерна. Возможно незначительное и кратковременное повышение температуры. Иногда процесс затягивается.
Хроническое течение сопровождается периодическими явлениями диареи или разжижения фекальных масс. На общем состоянии и аппетите животных патология почти не отражается, но больной молодняк отстает в росте, развитии и становится предрасположенным к другим желудочно-кишечным и респираторным заболеваниям. Со временем у таких больных нередко развивается нефрит или уроцистит протейной природы.
Патологоанатомические признаки. При вскрытии обнаруживают характерную картину энтерита, содержимое тонкого кишечника жидкое, зловонное, сосуды инъецированы, слизистая набухшая с десквамированным эпителием. Реже отмечают катаральный или катарально-геморрагический колит.
Выявляют зернистую дистрофию печени, увеличение перито-неальных лимфоузлов, дряблость почек с точечными кровоизлияниями под капсулой, инъекцию сосудов и отечность слизистой почечной лоханки и мочевого пузыря. Все признаки более выражены у истощенных трупов после хронического течения протейной инфекции.
Диагноз. Диагностика протейной инфекции комплексная, базирующаяся на эпизоотологических данных, клинических признаках, патологоанатомических изменениях. Основой постановки диагноза являются бактериологические исследования с обязательной постановкой биопробы.
Бактериологические исследования осуществляются по общепринятой схеме и включают окраску по Граму и микроскопию мазков-отпечатков патматериала (соскобы промытой слизистой кишечника, лимфатические узлы, печень, селезенка, кровь из сердца, красный костный мозг); посевы на МПА, МПБ, П-1 (Калина, 1975), содержащую полимиксин и соли желчных кислот, инги-бирующие рост других микроорганизмов, кровяной агар, агары Левина, Плоскирева; просмотр колоний и микроскопию окрашенных культур; определение биохимических свойств возбудите- j ля (не обязательно) и, обязательно, патогенности для лаборатор- ! ных животных. В необходимых случаях прибегают к серологической идентификации в РИГА.
Дифференциальный диагноз. Протейную инфек- | цию дифференцируют от сходно протекающих заболеваний мо- ' лодняка: эшерихиоза, сальмонеллеза, клебсиеллеза, псевдомоно-за, стрептококкоза, диспепсии, рота-, корона-, парво-, аденовирусных инфекций, вирусной диареи, дизентерии свиней. Основой дифференциальной диагностики являются бактериологические исследования. Дифференциальная лабораторная диагностика протейной инфекции не вызывает затруднений — протей легко отличим по культуральным свойствам.
Лечение. Из средств специфического лечения разработаны поливалентная сыворотка против колибактериоза, сальмонеллеза, клебсиеллеза и протейной инфекции молодняка сельскохозяйственных животных, а также протейный бактериофаг и полифаг. Применение сыворотки заболевшим острым кишечным заболеванием телятам позволяет снизить их летальность в среднем на 70 %. В условиях ферм монофаги недостаточно эффективны в связи с участием множества возбудителей острых кишечных заболеваний молодняка сельскохозяйственных животных. Так, эффективность протейного бактериофага составила 54 %. Полифаг, включающий в состав эшерихиозный, протейный, стафилококковый, клебсиел-лезный и псевдомонозный бактериофаги, оказал высокий терапевтический эффект — лечебная эффективность составила 98,2 % (Д.А. Девришов, 2000).
Применяют антибиотики и другие химиотерапевтические средства с определенной (подтитрованной) чувствительностью протея к ним. Протейные палочки резистентны ко многим антибиотикам и сульфаниламидным препаратам. Специалисты отмечают активность к протею неомицина, колимицина и мономицина. Их применяют 2—3 раза в день с кормом по 20—30 мг/кг массы животного, мономицин также вводят и внутримышечно по 15000— 20000 ЕД/кг 2—3 раза в день. Эффективно применение препаратов (на 1 кг массы животного): энрофлоксацина — 5 мг 1—2 раза в сутки; гентамицина и левомицетина — 20 мг 2—3 раза в день перо-рально; леванзама — 0,25г; флубактина—12мг; рифана — 0,3г 2 раза в сутки перорально; палехина и эридина — 200 мг 1—2 раза в день внутрь с кормом или водой, а также кол истина в дозе 2 кг/т корма. Последними исследованиями показана наибольшая чувствительность протея к ципрофлоксацину, офлоксацину, норф-локсацину, клафорану, байтрилу.
Со 2—3-го дня после применения антибиотиков необходимо за 10—15 мин до кормления задавать больным внутрь пробиотики: ацидофиллин, лактобактерин, сгол, бифитрилак, ветом 1.1 и ве-том 3, лактобифадол, споробактерин и др. Для комплексного лечения необходима инфузия глюкозо-солевых растворов, выпойка отваров конского щавеля, ромашки аптечной, коры дуба, сенного отвара, дача адсорбентов. Установлена высокая сорбционная активность энтеросорбента ЭСТ-1 в отношении органических красителей, алкалоидов, ароматических соединений, а также микробных клеток Е coli, Pseudomonas aeroginosa, Proteus vulgaris, Salmonella enteritidis. Он повышает чувствительность кишечной микрофлоры к наиболее используемым в ветеринарной практике антибиотикам. Применение ЭСТ-1 в дозе 200 мг/кг массы животного 1 раз в сутки в комплексе с гипериммунной аллогенной сывороткой оказало высокую терапевтическую эффективность при острой протейной инфекции.
Иммунитет. Переболевшие животные, как правило, протейной инфекцией больше не заболевают. При соблюдении ветеринарных и зоотехнических требований иммунитет после переболевания довольно стоек в течение года, т. е. до возрастного периода невосприимчивости.
Для активной иммунизации разработана ассоциированная инактивированная вакцина против острых кишечных заболеваний молодняка сельскохозяйственных животных, в том числе протейной инфекции.
Профилактика и меры борьбы. Основы профилактики протейной инфекции — высокая санитарная культура ведения животноводства в хозяйстве; соблюдение комплекса мероприятий по выращиванию здорового молодняка, включающего полноценное и сбалансированное кормление; вовремя проведенные в полном объеме выпойки молозива; контроль параметров микроклимата в помещении для содержания подсосного и послеотъемного молодняка.
Эффективна вакцинация стельных коров и супоросных свиноматок за 30 и 15 дней до родов, затем молодняка в 20-дневном возрасте. Наилучшие результаты сохранности поголовья молодняка получены при одновременной активной иммунизации вакцинами и применением иммуностимуляторов (Т- и В-активина, бурсина, миелопептида, иммунофана, достима и др.). Профилактируют развитие протейной инфекции дачей молодняку пробиотиков и бактериофагов против протея (полифага) в первые недели жизни, выпойкой молока, закисленного муравьиной кислотой.
Клебсиеллез (Klebsiellosis) — инфекционная болезнь, характеризующаяся поражением желудочно-кишечного тракта и респираторных органов.
Возбудитель. Болезнь вызывают бактерии рода Klebsiella. Это грамотрицательные, неподвижные, не образующие спор и образующие капсулу палочки семейства Enterobacteriaceae размером 0,3—1,0x0,6—6,0 мкм. В мазках они располагаются поодиночке, парами или короткими цепочками. Неподвижны, утилизируют цитрат и глюкозу, ферментируют инозит, гидролизуют мочевину, образуют сероводород. В отличие от эшерихий не выделяют индол (исключение — К. oxytoca).
Клебсиеллы хорошо растут на МПА, МПБ и других питательных средах. Наличие капсулы обусловливает образование крупных, выпуклых, влажных, часто сливающихся колоний слизистой консистенции. В жидких средах рост сопровождается равномерным помутнением, образованием осадка и поверхностной пленки. На агаре Эндо образуют красные и розовые колонии с металлическим блеском, так как среди клебсиелл имеются штаммы как хорошо ферментирующие лактозу, так и слабоферменти-рующие.
Род Klebsiella представлен четырьмя видами: К. pneumoniae, К. oxytoca, К. Terrigena и К. planticola. Последние два вида в большинстве случаев выделяют из объектов окружающей среды. К. oxytoca и К. pneumoniae подвида pneumonia — постоянная микрофлора кишечника, но в зависимости от вирулентности, количества возбудителя, условий размножения и иммунного статуса восприимчивого организма могут вызывать энтеритную форму заболевания желудочно-кишечного тракта, а также пневмонии, сепсис. К. pneumoniae может играть роль этиологического фактора при метритах, маститах, конъюнктивитах. Патогенные клебсиеллы серологически идентичны возбудителю склеромы человека.
Кроме подвида pneumoniae К. pneumoniae подразделяется еще на подвиды ozaenae и rhinoscleromatis, имеющие основные отличия по утилизации муката, уреазной активности, использовании малоната натрия и цитратов.
В. И. Терехов и Н. Н. Гугушвили установили, что основным видом, циркулирующим на фермах выращивания крупного рогатого скота, является К. pneumoniae подвида pneumoniae (67,4 %). Выделенные клебсиеллы обладали альфа-гемолитической активностью и были патогенны для лабораторных животных. Этиологическим фактором клебсиеллеза поросят авторы, в основном, выделяют также К. pneumoniae подвида pneumoniae.
При острых кишечных заболеваниях новорожденных телят выделяют 12—13 % патогенных клебсиелл. В видовом составе преобладают К. pneumoniae (93—95 %) и К. oxytoca (4—6 %). По биохимической активности выделенные клебсиеллы в рамках вида практически однородны, однако их серотипирование выявило значительную вариабельность. Среди молодняка сельскохозяйственных животных циркулируют преимущественно 15 серотипов бактерий.
Клебсиеллы в фекалиях и слизи сохраняются до 40 дней, в воде и почве — до нескольких мес. К высокой температуре и дезинфекционным средствам устойчивы слабо. При 100 °С погибают мгновенно, при 80 °С — в течение 20 мин. Губительно действуют на клебсиелл: 4%-ный горячий раствор натрия гидроксида, 5%-ная эмульсия ксилонафта, 10%-ная эмульсия креолина, 20%-ная взвесь свежегашеной извести, осветленный раствор кальция ги-похлорида, содержащий 3 % активного хлора и др.
Эпизоотологические данные. Источник возбудителя инфекции — больные животные (телята, поросята) и свиноматки-бактерионосители. Возбудителя выделяли из носовой слизи, мокроты при кашле, экссудата из глаз, фекалий.
Чаще болезнь регистрируют среди молодняка, подвергшегося воздействию неблагоприятных факторов внешней среды (отъем от свиноматок в раннем возрасте, перегруппировки, неудовлетворительный микроклимат в помещениях, высокая запыленность воздуха, транспортировка, переохлаждение, перегревание). Основные пути передачи — алиментарный и аэрогенный.
Заболевают поросята обычно через 8—10 дней после отъема от свиноматок, однако нередки случаи болезни поросят под матками до 20-дневного возраста. Они представляют особую опасность как источник возбудителя инфекции при переводе их на групповое содержание. Преобладающие формы болезни для поросят — респираторная и септическая.
Телята, как правило, заболевают в профилакторный период эн-теритной формой. Редко отмечают респираторную форму клебсиеллеза у телят с 20-дневного возраста.
По последним данным, клебсиеллез может развиваться как вторичная инфекция на фоне поражения молодняка вирусами (рота- и корона-), что приводит к более высокой заболеваемости и летальности животных.
Патогенез. Как и все энтеробактерии клебсиеллы обладают экзо- и эндотоксином. Повышение вирулентности возбудителя приводит к воздействию токсинов на слизистую кишечника, снижению местной резистентности, дисбактериозу. Проникая в кровь, клебсиеллы вызывают септикопиемию. Выделяемые токсины обусловливают развитие угнетения и другие клинические признаки болезни.
Клинические признаки. Инкубационный период длится от нескольких часов до 5 дней. Болезнь протекает остро, подостро и хронически.
При остром течении у телят повышается температура тела до 40 "С, развиваются угнетение, анорексия и диарейный синдром. Фекальные массы — зловонные, жидкие, от светло-жел-того до серого цвета.
У поросят повышается температура тела до 40,5—41 "С. Животные угнетены, дыхание затрудненное, учащенное, болезненное, возникают приступы кашля, напряженность и болезненность брюшной стенки, у некоторых животных появляется рвота и диарея. Поросята стараются принять позу, позволяющую снизить давление на грудную клетку (широко расставляют конечности).
При септической форме развивается еще более выраженные лихорадка и угнетение. Животные отказываются от корма, тяжело дышат, развивается отсутствие реакции на внешние раздражители. При пальпации брюшная стенка болезненна, при перкуссии устанавливают зоны притупления в легких. Гибель наступает через 2— 4сут.
При подостром течении симптомы болезни нарастают медленнее, клинические признаки менее выражены, лихорадка ремитирующего типа. Подострое и хроническое течение клебси-еллеза как у поросят, так и у телят более характерны при респираторной форме.
При хроническом течении развивается тахипное и периодический приступообразный влажный глубокий кашель. Животные резко отстают в росте и развитии, у них отмечают слезотечение и истечения из носовых отверстий.
Патологоанатомические изменения. У погибших при остром течении болезни видимые слизистые оболочки бледные, с синюшным оттенком. Обнаруживают признаки острого катарального энтерита, увеличение лимфоузлов брюшной полости, дистрофию печени. При септической форме отмечают слипчивость кишечника и отек легких с участками катаральной бронхопневмонии. Печень несколько кровенаполнена, селезенка, как правило, увеличена в 2—4 раза, дряблой консистенции.
У погибших при подостром течении болезни выражены отложения фибрина на плевре, участки катаральной бронхопневмонии или крупозной пневмонии в стадии красной гепатиза-ции. Сосуды тонкого кишечника инъецированы. Отмечают преимущественное поражение бронхиальных лимфоузлов (лимфаденит с очаговым некрозом).
В случае гибели при хроническом течении клебсиел-леза устанавливают большое разнообразие патологоанатомичес-ких изменений, преимущественно респираторного характера.
Кроме того, отмечают системное поражение паренхиматозных органов: зернистая дистрофия печени, селезенки. Почки кровена-полнены — в них очаговые, реже разлитые кровоизлияния. Отмечают также кровоизлияния под эпикардом.
Диагноз. Постановка диагноза должна основываться на комплексном анализе эпизоотологических данных, клинических признаков, патологоанатомических изменений и результатов бактериологического исследования. Патологический материал берут не позднее 4—6 ч после гибели животного, предпочтительнее у павшего с признаками острого течения болезни и не подвергавшегося лечению антибиотиками. Из патологического материала готовят мазки, окрашивают их по Граму и микроскопируют. В мазках возбудитель имеет вид полиморфных грамотрицательных палочек. Также мазки исследуют в реакции иммунофлюоресценции.
Чистую культуру выделяют посевами на накопительные и дифференциальные среды. Важное диагностическое значение имеет посев культуры на биохимический ряд (среды Гисса), после родового определения проводят серологическую идентификацию и устанавливают патогенность для лабораторных животных (белые мыши).
Дифференциальный диагноз. Клебсиеллез телят необходимо дифференцировать от других энтеробактериальных инфекций (эшерихиоз, сальмонеллез, протейная инфекция), от ротавирусного энтерита, коронавирусного гастроэнтерита, диспепсии. При хроническом течении — от пастереллеза, хламидиоз-ной бронхопневмонии, аденовирусной и других респираторных инфекций. Важнейшее дифференциальное значение имеет лабораторный анализ.
Клебсиеллез поросят требует дифференциации от актиноба-циллезной плевропневмонии, пастереллеза, микоплазмоза, стреп-тококкоза, гемофилезного полисерозита и энтеротоксемии.
Лечение. В день заболевания новорожденных телят пропускают очередную выпойку им молозива (молока) и заменяют его теплым физиологическим раствором. Выдерживают животных 8—12 ч на голодной диете, а затем к физраствору добавляют в количестве 50 % суточной нормы молозиво (молоко) и выпаивают 3—4 раза в сутки.
В качестве специфического лечения предложена поливалентная гипериммунная сыворотка, которую вводят подкожно, внутримышечно или внутривенно в дозах 1—2 см 3 /кг массы животного.
Применение гамма-интерферона для профилактики клебсиел-леза показало, что 2—3 инъекции препарата предотвращают заболеваемость более чем у 90 % поросят-сосунов и новорожденных телят.
С профилактической и лечебной целями применяют поливалентный бактериофаг против сальмонеллеза, эшерихиоза, клебси-еллеза и протейной инфекции молодняка сельскохозяйственных животных. Его дают перорально 3 раза через каждые 2 ч. Перед дачей разводят в 100—150 мл кипяченой, охлажденной до 20— 25 °С воды. Рекомендуется за 10—15 мин до применения фага дать больному животному 25—30 мл 3—5%-ного раствора натрия гидрокарбоната. После 3-дневного лечения бактериофагом делают перерыв на 1—2 дня и в случае необходимости дачу его повторяют.
Высок терапевтический эффект антибиотиков, выбор которых основывается на обязательном определении чувствительности патогенных клебсиелл к ним. Хорошего результата добились, применяя биомицин, левомицетин, синтомицин в дозах 10—20мг/кг массы животного 3 раза в день в течение 5—7 дней. Эффективно применение сорбофура, полипаренхимина, ветсептола, тамерита.
По мере выздоровления животного постепенно увеличивают количество выпаиваемого молока до нормы, установленной в хозяйстве. Вслед за антибиотикотерапией применяют пробиотики: АБК, ПАБК, лактобифадол, сгол и др.
При респираторной форме получены положительные результаты при внутримышечных инъекциях гентамицина — 2 раза в день в дозе 1,5—2 мг/кг, а также при пероральном введении суль-фотрима — 2 раза в день в дозе 30 мг/кг массы животного. Суль-фамонометоксин в дозе 25—35 мг/кг массы животного дают в 100 мл кипяченой воды за 1 ч до выпаивания молозива 2—3 раза в день в течение 3 сут. Назначают также (на 1 кг массы животного): полимиксина М сульфат — 20 тыс. ЕД; неомицин — 10 тыс. ЕД, хлортетрациклин — 20 мг; фуразолидон — 7 мг и аскорбиновую кислоту — 5 мг. Удовлетворительные результаты получают при внутримышечных инъекциях растворов тетраолеана в дозе 20 мг и 1 см* 10%-ного раствора кофеина 2 раза в течение 2 дней, при назначении фуразолидона в дозе 0,3 г и сульфадимезина в дозе 0,5 г в течение 7 дней после отъема, а также триметасула-3 в дозе 1 г на одно животное с кормом 2 раза в день. Эффективна дача абактана из группы фторхинолонов, который задают с кормом или водой в дозе 5 мг/кг массы животного в течение 3 дней после отъема от свиноматок.
Телятам применяют поливинил пироллидон. Его выпаивают в водном растворе в дозе 3—6 мг/кг массы животного 2 раза в день в течение 1—5 дней. Внутримышечно инъецируют 1 раз в 3 дня лиг-фол в дозе 0,1 см 3 /кг.
В первые дни болезни эффективно внутримышечное введение 2%-ных растворов антигистаминных препаратов (пипольфен, суп-растин) 2—3 раза в сутки в дозе 0,03—0,04 см 3 /кг.
Одновременно вводят витаминные препараты: тривитамин, тетравит, аскорбиновую кислоту, а для поросят еще витамины группы В (комплексные препараты — аминовит, гамавит, урсовит и др.). При развитии респираторного синдрома применяют бронхолитики и отхаркивающие препараты. Экономически целесообразно использовать для этих целей отвар хвои сосны лесной, листьев мать-и-мачехи, головок клевера.
Иммунитет. Инфекционный процесс клебсиеллеза у свиней сопровождается образованием в организме антител, а их защитная функция подтверждается наличием выраженного колострального иммунитета.
Положительный эффект дает применение ассоциированной инактивированной вакцины против острых кишечных заболеваний молодняка, содержащей антигены клебсиелл.
Профилактика и меры борьбы. Основа профилактики — оптимальные условия содержания и кормления молодняка, вовремя выпоенное молозиво, гигиена родов.
Чтобы предупредить возникновение клебсиеллеза новорожденным в первые 2—4 ч жизни перорально и внутримышечно вводят поливалентную сыворотку, бактериофаг, нормальные глобулины сывороток крови животных, пробиотики.
Для профилактики клебсиеллеза у поросят им с 5-го дня скармливают железосодержащие препараты, а 10-го — витаминные корма и приучают к поеданию концентрированных кормов. Для предупреждения стресса при отъеме поросят 10—15 дней оставляют на месте, а затем переводят на доращивание и скармливают те же корма. В первые 3 нед после отъема в воду целесообразно добавлять препарат пиглет. В период отъема поросятам дают с молоком по одной столовой ложке 3—5%-ного раствора кальция хлорида 1—2 раза в день; 0,1%-ный раствор селенита натрия (по 0,01—0,02 мг/кг их массы) за 5 дней до отъема и на 10—12-е сутки после отъема.
Важный момент в профилактике клебсиеллеза — вакцинация животных, особенно она эффективна для супоросных свиноматок и при назначении коровам в сухостойный период, за 25—30 и 15 дней до родов.
Мероприятия по специфической профилактике не достаточны для высокоэффективной борьбы с инфекцией. Только комплекс мер, включая зоотехнический контроль и ветеринарно-са-нитарные мероприятия, позволит эффективно бороться с заболеванием. Перед входом в профилакторий необходимо оборудовать дезковрик или дезванну. Для дезинфекции помещения применяют одно из следующих средств: 4%-ный горячий раствор натрия гидроксида, 2%-ный раствор хлорамина или гипохлора, содержащего 3 % активного хлора; 3%-ный раствор препаратов парасод или фоспар, аэрозольно формалин из расчета 20 мл/м 3 помещения и др.
При возникновении болезни хозяйство объявляют неблагополучным. Больных изолируют и лечат комплексно, используя специфические и неспецифические средства. Животных, подозреваемых в заболевании (условно больных) обрабатывают гипериммунной антитоксической сывороткой или бактериофагом в лечебных дозах дву- или трехкратно.

В последние годы инфекционисты отмечают рост заболеваний, обусловленных нетрадиционными микроорганизмами. Особое место занимает протейная инфекция. Ее кишечная форма, вызванная бакетриями рода Протей — P. vulgaris протекает тяжелее у детей раннего возраста. Не менее опасны гнойно-воспалительные заболевания мочевыводящей системы, вызываемые P. mirabilis, P. rettgeri и P. morganii.
В греческой мифологии Протей – божество, способное менять облик. Отсюда название полиморфных, мелких, нитевидных палочек, отличающихся активной подвижностью. Размеры клеток составляют 0,5 — 3 мкм. P. morganii, P. rettgeri — менее полиморфны и малоподвижны.
Протейная инфекция: причины, развитие, опасность для организма
Возбудителями протейной инфекции являются грамотрицательные условно-патогенные микроорганизмы семейства энтеробактерий, которые присутствуют в нормальной микрофлоре кишечника, а также повсеместно распространены в воздухе, почве и воде. Бактерии рода Proteus в течение долгого времени не причислялись к возбудителям серьезных инфекционно-воспалительных заболеваний. Однако в связи с последними достижениями в области диагностики было обнаружено, что эти микроорганизмы способны вызывать трудно поддающиеся лечению патологии (протеозы), поражающие преимущественно ЖКТ и мочеполовую систему.
Протей – факультативный анаэроб, палочковидная, неспороносная, подвижная, грамотрицательная бактерия. В микробиологическом анализе кала протей встречается в комплексе с другими условно-патогенными бактериями семейства энтеробактерий. Кроме протея, в составе нормальной микрофлоры кишечника человека определяются: клебсиелла, энтеробактер, гафния, серратия, морганелла, провиденция, цитробактер. В 1 г кала должно быть меньше 10 4 общего количества этих бактерий. Большее количество перечисленных бактерий является признаком дисбактериоза.
В природе бактерии рода Proteus обнаруживаются: в сточных водах, в земле, в водоемах, на овощах, в разлагающихся органических веществах. Эти микроорганизмы — сапрофиты, они живут на слизистых оболочках, на коже, в кишечнике человека и животных. Протеи устойчивы во внешней среде и сохраняют жизнедеятельность в слабых растворах фенола и других средств. Выявлена также резистентность ко многим антибиотикам.
Причины протейной инфекции
Протейная палочка, присутствующая в кишечной микрофлоре в небольших количествах, не причиняет организму никакого вреда. При определенных обстоятельствах (снижение иммунитета, неправильное питание, длительный прием антибиотиков) она может активизироваться и начать интенсивно размножаться. Также инфицирующее количество этих бактерий способно проникнуть в организм из внешней среды.
Основными путями передачи инфекции являются пищевой и контактно-бытовой. Чаще всего заражение происходит при употреблении белковых продуктов (мяса, рыбы, молока, колбасы), которые хранились с нарушением надлежащих сроков и условий. Значительно реже инфицирование осуществляется через немытые руки, во время купания или при употреблении зараженной воды.
Инфицирование протеем может произойти через полуфабрикаты, сырые продукты или готовые блюда из мяса, рыбы, молока, колбасы, студня. В них происходит быстрое размножение бактерий с образованием токсинов. Реже отмечают водный путь передачи: при купании в загрязненных водоемах или употреблении инфицированной воды. Возможен и контактный путь передачи на инфицированных руках зараженного человека.
Развитие патологии
При непосредственном попадании протея в ЖКТ вместе с продуктами питания инфекционное заболевание развивается очень стремительно. Первые симптомы ярко выражены, а общая клиническая картина совпадает с проявлениями сильного пищевого отравления. При контактно-бытовом способе заражения развитие признаков инфекции обычно происходит медленнее.
Если инфекционный процесс протекает в легкой форме, больной испытывает слабость, у него отмечаются повышение температуры, рвота, боль в животе, частый водянистый стул, в котором могут обнаруживаться слизь и зеленые включения. При тяжелом течении заболевания приступы рвоты случаются около 10 раз за сутки и более, а температура обычно поднимается до 40°С.
При условии своевременного и адекватного лечения вся острая симптоматика протеоза легкой или средней степени тяжести исчезает спустя несколько дней, после чего больной быстро идет на поправку.
Протеи выделяют токсические вещества — эндотоксины с гемолитическими свойствами и с различной степенью биохимической активности. У штаммов P. vulgaris обнаружена лецитиназная активность. Протеи обладают способностью адгезии к уротелию при помощи ресничек. Отмечают, что резистентность к антибиотикам связана с адгезивной способностью уропатогенных протеев.
Острой кишечной протейной инфекцией, протекающей по типу гастроэнтерита, гастрита и колиэнтерита часто болеют дети раннего возраста с пониженным иммунитетом и после бесконтрольного назначения антибиотиков. Заболевание сопровождается симптомами токсикоза — повышением температуры, рвотой, метеоризмом, схваткообразными болями в животе, нарушением аппетита, кратковременными судорогами, появлением водянистого, зловонного, учащенного стула.
В тяжелых случаях могут развиться осложнения: гемолитико-уремический синдром, а также симптомы острой гемолитической тромбопении, анемии или острой почечной недостаточности.
Клинические проявления внутрибольничной инфекции протейной этиологии весьма разнообразны: поражения мочевыводящей системы, отиты, холециститы, нагноения ран и септические состояния. Попадание протеев в пупочную ранку новорожденного может привести к бактериемии или развитию менингита.
Данные заболевания могут развиться: при передаче возбудителя контактно-бытовым или воздушно-капельным путями, при заносе с катетером, другими урологическими инструментами.
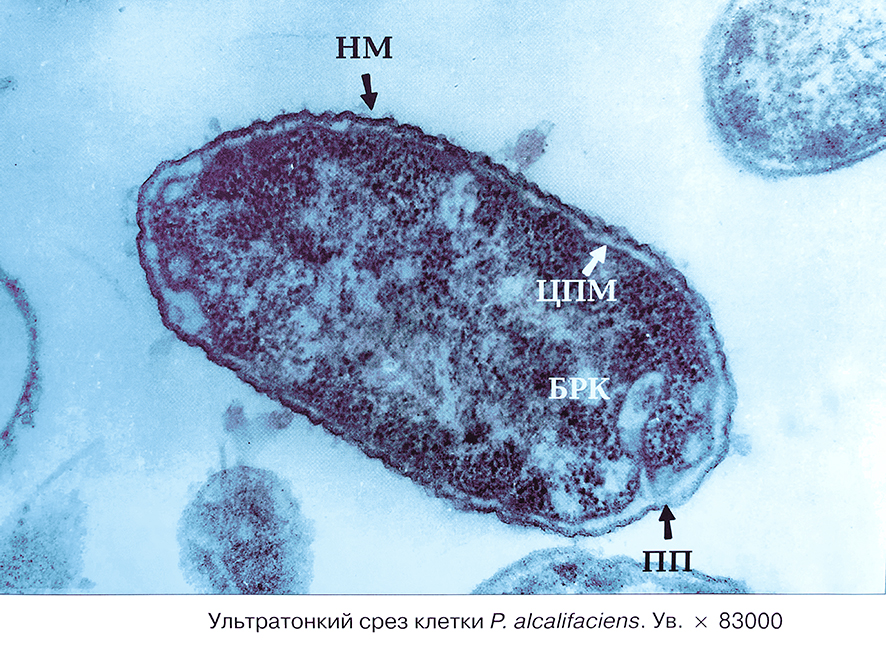
Ультратонкий срез клетки Proteus alcalifaciens. Увеличение *83000
Если в мазках исследуемого материала (участки ожоговой ткани, гной, раневое отделяемое, испражнения) обнаруживаются грамотрицательные палочки, то бактериоскопический метод позволяет сделать предварительное заключение. Бактериологическим методом на средах определяют колонии протея в виде тонкого стелющегося налета. Активно размножаются протеи на белковой питательной среде вызывают гниение мяса, рыбы, других белковых продуктов.
Важнейшие профилактические меры — это соблюдение санитарного режима в детских учреждениях и стационарах, проведение общесанитарных мероприятий. Для профилактики протея каждому необходимо соблюдать правила личной гигиены, исключить потребление подозрительных продуктов в питании, избегать контактов с больными детьми и взрослыми.
При лечении протейной инфекции следует придерживаться лечебной щадящей диеты с исключением жареных, острых блюд, белковых продуктов. В острый период протейного инфицирования, при поражении желудочно-кишечного тракта — необходимо обеспечить восполнение потерянной жидкости. Полезно употреблять отвары трав – тысячелистника, алтея, зверобоя, ромашки, календулы; морсы, компоты с клюквой, черной смородиной, абрикосами, черникой, яблоками. Применять антибиотики можно только по назначению врача, в соответствии с данными анализов чувствительности бактерии протея к ним.
Обязательно нужно принимать препараты – пробиотики, пребиотики, синбиотики для восстановления нормальной флоры кишечника.
Синбиотические комплексы Нормофлорины, содержащий живые активные лакто- и бифидобактерии, секретирующие молочную, уксусную, масляную, пропионовую кислоты, оказывающие защитное, антисептическое, противовоспалительное, сорбционное действие – уменьшает интоксикацию, улучшает моторику кишечника, функцию печени, повышает иммунную реактивность. Это помогает в борьбе с протейной инфекцией, восстанавливает работу желудочно-кишечного тракта, общее самочувствие, повышает иммунитет.
Схема (возрастные дозировки для детей или взрослых): (взрослый) нормофлорин Л – 20 мл (при диарее) – 40 (при запорах) мл утром перед едой, Д — 40 мл вечером за 20 мин до еды, Б – 20-30 мл на ночь в клизме. При диарее в обед можно добавить Д – 30-40 мл, при запорах в обед + Л – 30-40 мл.
Курс приема нормофлоринов — 1 — 1,5 месяца, для выведения токсинов, патогенной микрофлоры, восстановления полезных собственных бактерий. Уникальный состав нормофлоринов, не содержащих белков коровьего молока, молочного сахара, консервантов позволяет при протейной инфекции успешно применять его у детей с первых дней жизни, беременных, кормящих, больных сахарным диабетом, аллергическими заболеваниями, т.е. у взрослых при любой сопутствующей патологии.
Опасность протейной инфекции

Протейная инфекция
Тяжелые формы патологии могут осложняться состояниями, требующими срочной госпитализации больного, такими как сильное обезвоживание, судороги, инфекционно-токсический шок.
protey_mirabilis
Помимо острых инфекций пищеварительной системы бактерии Proteus способны поражать другие органы, распространяясь через кровь или по лимфатическим сосудам. Очаг воспаления может локализоваться в мочеполовой системе, глазах, ушах, легких и даже в костной ткани или мозговых оболочках. Данные патологии достаточно часто переходят в хроническую форму с упорным рецидивирующим течением, которая тяжело поддается терапии.
Если протейная инфекция заносится на незажившие поверхности кожи и слизистых оболочек (послеоперационные раны, ожоги), вызванный ею воспалительный процесс значительно замедляет регенерацию тканей и снижает эффективность лечебных мероприятий.
Следует отметить, что даже незначительное превышение нормального количества протейной палочки в кишечной микрофлоре может негативно отразиться на состоянии здоровья. Так, если у человека имеются аутоиммунные болезни, существует высокий риск их обострения из-за возросшей активности протейной палочки. Атопический дерматит, астма, аллергические заболевания и другие иммунозависимые патологии могут впервые развиться или обостриться под воздействием бактерий Proteus.
Читайте также:

