Раневые инфекции в больницах
Обновлено: 18.04.2024
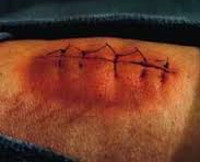
Раневая инфекция – это комплекс общих и местных патологических проявлений, возникающих при развитии инфекции в случайных или операционных ранах. Патология проявляется болью, ознобом, лихорадкой, увеличением регионарных лимфатических узлов и лейкоцитозом. Края раны отечные, гиперемированные. Наблюдается выделение серозного или гнойного отделяемого, в отдельных случаях образуются участки некроза. Диагноз выставляется на основании анамнеза, клинических признаков и результатов анализов. Лечение комплексное: вскрытие, перевязки, антибиотикотерапия.
МКБ-10
Общие сведения
Раневая инфекция – осложнение раневого процесса, обусловленное развитием патогенной микрофлоры в полости раны. Все раны, в том числе и операционные, как в гнойной хирургии, так и в травматологии считаются первично загрязненными, поскольку какое-то количество микробов попадает на раневую поверхность из воздуха даже при безукоризненном соблюдении правил асептики и антисептики. Случайные раны загрязнены сильнее, поэтому в таких случаях источником инфекции обычно является первичное микробное загрязнение. При операционных ранах на первый план выступает эндогенное (из внутренней среды организма) или внутригоспитальное (вторичное) инфицирование.

Причины
В большинстве случаев возбудителем инфекции в случайных ранах становится стафилококк. Редко в качестве основного возбудителя выступает протей, кишечная и синегнойная палочка. В 0,1% случаев встречается анаэробная инфекция. Через несколько дней пребывания в стационаре флора меняется, в ране начинают преобладать устойчивые к антибактериальной терапии грамотрицательные бактерии, которые обычно становятся причиной развития раневой инфекции при вторичном инфицировании как случайных, так и операционных ран.
Раневая инфекция развивается в случае, когда количество микробов в ране превышает некий критический уровень. При свежих травматических повреждениях у ранее здорового человека этот уровень составляет 100 тыс. микроорганизмов на 1 г ткани. При ухудшении общего состояния организма и определенных особенностях раны этот порог может существенно снижаться.
К числу местных факторов, повышающих вероятность развития раневой инфекции, относится присутствие в ране инородных тел, сгустков крови и некротических тканей. Также имеет значение плохая иммобилизация при транспортировке (становится причиной дополнительной травмы мягких тканей, вызывает ухудшение микроциркуляции, увеличение гематом и расширение зоны некроза), недостаточное кровоснабжение поврежденных тканей, большая глубина раны при малом диаметре раневого канала, наличие слепых карманов и боковых ходов.
Общее состояние организма может провоцировать развитие раневой инфекции при грубых расстройствах микроциркуляции (централизация кровообращения при травматическом шоке, гиповолемические расстройства), нарушениях иммунитета вследствие недостаточного питания, нервного истощения, химических и радиационных поражений, а также хронических соматических заболеваний. Особенно значимы в таких случаях злокачественные новообразования, лейкемия, уремия, цирроз, сахарный диабет и ожирение. Кроме того, снижение сопротивляемости инфекции наблюдается при проведении лучевой терапии и при приеме ряда лекарственных средств, в том числе – иммунодепрессантов, стероидов и больших доз антибиотиков.
Классификация
В зависимости от преобладания тех или иных клинических проявлений гнойные хирурги выделяют две общие формы раневой инфекции (сепсис без метастазов и сепсис с метастазами) и несколько местных. Общие формы протекают тяжелее местных, вероятность летального исхода при них повышается. Самой тяжелой формой раневой инфекции является сепсис с метастазами, который обычно развивается при резком снижении сопротивляемости организма и раневом истощении вследствие потери больших количеств белка.
К числу местных форм относятся:
- Инфекция раны. Является локализованным процессом, развивается в поврежденных тканях с пониженной сопротивляемостью. Зона инфицирования ограничена стенками раневого канала, между ней и нормальными живыми тканями есть четкая демаркационная линия.
- Околораневой абсцесс. Обычно соединен с раневым каналом, окружен соединительнотканной капсулой, отделяющей участок инфекции от здоровых тканей.
- Раневая флегмона. Возникает в случаях, когда инфекция выходит за пределы раны. Демаркационная линия исчезает, процесс захватывает прилежащие здоровые ткани и проявляет выраженную тенденцию к распространению.
- Гнойный затек. Развивается при недостаточном оттоке гноя вследствие неадекватного дренирования или зашивании раны наглухо без использования дренажа. В подобных случаях гной не может выйти наружу и начинает пассивно распространяться в ткани, образуя полости в межмышечных, межфасциальных и околокостных пространствах, а также в пространствах вокруг сосудов и нервов.
- Свищ. Образуется на поздних стадиях раневого процесса, в случаях, когда на поверхности рана закрывается грануляциями, а в глубине сохраняется очаг инфекции.
- Тромбофлебит. Развивается через 1-2 мес. после повреждения. Является опасным осложнением, обусловлен инфицированием тромба с последующим распространением инфекции по стенке вены.
- Лимфангит и лимфаденит. Возникают вследствие других раневых осложнений, исчезают после адекватной санации основного гнойного очага.
Симптомы раневой инфекции
Как правило, патология развивается спустя 3-7 дней с момента ранения. К числу общих признаков относится повышение температуры тела, учащение пульса, ознобы и признаки общей интоксикации (слабость, разбитость, головная боль, тошнота). В числе местных признаков – пять классических симптомов, которые были описаны еще во времена Древнего Рима врачом Аулусом Корнелиусом Сельсусом: боль (dolor), местное повышение температуры (calor), местное покраснение (rubor), отек, припухлость (tumor) и нарушение функции (functio laesa).
Характерной особенностью болей является их распирающий, пульсирующий характер. Края раны отечны, гиперемированы, в полости раны иногда имеются фибринозно-гнойные сгустки. Пальпация пораженной области болезненна. В остальном симптоматика может варьироваться в зависимости от формы раневой инфекции. При околораневом абсцессе отделяемое из раны нередко незначительное, наблюдается выраженная гиперемия краев раны, резкое напряжение тканей и увеличение окружности конечности. Образование абсцесса сопровождается снижением аппетита и гектической лихорадкой.
При раневых флегмонах выявляется существенное повышение местной температуры и резкое ухудшение состояния больного, однако рана выглядит относительно благополучно. Формирование гнойного затека также сопровождается значительным ухудшением состояния пациента при относительном благополучии в области раны. Температура повышается до 40 градусов и более, отмечаются ознобы, вялость, адинамия и снижение аппетита. Гнойное отделяемое отсутствует или незначительное, гной выделяется только при надавливании на окружающие ткани, иногда – удаленные от основного очага инфекции. При свищах общее состояние остается удовлетворительным или близким к удовлетворительному, на коже формируется свищевой ход, по которому оттекает гнойное отделяемое.
Осложнения
Осложнения обусловлены распространением инфекции. При гнойных тромбофлебитах общее состояние ухудшается, в зоне поражения определяются умеренные признаки воспаления, при расплавлении стенки вены возможно формирование флегмоны или абсцесса. Лимфангит и лимфаденит проявляются болезненностью, отечностью мягких тканей и гиперемией кожи в проекции лимфатических узлов и по ходу лимфатических сосудов. Отмечается ухудшение общего состояния, ознобы, гипертермия и повышенное потоотделение. При сепсисе состояние тяжелое, кожа бледная, наблюдается снижение АД, выраженная тахикардия, бессонница и нарастающая анемия.
Лечение раневой инфекции
Лечение заключается в широком вскрытии и дренировании гнойных очагов, а также промывании раны антисептиками. В последующем при перевязках используются сорбенты и протеолитические ферменты. В фазе регенерации основное внимание уделяется стимуляции иммунитета и защите нежных грануляций от случайного повреждения. В фазе эпителизации и рубцевания при больших, длительно незаживающих ранах выполняют кожную пластику.
Прогноз и профилактика
Прогноз определяется тяжестью патологии. При небольших ранах исход благоприятный, наблюдается полное заживление. При обширных глубоких ранах, развитии осложнений требуется длительное лечение, в ряде случаев возникает угроза для жизни. Профилактика раневой инфекции включает в себя раннее наложение асептической повязки и строгое соблюдение правил асептики и антисептики в ходе операций и перевязок. Необходима тщательная санация раневой полости с иссечением нежизнеспособных тканей, адекватным промыванием и дренированием. Пациентам назначают антибиотики, проводят борьбу с шоком, алиментарными нарушениями и белково-электролитными сдвигами.

Сотрудники Центра ран и раневых инфекций проводят приоритетные научные исследования в области диагностики и лечения пациентов с тяжёлой гнойной инфекцией, в том числе на фоне сахарного диабета. Цель научного поиска - снижение смертности и инвалидизации пациентов, уменьшение риска развития рецидивов воспалительного процесса.
Так, разработанные здесь активная хирургическая тактика, уникальные методики операций и интенсивной терапии позволяют достигать высоких результатов в лечении сепсиса, анаэробной инфекции, обширных гнойных ран, посттравматического и гематогенного остеомиелита, трофических язв, гнойно-некротических форм диабетической стопы, различных послеоперационных гнойных осложнений, несформированных кишечных свищей и т.д.


В результате проведённых научных исследований специалисты Центра ран и раневых инфекций установили оптимальные сроки, последовательность и комбинации хирургических операций у больных трофическими язвами голени, которые вызваны заболеваниями вен. Также они разработали технику эндоскопической диссекции перфорантных вен голени у больных с обширными трофическими язвами голени, доказав её эффективность.
Важное направление научных исследований и клинической деятельности специалистов Центра - комплексное хирургическое лечение (в том числе с использованием эндоваскулярных вмешательств) больных с гнойно-некротическими формами синдрома диабетической стопы для сохранения конечности при критической ишемии.
Совместно с коллегами из отделения торакальной хирургии Института им.Вишневского специалисты Центра ран и раневых инфекций разрабатывают методы лечения хронического остеомиелита грудины и рёбер. Институт занимает лидирующие позиции в Российской Федерации по данному направлению хирургии.
Разработки Центра ран и раневых инфекций успешно используются при оказании помощи пострадавшим при чрезвычайных ситуациях.
Внутрибольничные инфекции – различные инфекционные заболевания, заражение которыми произошло в условиях лечебного учреждения. В зависимости от степени распространения различают генерализованные (бактериемию, септицемию, септикопиемию, бактериальный шок) и локализованные формы внутрибольничных инфекций (с поражением кожи и подкожной клетчатки, дыхательной, сердечно-сосудистой, урогенитальной системы, костей и суставов, ЦНС и т. д.). Выявление возбудителей внутрибольничных инфекций проводится с помощью методов лабораторной диагностики (микроскопических, микробиологических, серологических, молекулярно-биологических). При лечении внутрибольничных инфекций используются антибиотики, антисептики, иммуностимуляторы, физиотерапия, экстракорпоральная гемокоррекция и т. д.

Общие сведения
Внутрибольничные (госпитальные, нозокомиальные) инфекции - инфекционные заболевания различной этиологии, возникшие у пациента или медицинского сотрудника в связи с пребыванием в лечебно-профилактическом учреждении. Инфекция считается внутрибольничной, если она развилась не ранее 48 часов после поступления больного в стационар. Распространенность внутрибольничных инфекций (ВБИ) в медицинских учреждениях различного профиля составляет 5-12%. Наибольший удельный вес внутрибольничных инфекций приходится на акушерские и хирургические стационары (отделения реанимации, абдоминальной хирургии, травматологии, ожоговой травмы, урологии, гинекологии, отоларингологии, стоматологии, онкологии и др.). Внутрибольничные инфекции представляют собой большую медико-социальную проблему, поскольку утяжеляют течение основного заболевания, увеличивают длительность лечения в 1,5 раза, а количество летальных исходов - в 5 раз.

Этиология и эпидемиология внутрибольничных инфекций
Основными возбудителями внутрибольничных инфекций (85% от общего числа) выступают условно-патогенные микроорганизмы: грамположительные кокки (эпидермальный и золотистый стафилококк, бета-гемолитический стрептококк, пневмококк, энтерококк) и грамотрицательные палочковидные бактерии (клебсиеллы, эшерихии, энтеробактер, протей, псевдомонады и др.). Кроме этого, в этиологии внутрибольничных инфекций велика удельная роль вирусных возбудителей простого герпеса, аденовирусной инфекции, гриппа, парагриппа, цитомегалии, вирусных гепатитов, респираторно-синцитиальной инфекции, а также риновирусов, ротавирусов, энтеровирусов и пр. Также внутрибольничные инфекции могут быть вызваны условно-патогенными и патогенными грибами (дрожжеподобными, плесневыми, лучистыми). Особенностью внутригоспитальных штаммов условно-патогенных микроорганизмов служит их высокая изменчивость, лекарственная резистентность и устойчивость к воздействию факторов среды (ультрафиолета, дезинфектантов и пр.).
Источниками внутрибольничных инфекций в большинстве случаев выступают пациенты или медицинский персонал, являющиеся бактерионосителями или больными стертыми и манифестными формами патологии. Как показывают исследования, роль третьих лиц (в частности, посетителей стационаров) в распространении ВБИ невелика. Передача различных форм госпитальной инфекции реализуется с помощью воздушно-капельного, фекально-орального, контактного, трансмиссивного механизма. Кроме этого, возможен парентеральный путь передачи внутрибольничной инфекции при проведении различных инвазивных медицинских манипуляций: забора крови, инъекций, вакцинации, инструментальных манипуляций, операций, ИВЛ, гемодиализа и пр. Таким образом в медучреждении возможно заразиться гепатитами В, С и D, гнойно-воспалительными заболеваниями, сифилисом, ВИЧ-инфекцией. Известны случаи внутрибольничных вспышек легионеллеза при приеме больными лечебного душа и вихревых ванн.
Факторами, участвующими в распространении внутрибольничной инфекции, могут выступать контаминированные предметы ухода и обстановки, медицинский инструментарий и аппаратура, растворы для инфузионной терапии, спецодежда и руки медперсонала, изделия медицинского назначения многоразового использования (зонды, катетеры, эндоскопы), питьевая вода, постельные принадлежности, шовный и перевязочный материал и мн. др.
Значимость тех или иных видов внутрибольничной инфекции во многом зависит от профиля лечебного учреждения. Так, в ожоговых отделениях преобладает синегнойная инфекция, которая в основном передается через предметы ухода и руки персонала, а главным источником внутрибольничной инфекции являются сами пациенты. В учреждениях родовспоможения основную проблему представляет стафилококковая инфекция, распространяемая медицинским персоналом-носителем золотистого стафилококка. В урологических отделениях доминирует инфекция, вызываемая грамотрицательной флорой: кишечной, синегнойной палочкой и др. В педиатрических стационарах особую значимость имеет проблема распространения детских инфекций – ветряной оспы, эпидемического паротита, краснухи, кори. Возникновению и распространению внутрибольничной инфекции способствуют нарушение санитарно-эпидемиологического режима ЛПУ (несоблюдение личной гигиены, асептики и антисептики, режима дезинфекции и стерилизации, несвоевременное выявление и изоляция лиц-источников инфекции и т. д.).
К группе риска, в наибольшей степени подверженной развитию внутрибольничной инфекции, относятся новорожденные (особенно недоношенные) и дети раннего возраста; пожилые и ослабленные пациенты; лица, страдающие хроническими заболеваниями (сахарным диабетом, болезнями крови, почечной недостаточностью), иммунодефицитом, онкопатологией. Восприимчивость человека к внутрибольничным инфекциям увеличивается при наличии у него открытых ран, полостных дренажей, внутрисосудистых и мочевых катетеров, трахеостомы и других инвазивных устройств. На частоту возникновения и тяжесть течения внутрибольничной инфекции влияет долгое нахождение пациента в стационаре, длительная антибиотикотерапия, иммуносупрессивная терапия.
Классификация внутрибольничных инфекций
По длительности течения внутрибольничные инфекции делятся на острые, подострые и хронические; по тяжести клинических проявлений – на легкие, среднетяжелые и тяжелые формы. В зависимости от степени распространенности инфекционного процесса различают генерализованные и локализованные формы внутрибольничной инфекции. Генерализованные инфекции представлены бактериемией, септицемией, бактериальным шоком. В свою очередь, среди локализованных форм выделяют:
- инфекции кожи, слизистых и подкожной клетчатки, в т. ч. послеоперационных, ожоговых, травматических ран. В частности, к их числу относятся омфалит, абсцессы и флегмоны, пиодермия, рожа, мастит, парапроктит, грибковые инфекции кожи и др.
- инфекции полости рта (стоматит) и ЛОР-органов (ангина, фарингит, ларингит, эпиглоттит, ринит, синусит, отит, мастоидит)
- инфекции бронхолегочной системы (бронхит, пневмония, плеврит, абсцесс легкого, гангрена легкого, эмпиема плевры, медиастинит)
- инфекции пищеварительной системы (гастрит, энтерит, колит, вирусные гепатиты)
- глазные инфекции (блефарит, конъюнктивит, кератит)
- инфекции урогенитального тракта (бактериурия, уретрит, цистит, пиелонефрит, эндометрит, аднексит)
- инфекции костно-суставной системы (бурсит, артрит, остеомиелит)
- инфекции сердца и сосудов (перикардит, миокардит, эндокардит, тромбофлебиты).
- инфекции ЦНС (абсцесс мозга, менингит, миелит и др.).
Диагностика внутрибольничных инфекций
Критериями, позволяющими думать о развитии внутрибольничной инфекции, служат: возникновение клинических признаков заболевания не ранее чем через 48 часов после поступления в стационар; связь с проведением инвазивного вмешательства; установление источника инфекции и фактора передачи. Окончательное суждение о характере инфекционного процесса получают после идентификации штамма возбудителя с помощью лабораторных методов диагностики.
Для исключения или подтверждения бактериемии проводится бактериологический посев крови на стерильность, желательно не менее 2-3-х раз. При локализованных формах внутрибольничной инфекции микробиологическое выделение возбудителя может быть произведено из других биологических сред, в связи с чем выполняется посев мочи, кала, мокроты, отделяемого ран, материала из зева, мазка с конъюнктивы, из половых путей на микрофлору. Дополнительно к культуральному методу выявления возбудителей внутрибольничных инфекций используются микроскопия, серологические реакции (РСК, РА, ИФА, РИА), вирусологический, молекулярно-биологический (ПЦР) методы.
Лечение внутрибольничных инфекций
Сложности лечения внутрибольничной инфекции обусловлены ее развитием в ослабленном организме, на фоне основной патологии, а также резистентностью госпитальных штаммов к традиционной фармакотерапии. Больные с диагностированными инфекционными процессами подлежат изоляции; в отделении проводится тщательная текущая и заключительная дезинфекция. Выбор противомикробного препарата основывается на особенностях антибиотикограммы: при внутрибольничной инфекции, вызванной грамположительной флорой наиболее эффективен ванкомицин; грамотрицательными микроорганизмами – карбапенемы, цефалоспорины IV поколения, аминогликозиды. Возможно дополнительное применение специфических бактериофагов, иммуностимуляторов, интерферона, лейкоцитарной массы, витаминотерапии.
При необходимости проводится чрескожное облучение крови (ВЛОК, УФОК), экстракорпоральная гемокоррекция (гемосорбция, лимфосорбция). Симптоматическая терапия осуществляется с учетом клинической формы внутрибольничной инфекции с участием специалистов соответствующего профиля: хирургов, травматологов, пульмонологов, урологов, гинекологов и др.
Профилактика внутрибольничных инфекций
Основные меры профилактики внутрибольничных инфекций сводятся к соблюдению санитарно-гигиенических и противоэпидемических требований. В первую очередь, это касается режима дезинфекции помещений и предметов ухода, применения современных высокоэффективных антисептиков, проведения качественной предстерилизационной обработки и стерилизации инструментария, безукоснительного следования правилам асептики и антисептики.
Медицинский персонал должен соблюдать меры индивидуальной защиты при проведении инвазивных процедур: работать в резиновых перчатках, защитных очках и маске; осторожно обращаться с медицинским инструментарием. Большое значение в профилактике внутрибольничных инфекций имеет вакцинация медработников от гепатита В, краснухи, гриппа, дифтерии, столбняка и других инфекций. Все сотрудники ЛПУ подлежат регулярному плановому диспансерному обследованию, направленному на выявление носительства патогенов. Предупредить возникновение и распространение внутрибольничных инфекций позволит сокращение сроков госпитализации пациентов, рациональная антибиотикотерапия, обоснованность проведения инвазивных диагностических и лечебных процедур, эпидемиологический контроль в ЛПУ.

Под термином "антибактериальная химиотерапия" понимают использование химических соединений, назначаемых при инфекционных заболеваниях и вызывающих гибель их возбудителей без повреждения тканей хозяина.
К сожалению, многие из препаратов, разработанных в 40-60 годах, в настоящее время во многом утратили свою клиническую значимость, что обусловлено эволюцией микроорганизмов, возникновением их устойчивости к действию антибиотиков.
Этот биологический феномен - антибиотикорезистентность - определяет как тактику терапии и направления деятельности фармацевтической промышленности, вынужденной производить все новые антибактериальные препараты, так и направления научных исследований по поиску новых групп препаратов, более эффективных для лечения раневой инфекции.
Раневая инфекция в общей структуре хирургической заболеваемости занимает одно из ведущих мест.
Гнойно-воспалительные процессы наблюдаются у 35% – 45% хирургических больных. Инфекция является причиной не только различных хирургических заболеваний, но и многочисленных послеоперационных осложнений: от нагноения послеоперационной раны до развития хирургического сепсиса, который часто приводит к смерти больного.
Причины возрастания частоты и течения гнойной инфекции в хирургии многообразны и включают в себя следующие факторы: увеличение объема оперативных вмешательств, особенно у больных группы риска, широкое использование методов инструментального обследования и лечения, сопровождающееся инфицированием больного (внутрисосудистые и мочевые катетеры, интубационные трубки, эндоскопические манипуляции и др.), распространение антибиотикоустойчивых штаммов микроорганизмов. Указанные факторы, а также нерациональное использование антибиотиков привели к увеличению частоты внутрибольничных инфекций, вызываемых множественно устойчивыми условно-патогенными возбудителями.
Более половины всех используемых в настоящее время в мире антибиотиков составляют беталактамы (пенициллины, цефалоспорины, цефамицины, карбапенемы, монобактамы).
Данные бактериологических исследований, проведенных в различных клиниках, свидетельствуют о приобретении патогенными микроорганизмами устойчивости к длительно применяемым в практике антибактериальным препаратам (пенициллин, стрептомицин, ампициллин, амоксициллин, цефазолин и др.).
Наиболее значимым механизмом формирования резистентности к беталактамным антибиотикам является продукция бактериями беталактамаз – с ним связано приблизительно 80% случаев устойчивости как грамположительных, так и грамотрицательных микроорганизмов, что является одной из основных причин снижающейся эффективности многих традиционных для каждого стационара антибактериальных препаратов.
Одним из путей преодоления антибиотикорезистентности является использование ингибиторов беталактамаз в сочетании с пенициллинами или цефалоспоринами в составе комбинированных препаратов. На основе ингибитора беталактамаз клавулановой кислоты создан комбинированный препарат амоксициллин/клавуланат калия, на основе ингибитора беталактамаз сульбактама созданы комбинированные препараты тикарциллин/клавулановая кислота, ампициллин/сульбактам, цефоперазон/сульбактам, на основе ингибитора беталактамаз тазобактама – пиперациллин/тазобактам.
Изучение возбудителей тяжелых хирургических гнойных осложнений и их чувствительности к антибактериальным препаратам позволяет считать наиболее эффективными лекарственными средствами:
- аминогликозиды 3 поколения (нетилмицин, амикацин, сизомицин),
- цефалоспорины III-IY поколения,
- фторхинолоны,
- линкозамины,
- имипенем, меропенем,
- антибиотики в комбинации с ингибиторами беталактамаз (ампициллин и цефоперазон с сульбактамом, амоксициллин с клавулановой кислотой, пиперациллин с тазобактамом).
При выявлении метициллинрезистентных микроорганизмов – ванкомицин, тейкапланин. Достаточно высокую клиническую значимость сохраняют давно известные антимикробные препараты – диоксидин и фурагин-растворимый.
Выбор антибактериального препарата должен быть обоснован не только данными бактериологического исследования, но и тяжестью проявления клиники интоксикации, степенью выраженности полиорганной недостаточности, обширностью гнойного процесса.
При ограниченном гнойном процессе, отсутствии клинико-лабораторных признаков интоксикации предпочтение должно отдаваться пероральным формам препаратов.
При установлении осложненного течения раневой инфекции с вовлечением внутренних органов антибактериальная терапия должна базироваться только на инъекционных формах. в этих случаях все антибиотики должны вводиться только через катетеры, установленные в центральные вены или в артерии, при наличии гнойного процесса на нижних конечностях.
Современная антибактериальная терапия раневой инфекции базируется на обязательности адекватного хирургического лечения гнойного очага, дополненного новыми антибактериальными препаратами, назначаемыми рациональным путем и в адекватных дозах, ориентируясь на тяжесть раневого процесса при регулярном контроле состава микрофлоры в ранах и контроля переносимости проводимой терапии.
В экстренных случаях, при отсутствии возможности выполнения бактериологических исследований, иногда допускается использование антибактериальных препаратов, перечисленных в программах эмпирической и этиотропной антибактериальной терапии больных с раневой инфекцией (рис. 30).
ИСТОРИЯ РАЗВИТИЯ АНТИБАКТЕРИАЛЬНОЙ ХИМИОТЕРАПИИ
В развитии химиотерапии можно проследить три периода: до работ П. Эрлиха (до 1891 г.), период исследований П. Эрлиха и после 1935 г., когда были открыты сульфаниламиды и антибиотики.
Непреходящее и сегодня значение сохраняют тезисы Эрлиха, сформулированные на основе опыта и логики поисковой работы: "Химиотерапия ставит себе задачу найти такие вещества, которые при большом влиянии на паразитов принесли бы возможно менее вреда организму".
Важнейшие для медицинской практики антибиотики ХХ века были открыты или случайно (пенициллин), или путем так называемого направленного скрининга.
Продукты жизнедеятельности грибов и микроорганизмов (Penicillium, Streptomyces, Bacillus, а также высших грибов), обладающие способностью убивать возбудителей болезни, обозначают в узком смысле как антибиотики.
"Глядя на зараженные раны, на людей, которые мучились и умирали, я сгорал от желания найти какое-нибудь средство, которое способно убить микробы" (Флеминг А., 1881-1995 гг.).
Сегодня каждый прохожий молча, почтительно склонит голову, прочитав на могильном памятнике "Сэр Александр Флеминг - изобретатель пенициллина".
Народ нашей страны всегда будет благодарен З.В. Ермольевой - создателю отечественного пенициллина, спасшего тысячи жизней раненых в годы Великой отечественной войны.
В 1943 г. Фармакологический комитет по докладу З.В. Ермольевой принимает решение о медицинском применении отечественного пенициллина. С этой даты началась эра антибиотиков в нашей стране. З.В. Ермольева, Н.И. Гращенков, И.Г. Руфанов проводят в течение двух месяцев детальное изучение эффективности пенициллина при лечении более чем 1200 раненых (эвакогоспиталь № 5004).
1943 г. - лечение и схемы применения первого отечественного пенициллина на 25 "безнадежных" и впоследствии выздоровевших септических больных проводила врач-хирург Анна Марковна Маршак.
"Боевое крещение" отечественный пенициллин получил на 1-ом Прибалтийском фронте под руководством главного хирурга Армии Н.Н. Бурденко.
Ученик З.В.Ермольевой - С.М.Навашин, академик РАМН, профессор, лауреат Государственной премии, директор Государственного центра по антибиотикам, продолжил основные направления ее фундаментальные исследования в комплексной науке об антибиотиках с начала 50-х годов.
Под руководством С.М.Навашина за 50-летний период в ГНЦА были разработаны антибактериальные препараты практически всех групп:
- природные, пролонгированные и полусинтетические пенициллины,
- природные и полусинтетические аминогликозиды,
- полусинтетические цефалоспорины,
- тетрациклины,
- макролиды,
- резервные противотуберкулезные антибиотики,
- рифампицин и его производные,
- линкомицин,
- фузидин,
- противоопухолевые антибиотики,
- полимиксины,
- липосомальные формы антибиотиков.
Разработана отечественная технология важнейших фторхинолонов 1 поколения.
Уже в 70-е годы отечественная промышленность антибиотиков занимала второе место в мире, как по объему, так и по номенклатуре выпускаемых препаратов. В таблице на рис.1 приведена классификация антибактериальных средств.
"Золотая эра" антибиотикотерапии ознаменовалась выдающимися достижениями во всех областях медицины – снижением распространения инфекций, тяжести их течения и снижением показателя смертности при инфекционных заболеваниях. Ушли в прошлое представления о неизлечимости многих инфекционных заболеваний (сепсис, туберкулез, эндокардит, многих особо опасных инфекций и др.). Об эффективности антибиотикотерапии можно судить, например, по показателям смертности при пневмонии: до 40-х годов – 30-40%, после внедрения пенициллина - 5% (С.М. Навашин, 1997 г.).
ПРОТИВОГРИБКОВЫЕ ПРЕПАРАТЫ
Больные с раневой инфекцией, получающие длительную антибактериальную терапию сразу несколькими препаратами, являются группой высокого риска поражения микотическими инфекциями. Летальность при инвазивных микозах, вызванных, например, грибами рода Candida, достигает 85%. Кандидоз, являясь эндогенной инфекцией, может проявляться клиникой поражения грибами мозга, печени, селезенки, почек, сердца, легких, суставов. Для лечения в арсенале врача имеется только пять эффективных противогрибковых препаратов: амфотерицин В, флуконазол, итраконазол, флюцитозин и липосомальный амфотерицин В.
Наибольшее распространение в клиниках получили первые два – амфотерицин В и флуконазол. Вместе с тем, несмотря на высокую клиническую эффективность к амфотерицину В, при лечении кандидемии этот препарат используется значительно реже из-за его токсического воздействия на почки. Липосомальный амфотерицин В менее токсичен, более удобен в использовании, так как его можно вводить через периферические вены. Флуконазол считается препаратом выбора при кандидемии, раневой инфекции, перитоните, инфекции мочевыводящих путей
ЭУБИОТИКИ ДЛЯ ПРОФИЛАКТИКИ ДИСБАКТЕРИОЗА У БОЛЬНЫХ С РАНЕВОЙ ИНФЕКЦИЕЙ
Длительная антибактериальная терапия, лучевая терапия, гормоно- и химиотерапия неизбежно приводят к значительным качественным и количественным изменениям в составе нормальной микрофлоры человека. Для профилактики эндогенной инфекции у тяжелых больных применяется селективная деконтаминация пищеварительного тракта. Используется пероральное или интрагастральное введение антибиотиков, не всасывающихся в кишечнике. При раневой инфекции, если позволяет клиническая ситуация, предпочтение отдается химиотерапевтическим препаратам для местного применения. В профилактике и лечении дисбактериозов при раневой инфекции в настоящее время упор делается на применение бактериальных биологических препаратов из нормальной микрофлоры, т.е. применение эубиотиков, изготовляемых на основе бифидумбактерий, лактобацилл, кишечной палочки, споровых форм бактерий. Последними исследованиями установлена высокая эффективность биопрепарата "Бифилиз" (сочетание лизоцима и бифидумбактерина).
Для сохранения нормальной экологии кишечника необходимо включение в комплексное лечение пробиотиков.
- монокомпонентных (бифидумбактерин, лактобактерин, колибактерин, споробактерин, бактиспорин, бактисубтил и др.);
- поликомпонентных (бифилонг, ацилакт, ацинол, линекс, биоспорин);
- комбинированных (бифидумбактерин форте, бифилиз).
ПУТИ ВВЕДЕНИЯ АНТИБИОТИКА
Эффективность действия антибиотика зависит от создания высокой его концентрации в очаге поражения, что достигается назначением соответствующей дозы препарата и введением его оптимальным путем.
При местном характере гнойной инфекции с целью купирования острого гнойного процесса достаточно использование одного антибактериального препарата с обязательным местным лечением гнойной раны под повязками с мазями на полиэтиленгликолевой основе, обладающими широким спектром антимикробной активности, или современными йодофорами, диоксидином, усиливающими антимикробное действие препаратов, назначенных для общей антибактериальной терапии.
При обширных гнойных очагах, сепсисе необходимо повышать дозы антибиотиков до максимальных, с учетом видового состава микрофлоры, выделенной из разных биологических сред. Целесообразно использовать комбинации 2-3 препаратов. Препараты необходимо вводить через катетеры, установленные в центральные вены, что позволяет при лечении генерализованных форм создать и длительно поддерживать на нужном уровне концентрацию антибиотика не только в очаге поражения, но и во всем организме больного.
При локализации гнойного очага на нижних конечностях эффективно внутриартериальное введение препаратов в нижнюю надчревную артерию методом круглосуточной инфузии с помощью перфузоров.
Длительная внутриартериальная инфузия позволяет создавать и поддерживать достаточно высокую концентрацию препаратов в тканях поврежденной конечности, оставляя при этом концентрацию антибиотиков в общем кровотоке на более низком уровне. Это способствует повышению эффективности антибактериальной терапии и уменьшает возможность общего токсического воздействия антибиотиков.
КОНТРОЛЬ ЛЕКАРСТВЕННОЙ ПЕРЕНОСИМОСТИ ПРИ ДЛИТЕЛЬНОЙ ОБШЕЙ И МЕСТНОЙ АНТИМИКРОБНОЙ ТЕРАПИИ РАНЕВОЙ ИНФЕКЦИИ
Чрезмерное, часто неконтролируемое увлечение каким-нибудь одним препаратом, несоблюдение правила чередования лекарственных средств с учетом стадии течения раневого процесса или назначение одномоментно нескольких лекарственных форм, содержащих одинаковый антимикробный компонент, могут привести к сенсибилизации организма с последующим развитием местной или общей аллергической реакции, иногда с проявлениями токсического поражения внутренних органов. Для своевременной диагностики развивающейся реакции целесообразно внедрение в практику медикаментозного теста "In vitro" индекс лекарственной чувствительности (ИЛЧ) по Демьяненко С.М. (1989 г.).
При хорошей переносимости различных препаратов ИЛЧ составляет 0,96 - 1,0, а в группе с развивающейся аллергической реакцией на какой-нибудь препарат, входящий в комплексное лечение, этот показатель находится на уровне 0,76 - 0,83.
Регулярная постановка данного теста в группе больных с длительной терапией или при многокомпонентной терапии позволяет своевременно диагностировать процесс формирования замедленной аллергической реакции, уточнить истинный причинный препарат (анестетики, растворители препаратов, витамины, белковые препараты, сосудистые препараты и др.) и в ряде случаев избежать ошибочной отмены антибактериального препарата.
ПРОДОЛЖИТЕЛЬНОСТЬ АНТИБАКТЕРИАЛЬНОЙ ТЕРАПИИ
При местном гнойном процессе достаточно введение антибиотика в течение 3-5 суток. Более длительная терапия проводится в группах больных с острыми гнойными заболеваниями мягких тканей, с генерализацией инфекционного процесса. Критерием необходимости продолжения терапии или отмены препаратов должны служить данные бактериологического контроля, а также динамика клинических показателей.
Основными критериями отмены терапии являются исчезновение патогенной микрофлоры из гнойного очага или снижение количества микробов в 1 г ткани раны, отчетливая положительная динамика клинико-лабораторных показателей раневого процесса, нормализация температуры, улучшение общего состояния больного и т.д.
Ранняя отмена антибактериальной терапии до достижения стойкого клинического эффекта может привести к рецидиву или затяжному течению заболевания и значительно осложнить дальнейшее лечение.
СТУПЕНЧАТАЯ АНТИБАКТЕРИАЛЬНАЯ ТЕРАПИЯ РАНЕВОЙ ИНФЕКЦИИ
В настоящее время антибиотики выпускаются в лекарственных формах, предназначенных как для парентерального введения, так и для приема внутрь (например, офлоксацин, ципрофлоксацин, пефлоксацин и др.)
Наличие двух лекарственных форм одного и того же препарата позволяет последовательно использовать их (сначала парентерально, а затем внутрь). Ориентируясь на динамику клинических признаков раневого процесса, можно сократить сроки введения препарата парентерально и перейти на прием внутрь, что значительно сокращает общие затраты на лечение (расходные материалы, трудозатраты медперсонала), улучшает комфортность лечения, сокращает сроки пребывания больного в стационаре.
Что такое открытая рана? Причины возникновения, диагностику и методы лечения разберем в статье доктора Николенко Виталия Александровича, травматолога со стажем в 12 лет.
Над статьей доктора Николенко Виталия Александровича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Раной называют повреждение кожных покровов или слизистых оболочек, вызванное внешним воздействием механических сил.
Исходя из приведённого определения, причиной раны, как нозологической формы, может являться исключительно травмирующий агент.

Природа раны всегда экзогенная (возникает под воздействием внешних факторов). Даже если речь идёт о травматизации мягких тканей изнутри костями или разрыве кожи от перенапряжения — всё же изначальной причиной поврежения является приложенная извне сила, которая превысила предел прочности тканей и привела к ране косвенным путём. [1]
В большинстве случаев рана — результат прямого нарушения целостности покровной ткани тем или иным ранящим объектом. Характер раны, тактика лечения, вероятные осложнения и её клинический исход напрямую зависят от изначального воздействия и свойств ранящего объекта (преимущественно его геометрии и силе соударения). [2]
Как отдельные варианты ранения рассматриваются размозжение тканей и травматические отслойки тканей в результате тупой травмы тела. Последний вариант отличается обширной зоной деструкции и дополнительными факторами, отягощающими раневой процесс в отсроченном периоде. [3]
Огнестрельные раны также рассматриваются обособленно в силу особого подхода в лечении. Ранящий источник в этом случае, обладая значительной кинетической энергией, образует вокруг раны область контузии тканей. [4]
Тяжесть раневого процесса определяется способом воздействия. В настоящее время достаточно изучен профиль осложнений, характерный для каждого вида раны. Наглядным примером комплексного раневого процесса, приводящего к общему заболеванию, служит глубокая колотая рана, осложнившаяся клостридиальной инфекцией. [5]
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы открытой раны
Первым и патогномоничным симптомом, характерным для раны, является нарушение целостности кожных покровов или слизистой оболочки. Другими неотъемлемыми клиническими признаками являются:
- диастаз краёв повреждённых тканей;
- кровотечение из зоны повреждения;
- боль и функциональные расстройства.
Перечисленная тетрада, четко и академично характеризует рану. [6]
Под диастазом понимают расхождение краёв раны, неизменно возникающее при любом ранении в той или иной степени выраженности. Даже резаная рана с гладкими краями имеет диастаз, в том числе при макроскопически адаптированных краях раны.
Кровотечение из раны присутствует всегда, за исключением редких случаев коагулопатии (нарушений свёртываемости крови). [7] Собственно кровотечение может нести раннюю и непосредственную угрозу жизни. Оно явным образом даёт понять, что человек имеет дело именно с раной. Капиллярное, венозное, артериальное или смешанное кровотечение — компонент, присущий любой ране.
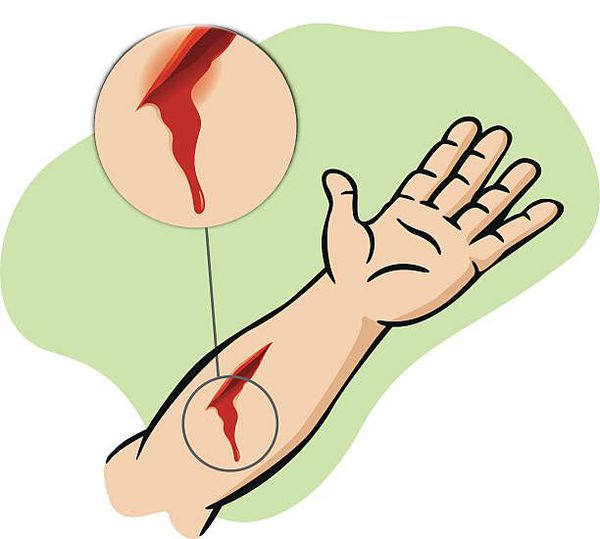
Боль — специфичный вариабельный признак раны. Его вариабельность обусловлена не только характером и локализацией раны, но и общим состоянием организма, индивидуальной лабильностью и уровнем болевого порога.
Диагноз можно установить при одновременном сочетании всех перечисленных выше симптомов, однако это не ограничивает спектр всех проявлений раны. Диагностирование раны не представляет особой сложности ввиду внешних очевидных признаков травмы. Кроме того, при осмотре обращает на себя внимание выраженное нарушение функции, которое следует рассматривать как симптомокомплекс. [8]
Нарушение функции проявляет себя неспецифически, то есть может быть присуще не только последствиям ранения, но и сочетанных повреждений.
Функциональные расстройства, связанные с раной, стоит разделить на локальные и системные — это упрощает диагностику и поясняет природу симптоматики раны.
- К локальным нарушениям функции относят последствия острой воспалительной и посттравматической реакций, которые характерны для отёка. [9]
- К системным функциональным расстройствам относят общие реакции организма (например, лихорадку).
Под нарушением функции в симптоматике раны, как правило, понимают не дисфункцию на тканевом уровне с патогенетическими сдвигами, а глобальные проявления анатомического характера: нарушение подвижности в сегменте, вплоть до утери опороспособности и объёма движений. [10]
Патогенез открытой раны
Патогенез ранений детально изучен. На его основе строится лечение ран. Неизменность патогенетических звеньев при ранении позволяет говорить о раневом процессе и его течении как об общем комплексе типичных проявлений, характерных для любой раны, независимо от её морфологии.
Существуют различные класификации терминологий и длительности фаз, однако классификация Росса заслужила признание повсеместно. Согласно ей, выделяют три фазы раневого процесса:
- воспалительная фаза;
- пролиферативная фаза;
- реорганизационная фаза. [11]
Воспалительная фаза
В первой фазе происходит острая сосудистая реакция, характеризующаяся:
- вазоспазмом (сужением артерий и капилляров) с целью локального гемостаза (остановки кровотечения);
- выбросом гуморальных факторов свёртывания, катализаторов местных иммунных реакций.
Задача воспалительной фазы — мобилизовать силы организма с целью локализации процесса и подготовки к успешной репарации (восстановлению) в дальнейшем. [12]
Второй этап этой фазы состоит в элиминации (устранении) организмом поврежденных структур. Длительность перечисленных процессов — от трёх до пяти суток. После чего наступает следующая стадия раневого процесса.
Пролиферативная фаза
Как видно из названия, в этот период начинается восстановление повреждённых и замещение утраченных тканей.
Как правило, эта фаза протекает от нескольких суток до нескольких недель. Существует прямая зависимость от количества утраченной ткани при ранении. В основе пролиферативной фазы лежит преобладание процессов синтеза за счёт клеток-предшественников. [14]
Реорганизационная фаза
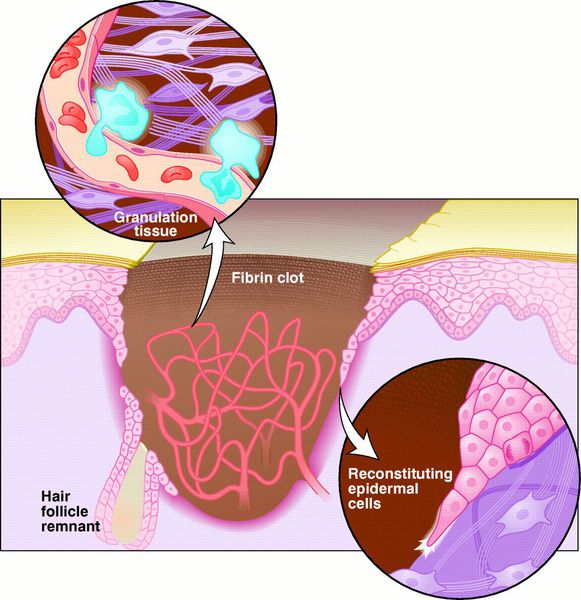
Заживление ран проходит по одному из трёх путей: первичным или вторичным натяжением, или под струпом. [19]
Первичное натяжение — самый благоприятный способ заживления. Для него, однако, требуются изначальные благоприятные условия: рана с минимальной микробной контаминацией, плотно соприкасающиеся края раны, отсутствие некротических тканей.
Вторичное натяжение — вариант заживления раны, противоположный описанного выше натяжения. Этот тип заживления характерен для инфицированных ран. [20]
Заживление под струпом — заживление, характерное для ран с большой площадью, но малой глубиной. При этом, протекает процесс, аналогичный заживлению первичным натяжением, но ориентированный в продольной плоскости. Кроме того, раневая поверхность покрывается струпом — слоем высохшей крови, тканевой жидкости и детрита. [21] Струп выполняет функцию биологической повязки до заживления и эпителизации раны.
Классификация и стадии развития открытой раны
Классификация ран обширна, в основном, за счёт обилия классифицируемых признаков.
В основную класификацию ран, радикально влияющую на способ их ведения, включают инфицированные и неинфицированные повреждения или, как их называют врачи, гнойные и чистые раны.
По способу и обстановке нанесения раны делятся на хирургические, случайные, умышленные и раны военного времени.
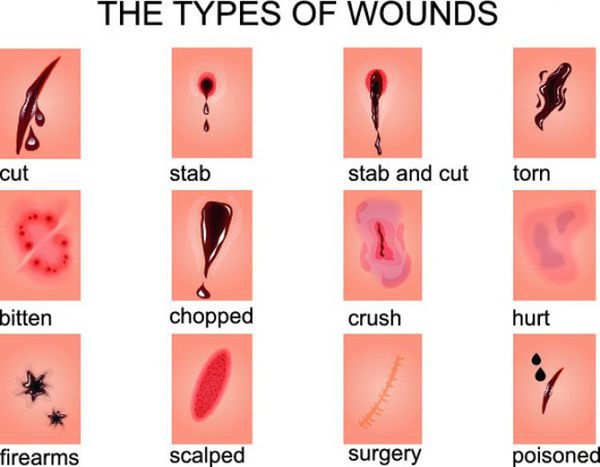
По характеру раневых ворот, что зависит от механизма нанесения раны:
- огнестрельные;
- размозженные;
- укушенные;
- резаные;
- ушибленные;
- колотые;
- рубленные;
- рваные;
- скальпированные;
- раздавленные. [16]
В классификациях по данному признаку встречаются раны смешанного характера (например, укушено-рваные или размозжено-рваные).
По обширности выделяют рану с малой зоной повреждения и обширную рану.
По количеству ран: одиночная и множественные раны. Эта классификация включает дополнительный критерий: множественные раны разделяются на сочетанные и комбинированные. [17]
По характеру раневого канала раны разделяются на слепые, сквозные, касательные, проникающие и непроникающие.
По наличию осложнений раны могут быть осложненными и неосложненными. Осложниться раны могут общими и местными процессами.
Независимо от характера раны, ей присуща клиническая стадийность, которая отражает аналогичную последовательность патогенеза.
Непосредственно после нанесения раны, возникает первичный рефлекторный спазм сосудов микроциркуляторного русла, как нейровегетативный ответ на травму. [18] Это короткий период, с характерным отсутствием кровотечения, несмотря на масштаб повреждения. После чего, развивается кровотечение.
Независимо от характера и интенсивности кровотечения, организм стремится к гемостазу сосудистым и гуморальным звеном. Если гемостаз наступил, и состояние после кровопотери стабилизировано — начинается репаративная фаза.
Осложнения открытой раны
Осложнения ран делятся на местные и общие. И те, и другие могут быть ранними и поздними, в зависимости от сроков развития.
Местные осложнения ран могут носить инфекционный и неинфекционный характер. Инфекционные местные осложнения — присоединение активного микробного заражения раны с клиническим проявлением воспалительной реакции. [22]
Инфицирование раны — бесспорное осложнение, замедляющее заживление раны, снижающее вероятность первичного заживления, приносящее риск генерализованных осложнений и ухудшающее отдалённый прогноз. [23]
Некроз — гибель тканей в зоне раны. Это вторичный процесс, развивающийся уже в отделённом времени после получения раны.
Как отдельный вид местных осложнений, рассматривают вторичное кровотечение, возникшее после изначально выполненного гемостаза раны. В случае выполненного хирургического лечения возможны осложнения раны другого характера — несостоятельность швов.
К неинфекционным местным осложнениям относят повреждение крупных нервов, магистральных сосудов, сухожилий. Это приводит к необходимости расширения объёмов оперативного пособия (и даёт абсолютные показания к нему), резко уменьшая шансы на восстановление функции сегмента. [25]
Общие или генерализованные осложнения раны опасны нарушениями жизненных функций организма. Общие осложнения ран могут стать фатальными для пациента.
Выделяют следующие неинфекционные осложнения общего характера:
- Геморрагический шок — декомпенсация витальных показателей организма, на фоне массивной кровопотери. Это раннее общее осложнение, которое встречается наиболее часто.
- Травматический шок — преобладание болевой импульсации, как ключевого компонента в нарушении гемостаза. Травматический шок включает в себя понятие массивной кровопотери, но связан с отягощением раны другой травмой либо множественными ранами. [26]
Общие осложнения инфекционной причины: сепсис, клостридиальная инфекция.
Осложнения местные и общие тесно связаны. Генерализация осложнений напрямую указывает на вероятную ошибку в подходах к лечению. Любой раневой процесс может генерализоваться даже при правильных тактических решениях врача. [16]
Диагностика открытой раны
Диагностика раны в своем большинстве — визуальна. Результатов осмотра достаточно, чтобы установить предварительный и, в большинстве случаев, полный диагноз. Нарушение целостности тканей, зияние краёв раны, кровотечение — критерии диагноза. [3]
Не стоит пренебрегать сбором жалоб пациента, уточнением деталей об обстоятельствах получения раны с целью моделирования механизма нанесения раны. Общеклинический план опроса пациента позволит дополнить диагноз сопутствующей патологией, важной для лечения раны.
В ряде случаев, определить повреждение подлежащих анатомических структур позволят клинические тесты. Оценка объёмов движений сегмента при ранении в проекции сухожилий, нагрузочные тесты выявляют полные или частичные повреждения, которые могут быть не визуализированы во время ревизии. [10]
Инструментальные методы диагностики раны направлены на исключение сопутствующего повреждения сосудов, нервов, внутренних органов. Рентген-визуализация выявляет рентгеноконтрастные инородные тела, что станет ценной информацией для хирурга перед операцией.
Лабораторный минимум — общий анализ крови, коагулограмма. Они позволят в кратчайшие сроки оценить объём кровопотери и проблемы с гемостазом.
Одним из немногих специфичных для раны лабораторных тестов является посев раневого содержимого на рост бактериальной флоры с определением чувствительности к антибиотикам.
Лечение открытой раны
Лечение ран бывает общим и местным, консервативным и оперативным.
Монотерапия (только общее или местное) раны не применятся, за редким исключением.
Показания к консервативному лечению — поверхностные и осаднённые раны, раны с адаптированными краями, отказ пациента от оперативного лечения, терминальное состояние пациента либо абсолютные противопоказания к выполнению наркоза или анестезии. [28] Условным показанием к консервативному лечению, является первичное инфицирование раны. В этом случае применимы отсроченные швы либо консервативное ведение.
Технически, лечение раны консервативным способом заключается в регулярных перевязках раны до заживления с целью минимизации риска инфекционных осложнений. Вопрос о хирургическом лечении в таком случае, может быть поставлен в ходе динамического наблюдения. [12]
Вакуум-терапия
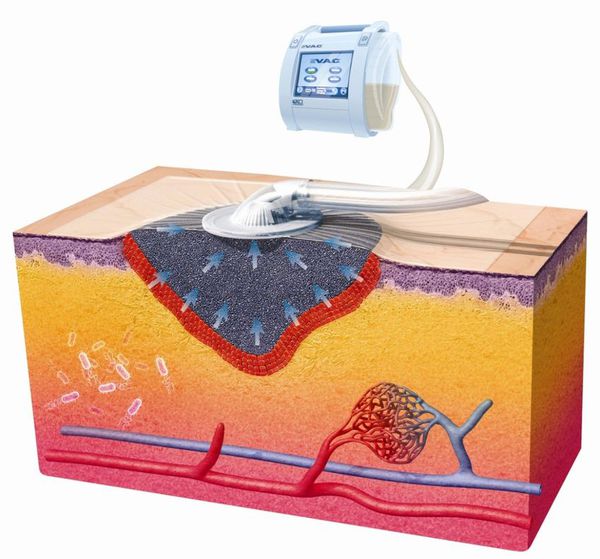
Эффективный и современный способ консервативного лечения ран — вакуум терапия, проводимая с использованием окклюзионных повязок. Отрицательное давление, импульсный и переменный режимы приводят к положительным эффектам: адекватному дренированию раны, щадящей стимуляции репаративных процессов, устранению затёков и отслойки кожи. [29]
Этот способ лечения подходит как для чистых, так и для инфицированных ран, не ограничивая способность пациента к передвижению.
Физиолечение
Как вспомогательный метод местной терапии, применяется физиолечение — ультрафиолетовое облучение раны, гипербарическая оксигенация, воздействие холодным плазменным потоком. [27]
Хирургические способы лечения
Раневой процесс может протекать таким образом, что показания к хирургической активности появляются в отдаленном периоде. [8]
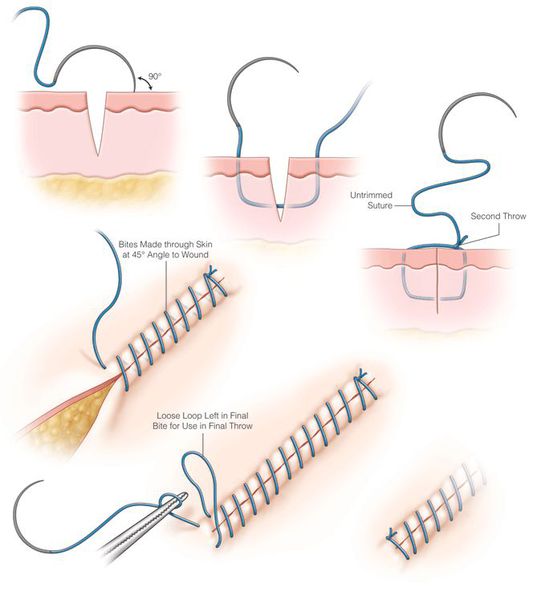
Лечение раны оперативным путём заключается в хирургической обработке: ревизии, гемостазе, иссечении нежизнеспособных тканей, анатомическом (послойном) восстановлении целостности тканей путём ушивания либо сопоставления и удержания скобами.
При ранах с дефектами тканей применима первичная пластика раны с целью реконструкции сегмента и профилактики неминуемых некротических и инфекционных осложнений.
Общая терапия
Общее лечение раны выполняется с соблюдением комплексных принципов: антибиотикотерапия, анальгетики, инфузионно-трансфузионная терапия (при показаниях), введение противостолбнячной, противогангренозной сыворотки, применение анаболических препаратов, поливитаминных комплексов, лечение сопутствующей патологии организма с целью повышения его компенсаторных возможностей. [27]
Отсутствие хирургического, местного лечения раны или его несостоятельность не компенсируется общим лечением и, в том числе, мощной антибиотикотерапией. Санация (лечение) локального очага — приоритетная. Заживление раны без адекватной хирургической обработки затягивается на недели и месяцы.
Прогноз. Профилактика
Прогноз раны определяется её характером — очевидно, что рваная рана заживает длительнее и хуже, чем резаная. [11] Обширность повреждения, сопутствующая и сочетанная патология значительно повлияют на сроки заживления.
Во многом, течение раневого процесса подвластно осложнениям. Осложнения, возникшие в отдалённом периоде, могут замедлить хорошо протекавшее ранее заживление.
Опыт врача хирурга, радикальность обработки раны, способ хирургического пособия и ошибки в его выполнении, техническая и материальная база лечебного учреждения — всё это переменные факторы, объясняющие условность прогноза. [19]
Неблагоприятный прогноз несут раны с дефектами мягких тканей, с нарушением целостности сосудов, нервов, мышц и сухожилий, а также раны, сопровождающиеся переломами.
Отдельного внимания заслуживает прогноз ран инфицированных неспецифичной и специфичной флорой. [11] Первая группа характеризуется вариабельным течением раневого процесса со сроками, превышающими время заживления неинфицированных ран. Вторая группа ран может нести инвалидизирующее влияние: анаэробная агрессивная флора вынуждает хирургов выполнять ампутации и экзартикуляции с целью спасения жизни. [16]
Получение случайных ран не подвержено контролю. Это объясняет трудность их профилактики. Производственный травматизм — единственное звено, подвластное влиянию профилактики. Соблюдение техники безопасности на рабочих местах значительно снижает риск ранений. В остальном, профилактика направлена на раннее и корректное лечение раны с целью минимизации раневых осложнений. [4]
Читайте также:

