Развитие оппортунистических инфекций у онкологических больных
Обновлено: 24.04.2024
Онкологические больные являются группой риска в отношении развития инфекционных осложнений. Существуют множество механизмов защиты организма против инфекции. Их развитие – это результат длительного эволюционного пути. Они представляют собой мощный барьер, препятствующий проникновению патогенов внутрь организма, размножению их и, как следствие, развитию заболевания. Степень необычного повышения чувствительности больного к окружающей его микрофлоре зависит от того, какой из механизмов его иммунной защиты поврежден, насколько тяжелы имеющиеся расстройства и как они взаимодействуют между собой.
Выделяют специфические и неспецифические механизмы защиты. К неспецифическим относятся так называемые физические и химические барьеры: кислотность желудочного содержимого, эндогенная микрофлора, сфинктеры, морфологическая целостность кожных покровов, слизистых оболочек [7]. Специфические механизмы представлены клеточным и гуморальным иммунитетом.
Онкологические больные – особая группа больных. У этих пациентов всегда присутствуют дефекты иммунной системы, с чем связано, прежде всего, развитие самого онкологического заболевания. Дефекты Т-лимфоцитов или моноцитарно-фагоцитарной системы (клеточного иммунитета) имеют место при остром и хроническом лимфобластном лейкозе, лимфогранулематозе, после трансплантации костного мозга, трансплантации органов (почек, сердца). Дисфункция В-клеток может привести к развитию хронического лимфоцитарного лейкоза, множественной миеломы. Дефекты гуморального иммунитета, обычно, представлены нарушением выработки брадикининов, фибринолитической системы, системы арахидоновой кислоты и так далее. Кроме того, сама опухолевая ткань вырабатывает биологически активные вещества, обладающие имуносупрессивным действием. Все онкологические больные получают терапию кортикостероидами, химиолучевое лечение, имеют длительные эпизоды нейтропении. Все эти факторы в комплексе способствуют усугублению иммунодефицита, увеличению частоты различных инфекционных заболеваний.
Возбудителями инфекции, как правило, являются те микроорганизмы, которые колонизируют тот или иной орган, то есть являются его постоянными обитателями. Нормальная микрофлора присутствует на поверхности кожных покровов, слизистых оболочках мочевыделительных путей, желудочно-кишечного тракта, дыхательных путей. Это первая линия защиты, препятствующая инвазии патогенов внутрь организма. В норме поверхность кожи и слизистых колонизирована собственной эндогенной микрофлорой, которая представлена стафилококками, стрептококками, энтерококками, гемофильными палочками, коринебактериями, бактериями семейства Enterobacteriaceae. Так, например, слизистая оболочка пищевода колонизирована различными аэробными и анаэробными микроорганизмами, включая зеленящие стрептококки, энтерококки, дифтероиды, стафилококки, пневмококки, молочнокислые бактерии, микоплазмы, вибрионы, нейссерии, гемофильные палочки, дрожжеподобные грибы рода кандида, бактероиды, вейллонеллы, актиномицеты и др. На уровне пищевода, желудка концентрация микроорганизмов составляет от 100 до 100000 бактерий в 1 мл содержимого [6]. Микроорганизмы, представляющие нормальную микрофлору человека, различаются по вирулентности, т.е. способности вызывать инфекционный процесс. Например, бифидо- и лактобактерии никогда не вызывают заболеваний человека, тогда как E.coli, K. pneumoniae, H. influenzae являются частыми этиологическими агентами, их относят к условно-патогенным микроорганизмам. На поверхности кожи, дыхательных путей можно обнаружить Acinetobacter spp., а на слизистой желудочно-кишечного тракта – Pseudomonas aeruginosa. Эти микроорганизмы обладают выраженной патогенностью, возможностью развития резистентных форм за короткий период времени.
Нормальная секреторная функция кожных желез, быстрая регенерирующая активность эпителия, отшелушивание омертвевших эпителиальных клеток также обеспечивают защиту организма, уменьшая количество потенциальных патогенов на поверхности кожных покровов. В секрете слюны, слезной жидкости, секрете цервикального канала и других секреторных жидкостях организма присутствуют вещества, обладающие антимикробным эффектом. К ним относятся, например, лизоцим, N-ацетил мурамил-L-аланинамидаза, IgG, IgA [7]. Они способны агглютинировать (связывать) микроорганизмы, ингибировать их присоединение к рецепторам клеток или препятствовать их размножению.
В условиях нарушения целостности кожных покровов и слизистых оболочек нормальная микрофлора может стать патогенной и привести к развитию как локальных инфекций (фурункулез, стрептодермия, нагноение ран, формирование абсцессов и многое другое), так и системных.
Особенно важна целостность и функциональная активность кожных покровов и слизистых оболочек для иммунокомпрометированных больных, к которым собственно и относятся онкологические пациенты [9]. В следствие иммуносупрессивной терапии, которую получают все больные (кортикостероиды, химиотерапия, лучевая терапия), снижаются секреторная функция кожных желез и регенерирующая активность эпителия, повышается проницаемость кожных покровов для микроорганизмов. Могут возникать воспалительные изменения слизистых оболочек – мукозиты [11]. Например, при вовлечении в процесс слизистой оболочки полости рта развиваются стоматиты, слизистой желудочно-кишечного тракта – эзофагиты, гастриты. Особенно эта проблема актуальна для больных, длительно находящихся в глубокой нейтропении (после высокодозной химиотерапии, трансплантации костного мозга), у которых мукозиты могут представлять собой жизнеугрожающие ситуации [12]. Этиологическими агентами являются бактерии, грибы, вирусы. Чаще всего наблюдается комбинация возбудителей. Бактериальными патогенами будут являться те микроорганизмы, которые ранее являлись нормальной микрофлорой слизистых оболочек, грибы – чаще всего представлены Candida spp., вирусы – вирус простого герпеса 1 и 2 типа (ВПГ1 и ВПГ2). Клиническими проявлениями являются многочисленные эрозии, язвенные дефекты, возможно, наличие беловато-серого налета на их поверхностях. Кроме того, у пациентов с выраженной иммуносупрессией, с длительной глубокой нейтропенией возможна инвазия патогенов в кровь с развитием бактериемии, фунгемии, вирусемии [11].
Целостность кожных покровов нарушается при установке различных имплантируемых устройств (артериальные и венозные катеты, трахео-, холангио-, нефростомы). В настоящее время не существует материалов, используемых для создания этих устройств, которые были бы биологически инертны. Микроорганизмы связываются с их поверхностями (адгезия), формируют отдельные колонии, которые сравнительно быстро (в течение 24 ч) формируют сплошную биопленку. Большинство микроорганизмов, находящихся в составе биопленки, пребывают в состоянии покоя. Однако на отдельных участках периодически возникают очаги размножения, и вновь возникшие клетки выделяются в окружающую среду: кровь, желчь, мочевые органы и т.д. (в зависимости от локализации имплантируемого устройства), вызывая развитие инфекционного процесса.
Всем онкологическим больным в связи с длительным лечением устанавливают центральные венозные катетеры или порты. Внутрисосудистый катетер устраняет необходимость венепункции для взятия образцов крови, кровезаменителей, антибиотиков, цитостатиков. Инфекции являются основным осложнением, связанным с внутрисосудистыми катетерами, причем в 80% случаев они вызываются грамположительными бактериями, как правило, стафилококками. Встречается инфекция наружной части катетера, туннельная инфекция, катетер ассоциированная бактериемия или фунгемия. Возможно сочетание всех перечисленных вариантов. Микроорганизмы, образующие биопленку в просвете катетера, продуцируют гликокаликс (особенно это касается коагулазонегативных стафилококков). Это вещество защищает бактерии от фагоцитов хозяина и ингибирует действие антибиотиков. Наличие данных о подкожной туннельной или перипортальной инфекции, септические эмболы, гипотензия, связанная с использованием катетера, являются показанием для срочного его удаления одновременно с немедленным назначением антибиотиков. Для профилактики катетер ассоциированных инфекций ряд исследователей предлагает использование импрегнированных антибиотиками катетеров, ротацию доставки антибиотиков через многопросветные катетеры, использование антибиотик-содержащих гепариновых растворов.
Онкологические больные зачастую длительно получают антибактериальную терапию препаратами широкого спектра действия. Это связано с эпизодами панцитопении, расширенными и комбинированными оперативными вмешательствами, которые часто сочетаются с термоабляцией, интраоперационной химиотерапией. Встречается нерациональное использование антибактериальных препаратов: назначение антибиотиков при контаминациях тех или иных органов, длительная антимикробная терапия после операций при отсутствии инфекции [1]. Как следствие происходит гибель нормальной микрофлоры кожных покровов и слизистых, замещение ее патогенными штаммами. Инфекционные осложнения у этих больных, обычно, вызваны комбинацией госпитальных микроорганизмов. В результате лечение инфекции у больных становится непростой задачей, требующей слаженной работы микробиологов и клинических фармакологов.
Развитие инфекций у больных является следствием обструкции опухолью тех или иных органов: бронхиального дерева, пищеварительного тракта, мочевыводящих путей, желчевыводящих путей. Например, обструкция просвета бронха опухолевой массой или сдавление бронхиального дерева опухолью извне приводит к развитию воспалительных изменений в легочной ткани [16]. Обструкция просвета пищевода тканью опухоли может привести к развитию аспирационных пневмоний, возможно развитие эмпиемы плевры, медиастинитов [3].
Опухолевая ткань, особенно с распадом, представляет питательную среду для развития микроорганизмов, их количество возрастает многократно, и они, в свою очередь, становятся возбудителями инфекционных осложнений.
В процессе хирургического вмешательства микроорганизмы проникают в исходно стерильные или заселенные нормальной микрофлорой органы и ткани, вызывая их бактериальное загрязнение, происходит изменение местных и общих иммунных реакций организма, что может явиться предрасполагающим фактором развития инфекции в послеоперационном периоде [2].
Химиолучевое лечение часто предшествует хирургическому вмешательству. В процессе терапии происходит повреждение не только опухолевых клеток, но и здоровых клеток организма, в том числе и клеток, ответственных за уничтожение патогенов. В процессе полихимиотерапии происходит подавление ростков кроветворения. В результате развивается лейко-тромбоцитопения. При глубокой лейкопении количество нейтрофилов не превышает 100-500/мм³ Риск развития тех или иных инфекционных осложнений напрямую зависит от глубины нейтропении и ее длительности. Подсчитано, что за один день пребывания в больнице меняется приблизительно половина эндогенной флоры кожи и кишечника больного, находящегося в состоянии нейтропении, при этом обычные грамположительные аэробы и анаэробные бактерии замещаются аэробными грамотрицательными микроорганизмами. Инфекции больным с нейтропенией могут передаваться с пищей и водой, молочными продуктами, свежими овощами, недостаточно термически обработанными мясными и рыбными продуктами. Микроорганизмы (потенциальные возбудители инфекции) обнаруживаются на кранах в ванной, в туалете, в душе. Они представлены энтеробактериями, Pseudomonas spp, Klebsiella spp, Cryptosporidium, Aspergillus spp, Legionella spp. Велика опасность инфицирования энтеробактериями, Pseudomonas spp, Klebsiella spp, Listeria spp, Staphylococcus spp, Streptococcus spp, Salmonella spp, Campylobacter spp, Toxoplasma gondii, грибы [5]. Химиотерапия нарушает функцию реснитчатого эпителия дыхательных путей, сократительную способность желудочно-кишечного тракта, целостность слизистых оболочек, приводит к уничтожению естественной микрофлоры дыхательных, пищеварительных путей и других отделов организма и замещению собственных микроорганизмов госпитальными штаммами. Многие режимы полихимиотерапии включают кортикостероидные препараты. Данная группа лекарственных средств обладает выраженным иммуносупрессивным действием, поскольку, кортикостероиды ингибируют комплемент-индуцированную агрегацию гранулоцитов, повышая тем самым риск развития инфекции [6].
Таким образом, онкологические больные требуют тщательной разработки подходов к профилактике и лечению инфекционных осложнений.
Список литературы:
6. Mims C., Playfair J., Roitt I., Wakelin D., Williams R., Medical microbiology, Mosby, Edinburg, 2002, 584.
7. Tramont C.E., Hoover D.L., Innate (general or non-specific) host defense mechanisms. Basic Principles in the Diagnosis and Management of Infectious diseases. Vol.1, 5th ed. Philadelphia: Churchill-Livingstone, 2000:31.
8. Giamarellou H., Antoniadou A. Infections complications of febrile leukopenia. Infections in the compromised host. Inf. Dis. Clin. of N Am. 2001; 15(2):457-482.
9. Finberg R.W. Infection in cancer patients. Cancer Medicine and Hematology. Harvard Medical School Department of Continuing Education, October 26, 1999.
10. Serody J.S., Shea T.C. Prevention of infections in bone marrow transplant recipients. Nosocomial Infections. Inf. Dis. Clin. Of N Am. 1997 2(2):459-477.
11. Leather H.L., Wingard J.R. Infections following hematopoetic stem cell transplantation. Infections in the compromised host. Inf. Dis. Clin. of N Am. 2001; 15(2):487-520.
12. Ibrahim N.K., Sahin A.A., Dubrow R.A., Lynch P.M., Boehnke-Michaud L., Valero V., Busdar A.U., Hortobagyi G.N. Colitis associated with docetaxel-based chemotherapy in patients with metastatic breast cancer. Lancet 2000; 355(9200):281-283.
13. Segal H.B., Walsh T.J., Holland S.M. Infections in the cancer patient. In: De Vita VT Jr, Hellman S., Rosenberg S.A., eds. Cancer Principles and Practice of Oncology. 6th ed. Philadelphia: Lippincott Williams and Wilkins, 2001:32855-2858.
14. Ang B.S., Telenti A., King B., Steckelberg J.M., Wilson W.R. Candidemia from a urinary tract source; microbiological aspects and clinical significance. Clin. Infect. Dis.1991; 75: 391.
15. Koozeniowski O.M. Urinary tract infections in the impaired host. Med. Clin. N Am. 1991; 75:391.
Copyright © Российское общество клинической онкологии (RUSSCO).
Полное или частичное использование материалов возможно только с разрешения администрации портала.
Оппортунистические инфекции – это большая группа инфекционных заболеваний, которые развиваются у пациентов с различными типами иммунодефицитов и нехарактерны для людей с нормальным иммунным статусом. Патологии поражают любую систему органов и вызывают соответствующую симптоматику. К общим клиническим проявлениям относят длительный субфебрилитет, лимфаденопатию, астенический синдром. Диагностика оппортунистических инфекций включает серологические, молекулярно-генетические, бактериологические и другие методы детекции патогенных возбудителей. Программы лечения сочетают длительную этиотропную терапию с методами иммунокоррекции.
МКБ-10


Общие сведения
Проблема оппортунистических инфекций (ОПИ) становится все более актуальной, что вызвано ростом числа ВИЧ-инфицированных людей, разработкой эффективных, однако агрессивных методов лечения онкопатологии. При этом многие люди являются бессимптомными носителями возбудителей ОПИ: 60% инфицированы цитомегаловирусом, 90% – герпесвирусами 1 и 2 типов, около 30% – токсоплазмой. Учитывая клинический полиморфизм и отсутствие специфических симптомов, диагностика и лечение оппортунистических болезней представляет серьезную мультидисциплинарную проблему.

Причины
Для манифестации оппортунистических инфекций необходимо заражение патогенным микроорганизмом: вирусом, бактерией, грибком или простейшим. Известно более 20 типичных возбудителей ОПИ, в современной инфектологии этот перечень постоянно дополняется. Болезнь возникает при активации латентного очага, реже выступает следствием текущего заражения. Первостепенную важность играет нарушение иммунного статуса вследствие следующих патологий:
- ВИЧ-инфекция. Самая частая причина, поскольку на определенном этапе снижения числа CD4-клеток ОПИ развиваются у каждого больного. Инфекционные болезни используются для диагностики заражения ВИЧ и определения стадии заболевания, поэтому в данном контексте они называются СПИД-ассоциируемыми или СПИД-индикаторными патологиями.
- Злокачественные новообразования. Патофизиология любого опухолевого процесса предполагает угнетение собственной иммунной системы пациента и снижение ее ответа на чужеродные агенты. При этом уменьшается число Т-клеток, угнетаются процессы фагоцитоза. Проблема наиболее выражена при гемобластозах – лейкозах и лимфомах.
- Хроническая соматическая патология. Угнетение активности клеточного и гуморального иммунитета происходит при эндокринных заболеваниях (сахарный диабет, гипотиреоз), почечной недостаточности, тяжелых воспалительных патологиях ЖКТ.
- Ятрогенные факторы. Применение цитостатиков и других видов иммуносупрессоров является важным предиктором развития оппортунистических инфекций. Подобная ситуация наблюдается в группе пациентов после лучевой терапии, трансплантации органов и костного мозга.
- Первичные иммунодефициты. В эту группу относят все виды иммунной недостаточности, которые имеют генетический характер или возникают внутриутробно под влиянием тератогенов. Они манифестируют в раннем детском возрасте, проявляются затяжными оппортунистическими болезнями, которые с трудом подаются терапии.
Патогенез
Хотя возбудители оппортунистических инфекций таксономически неоднородны, в развитии заболеваний большую роль имеют общие особенности их патогенности и вирулентности. К свойствам микроорганизмов, вызывающих ОПИ, относят возможность длительного и даже пожизненного персистирования в организме человека, внутриклеточное паразитирование, склонность к поражению клеток моноцитарно-макрофагальной системы.
Инфекции активизируются при иммунодефицитах любой этиологии и склонны к хроническому течению с периодическими обострениями, поражением жизненно важных органов. Для оппортунистических болезней характерна лимфогенная и гематогенная диссеминация микроорганизмов, образование эктопических очагов. Собственный иммунитет пациента не способен оказать должное сопротивление инфекционному агенту, лекарственные средства не всегда эффективны.
Сложность и опасность оппортунистических инфекций заключается еще и в том, что они способны подавлять естественный иммунитет. В последние годы говорят о возможности пожизненной иммуносупрессии при персистировании герпесвирусов. Таким образом, формируется порочный круг, когда иммунодефицит провоцирует активацию возбудителей ОПИ, которые усугубляют явления иммунной недостаточности и потенциируют дальнейшие полиорганные нарушения.

Классификация
Единой систематизации оппортунистических инфекций на сегодня не существует. Условно возбудителей объединяют в 3 группы: патогены, которые поражают лиц с нарушениями иммунитета и здоровых людей; микробы, встречающиеся только при иммунодефицитах; вакцинные штаммы микроорганизмов. Общепринятой является классификация ОПИ согласно типу возбудителя:
Симптомы оппортунистических инфекций
В инфектологии выделяют общую группу клинических признаков, которая встречается при любом варианте ОПИ. Наиболее типичным симптомом признан длительный субфебрилитет, которые возникает без видимой причины и беспокоит пациента больше 1 месяца. Нередко повышение температуры возникает после перенесенного ОРВИ или кишечной инфекции, которые выступают пусковым фактором активации оппортунистического заболевания.
Вторым настораживающим симптомом считается лимфаденопатия – увеличение лимфатических улов. Чаще всего в процесс вовлекается лимфоидная ткань шейно-подчелюстной, подмышечной и паховой зоны. Лимфоузлы достигают диаметра около 1 см, имеют плотноэластическую консистенцию, не спаяны с окружающими тканями и безболезненны при ощупывании.
Третью группу общей симптоматики оппортунистических инфекций составляет астенический синдром. Он включает слабость, повышенную утомляемость, снижение переносимости умственных и физических нагрузок. Зачастую пациенты жалуются на ночную потливость, головокружения и головные боли, нарушения сна. При длительном существовании таких признаков наблюдается когнитивная дисфункция, эмоциональная подавленность, стойкое снижение работоспособности.
Пациента с иммуносупрессией должен насторожить кашель и одышка – типичные признаки туберкулеза и пневмоцистной пневмонии (ПЦП), снижение остроты зрения – возможное проявление цитомегаловирусного ретинита, длительно сохраняющаяся диарея – признак криптоспоридиоза, микроспоридиоза. Жжение и сухость полости рта в комбинации с эрозиями и белыми налетами на слизистых указывают на орофарингеальный кандидоз.
Оппортунистические болезни не имеют четко выраженного тропизма. Один и тот же вид возбудителя может вызывать миокардит, плеврит, артрит, менингит и другие нозологические формы. Зачастую они имитируют симптомы хронических соматических заболеваний, с которыми пациенты длительно и безрезультатно посещают врачей разных специальностей. Исключение составляет пневмоцистоз, который в основном поражает легкие с развитием ПЦП.
Осложнения
Оппортунистические инфекции – тяжелые и потенциально смертельные заболевания. Среди пациентов с терминальными стадиями ВИЧ-инфекции ОПИ составляют 90% в структуре летальности, оставшиеся 10% приходятся на саркому Капоши, лимфомы и прочие неинфекционные последствия СПИДа. Смертность при церебральном токсоплазмозе составляет около 33%, при криптококковом менингите – 20-30%, при пневмоцистной пневмонии – 10-20%.
Особую тревогу вызывает сочетание нескольких видов оппортунистических заболеваний у одного пациента. Микробные ассоциации более характерны для позднего периода и хронического течения основной патологии, вызвавшей иммунодефицит. Сочетанное инфицирование типично для иммунокомпрометированных пациентов, пребывающих на стационарном лечении: у 40-50% больных в послеоперационном периоде, у 70-80% при перитонитах и плевритах.
Распространение оппортунистических инфекций негативно сказывается на репродуктивном здоровье населения. Они обуславливают многие случаи самопроизвольного прерывания беременности, эмбриопатий и фетопатий, задержки внутриутробного развития. Дети, рожденные от матерей с ОПИ, находятся в группе риска развития заболеваний новорожденных, перинатальных энцефалопатий.

Диагностика
Обследование пациентов проводится мультидисциплинарной командой врачей, в которую входят врач-инфекционист, иммунолог, онколог и другие узкопрофильные специалисты. Большое клиническое значение имеет выяснения времени и условий появления симптоматики, характера течения заболевания, наличия факторов риска иммунодефицитных состояний. Для подтверждения оппортунистических инфекций проводятся следующие методы диагностики:
Лечение оппортунистических инфекций
В процессе лечения практикующие инфекционисты сталкиваются с такими нюансами, как множественная лекарственная устойчивость патогенов, гетерогенность популяции возбудителей, низкая активность естественных иммунных факторов. Основу терапии составляет прием этиотропных противомикробных препаратов: антибиотиков, антимикотиков, противопротозойных и противовирусных. Лечение ОПИ имеет ряд особенностей:
- в основном назначаются комбинации из 2-3 препаратов для повышения их эффективности;
- продолжительность противомикробной терапии повышается в 1,5-2 раза и более в сравнении с лечением инфекционных болезней у иммунокомпетентных лиц;
- при подборе терапии ориентируются не только на клиническую картину болезни, но и на текущий иммунный статус пациента;
- при вирусных инфекциях обязательно назначаются этиотропные препараты, тогда как у людей без иммуносупрессии противовирусные средства используют только по показаниям.
Для успешного лечения ОПИ требуется максимально возможное восстановление иммунной функции. В группе пациентов с ВИЧ-инфекцией назначаются протоколы антиретровирусной терапии (ВААРТ), чтобы повысить число CD4-клеток и улучшить отдаленные прогнозы. При ведении онкологических больных используются персональные схемы иммуномодуляторов, экспериментальные направления иммунотерапии и регенеративной медицины с применением стволовых клеток.
Прогноз и профилактика
Течение любой инфекции на фоне иммуносупрессии является сложным и непредсказуемым, однако усовершенствованные протоколы лечения позволяют достичь стойкой ремиссии или даже полного излечения. К прогностически неблагоприятным факторам относят пожилой и старческий возраст, неправильно подобранную терапию, невозможность проведения иммунокоррекции основного заболевания.
При иммунодефицитах показана первичная медикаментозная профилактика оппортунистических инфекций. Применяют сульфаниламиды, макролиды‑азалиды, противогрибковые средства. При положительной пробе Манту или недавнем контакте с больным туберкулезом назначается химиопрофилактика сроком на 6 месяцев. Также пациентам рекомендовано строго соблюдать противоэпидемические меры, в периоде резкой иммуносупрессии необходимо пребывание в стерильных боксах.
3. Клинические особенности сочетанных оппортунистических инфекций (обзор)/ В.В. Шкарин, Н.В. Саперкин// Медицинский альманах. – 2017. – №4.
4. Оппортунистические инфекции: проблемы и перспективы/ Под общ. ред. проф. Ю.В. Редькина, О.А. Мирошника, В.В. Лобова. – 2002.
Инфекции у больных раком при подавлении иммунитета
Инфекции — главные причины смерти при раке. Они не только часто встречаются, но нередко имеют более тяжелое течение, чем у других пациентов, менее подверженных действию терапии, и иногда вызываются организмами, которые не патогенны для здоровых людей. Такая восприимчивость является следствием подавления защитных механизмов больного, вызванного опухолью и ее лечением.
Кожа и слизистые оболочки служат барьером для инфекции. Опухолевая инфильтрация и местная лучевая радиотерапия могут привести к повреждению лимфатических или венозных сосудов, что приводит к увеличению восприимчивости к локальной инфекции. Воспроизводство эпителиальных клеток в желудочно-кишечном тракте подавляется химиотерапией, из-за чего повреждается и изъязвляется слизистая, что позволяет организмам из кишечника попасть в систему воротной вены.
Кожа повреждается внутривенными иглами и канюлями, особенно туннельными подкожными каналами. Это частые источники инфекции, которые вызываются такими кожными организмами, как Staphylococcus epidermidis. В носоглоточной полости возникают инфекции, вызванные Candida albicans.
Рак при запущенной стадии иногда связан с ухудшением функций и нейтрофилов, и моноцитов. Было описано подавление хемотаксической, фагоцитарной и бактерицидной активностей.
Ослабленная замедленная гиперчувствительность довольно распространена при запущенной болезни Ходжкина, но менее часта в других случаях злокачественных опухолей. Лимфопения неизменно вызывается действием алкилирующих агентов и массивной радиотерапией. Клеточный иммунитет особенно важен при защите организма хозяина от грибов, вирусов, туберкулеза и простейших.
Интенсивная цитотоксическая химиотерапия ведет к ухудшению образования антител к бактериальным и вирусным антигенам.
Циркулирующие бактерии удаляются фагоцитарными клетками, находящимися в синусах ретикулоэндотелиальной системы, особенно в печени и селезенке. Для этой чистки важны антитела и белки системы комплемента. Спленэкто-мия увеличивает риск серьезной бактериальной инфекции, особенно пневмококковый сепсис в детском возрасте и в меньшей степени во взрослом.
Возбудители сепсиса
Бактериемия и септицемия у больных раком
Инфекции кровяного русла довольно часты у пациентов с гранулоцитопенией. Патогенами часто являются грамотрицательные бактерии (Escherichia coli, Pseudomonas aeruginosa), стафилококки и стрептококки. Увеличивается частота инфекций, вызванных грамположительными бактериями, особенно Staphylococcus epidermidis. Пациенты с тунельными подкожными каналами особенно подвержены поражениям этим организмом.
Жар у пациента с нейтропенией при раке — показатель присутствия бактерий в крови и под кожей. Если существует очевидный источник инфекции, например инфицированный порт для инфузий, следует взять культуру бактерий и удалить канюлю. Лечение не следует откладываеть для пациента с нейтропенией. Пациенты с лихорадочной нейтропенией с относительно низким риском развития серьезных осложнений относятся к тем, кого лечат короткими циклами химиотерапии для солидных опухолей.
Эти пациенты должны быть госпитализированы. Недавние исследования показали, что пероральный прием амоксициллина-клавуланата комбинированный с пероральным приемом ципрофлоксацина так же эффективен, как и внутривенная химиотерапия в этой группе (70% пациентов). Пациенты с высоким риском (с неконтролируемым раком или на стационарном лечении интенсивной терапией) лечатся внутривенными антибиотиками, в том числе b-лактамом и аминогликозидом или цефтазидимом.
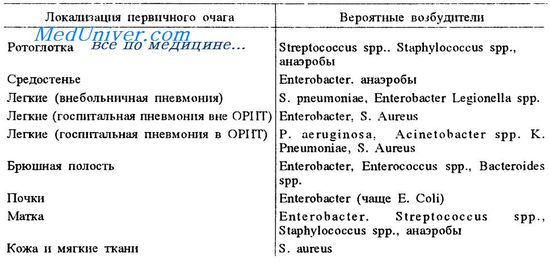
Респираторные инфекции у больных раком
У пациента с серьезным подавлением иммунитета довольно часто возникает жар с легочным инфильтратом. Главные причины этого даны в таблице.
Осложнения в постановке диагноза могут быть значительны, поскольку тесты слюнных и кровеносных культур иногда отрицательны, а более инвазивные процедуры, такие как трансбронхиальная биопсия, невозможны из-за тромбоцитопении или общего состояния пациента.
Существуют некоторые клинические особенности, которые помогают при постановке диагноза. Кавитация наиболее часто сопровождает поражения анаэробными бактериями, стафилококками и микобактериями. Инфекции Pneumocystis вызывают заметную одышку, а на рентгенограмме грудной клетки видны билатеральные инфильтраты, обычно состоящие из хилуса. Болезнь, однако, может протекать вяло и вызвать долевое уплотнение. Цитомегаловирусные инфекции встречаются главным образом у пациентов с серьезным подавлением иммунитета, в частности в течение аллогенной ВМТ. Болезнь может также вызывать миокардит, невропатию или офтальмию.
Легочные инфильтраты обычно билатеральны. Инфекции Candida вызывают широкое разнообразие изменений в рентгенограмме. Инфекции Aspergillus обычно быстро прогрессируют. Тесты культур крови обычно отрицательны, а инфильтраты возможны в одном или двух легких.
При затруднениях в постановке диагноза можно следовать следующей схеме.
У пациентов без нейтропении или тромбоцитопении исследовать посевы крови, слюны, бронхоскопические промывания и трансбронхиальную биопсию там, где это возможно. Если кровяные и слюнные культуры отрицательны, лечить антибиотиками широкого антибактериального спектра действия (обычно в комбинации с аминогликозидом, пенициллином и метронидазолом или аналогичными соединениями). Если возможной причиной инфекции является Pneumocystis, следует давать высокие дозы котримоксазола. Если ответа нет, рассмотрите ацикловир для вируса простого герпеса и противогрибковую терапию с амфотерицином или кетоконазолом. Ацикловир не эффективен против цитомегаловирусов.
Если кровяные или слюнные тесты положительны, лечите соответствующе, но если ответа нет, рассмотрите смешанные инфекции.
Пациентам с нейтропенией или тромбоцитопенией проводят бронхоскопию, но биопсия не всегда возможна, и лечение продолжают без дальнейшего диагностического исследования. До и после бронхоскопии иногда необходимы антибиотики и переливание тромбоцитов.

Инфекции мочевыводящих путей у больных раком
Инфекции часты у пациентов с затрудненным мочеиспусканием. Затруднения могут быть вызваны опухолью или ослаблением мочевого пузыря у пациентов с компрессией спинного мозга и его корешков. Диагноз ставится после исследования уринокультуры, и лечение осуществляется антибиотиками и снятием осложнений, если это возможно.
Желудочно-кишечные инфекции у больных раком
Молочница ротовой полости (инфекция, вызываемая Candida albicans) — частое осложнение химиотерапии. Она особенно распространена у пациентов с подавленным иммунитетом, у пациентов, принимающих стероиды и тех, кого лечат антибиотиками с широким спектром действия. Рот и глотка становятся очень болезненными, а белые пятна грибков видны на эри-темной основе. У плохо питающихся пациентов инфекция может проникать глубже и распространяться по пищеводу, желудку и кишечнику. Обычно эффективен пероральный прием нистатина, амфотерицина или миконазола.
Проявление вируса простого герпеса на губах часто проблематично для пациентов с лейкопенией, и повреждения могут быть довольно обширными. В данном случае необходимо местное применение ацикловира для пациентов с подавленным иммунитетом или систематический прием ацикловира при более серьезных инфекциях.
Инфекции, вызванные Candida в пищеводе, необходимо лечить пероральным приемом суспензии нистатина, но если такое лечение неэффективно, то необходимо применение кетоко-назола или короткий курс амфотерицина. Кишечные инфекции, возникающие при поражении Candida, должны лечиться амфотерицином.
Перианальные инфекции распространены среди пациентов с нейтропенией. Всегда необходимо применять профилактические меры совместно с тщательной гигиеной промежности и смягчителями стула для предотвращения запора и анальных трещин. Распространяющиеся перинеальные (паховые) инфекции могут угрожать жизни пациента, и требуется срочное лечение внутривенными антибиотиками, действующими против грамотрицательных и анаэробных бацилл.
Менингит у больных раком
Инфекции центральной нервной системы (ЦНС) довольно редки, но у пациентов с лимфомой или лейкемией иногда развивается менингит из-за Cryptococcus neoformans. Начало заболевания индивидуально у каждого и сопровождается головной болью. Микроорганизм обнаруживают при окрашивании India ink спинномозговой жидкости (CSF).
Выявление антигенов Cryptococcus в крови и CSF возможно у большинства пациентов. Состояние многих пациентов улучшается при приеме амфотерицина, некоторые вылечиваются.
Кожные инфекции у больных раком
В отличие от инфекции, представленной на портах для вливания, наиболее частое кожное заболевание — опоясывающий лишай (varicella zoster). Возникает из-за реактивации вируса varicella zoster в ганглии дорсального корешка, вызывает кожную пузырчатую сыпь, которая особенно серьезна у людей с подорванным иммунитетом, может распространяться как ветряная оспа и вызывать фатальную пневмонию. Пациентов следует лечить ацикловиром как можно быстрее.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Осложнения у больного при онкологических заболеваниях.
В этой главе анализируются лихорадочные состояния и нарушения дыхания у больных со злокачественными новообразованиями; во второй части речь идет об осложнениях, связанных с гиперлейкоцитозом и неотложными неврологическими состояниями.
1. Решения о проведении любых лечебных вмешательств у онкологических больных в критическом состоянии должны приниматься с учетом целей основной лечебной тактики. Большое значение имеют характер течения основного заболевания, степень истощения больного, нарушения функции различных органов, а также наличие предшествующей химиотерапии. Не описанные в этих двух главах общие для онкологических больных состояния встречаются в других разделах (Кровотечения, Электролитные расстройства, Почечная недостаточность). Неотложные состояния, возникающие вследствие лечебных мероприятий, требуют устранения опасного фактора и симптоматической терапии. В числе осложнений химиотерапии нужно назвать застойную сердечную недостаточность при приеме антрациклинов (в зависимости от дозы), пневмониты, почечную недостаточность в результате приема метотрексата или цисплатины, тромбоз сосудов мозга, при лечении L-аспарагиназой либо блеомицином.
2. Часто встречающийся у онкологических больных иммунодефицит объясняет легкость возникновения оппортунистических инфекций и генерализованного бактериального сепсиса. Высокая вероятность серьезных инфекционных осложнений объясняется нарушением целостности естественных барьеров (например, изъязвление кожи или слизистой ЖКТ, перианальные трещины, катетеризация центральных вен), а также наличием нейтропении (количество нейтрофилов
3. Причиной появления паренхиматозных инфильтратов могут быть: инфекция, химиотерапия (препараты группы нитромочевины, миелосан, блеомицин, циклофосфан, метотрексат), лучевой пневмонит (обычно через 2—6 мес после облучения), либо кровотечения. При инфекции неизвестной этиологии назначают препараты, действующие как на обычные бактериальные, так и на оппортунистические возбудители; например, антибиотики широкого спектра действия в сочетании с амфотерицином; триметоприм/сульфаметоксазолом и эритромицином. Лечение возникшего в результате химиотерапии пневмонита заключается в исключении данного препарата из лекарственной схемы и в некоторых случаях назначения стероидных гормонов. Эмболия легочной артерии наблюдается главным образом при карциономах желудка и поджелудочной железы. Появление объемного образования в средостении с синдромом верхней полой вены чаще всего встречается при лимфомах, других лейкозах и бронхогенной карциноме, но может быть связано с раком пищевода, толстой кишки, молочной железы и яичка. В числе симптомов следует назвать диспноэ, отеки на лице, туловище, а также верхних конечностях. Диагностика основана на немедленной биопсии, если возможно, под местной анестезией; далее проводится неотложная лучевая или соответствующая химиотерапия.
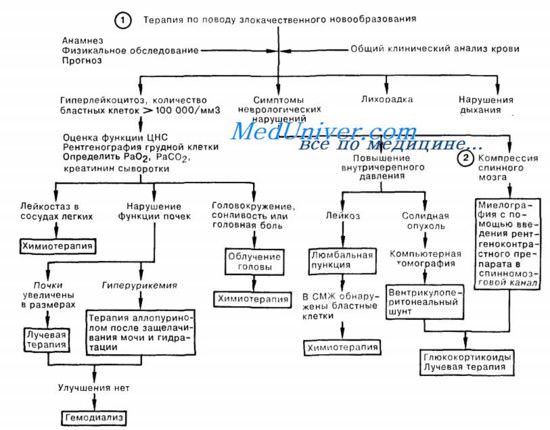
Далее рассмотрены ситуации, в которых у больного с леченным ранее злокачественным новообразованием обнаруживают гиперлейкоцитоз, а также признаки и симптомы неврологического расстройства.
1. Гиперлейкоцитоз при лейкозе с числом бластных клеток более 100000/мкл может привести к фатальным осложнениям вследствие повышения вязкости крови с лейкостазом в сосудах ЦНС и легких, к внутричерепным кровоизлияниям, нарушениям функции почек из-за инфильтрации лейкозными клетками или гиперурикемии, а также к электролитным расстройствам при лизисе опухолевых клеток, сопровождающимся высвобождением внутриклеточного содержимого. По мере возникновения этих осложнений следует незамедлительно проводить соответствующее лечение. До начала терапии добиваются адекватной гидратации больного при щелочной реакции мочи на фоне приема аллопуринола и уровня мочевой кислоты в сыворотке крови менее 0,59 ммоль/л; затем начинают химиотерапию уменьшающимися дозами до снижения числа бластных клеток менее 100000/мкл.
2. Наиболее частыми симптомами сдавления спинного мозга являются боль, парестезии, слабость. Чтобы предотвратить необратимые повреждения, необходимо своевременно локализовать сдавление с помощью компьютерной томографии после введения рентгеноконтрастного препарата и немедленно начать прием глюкокортикоидов и лучевую терапию. Повышение внутричерепного давления вследствие роста первичной или метастатической опухоли требует введения кортикостероидов, неотложного наложения вентрикулоперитонеального шунта, а также начала лучевой терапии. Лейкозное поражение мозговых оболочек, лежащее в основе повышения внутричерепного давления, служит показанием к интратекальному введению противоопухолевых препаратов.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Лучевая диагностика оппортунистических инфекций позвоночника
а) Определения:
• Инфекционные заболевания, развивающиеся на фоне иммунодефицитных состояний, хронических/системных заболеваний, терапии глюкокортикоидами, онкологических заболеваний ± химиотерапии
б) Лучевая диагностика:
1. Общие характеристики:
• Наиболее значимый диагностический признак
о Интрамедуллярные, интрадуральные экстрамедуллярные или экстрадуральные очаги поражения
о Системные проявления инфекции, например, поражение легких
4. Рекомендации по визуализации:
• Наиболее оптимальный метод диагностики:
о КТ → оценка характера костных изменений
о МРТ → оценка характера и распространения интрамедуллярного, интрадурального экстрамедуллярного и экстрадурального процесса
5. Радиоизотопные исследования:
• Сцинтиграфия с мечеными лейкоцитами:
о Клетки, меченые эксаметазимом 99m Тс или оксином 111 In:
- Метод менее информативен в отношении диагностики заболеваний, при которых первичный ответ организма опосредован не нейтрофилами, но другими звеньями иммунитета, что как раз и бывает при большинстве оппортунистических инфекций и спондилите
• При сцинтиграфии с хитиназой, меченой 123 I, отмечается накопление изотопа в тканях при поражении их Candida albicans и Aspergillus fumigatus:
о → метод используется для диагностики грибковых инфекций
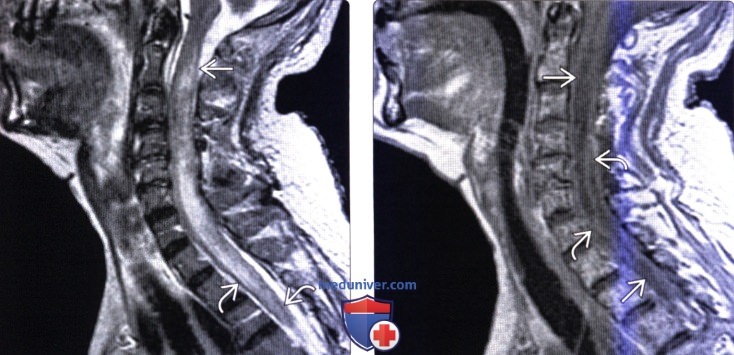
(Слева) Сагиттальный срез, Т2-ВИ: увеличение объема спинного мозга с гиперинтенсивностью сигнала его паренхимы. Изменения сигнала распространяются от уровня С2 до верхнегрудного отдела позвоночника. Пациент длительное время принимал глюкокортикоиды по поводу артрита, на фоне чего развился абсцесс спинного мозга, вызванный Listeria, и листериозный менингит.
(Справа) Сагиттальный срез, Т1-ВИ с КУ: гипоинтенсивность сигнала и увеличение объема спинного мозга с гетерогенным контрастированием паренхимы спинного мозга и контрастным усилением сигнала мягких мозговых оболочек. Такая картина является проявлением абсцесса спинного мозга и менингита, вызванных Listeria.
в) Дифференциальная диагностика оппортунистических инфекций:
1. Гранулематозный спондилит:
• Инфекционное поражение позвоночника и окружающих мягких тканей, вызванное возбудителями туберкулеза или бруцеллеза
• Туберкулез: выраженная кифотическая деформация позвонков при относительном сохранении целостности межпозвонковых дисков, массивные паравертебральные абсцессы:
о Поражение задних элементов
о Распространение инфекции по подсвязочным пространствам на смежные и несмежные уровни
• Бруцеллез: спондилит нижнепоясничных позвонков в сочетании с двусторонним сакроилиитом:
о Поражение переднего отдела замыкательных пластинок в области прикрепления межпозвонкового диска
2. Пиогенный спондилит:
• Инфекционное поражение позвонков и межпозвонковых дисков, вызванное гноеродной бактериальной флорой
• Гипоинтенсивность Т1-/гиперинтенсивность Т2-сигнала костного мозга тел позвонков с нечеткими контурами и изменениями замыкательных пластинок:
о Первичное инфекционное поражение субхондральной кости, непосредственно прилегающей к замыкательным пластинкам
о Снижение высоты межпозвонкового диска ± гиперинтенсивность Т2-сигнала ± контрастное усиление сигнала
о Инфильтративные изменения паравертебральных ± эпидуральных тканей ± жидкостные скопления
о Сдавление спинного мозга ± гиперинтенсивность Т2-сигнала его паренхимы
3. Грибковые и прочие спондилиты:
• Инфекции, вызванные неказеозообразующей кислотонеустойчивой флорой, развивающиеся в первую очередь как оппортунистические инфекции у лиц с иммунодефицитом
• Костно-деструктивный процесс ± поражение межпозвонковых дисков, эпидурального пространства и паравертебральных тканей
5. ВИЧ-ассоциированный миелит:
• Гиперинтенсивность Т2-сигнала спинного мозга ± пятнистое контрастное усиление
• Атрофия спинного мозга
• Грудной > шейный отдел спинного мозга с краниальным распространением процесса по мере прогрессирования заболевания
6. Вирусный миелит:
• Острое воспалительное поражение спинного мозга в результате прямой инвазии возбудителя либо иммуноопосредованное повреждение после перенесенной вирусной инфекции
• Протяженное увеличение объема и отек спинного мозга при отсутствии очагового поражения
• Различной степени выраженности неочаговое контрастное усиление сигнала пораженных сегментов спинного мозга
7. Острый диссеминированный энцефаломиелит, поражение спинного мозга:
• Иммуноопосредованное демиелинизирующее заболевание
• Мультифокальные в форме языков пламени очаги поражения белого вещества при относительно минимально выраженных объемных эффектах или вазогенном отеке
• Различная степень контрастного усиления сигнала, связанная со стадией заболевания
• Практически всегда одновременно развивается поражение головного мозга
8. Острый поперечный миелит, идиопатический:
• Воспалительное заболевание, поражающее обе половины спинного мозга
о → двусторонние двигательные, чувствительные и вегетативные неврологические нарушения
• Периферическое контрастное усиление сигнала вокруг центрально расположенных гиперинтенсивных в Т2-режиме очагов поражения
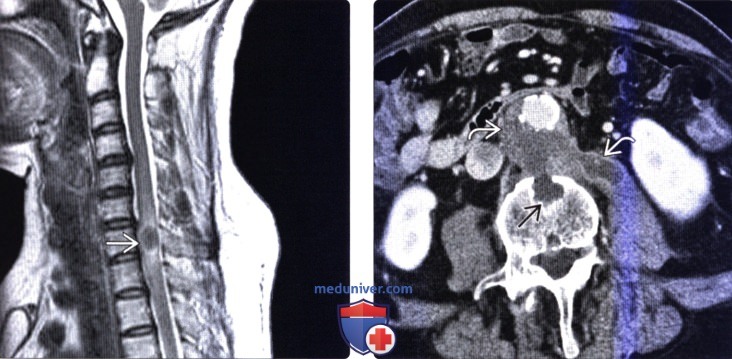
(Слева) Сагиттальный срез, Т2-ВИ: увеличение объема спинного мозга и гипоинтенсивное интрамедуллярное образование на уровне С7, окруженное гиперинтенсивной зоной отека. Гипоинтенсивность Т2-сигнала характерна для туберкулеза.
(Справа) Аксиальный КТ-срез с КУ: мягкотканное образование неправильной формы, окружающее инфицированный протез брюшной аорты и прилежащее к поясничной мышце, с формированием абсцесса, распространяющегося в передний отдел тела L3. Костно-деструктивный процесс в данном случае вызван грибковой инфекцией.
г) Клинические вопросы:
1. Клиническая картина:
• Наиболее распространенные симптомы/признаки:
о Лихорадка, боль в спине/шее
о Парапарез
о Цитомегаловирусная полирадикулопатия с поражением пояснично-крестцовых корешков спинного мозга → острый восходящий вялый паралич нижних конечностей с арефлексией, парестезиями, нарушением функции сфинктеров
• Другие симптомы/признаки:
о Симптомы поражения легких
2. Демография:
• Эпидемиология:
о Состояния, приводящие к развитию иммунодефицита:
- Длительный прием глюкокортикоидов
- Нейтропения, снижение активности нейтрофилов, подавление гемопоэза
- ВИЧ-инфекция:
Прогностическим фактором течения заболевания является число CD4 клеток
Легкое и умеренное снижение их числа (>200 клеток в мм 3 ) → дисцит/спондилит, откликающиеся на антибактериальную терапию
Выраженное снижение (50-200 клеток в мм 3 ) → туберкулез позвоночника
Наиболее низкие уровни CD4-клеток → эпидуральный абсцесс
Частота спондилодисцитов у ВИЧ-положительных пациентов напрямую связана с числом CD4 Т-лимфоцитов
При снижении числа CD4-клеток < 100/мкл увеличивается вероятность развития смешанных инфекций
- Рак ± цитотоксическая химиотерапия:
Blastoschizomyces capitatus → недавно выявленный грибковый патоген, являющийся причиной спондилодисцита у онкологических пациентов
- Трансплантация органов и иммуносупрессивная терапия
о Реципиенты органов (получающие иммуносупрессивную терапию) → туберкулез позвоночника
о Воспалительный синдром восстановления иммунитета (ВСВИ):
- У пациентов с синдромом приобретенного иммунодефицита(СПИД) после начала высокоактивной антиретровирусной терапии повышен риск развития ВСВИ с поражением ЦНС:
ВСВИ обычно связан с микобактериальными инфекциями (вызванными, например, Mycobacterium avium), инфекциями, вызванными герпес-вирусами (вирус опоясывающего лишая или цитомегаловирус [ЦМВ]), и микозами
Васкулопатия, вызванная вирусом ветряной оспы
Рецидивирующая миелопатия, вызванная возбудителем туберкулеза
о Цитомегаловирусная пояснично-крестцовая полирадикулопатия → осложнение течения ВИЧ-инфекции у пациентов с числом CD4-клеток < 40 в мкл
о Острый фокальный или диффузный менингит и энцефалит с деструкцией клеток и признаками воспаления, вызванные Toxoplasma gondii:
- Абсцесс спинного мозга, адгезивный арахноидит
о Грибковый спондилит
о Саркоид → криптококковый спондилит с поражением спинного мозга
о Инфекции, вызванные Nocardia → основным синдромом является поражение дыхательных путей:
- В 50% случаев - гематогенная диссеминация
- Первичная инфекция ЦНС (5-7%)
о Системная красная волчанка → повышенный риск развития костно-суставного туберкулеза
о Инвазивные инфекционные поражения, вызванные грибами Aspergillus → 0-12% пациентов с ВИЧ-инфекцией, высокий уровень летальности в терминальные стадии СПИДа:
- Инфекции, вызванные Aspergillus → длительно существующая иммуносупрессия и большое число оппортунистических инфекций
- У больных СПИДом развивается острый инвазивный аспергиллез легких → быстрое прогрессирование локального процесса и гематогенная диссеминация
3. Течение заболевания и прогноз:
• Развитие у ВИЧ-положительных пациентов спондилодисцитов сопровождается высокими цифрами летальности
4. Лечение оппортунистических инфекций:
• Таргетная терапия в зависимости от причинного патогена
• Консервативное или хирургическое лечение спондилодисцита:
о Риск осложнений хирургического лечения спондилодисцита на фоне ВИЧ-инфекции не увеличивается
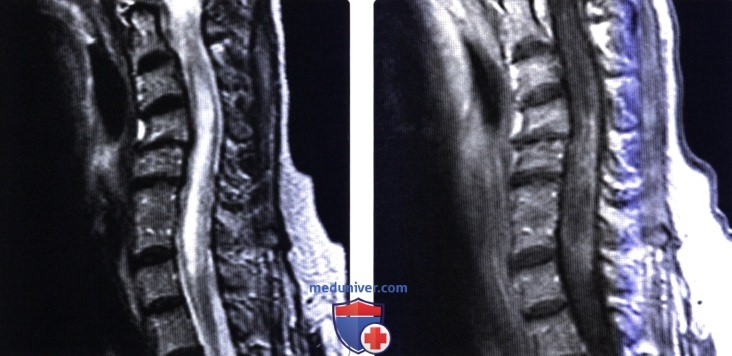
(Слева) Сагиттальный срез, Т2-ВИ: на протяжении шейного отдела спинного мозга отмечается гиперинтенсивность сигнала с диффузным увеличением объема спинного мозга, распространяющимся до грудного отдела и связанным с герпетической инфекцией. Мультисегментарное поражение с контрастным усилением сигнала свидетельствует в пользу непосредственного вирусного поражения паренхимы спинного мозга либо вторичного (после перенесенной вирусной инфекции) демиелинизирующего заболевания.
(Справа) Сагиттальный срез, Т1-ВИ с КУ: протяженное неравномерное, но в то же время неочаговое контрастное усиление сигнала спинного мозга от уровня С4 до С7-Т1. Распространенный отек спинного мозга и контрастное усиление сигнала в данном случае связан с герпетической инфекцией.
д) Диагностический поиск:
1. Помните:
• КТ/МРТ позвоночника и спинного мозга показана всем пациентам с иммунодефицитами и развивающейся неврологической симптоматикой
2. Нюансы интерпретации изображений:
• У пациентов с признаками деструктивного поражения позвоночника, особенно когда подозревается туберкулез, в круг дифференциальной диагностики должен обязательно включаться в т.ч. грибковый спондилит
е) Список использованной литературы:
1. Royer М etal: Mucormycosis in systemic autoimmune diseases. Joint Bone Spine. 81(4):303-7, 2014
2. Tan AC et al: Candida glabrata vertebral osteomyelitis in an immunosuppressed patient. Int J Rheum Dis. 17(2):229-З1, 2014
3. Berngard SC et al: Salmonella spinal infection: a rare case in a patient with advanced AIDS. J Int Assoc Provid AIDS Care. 12(4):241-4, 2013
4. Patkar D et al: Central nervous system tuberculosis: pathophysiology and imaging findings. Neuroimaging Clin N Am. 22(4):677-705, 2012
5. Nfoussi H et al: [Paraparesis and fever in a Tunisian woman: cryptococcal spondylitis with spinal involvement.] Med Trap (Mars). 70(1):85-7, 2010
6. Celik AD et al: Spondylodiscitis due to an emergent fungal pathogen: Blastoschi zomyces capitatus, a case report and review of the literature. Rheumatol Int. 2900:1237-41, 2009
Читайте также:

