Резистентность к препаратам вич бланк на анализ
Обновлено: 13.05.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Напоминаем вам, что самостоятельная интерпретация результатов недопустима, приведенная ниже информация носит исключительно справочный характер.
Антитела к ВИЧ-1/2 и антиген ВИЧ-1/2 (HIV Ag/Ab Combo): показания к назначению, правила подготовки к сдаче анализа, расшифровка результатов и показатели нормы.
ВИЧ-инфекция - инфекционная болезнь, развивающаяся в результате многолетнего персистирования (постоянного пребывания) в лимфоцитах, макрофагах и клетках нервной ткани вируса иммунодефицита человека (далее - ВИЧ), характеризующаяся медленно прогрессирующим дефектом иммунной системы, который приводит к гибели больного от вторичных поражений, описанных как синдром приобретенного иммунодефицита (далее - СПИД).
ВИЧ (Вирус Иммунодефицита Человека) – вирус, относящийся к семейству ретровирусов (семейство РНК-содержащих вирусов, заражающих преимущественно позвоночных), который поражает клетки иммунной системы человека. Через несколько недель с момента заражения начинают вырабатываться антитела к ВИЧ.
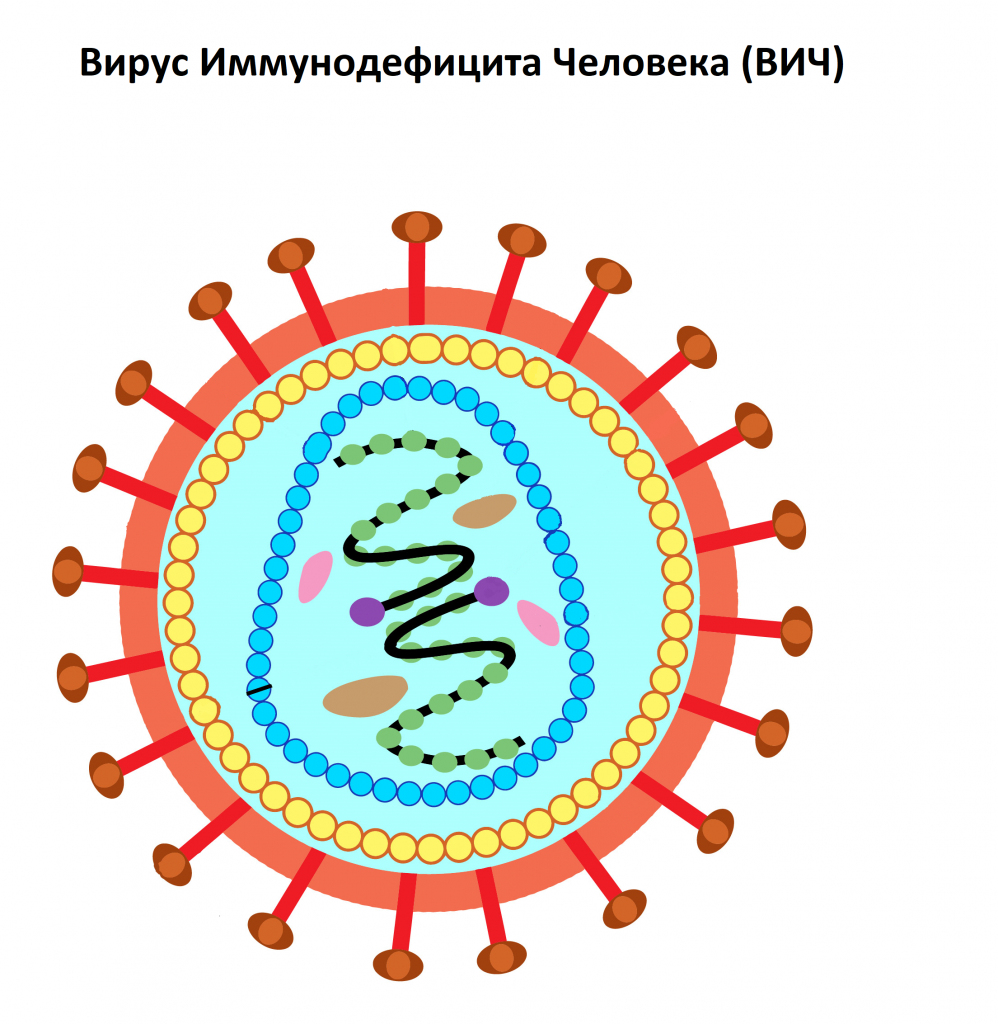
Показания на проведение исследования
Показаниями для назначения анализа является подготовка к госпитализации и плановому оперативному вмешательству. В профилактических целях следует провести исследование при подозрении на заражение при половом контакте. В первую очередь это касается лиц групп риска: употребляющих наркотики, вводимые внутривенно, часто меняющих половых партнеров и не использующих средств защиты.
Вирус иммунодефицита человека размножается в организме человека достаточно медленно, и количественный результат в отношении антигенов и антител к вирусу можно получить, как правило, не ранее чем через 3-6 недель после инфицирования. При этом клинические симптомы заболевания еще отсутствуют.
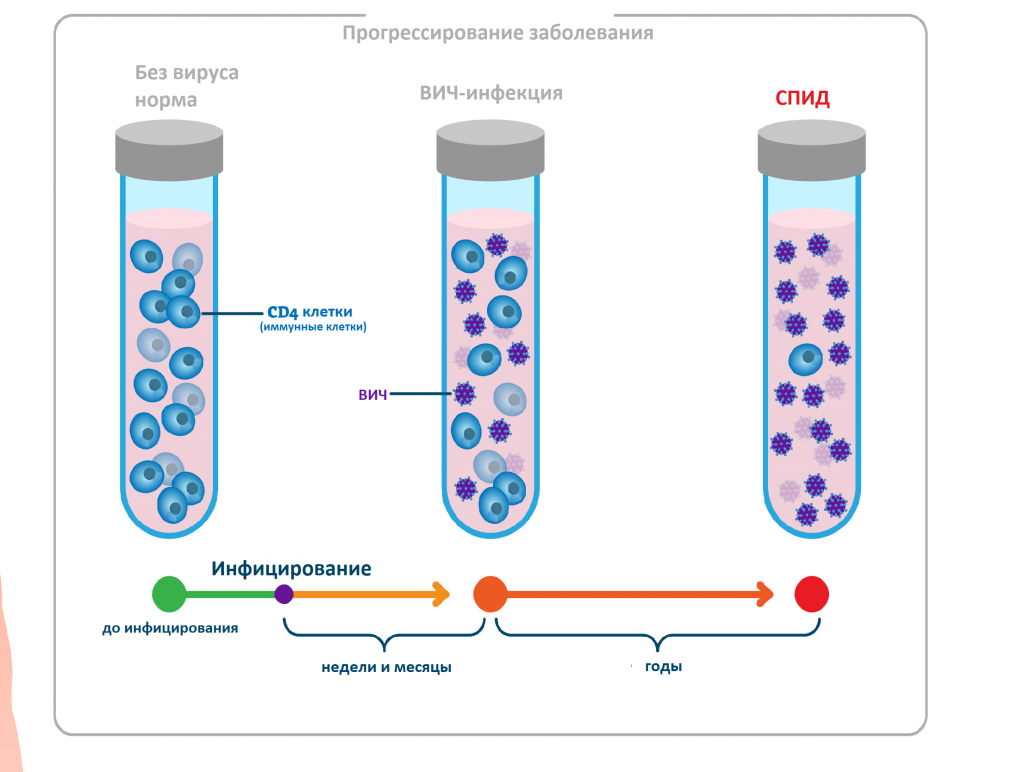
Через три месяца антигены ВИЧ и антитела к вирусу определяются практически у всех заболевших. Благодаря появлению новых комбинированных тест-систем четвертого поколения получение точного результата качественного анализа на ВИЧ-инфекцию возможно уже через две недели с момента попадания вируса в организм. При этом исследовании выявляют антиген р24 ВИЧ – белок вирусного капсида (внешней оболочки вируса).
Анализ на антитела к ВИЧ 1/2 и антиген ВИЧ 1/2 назначают на этапе планирования и при ведении беременности, когда возможна передача вируса плоду. Анализ проводят и после родов, поскольку ребенок ВИЧ-положительной матери может быть инфицирован во время прохождения через родовые пути и при кормлении грудью.

Лихорадка, потеря веса без объективных причин, повышенная утомляемость, увеличение регионарных лимфатических узлов, потливость, особенно в ночное время, длительный кашель, диарея – эти устойчивые клинические симптомы неясного происхождения, отмечаемые в течение 2-3 недель, также служат показанием к проведению исследования на антитела к ВИЧ 1/2 и антиген ВИЧ 1/2.
Кожные проявления также могут быть симптомом ВИЧ-инфекции, поскольку развиваются на фоне ослабления иммунитета. К их числу относится рецидивирующая герпетическая сыпь, поражающая обширные участки кожи, полость рта, половые органы. Герпес поражает и глубокие слои кожи с развитием язвенно-некротической формы. Образуются язвы и эрозии с последующим образованием рубцов, которых не бывает при обычном герпесе.
Еще один характерный симптом ВИЧ-инфекции – волосатая лейкоплакия, которая связана с активацией латентной инфекции, вызванной вирусом Эпштейна-Барр (что свидетельствует об иммуносупрессии). Заболевание проявляется нитевидными образованиями белого цвета с дальнейшим ороговением пораженных участков языка и слизистой оболочки рта.
Обширные грибковые поражения (в первую очередь дрожжевыми грибками рода Candida) также служат типичным признаком, сопровождающим ВИЧ-инфекцию. Сначала кандидоз поражает слизистую оболочку рта и пищевода, затем распространяется на слизистые желудочно-кишечного и мочеполового тракта. При этом формируются обширные очаги, характеризующиеся болезненностью и склонностью к изъязвлению.
ВИЧ-инфекция может сопровождаться развитием обширного папилломатоза. У ВИЧ-инфицированных женщин папилломы цервикального канала склонны быстро вызывать рак шейки матки.
СПИД-индикаторным заболеванием служит саркома Капоши – многоочаговая сосудистая опухоль, которая поражает кожные покровы и слизистые оболочки. Ее очаги в виде красноватых или буроватых узелков и бляшек сливаются, быстро распространяясь по всему телу. Со временем они образуют опухолевые поля, которые изъязвляются и нагнаиваются.
К числу патологических состояний, которые почти у всех пациентов сопровождают ВИЧ-инфекцию, относят полиаденопатию (увеличение лимфатических узлов). Как правило, в первую очередь увеличиваются под- и надключичные, подбородочные, околоушные и шейные лимфоузлы. В дальнейшем к ним может присоединяться увеличение паховых и бедренных лимфатических узлов. Они могут быть мягкими или плотными на ощупь, безболезненными и подвижными. Иногда несколько лимфоузлов сливаются, образуя своеобразный конгломерат. Воспаление двух и более групп лимфоузлов считают признаком генерализованной лимфаденопатии. Поражение лимфатических узлов может наблюдаться в течение нескольких лет, при этом периоды обострения сменяются ремиссией.
К легочным заболеваниям, сопровождающим ВИЧ-инфекцию, относят туберкулез и пневмонию.
Анализ на антигены и антитела к ВИЧ рекомендуют сделать, если у пациента выявлены заболевания, передаваемые половым путем (сифилис, хламидиоз, гонорея, генитальный герпес, бактериальный вагиноз).
ЖПС — жидкая питательная среда
КУМ-МБТ — кислотоустойчивые микобактерии
ЛЖВ — люди, живущие с ВИЧ
ЛМ — люминесцентная микроскопия
ЛУ-МБТ — устойчивость микобактерий туберкулеза
МБТ — микобактерии туберкулеза
МГМ — молекулярно-генетический метод
МЛУ— множественная устойчивость к лекарствам
МЛУ-ТБ — туберкулез c МЛУ
ПАСК — парааминосалициловая кислота
ППС — плотная питательная среда
ПТП — противотуберкулезные препараты
ТЛЧ — тест чувствительности к лекарствам
ШЛУ — широкая устойчивость к лекарствам
ШЛУ-ТБ — туберкулез с ШЛУ
Лечение больных МЛУ-ТБ более сложное, длительное (до 2 лет), дорогостоящее и менее эффективное, чем лечение пациентов с ТБ, чувствительным к лекарствам. Доля успешно пролеченных пациентов с ЛЧ-ТБ составляет 83% (мировая когорта 2014 г.), в то время как эффективность лечения больных МЛУ-ТБ составляет лишь 52% (мировая когорта 2013 г.), и только 28% для ТБ с широкой устойчивостью к лекарствам (ШЛУ-ТБ) [2]. Именно поэтому в настоящее время активно разрабатываются и внедряются в практику краткосрочные режимы химиотерапии [3—5]. В рекомендации ВОЗ 2016 г. вошли новый, более короткий режим лечения больных МЛУ-ТБ, а также новые методы выявления резистентности к препаратам второго ряда [6].
Результаты исследований о взаимосвязи ВИЧ-инфекции и наличии устойчивости к лекарствам у больных ТБ несколько противоречивы. По некоторым данным, МЛУ-ТБ встречается достоверно чаще у пациентов с ВИЧ-инфекцией [7—9]. Другие исследования не выявили достоверной связи между частотой развития МЛУ-ТБ и ВИЧ-инфекцией [10, 11]. Однако данные одного из последних метаанализов, посвященных этой проблеме, показали корреляцию между МЛУ-ТБ и ВИЧ-инфекцией — риск наличия МЛУ-ТБ у ВИЧ-инфицированных выше на 24% [12].
Существует несколько теорий, объясняющих взаимосвязь MЛУ-ТБ и ВИЧ-инфекции: теория наличия мальабсорбции у инфицированных ВИЧ пациентов [13, 14]; теория особенностей фармакокинетики противотуберкулезных препаратов (ПТП), в том числе в связи с межлекарственными взаимодействиями [15]; теория менее благополучного социального статуса больных ВИЧ-инфекцией, влияющего на полноту соблюдения схемы назначенного лечения [16]; теория о том, что у больных с коинфекцией (ВИЧ-и/ТБ) удельный вес штаммов микобактерий ТБ (МБТ), обладающих высокой жизнеспособностью, в 2 раза выше, чем у лиц без ВИЧ-инфекции, и МБТ в условиях бурного размножения за счет накопления мутаций может быстрее формировать устойчивость к лекарствам [17]. Представленные теории вряд ли можно отнести к ведущим, так как доказано, что пациенты с сочетанной инфекций в наибольшей степени отличаются от больных ТБ с негативным статусом по ВИЧ именно по частоте развития первичной, чем вторичной устойчивости МБТ к лекарствам (ЛУ-МБТ) [14, 16].
Вероятно, более значительным для взаимосвязи ВИЧ-инфекции и МЛУ-ТБ является то, что люди, живущие с ВИЧ (ЛЖВ), чаще попадают в окружение с высоким уровнем МЛУ-ТБ (стационары, места лишения свободы) и за счет иммунодефицита у них инфицирование происходит чаще и быстрее, чем у людей с ненарушенным иммунитетом. К тому же активация МБТ-инфекции ВИЧ-инфицированных происходит в ближайшее время в отличие от не инфицированных ВИЧ пациентов, у которых ТБ чаще обусловлен реактивацией латентной туберкулезной инфекции, приобретенной в период, когда МЛУ-ТБ не был распространен столь широко [18, 19].
В России проблема ЛУ-МБТ особенно актуальна. По данным ВОЗ, Россия относится к одной из стран с наибольшим бременем МЛУ-ТБ [2].
Официальной статистики о распространенности МЛУ-ТБ среди ЛЖВ в России нет, так как такая когорта пациентов пока не выделяется. Имеются лишь данные по отдельным госпитальным и региональным исследованиям. Так, по данным А.М. Пантелеева [21], МЛУ-МБТ на фоне ВИЧ-инфекции регистрируется в 56,1% случаев среди всех наблюдавшихся в специализированном отделении туберкулеза у больных ВИЧ-инфекцией городской туберкулезной больницы № 2 Санкт-Петербурга и Санкт-Петербургском городском центре по профилактике и борьбе со СПИД и инфекционными заболеваниями пациентов. Согласно исследованиям И.В. Викторовой и соавт. [22] МЛУ среди ВИЧ-инфицированных с впервые установленным диагнозом ТБ за 2013 г. выявлена в 53,8% в Кемерове и в 56,5% в Новокузнецке.
В то же время доказано, что у больных ТБ на фоне ассоциированной с ВИЧ иммуносупрессии отсутствие данных о первичной ЛУ-МБТ повышает в 4,5 раза риск смерти в течение первых 3 мес от начала заболевания [21], что делает методы быстрого выявления устойчивости к лекарствам у подобных больных ключевым компонентом успешности лечения.
По данным Федерального научно-методического центра по профилактике и борьбе со СПИДом, основные эпидемиологические показатели Пермского края по ВИЧ-инфекции в 2015 г. следующие: заболеваемость 132,5 на 100 тыс., пораженность 879,4 на 100 тыс. населения. Таким образом, по основным показателям развития эпидемии ВИЧ-инфекции Пермский край превышает аналогичные среднероссийские показатели [23].
Цель исследования — в регионе с высокой пораженностью ВИЧ-инфекцией (Пермский край) изучить частоту обнаружения и спектр ЛУ-МБТ у впервые выявленных больных ТБ в зависимости от ВИЧ-статуса.
Материалы и методы
Обследование пациентов выполняли в рамках стандартного алгоритма обследования пациентов с подозрением на ТБ после подписания ими информированного согласия на обследование и лечение в данном учреждении. Анализ результатов проведен ретроспективно по данным медицинской документации.

Данные о результатах обследования каждого пациента вносили в специально разработанную базу данных электронной таблицы Таблица 1. Характеристика ЛУ-МБТ у больных ТБ в зависимости от статуса по ВИЧ по результатам ТЛЧ Примечание. R — рифампицин; Н — изониазид; МЛУ— множественная устойчивость к лекарствам; ШЛУ — широкая устойчивость к лекарствам. Microsoft Excel 2003. Кроме информации об исследовании на МБТ из медицинской документации вносили все сведения о пациенте, которые можно получить при сборе анамнеза и обычном обследовании.
Статистический анализ осуществляли с помощью программы Statistica v.6, а также использовали вычислительные возможности электронной таблицы Excel. Для оценки различий значений в группах сравнения использовали для качественных показателей критерий χ 2 и для количественных — дисперсионный анализ. Различия считали достоверными при p
Результаты и обсуждение
Сравнительный анализ выявления МБТ у больных ТБ с различным статусом по ВИЧ. При анализе выявления МБТ классическими фенотипическими методами (ЛМ и посев на ППС) установлено, что у больных без ВИЧ-инфекции обнаружить КУМ-МБТ с помощью ЛМ удавалось достоверно чаще, чем у ЛЖВ, — у 116 (32,8%) и 43 (24,2% соответственно; р=0,032), а информативность культуральной диагностики оказалась сопоставимой в обеих группах — у 202 (57,1%) и 108 (60,7%; р>0,05).

Частота развития и спектр ЛУ-МБТ у больных ТБ в зависимости от статуса по ВИЧ. Тест определения ЛУ-МБТ (тест чувствительности к лекарствам — ТЛЧ) методом последовательных разведений на ППС Левенштейна—Йенсена получен у 108 больных ВИЧ-и/ТБ и 197 больных ТБ (у 100 и 97,5% от числа больных с положительным результатом посева). Чувствительность ко всем определяемым препаратам сохранена только у 23 (19,5%) больных ВИЧ-и/ТБ и у 85 (43,2%) больных ТБ (р=0,0001). В табл. 1, 2 Таблица 2. Частота выявления устойчивости МБТ к отдельным ПТП в зависимости от статуса ВИЧ пациентов по результатам ТЛЧ Примечание. ПАСК — парааминосалициловая кислота. представлены частота развития и спектр ЛУ-МБТ у больных ТБ в зависимости от статуса по ВИЧ.
Результаты анализа свидетельствуют, что устойчивость к рифампицину ассоциировалась с устойчивостью к изониазиду у всех больных с ТБ и у 97,2% больных ВИЧ-и/ТБ. Отмечен колоссально высокий уровень первичной МЛУ-МБТ в обеих группах, при этом число ВИЧ-инфицированных пациентов с МЛУ-ТБ оказался практически на 1/3 больше, чем среди лиц без ВИЧ-инфекции (60,2 и 41,6%; р<0,001). Практически в 2 раза чаще регистрировали ШЛУ-МБТ среди ЛЖВ, однако ввиду небольшого числа случаев в абсолютных числах достоверных различий не получено (7,63 и 4,06%; р>0,05).
При сравнительном анализе устойчивости МБТ к отдельным препаратам практически по каждому из них (исключая канамицин и ПАСК) выявлены достоверные различия по частоте выявления в сравниваемых группах. Особенно настораживает выявленный уровень устойчивости к офлоксацину как маркеру неблагоприятного исхода при лечении больных МЛУ-ТБ [24]. Устойчивость к фторхинолону выявлена у 22,9% больных ВИЧ-и/ТБ и у 12,2% больных ТБ (р<0,05).
Сравнительный анализ ЛУ-МБТ у больных с сочетанной инфекцией (ВИЧ-и/ТБ) при фенотипических методах тестирования и МГМ. Среди 178 больных с сочетанной инфекцией (ВИЧ-и/ТБ) МБТ выявлены методом ЛМ у 43, МГМ — у 127, посевом на ППС Левенштейна—Йенсена — у 108, посевом на ЖПС — у 104.
ЛУ-МБТ методом последовательных концентраций на ЖПС в автоматизированной системе учета роста микроорганизмов BACTEC MGIT 960 определена у 104 больных ВИЧ-и/ТБ. Среди тестируемых устойчивость к пиразинамиду отмечена у 38 (36,5%) больных ВИЧ-и/ТБ (на ППС тестирование не проводится). Одновременно устойчивость к рифампицину, изониазиду, офлоксацину, этамбутолу определена на ППС и ЖПС у 93 пациентов. Отмечено совпадение устойчивости к офлоксацину на ППС и ЖПС во всех случаях. Дискордантные результаты получены по рифампицину у 1, по этамбутолу у 2, по изониазиду у 3 больных.
Генетического материала оказалось достаточно для выявления мутаций, ответственных за устойчивость к ПТП, лишь у 72 (56,6%) из 127 пациентов с положительным результатом выявления ДНК МБТ. Одновременно ЛУ-МБТ к рифампицину и изониазиду тестирована фенотипическими (методом последовательных разведений на ППС Левенштейна—Йенсена) и МГМ у 61 больного.
Совпадение результатов определения устойчивости к изониазиду отмечено у 53 (86,8%) больных, в 8 случаях дискордантность результатов: в 3 — устойчивость к изониазиду, определяемая фенотипически, при сохраненной чувствительности МГМ, и в 5 — чувствительность к изониазиду, определяемая фенотипически при регистрации устойчивости МГМ.
Совпадение результатов определения устойчивость к рифампицину отмечено у 54 (88,5%) больных, в 7 случаях — дискордантность результатов: в 5 — устойчивость к рифампицину, определяемая фенотипически при сохраненной чувствительности МГМ, и в 2 —к рифампицину, определяемая фенотипически, при регистрации устойчивости МГМ.
Полученные данные согласуются с результатами большинства исследований, посвященных дискордантности результатов различных методов определения ЛУ-МБТ, которые показывают невысокую частоту расхождения результатов ТЛЧ по отношению к изониазиду и рифампицину. Однако, по данным литературы, чаще ложноотрицательные результаты ТЛЧ к рифампицину встречаются при использовании фенотипических методов, а к изониазиду — МГМ [25—28].
Внедрение АРВ препаратов в практику лечения ВИЧ-инфекции позволило значительно увеличить продолжительность и улучшить качество жизни пациентов. Однако возникновение устойчивых штаммов ВИЧ – одна из основных причин неэффективности АРВ терапии.
Быстрое развитие устойчивости обусловлено высокой скоростью репликации ВИЧ, а также очень большой частотой ошибок репликации, совершаемых обратной транскриптазой ВИЧ. Это приводит к частому появлению мутаций и постоянному образованию новых штаммов вируса даже в отсутствии лечения. Под давлением АРВ препаратов происходит селекция устойчивых вариантов вируса, которые начинают активно реплицироваться, занимая доминирующее положение. Первый индикатор активации ВИЧ на фоне развития лекарственной устойчивости – увеличение вирусной нагрузки. При сохранении прежней схемы терапии ВИЧ-инфекция быстро прогрессирует. Для оптимальной модификации схемы лечения необходимо знать профиль устойчивости ВИЧ у пациента.
Исследования, направленные на определение резистентности ВИЧ к лекарственным препаратам, разделяют по принципу действия на две большие группы: основанные на фенотипировании (определении свойств) или генотипировании (анализ генома) вируса. С помощью фенотипических тестов оценивают способность вируса расти в присутствии различных противовирусных препаратов in vitro. Для этого определяют показатель IC50, показывающий концентрацию препарата, необходимую для подавления вирусной репликации на 50%. В результате теста оценивают кратность увеличения IC50 по сравнению с данным показателем для дикого вируса. В настоящее время сертифицированы и доступны для использования методы на основе рекомбинантных вирусов. Ввиду большей трудоемкости и высокой себестоимости фенотипические методы в рутинной практике в РФ не используют. Основным методом определения лекарственной устойчивости ВИЧ в РФ является выявление специфических мутаций устойчивости в генах ВИЧ, которые являются мишенями для современных АРВ препаратов (гены обратной транскриптазы, протеазы, интегразы, поверхностных белков gp41 и gp120) методом определения нуклеотидной последовательности (секвенирования) генома ВИЧ.
Результатом исследования лекарственной устойчивости ВИЧ с помощью генотипического подхода является список выявленных мутаций в геноме вируса, приводящих к фенотипическим изменениям, которые выражаются в способности вируса к репликации в присутствии АРВ препаратов. На основании этого подбирается комбинация препаратов для наиболее эффективной терапии.
Исследование лекарственной устойчивости ВИЧ к АРВ препаратам имеет ряд ограничений, которые необходимо учитывать, оценивая результаты исследования и проводя его интерпретацию:
Показания к обследованию для определения лекарственной устойчивости ВИЧ
Для данного исследования лаборатория принимает следующий биоматериал:
Подготовка к исследованию
Взятие крови проводится не ранее, чем через 3 часа после последнего приема пищи, допускается употребление негазированной воды.
Услуга оформляется только дозаказом к услуге 032102 в течение 14 к.д. от даты регистрации услуги 032102, если вирусная нагрузка составила более 1000 копий/мл.
Метод исследования
ВНИМАНИЕ! Оформление заказа на выполнение исследований для определения резистентности к АРВП возможно с помощью двух алгоритмов.
Алгоритм 1. Заказывается количественное исследование 032102 РНК HIV (тип 1), при выявлении концентрации РНК ВИЧ более 1 000 копий/мл оформляется дозаказ в течение 14 к.д. от даты регистрации указанной услуги на исследование:
- 032106 РНК HIV-1, опред. резистентности ВИЧ к ингибиторам протеазы и обратной транскриптазы
Алгоритм 2. В составе комплексной программы:
- 300250 Количественное определение РНК HIV-1 и мутации резистентности ВИЧ к ингибиторам протеазы и обратной транскриптазы;
- В случае, если концентрация РНК ВИЧ в плазме крови составляет менее 1 000 копий/мл, определение мутаций резистентности выполняться не будет, стоимость будет взиматься только за выполненное исследование (Количественное определение РНК HIV-1).
В настоящее время для лечения больных ВИЧ-инфекцией используется антиретровирусная терапия (АРТ). АРТ не позволяет полностью удалить ВИЧ из организма, однако останавливает размножение вируса, что приводит к восстановлению иммунитета, предупреждению развития или регрессу вторичных заболеваний, сохранению или восстановлению трудоспособности пациента, увеличению продолжительность жизни пациента.
Несвоевременный прием препаратов, перерывы в применении, либо прекращение терапии приводят к развитию устойчивости (резистентности) ВИЧ к антиретровирусным препаратам (АРВП). Распространение резистентности ВИЧ к АРВП приводит к снижению эффективности лечения, увеличению смертности от ВИЧ/СПИД и росту стоимости антиретровирусной терапии.
Снижение чувствительности ВИЧ к АРТ обусловлено возникновением мутаций в генах-мишенях АРТ (кодирующих нуклеотидные последовательности ревертазы, протеазы, интегразы, поверхностных и структурных белков). Резистентные варианты ВИЧ могут возникнуть за счет развития мутаций вируса у пациентов, принимающих АРТ (приобретенная резистентность), или быть переданы неинфицированным ранее людям от лиц, у которых такие варианты присутствуют (первичная, передаваемая резистентность). Как первичная, так и приобретенная резистентность ВИЧ может приводить к снижению эффективности терапии ВИЧ-инфекции как у отдельных пациентов, так и в популяции в целом, ограничивает возможности выбора АРВП.
Вирусологическими критериями неэффективности терапии являются:
- отсутствие снижения концентрации РНК ВИЧ до недетектируемого уровня через 24 недели лечения, если не было перерыва в приеме препарата;
- выявление РНК ВИЧ (в двух определениях с интервалом 1 месяц) после исходной супрессии до недетектируемого уровня, если не было перерыва в приеме препарата.
- Данное исследование предназначено для определения первичной или приобретенной резистентности к ингибиторам протеазы и обратной транскриптазы с целью повышения эффективности АРВТ.
Показания к исследованию:
- ВИЧ-инфицированные при неэффективности АРТ, если нет других явных причин неэффективности терапии (нарушение приема АРВ препаратов, нарушение всасывания препарата);
- ВИЧ-инфицированные в период острой инфекции перед началом АРТ, если заражение ВИЧ произошло от партнера с неэффективной АРТ. В остальных случаях острой инфекции проведение исследования до начала АРТ не рекомендуется до тех пор, пока уровень первичной резистентности в регионе не достигнет 5%.
Исследование позволяет определить резистентность ВИЧ к препаратам:
| Тип препарата | Название препарата |
|---|---|
| Ингибиторы протеазы (Protease inhibitors) | Артазанавир (ATV/r) |
| Дарунавир (DRV/r) | |
| Фосампренавир (FPV/r) | |
| Индинавир (IDV/r) | |
| Лопинавир (LPV/r) | |
| Нелфинавир (NFV/r) | |
| Саквинавир (SQV/r) | |
| Типранавир (TPV/r) | |
| Нуклеозидные ингибиторы обратной транскриптазы (Nucleoside RTI) | Тенофовир (TDF) |
| Эмтрицитабин (FTC) | |
| Зидовудин (AZT) | |
| Ставудин (D4T) | |
| Диданозин (DDI) | |
| Ламивудин (3TC) | |
| Абакавир (ABC) | |
| Ненуклеозидные ингибиторы обратной транскриптазы (Non-Nucleoside RTI) | Рилпивирин (RPV) |
| Эфавиренц (EFV) | |
| Этравирин (ETR) | |
| Невирапин (NVP) |
Аналитическая чувствительность теста составляет 1000 копий/мл.
По результатам проведенного исследования врач получает информацию о наличии мутаций устойчивости к ингибиторам протеазы, нуклеозидным и ненуклеозидным ингибиторам обратной транскриптазы, а также информацию по каждой аминокислотной позиции, ассоциированной с мутацией лекарственной устойчивости.
При единовременном заказе нескольких услуг, услуга по сбору биоматериала оплачивается только один раз.
• ЧТО ТАКОЕ РЕЗИСТЕНТНОСТЬ?
• КАК РАЗВИВАЕТСЯ РЕЗИСТЕНТНОСТЬ?
• ТИПЫ РЕЗИСТЕНТНОСТИ
• ФЕНОТИПИЧЕСКОЕ ТЕСТИРОВАНИЕ
• ГЕНОТИПИЧЕСКОЕ ТЕСТИРОВАНИЕ
• ВИРТУАЛЬНЫЙ ФЕНОТИП
• КРОСС-РЕЗИСТЕНТНОСТЬ
• ПРОБЛЕМЫ, СВЯЗАННЫЕ С ТЕСТИРОВАНИЕМ НА РЕЗИСТЕНТНОСТЬ
Всего одна мутация способна сделать ВИЧ резистентным к определенным препаратам. Так происходит при приеме 3TC (Эпивир) и не-нуклеозидных ингибиторов обратной транскриптазы (ННИОТ). Но ВИЧ должен произвести ряд мутаций, чтобы развить резистентность к другим препаратам, включая большинство ингибиторов протеазы.
Наилучший способ предотвратить появление резистентности – принимать сильные АРВ-препараты. Если ты пропускаешь прием препаратов, ВИЧ размножается гораздо легче. Будет появляться больше мутаций, некоторые из которых могут являться причиной резистентности.
Если тебе необходимо прекратить прием какого-либо одного или всех АРВ-препаратов, проконсультируйся со своим врачом. Возможно, тебе потребуется прекратить прием одних препаратов раньше, чем всех остальных. Если ты прекратишь прием препарата в тот момент, когда вирус находится под контролем, должна остаться возможность возобновить прием этого препарат в будущем.
ТИПЫ РЕЗИСТЕНТНОСТИ
Существует три типа резистентности:
• Клиническая резистентность: ВИЧ быстро размножается в твоем организме, несмотря на прием АРВ.
• Фенотипическая резистентность: ВИЧ размножается в пробирке, когда добавляются АРВ-препараты.
• Генотипическая резистентность: Генетический код ВИЧ имеет мутации, которые связаны с резистентностью препаратам.
Клиническая резистентность появляется при повышенной вирусной нагрузке, пониженном количестве СД4 или при наличии оппортунистических инфекций (см. Брошюра 500). С помощью лабораторных испытаний можно измерить фенотипическую и генотипическую резистентность.
Фенотипический тест стоит около $800. Раньше требовалось не меньше месяца, чтобы получить результаты. Новые фенотипические тесты дают результат несколько быстрее.
ВИРТУАЛЬНЫЙ ФЕНОТИП
Этот анализ – на самом деле интерпретации результатов генотипического тестирования. Во-первых, проводится генотипическое тестирование образца. Результаты фенотипических анализов других образцов вируса, близких по генотипу, отбираются в базе данных. С помощью этих образцов можно понять наиболее вероятные пути развития вируса. Виртуальный фенотип составляется быстрее и стоит дешевле, чем фенотипическое тестирование.
Читайте также:

