Роль химико-токсикологического анализа в центрах по лечению отравлений
Обновлено: 25.04.2024
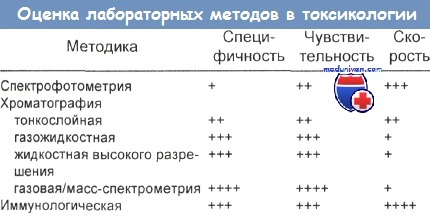
Методы токсикологического скрининга (анализа) и их эффективность
Использовать токсикологический анализ без понимания его ограничений опасно. Токсикологический скрининг характеризуется хорошей специфичностью. Специфичность пропорциональна процентной доле пациентов, в организме которых токсичные вещества присутствуют, но результат анализа отрицательный (хорошая специфичность означает, что тест дает мало ложноположительных результатов).
Однако чувствительность его низка, поскольку многие случаи присутствия токсичных веществ не выявляются. Чувствительность — это доля больных с данным токсином, для которых получен положительный результат (если она высока, ложноотрицительных результатов мало).
Диагностическая ценность отрицательного результата (т. е. доля истинно отрицательных результатов среди всех отрицательных) составляет около 40 %. Для повышения чувствительности и диагностической ценности скрининга необходимы совершенствование аналитических методов, тесное взаимодействие между врачами и лабораториями, правильное взятие проб и понимание ограничений и ценности конкретных тестов.
Ограничения методов токсикологического скрининга
Для скрининга токсинов токсикологические лаборатории применяют несколько методов, поскольку единственного точного и недорогого метода для выявления всех токсинов не существует. Эти методы различаются по стоимости, точности, сложности, скорости и специфичности. Надежность отдельного теста зависит от опыта аналитика, оборудования, метода и числа обрабатываемых заказов.
Трудности возникают в связи с изменениями биологических жидкостей при их хранении, переносом веществ из пробирки в пробирку и стандартами, используемыми при анализе.
Порча колонок для газожидкостной хроматографии приводит к появлению неизвестных остатков, а ионизация газов чревата расщеплением химикатов. Кроме того, лабильные метаболиты подвергаются химическим изменениям, зависящим от используемой аналитической методики. Таким образом, для правильного использования лаборатории необходимо знакомство с ее специфическими потребностями, процессами и ограничениями. Для интерпретации результатов токсикологического скрининга важно знать ответы на следующие вопросы.
1. Какой метод используется для каждой категории веществ и какова его специфичность?
2. Какие вещества выявляются при токсикологическом скрининге и какие его варианты доступны (например, специально для агентов, вызывающих кому, эпилептические припадки; психоактивных средств)?
3. Какая информация необходима в запросе?
4. Какие образцы лучше всего подходят для конкретного анализа?
5. Какие тесты дают количественные и качественные результаты и насколько быстро?
Сравнение аналитических методов токсикологического скрининга
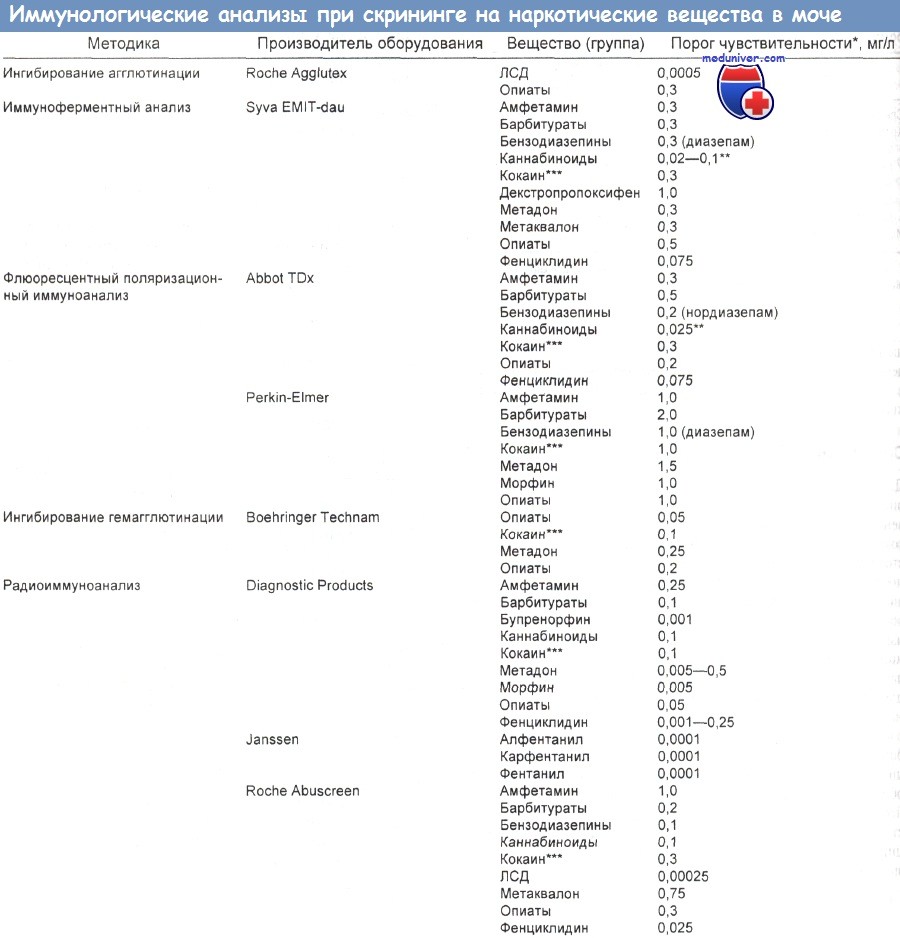
Чаще всего используемая в качестве аналитического метода хроматография основана на разделении веществ при прохождении потока жидкости или газа через твердую (стационарную) фазу, содержащую неизвестный агент. Иммуноанализ (иммуноферментный, радиоиммуноанализ) чувствителен, но менее специфичен, чем хроматография или масс-спектрометрия.
Тонкослойная хроматография
Тонкослойная хроматография (ТСХ) — это простой и недорогой метод качественного скрининга, не дающий количественных результатов. Разделение фракций основано на различной абсорбции веществ при прохождении растворителя через стационарный сорбент (обычно кремниевую кислоту или оксид алюминия). Каждому веществу соответствуют характерное расстояние миграции после нанесения образца на исходную линию и применения соответствующего растворителя. Анализ занимает 2 ч, а его результаты должны интерпретироваться опытным персоналом.
В продаже имеются системы ТСХ для токсикологического скрининга, которые требуют меньше профессиональной подготовки, чем необходима для стандартной ТСХ.
Ультрафиолетовая спектрофотометрия
Ультрафиолетовая спектрофотометрия (УФС) — это простой, экономичный количественный метод, позволяющий выявить токсические уровни ацетаминофена и салицилата в крови, а также повышенный уровень фенотиазина в моче.
Однако точность результата сильно снижается при потреблении нескольких веществ, что в настоящее время ограничивает применимость данного анализа.
Газожидкостная хроматография
Газожидкостная хроматография (ГЖХ) — очень точный и специфичный метод, но требующий довольно много времени. Жидкий или растворенный образец впрыскивают в колонку, он переводится в пар нагреванием. Поток инертных газов пофракционно изгоняет образец из колонки, и появление на выходе различных фракций регистрируется химическими детекторами.
Сравнение времени удержания и площади пиков с известными стандартами позволяет идентифицировать вещества и определить их количества. Этим методом эффективно определяется уровень в крови летучих жидкостей (метанола, этанола, этиленгликоля).
Жидкостная хроматография высокого давления (разрешения)
Жидкостная хроматография высокого разрешения (ЖХВР) по скорости, специфичности и стоимости сходна с газожидкостной хроматографией, но позволяет определить не только летучие вещества. Высокое давление (7000—42 000 кПа) облегчает движение образца через колонку, что способствует разделению сложных соединений, включая конъюгированные метаболиты.
Радиоиммуноанализ
Радиоиммуноанализ самый медленный и дорогой метод, но зато очень точный. Смешивание известных количеств специфичного к веществу антитела с этим же веществом, несущим радиоактивную метку, позволяет анализировать осадок с помощью счетчиков гамма-квантов. Уровень излучения обратно пропорционален количеству выявляемого вещества. Этот тест прекрасно подходит для определения крайне низких концентраций, например каннабинолов, ЛСД, дигоксина, параквата.
Иммуноферментный анализ
Быстрый, дорогой и простой метод, обеспечивающий среднюю точность и специфичность результатов, иммуноферментный анализ (ИФА), основан на том, что количество присутствующего в образце вещества пропорционально степени ингибирования реакции фермента с субстратом. Известное количество искомого вещества метят, химически присоединяя к ферменту.
Специфичные к веществу антитела, добавляемые к образцу, связывают этот комплекс, снижая тем самым его ферментативную активность. Свободное вещество в составе образца конкурирует с тем, что помечено ферментом, а это ограничивает вызываемую антителом инактивацию последнего.
Ферментативная активность, коррелирующая с концентрацией вещества в образце, измеряется по изменению поглощения, происходящему при каталитическом действии фермента на субстрат. ИФА предпочтительнее радиоиммунологического метода в неотложных ситуациях благодаря своей простоте и быстроте получения данных о концентрации токсичного агента.
При его использовании не нужна сложная стадия разделения, обязательная для последнего метода. В мелких лабораториях применяется система st (single test) с компактным спектрофотометром, а в крупных больницах — система dan (drugs of abuse), предназначенная специально для случаев токсикомании. Отрицательный результат, впрочем, не исключает присутствия очень малых количеств искомого агента.
Перекрестные реакции с антителами, способные привести к ложноположительному результату, дают следующие вещества:
• наркотики:
маковое семя,
декстрометорфан,
хлорпромазин,
дифеноксилат;
• амфетамины:
эфедрин,
фенилэфрин,
псевдоэфедрин,
N-ацетилпрокаинамид,
хлорохин,
прокаинамид;
• фенциклидин:
декстрометорфан,
дифенгидрамин,
хлорпромазин,
доксиламин,
тиоридазин.
Самая распространенная причина ложноположительного результата — перекрестная реакция антитела с веществом, которое по структуре сходно с искомым агентом, например с компонентами макового семени, включающими опийные алкалоиды, что дает положительный результат скрининга на опиаты.
Хорошо известна также способность противозастойных капель для носа, в частности эфедрина и фенилпропаноламина, показывать при скрининге мочи положительную реакцию на амфетамины. К такому ложноположительному результату может привести перекрестная реакция антител с L-эфедрином и фенметразином.
Причины ложноотрицательного результата токсикологического скрининга
Причины ложноотрицательных результатов анализа можно разделить на три категории: технологические недостатки, токсикокинетические свойства и предумышленная порча или подмена образца.
Технологические недостатки:
— метод не рассчитан на данное вещество,
— вещество структурно не соответствует прототипу данного класса соединений, например фентанилу,
— низкое качество лабораторной работы.
Токсикокинетические свойства:
— большой объем распределения,
— короткое время полувыведения.
Предумышленная порча или подмена образца:
— предъявление "чистой" мочи другого человека,
— предъявление не мочи, а другой жидкости,
— питье большого количества жидкости,
— прием диуретиков,
— добавка в мочу отбеливателя, едкого агента, "чая" из желтокорня, лимонного сока, соли, мыла или уксуса.
Атомно-абсорбционная спектрофотометрия
Атомно-абсорбционная спектрофотометрия — это обычный метод выявления неорганических агентов (например, свинца, ртути, таллия, кадмия), плохо подходящий для токсикологического скрининга, поэтому большинство его вариантов тяжелых металлов не выявляют.
Плазменная атомно-эмиссионная спектроскопия с индуктивным сопряжением (ПАЭС-ИС) — новый метод, позволяющий проводить одновременный анализ нескольких элементов и полезный в промышленности. Он определяет содержание в одной пробе 17 элементов: алюминия, бария, кадмия, хрома, меди, железа, лантана, свинца, марганца, молибдена, никеля, платины, серебра, стронция, олова, титана и цинка.
Газовая хроматография — масс-спектрометрия
Вероятно, лучшим методом, определяющим присутствие в пробе определенного вещества, является газовая хроматография с масс-спектрометрией (ГХ-МС), однако высокие капитальные и эксплуатационные издержки ограничивают применение его эталонными центрами.
К веществам, знание уровня которых в крови может быть полезным для лечения отравлений, относятся ацетаминофен, салицилаты, карбоксигемоглобин, метгемоглобин, метанол, этиленгликоль, литий, железо, паракват, дигоксин, теофиллин и фосфорорганические соединения. Специфическое применение этой информации рассмотрено в соответствующих отдельных статьях на сайте (рекомендуем пользоваться формой поиска на главной странице сайта).
Гипокальциемия при отравлении
Гипокальциемия особенно часто наблюдается при отравлении фтороводородом, оксалатами, этиленгликолем и органическими соединениями олова, причем нередко у больных в критическом состоянии, сочетающемся с сердечно-сосудистой или нервно-мышечной недостаточностью.
Кристаллурия при отравлении
Кристаллурия может быть следствием отравления сульфаниламидами, четыреххлористым углеродом, примидоном и ампициллином. Массивная кристаллурия обычно связана с потреблением оксалатов или этиленгликоля.
Анализ пота при отравлении
К веществам, выявляемым путем анализа "пятен пота", относятся кокаин, героин, метамфетамин, фенциклидин и тетрагидроканнабинол.
Тесты у постели больного с отравлением
К тестам на присутствие в организме отравляющего вещества, не требующим отправки образцов в лабораторию, относятся определение специфического запаха, скрининг хлоридом трехвалентного железа на салицилаты (положительный результат подтверждает их наличие в сыворотке), нитропруссидная проба на кетоны (Ацетест), визуальное исследование крови на эритроцитарные аномалии, микроскопическое исследование мочи на кристаллы, проверка с помощью тест-палочки на острый некроз скелетных мышц или гемолиз, диагностическое использование налоксона, проверка тест-палочкой на этанол, применение индикаторной трубки для выявления этанола, метанола и изопропанола, а также некоторые другие тесты, ценность которых еще недостаточно изучена (на ацетаминофен, цианид, салицилат свинца, теофиллин — описаны в отдельных статьях на сайте (рекомендуем пользоваться формой поиска на главной странице сайта).
ЭКГ при отравлении
Электрокардиомониторинг полезен для обнаружения фармакогенных аритмий и нарушений калиевого, магниевого и кальциевого баланса.

Учебное видео расшифровки ЭКГ при электролитных нарушениях

Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
- Также рекомендуем "N"
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Основной задачей химико-токсил. анализа является установление
природы яда (общие исследования на неизвестный яд или частное исследование на
Этапы химико-токсил. анализа.
1. Выбор объекта исследования
2. Определение количества расходуемого объекта.
3. Выбор метода изолирования
4. Очистка яда от эндогенных соединений
5. Проведение идентификации и количественного определения.
6.Оценка результатов проведенного анализа
Особенности химико-токсил. анализа.
1. Характеристика объекта исследования
2. Разнообразие ядов, встречаемых при отравлениях по мере поступления в организм и
нахождения в нем.
3. Значительные изменения объекта во времени
4. Изменение токсического вещества в объекте
5. Близость структуры яда и эндогенного соединения
6.Разнообразие объектов исследования :органы трупов, моча и кровь трупов, рвотные массы, экскременты, волосы, ногти, промывные воды желудка, остатки пищи, напитки, пестициды, части растений, обработанные пестицидами, вода водоемов, пробы воздуха промышленных предприятий, почва, предметы домашнего обихода, одежда и др.
Химико-токсикологический анализ характеризуется разнообразием объектов исследования, содержащих незначительные количества токсических веществ. Эти вещества являются микрокомпонентами в большом количестве биол. м-ла. Прежде чем приступить к обнаружению и количественному определению токсических веществ, необходимо выделить их из соответствующих объектов. Выбор методов выделения токсических веществ зависит от характера объекта исследования. При использовании неподходящего метода выделения токсического вещества из исследуемого объекта оно может быть частично или полностью потеряно в ходе химико-токсил. анализа. Причем в ряде случаев для выделения одного и того же вещества из различных объектов необходимо применять разные методы.
Одной из особенностей химико-токсил. анализа является и то, что наряду с исследованием веществ, вызвавших отравление, необходимо выделять из биол. м-ла и определять их метаболиты.
14. Острая алкогольная интоксикация.
Эта патология обусловлена приемом этанола или различных алкогольных напитков с содержанием этанола более 12%. При поступлении в организм этанол претерпевает две четко выраженные фазы распределения: резорбциии (всасывание) и элиминации (выделение). Легко проникая через тканевые мембраны, алкоголь быстро всасывается в желудке: около 20% и в тонком кишечнике - около 80%. В среднем через 1,5 часа после поступления этанола в организм, его концентрация в крови достигает максимального уровня. Конц. спиртовые напитки с концентрацией этанола более 30%, всасываются быстрее. Пищевые массы в желудке замедляют всасывание вследствие своих адсорбционных свойств. При приеме алкоголя натощак, при повторных приемах, а также у людей с заболеваниями желудка (гастрит, язва), скорость всасывания значительно выше. 90% поступающего в организм алкоголя подвергается окислению в печени. Скорость окисления -6-7 г/ч. В окислении принимает участие алкогольдегидрогеназа. В обычных условиях незначительная часть этанола (1 - 2%) окисляется до ацетальдегида ферментом каталазой, которая находится во всех тканях организма. Около 10% всосавшегося этанола выделяется в неизменном виде через легкие и с мочой в течении 7-12 часов. Этанол обладает психотропным действием, связанным с наркотическим эффектом на ЦНС. Наркотический эффект зависит от фазы интоксикации. Так, в фазе резорбции эффект больше, чем в фазе элиминации, несмотря на то, что концентрация этанола в крови в обеих фазах будет одинаковой. Наркотический эффект также зависит от концентрации этанола в крови, от степени развития толерантности больного к алкоголю. Смертельная доза этанола при однократном приеме составляет 4 - 12 г на 1 кг веса тела. В среднем это 300 мл 96% спирта при отсутствии толерантности. Алкогольная кома развивается при концентрации алкоголя в крови около 3 г/л, а смертельная концентрация - 5 - 6 г/л. В течении острого алкогольного отравления можно выделить следующие характерные патологические синдромы. В токсикогенном периоде это: коматозное состояние, невралгические расстройства, нарушение дыхания, нарушение функций сердечно-сосудистой системы (ССС). В соматогенный период проявляются психоневрологические расстройства, воспалительные поражения органов дыхания.
В токсикогенный период тяжесть состояния больного определяется глубиной комы и сопутствующими осложнениями. Существует 2 стадии алкогольной комы: 1) поверхностная и 2) глубокая кома. Стадия поверхностной комы характеризуется потерей сознания, снижением зрачковых рефлексов, резким угнетением болевой чувствительности и отсутствием контакта. Стадия глубокой комы выражается утратой болевой чувствительности, отсутствием или резким снижением зрачковых и сухожильных рефлексов, мышечной атонии и снижением температуры тела. Диагностика алкогольной комы основывается на :
1. клинической картине отравления;
3. лабораторных данных;
Наибольшие трудности представляет дифференцированная диагностика алкогольной комы от коматозных состояний, вызванных следующей патологией, сочетающейся с алкогольным опьянением: черепно-мозговая травма, острое нарушение мозгового кровообращения, отравление ложными суррогатами алкоголя, галогенпроизводными, метанолом, этиленгликолем, снотворными препаратами и транквилизаторами, а также диабетическая кома.
15-16.Острые отравления лекарственными препаратами. Экпресс-методы.
Как и в случае любых химических токсикантов, специфическое ток¬сическое действие лекарственных веществ проявляется на ранней стадии острых отравлений — в токсикогенном периоде. Неспецифиче¬ское действие характерно для соматогенного периода. Специфическое действие токсиканта приводит к многочисленным патологическим про¬цессам, поэтому важно определить природу лекарственного вещества в начале токсикогенного периода.В настоящем разделе рассматриваются результаты химико-токсил. исследования лекарственных средств, отравления которы¬ми происходят наиболее часто.
Производные барбитуровой кислоты оказывают тормозящее действие на ЦНС. Лекарственные средства этой группы используют в качестве ус¬покоительных, снотворных, противосудорожных и средств для наркоза. Барбитураты быстро всасываются из желудочно-кишечного тракта. Для скринингового определения барбитуратов используют иммуно-химические методы (ИФА, РИА, ПФИА). При определении барбитуратов методом ТСХ их экстрагируют из биожидкости, которую предварительно подкисляют. В качестве экстрагентов применяют различные растворители, а также двух- и трехкомпонентные смеси: бензол-этилацетат (2:1), хлороформ-изопропанол-аммиак (5:5:1) И качестве реагентов для проявления используют сернокислый раствор сульфата ртути и дифенилкарбазон. Сине-фиолетовое окрашивание пятен, совпадающих по Rf со стандартами определяемых веществ, позволяет сделать вывод о присутствии барбитуратов в анализируе¬мой пробе. Количественное определение производных барбитуровой кислоты можно проводить спектрофотометрически в ультрафиолетовой области по полосе поглощения с ^тах = 260 нм, измеряя разность абсорбции щелочного раствора барбитурата (тетраборатный буфер) при рН среды 10,0 и 13,0.Производные барбитуровой кислоты определяют также методом ГЖХ с использованием полярных и неполярных жидких фаз. Опреде¬ление осложняется адсорбцией барбитуратов на твердых носителях. Для подготовки пробы в образец вводят 0,25 М серную кислоту и очи¬щенный хлороформ. Проводят экстракцию и центрифугируют (8000 об/мин). Для анализа отбирают 1—5 мкл хлороформного извлечения. Используют ступенчатые температурные режимы колонки, например 180, 200 °С для барбитала, барбамила, нембутала и 230 °С для фено-барбитала.
Отравления лекарственными средствами группы бензодиазепинов
Лекарственные средства группы бензодиазепинов например хлордиазепоксид (хлозепид), медазепам, диазепам (сибазон), оксазепам, нитразепам, феназепам, алпрозолам — высокоактивные транквилизаторы с относительно малой токсичностью. Эта группа лекарственных средств ежегодно пополняется вновь синтезиро¬ванными соединениями с раз-личными заместителями. Относительная доступность бензодиазепинов приводит к злоупот-реблениям и передозировкам.Производные бензодиазепина легко всасываются из желудочно-ки¬шечного тракта, максимальное количество в крови обнаруживается че¬рез 1—3 ч. Степень связывания с белками плазмы высокая (например для диазепама степень связывания достигает 98%). Производные бензо¬диазепина как липофильные вещества депонируются в жировой ткани с последующим постепенным высвобождением в кровь. По этой причи¬не бензодиазепины имеют довольно большой период полувыведения, например, для диазепама он составляет около 98 ч. Экскреция веществ этой группы — почечная (более 60% дозы) и кишечная.Экспресс-анализ бензодиазепинов проводят имунными методами (ИФА, РИА, ПФИА), оценивая общее содержание этих соединении.Определение бензодиазепинов проводят или по продуктам гидролиза — бензофенонам, или по исходным веществам и их метаболитам. Для проведения гидролиза анализируемую пробу биожидкости помещпнп и 6 М НС1 и нагревают при 140 °С в течение 60 мин. Экстракцию образующихся в процессе гидролиза аминобензофенонов проводят гептаном при рН 6,0—8,0. Анализ экстрактов проводят хроматографическими методами.При определении бензодиазепинов методом ТСХ в качестве подвиж¬ной фазы используют бензол. Обнаружение после разделения проводят по собственной желтой окраске с флюоресценцией в ультрафиолетовом свете. Предел обнаружения составляет 1—5 мкг в пятне. Элюаты хрома-тограмм используют для снятия электронного спектра или газохромато-графического исследования. Основные полосы поглощения аминобензо¬фенонов в этаноле 230—240 и 390—400 нм. Количественное определение можно проводить фотоколориметрическим методом по окрашенным продуктам реакции бензофенона с образованием азокрасителя.Анализ биологической пробы без предварительного гидролиза поз¬воляет обнаружить индивидуальные вещества и их метаболиты. Для этого проводят экстракцию бензодиазепинов из биообъектов органиче¬скими растворителями при рН 6,0—8,0 и последующее хроматографи-ческое определение.Для определения методом ТСХ применяют системы хлороформ-метанол (9:1), этилацетат—метанол—аммиак (85:10:5). Используя элю¬аты с ТСХ-пластин, проводят определение методом ГХ-МС по нативным соединениям или их летучим производным (дериватам).Возможно ВЭЖХ-определение производных бензодиазепина по нативным веществам или продуктам гидролиза. В качестве подвижной фазы можно использовать смесь ацетонитрил—0,05 М водный двузамещенный фосфат аммония (35:65 для нативных соединений или 55:45 для бензофенонов). Детектирование в ультрафиолетовых лучах прово-дят при 230—220 нм.
Отравление лекарственными средствами группы фенотиазинов
Лекарственные средства группы фенотиазина используются как транквилизаторы, антидепрессанты, антигистаминные и антиангинальные средства. Из алкильных производных фенотиазина наиболее известны аминазин (хлорпромазин), пропазин (промазин), левомепразин (тизерцин), метеразин (прохлорперазин), тиоридазин, хлорпротиксен, трифтазин.Из ацильных производных фенотиазина широко применяются этацизин, этмозин, нонахлазин и др.Производные фенотиазина химически очень лабильны и в орга¬низме подвергаются биотрансформации. Для экспресс-определения фенотиазинов в моче используют реак¬цию с FNP-реактивом, который состоит из смеси водного раствора хлорида железа (III), хлорной кислоты (НСЮ4) и азотной кислоты (1:9:10). Появляющаяся окраска от розовой до сине-фиолетовой свидетельствует о присутствии фенотиазинов или их метаболитов. Вслед¬ствие недостаточной специфичности реакции возможно получение ложноположительных результатов. Определению мешают салицилаты, желчные пигменты и другие соэкстрактивные вещества биологической пробы.Дальнейшее определение проводят методами ТСХ, ГЖХ, ВЭЖХ. При подготовке проб мочи и крови для ана¬лиза проводят гидролиз. Затем экстрагируют фенотиазины смесью гептан—3% изопентанол. Для ТСХ используют системы бензол— диоксан—25% аммиак (60:35:5) и этилацетат—ацетон—25% аммиак в этаноле 1:1 (50:45:4). Применяют также системы толуол—ацетон-этанол—25% аммиак (45:45:7,5:2,5) и диоксан—хлороформ—аце¬тон—25% аммиак (47,5:45:5:2,5). Детектирование проводят спирто¬вым раствором конц. серной кислоты (9:1) или реактивом Марки (H2SO4 + СН2О). Все фенотиазины дают красное или темно-красное окрашивание, кроме левомепразина, имеюще¬го голубую окраску. Количественное определение проводят фото¬метрическим методом по окрашенному продукту взаимодействия производного фенотиазина с метиленовым оранжевым или кисло¬тами.Для определения фенотиазинов методом ГЖХ используют тот же экстракт, температура колонки 230 °С или программирование от 130 до 290 °С со скоростью 20 °С/мин при температуре испарителя 250 °С.Для определения фенотиазинов используют ГХ-МС элюатов с ТСХ-пластин по нативным соединениям или ацето- и фторзамещенным де¬риватам.Возможно ВЭЖХ-определение производных фенотиазина в моче и сыворотке крови с использованием автоматических анализаторов; пре¬дел обнаружения 0,1 мкг/мл.
Отравление лекарственными средствами группы трициклических антидепрессантов
К группе трициклических антидепрессантов относятся амитриптилин, имизин, соответствующие N-дезметильные аналоги нортриптилин и дезипрамин. В анализе химико-токсикологические лаборатории вы¬полняют качественное обнаружение амитриптилина в моче методом ТСХ. При скрининговых исследованиях проводят экстракцию из мочи хлороформом или эфиром при рН 10,5—11,0. Упаренный экстракт на¬носят на пластинку и проводят хроматографирование в различных сис¬темах, например этилацетат—ацетон—раствор аммиака в этаноле (50:45:5), бензол—диоксан—аммиак (60:35:5). Проявление проводят оп¬рыскиванием конц. серной кислотой; наблюдается оран¬жево-кирпичная окраска. Предел обнаружения составляет 0,1 мкг в пятне.Количественное определение амитриптилина и нортриптилина про¬водят экстракционно-фотометрическим методом по комплексу с бром-феноловым синим после экстракционной и хроматографической очи¬стки. Предел обнаружения составляет 1 мкг/мл (в случае смертельных отравлений). Для экспресс-диагностики антидепрессантов в крови и моче ис¬пользуют также иммунохимические методы, например ПФИА. При этом удается снизить предел обнаружения на порядок — до 0,01 мкг/мл. Таким образом, иммунохимический метод позволяет выявить передо¬зировку лекарственного средства, что особенно важно в связи с малой широтой терапевтического интервала (близость терапевтических и ток¬сических доз).Для дифференциальной диагностики, изучения фармако- и токсикокинетики используют методы ГЖХ и ВЭЖХ (предел обнаружения 1 мкг/мл). При определении токсических концентраций в крови для снижения предела обнаружения (до 0,2 мкг/мл) проводят предвари¬тельное превращение в трифторацетатные производные.
Отравление антигистаминными лекарственными средствами
К антигистаминным средствам относятся вещества, блокирующие Н-гистаминовые рецепторы. Это представители разных химических классов органических веществ (например, димедрол, супрастин, тавегил, диазолин), что объясняет применение различных методик для их определения. Дифенилгидрамин довольно легко всасывается после приема внутрь (биодоступность 50%). Связывание с белками плазмы достига¬ет 72—98%, период полувыведения из крови 3—10 ч. Основные пути метаболизма - N-дезалкилирование, окислительное дезаминирование, конъюгация. Лишь 2-4% дозы выводится в неизмененном виде с мочой.Анализ на дифенилгидрамин проводится после экстракции веществ основного характера. Определение методом ТСХ проводят в общих си¬стемах, например бензол—диоксан—аммиак (60:35:5); проявляют оп¬рыскиванием конц. серной кислотой - образуется лимонно-желтое окрашивание.Для ГЖХ-анализа используют тот же экстракт; температура колонки 230 °С или программирование от 130 до 290 °С со скоростью 20 °С/мин, температура испарителя 250 °С.
Отравление лекарственными средствами группы сердечных гликозидов
К группе сердечных гликозидов относятся дигитоксин и другие кардиотоксичные гликозиды, которые содержатся, например, в наперстян¬ке. Их применяют как антиаритмические средства. Из структуры дигоксина следует, что гликозиды имеют высокую молярную массу, химически неустойчивы. Их терапевтические и токсические концент¬рации очень низкие, в связи с чем определение этих веществ, особенно в биологических м-лах, представляет определенные трудности. Доля связывания с бел¬ками 20-40%, доля выведения с мочой 60-90%, период полувыведения из плазмы 4—100 ч. Методы ВЭЖХ, ТСХ можно применять для определения сердечных гликозидов в сырье или в вещественных доказательствах, но не в биоло¬гических жидкостях, где их концентрация очень мала. Для определения гликозидов в моче используют иммунохимические методы.
Организация работы химико-токсикологической лаборатории
1. Особенности работы ХТЛ центра острых отравлений.
Ведущее направление диагностики заболеваний химической этиологии — идентификация токсичных химических веществ в организме пострадавшего. Для этого необходимо наличие специализированной ХТЛ в составе токсикологических центров.
Стоит отметить, что существующие практически на каждой территории судебно-химические отделения в составе бюро судебно-медицинской экспертизы или химико-токсикологические лаборатории наркологических диспансеров решают свои задачи в плановом порядке, в дневное время, и не предназначены по штатному расписанию и принятым методикам для экстренных круглосуточных исследований.
В силу ряда причин, прежде всего материально-технического характера, химико-токсикологическая лабораторная диагностика — пока наименее развитое направление специализированной медицинской помощи. Именно поэтому вопросы организации химико-токсикологической лабораторной диагностики представляют особую проблему по наличию специального оборудования и кадров.
Говоря об организации работы ХТЛ в рамках стационарного лечебного учреждения, необходимо четко определить задачи, которые должна выполнять лаборатория. К ним прежде всего относятся экстренная круглосуточная качественная идентификация и количественное определение токсиканта в биосредах пациента, поскольку от этого зависят постановка диагноза отравления, выбор метода, оценка эффективности лечения. Соответственно лаборатория должна быть расположена в пределах лечебного учреждения, в котором организован центр (отделение), иметь круглосуточный режим работы и необходимые для этого штатное расписание и диагностическое оборудование.
Эти вопросы отражены в приказе Минздрава РФ от 08.01.2002 г. №9, "О мерах по совершенствованию организации токсикологической помощи населению Российской Федерации" в соответствии с которым ХТЛ является функциональным подразделением центра (отделения) лечения острых отравлений на правах отделения. Организация ХТЛ проходит в установленном порядке в медицинском учреждении, в состав которого входит центр (отделение) лечения острых отравлений, для проведения химико-токсикологического экспресс-исследования биологических объектов на наличие токсичных веществ, вызвавших отравление.
В соответствии с приказом № 9 Минздрава РФ и по существу своих задач ХТЛ выполняет исследования биологических объектов в целях диагностики отравления, оценки эффективности лечения, т.е, исследования следует отнести к категории клинических. Именно поэтому исследования в целях экспертизы или установления факта приема алкоголя, наркотических, лекарственных и других токсичных веществ не входят в круг обязанностей ХТЛ. Для этой цели существуют химико-токсикологические лаборатории при наркологических диспансерах, судебно-химические отделения бюро судебно-медицинской экспертизы.
Это должно быть обязательно обозначено в Положении о работе ХТЛ, включенном в приказ об организации городского (краевого, областного, республиканского) центра острых отравлений.
В этом документе должны быть отражены и другие функции ХТЛ. В частности, выполнение диагностических исследований для других отделений базовой больницы, а также различных стационаров обслуживаемой территории при необходимости диагностики или дифференциальной диагностики отравления у больных, госпитализированных с различными заболеваниями (комой неясной этиологии, нейроинфекциями, нарушением мозгового кровообращения и др.), когда лечащие врачи подозревают отравление. В этих случаях исследование проводят только после предварительной телефонной или очной консультации с врачом-токсикологом, который и определит необходимость, обоснованность и направление исследования (перечень токсичных веществ или групп токсикантов, предполагаемых в качестве причины отравления). Следует заметить, что ХТЛ не проводит поиск так называемого неизвестного яда, так как для этого потребуется целый ряд различных поисковых и подтверждающих исследований, получение, помимо обычных анализов крови и мочи, желудочного содержимого других объектов (кусочков органов), большего промежутка времени (до нескольких дней). Такие исследования относятся к компетенции бюро судебно-медицинской экспертизы.
Результаты доводят до сведения дежурного токсиколога немедленно по окончании исследования, с последующим письменным подтверждением.
На территориях, где отсутствуют центры (отделения) острых отравлений, химико-токсикологические исследования в целях экспресс-диагностики острых отравлений могут выполнять клинические, биохимические и другие лаборатории лечебных учреждений, лицензированные на данный вид деятельности. Однако при этом объем и методы исследований будут существенно меньше, ограничиваясь самыми актуальными, такими как определение наличия и исследование уровня спиртов и других летучих соединений методом газожидкостной хроматографии, определение наличия лекарственных средств методом тонкослойной хроматографии, выявление наркотических средств (опиатов, амфетаминов, каннабиноидов) с помощью иммунохроматографических тестов.
В небольших регионах для более рационального использования лабораторного оборудования химико-токсикологические диагностические исследования могут быть возложены на бюро судебно-медицинской экспертизы, однако нужно учитывать, что исследование не будет проведено в экстренном режиме.
1. Особенности работы ХТЛ центра острых отравлений.
Ведущее направление диагностики заболеваний химической этиологии — идентификация токсичных химических веществ в организме пострадавшего. Для этого необходимо наличие специализированной ХТЛ в составе токсикологических центров.
Стоит отметить, что существующие практически на каждой территории судебно-химические отделения в составе бюро судебно-медицинской экспертизы или химико-токсикологические лаборатории наркологических диспансеров решают свои задачи в плановом порядке, в дневное время, и не предназначены по штатному расписанию и принятым методикам для экстренных круглосуточных исследований.
В силу ряда причин, прежде всего материально-технического характера, химико-токсикологическая лабораторная диагностика — пока наименее развитое направление специализированной медицинской помощи. Именно поэтому вопросы организации химико-токсикологической лабораторной диагностики представляют особую проблему по наличию специального оборудования и кадров.
Говоря об организации работы ХТЛ в рамках стационарного лечебного учреждения, необходимо четко определить задачи, которые должна выполнять лаборатория. К ним прежде всего относятся экстренная круглосуточная качественная идентификация и количественное определение токсиканта в биосредах пациента, поскольку от этого зависят постановка диагноза отравления, выбор метода, оценка эффективности лечения. Соответственно лаборатория должна быть расположена в пределах лечебного учреждения, в котором организован центр (отделение), иметь круглосуточный режим работы и необходимые для этого штатное расписание и диагностическое оборудование.
Эти вопросы отражены в приказе Минздрава РФ от 08.01.2002 г. №9, "О мерах по совершенствованию организации токсикологической помощи населению Российской Федерации" в соответствии с которым ХТЛ является функциональным подразделением центра (отделения) лечения острых отравлений на правах отделения. Организация ХТЛ проходит в установленном порядке в медицинском учреждении, в состав которого входит центр (отделение) лечения острых отравлений, для проведения химико-токсикологического экспресс-исследования биологических объектов на наличие токсичных веществ, вызвавших отравление.
В соответствии с приказом № 9 Минздрава РФ и по существу своих задач ХТЛ выполняет исследования биологических объектов в целях диагностики отравления, оценки эффективности лечения, т.е, исследования следует отнести к категории клинических. Именно поэтому исследования в целях экспертизы или установления факта приема алкоголя, наркотических, лекарственных и других токсичных веществ не входят в круг обязанностей ХТЛ. Для этой цели существуют химико-токсикологические лаборатории при наркологических диспансерах, судебно-химические отделения бюро судебно-медицинской экспертизы.
Это должно быть обязательно обозначено в Положении о работе ХТЛ, включенном в приказ об организации городского (краевого, областного, республиканского) центра острых отравлений.
В этом документе должны быть отражены и другие функции ХТЛ. В частности, выполнение диагностических исследований для других отделений базовой больницы, а также различных стационаров обслуживаемой территории при необходимости диагностики или дифференциальной диагностики отравления у больных, госпитализированных с различными заболеваниями (комой неясной этиологии, нейроинфекциями, нарушением мозгового кровообращения и др.), когда лечащие врачи подозревают отравление. В этих случаях исследование проводят только после предварительной телефонной или очной консультации с врачом-токсикологом, который и определит необходимость, обоснованность и направление исследования (перечень токсичных веществ или групп токсикантов, предполагаемых в качестве причины отравления). Следует заметить, что ХТЛ не проводит поиск так называемого неизвестного яда, так как для этого потребуется целый ряд различных поисковых и подтверждающих исследований, получение, помимо обычных анализов крови и мочи, желудочного содержимого других объектов (кусочков органов), большего промежутка времени (до нескольких дней). Такие исследования относятся к компетенции бюро судебно-медицинской экспертизы.
Результаты доводят до сведения дежурного токсиколога немедленно по окончании исследования, с последующим письменным подтверждением.
На территориях, где отсутствуют центры (отделения) острых отравлений, химико-токсикологические исследования в целях экспресс-диагностики острых отравлений могут выполнять клинические, биохимические и другие лаборатории лечебных учреждений, лицензированные на данный вид деятельности. Однако при этом объем и методы исследований будут существенно меньше, ограничиваясь самыми актуальными, такими как определение наличия и исследование уровня спиртов и других летучих соединений методом газожидкостной хроматографии, определение наличия лекарственных средств методом тонкослойной хроматографии, выявление наркотических средств (опиатов, амфетаминов, каннабиноидов) с помощью иммунохроматографических тестов.
В небольших регионах для более рационального использования лабораторного оборудования химико-токсикологические диагностические исследования могут быть возложены на бюро судебно-медицинской экспертизы, однако нужно учитывать, что исследование не будет проведено в экстренном режиме.
2. Особенности работы ХТЛ наркологического диспансера.
Химико-токсикологическая лаборатория наркологического диспансера (наркологической больницы) (далее - ХТЛ) является структурным подразделением наркологического диспансера или наркологической больницы. Работа данной ХТЛ осуществляется в соответствии с Приказом Минздравсоцразвития РФ от 27.01.2006 N 40 "Об организации проведения химико-токсикологических исследований при аналитической диагностике наличия в организме человека алкоголя, наркотических средств, психотропных и других токсических веществ".
ХТЛ организуется для проведения химико-токсикологических исследований биологических жидкостей организма человека (кровь, моча, слюна) на наличие алкоголя и его суррогатов, наркотических средств, психотропных и других токсических веществ, вызывающих опьянение (интоксикацию), и их метаболитов, а также альтернативных объектов (смывы с поверхности кожи, волосы, ногти и пр.) на наличие наркотических средств, психотропных и других токсических веществ, вызывающих опьянение (интоксикацию), и их метаболитов (далее - биологические объекты).
ХТЛ возглавляется заведующим, который подчиняется главному врачу наркологического диспансера (наркологической больницы). Штаты ХТЛ укомплектовываются врачами, провизорами, специалистами с немедицинским образованием, допущенными к занятию должности врача клинической лабораторной диагностики в установленном порядке, имеющими сертификат по специальности "Клиническая лабораторная диагностика" и прошедшими дополнительную подготовку по аналитической токсикологии наркотических средств, психотропных и других токсических веществ.
ХТЛ располагается в отдельном, изолированном помещении, исключающем доступ посторонних лиц и отвечающем требованиям техники безопасности при работе персонала в ХТЛ и санитарно-гигиеническим требованиям, обеспечивающим выполнение возложенных на нее задач. ХТЛ оснащается необходимым оборудованием, оргтехникой, инвентарем, реактивами, справочной литературой, нормативно-технической документацией, средствами связи и охранной сигнализацией.
ХТЛ осуществляет следующие функции:
· Прием в установленном порядке на химико-токсикологические исследования биологических объектов.
· Хранение биологического объекта для повторных химико-токсикологических исследований в течение двух месяцев с соблюдением установленных для этого требований.
· Проведение химико-токсикологических исследований принятых биологических объектов на наличие алкоголя и его суррогатов, наркотических средств, психотропных и других токсических веществ, вызывающих опьянение (интоксикацию), и их метаболитов. Ведение рабочего журнала проводимых исследований в произвольной форме с описанием биологического объекта и результатов.
· Оформление результатов химико-токсикологических исследований о наличии (отсутствии) в исследуемых биологических объектах алкоголя и его суррогатов, наркотических средств, психотропных и других токсических веществ, вызывающих опьянение (интоксикацию), и их метаболитов по установленной форме.
· Выдача Справок о результатах химико-токсикологических исследований биологических объектов (учетная форма N 454/у-06).
Контроль за деятельностью ХТЛ, расходом реагентов и правильным использованием оборудования осуществляется руководителем (заместителем руководителя) наркологического диспансера (наркологической больницы), структурным подразделением которого является ХТЛ.
Учетная форма N 452/у-06 "Направление на химико-токсикологические исследования" (далее - Направление) заполняется и выдается структурными подразделениями медицинских организаций, проводящих медицинское освидетельствование на состояние опьянения и (или) диагностику факта употребления алкоголя и его суррогатов, наркотических средств, психотропных и других токсических веществ, вызывающих опьянение (интоксикацию), и их метаболитов (далее - Подразделение) в случаях, когда требуется лабораторное подтверждение или исключение наличия алкоголя и его суррогатов, наркотических средств, психотропных и других токсических веществ, вызывающих опьянение (интоксикацию), и их метаболитов в биологических объектах.
На основании Направления ХТЛ проводит химико-токсикологические исследования и выдает Справку о результатах химико-токсикологических исследований (учетная форма N 454/у-06) о наличии или отсутствии алкоголя и его суррогатов, наркотических средств, психотропных и других токсических веществ, вызывающих опьянение (интоксикацию), и их метаболитов в представленном на химико-токсикологические исследования биологическом объекте.
В Направлении указывается: дата его заполнения и его номер; наименование медицинской организации и Подразделения, выдавшего Направление; наименование ХТЛ, куда направляется биологический объект; фамилия и инициалы освидетельствуемого (при анонимном обращении - штрих-код); возраст; код биологического объекта (штрих-код), дата и время (часы, минуты) отбора биологического объекта, условия хранения биологического объекта после его отбора, включающие температурный режим хранения; биологический объект (кровь, моча, слюна и пр.), для крови и мочи - объем в мл; физико-химические показатели для мочи; если проводился медицинский осмотр - предварительные результаты осмотра биологического объекта; цель химико-токсикологических исследований: на какое вещество (средство) или группы веществ (средств) требуется провести исследования.
Направление на химико-токсикологические исследования заполняется и подписывается работником Подразделения, производившим отбор биологического объекта. Направления хранятся в ХТЛ в течение одного года, после чего уничтожаются.
3. Общие приказы, регламентирующие работу ХТЛ.
Деятельность лаборатории регламентируется другими специальными нормативными документами, в частности следующими приказами:
4. Материально-техническое оснащение ХТЛ.
В зависимости от объема работы лаборатория может занимать несколько помещений. Обязательно должны быть:
❖ кабинет материально ответственного лица с соответствующим оснащением — сейфами для хранения учетных реактивов и стандартных веществ, наркотических веществ, этилового спирта и т.д., сигнализацией. Это может быть кабинет заведующего лабораторией или лица, исполняющего обязанности старшего лаборанта;
❖ комната-кладовая для хранения неучетных материалов - реактивов, расходных материалов, отдельно должны храниться огнеопасные и взрывоопасные вещества;
❖ лабораторные производственные помещения для выполнения собственно анализов;
❖ помещение для приема биологических проб;
❖ помещение для хранения биологических объектов;❖ помещение для отдыха персонала.
Лабораторные производственные помещения могут быть представлены несколькими комнатами по видам деятельности или общим залом, где выделены зоны производственной деятельности, например, для:
❖ пробоподготовки (оснащена тягами, песчаными банями, электрическими нагревателями);
❖ выполнения тонкослойной хроматографии (оснащена тягой, феном для просушивания пластин);
❖ газохроматографических методов (с подводкой туда соответствующих газов);
Должно быть выделено место, где проводят прием, регистрацию и размещение образцов для анализа, регистрацию полученных результатов, заполнение соответствующей документации.
ХТЛ должна быть оснащена необходимыми (табельными) приборами, оборудованием, оргтехникой, инвентарем, реактивами, справочной литературой, нормативно-технической документацией и средствами связи.
Перечень рекомендуемого оборудования зависит от объема и задач исследования, используемых методов. При этом должен быть обязательный минимально необходимый комплект приборов и оборудования с учетом частоты выполнения тех или иных исследований, определяемых структурой острых отравлений, в частности, обязательно должно быть оборудование для определения этанола и алифатических спиртов (газовый хроматограф с детектором по теплопроводности), растворителей и других промышленных ядов (газовый хроматограф с детектором по ионизации пламени), лекарственных средств и наркотических веществ (набор для тонкослойной хроматографии, газовый хроматограф с детекторами по теплопроводности, азотно-фосфорным, электронного захвата и ионизации пламени, наборами для иммунохроматографического анализа). Специфические биохимические исследования предполагают использование методов фотоколориметрии и/или ультрафиолетовой спектрофотометрии.
Перечень методов и аналитических приборов может быть расширен при соответствующих финансовых возможностях базовой больницы. В число таких дополнительных методов целесообразно включить высокоэффективную жидкостную хроматографию, флуороиммуноанализ, газов>то хроматографию с масс-спектрометрией. Однако нужно учитывать, что эти методы потребуют дополнительного обучения специалистов лаборатории, а для полноценной работы всего оборудования необходимо запланировать и выделить средства для приобретения расходных материалов и реактивов.
Читайте также:

