Ротавирусная инфекция при гастрите
Обновлено: 24.04.2024
Острые кишечные инфекции (ОКИ) — это большая группа инфекционных заболеваний человека с энтеральным механизмом заражения, вызываемых патогенными и условно-патогенными бактериями, вирусами или простейшими
Острые кишечные инфекции (ОКИ) — это большая группа инфекционных заболеваний человека с энтеральным (фекально-оральным) механизмом заражения, вызываемых патогенными (шигеллы, сальмонеллы и др.) и условно-патогенными бактериями (протеи, клебсиеллы, клостридии и др.), вирусами (рота-, астро-, адено-, калицивирусы) или простейшими (амеба дизентерийная, криптоспоридии, балантидия коли и др.).
Ведущим компонентом терапии ОКИ является рациональное лечебное питание, адаптированное к возрасту ребенка, характеру предшествующего заболевания и вскармливания.
Цель диетотерапии — уменьшение воспалительных изменений в желудочно-кишечном тракте, нормализация функциональной активности и процессов пищеварения, максимальное щажение слизистой оболочки кишечника.
Основные требования к диете при ОКИ:
включение в диеты низко- и безлактозных продуктов и кисломолочных продуктов, обогащенных бифидо- и лактобактериями;
снижение объема пищи в первые дни болезни на 15–20% (при тяжелых формах до 50%) от физиологической потребности;
Из диеты исключаются стимуляторы перистальтики кишечника, продукты и блюда, усиливающие процессы брожения и гниения в кишечнике: сырые, кислые ягоды и фрукты, соки, сырые овощи, сливочное и растительные масла (в чистом виде), сладости, свежая выпечка. Не следует давать бобовые, свеклу, огурцы, квашеную капусту, редис, апельсины, груши, мандарины, сливы, виноград. Не рекомендуется овсяная крупа, так как она усиливает бродильные процессы. Должны быть исключены из питания жирные сорта мясных и рыбных продуктов (свинина, баранина, гусь, утка, лосось и др.).
Цельное молоко в остром периоде кишечных инфекций назначать не следует, так как оно усиливает перистальтику кишечника и бродильные процессы в результате нарушения расщепления молочного сахара (лактозы), что сопровождается усилением водянистой диареи и вздутием живота.
В первые дни заболевания исключается также черный хлеб, способствующий усилению перистальтики кишечника и учащению стула.
При уменьшении проявлений интоксикации, прекращении рвоты и улучшении аппетита вводится творог, мясо (говядина, телятина, индейка, кролик в виде котлет, фрикаделек, кнелей), рыба нежирных сортов, яичный желток и паровой омлет. Разрешаются тонко нарезанные сухари из белого хлеба, каши на воде (кроме пшенной и перловой), супы слизистые, крупяные с разваренной вермишелью на слабом мясном бульоне.
В остром периоде заболевания рекомендуется использовать молочнокислые продукты (кефир, ацидофильные смеси и др.). Молочнокислые продукты за счет активного действия содержащихся в них лактобактерий, бифидобактерий, конечных продуктов протеолиза казеина (аминокислот и пептидов, глутаминовой кислоты, треонина и др.), увеличенного количества витаминов В, С и др. способствуют улучшению процессов пищеварения и усвоению пищи, оказывают стимулирующее влияние на секреторную и моторную функции кишечника, улучшают усвоение азота, солей кальция и жира. Кроме того, кефир обладает антитоксическим и бактерицидным действием на патогенную и условно-патогенную флору за счет наличия молочной кислоты и лактобактерий. Однако длительное применение только кефира или других молочнокислых смесей нецелесообразно, поскольку эти продукты бедны белками и жирами. Лечебным кисломолочным продуктом является Лактофидус — низколактозный продукт, обогащенный бифидобактериями.
При лечении детей с ОКИ в периоде выздоровления необходимо широко использовать плодово-овощные продукты (яблоки, морковь, картофель и др.), так как они содержат большое количество пектина. Пектин — коллоид, обладающий способностью связывать воду и набухать, образуя пенистую массу, которая, проходя по кишечному тракту, адсорбирует остатки пищевых веществ, бактерий, токсических продуктов. В кислой среде от пектина легко отщепляется кальций, оказывая противовоспалительное действие на слизистую оболочку кишечника. Фрукты и овощи содержат органические кислоты, обладающие бактерицидным действием, а также большое количество витаминов, глюкозу, фруктозу, каротин и др. Применение вареных овощей и печеных фруктов уже в остром периоде кишечных инфекций способствует более быстрому исчезновению интоксикации, нормализации стула и выздоровлению.
Питание детей грудного возраста
В последнее время в клинике кишечных инфекций предпочтение отдается назначению детям, находящимся на искусственном вскармливании, низко- и безлактозных смесей (Низколактозный Нутрилон, Фрисопеп, Хумана ЛП+СЦТ, соевые смеси). При тяжелых формах ОКИ и развитии гипотрофии широко используются гидролизованные смеси (Нутрилон Пепти ТСЦ, Нутримиген, Алфаре, Прегестимил и др.), способствующие быстрому восстановлению процессов секреции и всасывания в кишечнике и усвоению белков, жиров и углеводов, что предупреждает развитие ферментопатии в исходе кишечной инфекции (табл).
По нашим данным, в результате клинико-лабораторной оценки влияния низколактозных смесей на клиническую картину и состояние микробиоценоза кишечника при вирусных диареях у детей раннего возраста был получен положительный эффект стимуляции функциональной активности нормальной и, в первую очередь, сахаролитической микрофлоры (по стабилизации показателей уксусной, масляной и пропионовой кислот), а также регулирующее влияние на процессы метаболизма углеводов и жиров в острый период заболевания. Клинический эффект заключался в быстром и стойком купировании основных проявлений болезни: рвоты, диареи, абдоминального синдрома и эксикоза, что наряду с хорошей переносимостью позволило рекомендовать низколактозные смеси для использования в качестве лечебного питания у детей раннего возраста в острый период кишечных инфекций вирусной этиологии.
При разгрузке в питании ежедневно объем пищи увеличивается на 20–30 мл на одно кормление и соответственно изменяется кратность кормлений, то есть увеличивается интервал между кормлениями. При положительной динамике заболеваний и улучшении аппетита необходимо довести суточный объем пищи до физиологической потребности не позднее 3–5 дня от начала лечения.
Детям 5–6 месяцев при улучшении состояния и положительной динамике со стороны желудочно-кишечного тракта назначается прикорм кашей, приготовленной из рисовой, манной, гречневой круп на половинном молоке (или воде при ротавирусной инфекции). Кашу назначают в количестве 50–100–150 г в зависимости от возраста ребенка и способа вскармливания до заболевания. Через несколько дней добавляют к этому прикорму 10–20 г творога, приготовленного из кипяченого молока, а затем — овощные пюре, ягодный или фруктовый кисель в количестве 50–100–150 мл, соки.
Питание детей 7–8 месяцев должно быть более разнообразным. При улучшении состояния им назначают не только каши, творог и кисели, но и овощные пюре, желток куриного яйца на 1/2 или 1/4 части, затем бульоны, овощной суп и мясной фарш. В каши и овощное пюре разрешается добавлять сливочное масло. Желток (яйцо должно быть сварено вкрутую) можно давать отдельно или добавлять его в кашу, овощное пюре, суп.
Питание детей старше года строится по такому же принципу, как и у детей грудного возраста. Увеличивается лишь разовый объем пищи и быстрее включаются в рацион продукты, рекомендуемые для питания здоровых детей этого возраста. В остром периоде болезни, особенно при наличии частой рвоты, следует провести разгрузку в питании. В первый день ребенку назначают кефир по 100–150–200 мл (в зависимости от возраста) через 3–3,5 часа. Затем переходят на питание, соответствующее возрасту, но с исключением запрещенных продуктов. В остром периоде заболевания всю пищу дают в протертом виде, применяется паровое приготовление вторых блюд. Крупу для приготовления каши и гарнира, овощи разваривают до мягкости. Набор продуктов должен быть разнообразным и содержать кисломолочные смеси, кефир, творог, сливки, сливочное масло, супы, мясо, рыбу, яйца, картофель, свежие овощи и фрукты. Можно пользоваться овощными и фруктовыми консервами для детского питания. Из рациона исключают продукты, богатые клетчаткой и вызывающие метеоризм (бобовые, свекла, репа, ржаной хлеб, огурцы и др.). Рекомендуются арбузы, черника, лимоны, кисели из различных ягод, желе, компоты, муссы, в которые желательно добавлять свежевыделенный сок из клюквы, лимона.
Правильно организованное питание ребенка с кишечной инфекцией с первых дней заболевания является одним из основных условий гладкого течения заболевания и быстрого выздоровления. Неадекватное питание и погрешности в диете могут ухудшить состояние ребенка, равно как и длительные ограничения в питании. Важно помнить, что на всех этапах лечения ОКИ необходимо стремиться к полноценному физиологическому питанию с учетом возраста и функционального состояния желудочно-кишечного тракта ребенка.
Значительные трудности в диетотерапии возникают у детей с развитием постинфекционной ферментопатии, которая развивается в разные сроки заболевания и характеризуется нарушением переваривания и всасывания пищи вследствие недостатка ферментов.
При ОКИ, особенно при сальмонеллезе, кампилобактериозе, протекающих с реактивным панкреатитом, наблюдается нарушение всасывания жира и появление стеатореи — стул обильный с блеском, светло-серый с неприятным запахом. Диетотерапия при стеаторее проводится с ограничением жира в рационе, но не более 3–4 мг/кг массы тела в сутки для детей первого года жизни. Это достигается путем замены части молочных продуктов специализированными низкожировыми продуктами (Ацидолакт) и смесями зарубежного производства, в состав которых в качестве жирового компонента входят среднецепочечные триглицериды, практически не нуждающиеся в панкреатической липазе для усвоения (Нутрилон Пепти ТСЦ, Хумана ЛП+СЦТ, Алфаре, Прегестимил, Фрисопеп и др.). При появлении признаков острого панкреатита из рациона исключают свежие фрукты, ягоды, овощи, концентрированные фруктовые соки на срок до 1 мес.
При лактазной недостаточности рекомендуется использование адаптированных низколактозных смесей (Низколактозный Нутрилон, Фрисопеп, Хумана ЛП+СЦТ и др.) или соевых смесей (Нутрилон Соя, Фрисосой, Хумана СЛ, Симилак Изомил, Энфамил Соя и др.). При их отсутствии — 3-суточный кефир; детям первых трех месяцев жизни можно давать смесь типа В-кефир, состоящую из 1/3 рисового отвара и 2/3 3-суточного кефира с добавлением 5% сахара (глюкозы, фруктозы), 10% каши на воде, овощных отварах.
В качестве прикорма этим больным дают безмолочные каши и овощные пюре на воде с растительным или сливочным маслом, отмытый от сыворотки творог, мясное пюре, печеное яблоко. Схемы введения прикормов могут быть индивидуализированы, следует обратить внимание на раннее назначение мясного (суточная доза в 3–4 приема). Избегают применения сладких фруктовых соков, продуктов, повышающих газообразование в кишечнике и усиливающих перистальтику (ржаной хлеб, белокочанная капуста, свекла и другие овощи с грубой клетчаткой, кожура фруктов, чернослив, сухофрукты). Длительность соблюдения низколактозной диеты индивидуальна — от 1,5–2 до 6 месяцев.
После тяжелых кишечных инфекций может возникнуть непереносимость не только лактозы, но и других дисахаридов, реже — полная углеводная интолерантность (глюкозо-галактозная мальабсорбция), при которой у больных отмечается выраженная диарея, усиливающаяся при применении смесей и продуктов, содержащих дисахариды, моносахариды и крахмал (молочные и соевые смеси, крупы и практически все фрукты и овощи). Это чрезвычайно тяжелое состояние, приводящее к обезвоживанию и прогрессирующей дистрофии, требует строгого безуглеводного питания и парентерального введения глюкозы или полного парентерального питания. В отдельных случаях возможно пероральное введение фруктозы. При индивидуальной переносимости в диете сохраняются белок и жиросодержащие продукты: нежирное мясо — индейка, конина, говядина, кролик, растительное масло, ограниченный ассортимент овощей с низким содержанием сахарозы и глюкозы — цветная и брюссельская капуста, шпинат, стручковая фасоль, салат.
Дефицит белка возникает за счет нарушения утилизации, всасывания либо за счет потери эндогенного белка, особенно у детей с исходной гипотрофией. Коррекция потерь белка проводится путем назначения гидролизованных смесей (Нутрилон Пепти ТСЦ, Нутримиген, Алфаре, Прегестимил, Фрисопеп и др.).
При длительных постинфекционных диареях, особенно у детей, получавших повторные курсы антибактериальных препаратов, возможно развитие вторичной пищевой аллергии, сопровождающейся сенсибилизацией к белкам коровьего молока, реже — к яичному протеину, белкам злаковых культур. Такие нарушения могут возникать не только у детей с аллергическим диатезом, но и у больных без отягощенного преморбидного фона. Клинически постинфекционная пищевая аллергия проявляется гиперчувствительностью к ранее хорошо переносимым продуктам — молочным смесям, молочным кашам, творогу и др. У детей отмечаются боли в животе, вздутие после кормления, срыгивания, жидкий стул с мутной стекловидной слизью, иногда с прожилками крови, при копрологическом исследовании в кале обнаруживаются эозинофилы. Характерна остановка прибавки массы тела, вплоть до развития гипотрофии.
При выявлении аллергии к белкам коровьего молока в питании детей первого года жизни используются смеси на соевой основе (Нутрилак Соя, Нутрилон Соя, Фрисосой, Хумана СЛ, Энфамил Соя и др.) и на основе гидролизатов белка (Нутрилон Пепти ТСЦ, Нутримиген, Прегестимил, Фрисопеп и др.).
Отсутствие специализированных продуктов не является непреодолимым препятствием в организации безмолочного рациона. Элиминационная диета в этом случае составляется на основе безмолочных протертых каш (рисовой, гречневой, кукурузной), фруктовых и овощных пюре, картофеля, кабачков, цветной капусты, тыквы, из печеного яблока, банана, растительного и сливочного масла, мясного пюре. При этом необходимо учитывать физиологические потребности ребенка в основных пищевых веществах и энергии. Мясное пюре, как основной источник белка, при отсутствии специализированных смесей можно назначать с 2–3-месячного возраста. Предпочтительно использовать конину, мясо кролика, птицы, постную свинину, а также диетические мясные консервы — Конек-Горбунок, Чебурашка, Петушок, Пюре из свинины и др.
У детей старше года принцип составления рациона тот же. При назначении безмолочной диеты необходимо полностью компенсировать недостающее количество животного белка протеинами мяса, соевых смесей, а также исключить из диеты продукты, обладающие повышенной сенсибилизирующей активностью (шоколад, рыба, цитрусовые, морковь, свекла, красные яблоки, абрикосы и другие плоды оранжевой или красной окраски, орехи, мед). При постинфекционной пищевой аллергии срок соблюдения указанной диеты составляет не менее 3 месяцев, а чаще — от 6 до 12 месяцев. Эффект от элиминационной диеты оценивается по исчезновению симптомов заболевания, прибавке массы тела, нормализации стула.
Л. Н. Мазанкова, доктор медицинских наук, профессор Н. О. Ильина, кандидат медицинских наук Л. В. Бегиашвили РМАПО, Москва
Ротавирусная инфекция у детей – острое инфекционное заболевание, вызываемое патогенными ротавирусами и протекающее с преимущественным поражением желудочно-кишечного тракта. При ротавирусной инфекции у детей развивается острый гастроэнтерит с лихорадкой, тошнотой, рвотой, диареей и абдоминальными болями, сопровождающийся интоксикацией и респираторным синдромом. Диагноз ротавирусной инфекции у детей ставится на основании комплекса клинических и эпидемиологических данных и результатов лабораторных исследований. Лечение ротавирусной инфекции у детей включает регидратационную, дезинтоксикационную терапию, лечебную диету, прием спазмолитиков, ферментов, энтеросорбентов, пробиотиков, противовирусных и иммунотропных препаратов.

Общие сведения
Ротавирусная инфекция относится к группе вирусных диарей, встречающихся в любом возрастном периоде, но наиболее часто регистрируется у детей. Это распространенное заболевание в практике педиатров, детских гастроэнтерологов, детских инфекционистов. Естественная восприимчивость детей к ротавирусной инфекции очень высока. Практически все дети переболевают ротавирусной инфекцией (иногда неоднократно) в первые 5 лет жизни, причем 70–80% случаев заболевания приходится на детей в возрасте от 6 месяцев до 2 лет, особенно находящихся на искусственном вскармливании. Дети первых 3-х месяцев жизни болеют ротавирусной инфекцией относительно редко из-за наличия пассивного иммунитета, полученного трапсплацентарно или с грудным молоком, однако при его отсутствии могут заболевать и новорожденные. Повторные случаи ротавирусной инфекции у детей возможны спустя 6-12 месяцев после перенесенного заболевания при заражении другим сероваром ротавируса. Дети, переболевшие ротавирусной инфекцией, обычно легче переносят последующие случаи заболевания.

Причины ротавирусной инфекции у детей
Источником ротавирусной инфекции у детей является больной человек с манифестной или бессимптомной формой заболевания. Механизм передачи ротавирусной инфекции у детей - фекально-оральный, может осуществляться через пищевые продукты (чаще молочные), водопроводную воду, а также через бытовые контакты (грязные руки, загрязненные предметы обихода, игрушки, белье).
Наибольшее выделение вирусных частиц больным наблюдается в первые 3-5 суток заболевания. Ротавирусная инфекция у детей активизируется сезонно; подъем заболеваемости отмечается в зимне-весенний период, иногда возникают спорадические случаи. Нередко отмечаются групповые заболевания и массовые вспышки в детских коллективах (дошкольных и школьных учреждениях, стационарах).
Возбудителями ротавирусной инфекции у детей являются энтеротропные РНК-содержащие вирусы рода Rotavirus, включающие 7 серогрупп (большинство ротавирусов человека относятся к группе A). Ротавирусы высокоустойчивы во внешней среде, сохраняют многомесячную жизнеспособность при замораживании, но быстро погибают при кипячении. Ротавирусная инфекция вызывает повреждение и разрушение микроворсинок тонкой кишки, приводящее к вторичной дисахаридазной недостаточности, накоплению негидролизованных дисахаридов (лактозы), нарушению реабсорбции воды и электролитов, развитию у ребенка диарейного синдрома и дегидратации.
Снижение интерфероногенеза в острую фазу и в период реконвалесценции при ротавирусной инфекции у детей является одной из причин затяжного и хронического течения заболевания.
Симптомы ротавирусной инфекции у детей
Инкубационный период ротавирусной инфекции у детей может продолжаться от 12 часов до 1-5 суток. В клинической картине на первый план выходит поражение ЖКТ в форме острого гастроэнтерита и интоксикация; респираторный синдром может сопровождать или предшествовать основным расстройствам. Симптомы ротавирусной инфекции у детей характеризуются острым началом и развиваются в течение суток, иногда может иметь место продромальный период с незначительным изменением состояния. По тяжести течения ротавирусная инфекция разделяется на легкую, среднетяжелую и тяжелую формы. Могут иметь место атипичные стертые формы (как правило, у недоношенных и новорожденных детей), а также носительство ротавируса. Ротавирусная инфекция у детей имеет циклическое течение, тяжесть заболевания зависит от продолжительности и степени дегидратации (эксикоза I, II, III степени) и интоксикации.
В стадию выраженных клинических проявлений отмечается лихорадка (38,5-39ºC), тошнота, рвота повторного или многократного характера, диарея, абдоминальные боли, метеоризм, урчание по ходу кишечника. Для ротавирусной инфекции у детей характерен обильный, водянисто-пенистый стул желто-зеленого цвета, с резким запахом, без видимых патологических примесей, иногда со слизью. В зависимости от тяжести заболевания частота стула колеблется от 3 до 20 раз в сутки; диарея сохраняется до 3-7 дней.
Интоксикационный синдром у детей при легком и среднетяжелом течении ротавирусной инфекции характеризуется резкой слабостью, бледностью кожных покровов, головной болью, в тяжелых случаях – адинамией, головокружением, обморочным состоянием, судорогами мышц конечностей; у детей первого года жизни отмечается падение массы тела, снижение тургора тканей.
Респираторными проявлениями ротавирусной инфекции у детей служат умеренная гиперемия и боль в горле, насморк, небольшой суховатый кашель, конъюнктивит. Выздоровление при ротавирусной инфекции у детей наступает обычно через 5-12 дней, при тяжелом течении - позднее.
Осложнениями ротавирусной инфекции у детей могут выступать циркуляторные расстройства, острая сердечно-сосудистая и почечная недостаточность, присоединение бактериальной инфекции, обострение имеющейся гастроэнтерологической патологии - хронического гастрита, энтероколита, дисбактериоза кишечника.
Диагностика
Диагноз ротавирусного гастроэнтерита у детей ставится на основании комплекса клинических и эпидемиологических данных, результатов лабораторных исследований (вирусологических, бактериологических, серологических, молекулярно-генетических).
Учитываются ведущий клинический синдром, сочетание и последовательность появления симптомов, локализация патологического процесса (гастрит, энтерит, колит и т. д.), возраст ребенка, наличие острой кишечной инфекции в его окружении, предполагаемый источник заражения, сезонность. Диагностика ротавирусной инфекции у детей облегчается при наличии семейного очага или эпидемической вспышки заболевания.
Подтверждением ротавирусной инфекции у детей является обнаружение вирусных частиц и антигенов, вирусной РНК и специфических антител в фекалиях, рвотных массах, сыворотке крови. Генетический материал ротавируса в фекалиях позволяют выявить ПЦР, метод точечной гибридизации, электрофорез РНК в ПААГ. Морфологическая идентификация ротавирусной инфекции у детей проводится с помощью электронной микроскопии, ИФА, РПГА, реакции диффузной преципитации, латекс-агглютинации, РИФ, выделения ротавируса в культуре клеток, радиоиммунного анализа (РИА). Определение специфических антител к ротавирусу в крови больного (методами твердофазной реакции коагглютинации, РТГА, РСК, РНВ) проводят с 5-го дня от начала заболевания.
При ротавирусной инфекции у детей результаты бактериологического исследования кала на основные кишечные инфекции – отрицательные. Вспомогательное значение в постановке диагноза имеет микроскопическое исследование кала – копрограмма, общий анализ мочи и крови.
Дифференциальная диагностика ротавирусной инфекции у детей проводится с дизентерией, сальмонеллезом, эшерихиозом, легкими формами холеры, пищевым отравлением, вирусными диареями другой этиологии (энтеровирусными и др.). В сложных, сомнительных случаях может быть проведена ректороманоскопия с аспирационной биопсией слизистой оболочки толстой кишки.
Лечение ротавирусной инфекции у детей
При ротавирусной инфекции у детей очень важны ранняя диагностика и своевременно начатое лечение. Дети с тяжелой и среднетяжелой формой ротавирусной инфекции подлежат госпитализации. Терапия заболевания является патогенетической и направлена на борьбу с дегидратацией, функциональными нарушениями со стороны сердечно-сосудистой и мочевыделительной систем, расстройствами пищеварения.
При развитии обезвоживания проводят регидратационную терапию: при I-II степени эксикоза ограничиваются пероральным приемом регидрона, глюкосолана; при III степени эксикоза – парентерально применяются растворы трисоль, ацесоль; с целью дезинтоксикации и улучшения гемодинамики - гемодез, полиглюкин. В случае необходимости назначаются жаропонижающие и спазмолитические препараты.
При ротавирусной инфекции применяются энтеросорбенты (активированный уголь, комбинированные препараты), ферменты (панкреатин), пробиотики (лактобактерии, бифидобактерии), пребиотики (лактулоза). Показана лечебная щадящая диета, соответствующая тяжести течения заболевания и возрасту ребенка. В острый период из пищевого рациона исключаются молоко и молочные продукты, ограничивается пища, богатая углеводами.
Этиотропное лечение ротавирусной инфекции у детей может включать противовирусные и иммунотропные средства (умифеновир, иммуноглобулин, рекомбинантный интерферон альфа), помогающие сокращению сроков клинических проявлений заболевания.
Прогноз и профилактика ротавирусной инфекции у детей
Прогноз ротавирусной инфекции зависит от тяжести клинических проявлений: при легкой и среднетяжелой форме – исход практически всегда благоприятный; при резком и длительном обезвоживании из-за развития сердечно-сосудистой и почечной недостаточности возможен летальный исход, особенно у детей из групп риска (новорожденных, недоношенных, детей с гипотрофией).
В целях профилактики ротавирусной инфекции у детей необходимо соблюдение правил личной гигиены и питания, грудное вскармливание, раннее выявление больных и их своевременная изоляция, соблюдение санитарно-гигиенического режима в очаге заболевания (семье и детском учреждении). В качестве специфической профилактики ротавирусной инфекции у детей используется вакцинация живыми оральными вакцинами.
Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободком, поэтому их стали называть ротавирусами (лат. rotа — колесо). Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гаст
Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободком, поэтому их стали называть ротавирусами (лат. rotа — колесо).
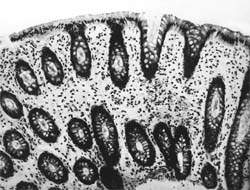 |
| Рисунок 1. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимально выраженный катаральный колит. х 100. |
Ротавирусы представляют собой род семейства Reoviridae, который объединяет большое количество сходных по морфологии и антигенной структуре вирусов, вызывающих гастроэнтерит у человека, млекопитающих и птиц. Систематическое изучение ротавирусов человека началось с 1973 года, когда они были обнаружены при электронной микроскопии ультратонких срезов биоптатов слизистой оболочки двенадцатиперстной кишки, полученных от больных острым гастроэнтеритом детей Австралии (Р. Бишоп и соавторы). В том же году Т. Флеветт обнаружил сходный вирус в копрофильтратах больных гастроэнтеритом методом электронной микроскопии при негативном контрастировании препаратов.
Вирусные частицы имеют диаметр от 65 до 75 нм. При проникновении контрастирующего вещества в вирион выявляется электронно-плотный центр диаметром 38 — 40 нм, который представляет собой так называемую сердцевину, окруженную электронно-прозрачным слоем. Внешний вид вирусных частиц напоминает колесо с широкой ступицей, короткими спицами и четко очерченным ободом, поэтому их стали называть ротавирусами (лат. rota — колесо).
Ротавирусы имеют две белковые оболочки — наружный и внутренний капсиды. Сердцевина содержит внутренние белки и генетический материал, представленный двунитчатой фрагментированной РНК. Геном ротавирусов человека и животных состоит из 11 фрагментов, которые могут быть разделены при электрофорезе в полиакриламидном геле (ПААГ) или агарозе. В составе ротавирусов обнаружено четыре антигена; основной из них — это групповой антиген, обусловленный белком внутреннего капсида. С учетом группоспецифических антигенов все ротавирусы делятся на пять групп: A, B, C, D, E. Ротавирусы одной группы имеют общий групповой антиген, который выявляется иммунологическими реакциями: иммуноферментный анализ, иммунофлюоресценция, иммунная электронная микроскопия и др. Большинство ротавирусов человека и животных относятся к группе A.
| Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями |
Источником инфекции при ротавирусном гастроэнтерите является инфицированный человек — больной манифестной формой заболевания или бессимптомно выделяющий ротавирусы с фекалиями. Вирусы в фекалиях заболевших появляются одновременно с развитием клинических симптомов, наибольшая концентрация их в кале (до 109 — 1011 вирусных частиц в 1 г) регистрируется в первые 3 — 5 дней болезни. В эти дни больные представляют наибольшую эпидемиологическую опасность для лиц, контактирующих с ними. Наиболее частым источником заболевания для детей первого года жизни являются инфицированные ротавирусом матери; для взрослых и детей более старшего возраста — дети, в основном из детских коллективов. Возможность заражения человека от животных не доказана.
Патогенез ротавирусной инфекции характеризуется проникновением вируса в эпителиоциты слизистой оболочки желудочно-кишечного тракта, преимущественно тонкой кишки, что приводит к их повреждению и отторжению от ворсинок. Вследствие этого на ворсинках тонкой кишки появляются функционально и структурно незрелые энтроциты с низкой способностью синтезировать пищеварительные ферменты. При ротавирусном гастроэнтерите это проявляется снижением уровня дисахаридаз, развивается вторичная дисахаридазная недостаточность, при которой в просвете тонкой кишки накапливаются нерасщепленные дисахариды, что создает повышенное осмотическое давление и приводит к выводу в просвет кишечника воды и электролитов из тканей организма. Это является основной причиной диареи и дегидратации и определяет основные клинические проявления болезни.
Ротавирусный гастроэнтерит как инфекционное заболевание имеет циклическое течение. Инкубационный период продолжается чаще всего от 12 — 24 часов до двух суток. Клиническая картина ротавирусного гастроэнтерита характеризуется в основном острым началом, однако в ряде случаев может иметь место продромальный период длительности от 12 до 48 — 72 часов. В этот период больные отмечают недомогание, общую слабость, повышенную утомляемость, снижение аппетита, головную боль, познабливание, урчание и неприятные ощущения в животе, умеренно выраженные катаральные явления: заложенность носа, першение в горле, легкий кашель.
В клинической картине ротавирусного гастроэнтерита в период развернутых клинических проявлений ведущими являются синдромы гастроэнтерита и интоксикации. Выраженность диареи и обусловленной ею той или иной степени дегидратации организма, а также токсикоза, продолжительность этих симптомов в значительной мере определяет тяжесть течения заболевания.
Синдром гастроэнтерита характеризуется развитием диареи, снижением аппетита, появлением урчания и болей в животе, тошноты и рвоты. Наиболее типичен для ротавирусного гастроэнтерита обильный водянистый пенистый стул желтого или желто-зеленого цвета. У больных с легким течением заболевания стул может быть кашицеобразным. Как правило, патологические примеси в стуле отсутствуют. Боль локализуется преимущественно в верхней половине живота или является диффузной, она может быть разной интенсивности. Почти всегда она сопровождается громким урчанием в животе.
Синдром интоксикации появляется в самом начале заболевания. Слабость, зачастую резкая, является наиболее частым проявлением этого синдрома; реже отмечается головная боль. При более тяжелом течении имеют место головокружение, обморочное состояние, коллапс. Обращает на себя внимание следующая особенность ротавирусного гастроэнтерита: два ведущих в клинической картине болезни синдрома развиваются в процессе заболевания не всегда однонаправленно; у некоторых больных на фоне сравнительно слабо выраженных диспепсических явлений могут наблюдаться резко выраженные симптомы общей интоксикации, особенно слабость.
Повышение температуры тела не всегда может отмечаться при ротавирусном гастроэнтерите, особенно у взрослых. У некоторых больных может быть озноб без повышения температуры. В то же время нередко в разгар заболевания выраженность лихорадочной реакции варьируется от субфебрильных цифр и выше и может достигать 38 — 39°С как у детей, так и у взрослых.
Важным в диагностическом плане для ротавирусного гастроэнтерита считается сочетание двух ведущих клинических синдромов с симптомами поражения верхних дыхательных путей. Катаральный синдром встречается приблизительно у 50% больных и проявляется в виде гиперемии и зернистости слизистых оболочек мягкого неба, небных дужек, язычка, задней стенки глотки, а также насморка, заложенности носа, кашля, болей в горле. В ряде случаев катаральные симптомы наблюдаются уже в продромальном периоде, до проявления симптомов гастроэнтерита.
В разгар болезни отмечается изменение функционального состояния сердечно-сосудистой системы, чаще у пациентов с более тяжелым течением и при наличии сопутствующих заболеваний органов кровообращения. У большинства пациентов отмечается тенденция к артериальной гипертензии, тахикардия, определяется глухость сердечных тонов при аускультации. У больных с тяжелым течением заболевания, как правило, возникают обмороки и коллапсы из-за выраженных расстройств гемоциркуляции, в генезе которых наряду с токсическими воздействиями существенное значение имеет гиповолемия. Потери жидкости и электролитов вследствие рвоты и диареи могут быть значительными и приводят к развитию дегидратации. Клинические проявления дегидратации зависят от ее степени. При легком и среднетяжелом течении ротавирусного гастроэнтерита отмечается жажда, сухость во рту, слабость, бледность (дегидратация I — II степени), при тяжелом течении наряду с этими симптомами наблюдаются также осиплость голоса, судороги мышц конечностей, акроцианоз, снижение тургора кожи, уменьшение диуреза (дегидратация III степени).
В связи с развитием при ротавирусном гастроэнтерите возможных осложнений, главным образом циркуляторных расстройств, острой сердечно-сосудистой недостаточности, нарушений гомеостаза, выделяют группы больных повышенного риска, в которые включают новорожденных, детей младшего возраста, лиц пожилого возраста, а также больных с тяжелыми сопутствующими заболеваниями. Описанные в литературе и наблюдавшиеся нами случаи ротавирусного заболевания с летальным исходом относятся именно к этим группам.
Выделяются две основные клинические формы ротавирусного заболевания — гастроэнтерическая и энтерическая. Симптомы только острого гастрита (гастритический вариант) встречаются в 3 — 10% случаев. Функциональные и морфологические нарушения со стороны желудочно-кишечного тракта, возникающие при ротавирусном гастроэнтерите в случае наличия у пациентов фоновой гастроэнтерологической патологии, нередко способствуют развитию таких осложнений основного заболевания, как обострение сопутствующих болезней: хронического гастрита, энтероколита, панкреатита, часто в сочетании с выраженными явлениями дисбактериоза кишечника, требующими коррекции при лечении.
Методы диагностики ротавирусной инфекции
При ротавирусном гастроэнтерите гемограмма изменяется следующим образом: в остром периоде заболевания с высокой частотой выявляются лейкоцитоз с нейтрофилезом и повышенная СОЭ. В периоде реконвалесценции картина крови обычно нормализуется полностью. Изменения урограммы у большинства больных имеют кратковременный характер и проявляются чаще всего небольшой протеин-, лейкоцит- и эритроцитурией; в редких случаях в моче появляются гиалиновые цилиндры в незначительном количестве. При тяжелом течении заболевания нарушения функции почек могут быть более выраженными, с повышением уровня мочевины крови, олигоурией или анурией, снижением клубочковой фильтрации. На фоне проводимой терапии указанные изменения быстро исчезают и при повторных обследованиях не отмечаются.
В качестве примера, иллюстрирующего особенности клинического течения ротавирусного гастроэнтерита, приводим выписку из истории болезни.
Лечение: обильное питье солевых растворов, парентеральная регидратационная и дезинтоксикационная терапия — трисоль 1000 мл внутривенное капельное введение, внутрь ферментные препараты: абомин, панкреатин, тансол, карболен. Течение заболевания без осложнений. На третий день болезни — субфебрильная температура, оставалась слабость; боли в животе прекратились. Стул кашицеобразный до пятого дня от начала заболевания. Полное выздоровление наступило на седьмой день болезни.
Дифференциальный диагноз у больных ротавирусным гастроэнтеритом проводят с другими острыми кишечными инфекциями как вирусной так и бактериальной этиологии, прежде всего в тех случаях, когда в клинической картине на первый план выступает синдром гастроэнтерита: с вирусными диареями различной этиологии (аденовирусы, коронавирусы, астровирусы, калицивирусы, вирус Норфолк, энтеровирусы Коксаки и ЕСНО); с гастроинтестинальной формой сальмонеллеза, с гастроэнтеритическим и гастроэнтероколитическим вариантами острой дизентерии, с пищевыми токсикоинфекциями, вызванными условно-патогенными бактериями; с холерой.
Обнаружение специфических антител и нарастание их титра в сыворотке крови больных и переболевших ротавирусным гастроэнтеритом при помощи серологических реакций с целью текущей диагностики на практике в настоящее время широкого распространения не получило и используется в основном для ретроспективного анализа различных эпидемиологических ситуаций.
Методы обнаружения вирусспецифической РНК, которые можно назвать высокочувствительными и специфичными, имеют, однако, ряд недостатков, ограничивающих их практическое применение (необходимость наличия специальной аппаратуры, реактивов, квалифицированного персонала и др.) Наиболее простой метод в этой группе — электрофорез ротавирусной РНК в полиакриламидном геле. Этот метод, позволяющий идентифицировать штаммы вирусов, вызвавшие заболевание, и дать характеристику штаммов, циркулирующих на данной территории, в основном применяется при эпидемиологических исследованиях.
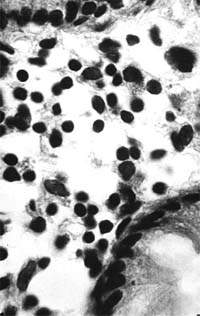 |
| Рисунок 2. Слизистая оболочка толстой кишки при ротавирусном гастроэнтерите. Минимальное содержание плазматических клеток в собственной пластинке, увеличение в ней числа макрофагов. х 400 |
В клинической практике врач нередко сталкивается с обстоятельствами (сомнительные результаты вирусологических и серологических исследований, случаи микст-инфекций), когда возникает необходимость в применении дополнительных методов для верификации диагноза. С этой целью может быть использован доступный для практического здравоохранения интрументальный метод исследования — ректороманоскопия с аспирационной биопсией слизистой оболочки толстой кишки. При гистологическом, морфометрическом и гистохимическом исследованиях биоптатов при ротавирусном гастроэнтерите выявляются характерные изменения в виде поверхностного минимально выраженного катарального колита с незначительной дистрофией эпителия (рис. 1), снижения числа серотонинсодержащих желудочно-кишечных эндокриноцитов (ЕС-клетки) в эпителиальном пласте кишечных желез, умеренной инфильтрацией собственной пластинки плазматическими клетками и увеличением в ней числа макрофагов (рис. 2). Эти особенности имеют дифференциально-диагностическое значение, поскольку отличаются указанным показателем от других острых кишечных инфекций, что может быть использовано в диагностически сложных случаях.
Здравоохранение в настоящее время не располагает препаратами, обладающими специфическим антиротавирусным действием, поэтому терапия ротавирусного гастроэнтерита является патогенетической. Основные ее цели — борьба с дегидратацией, токсикозом и связанными с ними наиболее часто встречающимися при ротавирусном гастроэнтерите нарушениями функции жизненно важных органов — сердечно-сосудистой системы и органов мочевыделения, степень выраженности которых во многом определяет тяжесть течения заболевания и его прогноз.
Для правильного выбора характера и объема проводимой регидратационной терапии в первую очередь необходимо установить степень дегидратации у того или иного пациента. При эксикозе I — II степени следует ограничиваться пероральной регидратационной терапией (препараты регидрон, глюксолан и др.). При дегидратации III степени целесообразно прибегать к комбинированной парентеральной и пероральной регидратации. Для парентеральной регидратации применяют растворы трисоль, квартасоль, ацесоль и др. С целью дезинтоксикации и улучшения гемодинамики при среднетяжелом и тяжелом течении заболевания показаны коллоидные растворы (гемодез, полиглюкин и др.).
| Для ротавирусной инфекции характерно сочетание гастроэнтерита, интоксикации и симптомов поражения верхних дыхательных путей |
Современными представлениями о патогенезе диарейного синдрома при ротавирусном гастроэнтерите обусловлено и назначение соответствующих средств, способствующих нормализации состояния пищеварительного тракта, а также диеты. Учитывая нарушения активности ряда пищеварительных ферментов, в частности лактазы, рекомендуется исключить в острый период заболевания из пищевого рациона больных молоко и молочные продукты. Кроме того, по этой же причине целесообразно ограничивать и пищу, богатую углеводами. В связи с вышеизложенным, в острый период необходимы энзимные препараты (панзинорм-форте, фестал и др). Кроме того, в остром периоде заболевания могут быть использованы адсорбирующие и вяжущие средства, способствующие ускоренному формированию стула (смекта, карболен и др.) также возможно применение хилака-форте. Высокой частотой дисбактериозов кишечника различной степени выраженности у больных ротавирусным гастроэнтеритом обусловлена необходимость применения в комплексной терапии бактерийных биологических препаратов. Лучшая терапевтическая эффективность при ротавирусном гастроэнтерите отмечена при применении лактосодержащих бактерийных биологических препаратов (ацилакт, лактобактерин и др.), что, по-видимому, связано с заместительным действием бактериальной лактазы, содержащейся в лактобактериях. В последние годы в комплексной терапии ротавирусного гастроэнтерита начал применяться комплексный иммуноглобулиновый препарат (КИП), который разработан и выпускается в МНИИЭМ им. Г. Н. Габричевского. Это первый отечественный иммуноглобулиновый препарат для энтерального применения. КИП характеризуется повышенной концентрацией антител к микроорганизмам, возбудителям острых кишечных инфекций, в том числе ротавирусам, сальмонеллам, шигеллам, эшерихиям и др. Применение КИП в комплексной терапии больных ротавирусным гастроэнтеритом оказывает отчетливый положительный терапевтический эффект, существенно сокращая продолжительность интоксикации и диареи, что открывает новые возможности в лечении этого заболевания.
Литература
1. Букринская А. Г., Грачева Н. М., Васильева В. И. Ротавирусная инфекция. М., 1989.
2. Дроздов С. Г., Покровский В. И., Шекоян Л. А., Машилов В. П. и др. Ротавирусный гастроэнтерит. М., 1982.
3. Новикова А. В. и др. Архив патологии, 1989, №6.
4. Щербаков И. Т. и др. Архив патологии, 2995, №3.
5. Юшук Н. Д., Царегородцев А. Д.. Лекции по инфекционным болезням. М., 1996.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Ротавирусная инфекция: причины появления, симптомы, диагностика и способы лечения.
Определение
Ротавирусная инфекция (ротавирус) – это острое инфекционное заболевание, вызываемое ротавирусом и характеризующееся поражением желудочно-кишечного тракта по типу гастроэнтерита с развитием синдрома дегидратации (обезвоживания).
Причины появления ротавирусной инфекции
Возбудителем заболевания выступает вирус семейства Reoviridae, рода Rotavirus. Ротавирусы устойчивы к воздействию факторов окружающей среды, в питьевой воде, открытых водоемах и сточных водах они сохраняют жизнеспособность до нескольких месяцев, на овощах и фруктах – до 30 дней.
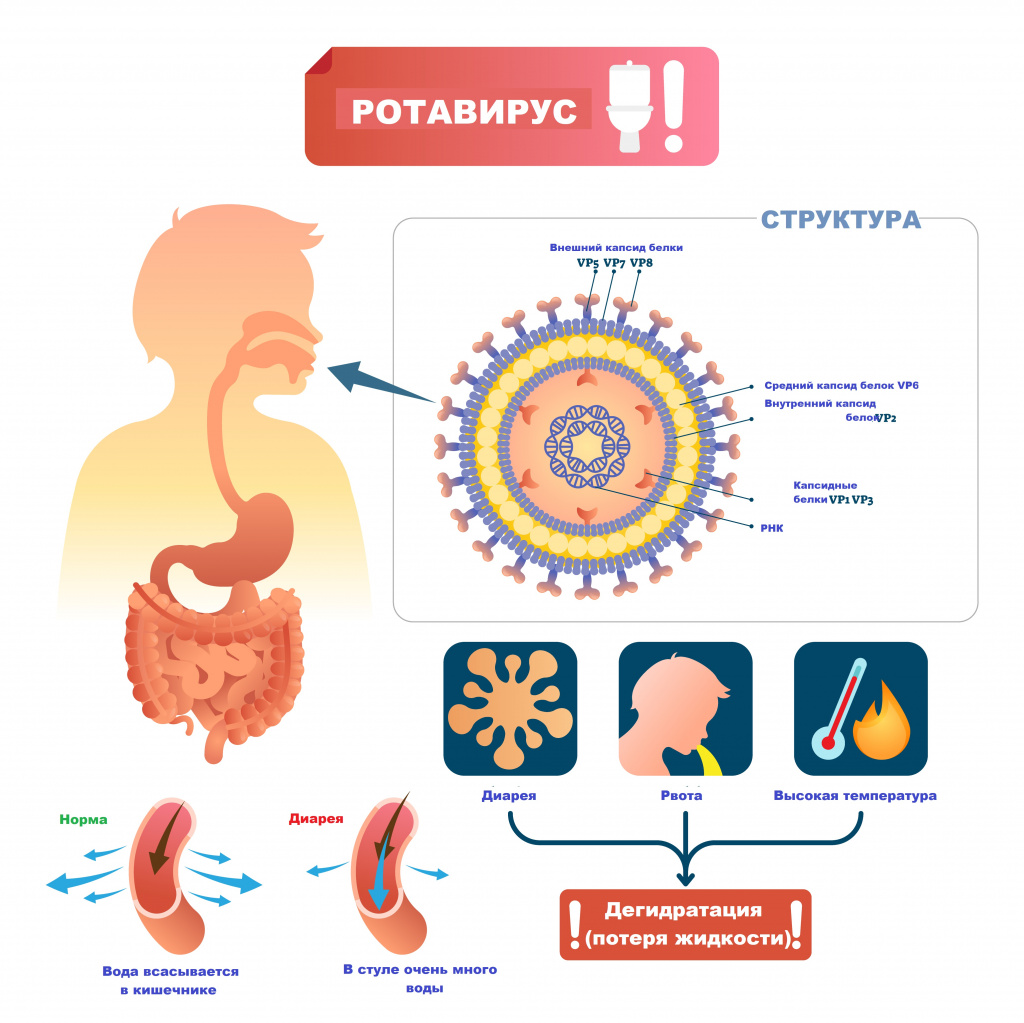
Основной источник и резервуар ротавирусной инфекции – больной человек в конце инкубационного периода и в первые дни болезни, выделяющий с фекалиями вирус, а также вирусоносители. Механизм передачи возбудителя – фекально-оральный.
- контактно-бытовой (через грязные руки и предметы обихода);
- водный (при употреблении воды, в которой присутствуют вирусы);
- пищевой (чаще всего при употреблении молока, молочных продуктов);
- реже – воздушно-капельный путь.
Ротавирусным гастроэнтеритом болеют люди любого возраста, но максимальная заболеваемость отмечается у детей первых двух лет жизни, людей пожилого возраста и лиц с нарушением функционирования иммунной системы.
Наблюдается зимне-весенняя сезонность, спорадические случаи заболевания регистрируются в течение всего года.
Ротавирусы проникают внутрь эпителия слизистой оболочки двенадцатиперстной кишки и верхних отделов тощей кишки. Размножение и накопление вируса приводит к гибели зрелых эпителиоцитов кишки и их отторжению. В результате нарушается абсорбция углеводов и простых сахаров, и они накапливаются в избыточном количестве. В просвете кишечника повышается осмотическое давление, нарушается всасывание воды и электролитов. Возникает водянистая диарея. Образование большого количество органических кислот, водорода, углекислого газа в процессе ферментации нерасщепленных дисахаридов кишечной микрофлорой ведет к повышению газообразования в кишечнике.
У детей с иммунными нарушениями ротавирус может стать причиной развития гепатита, нефрита, пневмонии, экзантемы, энцефалита с высоким риском летального исхода.
Классификация заболевания
Формы ротавирусной инфекции:
- типичная (гастрит, гастроэнтерит, энтерит);
- атипичная (стертая, бессимптомная);
- вирусоносительство.
- легкое;
- среднетяжелое;
- тяжелое.
- гладкое;
- негладкое (с обострениями и рецидивами).
- острое (до 1 месяца);
- затяжное (до 3 месяцев);
- хроническое (более 3 месяцев).
Инкубационный период ротавирусной инфекции составляет от 14 часов до 7 дней (в среднем 1-4 дня). Заболевание чаще всего начинается остро с повышения температуры тела от субфебрильных до фебрильных значений, появляются симптомы интоксикации (вялость, слабость, снижение аппетита), диарея и повторная рвота.
Кишечная дисфункция характеризуется жидким, водянистым, пенистым стулом желтого цвета без патологических примесей. При обильном жидком стуле развивается обезвоживание.
В тяжелых случаях возможно уменьшение количества мочи вплоть до полного ее отсутствия, снижение артериального давления.
В течение 3–6 дней могут присутствовать умеренные или сильные схваткообразные или постоянные боли в верхней половине живота. У детей младшего возраста в начале заболевания могут наблюдаться катаральные явления, которые предшествуют дисфункции кишечника: покашливание, насморк или заложенность носа, редко – конъюнктивит, катаральный отит. У детей раннего возраста на фоне высокой температуры могут развиться генерализованные судороги, сопровождающиеся потерей сознания.
Для легких форм ротавирусной инфекции характерны следующие симптомы:
- температура тела 37,1-38,0°C;
- умеренная интоксикация в течение 1–2 дней;
- нечастая рвота;
- стул жидкой кашицей до 5-10 раз в сутки.
- температура тела 38,0-39,0°C;
- выраженная интоксикация;
- повторная рвота в течение 1,5-2 дней;
- обильный водянистый стул от 10 до 20 раз в сутки;
- обезвоживание I–II степени.
- бурным началом;
- значительными потерями жидкости (обезвоживание II–III степени),
- многократной рвотой;
- водянистым стулом более 20 раз в сутки;
- снижением артериального давления.
Типичный ротавирусный гастроэнтерит характеризуется доброкачественным циклическим течением, наличием специфических признаков заболевания, а также обнаружением возбудителя в фекалиях.
К атипичным формам ротавирусного гастроэнтерита относятся:
- стертая и субклиническая формы со слабо выраженными и быстро проходящими симптомами;
- бессимптомная форма с отсутствием клинических признаков болезни, но с нарастанием титров специфических антител в крови;
- носительство ротавирусов после перенесенного острого ротавирусного гастроэнтерита, у здоровых лиц в очагах с инфекционной диареей;
- хроническая форма, сохраняющаяся более 3 месяцев.
Сочетание поражения желудочно-кишечного тракта и симптомов интоксикации, развитие обезвоживания, наличие ротавирусной инфекцией у лиц, контактирующих с больным, имеют большое значение в диагностике заболевания.
Окончательный диагноз ротавирусной инфекции ставится только на основании лабораторного подтверждения. Используют:
- методы, основанные на обнаружении ротавируса и его антигенов в фекалиях (электронная и иммуноэлектронная микроскопия, РЛА, ИФА);
- методы обнаружения вирусной РНК в копрофильтратах (метод молекулярных зондов – ПЦР и гибридизации, электрофорез РНК в полиакриламидном геле или агарозе);
- методы обнаружения специфических антител к ротавирусам в сыворотке крови (ИФА, РСК, РТГА, РНГА).
Читайте также:

