Ротавирусная инфекция при сахарном диабете
Обновлено: 17.04.2024
Наибольшую угрозу с наибольшим количеством осложнений, вплоть до возникновения критических дисфункций и летального исхода, ОРВИ и грипп представляют для пациентов с диабетом и сердечно-сосудистой патологией.
Простудным заболеваниям, самой распространенной группе инфекционных патологий, подвержены люди любых возрастов и социальных групп. Наибольшую угрозу, однако, ОРВИ и грипп представляют для пациентов с нарушениями функционирования сердечно-сосудистой и эндокринной систем. Именно у них, согласно медицинской статистике, наблюдается наибольшее количество осложнений, вплоть до возникновения критических дисфункций и летального исхода.
Сахарный диабет и сердечно-сосудистая недостаточность являются заболеваниями системными, они негативно влияют на состояние всех органов, в значительной мере снижают сопротивляемость организма к любой инфекции. Из-за слабой реактивности иммунной системы респираторная инфекция часто протекает длительно, возникают осложнения: синуситы, бронхиты, пневмония. Высокая активность инфекционного процесса в свою очередь приводит к еще большей декомпенсации основного заболевания, замыкая порочный круг.
Сахарный диабет нередко наблюдается совместно с гипертонической болезнью и атеросклерозом в составе метаболического синдрома. Такие пациенты при простуде требуют особенно внимательного наблюдения, как со стороны терапевта, так и со стороны кардиолога и эндокринолога.
ОРВИ при сахарном диабете
При инфекционном процессе запускается каскад биохимических реакций, способствующих, в том числе, активному синтезу кортикостероидов, обладающих контринсулярным действием: гормон блокирует работу инсулина на клеточном уровне и тормозит его образование в поджелудочной железе. Суммарное действие кортикостероидов и других биологически активных веществ существенно превосходит эффект инсулина в привычной пациенту дозировке.
При отсутствии должного контроля уровня гликемии, который при ОРВИ желательно проводить каждые 2-3 часа, значительно повышается риск кетоацидоза или гиперосмолярной комы. Нередки случаи, когда ухудшение состояния пациента принимается за явления вирусной интоксикации и непосредственная угроза для жизни диагностируется поздно.
ОРВИ при ИБС
Западные публикации свидетельствуют, что РНК вирусов гриппа обнаруживаются в атеросклеротических бляшках 2 . Таким образом вирусный агент, вероятно, сохраняется в организме, вызывая персистирующую инфекцию и, одновременно, прогрессивный рост бляшки за счет активации аутоиммунных механизмов 3 4 .
Во время простуды в крови существенно повышается концентрация С-реактивного белка, общего холестерина, триглицеридов, молекул адгезии к эндотелию. Моноциты, инфицированные вирусом гриппа, обладают прокоагулянтными свойствами, а некоторые цитокины (интерлейкины 6, 8) могут инициировать за счет локального воспаления разрыв атеросклеротической бляшки 5 .Таким образом, при ОРВИ имеется большой риск нестабильности бляшки, ее роста и/или отрыва с окклюзией коронарной артерии.
Проблема терапии ОРВИ и гриппа у коморбидных больных
ОРВИ и грипп осложняют течение сердечно-сосудистой патологии и сахарного диабета и резко повышают вероятность декомпенсации заболевания. Именно поэтому поиск препаратов для защиты таких пациентов, максимально быстрого и безопасного лечения ОРВИ, является очень насущным вопросом.
Большинство существующих противовирусных препаратов работает только против вируса гриппа, что затрудняет их назначение. Сами препараты довольно агрессивные, имеют длинный список противопоказаний и побочных эффектов. Так, их назначения следует избегать при нарушениях со стороны почек и печени, которые нередко сопровождают ИБС и диабет.
Необходимо также учитывать проблему лекарственного взаимодействия: противовирусные и симптоматические препараты нередко плохо сочетаются со средствами постоянной терапии основных заболеваний.
Противовирусное действие интерферона и препараты его эндогенного синтеза
В последнее время средствами выбора при коморбидной патологии все чаще называют препараты интерферона и стимуляторы его эндогенного синтеза. Противовирусная активность интерферона всесторонне изучена и доказана. Она базируется на препятствовании проникновению вирусного агента в клетку, активации синтеза специфических веществ, нарушающих вирусную репликацию и на ускоренном лизисе инфицированных клеток 6 .
Релиз-активные препараты Эргоферон и Анаферон способствуют повышению продукции эндогенных интерферонов при контакте организма с вирусной инфекцией, а также улучшают связывание молекулы интерферона со своим рецептором, обеспечивая нормальное протекание противовирусного иммунного ответа. Данные препараты обладают рядом преимуществ:
• Они почти не имеют противопоказаний.
• Имеют благоприятный профиль безопасности, а риск атопических реакций гораздо ниже, чем при приеме натурального интерферона
• Их можно легко принимать с препаратами других фармакологических групп
• Благодаря сочетанию нескольких механизмов действия, назначение Эргоферона или Анаферона позволит максимально снизить дозу симптоматических средств и, соответственно, нагрузку на печень.
• Эндогенный синтез интерферона коррелирует с содержанием в организме вируса, благодаря чему отсутствует риск гиперстимуляции системы интерферона.
Как работают релиз-активные препараты
Эффективность Анаферона и Эргоферона обусловлена содержанием аффинно очищенных антител в релиз-активной форме. Недавние исследования убедительно показали, что антитела в релиз-активной форме (РА АТ) к ИФН-у модифицируют пространственную структуру ИФН, вызывая конформационные изменения именно в тех участках молекулы, которые ответственны за связывание интерферона-y с его рецептором. Данные препараты реализуют свои терапевтические эффекты за счет влияния на молекулы регуляторы и медиаторы, участвующие в формировании противовирусного иммунного ответа и развитии инфекционного воспаления.
По мере элиминации вирусных частиц, синтез эндогенного интерферона постепенно снижается до нормальных значений, а в случае обострения – снова активизируется. Такая гибкость действия препаратов на основе РА АТ помогает избежать гиперстимуляции и гипореактивности системы интерферона.
Наряду с противовирусным, иммуномодулирующим и противовоспалительным действием, Эргоферон также оказывает антигистаминный эффект за счет содержания РА АТ к CD-4 и гистамину 7 .
Клинические доказательства эффективности Эргоферона
Доказательная база представлена рандомизированными клиническими исследованиями, в том числе с участием пациентов с нарушениями работы эндокринной и сердечно-сосудистой систем.
В 2016 году Яковлевой Е. Е. была проведена работа по изучению применения Эргоферона при ОРВИ у пациентов с внелегочной патологией. Пациенты из группы, принимавшей Эргоферон, продемонстрировали высокие темпы выздоровления и положительную динамику в оценке показателей физиологической адаптации по опроснику Л. Х. Гаркави 8 .
В исследовании Шаповаловой Ю. С. Эргоферон назначался при простуде пациентам кардиологического профиля, госпитализированным по поводу нестабильной стенокардии, острого инфаркта миокарда, хронической сердечной недостаточности. В 60% случаев Эргоферон назначался в виде монотерапии, в 40% - с другими противовирусными препаратами. Симптомы ОРВИ полностью купировались на 5-10 день приема препарата. У пациентов не отмечалось нежелательных реакций или ухудшения показателей по основному заболеванию 9 .
Препараты на основе антител к ИФН-у в релиз-активной форме соответствуют всем критериям безопасности при назначении пациентам с сердечно-сосудистой патологией и сахарным диабетом. Клинические исследования показывают отличную переносимость препаратов, их высокую противовирусную активность. Восстановление нормального иммунного ответа организма при ОРВИ позволит свести к минимуму риск опасных осложнений хронических заболеваний.
1) Жукова Ю.В, Масычева В.И, Никитин Ю. П. Влияние острых респираторных вирусных инфекций на течение ишемической болезни сердца. Сибирскийнаучныймедицинскийжурнал. 2008.
3) Плесков В.М., Банников А.И., Гуревич В.С., ПлесковаЮ.В. Вирусыгриппаиатеpосклеpоз: pольатеpосклеpотическихбляшеквподдеpжаниипеpсистентнойфоpмыгpиппознойинфекции // Вестн. РАМН. 2003(4) 4. 10-13 c.
4) Gurevich V.S., Pleskov V.M., Levaya M.V. Autoimmune nature of influenza atherogenicity // Ann. NY Acad. Sci. 2005. 1050(2): 410-416 p.
5) Bouwman J.J., Visseren F.L., Bosch M.C. et al. Procoagulant and inflammatory response of virus-infected monocytes//Eur. J. Clin. Invest. 2002. 32(10):759-766p.
8) Яковлева Е.В. Эргоферон: возможность оптимального комплексного подхода в лечении ОРВИ у взрослых. Рецепт. 2016;2:196-206.
Согласно результатам статьи, опубликованной в журнале Public Library of Science, ротавирусная инфекция может играть роль в развитии сахарного диабета 1 типа.
Основной причиной детского гастроэнтерита на сегодняшний день является ротавирусная инфекция. Появление вакцины против данного вируса позволило значительно снизить смертность от вызываемого им заболевания. Проведенные ранее исследования позволили обнаружить роль ротавирусной инфекции в развитии сахарного диабета 1 типа у генетически предрасположенных к нему людей. Кроме того, австралийским ученым удалось обнаружить следующее: увеличение количества вакцинированных против ротавирусной инфекции детей привело к снижению частоты возникновения сахарного диабета у детей в возрасте до 4 лет на 15%.
Леонард Хариссон, исследователь из Мельбурнского института, в своей статье делает акцент на молекулярном сходстве вируса и аутоантител к островковой доле поджелудочной железы. Но все же точные механизмы воздействия ротавируса в патогенезе сахарного диабета 1 типа до сих пор неизвестны и требует дальнейшего изучения.
Авторы публикации утверждают, что вакцинация против ротавируса сможет послужить первичной профилактикой сахарного диабета 1 типа у некоторых детей.
Подписывайтесь на нашу email рассылку и оставайтесь в курсе самых важных медицинских событий
Актуальные проблемы
Специализации
- Premium
- Аллергология
- Бронхопульмонология
- Вакцинопрофилактика
- Гастроэнтерология
- Гепатология
- Гинекология
- Дерматовенерология
- Иммунология
- Инфекции
- Кардиология
- ЛОР-патология
- Медтехника
- Неотложная помощь
- Нутрициология
- Онкология
- Педиатрия
- Психоневрология
- Ревматология
- Сезонная аллергия
- Терапия
- Уронефрология
- Фармакология
- Эндокринология
- ИТ в здравоохранении
Календарь событий:
Статья почвящена инфекционным факторам развития сахарного диабета у детей. Подчеркивается необходимость настороженности врачей в отношении энтеровирусной инфекции, полиморфизма ее проявлений, тяжелых поражений многих органов и систем с формированием сомат
The article is dedicated to infectious factors of diabetes mellitus in children. The need for doctors caution in respect of enteroviral infection, polymorphism of its representations, severe lesions of multiple organs and systems with formation of somatic problems were highlighted.
Сахарный диабет (СД) является одним из наиболее важных и сложных для современной медицины заболеваний, что обусловлено его широким распространением, клиническим полиморфизмом и тяжестью осложнений [1–6]. Летальность при СД выше в 2–3 раза по сравнению с больными без него. Всемирная организация здравоохранения (ВОЗ) характеризует инсулинзависимый СД (ИЗСД, или СД 1-го типа) как эпидемию неинфекционного генеза из-за значительного роста среди детей и подростков [2–5]. Прогнозируется, что заболеваемость ИСЗД за период с 2005 по 2020 гг. у детей младше 5 лет увеличится в 2 раза, а общая распространенность его у детей до 15 лет возрастет на 70%, поэтому госпитализация также увеличится [7].
В настоящее время смертность от острых осложнений СД (диабетической комы) не превышает 1%, но вместе с повышением продолжительности жизни больных возникла новая проблема — сосудистые осложнения СД [8]. Развитие СД сопровождается 3–4-кратным увеличением риска смерти от сердечно-сосудистых заболеваний (ССЗ) и уменьшением ожидаемой продолжительности жизни по сравнению с лицами, не имеющими СД. Возникающие кардиоваскулярные нарушения в детском возрасте при ИЗСД становятся основной причиной смертности у взрослых пациентов. Миокардиодистрофия в большинстве случаев приводит к развитию сердечной недостаточности, артериальной гипертензии (АГ), прогрессированию макро- и микрососудистых осложнений СД 1-го типа.
На сегодняшний день существуют только единичные работы, посвященные данной проблеме у детей. Основная же масса представленных работ касается взрослого контингента, хотя известно, что формирование осложнений начинается в детском возрасте, когда данные изменения еще обратимы и есть возможность предотвратить их прогрессирование. Кроме того, имеет место неоднозначная трактовка результатов исследования ввиду их малочисленности и отсутствия единой комплексной оценки всех звеньев патогенеза сосудистых осложнений.
Основным патогенетическим механизмом, участвующим в развитии кардиоваскулярных нарушений при СД 1-го типа, является диффузный генерализованный патологический процесс, который поражает всю систему микроциркуляции — микроангиопатия с нарушением метаболизма сердечной мышцы, изменение нервной регуляции сердца, развитие изменений в рамках кардиоренального синдрома и эндотелиальной дисфункции. У детей и подростков, больных СД 1-го типа, на ранних его стадиях происходит также развитие диабетической микроангиопатии зрительного анализатора, обусловленного хронической гипергликемией, хронической гипоксией, активизирующей процессы ангиогенеза [9]. Признанным механизмом повреждения миокарда при СД является уменьшение коронарного резерва вследствие гипергликемии (микроангиопатии), гипертриглицеридемии, эндотелиальной дисфункции.
Поражение сердца при СД развивается вследствие воздействия ряда неблагоприятных факторов, приводящих к повреждению миокарда, его реактивной гипертрофии, фиброзу на фоне функциональных и структурных изменений мелких сосудов, метаболических нарушений и кардиальной автономной нейропатии [10]. СД является мощным и независимым фактором риска развития мерцательной аритмии и трепетания предсердий. Следует отметить, что нередко асимптоматические пароксизмы и пароксизмы, сопровождающиеся клинической симптоматикой, находятся в соотношении 12:1, и задачей клиницистов является раннее предупреждение этих состояний [11]. СД и мерцательная аритмия тесно связаны между собой по ряду факторов, ускоренному развитию атеросклероза с формированием фибросклероза с ишемизирующим воздействием на миокард, ремоделированием иннервации предсердий и другие.
Клинический полиморфизм при энтеровирусной инфекции проявляется не только разнообразием клинических форм, но и тем, что у одного и того же больного данная инфекция может проявляться в различных вариантах.
Было проведено изучение морфологических маркеров вирусов при биопсии у 57 больных с аритмогенной кардиопатией правого желудочка (АКПЖ) (средний возраст пациентов 48 ± 12 лет). Результаты исследования (биопсийного и аутопсийного) свидетельствовали в пользу врожденного генеза кардиомиопатии. В преобладающем количестве случаев у пациентов были выявлены энтеровирусы. Экспрессия антигена энтеровирусов была обнаружена в цитоплазме кардиомиоцитов, гладкомышечных клетках, эндотелиоцитах сосудов [12].
Отечественная история изучения значения различных вирусов как причин манифестации ИЗСД относится к 1980-м гг. и связана с именами таких ученых, как Л. С. Лозовская, В. В. Смирнов, Н. А. Мазурина и др. [14, 15].
К энтеровирусной инфекции в последние годы приковано внимание специалистов всего мира. Преимущественно зарубежными учеными в последние годы были собраны метаанализы, разрабатываются программы, методы диагностики и профилактики энтеровирусной инфекции. Столь пристальное внимание обусловлено серьезностью и тяжестью последствий энтеровирусной инфекции во многих областях медицины и, в частности, в эндокринологии. ВОЗ характеризует ИЗСД как эпидемию. К сожалению, среди отечественных специалистов-эндокринологов пока нет такой настороженности и понимания значения этой инфекции как причины развития ИЗСД, хотя за рубежом уже создается вакцина от энтеровирусной инфекции для предупреждения развития СД [16, 17].
Учитывая важность настоящей проблемы, первоначально мы преследовали основную цель — выявить изменения со стороны сердечно-сосудистой системы у детей, умерших от ИЗСД за 20-летний период времени (1991–2011). Однако, принимая во внимание данные литературы последних лет, в ходе исследования был проведен анализ патологоанатомических данных и поиск этиотропных вирусов, которые обладают полиорганным поражением (сердца, бета-клеток поджелудочной железы и др. органов).
За данный период времени, по материалам вскрытий Морозовской ДГКБ, умерло 16 детей (8 мальчиков и 8 девочек) с диагнозом СД 1-го типа (рис. 1).
Как видно из рис. 1, большинство летальных исходов у детей с СД 1-го типа приходилось на 1991–2003 гг. В последующие годы, очевидно, в связи с отработкой методов лечения и контроля как во всем мире, так и у нас в стационаре, количество летальных исходов значительно уменьшилось.
ИЗСД впервые выявленный был у 11 детей, СД 1-го типа со стажем от 1,5 до 12,5 лет — у 5 детей (31,3%). Возраст детей был следующим: 1–3 года — 2 чел.; 3–6 лет — 3; 6–9 лет — 4; 9–12 лет — 1; 12–15 лет — 6. Таким образом, 56,3% детей были в возрасте от 1 до 9 лет и 43,7% — старше 9 лет. Основным диагнозом при поступлении у всех больных был СД 1-го типа, кетоацидотическая кома. Причина летального исхода — отек головного мозга.
Анализируя клиническую симптоматику дебюта заболевания и тех симптомов, с которыми дети поступали в стационар, следует сказать, что у 14 больных (87,5%) заболевание началось с характерных симптомов — жажды и похудания, однако у 11 детей (68,8%) имели место симптомы инфекционного заболевания, такие как острое респираторное заболевание (4 чел.), боль в горле (1 чел.), пневмония (1 чел.), энцефалит (1 чел.), аппендицит (?) (у детей с болями в животе) (табл. 1). У одного ребенка диагноз был установлен случайно во время диспансеризации, другой поступил в стационар в кардиологическое отделение с пароксизмальной тахикардией. Сложность диагностики во многом была связана с краткостью пребывания в стационаре. Так, 9 детей (56,3%) погибли в первые сутки пребывания в отделении реанимации и интенсивной терапии (ОРИТ), находясь в коме.
По данным патологоанатомического исследования оказалось, что у большего количества детей (14 из 16) имели место различные фетодисплазии, которые ни у одного ребенка, несмотря на возраст (многие из них старшего возраста) не были выявлены. Среди фетодисплазий выделены 2 группы: у 5 детей — нарушение лобуляции легких, у 8 — пороки развития (головного мозга — 3, сердца — 1, почек — 2, добавочная селезенка — 1, гепатобластома — 1).
Основными осложнениями были следующие:
- двухсторонняя пневмония — 10 (62,5%);
- панкреатит — 10 (62,5%);
- менингит, энцефалит — 6 (37,5%);
- миокардит — 6 (37,5%);
- вторичный иммунодефицит — 3 (18,8%).
Возбудители, выделенные по результатам патологоанатомических исследований, представлены в табл. 3.
У 12 детей были выделены следующие вирусы — энтеровирусы (у 8 пациентов), вирусы респираторной группы (аденовирусы, респираторно-синцитиальный вирус, парагрипп, грипп) — у 5 больных. У двух больных были обнаружены герпесвирусы.
Таким образом, преобладающими возбудителями были энтеровирусы, обнаруженные у 8 детей (50% случаев). Однако у 5 детей с неуточненной генерализованной инфекцией (им не было проведено вирусологическое обследование) изменения в органах были однотипны таковым у 8 больных с энтеровирусами, поэтому, возможно, энтеровирусная инфекция имела место у большего количества детей. Энтеровирусная инфекция была представлена следующими серотипами: Коксаки А (3, 4, 5) — у 6 детей; Коксаки В — у 4, энтеровирусы — у 3 детей; смешанное течение — у 4. Для энтеровирусной инфекции были характерны поражения следующих органов: сердца — 7 пациентов (87,5% случаев), головного мозга — 6 (75%), поджелудочной железы — 5 (62,5%), печени — 5 (62,5%), почек — 4 (50%), фетодисплазии — 6 (75%), желудочно-кишечного тракта — 2 (25%).
Изменения со стороны сердечно-сосудистой системы были оценены нами ретроспективно по анализу электрокардиограммы (ЭКГ) (прижизненно), а также после вскрытия (по его результатам и гистологии). По результатам ЭКГ регистрировалась перегрузка правых отделов сердца, аритмия, брадикардия, удлинение систолы желудочков, нарушение внутрижелудочковой проводимости. У одного ребенка имела место пароксизмальная тахикардия. Артериальная гипотензия превалировала и была выявлена у 6 детей, гипертензия — у 2.
У всех 16 детей с ИЗСД проводилась морфологическая и гистологическая оценка состояния сердечно-сосудистой системы по следующим параметрам: масса сердца, наличие гипертрофии камер сердца, фиброэластоз, состояние коронарных сосудов.
На вскрытии у 7 детей имело место увеличение размеров сердца, у 7 — уменьшение, причем эти изменения не зависели от давности течения СД. Дилатационная кардиомиопатия была выявлена у большинства — у 12 детей (75% случаев), фиброэластоз эндокарда — у 11 больных (68,7% случаев), миокардит — у 6 (37,5%). Коронарные сосуды изменены не были практически ни у кого из детей, за исключением одного ребенка, у которого обнаружено утолщение коронарных артерий (сочетание энтеро- и вирусов респираторной группы). Описаны общие следующие изменения миокарда: миокард дряблый, очаги гистиоцитарной инфильтрации, очаговый склероз, фиброз, миксоматоз клапанов, утолщение створок, их сращение, агломерация папиллярных мышц. Отмечается белковая дистрофия кардиомиоцитов, гибель клеток, распад миофибрилл. В сосудах — очаговый фиброз, дистрофия стенок. Выявленные изменения, в первую очередь, имели место у всех детей с энтеровирусной инфекцией.
Следует заметить, что изменения со стороны сердца и поджелудочной железы взаимосвязаны у детей. Наши данные аналогичны таковым, полученным авторами из г. Новосибирска А. В. Деминой и С. В. Нетесовым, которые выделяли формы энтеровирусной инфекции, связанные с серологическими штаммами. Например, перикардит и миокардит встречался при вирусах Коксаки В 1–5 типов, вирусах ЕСНО 1-го, 6-го, 9-го, 19-го типов; а диабет регистрировался при вирусах Коксаки А 9-го, В 1–5 типов [18].
Со слов мамы, ранее не болел, но врачи отмечали вегетососудистую дистонию по гипотоническому типу.
По результатам патологоанатомического исследования был установлен следующий диагноз: генерализованная смешанная инфекция: менингоэнцефалит с лейкомаляцией, мелкоочаговый продуктивный панкардит, продуктивный полиневрит, продуктивный гепатит, интерстициальный нефрит. Вирусологическое обследование: были выделены следующие вирусы: энтеровирусы групп А, В, С, а также вирусы респираторной группы (гриппа, парагриппа, аденовирус).
Выявлены следующие фетодисплазии: трехстворчатого клапана, гипоплазия хрящевых пластин субсегментарных бронхов, двудолевое правое легкое, добавочная селезенка, атрофия тимуса, внутренняя гидроцефалия.
Патологоанатомический эпикриз: смерть ребенка 3 лет с множественными дисплазиями, генерализованной смешанной инфекцией, СД 1-го типа впервые выявленным с развитием кетоацидоза и гиперосмолярной комой наступила от лейкомаляции вещества головного мозга.
Патологоанатомические исследования сердца: на разрезе — истончение миокарда правого желудочка до 0,2 см (норма — 0,27 см), расширение полостей желудочков, утолщение миокарда левого желудочка. Папиллярные мышцы в правом желудочке практически отсутствуют, хордальные нити прикрепляются к стенке желудочка, остальные укорочены, хаотически расположены, третьи — несколько удлинены. На створках клапанов мелкие мукоидные прозрачные узелки. Гистология сердца: утолщение коронарных артерий, мукоидное набухание клапанов, мелкие очаги лимфоидной инфильтрации в эпикарде, миокарде, эндокарде, отек интерстиция. В некоторых нервных стволах эпикарда — гибель клеточных элементов и гистиоцитарная инфильтрация.
На рис. 2 представлены гистологические изменения сердца ребенка.
_575.jpg)
Данный случай демонстрирует взаимосвязь поражений многих органов и систем, в частности, сердца и поджелудочной железы с энтеровирусной инфекцией. Принимая во внимание наличие фетодисплазий, заражение, вероятнее всего, произошло во внутриутробном периоде. Известно, что энтеровирусная инфекция может иметь персистирующее течение, принимать аутоиммунные формы и обостряться под действием вирусов респираторной группы, как, возможно, в данном случае.
Подводя итог данной работы, хочется еще раз подчеркнуть особую важность и необходимость настороженности врачей многих специальностей в отношении энтеровирусной инфекции, полиморфизма ее проявлений, тяжелых поражений многих органов и систем с формированием соматических проблем (миокардит, панкреатит, интерстициальный нефрит, ИЗСД, менингит и т. д.). На сегодняшний день необходимо развивать диагностику энтеровирусной инфекции, так как даже при большом желании мы не имеем возможности полноценного обследования на эту инфекцию не только в Москве, но и в России в целом. Увеличение количества случаев энтеровирусной инфекции в виде вспышек, эпидемий, рост заболеваемости менингитами, СД 1-го типа во всем мире — тому подтверждение.
Литература
Т. А. Полилова*
М. С. Савенкова*, доктор медицинских наук, профессор
В. В. Смирнов* , 1 , доктор медицинских наук, профессор
Е. Е. Петряйкина**, доктор медицинских наук, профессор
И. Е. Колтунов**, доктор медицинских наук, профессор
Л. Н. Каск**
Н. В. Бузина**
* ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва
** ГБУЗ Морозовская ДГКБ ДЗМ, Москва
Что такое сахарный диабет 2 типа? Причины возникновения, диагностику и методы лечения разберем в статье доктора Хитарьяна Александра Георгиевича, диабетолога со стажем в 31 год.
Над статьей доктора Хитарьяна Александра Георгиевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов

Определение болезни. Причины заболевания
Эпидемия сахарного диабета (СД) длится уже достаточно долго. [9] По данным Всемирной организации здравоохранения (ВОЗ) в 1980 году на планете было около 150 миллионов человек, страдающих от СД, а в 2014 году — около 421 миллионов. К сожалению, тенденция к регрессу заболеваемости за последние десятилетия не наблюдается, и уже сегодня можно смело заявить, что СД является одним из распространённых и тяжёлых болезней.
Сахарный диабет II типа (Type 2 diabetes) — хроническое неинфекционное, эндокринное заболевание, которое проявляется глубокими нарушениями липидного, белкового и углеводного обменов, связанного с абсолютным или же относительным дефицитом гормона, производимого поджелудочной железой.
У пациентов с СД II типа поджелудочная железа продуцирует достаточное количество инсулина — гормона, регулирующего углеводный обмен в организме. Однако из-за нарушения метаболических реакций в ответ на действие инсулина возникает дефицит этого гормона.
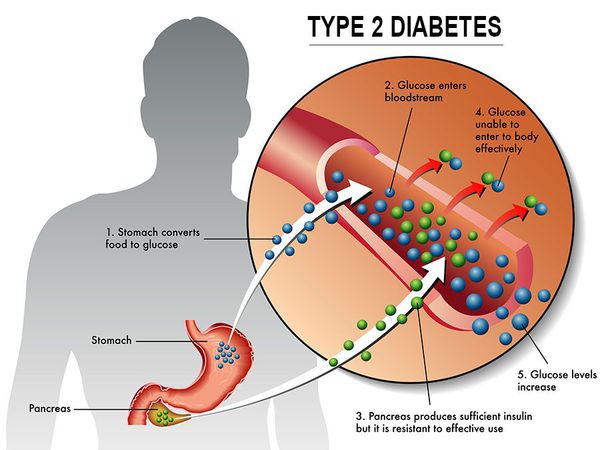
Инсулиннозависимый СД II типа имеет полигенную природу, а также является наследственным заболеванием.
Причиной возникновения данной патологии является совокупность определённых генов, а её развитие и симптоматика определяется сопутствующими факторами риска, такими как ожирение, несбалансированное питание, низкая физическая активность, постоянные стрессовые ситуации, возраст от 40 лет, бессонница. [1] [10]
Нарастающая пандемия ожирения и СД II типа тесно связаны и представляют основные глобальные угрозы здоровью в обществе. [3] Именно эти патологии являются причинами появления хронических заболеваний: ишемической болезни сердца, гипертонии, атеросклероза и гиперлипидемии.
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы сахарного диабета 2 типа
Чаще всего симптоматика при СД II типа выражена слабо, поэтому данное заболевание можно обнаружить благодаря результатам лабораторных исследований. Поэтому людям, относящимся к группе риска (наличие ожирения, высокого давления, различных метаболических синдромов, возраст от 40 лет), следует проходить плановое обследование для исключения или своевременного выявления болезни.
К основным симптомам СД II типа следует отнести:
- перманентную и немотивированную слабость, сонливость;
- постоянную жажду и сухость во рту;
- полиурию — учащённое мочеиспускание;
- усиленный аппетит (в период декомпенсации (прогрессирования и ухудшения) болезни аппетит резко снижается);
- кожный зуд (у женщин часто возникает в области промежности);
- медленно заживающие раны;
- затуманенное зрение;
- онемение конечностей.
Период декомпенсации заболевания проявляется сухостью кожи, снижением упругости и эластичности, грибковыми поражениями. В связи с аномально повышенным уровнем липидов возникает ксантоматоз кожи (доброкачественные новообразования).
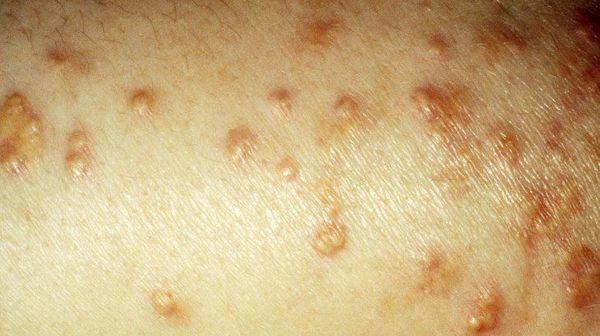
У больных СД II типа ногти подвержены ломкости, потере цвета или же появлению желтизны, а 0,1 – 0,3% пациентов страдают липоидным некробиозом кожи (отложения жиров в разрушенных участках коллагенового слоя).
Помимо симптомов самого СД II типа дают о себе знать также симптомы поздних осложнений заболевания: язвы на ногах, снижение зрения, инфаркты, инсульты, поражения сосудов ног и другие патологии.
Патогенез сахарного диабета 2 типа
Основная причина возникновения СД II типа — это инсулинорезистентность (утрата реакции клеток на инсулин), обусловленная рядом факторов внешней среды и генетическими факторами, протекающая на фоне дисфункции β-клеток. Согласно исследовательским данным, при инсулинорезистентности снижается плотность инсулиновых рецепторов в тканях и происходит транслокация (хромосомная мутация) ГЛЮТ-4 (GLUT4).
Повышенный уровень инсулина в крови (гиперинсулинемия) приводит к уменьшению количества рецепторов на клетках-мишенях. Со временем β -клетки перестают реагировать на повышающийся уровень глюкозы. В итоге образуется относительный дефицит инсулина, при котором нарушается толерантность к углеводам.
Дефицит инсулина приводит к снижению утилизации глюкозы (сахара) в тканях, усилению процессов расщипления гликогена до глюкозы и образования сахара из неуглеводных компонентов в печени, тем самым повышая продукцию глюкозы и усугубляя гимергликемию — симптом, характеризующийся повышенным содержанием сахара в крови.
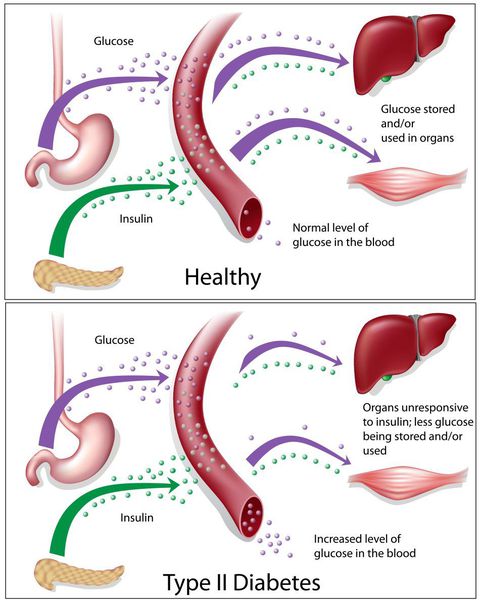
Окончания периферических двигательных нервов выделяют кальцитонин-подобный пептид. Он способствует подавлению секреции инсулина путём активизации АТФ-зависимых калиевых каналов (K+) в мембранах β-клеток, а также подавлению поглощения глюкозы скелетными мышцами.
Избыточный уровень лептина — главного регулятора энергетического обмена — способствует подавлению секреции инсулина, приводя к возникновению инсулинорезистентности скелетных мышц к жировой ткани.
Таким образом инсулинорезистентность включается в себя различные метаболические изменения: нарушение толерантности к углеводам, ожирение, артериальная гипертензия, дислипопротеидемия и атеросклероз. Главную роль в патогенезе этих нарушений играет гиперинсулинемия, как компенсаторное следствие инсулинорезистентности. [6]
Классификация и стадии развития сахарного диабета 2 типа
В настоящее время российские диабетологи классифицируют СД по степени тяжести, а также по состоянию углеводного обмена. Однако Международная Федерация диабета (МФД) довольно часто вносит изменения в цели лечения диабета и классификации его осложнений. По этой причине российские диабетологи вынуждены, постоянно изменять принятые в России классификации СД II типа по тяжести и степени декомпенсации заболевания.
Существуют три степени тяжести заболевания:
- I степень — наблюдаются симптомы осложнений, дисфункция некоторых внутренних органов и систем. Улучшение состояния достигается путём соблюдения диеты, назначается применение препаратов и инъекций.
- II степень — достаточно быстро появляются осложнения органа зрения, происходит активное выделение глюкозы с мочой, появляются проблемы с конечностями. Медикаментозная терапия и диеты не дают эффективных результатов.
- III степень - происходит выведение глюкозы и белка с мочой, развивается почечная недостаточность. В этой степени патология не поддаётся лечению.
По состоянию углеводного обмена выделяют следующие стадии СД II типа:
- компенсированная — нормальный уровень сахара в крови, достигнутый с помощью лечения, и отсутствие сахара в моче;
- субкомпенсированая — уровень глюкозы в крови (до 13,9 ммоль/л) и в моче (до 50 г/л) умеренный, при этом ацетон в урине отсутствует;
- декомпенсированная — все показатели, характерные для субкомпенсации, значительно повышены, в моче обнаруживается ацетон.
Осложнения сахарного диабета 2 типа
К острым осложнениям СД II типа относятся:
- Кетоацидотическая кома — опасное состояние, при котором происходит тотальная интоксикация организма кетоновыми телами, а также развивается метаболический ацидоз (увеличение кислотности), острая печёночная, почечная и сердечно-сосудистая недостаточность.
- Гипогликемическая кома — состояние угнетения сознания, развивающееся при резком уменьшении содержания глюкозы в крови ниже критической отметки.
- Гиперосмолярная кома — данное осложнение развивается в течение нескольких дней, в результате которого нарушается метаболизм, клетки обезвоживаются, резко увеличивается уровень глюкозы в крови.
Поздними осложнениями СД II типа являются:
- диабетическая нефропатия (патология почек);
- ретинопатия (поражение сетчатки глаза, способное привести к слепоте);
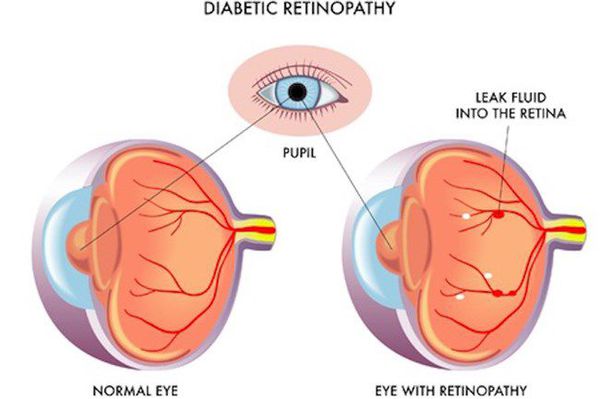
- полинейропатия (поражение периферических нервов, при котором конечности теряют чувствительность);
- синдром диабетической стопы (образование на нижних конечностях открытых язв, гнойных нарывов, некротических (отмирающих) тканей).
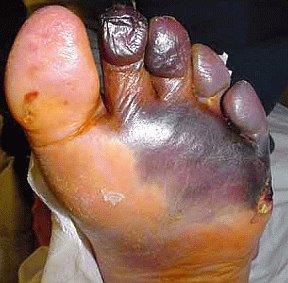
Диагностика сахарного диабета 2 типа
Для того чтобы диагностировать СД II типа необходимо оценить симптомы болезни и провести следующие исследования:
Лечение сахарного диабета 2 типа
Лечение СД II типа предполагает решение основных задач:
- компенсировать недостаток инсулина;
- скорректировать гормонально-метаболические нарушения;
- осуществление терапии и профилактики осложнений.
Для их решения применяется следующие методы лечения:
- диетотерапия;
- физические нагрузки;
- применение сахароснижающих препаратов;
- инсулинотерапия;
- хирургическое вмешательство.
Диетотерапия
Диета при СД II типа, как и обычная диета, предполагает оптимальное соотношение основных веществ, содержащихся в продуктах: белки должны составлять 16% суточного рациона, жиры — 24%, а углеводы — 60%. Отличие диеты при диабете II типа заключается в характере потребляемых углеводов: рафинированные сахара заменяются медленно усваиваемыми углеводами. Так как данное заболевание возникает у полных людей, потеря веса является важнейшим условием, нормализующим содержание глюкозы в крови. В связи с этим рекомендована калорийность диеты, при которой пациент еженедельно будет терять 500 г массы тела до момента достижения идеального веса. Однако при этом еженедельное уменьшение веса не должно превышать 2 кг, в противном случае это приведёт к избыточной потере мышечной, а не жировой ткани. Количество калорий, необходимое для суточного рациона пациентов с СД II типа, рассчитывается следующим образом: женщинам нужно умножить идеальный вес на 20 ккал, а мужчинам — на 25 ккал.
При соблюдении диеты необходимо принимать витамины, так как во время диетотерапии происходит избыточное выведение их с мочой. Нехватку витаминов в организме можно компенсировать при помощи рационального употребления полезных продуктов, таких как свежая зелень, овощи, фрукты и ягоды. В зимние и весенние периоды возможен приём витаминов в дрожжевой форме.
Физическая нагрузка
Верно подобранная система физических упражнений, с учётом течения заболевания, возраста и присутствующих осложнений, способствует значительному улучшению состояния больного СД. Эта методика лечения хороша тем, что необходимость применения инсулита практически отпадает, так как во время физических нагрузок глюкоза и липиды сгорают без его участия.
Лечение сахароснижающими препаратами
На сегодняшний день используют производные сахароснижающих препаратов:
- сульфонилмочевины (толбутамид, глибенкламид);
- бигуаниды, снижающие глюконеогенез в печени и повышающие чувствительность мышц и печени к инсулину (метформин);
- тиазолидиндионы (глитазоны), схожие по свойствам с бигуанидами (пиоглитазон, росиглитазон);
- ингибиторы альфа-глюкозидаз, снижающие темпы всасывания глюкозы в желудочно-кишечном тракте (акарбоза);
- агонисты рецепторов глюкагоноподобного пептида-1, стимулирующие синтез и секрецию инсулина, снижающие продукцию глюкозы печенью, аппетит и массу тела, замедляющие эвакуацию пищевого комка из желудка (эксенатид, лираглутид);
- ингибиторы депептидил-пептидазы-4, также стимулирующие синтез и секрецию инсулина, снижающие продукцию глюкозы печенью, не влияющие на скорость эвакуации пищи из желудка и оказывающие нейтральное действие на массу тела (ситаглиптин, вилдаглиптин);
- ингибиторы натрий-глюкозного котранспортера 2 типа (глифлозины), снижающие реабсорбцию (поглощение) глюкозы в почках, а также массу тела (дапаглифлозин,эмпаглифлозин).
Инсулинотерапия
В зависимости от тяжести болезни и возникающих осложнений врач назначает приём инсулина. Данный метод лечения показан примерно в 15-20% случаев. Показаниями к применению инсулинотерапии являются:
- быстрая потеря веса без видимой на то причины;
- возникновение осложнений;
- недостаточная эффективность других сахароснижающих препаратов.
Хирургическое лечение
Несмотря на множество гипогликемических препаратов, остаётся не решённым вопрос об их правильной дозировке, а также о приверженности пациентов к выбранному методу терапии. Это, в свою очередь, создаёт трудности при достижении длительной ремиссии СД II типа. Поэтому всё большую популярность в мире получает оперативная терапия данного заболевания — бариатрическая или метаболическая хирургия. МФД считает данный метод лечения пациентов с СД II типа эффективным. В настоящее время в мире проводится более 500 000 бариатрических операций в год. Существует несколько видов метаболической хирургии, самыми распространёнными являются шунтирование желудка и мини гастрошунтирование. [4]
Шунтирование желудка по Ру
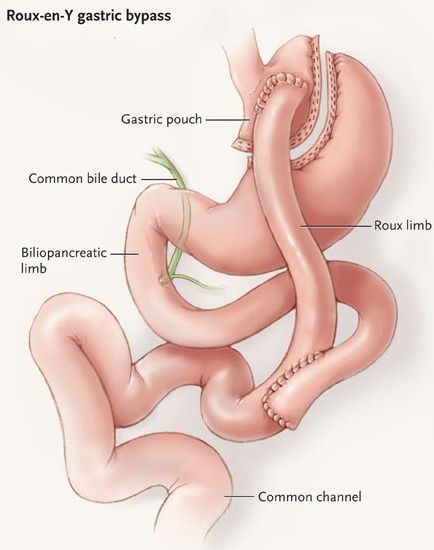
Во время шунтирования, желудок пересекается ниже пищевода таким образом, чтоб его объём сократился до 30 мл. Оставшаяся большая часть желудка не удаляется, а заглушается, предотвращая попадание в неё пищи. [5] В результате пересечения образуется маленький желудок, к которому затем пришивается тонкая кишка, отступив 1 м от её окончания. Таким образом пища будет прямиком попадать в толстую кишку, при этом обработка её пищеварительными соками снизится. Это, свою очередь, провоцирует раздражение L-клеток подвздошной кишки, способствующее снижению аппетита и увеличению роста клеток, синтезирующих инсулин.
Мини шунтирование желудка
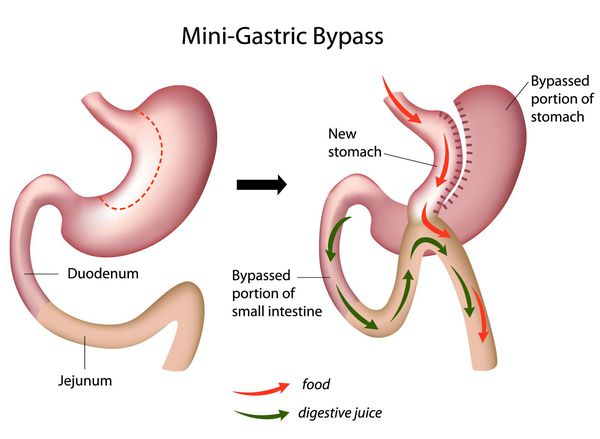
Главное отличие минигастрошунтирования от классического шунтирования желудка — сокращение количества анастомозов (соединений отрезков кишки). [2] При выполнении традиционной операции накладывается два анастомоза: соединение желудка и тонкой кишки и соединение разных отделов тонкой кишки. При минигастрошунтировании анастомоз один — между желудком и тонкой кишкой. Благодаря малому объёму вновь сформированного желудка и быстрому поступлению еды в тонкую кишку у пациента возникает чувство насыщения даже после приёма незначительных порций пищи.
К другим видам бариатрической хирургии относятся:
- гастропликация — ушивание желудка, предотвращающее его растягивание; [8]
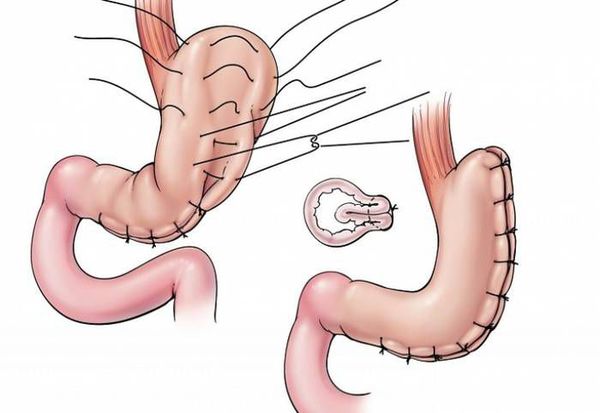
- рукавная гастропластика (иначе её называют лапароскопической продольной резекцией желудка) — отсечение большей части желудка и формирование желудочной трубки объёмом 30 мл, которое способствует быстрому насыщению, а также позволяет избежать соблюдения строгой диеты;
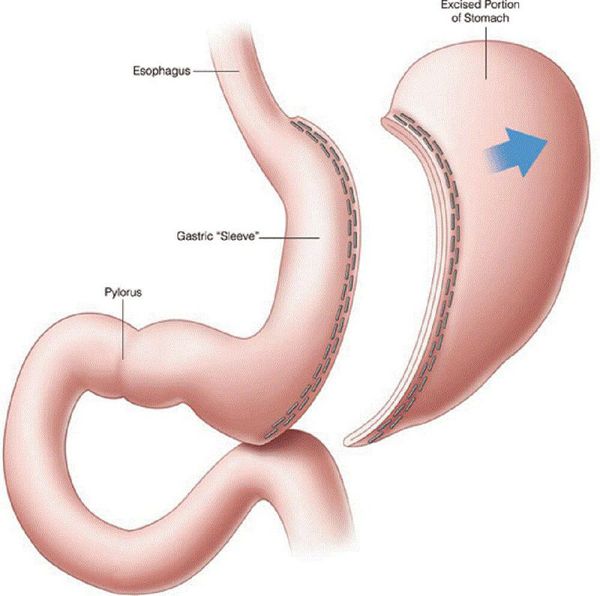
- бандажирование желудка — уменьшение объёма желудка с помощью специального кольца (бандажа), накладывающегося на верхнюю часть желудка (данное вмешательство обратимо).
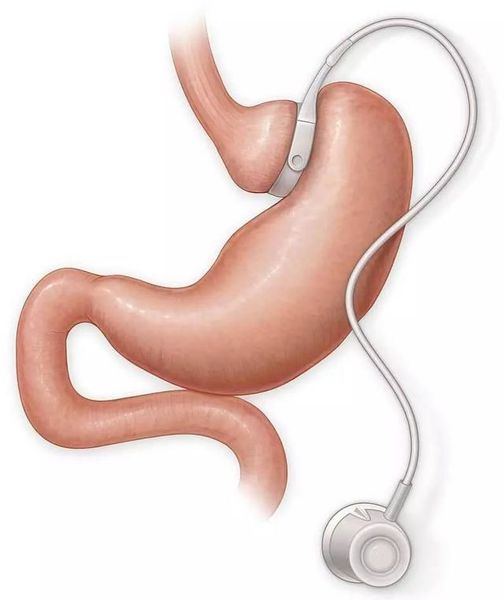
Противопоказания к проведению хирургического лечения — наличие у пациента эзофагита (воспаления слизистой оболочки пищевода), варикозного расширения вен пищевода, портальной гипертенззи, цирозща печени, язвенной болезни желудка или двенадцатиперстной кишки, хронического панкреатита, беременности, алкоголизма, тяжёлых заболеваний сердечно-сосудистой системы или психических расстройств, а также длительное применение гормональных препаратов.
Прогноз. Профилактика
К сожалению, полностью излечиться от СД II типа невозможно. Однако существуют способы улучшения качества жизни пациентов с данным заболеванием.
На сегодняшний день существует большое количество “баз”, где специалисты-эндокринологи объясняют пациентам, каким должен быть их уклад жизни, как правильно питаться, какие продукты не следует употреблять, какими должны быть ежедневные физические нагрузки.
Также создано огромное количество сахароснижающих препаратов, которые ежегодно совершенствуются. Для того, чтобы они оказывали положительное влияние на организма, медикаменты необходимо принимать регулярно.
Практика показывает, что соблюдение всех рекомендаций эндокринологов улучшает процесс лечения СД II типа.
Оперативным методом, повышающим качество жизни при СД II типа по мнению МФД, является бариатрическая хирургия.
Значительно улучшить состояние пациентов с данным заболеванием позволяет проведение гастроинтестинальных операций (терапия морбидного ожирения), вследствие которой нормализуется уровень гликогемоглобина и глюкозы в крови, теряется необходимость применения антидиабетических препаратов и инсулина.
Бариатрическая хирургия может привести к значительной и устойчивой ремиссии, а также к улучшению течения СД II типа и других метаболических факторов риска у тучных пациентов. Хирургическое вмешательство в течение 5 лет после установления диагноза чаще всего приводит к долговременной ремиссии.
Для предупреждения возникновения СД II типа необходимо соблюдать следующие меры профилактики:
Читайте также:

