Сафоцид отзывы от трихомонад
Обновлено: 24.04.2024
В течение последних лет в Российской Федерации заболеваемость урогенитальной хламидийной инфекцией вышла на первое место среди всех бактериальных инфекций, передаваемых половым путем (ИППП), и уступает по частоте только трихомониазу. Такая же картина в ст
В течение последних лет в Российской Федерации заболеваемость урогенитальной хламидийной инфекцией вышла на первое место среди всех бактериальных инфекций, передаваемых половым путем (ИППП), и уступает по частоте только трихомониазу. Такая же картина в странах Северной Америки и Европы, где урогенитальный хламидиоз уже много лет является самым распространенным бактериальным ИППП. Хотя доля Clamidia trachomatis (C. trachomatis) как этиологического агента в общей структуре уретритов у мужчин не превышает 50%, именно этот возбудитель остается главной причиной таких уретритов.
Классификация хламидийных инфекций. В принятой в большинстве стран мира международной классификации болезней Х пересмотра (МКБ-Х) урогенитальные хламидийные инфекции подразделяются:
1. На хламидийную инфекцию нижних отделов (неосложненную):
2. Инфекцию верхних отделов мочеполового тракта (осложненную):
Кроме этого, в МКБ-Х выделяют хламидийную инфекцию аноректальной области, хламидийные фарингиты, а также хламидийную инфекцию других локализаций.
Эта классификация более удобна для статистических отчетов, где требуется четкая рубрификация всех болезней. Специалисты нередко в клинической практике видоизменяют МКБ с целью большей адаптации ее для своей работы. Так, для назначения адекватной терапии хламидийных инфекций важно понять, какая из 3 форм урогенитального хламидиоза имеется у больного:
Клинические проявления хламидийной инфекции. Чаще всего у мужчин на практике встречается хламидийная инфекция нижних отделов урогенитального тракта — уретриты.
Уретриты, вызванные С. trachomatis, проявляются обычно скудной клинической симптоматикой, хотя могут сопровождаться и признаками острого воспаления, сходными с гонореей. Нередко инфицирование нижних отделов урогенитального тракта у мужчин хламидиями может протекать без какой-либо клинической симптоматики.
Наиболее частые проявления хламидийной инфекции нижних отделов урогенитального тракта у мужчин — это наличие слизисто-гнойных или слизистых необильных выделений из уретры, дизурии (зуда, жжения, болезненности при мочеиспускании), дискомфорт, зуд, жжение в области уретры. При клиническом обследовании у таких пациентов можно выявить гиперемию и отечность слизистой оболочки наружного отверстия мочеиспускательного канала, инфильтрацию стенок уретры, повышенный лейкоцитоз в материале из уретры.
Успешное излечение хламидийной инфекции во многом зависит от выбора правильной тактики терапии, поскольку ошибки на самом начальном этапе болезни, будь то диагностические ошибки или неадекватный выбор антибиотиков, могут привести к тому, что от инфекции избавиться не удастся, что грозит больному серьезными осложнениями.
К наиболее тяжелым осложнениям хламидийной инфекции относят: эпидидимиты, воспалительные заболевания органов малого таза (ВЗОМТ), бесплодие у лиц обоего пола, болезнь Рейтера, перигепатит, пельвиоперитонит, патологию плода и послеродовую патологию у матери, а также некоторые другие состояния. Их развитие может быть связано не только с хламидиями, но и с другими возбудителями, однако хламидии остаются наиболее частой причиной указанных осложнений.
Уникальность азитромицина базируется на его исключительной фармакокинетике. Азитромицин устойчив в кислой среде, благодаря чему хорошо всасывается после приема внутрь (Feise EF et al, 1990). Одновременный прием с пищей уменьшает всасывание на 50%, поэтому препарат принимают за 1 ч до или через 2 ч после еды. Этого недостатка лишена таблетированная форма препарата, которая может приниматься независимо от приема пищи.
После приема внутрь 500 мг азитромицина биодоступность препарата составляет 37%, а максимальная концентрация в плазме (0,4 мг/л) достигается через 2–3 часа, затем она плавно снижается к 24 ч, в последующие сроки препарат в крови не определяется (Комаров Р.В. с соавт, 2001). Этого недостаточно для достижения терапевтического эффекта при лечении инфекций, сопровождающихся бактериемией. Однако липофильность молекулы азитромицина обеспечивает, помимо высокого уровня всасывания в кишечнике, еще и отличное проникновение препарата в ткани. Быстрое проникновение азитромицина из крови в ткани обеспечивается также низким уровнем связывания азитромицина с белками крови, что дает возможность достигнуть быстрого терапевтического эффекта при инфекциях, поражающих клетки и ткани (Foulds G et al, 1990).
Эффективность антибиотиков обычно оценивается путем сравнения активности в условиях in vitro (это показатель минимальной подавляемой концентрации (МПК) и концентрации препарата в сыворотке крови. Эти сравнения могут приводить к ошибочным представлениям о реальной эффективности антибиотика. Для ее оценки необходимо принимать во внимание еще и концентрацию препарата в тканях и месте воспаления. Именно эти показатели азитромицина обеспечивают ему превосходство. В различных тканях концентрации азитромицина в десятки раз превышают концентрации в сыворотке крови (рис. 1).
В эксперименте и исследованиях на животных было показано, что клинический и бактериологический эффекты макролидных антибиотков прямо зависят от времени превышения их концентраций над значениями МПК90 возбудителей, причем условием положительного эффекта является превышение концентрациями МПК в течение как минимум 40% интервала дозирования. Учитывая, что, по данным Комарова Р.В. и соавт. (2001), через 3 дня после приема концентрации азитромицина в секрете/ткани предстательной железы в 16,8 раза превышали значения МПК и, принимая это значение времени за 40%, можно прогнозировать сохранение эффекта азитромицина в течение как минимум 7 дней после однократного приема.
Для антибактериальных препаратов важен не только уровень накопления в тканях, но и соотношение тканевых концентраций и значений МПК для возбудителей инфекций. Так, концентрации азитромицина в секрете и ткани предстательной железы, представленные выше (рис. 1), превышали МПК90 для хламидий во все сроки наблюдения, вплоть до 2-х недель (в исследовании LeBell M. et al (1996)).
Полученные данные подтверждают возможность однократного применения азитромицина при неосложненной хламидийной инфекции, когда необходимо 7-дневное воздействие на микроорганизм, перекрывающее 2 жизненных цикла хламидий, а также его назначения короткими курсами с длительными интервалами между ними при осложненном и персистирующем хламидиозе.
Накопление препарата в макрофагах и полиморфноядерных лейкоцитах и транспортировка его с ними к месту воспаления дополняют нацеленное действие азитромицина в очаге инфекции. Показано, что концентрация препарата в месте воспаления в значительной степени превышает его концентрацию в здоровой ткани (Pukander J, 1990).
Способность азитромицина к проникновению внутрь клеток обеспечивает активное воздействие на внутриклеточные микроорганизмы, к которым относится С. trachomatis. При заболеваниях, вызываемых внутриклеточными патогенами, эффект лечения и скорость элиминации возбудителя из организма зависят от уровня концентраций антибиотика внутри клеток (полиморфноядерные лейкоциты, макрофаги, клетки эпителия). Среди всех антибиотиков макролиды характеризуются наибольшей способностью концентрироваться внутри клетки. Азитромицин при этом особенно привлекателен, поскольку соотношение концентраций антибиотика внутри клетки и в экстрацеллюлярном пространстве составляет для него 40 и более. По этому показателю азитромицин превосходит не только эритромицин, но и другие полусинтетические макролиды (Фомина И.П. с соавт., 1996).
В эксперименте установлено, что азитромицин накапливается в лейкоцитах с последующим медленным высвобождением. При этом соотношение внутри-/внеклеточных концентраций в полиморфноядерных лейкоцитах и макрофагах in vitro после 2 ч инкубации с антибиотиком составляет 79, превышая соответствующие показатели для эритромицина в 4–5 раз. Внутриклеточная концентрация азитромицина обнаруживается в течение 24 ч и более. Установлено также, что предварительная обработка клеток азитромицином не влияет на захватывающую, переваривающую и киллерную функции фагоцитов (McDonald P. J. et al, 1991). К дополнительным важным свойствам азитромицина, способствующим быстрой реализации терапевтического эффекта, даже при коротких схемах применения относится концентрация антибиотика в фибробластах, превращающихся в своеобразный резервуар, из которого препарат высвобождается в очаге инфекции (Glodue R. P. et al, 1990).
Еще одна важная особенность азитромицина — продолжительный период полувыведения — 68 ч, который приводит к тому, что высокие уровни концентрации в месте инфекции, сохраняющиеся в течение продолжительного периода времени (до 10 дней), обеспечивают постоянное активное воздействие на патогенные микроорганизмы (Andriole V. T., 1990, Retsema J., et al, 1990). Сокращение времени приема антибиотика при сохранении терапевтической эффективности очень важный принцип при амбулаторном лечении пациента. По данным различных авторов, только 65% больных полностью выполняют предписания врача. Почти половина лиц, получающих лечение как половые партнеры инфицированных пациентов, полноценно не выполняют режим терапии. По данным Grob P. R., 1992, в течение первых 3–5 дней лечения неисполнительность отмечается приблизительно в половине случаев, на 6–7 день ее уровень возрастает до 71–81%. По этим причинам предпочтение отдается сегодня схемам лечения, предусматривающим однократный или по крайней мере не очень частый прием лекарств. Длительный период полувыведения азитромицина из организма, сохранение эффективных концентраций в очаге инфекции в течение 4–5 дней после прекращения лечения позволяют проводить укороченные курсы терапии, которые соответствуют по эффективности 10-дневным курсам лечения традиционными антибиотиками (Фомина И.П. с соавт., 1996). Азитромицин остается единственным на сегодня антибиотиком однократного приема для лечения неосложненной хламидийной инфекции. Еще в 1993 г. Lister P. J. et al показали, что однократный прием 1,0 грамма азитромицина не уступает по эффективности 7-дневному курсу доксициклина. Большое удобство применения азитромицина для больных и возможность контроля за приемом однократной дозы со стороны медицинского персонала позволяют обеспечить практически 100%-ное соблюдение режима лечения (Petitta ABS et al, 1999).
Азитромицин метаболизируется в печени, причем 50% выделяется с желчью в неизмененном виде, около 6% выводится с мочой.
При приеме азитромицина могут наблюдаться побочные эффекты со стороны желудочно-кишечного тракта (тошнота, рвота, диарея) и печени (повышение активности трансаминаз, холестаз, желтуха), а также аллергические реакции.
Механизм действия азитромицина, как и других макролидов, обусловлен влиянием на функцию бактериальных рибосом. Препарат связывается с 50S субъединицей рибосом рибосомы и таким образом подавляет биосинтез белков микроорганизма, оказывая бактериостатическое действие. Бактерицидное действие препарата начинается в концентрациях, превышающих МПК в несколько раз.
Азитромицин при уретритах нехламидийной этиологии. Азитромицин проявляет высокую активность не только в отношении хламидии, но и других инфекций, которые могут передаваться при сексуальных контактах: Ureaplasma urealyticum, Mycoplasma genitalium, Neisseria gonorrhoeae и Haemophilus ducreyi. Mycoplasma hominis в большинстве случаев резистентна к азитромицину.
Азитромицин активен также и в отношении грамположительной (St. aureus, St. epidermidis, включая штаммы, продуцирующие бета-лактамазы, различных видов стрептококков, за исключением штаммов, резистентных к макролидам, и энтерококков) и грамотрицательной флоры (Haemophilus influenzae, Moraxella catarrhallis и др). Эти микроорганизмы также могут быть обнаружены в мочеполовых путях, но их роль в возникновении уретрита не доказана.
Рекомендации по применению азитромицина при хламидийной инфекции. Для лечения больных хламидийной инфекцией нижних отделов урогенитального тракта все вышеназванные руководства в качестве метода выбора рекомендуют однократный прием азитромицина в дозе 1,0 грамм, за 1 ч до еды или через 2 ч после, если препарат используется в капсулах, или независимо от приема пищи при приеме таблеток. Другим препаратом выбора является доксициклин, который назначают по 100 мг 2 раза в сутки в течение 7 дней. К недостаткам азитромицина в сравнении с доксициклином можно было бы отнести более высокую стоимость азитромицина. Однако согласно результатам фармакоэкономических исследований, проведенных CDC, более высокая стоимость азитромицина в сравнении с доксициклином компенсируется снижением затрат, связанных с лечением ВЗОМТ, эктопической беременности и бесплодия, возникающими из-за неадекватной терапии, связанной с несоблюдением назначенной схемы лечения, что значительно чаще встречается при назначении доксициклина.
К преимуществам азитромицина перед доксициклином, помимо более высокой комплаентности лечения, относятся лучшая переносимость, а также возможность применения у подростков.
Заключение. Таким образом, уникальные фармакокинетические характеристики азитромицина — продолжительный период полувыведения, высокий уровень всасывания и устойчивость в кислой среде, способность этого антибиотика транспортироваться лейкоцитами к месту воспаления, высокая и продолжительная концентрация в тканях, возможность проникновения внутрь клетки, а также простые схемы применения, высокая клиническая эффективность и комплаентность лечения, низкая токсичность сохраняют позицию азитромицина как основного препарата при лечении хламидийных уретритов у мужчин и другой патологии, связанной с хламидийной инфекцией.
Гомберг М. А., доктор медицинских наук
Соловьев А. М., кандидат медицинских наук
МГМСУ, Москва
ОАО Многопрофильный медицинский центр "Запсибгазпром", Тюмень
ОАО Многопрофильный медицинский центр "Запсибгазпром", Тюмень
Современные комбинированные препараты при лечении урогенитального трихомониаза и ассоциированных уретрогенных инфекций у мужчин
Журнал: Клиническая дерматология и венерология. 2013;11(3): 63‑68
Леонтьев И.Г., Леонтьев Д.И. Современные комбинированные препараты при лечении урогенитального трихомониаза и ассоциированных уретрогенных инфекций у мужчин. Клиническая дерматология и венерология. 2013;11(3):63‑68.
Leont'ev IG, Leont'ev DI. Current combination drugs in the treatment of urogenital trichomoniasis and associated urethrogenic infections in males. Klinicheskaya Dermatologiya i Venerologiya. 2013;11(3):63‑68. (In Russ.).
ОАО Многопрофильный медицинский центр "Запсибгазпром", Тюмень
ОАО Многопрофильный медицинский центр "Запсибгазпром", Тюмень
ОАО Многопрофильный медицинский центр "Запсибгазпром", Тюмень
Несмотря на некоторое снижение заболеваемости урогенитальным трихомониазом, воспалительные заболевания мочеполовой системы и репродуктивных органов, обусловленные Trichomonas vaginalis, остаются актуальной медико-социальной проблемой [1—3]. Кроме того, в последние годы по-прежнему регистрируются неудачи при лечении трихомониаза, наблюдается трихомонадоносительство, резистентность возбудителя к противотрихомонадным препаратам [2—9]. Трихомонадная инфекция является причиной возникновения воспалительных заболеваний органов мочеполовой системы у 23—40% мужчин [10]. Одна из особенностей трихомонад — их исключительная способность к ассоциации с другими возбудителями инфекций, передаваемыми половым путем (ИППП), поэтому трихомониаз у человека довольно часто протекает в составе микстинфекции (вместе с гонореей, хламидийной инфекцией, M. genitalium, Ureaplasma spp., кандидозом) [4, 11—13], что затрудняет его лечение и способствует возникновению посттрихомонадных осложнений. Нередко трихомонады выполняют роль резервуаров, сохраняя этих возбудителей в неизмененном виде (эндоцитобиоз), а некоторые из них внутри трихомонады даже активно размножаются. С этой точки зрения комбинированное применение антипротозойных препаратов и антибиотиков обосновано, особенно в острый и подострый период болезни. Инфекция распространяется из уретры в предстательную железу (ПЖ) через выводные протоки ПЖ, семявыбрасывающие протоки на семенном бугорке в собственные протоки семенных пузырьков [14]. Острый уретрит — один из самых распространенных синдромов среди ИППП, диагностируемых у мужчин [15]. Наиболее частым осложнением урогенитального трихомониаза и ассоциированных уретрогенных инфекций является воспаление ПЖ [14]. Использование комбинированного антибактериального препарата Сафоцид при лечении урогенитального трихомониаза и ассоциированных уретрогенных инфекций явилось предметом наших исследований.
В состав набора таблеток Сафоцид входят три препарата для лечения и профилактики разных видов инфекций: секнидазол 1 г (2 таблетки), азитромицин 1 г (1 таблетка), флуконазол 150 мг (1 таблетка).
Секнидазол относится к синтетическим производным нитроимидазола. Его фармакологическое действие — противомикробное и противопротозойное. Проникая в клетку и трансформируясь в ней с образованием свободных радикалов, препарат взаимодействует с ДНК, вызывая ее дегенерацию, подавляет синтез нуклеиновых кислот. После приема внутрь всасывается около 80% препарата. Максимальная концентрация в сыворотке крови достигается через 4 ч. Секнидазол метаболизируется в печени, его период полувыведения составляет 19 ч, выводится почками (в течение 72 ч — 16% от принятой дозы). Преимущества препарата перед другими производными нитроимидазола — однократность приема, высокая эффективность, короткий курс приема, сокращенный период наблюдения.
Азитромицина дигидрат является представителем подгруппы макролидных антибиотиков — азалидов, при создании в очаге воспаления высоких концентраций оказывает бактерицидное действие. Азитромицин хорошо проникает в органы и ткани урогенитального тракта (в частности в ПЖ). При пероральном приеме данный антибиотик очень быстро всасывается из желудочно-кишечного тракта в кровь, не вызывает обычных для антибиотиков побочных явлений со стороны желудочно-кишечного тракта, транспортируется в очаг воспаления полиморфноядерными нейтрофилами. В плазме крови длительно поддерживается его высокая концентрация, а максимальная концентрация достигается через 2—3 ч после приема. Азитромицин сохраняется в бактерицидных концентрациях в очаге воспаления в течение 5—7 сут после прекращения приема. Способность препарата преимущественно накапливаться в лизосомах играет важную роль в элиминации внутриклеточных микроорганизмов. Концентрация азитромицина в очагах инфекции достоверно выше, чем в здоровых тканях (в среднем на 24—34%) и коррелирует со степенью воспалительного отека. Азитромицин имеет весьма длительный период полувыведения — 34—68 ч, поэтому эффект продолжается и после окончания антибиотикотерапии. Азитромицин является антибиотиком широкого спектра действия и соответствует международному стандарту лечения негонококковых уретритов [16].
Флуконазол — представитель класса триазольных противогрибковых средств, 80% которого выводится с мочой в неизмененном виде. При этом в моче создается концентрация препарата, достаточная для лечения инфекции, вызванной Candida spp. Высокая биодоступность (более 90%) при приеме внутрь и длительный период полувыведения (около 30 ч) делают этот противогрибковый препарат удобным для применения. Для лечения кандидоза флуконазол назначают в дозе 3 мг/кг в сутки (для взрослых 150 мг/сут). Обычно используется пероральная форма флуконазола.
Цель настоящей работы — изучение эффективности, безопасности и переносимости Сафоцида, применяемого однократно, а также его влияния на клиническое течение и лабораторные показатели при лечении урогенитального трихомониаза и ассоциированных уретрогенных инфекций у мужчин.
Дизайн исследования
В исследование были включены мужчины, ранее не принимавшие противопротозойные и противогрибковые препараты, и не принимавшие антибиотики из группы макролидов в течение предшествующих 30 сут. В клиническое обследование не вошли больные с сифилисом и гонореей. Клинические проявления заболевания и лабораторные показатели регистрировали до лечения, а также через 1—2, 7—10 и 30 сут после лечения.
Материал и методы

Спектр возбудителей был следующим: T. vaginalis+C. trachomatis — 10 (29%) человек, T. vaginalis+C. trachomatis+M. genitalium — 12 (35%), T. vaginalis+U. urealyticum+M. genitalium — 7 (21%) больных, T. vaginalis+M. genitalium +C. albicans — 5 (15%) мужчин (рис. 2). Рисунок 2. Распределение больных по спектру возбудителей. Следует отметить высокую частоту выделения T. vaginalis в ассоциации с C. trachomatis и M. genitalium по сравнению с ассоциацией с другими микробами. Эту особенность можно рассматривать как возможный признак симбиоза указанных микроорганизмов. Полученные результаты указывают на эффективность и необходимость проведения комплексных лабораторных исследований при скрининге ИППП.
Жалобы больных были разнообразными (рис. 3, рис. 4). Рисунок 3. Структура жалоб в исследуемых группах. Рисунок 4. Клинико-лабораторные признаки.
Гиперемию кожи крайней плоти и головки полового члена отметили 5 (15%) пациентов, болезненность при пальпации уретры — 14 (41%), выделения из уретры — 22 (65%), эритему и отек наружного отверстия уретры — 22 (65%), зуд и жжение в уретре — 30 (88%), дизурию — 26 (77%). Болезненность при пальпации ПЖ испытывали 12 (35%) человек, отечность и болезненность ПЖ наблюдались у 12 (35%), увеличение содержания лейкоцитов в отделяемом уретры выявлено у 34 (100%), увеличение содержания лейкоцитов в первой порции мочи — у 8 (24%), увеличение содержания лейкоцитов в секрете ПЖ — у 12 (35%).
Лечение проводили по схеме, рекомендованной фирмой-производителем: однократный прием внутрь одновременно 4 таблеток, входящих в состав блистера Сафоцида, за 1 ч до или через 2 ч после еды.
Мужчины с установленным диагнозом урогенитального трихомониаза и ассоциированных уретрогенных инфекций, их половые партнеры были информированы о характере и особенностях течения заболевания. Всем половым партнерам также было рекомендовано обследование и лечение. Были даны следующие рекомендации: во время лечения исключить половые контакты, использовать барьерные методы контрацепции при половых контактах вплоть до констатации выздоровления. К полному излечению относили клиническое и этиологическое выздоровление.
Контроль излеченности по трихомониазу осуществляли через 7—10 сут после окончания терапии Сафоцидом, по хламидийной инфекции и инфекции, вызванной M. genitalium и Ureaplasma spp., — через 30 сут после окончания антибиотикотерапии.
Результаты
Через 1—2, 7—10 и 30 сут после лечения у всех пациентов проведена оценка эффективности и безопасности Сафоцида. Кроме результатов клинико-лабораторных исследований, учитывали любые неблагоприятные явления с момента последнего визита.

При оценке динамики стихания клинических симптомов отмечено, что на фоне лечения достаточно быстро купируются основные проявления инфекции (табл. 1). Так, при лечении больных с использованием Сафоцида гиперемия кожи крайней плоти исчезла у 4 (80%) из 5 пациентов, болезненность при пальпации уретры — у 13 (92,8%) из 14 пациентов, уретральные выделения исчезли у 20 (91%) из 22 пациентов, эритема и отек наружного отверстия уретры регрессировали у 21 (95,4%) из 22, зуд, жжение в уретре удалось купировать у 28 (93,3%) из 30, дизурия уменьшилась у 24 (92,4%) из 26, болезненность при пальпации ПЖ — у 10 (83,4%) из 12. По окончании лечения при ректальном исследовании отечность ПЖ регрессировала у 11 (91,6%) из 12 пациентов.
Содержание лейкоцитов в отделяемом уретры по окончании лечения нормализовалось у 33 (97,06%) из 34 пациентов. В первой порции мочи количество лейкоцитов уменьшилось у 7 (87,5%) из 8 пациентов. Нормализация количества лейкоцитов в секрете ПЖ отмечена у 10 (83,4%) из 12 пациентов.
У 2 пациентов с уретропростатитом наблюдались необильные слизисто-гнойные выделения из уретры, сохранились зуд, дизурия и болезненность при пальпации ПЖ. Кроме того, у них сохранился лейкоцитоз в секрете ПЖ, в мазках были обнаружены трихомонады, что рассматривалось нами как отсутствие этиологического и клинического выздоровления.

Спектр возбудителей имел следующий вид: Trichomonas vaginalis до лечения был обнаружен у 34 (100%) человек, а после курса терапии — у 2 (5,8%), С. trachomatis — у 22 (64,7%) и 1 (2,9) соответственно, M. genitalium — у 24 (70,5%) и 2 (5,8%), U.urealyticum — у 7 (20,5%) и 1 (2,9%), C. albicans — у 5 (15%) и 1 (2,9%) пациента соответственно (рис. 5). Рисунок 5. Динамика бактериологических показателей (абсолютные числа).
Из приведенных данных следует, что эффективность лечения с использованием Сафоцида составляет при Trichomonas vaginalis — 94,2%, при С. trachomatis — 97,1%, при M. genitalium — 94,2%, при U. urealyticum — 97,1%, при C. аlbicans — 97,1%.
Показатели биохимической гепатограммы и общего анализа крови, как до начала терапии, так и по ее завершении, оставались в пределах нормы (табл. 2 и 3).
Таким образом, как ближайшие, так и отдаленные результаты лечения урогенитального трихомониаза и ассоциированных уретрогенных инфекций у мужчин свидетельствуют о высокой эффективности и безопасности Сафоцида в стандартных терапевтических дозах (секнидазол — 2000 мг, азитромицин — 1000 мг, флуконазол — 150 мг). Почти все больные лечение перенесли без побочных эффектов. Лишь в 2 (5,8%) случаях была отмечена 2-часовая головная боль, которая купировалась самостоятельно (без применения специальной терапии).
Заключение
На основании проведенных клинических исследований можно сделать следующие выводы.
Сафоцид — эффективный препарат для лечения урогенитального трихомониаза и ассоциированных уретрогенных инфекций.
Клиническая эффективность Сафоцида составляет 80—95,4% (в зависимости от симптомов), а бактериологическая — 94,2—97,1% (в зависимости от возбудителя).
Препарат отличается хорошей переносимостью и небольшим количеством побочных эффектов (наблюдались у 2 пациентов из 34), имеет доступную цену, а также малую токсичность, что соответствует требованиям ВОЗ, которым должны отвечать препараты для лечения ИППП. Возможны пероральный прием и однократное применение.
Препарат Сафоцид содержит все необходимые современные эффективные компоненты в одной упаковке, что позволяет использовать его при лечении смешанных инфекций. Кроме того, Сафоцид удобен в применении, что позволяет использовать его в амбулаторной практике.
До настоящего времени инфекции, передающиеся половым путем (ИППП), остаются важнейшей проблемой здравоохранения. Интерес к этой тематике обусловлен произошедшими в нашей стране глубокими социально-экономическими изменениями, приведшими к росту заболеваемости ИППП, которые нередко влекут за собой развитие осложнений со стороны репродуктивной системы мужчин и женщин.
В настоящей статье будут освещены вопросы терапии наиболее значимых урогенитальных инфекционных заболеваний.
Основными препаратами, применяемыми в терапии гонококковой инфекции, являются цефалоспорины III поколения (цефтриаксон, цефотаксим), фторхинолоны (ципрофлоксацин, офлоксацин) и спектиномицин.
До настоящего времени, несмотря на наличие высокоэффективных антимикробных препаратов, во всем мире гонорея остается трудноконтролируемым заболеванием, на эпидемиологию которого значительное влияние оказывают социальные, демографические и поведенческие факторы. Наиболее серьезной проблемой в терапии гонореи являются рост и быстрое распространение резистентности гонококка как к традиционно применяющимся, так и к новейшим антибиотикам.
В последние годы вопросами резистентности гонококка к антибактериальным препаратам занимаются исследователи многих стран мира. В Российской Федерации благодаря внедрению в 2004 г. системы мониторинга антибиотикорезистентности продемонстрирована высокая степень резистентности возбудителя к традиционно применяемым препаратам, а также выявлена тенденция к изменению чувствительности микроорганизма к препаратам, появившимся на фармацевтическом рынке сравнительно недавно. В 2006 г. обнаружены однонаправленные тенденции роста устойчивости гонококков к пенициллинам, тетрациклинам, ципрофлоксацину, а в ряде регионов – к спектиномицину, что позволило внести коррективы в схемы лечения гонореи в зависимости от региональной принадлежности штаммов. В настоящее время ввиду распространенности перекрестной резистентности штаммов гонококков можно прогнозировать возрастание уровня устойчивости как к ципрофлоксацину, так и к другим представителям группы фторхинолонов.
Одним из антибиотиков, обладающих активностью в отношении возбудителя гонококковой инфекции, является азитромицин. Согласно данным проведенных исследований, резистентность N. gonorrhoeae к нему до последнего времени оставалась на низком уровне и составляла в различных регионах от 1 до 3 %. Хотя в настоящее время азитромицин не входит в список препаратов, рекомендуемых международными руководствами для лечения гонореи, в некоторых ситуациях, в частности при непереносимости других лекарственных средств, его применение может быть вполне оправданным.
Следует особо подчеркнуть, что азитромицин является эффективным препаратом и для лечения другой распространенной ИППП – хламидийной инфекции. Урогенитальный хламидиоз довольно часто бывает ассоциирован с гонококковой инфекцией, однако воспалительный процесс, как правило, протекает без клинических симптомов, что в отсутствие своевременной диагностики и лечения может привести к длительному течению заболевания, развитию осложнений, нарушению репродуктивной функции.
Современные схемы лечения хламидийной инфекции основаны на применении одного из антибиотиков следующих фармакологических групп: макролидов (азитромицин, джозамицин, кларитромицин, рокситромицин и др.), фторхинолонов (офлоксацин, левофлоксацин, моксифлоксацин и др.) и тетрациклинов (доксициклин). Доза препарата и длительность лечения зависят от характера течения заболевания и определяются врачом.
Наиболее часто рекомендуется применение азитромицина. Среди макролидов он способен создавать самые высокие концентрации в тканях, характеризуется хорошей переносимостью. Прием пищи несколько снижает биодоступность этого препарата, поэтому желателен его прием натощак. Период полувыведения азитромицина достигает 55 часов, что позволяет однократно применять его при хламидиозе нижних отделов мочеполового тракта. Согласно данным Веселова А.В. и соавт. (2006), азитромицин при однократном применении обладает 96 %-ной эффективностью, что соответствует эффективности доксициклина, назначаемого дважды в день в течение 7 дней.
Азитромицин также является одним из препаратов выбора в терапии урогенитальных инфекционных заболеваний, ассоциированных с генитальными микоплазмами. По материалам публикаций, около 40 % воспалительных заболеваний мочеполовых органов ассоциированы с микоплазмами, три из которых (Ureaplasma urealyticum, Mycoplasma hominis, Mycoplasma genitalium) считаются возбудителями урогенитальных инфекций. Известно, что человек является хозяином 16 видов микоплазм, причем 6 выделяют в урогенитальном тракте: M. hominis, U. urealyticum, M. primatum, M. genitalium, M. spermatophilum и M. penetrans.
Результаты изучения этиологического спектра негонококковых уретритов свидетельствуют о том, что выявление M. genitalium и U. urealyticum является независимым фактором риска развития их хронических форм (Horner P.J., 2003). Что касается острого негонококкового уретрита, то из всех микоплазм только M. genitalium ассоциирована с этим заболеванием, в то время как U. urealyticum ответственна за рецидивирование уретритов после проведенного лечения.
Одним из самых распространенных заболеваний мочеполового тракта на сегодняшний день остается урогенитальный трихомониаз, который занимает ведущее место в структуре ИППП. В мире им страдают около 170 млн человек. Это широкораспространенное паразитарное заболевание, вызываемое Trichomonas vaginalis, одинаково часто поражает как мужчин, так и женщин.
По оценке CDC, 5 % клинических изолятов T. vaginalis показали некоторую степень устойчивости к метронидазолу и тинидазолу, что заставило исследователей заняться поиском альтернативных препаратов для лечения урогенитального трихомониаза. Одним из них является секнидазол с таким же спектром активности, как и другие нитроимидазолы, но, по мнению Videau D. и соавт. (1978), более предпочтителен ввиду длительного поддержания в крови активных концентраций, т. к. его период полувыведения составляет 19 часов (у тинидазола – 12 часов, у орнидазола – 14). По сравнению с метронидазолом секнидазол менее токсичен и лучше переносится пациентами.
Секнидазол широко применяется и в терапии бактериального вагиноза – общего инфекционного невоспалительного синдрома полимикробной этиологии, связанного с дисбиозом влагалищного биотопа, который характеризуется резким увеличением облигатных и факультативных анаэробных условно-патогенных микроорганизмов и снижением или полным исчезновением лактобактерий, особенно перекисьпродуцирующих. Активность секнидазола в отношении анаэробов дает возможность использовать его в лечении этого заболевания.
Наряду с бактериальным вагинозом в клинической практике специалисты нередко сталкиваются с другой причиной вагинальных выделений – урогенитальным кандидозом – инфекционным поражением слизистой оболочки вульвы и влагалища, вызываемым дрожжеподобными грибами рода Candida. Как в России, так и во многих других странах кандидоз занимает одно из ведущих мест в структуре акушерско-гинекологической заболеваемости и является одной из наиболее частых причин обращения женщин за медицинской помощью. Частота кандидозного вульвовагинита за последние 10 лет почти удвоилась и составляет 30–45 % среди инфекционных поражений вульвы и влагалища.
В настоящее время препаратом выбора при лечении кандидаинфекции является флуконазол. Его основным преимуществом перед другими препаратами, применяемыми в терапии урогенитального кандидоза, является отсутствие влияния на гормональный профиль макроорганизма, что значительно снижает частоту побочных реакций. Биодоступность флуконазола достигает 94 %, а длительный период полувыведения (30 часов) позволяет использовать однократный прием препарата при кандидозном вульвовагините. По данным Страчунского Л.С. и соавт. (2000), клинический эффект при длительном наблюдении сохранялся после применения флуконазола у 93 % пациентов, при неэффективности предыдущей терапии – у 98 %, при рецидивирующем кандидозном вульвовагините – у 95 %; в случае терапии заболевания клотримазолом эти показатели составили 84, 85 и 85 % соответственно.
Таким образом, за последние десятилетия возросло количество научных исследований, посвященных диагностике и лечению урогенитальных инфекций, появились новые данные о лекарственных средствах и схемах их применения при ИППП и нарушениях микробиоценоза влагалища (бактериальном вагинозе, кандидозном вульвовагините), что привело к необходимости оптимизации подходов к назначению тех или иных препаратов. Всемирная организация здравоохранения определила ряд критериев, которым должны соответствовать лекарственные средства, используемые при лечении ИППП:
- эффективность не менее 95 %;
- малая токсичность и хорошая переносимость;
- возможность однократного применения;
- пероральный прием;
- возможность назначения во время беременности;
- медленное развитие резистентности микроорганизмов к проводимой терапии;
- обеспечение высокой комплаентности;
- доступная цена.
В настоящее время на фармацевтическом рынке появился уникальный препарат, соответствующий вышеперечисленным критериям, – Сафоцид (содержит в одной блистерной упаковке одну таблетку азитромицина 1 г, две – секнидазола по 1 г и одну – флуконазола 150 мг), удобный для терапии микст-инфекций урогенитальной системы.
Показаниями к назначению Сафоцида являются ИППП (гонорея, трихомониаз, хламидиоз) и неспецифические урогенитальные заболевания (бактериальный вагиноз, в т. ч. в ассоциации с генитальными микоплазмами; урогенитальный кандидоз).
В 2007 г. в ГУ “Центральный научно-исследовательский кожно-венерологический институт” Росздрава проведено исследование, целью которого стало изучение эффективности, безопасности и переносимости препарата Сафоцид, применяемого однократно у больных ИППП (гонорея, урогенитальный трихомониаз, хламидиоз) и неспецифическими урогенитальными инфекционными заболеваниями (бактериальный вагиноз; урогенитальный кандидоз; заболевания урогенитальной системы, ассоциированные с генитальными микоплазмами).
В исследование были включены 40 пациентов обоего пола, разделенные на четыре группы:
- 1-я – 5 пациентов с гонореей в сочетании с другими ИППП и/или вышеуказанными неспецифическими урогенитальными заболеваниями;
- 2-я – 5 пациентов с урогенитальным трихомониазом в сочетании с другими ИППП и/или неспецифическими урогенитальными заболеваниями;
- 3-я – 15 пациентов с хламидиозом в сочетании с другими ИППП и/или неспецифическими урогенитальными заболеваниями;
- 4-я – 15 пациентов с неспецифическими урогенитальными заболеваниями в различных сочетаниях.
Перед включением пациентов в исследование выполнялись следующие процедуры: сбор анамнеза (демографические данные, сведения о сопутствующих заболеваниях и сопутствующей терапии), оценка витальных показателей (частота сердечных сокращений, артериальное давление, температура тела), физикальное обследование (наружный осмотр аногенитальной области, бимануальное гинекологическое исследование, обследование с помощью гинекологического зеркала Куско), тест на беременность, получение клинического материала для лабораторного исследования. Последнее включало: проведение аминотеста и рН-метрию влагалищного экссудата; микроскопическое исследование клинического материала из уретры, боковых и заднего сводов влагалища, цервикального канала и прямой кишки (U, C, R, V); культуральное исследование на N. gonorrhoeae, T. vaginalis, генитальные микоплазмы (M. hominis, U. urealyticum) с их количественным определением; бактериологическое исследование состава вагинального микробиоценоза (аэробные, анаэробные микроорганизмы, грибы Candida); определение чувствительности условно-патогенных микроорганизмов к антибактериальным препаратам; культуральное и/или ПИФ и/или ПЦР исследование на C. trachomatis; ПЦР исследование на M. genitalium; серологическое исследование на сифилис и ВИЧ; клинический анализ крови и мочи; биохимическое исследование крови.
На момент обращения за медицинской помощью длительность заболевания у пациентов составляла от трех дней до месяца.
Основными субъективными проявлениями урогенитальных инфекций были: патологические выделения из половых путей – в 26 (65,0 %) случаях, дизурия – в 18 (45,0 %), диспареуния – в 28 (70,0 %), зуд и/или жжение в области наружных половых органов – в 19 (47,5 %).
При физикальном обследовании клинические признаки уретрита (гиперемия, отек слизистой наружного отверстия уретры, патологические уретральные выделения) выявлены в 15 (37,5 %), вульвовагинита (гиперемия, отек слизистой вульвы и/или влагалища, патологические вагинальные выделения) – в 10 (25,0 %), цервицита (гиперемия, отек, рыхлость слизистой экто- и/или эндоцервикса, патологические выделения из цервикального канала) – в 15 (37,5 %), цистита (дизурические явления, лейкоцитурия) – в 8 (20,0 %) случаях.
У 18 (45,0 %) пациенток 3-й и 4-й групп при проведении аминотеста получены положительные результаты; значение рН вагинального экссудата превышало 4,5.
По результатам лабораторного исследования у пациентов 1-й группы диагностирована гонорея в двух наблюдениях в виде моноинфекции, в одном – в ассоциации с C. trachomatis, в двух – в ассоциации с условно-патогенными микроорганизмами (G. vaginalis, генитальные микоплазмы). У пациентов 2-й группы диагностирован урогенитальный трихомониаз в трех наблюдениях в виде моноинфекции, в двух – в ассоциации с условно-патогенными микроорганизмами (генитальные микоплазмы). У пациентов 3-й группы хламидиоз нижних отделов мочеполового тракта в виде моноинфекции наблюдался в 5 случаях, а его сочетание с условно-патогенными микроорганизмами G. vaginalis, Candida, генитальные микоплазмы) – в 10 наблюдениях. У пациентов 4-й группы урогенитальные инфекции были вызваны условно-патогенными микроорганизмами в различных ассоциациях (G. vaginalis, Candida, генитальные микоплазмы в титрах более 104 КОЕ/мл).
Все включенные в исследование пациенты получали терапию препаратом Сафоцид, назначенным однократно перорально (все 4 таблетки, входящие в блистер) за час до или через 2 часа после еды.
Через 7–10 дней после назначения терапии пациентам 1-й и 2-й групп и через 28 дней – пациентам 3-й и 4-й групп произведена оценка эффективности и безопасности Сафоцида. При этом осуществлялось физикальное обследование, в т. ч. исследование органов малого таза и определение признаков/симптомов по совокупности показателей (табл. 1); оценка витальных показателей; запись любых неблагоприятных явлений с момента последнего визита. Лабораторные исследования включали: микроскопическое исследование (U, C, V, R), культуральное исследование показателей вагинального микроценоза (аэробные и анаэробные микроорганизмы), культуральное исследование на N. gonorrhoeae (в 1-й группе), культуральное исследование на T. vaginalis (во 2-й группе), культуральное и/или ПИФ и/или ПЦР исследование на C. trachomatis (в 3-й группе), культуральное исследование на M. hominis и U. urealyticum (в 4-й группе). Во время контрольного визита дополнительно проводились клинические исследования крови и мочи, биохимическое исследование крови.
Как свидетельствуют представленные в табл. 1 данные, клиническая эффективность терапии достигнута в 80 % наблюдений у пациентов 1-й и 2-й и в 93,3 % – 3-й и
4-й групп. Субъективные симптомы в виде диспареунии у двух пациентов 1-й и 2-й групп расценены как остаточные явления перенесенного воспалительного процесса, т. к. при повторном обследовании через неделю после 2-го визита пациенты не предъявляли жалоб со стороны урогенитальной системы. У одной пациентки 4-й группы при контрольном обследовании выявлены клинические признаки бактериального вагиноза, аналогичные таковым до назначения терапии.
При оценке витальных показателей ни в одном из наблюдений не отмечено отклонений от нормы.
Микробиологическая эффективность проведенной терапии оценивалась через две–четыре недели после приема Сафоцида (в зависимости от этиологического агента). Результаты лабораторных исследований представлены в табл. 2.
Согласно полученным данным, эрадикация возбудителей ИППП (N. gonorrhoeae, T. vaginalis, С. trachomatis) достигнута в 100 % случаев. Во время 2-го визита ни у кого из пациентов 1-й и 2-й групп не наблюдалось отклонений от нормы при микроскопическом и микробиологическом исследованиях. У одной пациентки 3-й группы выявлен лейкоцитоз при микроскопическом исследовании цервикального секрета, что, возможно, связано с наличием у нее эрозии шейки матки. У 13 (86,7 %) пациентов 4-й группы достигнута эрадикация условно-патогенных микроорганизмов, в остальных наблюдениях отмечено снижение титров последних менее 103 КОЕ/мл. У одной пациентки во время 2-го визита отмечены клинические признаки бактериального вагиноза (положительный аминотест, рН > 4,5, “ключевые клетки”).
Следовательно, терапия препаратом Сафоцид позволила достичь эрадикации патогенных возбудителей в 100 %, а условно-патогенных – в 86,7 % наблюдений.
При анализе показателей клинических анализов крови и мочи во время 2-го визита выраженных отклонений от нормы не выявлено. В 2 (5,0 %) случаях отмечено повышение активности печеночных ферментов (АЛТ, АСТ) не более 100 % по сравнению с нормальным исходным уровнем. В остальных наблюдениях клинически значимых изменений биохимических параметров крови не зафиксировано.
Таким образом, по итогам проведенного исследования, Сафоцид продемонстрировал высокую эффективность в терапии урогенитальных инфекционных заболеваний, ассоциированных с патогенными и условно-патогенными микроорганизмами. Клиническая эффективность препарата составила 93,3–100,0 %, микробиологическая – 86,7–100,0 %. Полученные данные дают возможность рекомендовать Сафоцид для терапии урогенитальных инфекций как средство, характеризующееся высокой эффективностью, низкой частотой развития побочных эффектов и удобством применения, а также обеспечивающее высокую комплаентность.
В заключение необходимо еще раз подчеркнуть недопустимость самолечения ИППП, т. к. в подавляющем большинстве случаев только врач может правильно диагностировать заболевание и назначить адекватный курс терапии с учетом индивидуальных особенностей конкретного пациента. При самолечении нередко развивается резистентность возбудителей к тем или иным препаратам, что в дальнейшем ведет к необходимости назначения более длительных курсов терапии.
Что такое трихомониаз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Агапова Сергея Анатольевича, венеролога со стажем в 39 лет.
Над статьей доктора Агапова Сергея Анатольевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов
Определение болезни. Причины заболевания
Урогенитальный трихомониаз — это передающаяся половым путём инфекция мочеполовой системы, вызванная влагалищной трихомонадой (Trichomonas vaginalis).
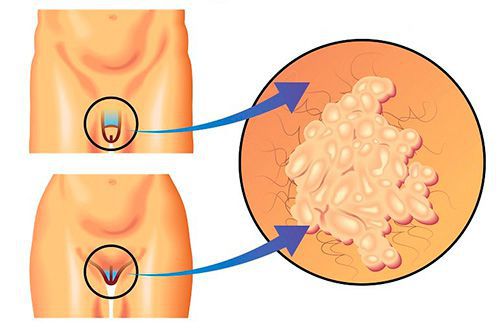
Насколько распространён трихомониаз
Что такое трихомониаз, трихомонады и их виды
Причиной заболевания является инфицирование мочеполовых органов влагалищной трихомонадой — одноклеточным жгутиковым простейшим организмом изменчивой формы, который в естественных условиях может существовать и размножаться только в организме человека. Помимо вагинальной трихомонады у человека могут паразитировать ещё два вида — кишечная трихомонада (Pentatrichomonas hominis) и ротовая (Trichomonas tenax), однако их роль в возникновении заболеваний мочеполовой системы не установлена.
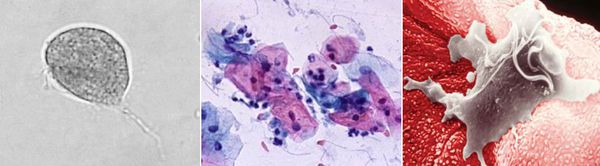
Трихомонада, так как не образует цист и других устойчивых форм, быстро погибает во внешней среде вследствие высыхания, легко разрушается при кипячении, воздействии антисептиков и этилового спирта. Однако может сохранять некоторое время жизнеспособность во влажной среде. Исследованиями установлено, что трихомонады могут выживать до 45 минут на сидениях унитазов, нижнем белье и в воде ванны. [3]
Как можно заразиться трихомониазом
Пути передачи инфекции:
Факторами риска являются:
- случайные половые связи;
- половой контакт, незащищённый барьерной контрацепцией (презервативом);
- злоупотребление алкоголем и наркомания; [7]
- атрофия шейки матки — вследствие снижения защитных свойств из-за уменьшения эстрогенов в тканях; [8]
- наличие других половых инфекций, таких как ВИЧ-инфекция, бактериальный вагиноз, вульвовагинальный кандидоз, генитальный герпес, хламидиоз. [9]
Защищает ли презерватив от трихомониаза
Использование презервативов снижает вероятность заражения. Однако микроорганизмы могут попасть на области, не закрытые ими, поэтому презервативы не могут полностью защитить от трихомониаза [52] .
Передаётся ли трихомониаз во время орального секса
Микроорганизмы способны поражать различные части тела, например, руки или рот. Оральный секс с инфицированным партнёром может привести к заражению трихомониазом ротовой полости [52] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы трихомониаза
Чаще трихомониаз диагностируется у женщин, чем у мужчин. У 10-30 % женщин и у 45-50 % мужчин отмечается асимптомное течение заболевания . [10]
Симптомы трихомониаза у женщин
У женщин трихомонады преимущественно поражают влагалище, откуда они могут проникать в уретру, бартолиновы железы, мочевой пузырь и канал шейки матки. В редких случаях трихомонады паразитируют в полости матки, маточных трубах, почечных лоханках и прямой кишке. [11]
Основными симптомами трихомониаза у женщин являются:
Редкими проявлениями трихомониаза у женщин являются:
- макулярный кольпит (клубничный цервикс) — кровоизлияния в слизистую влагалища и шейку матки, напоминающее ягоду клубники; [12]
- эрозивно-язвенные поражения вульвы и преддверия влагалища. [13]
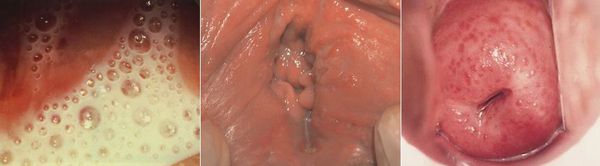
Симптомы трихомониаза у мужчин
У мужчин трихомонады поражают слизистую оболочку мочеиспускательного канала, нередко проникая в уретральные железы и лакуны. Ввиду неблагоприятных условий для существования в мужской уретре трихомонад, заболевание часто носит транзиторный (временный) характер. Этим же объясняется и большой процент асимптомных форм трихомониаза у мужчин. [14]
Основными симптомами трихомониаза у мужчин являются:
Редким проявлением трихомониаза у мужчин является баланопостит (воспаление головки и крайней плоти полового члена). Описаны его эрозивно-язвенные формы. [15]
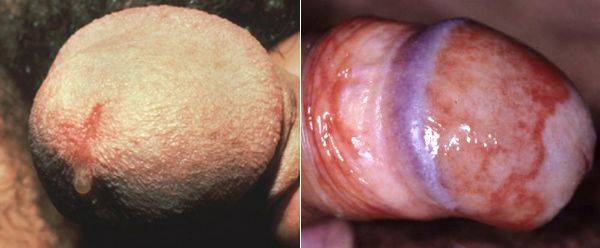
Патогенез трихомониаза
Проникая в урогенитальный тракт человека, трихомонады прикрепляются к эпителиальным клеткам, что приводит к повреждению и воспалительной реакции клеток эпителия. В этой реакции важное значение имеет адгезин — белок, продуцируемый паразитом. [16]
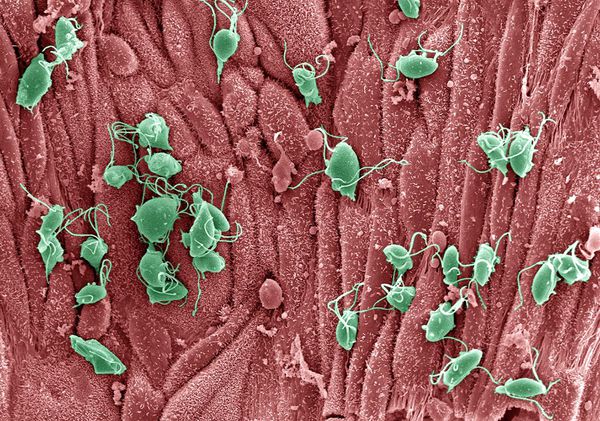
Трихомонады выделяют многочисленные протеолитические ферменты, которые участвуют в цитотоксичности, гемолизе (разрушении эритроцитов и выделении гемоглобина) и уклонении от иммунных реакций. Ферменты находятся во влагалищных выделениях инфицированных женщин вместе с антителами, которые их распознают. Важную роль играет фермент муциназа, который значительно облегчает проникновение трихомонад в слизистые оболочки. [17]
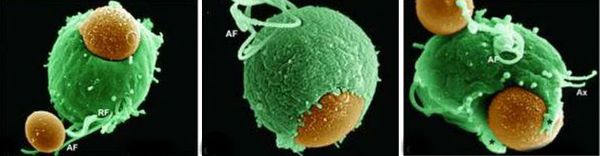
Трихомонадная инфекция вызывает клеточный, гуморальный и секреторный иммунные ответы. Однако эти реакции не способны защитить пациентов от реинфекции, поэтому повторное инфицирование встречается часто. Антитела и компоненты комплемента, присутствующие в сыворотке крови и секрете половых желез у некоторых больных, могут воздействовать на паразита путём стимуляции нейтрофилов, которые способствуют уничтожению трихомонад через классическую систему комплемента. Также антитела могут блокировать адгезию (прилипание) паразита к поверхности слизистой оболочки. [21]
Классификация и стадии развития трихомониаза
По Международной классификации болезней 10-го пересмотра трихомониаз разделяют на:
A59.0 Урогенитальный трихомониаз;
- Бели (вагинальные выделения), вызванные Trichomonas vaginalis; (N51.0), вызванный Trichomonas vaginalis;
A59.8 Трихомониаз других локализаций;
A59.9 Трихомониаз неуточнённый.
Стадии заболевания
После скрытого (инкубационного) периода, продолжающегося от 4 до 28 дней с момента заражения, приблизительно у 40-50% мужчин появляются признаки уретрита в виде слизистых выделений из уретры, а у 70-90% женщин — признаки вульвовагинита, характеризующегося зудом, жжением и наличием обильных мутных выделений из влагалища. [10] В остальных случаях болезнь протекает первоначально бессимптомно. В дальнейшем, если вовремя не получено лечение, развитие заболевания происходит по следующим сценариям:
- Длительное бессимптомное носительство, при котором нет никаких субъективных и объективных симптомов.
- Длительное рецидивирующее течение, при котором симптомы заболевания могут временно возобновляться и самопроизвольно исчезать.
- Ранее развитие осложнений может возникать как при течении заболевания с клиническими симптомами, так и при бессимптомном течении.
- Позднее развитие осложнений возникает при длительно текущем бессимптомном или хроническом рецидивирующем процессе.
Осложнения трихомониаза
В отличии от других половых инфекций – хламидийной и гонококковой — осложнения при трихомониазе встречаются гораздо реже.
Осложнения у мужчин
Эпидидимит — воспаление придатка яичка, очень редкое осложнение трихомонадной инфекции. Чаще всего это хронический процесс, хотя встречаются описания острых форм. [22]
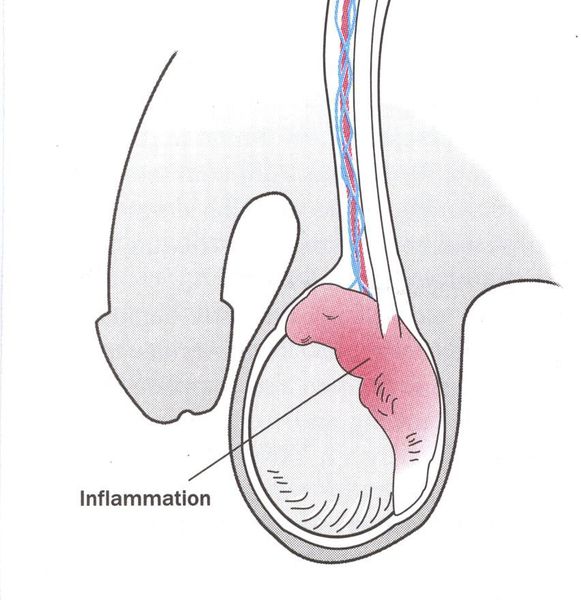
Редким осложнением трихомониаза является простатит. Сообщается о нескольких случаях хронического простатита, вызванного трихомонадной инфекцией. [23]
Нарушение фертильности. Проведенные исследования показывают негативное воздействие трихомонад на сперматозоиды мужчин в виде снижения их подвижности. [24]
Сообщается также о случае трихомонадного двухстороннего конъюнктивита. [31]
Осложнения у женщин
Воспалительные заболевания малого таза, вызванные вагинальной трихомонадной инфекцией, являющиеся причиной трубного бесплодия и синдрома хронической абдоминальной боли, описаны, в основном, у ВИЧ-позитивных женщин. [25]
Проведённые исследования указывают на повышенный риск преждевременных родов, рождения ребёнка с низким весом у инфицированных влагалищной трихомонадой женщин. [26]
Также трихомонадная инфекция в 2-3 раза увеличивает риск заражения ВИЧ. [32]
Очень редким осложнением трихомониаза является цистит. В медицинской литературе описано всего несколько случаев. [33]
Прочие осложнения
Сообщалось о паранефральном абсцессе [27] , абсцессе головного мозга [28] у новорождённого, абсцессе срединного шва полового члена [29] у мужчины, вызванных вагинальной трихомонадой.
Описаны случаи неонатальной трихомонадной пневмонии у новорождённых, успешно вылеченных метронидазолом. [30]
Диагностика трихомониаза
Для диагностики трихомониаза применяются микроскопические, цитологические, бактериологические, молекулярные лабораторные тесты и инструментальные методы обследования.
Показаниями для диагностики трихомониаза являются [2] :
- наличие признаков воспалительного процесса мочеполовых органов;
- беременность (при постановке на учёт по поводу беременности, при сроке беременности 27-30 недель и 36-40 недель, при поступлении на роды без документов о результатах обследования на половые инфекции);
- предстоящие оперативные вмешательства на половых органах и органах малого таза;
- бесплодие и выкидыши в анамнезе;
- половые контакты с больными половыми инфекциями;
- сексуальное насилие.
Микроскопическое исследование
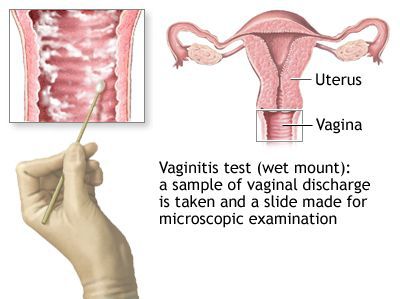
Микроскопия окрашенного препарата (окраска по Романовскому, Папаниколау) не рекомендуется из-за субъективизма при интерпретации результатов исследования. [2]
Культуральное исследование
Молекулярно-биологические методы
Материалом для исследования методом ПЦР при диагностике трихомониаза являются:
- у женщин: выделения из уретры, канала шейки матки, влагалища, первая порция мочи);
- у мужчин: выделения или соскоб из уретры, первая порция мочи, секрет предстательной железы, в редких случаях — сперма. [2]
Требования для получения достоверных результатов исследования:
- Забор материала должен осуществляться не ранее чем через месяц после полученного лечения.
- При отсутствии или скудных выделениях из уретры забор материала должен проводиться через 2-3 часа после последнего мочеиспускания, а при наличии обильных выделений — через 10-15 минут после мочеиспускания.
- Во время менструации забор материала для исследования проводить запрещается.
- Должны быть соблюдены сроки и условия доставки образцов в лабораторию.
Серологическое исследование
Метод иммуноферментного анализа (ИФА) для обнаружения антител классов IgA, IgM и IgG к антигенам T. vaginalis применять не допустимо. [2]
Применение биологических (парентеральное введение пирогенала, гоновакцины), химических (внутриуретральное введение растворов серебра) и алиментарных провокаций (приём алкоголя и острой пищи) с целью повышения выявляемости трихомонад при проведении лабораторных тестов нецелесообразно, так как эффективность этого метода не доказана. [2]
Лечение трихомониаза
Многочисленными исследованиями и клиническими испытаниями было установлено, что наиболее эффективными препаратами для лечения трихомониаза являются препараты группы 5-нитроимидазолов, а среди них — метронидазол, тинидазол и орнидазол.
Современными отечественными и зарубежными руководствами предложены следующие схемы лечения этими препаратами.
Метронидазол (Трихопол, Метрогил, Флагил) — эффективность его применения составляет 90-95%.
Для неосложнённых форм заболевания: 500 мг перорально 2 раза в сутки в течение 7 дней [36] или 2,0 г перорально однократно. [37]
Для осложнённых форм: 500 мг перорально 3 раза в сутки в течение 7 дней или 2,0 г внутрь 1 раз в сутки в течение 5 дней. [38]
Для беременных: 2,0 г однократно (лечение проводится не ранее II триместра беременности). [39]
Для детей: 10 мг на кг массы тела перорально 3 раза в сутки в течение 5 дней. [40]
Тинидазол (Фазижин, Тиниба) — эффективность применения составляет 86-100%.
Для неосложнённых форм заболевания: 500 мг перорально 2 раза в сутки в течение 5 дней или 2,0 г перорально однократно. [35]
Для осложнённых форм: 2,0 г перорально 1 раз в сутки в течение 3 дней. [37]
Орнидазол (Тиберал, Гайро, Дазолик) — эффективность применения составляет 90-100%.
Для неосложнённых форм заболевания: 500 мг перорально 2 раза в сутки в течение 5 дней [41] или 1,5 г перорально однократно. [42]
Для осложнённых форм: 500 мг перорально 2 раза в сутки в течение 10 дней. [38]
Для детей: 25 мг на кг массы тела перорально 1 раз в сутки в течение 5 дней. [39]
Другие препараты из группы 5-нитроимидазолов — менее распространены и изучены, чем вышеизложенные препараты, однако применяются в клинической практике:
- Тенонитрозол (Атрикан) — 250 мг перорально 2 раза в день в течение 4 дней; [43]
- Ниморазол (Наксоджин) — схемы применения при неосложнённом трихомониазе: 2,0 г перорально однократно или 1,0 г перорально через каждые 12 часов – три приёма, или 250 мг перорально 2 раза в день в течение 6 дней. [44]
- Секнидазол (Тагера) — 2,0 г перорально однократно (эффективность 97%). [45]
Причины неудач в лечении
В 5 % случаев трихомонады устойчивы (резистентны) к перечисленным препаратам [46] . Центры по контролю за заболеваемостью (США) в таких случаях рекомендуют увеличить дозировку и длительность применения медикаментов [47] : Метронидазол — 2,0 г перорально однократно в сутки в течении 7 дней или Тинидазол 2,0 г перорально однократно в сутки в течении 7 дней.
Дисульфирам-подобная реакция на препараты
Нитроимидазолы блокируют и снижают выработку фермента алкоголь-дегидрогеназы, что приводит к повышению уровня и накапливанию токсического ацетальдегида в крови. При приёме алкоголя в любых концентрациях во время лечения препаратами, входящими в группу нитроимидазолов, через 10-20 минут возникает реакция в виде тошноты, рвоты, головной боли, затруднения дыхания, судорог. Длительность её составляет несколько часов. Реакция наблюдается при приёме метронидазола, тинидазола [48] и орнидазола [49] .
Помимо исключения алкоголя, рекомендаций по изменению привычек или особенностям питания при лечении трихомониаза нет.
Установление излеченности трихомонадной инфекции
Проводится через две недели после окончания лечения микроскопией и культуральным посевом и через 4 недели методом ПЦР. При отрицательных результатах лабораторных тестов пациенты дальнейшему наблюдению не подлежат. [2]
Можно ли заниматься сексом при трихомониазе
Заниматься сексом можно через 7-10 дней после завершения лечения трихомониаза. Примерно каждый пятый выздоровевший заражается вновь в течение трёх месяцев после окончания лечения. Чтобы избежать повторного заражения, лечение должны пройти все сексуальные партнеры. Если симптомы возникли снова, нужно пройти повторное обследование [52] .
Прогноз. Профилактика
Прогноз при раннем выявлении и вовремя начатом лечении благоприятный. При неосложнённых формах трихомонадной инфекции после однократного курса выздоровление составляет 95-100%. Лица с осложнёнными формами и метронидазол-устойчивыми формами заболевания после проведённого лечения должны находиться под динамическим наблюдением.
Половые партнёры больных трихомониазом должны быть пролечены независимо от результатов их обследования на наличие трихомонад.
Самой эффективной мерой профилактики является использование презервативов при случайных половых контактах.
Ввиду бессимптомного течения инфекции лицам, имеющим несколько половых партнёров в год или случайные половые связи, рекомендовано ежегодное обследование на наличие трихомонад.
В настоящее время вакцины, предотвращающей заражение трихомониазом, не создано. В 80-е годы прошлого века была создана коммерческая вакцина Солкотриховак, состоящая из лиофилизата Lactobacillus acidophilus, которая по утверждению фирмы-производителя оказывает положительный эффект при рецидивирующем трихомониазе и бактериальном вагинозе. [50] Однако последующими исследованиями предположение о том, что защитный механизм действия вакцины связан на антигенном сходстве применяемых штаммов лактобацилл и вагинальной трихомонады, было отвергнуто. [51]
Читайте также:

