Сальмонеллезный менингит у детей
Обновлено: 14.05.2024
Бактериальные гнойные менингиты (БГМ) являются наиболее распространенной формой нейроинфекции у детей, особенно в возрасте до 5 лет. Группу риска представляют дети первых двух лет жизни, составляющие половину заболевших, вследствие высокой летальности (до 10-60%), частоты осложнений у 1/3 пациентов и тяжести резидуальных последствий. Этиология БГМ обусловлена возрастом ребенка: у новорожденных ведущими возбудителями являются листерии, эшерихии, стрептококк В, пневмококк, грибы, синегнойная палочка, клебсиелла, тогда как у детей в возрасте от 2 месяцев до 5 лет в 95% случаев БГМ вызываются менингококком, пневмококком, гемофильной палочкой, реже стафилококком и условно-патогенной флорой [8].
Анализ заболеваемости детей бактериальными гнойными менингитами свидетельствует об определенном изменении их этиологической структуры в последние годы [1, 4]. С 1990-92 гг. отмечается явный спад эпидемической заболеваемости менингококковой инфекцией: с 9,9 до 3,3 на 100 тысяч населения, а среди детей до 14 лет - с 21 до 8,1 и летальности - с 11-14% до 3-5%. На этом фоне растут БГМ неменингококковой этиологии, в основном Hib-менингиты. В клинической картине БГМ характерны остро или подостро возникающие симптомы: гипертермия до 39-40°, ухудшение общего состояния; общемозговые проявления, связанные с внутричерепной гипертензией - головная боль, повторные рвоты, вялость, двигательное беспокойство; менингеальные - выбухание родничка, пронзительный крик, ригидность затылочных мышц, симптомы Кернига, Брудзинского, Лессажа; поражение мозга - нарушение сознания, очаговая симптоматика.
У новорожденных развитие БГМ совпадает с генерализацией инфекции, выраженным токсикозом, судорогами, комой. У детей грудного возраста остро возникают беспокойство, немотивированный крик, тремор рук, подбородка, срыгивания, гиперестезия, запрокидывание головки, выбухание и напряжение большого родничка, тогда как типичные менингеальные знаки часто не определяются или появляются на 2-3-и сутки. Нередко в первые 48 часов развиваются клонико-тонические или локальные судороги. У детей более старшего возраста заболевание начинается с приступов головной боли и повторных рвот, психомоторного возбуждения, делириозного состояния, угнетения сознания, менингеальные симптомы резко выражены. На 2-4-й день, особенно при запоздалом лечении, выявляется очаговая неврологическая симптоматика: косоглазие, гемипарезы, тетрапарезы, судороги. При люмбальной пункции определяется мутный ликвор белого (при менингококковом менингите), желтовато-сероватого (при пневмококковом) или зеленоватого (при гемофильном) цвета. Ликворное давление повышено до 80-100 мм вод. ст., нейтрофильный плеоцитоз, как правило, более 1000х10 6 /л, повышение белка до 2-6 г/л, лактата и снижение глюкозы в ликворе.
Для БГМ наиболее типично острое течение заболевания с выздоровлением на 2-4-й неделе, что обусловливается быстрой диагностикой менингита, назначением адекватной антибиотикотерапии и патогенетических средств, направленных на детоксикацию и купирование внутричерепной гипертензии [2, 3]. Возможно молниеносное течение, которое приводит к летальному исходу через 12-48 часов вследствие отека мозга с развитием вклинения ствола мозга в большое затылочное отверстие. Причинами затяжного течения менингита являются поздняя диагностика и неадекватная терапия, снижение иммунитета, преморбидный статус (рахит, анемия, гипотрофия и др.). Рецидивирующее течение БГМ возникает в результате иммунного дефекта либо наличия первичных гнойных очагов инфекции.
Наибольшую актуальность в настоящее время представляют менингиты, вызванные гемофильной палочкой типа b (Hib-инфекция), в связи с ростом заболеваемости этой инфекцией как в странах Европы, особенно Скандинавии, так и на Американском континенте. Максимальное число заболевших Hib-менингитом (70%) приходится на возраст 3-18 месяцев и составляет 27 на 100 тысяч населения, тогда как у детей после 5 лет Hib-менингит встречается редко. Среди различных клинических форм Hib-инфекции у детей менингиты составляют 51%, летальность достигает 5-15%, неврологические осложнения развиваются в 25-35% случаев [2, 5, 9]. Значительное снижение заболеваемости Hib-инфекцией, в частности менингитом, происходит в результате проведения вакцинации, благодаря которой в США и странах Европы, например Финляндии, резко уменьшилась заболеваемость, что сделало Hib-инфекцию управляемой [4, 7]. Считается, что конъюгированная Hib-вакцина способствует сокращению частоты носительства и в сочетании с системным иммунитетом, выработанным у взрослых, может способствовать прекращению заболеваемости гемофильной инфекцией.
Микроорганизмы рода Haemophilus относятся к условно-патогенным, грамнегативным, вирулентность которых зависит от наличия липополисахаридной капсулы. Род Haemophilus насчитывает 16 видов, однако наибольшую значимость в патологии человека имеет Haemophilus influezae. Этот возбудитель имеет несколько специфических серотипов (а, b, с, d, е, f), из которых серотип b (Hib) является наиболее частым возбудителем генерализованных форм заболевания [3, 6]. К факторам вирулентности следует также отнести способность гемофильной палочки быстро приобретать устойчивость к антибиотикам in vivo.
Нами проведен клинический анализ 30 случаев БГМ гемофильной этиологии, подтвержденной бактериологически путем выделения штаммов Hib из крови и ликвора, у детей от 3 месяцев до 13 лет, поступивших в отделение нейроинфекций в 1997 году и за 5 месяцев 1998 года. Пациенты старше 2 лет составили две трети. Четкой сезонности не отмечается. Клиническая картина Hib-менингитов характеризуется различными вариантами течения.
Первый вариант. Сверхострое течение, обусловленное быстро (до 24 часов) развившимся Hib-менингитом, осложненным либо отеком головного мозга, либо синдромом Уотерхауза-Фридериксена. Заболевание начинается остро. Отмечается внезапный подъем в вечернее время температуры до 39-40°, в 80% случаев развивается судорожно-коматозный синдром, а в 20% - появляется геморрагическая сыпь с выраженным цианозом и гипостазами. Состояние при поступлении крайне тяжелое или терминальное, обусловленное отеком мозга с нарушением витальных функций или декомпенсированным шоком III степени. В цереброспинальной жидкости выявляется нейтрофильный нлеоцитоз (от 2 до 26 тыс. в мкл) и высокий уровень белка - от 1,5 до 6 г/л. В крови - лейкоцитоз до 16-29х10 9 /л с резким нейтрофильным сдвигом влево до юных палочкоядерных форм, составляющих до 40%, лимфопении (4-12%) и СОЭ, увеличенной до 50-60 мм/час.
Третий вариант. Hib-менингит с относительно благоприятным исходом. Чаще отмечалось острое развитие менингита. В половине случаев ему предшествует ОРВИ. Заболевание начинается остро с гипертермии, сопровождается головной болью, рвотой, выраженным беспокойством ребенка, перемежающимся с заторможенностью, оглушенностью, реже - развитием сопора и судорог. Характерно тяжелое состояние больных. Выражены симптомы интоксикации, общемозговые и менингеальные явления. В цереброспинальной жидкости отмечается высокий нейрофильный плеоцитоз и белок до 1-3 г/л, в анализах крови наиболее типичны выраженный лейкоцитоз со сдвигом формулы влево до юных и палочкоядерных форм, лим-фопения до 4%, в части случаев лейкопения и анемия. Санация цереброспинальной жидкости чаще наступает на 2-й, реже - на 3-4-й неделе болезни, что определяется выбором адекватной стартовой антибиотикотерапии и состоянием иммунных реакций макроорганизма.
Фактором, определяющим течение и исход Hib-менингита, является снижение или даже тотальная депрессия клеточного и гуморального иммунитета, особенно в условиях предшествующей вирусной инфекции. Известен синергизм между Hib и респираторными вирусами, что приводит к резкому повышению заболеваемости Hib-инфекцией в период нарастания респираторных инфекций, особенно гриппа [2, 4]. В наших наблюдениях развитие затяжного Hib-менингита отмечалось у ребенка с врожденным сифилисом и туберкулезным лимфаденитом. Преимущественное заболевание в раннем детском возрасте объясняется незрелостью иммунной системы ребенка и, в частности, неспособностью к выработке защитных антител в ответ на воздействие Hib. Доказано, что у детей младшего возраста после системной инфекции, вызванной палочкой Hib, и на фоне вакцинации иммунный ответ выражен слабо, тогда как у детей среднего возраста - умеренно, а у подростков и взрослых развивается выраженный иммунитет, не требующий повторной вакцинации. У части детей даже после системного заболевания антитела не вырабатываются, и они заболевают повторно клинически выраженной формой Hib-инфекции [5, 6, 8, 9]. Проблема лечения Hib-менингита и других форм данной инфекции связана с возросшей резистентностью микроба к антибиотикам, поскольку, чем скорее будет назначен эффективный химиопрепарат, тем больше шансов на полное выздоровление больных.
За последние 10 лет среди Hib, циркулирующих в Санкт-Петербурге, прослеживается тенденция увеличения числа полирезистентных штаммов с одновременным расширением спектров антибиотикорезистентности и включением в них новых антибиотиков. В конце 80-х и начале 90-х годов все штаммы Hib были чувствительны к левомицетину (100%), к гентамицину - 80% и в 50% случаев к ампициллину. В настоящее время резистентность Hib к ампициллину составляет 94%, к гентамицину - 82%, к цефалоспоринам, включая III поколение, - 88%, за исключением цефтриаксона (13,3%). Повысилась резистентность к левомицетину до 20%. Среди изученных 17 штаммов Hib только в одном случае (летальном) отмечена устойчивость к меронему (отсутствовала чувствительность и к другим антибиотикам). Резистентность к антибиотикам пенициллинового и цефалоспоринового ряда обусловлена р-лактамазной активностью палочки Hib, тогда как к левомицетину, тетрациклину, эритромицину предполагает и другие механизмы инактивации: способность вырабатывать хлорамфениколацетилтрансферазу, плазмидные механизмы устойчивости к антибиотикам.
Полирезистентность микроорганизма Hib и необходимость быстрого назначения адекватного антибиотика позволяет выдвинуть положение о стартовой терапии антибиотиком широкого спектра действия, воздействующего как на грамотрицательную, так и на грамположительную флору, не обладающего выраженными бактериолитическими свойствами (опасность углубления шока и отека головного мозга), но имеющего достаточный бактерицидный эффект.
Антибиотиком выбора в условиях тяжелой инфекции является меронем - представитель нового класса карбапенемов, который показал хорошую эффективность в ряде наших наблюдений при длительности терапии в течение 7-10 суток. Другой вариант монотерапии - назначение роцефина при длительности лечения им не менее 14 суток. Возможно применение и левомицетина, хотя возрастание резистентности Hib может привести к неэффективности лечения в первые дни болезни. При БГМ менингококковой этиологии стартовым антибиотиком остается пенициллин при отсутствии нарастающей геморрагической сыпи, тогда как при ее появлении - левомицетин, а при пневмококковом менингите - пенициллин.
Следует подчеркнуть, что начатое без промедления лечение антибиотиками - это лишь часть экстренных мероприятий, необходимых при БГМ. Развитие септицемии, инфекционно-токсического шока, ДВС-синдрома, которое наблюдается почти в каждом случае менингита, диктует необходимость непрерывного неврологического и лабораторного контроля, соответствующей коррекции терапии. Учитывая частоту развития синдрома неадекватной секреции антидиуретического гормона (гипоосмолярность и снижение электролитов крови при нарастании относительной плотности мочи), способствующего нарастанию отека мозга, необходимо ограничение первоначального объема вводимой жидкости. Купирование отека головного мозга достигается введением дексазона, осмо-диуретиков и онкодегидратантов. При развитии шока первые мероприятия также начинаются с обеспечения респираторной поддержки. В первые сутки требуется введение жидкости в количестве, достаточном для поддержания центральной гемодинамики, перфузии периферических тканей и мочеотделения, при необходимости - применение инотропных средств, гормонов (среди которых предпочтение отдается гидрокортизону) в адекватных фармакотерапевтических дозах.
Одним из проявлений шока и степени его тяжести является ДВС-синдром, в связи с чем необходима его ранняя профилактика и лечение в соответствии со стадиями процесса, направленное на нормализацию объема циркулирующей крови и ее реологических свойств: дезагреганты (трентал, кавинтон, аспирин, реополиглюкин), трансфузии свежезамороженной плазмы и даже свежезамороженной крови. Такие осложнения, как субдуральный выпот, контролируемый простой трансиллюминацией черепа, либо компьютерной томографией или УЗИ, с прогрессированием симптомов дислокации ствола мозга, требует срочной чрезродничковой пункции. Комплекс лечебных мероприятий, обеспечивающий адекватную этиотропную и патогенетическую терапию, особенно в первые дни болезни, предопределяет благоприятное течение менингита и выздоровление без неврологического дефицита.
Анализ 30 случаев Hib-менингита в Санкт-Петербурге в 1997-1998 гг. свидетельствует о возрастании роли Hib-инфекции, отсутствии сезонности и превалировании менингита у детей в возрасте старше 2 лет. Отмечено четкое увеличение резистентных штаммов Hib к антибиотикам пенициллинового и цефалоспоринового ряда, аминогликозидам и левомицетину, исключение составляет высокая чувствительность к роцефину и, особенно, к меронему, что следует учитывать при назначении стартовой терапии Hib-инфекции. Клиника заболевания отличается генерализованным характером инфекции, что проявляется не только менингитом, но и септицемией, наличием параменингеальных очагов инфекции, а в тяжелых случаях - развитием шока и отека мозга, осложненного дислокационным синдромом, особенно в случаях субдурального выпота, инфаркта мозга и синдрома неадекватной секреции антидиуретического гормона, что диктует необходимость дальнейшего совершенствования этиотропной и патогенетической терапии, с одной стороны, а с другой - постановки вопроса о вакцинации против Hib-инфекции.
Литература
1. Демина А.А., Покровский В.И., Самсонова И.М. Журн. Микробиол., 1996, N5, с. 99-104.
2. Внутренние болезни в 10 книгах. Книга 3. Пер. с англ. Под ред. Е. Браунвальда и др. - М., Медицина - 1993, с. 337-352.
3. Неотложная неврологическая помощь в детском возрасте. Под ред. Дж. Пеллока, Э.К. Майера. Пер. с англ. - М., Медицина - 1988, 576 с.
4. Покровский В.И. Сборник трудов научно-практической конференции "Актуальные вопросы эпидемиологии, клиники, диагностики и профилактики инфекций, вызываемой Н. influenzae тип В". Пастер Мерье Коннот, 1998, с. 4.
5. Покровская Н.Я., Покровский В.И. Гнойные менингиты и менингоэнцефалиты. Острые нейроинфекции у детей. Руководство для врачей. Под ред. Зинченко А.П. - Л., Медицина, 1986, С.23-57.
6. Руководство по инфекционным болезням. Под ред. Лобзина Ю.В., Казанцева А.П. - СПб, "Комета", 1996, С.350-354.
7. Суходоева Г.С., Добрица В.П. Гемофильная палочка - возбудитель инфекции и аллергии. Алма-Ата, "Наука" Казахской ССР, 1990.
8. Adams W.C. et al. JAMA. - V. 269, N2, p. 221-226.
9. Boody R., Makson E., Mak Farlane J. et al. Lancet, 1992, V.340, p.847.
10. Bradlte J.S. Hospital Practice Symp. Supplement, 1993, p. 15-19.
Сальмонелезный менингит - это вторичный гнойный менингит, развивающийся чаще как осложнение септической, реже - интестинальной формы сальмонеллеза. Характеризуется острым или постепенным началом, инфекционно-токсическим и/или менингеальным синдромом, тяжестью и длительностью течения.
Что провоцирует / Причины Сальмонеллезного менингита:
Возбудители менингита - сальмонеллы, которые пред¬ставляют собой мелкие (0,7–1,5 на 2–5 мкм) грам¬отрицательные бактерии, спор и капсул не образуют. Не обладают тропностью к каким-либо определенным органам и тканям. Устойчивы и долго (недели и месяцы) не только сохраняют жизнеспособность во внешней среде, продуктах питания, на овощах, в мясе, яйцах, но и способны размножаться в них с накоплением токсических продуктов, в том числе и эндотоксина. В настоящее время сальмонеллы устойчивы к большинству антибактериальных препаратов, но высокочувствительны к дезрастворам (осветленный 0,3% раствор хлорной извести убивает микроб через 1 час). Сальмонеллы имеют сложное антигенное строение, однако при серологической диагностике во внимание принимают только три основных антигена - О, Н и Vi. Этот принцип положен в основу классификации Кауфмана - Уайта, согласно которой в настоящее время насчитывается более 2324 сероваров и число их увеличивается с каждым годом. Сальмонеллезный менингит могут вызвать различные серотипы сальмонелл, но чаще других - S. typhimurium, S. enteritidis, S. heidelberg, S. newport.
Заболевания, вызываемые сальмонеллами, распространены повсеместно. Основным источником инфекции для детей раннего возраста является больные и бактерионосители, а также различные животные (коровы, собаки, кошки, свиньи), рыбы, птицы. Механизм заражения сальмонеллезом - фекально-оральный, а основными путями передачи инфекции является водный и пищевой, для детей имеет значение и контактно-бытовой путь. Инфицирование может происходить в стационарах через предметы быта и руки персонала.
Преимущественно сальмонеллезным менингитом болеют новорожденные и дети первых 6 месяцев жизни. Дети других возрастных групп болеют редко. Это обусловлено анатомо-физиологическими особенностями детского организма, и в первую очередь недостаточностью клеточного и гуморального иммунитета, повышенной проницаемостью клеточных и сосудистых мембран и несовершенством ГЭБ. Менингит чаще всего развивается как осложнение генерализованной или септической формы сальмонеллеза.
Патогенез (что происходит?) во время Сальмонеллезного менингита:
Симптомы Сальмонеллезного менингита:
У больных септической формой сальмонеллеза менингит развивается более постепенно. Септицемия протекает с выраженным токсикозом, нарушением функции сердечно-сосудистой системы - тахикардией, приглушением тонов сердца, снижением артериального давления, одышкой, снижением диуреза, гепатолиенальным синдромом, иногда с геморрагической сыпью. На высоте проявлений септицемии возникают септикопиемические очаги, в том числе и в мозговых оболочках, с развитием клинической картины менингита. Течение сальмонеллезного менингита тяжелое, длительное, с обострениями даже при проведении массивной антибиотикотерапии, часто заканчивается летально.
Диагностика Сальмонеллезного менингита:
Основные диагностические критерии сальмонеллезного менингита
1. Эпиданамнез: заболевание всегда возникает на фоне сальмонеллезной инфекции, преимущественно болеют новорожденные и дети первых 6 месяцев жизни.
2. Начало менингита острое или постепенное.
3. Протекает, как правило, с выраженным инфек¬ци¬он¬но-токсическим и менингеальным синдромами.
4. Течение тяжелое, длительное, часто с летальным исходом.
5. Бактериологическое выделение сальмонелл из цереброспинальной жидкости подтверждает диагноз.
Лабораторная диагностика
Общий анализ крови. В периферической крови выявляются лейкоцитоз, резкий сдвиг лейкоцитарной формулы влево, повышенная СОЭ.
Исследование ликвора. Цереброспинальная жидкость бывает прозрачной с относительно небольшим количеством клеток или гнойной с высоким нейтрофильным плеоцитозом и содержанием белка (до 3,0 г/л и более), со снижением концентрации глюкозы.
Бактериологическое исследование основано на посевах крови, мочи, кала, ликвора. Для этого используют среды обогащения (Мюллера, Кауфмана и др.) и дифференциально-диагностические среды (Плоскирева, Эндо, Левина, висмут-сульфитный агар). Исследовать кровь на наличие в ней сальмонелл необходимо в течение всего лихорадочного периода. Для этого кровь в количестве 5–8 мл засевают на 10–20% желчный бульон или среду Раппопорта.
Серологическое исследование проводится путем определения в сыворотке крови специфических антител. Наличие антител и их титр определяют с помощью реакций РА и РНГА с эритроцитарными диагностиками. Диагностическим считается титр 1:100 или нарастание титра антител в динамике заболевания с интервалом 7–10 дней в 4 и более раз. Возможно также применение реакции РПГА с цистеиновой пробой, позволяющей дифференцированно определять титры антител класса IgG. Диагностический титр цистеин-устойчивых антител в крови равен 1:80 (у детей первого года жизни - 1:20).
Лечение Сальмонеллезного менингита:
При подозрении на менингит необходима срочная госпитализация ребенка в специализированный стационар. При нарушениях сознания и дыхания транспортировку больного осуществляет реанимационная бригада. В стационаре проводят комплексное лечение, включающее охранительный режим, рациональное питание, этиотропную, патогенетическую и симптоматическую терапию. В остром периоде болезни необходимо соблюдение постельного режима. После проведения люмбальной пункции в течение 3 дней показан строгий постельный режим с укладкой на щите для профилактики постпункциональных осложнений.
Диета полноценная, высококалорийная, механически и химически щадящая. Детям первого года жизни проводят кормление сцеженным грудным молоком или адаптированными смесями с сохранением физиологического режима питания.
Выбор антибактериальных средств определяется этиологией менингита и проходимостью препарата через гемато-энцефалический барьер. Для стартовой антибактериальной терапии выбирают: левомицетина сукцинит в дозе 80 - 100 мг/кг/сутки внутримышечно или внутривенно с интервалом в 6 часов; бензилпенициллина натриевую соль в дозе 300 тыс. ЕД/кг/сутки внутримышечно или внутривенно с интервалом 4 ч. После бактериологического выделения, био- и серотипирования возбудителя проводят коррекцию антибактериальной терапии в соответствии с чувствительностью выделенного штамма. Препаратами резерва являются цефалоспорины III - IV поколений. Длительность антибактериальной терапии составляет не менее 10 - 14 дней. Показаниями к отмене антибиотиков являются: исчезновение симптомов интоксикации, стойкая нормализация температуры тела, восстановление формулы крови, санация ликвора (количество клеток не более 30 в 1 мкл, 70 % из них - лимфоциты).
С целью профилактики кандидоза при массивной и длительной антибактериальной терапии показано назначение нистатина, дифлюкана, амфитерицина Б (фунгизона).
Противовирусная терапия включает: препараты, нарушающие сборку нуклеиновых кислот вирусов; рекомбинантные интерфероны; индукторы эндогенного интерферона и иммуномодуляторы.
С иммуностимулирующей и заместительной целью применяют иммуноглобулины для внутривенного введения (эндобулин, сандоглобулин, пентаглобин) или специфические иммуноглобулины (против вируса клещевого энцефалита, противостафилококковый и др.).
Патогенетическая терапия направлена на борьбу с интоксикацией, на нормализацию внутричерепного давления и церебральной гемодинамики. При проведении дезинтоксикации необходимо обеспечить введение жидкости с учетом физиологической потребности и электролитного баланса. Введение жидкости осуществляется путем оральной регидратации (чай, 5 % раствор глюкозы, морс) или внутривенной инфузии. Для парентерального введения используют глюкозо-солевые (10 % глюкоза, 0,9 % NaCl, Рингера) и коллоидные (реополиглюкин, реомакродекс, гемодез) растворы в соотношении 3:1.
Одновременно назначают дегидратационную терапию (объем определяется степенью внутричерепного давления). В качестве стартового препарата в 1 - 2 сутки заболевания используют лазикс в дозе 1 - 2 мг/кг/сутки. Мочегонный эффект препарата начинается через 3 - 5 мин, достигает максимума через 30 мин и длится 1,5 - 3 часа.
Для улучшения кровоснабжения мозга и профилактики ишемии мозговой ткани используют сосудистые средства - трентал, кавинтон. Уменьшение энергодефицита нейронов и восстановление межнейрональных связей достигается применением препаратов ноотропного ряда (пирацетама, пантогама, перидитола) и вазоактивных нейрометаболитов (актовегина, инстенона). Длительность курса - до 6 мес. В тяжелых случаях ослабленным детям вводят лейковзвесь, свежезамороженную плазму; проводят сеансы УФО крови.
Основой комплексной интенсивной терапии отека-набухания головного мозга является адекватная респираторная поддержка (увлажненный кислород, эндотрахеальная интубация, ИВЛ), направленная на коррекцию кислотно-основного состояния и снижение выхода плазмы в периваскулярное пространство.
Широкое распространение получили осмодиуретики, действие которых основано на создании осмотического градиента между плазмой и мозговой тканью. С этой целью используют 15 % раствор манитола внутривенно (из расчета 0,5 - 1,0 г сухого вещества на 1 кг массы тела). Мочегонный эффект начинается через несколько минут и достигает максимума через 2 - 3 часа. Вследствие повреждения гематоэнцефалического барьера может возникнуть синдром "отдачи" - перемещение осмотически активного вещества из сосудистого русла в ткань мозга и усиление отёка. Для предупреждения данного состояния через 2 часа после начала введения манитола вводят лазикс.
К каким докторам следует обращаться если у Вас Сальмонеллезный менингит:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Сальмонеллезного менингита, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Что такое сальмонеллез? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, инфекциониста со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Сальмонеллёз — это острое инфекционное заболевание желудочно-кишечного тракта с возможностью дальнейшей генерализации процесса (распространением заболевания по всему организму). Причина развития сальмонеллёза — различные серотипы бактерий рода Salmonella. К клиническим характеристикам сальмонеллёза относят синдром общей инфекционной интоксикации, синдром поражения желудочно-кишечного тракта (гастрит, энтерит), синдром обезвоживания, гепатолиенальный синдром (увелечение печени и/или селезёнки) и иногда синдром экзантемы (высыпания).
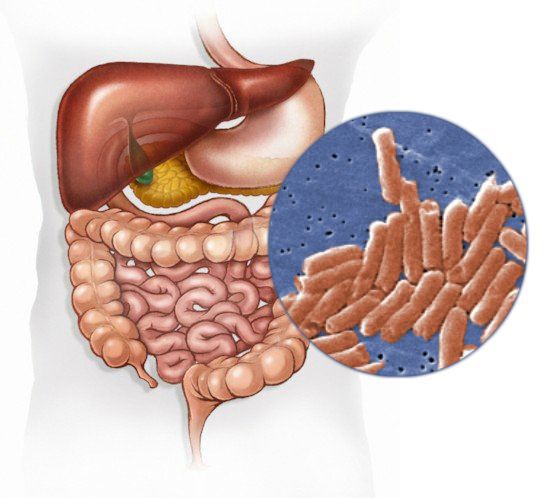
Возбудитель
семейство — кишечные бактерии (Enterobacteriaceae)
род — Сальмонелла (Salmonella)
Существует 7 подвидов (более 2500 сероваров). Наиболее актуальные серовары: typhimurium, enteritidis, panama, london.
Представлены следующей антигенной структурой:
- О-антиген (соматический, термостабильный);
- H-антиген (жгутиковый, термолабильный);
- К-антиген (поверхностный, капсульный);
- Vi-антиген (антиген вирулентности — степень способности штамма вызвать заболевание; является компонентом О антигена);
- М-антиген (слизистый).
К факторам патогенности (механизмам приспособления бактерий) относятся:
- холероподобный энтротоксин — интенсивная секреция жидкости в просвет кишки;
- эндотоксин (липополисахарид) — общее проявление интоксикации;
- инвазия — заражение.
Тинкториальные свойства: разлагают глюкозу и маннит, образовывая кислоту и газ, продуцируют сероводород. Грамм-отрицательные палочки подвижны, спор и капсул не образуют. Растут на обычных питательных средах, образуя прозрачные колонии, на мясо-пептонном агаре с образованием колоний голубоватого цвета, на среде Эндо образуют прозрачные розовые колонии, на среде Плоскирева — бесцветные мутные, на висмут-сульфитном агаре — чёрные с металлическим блеском.
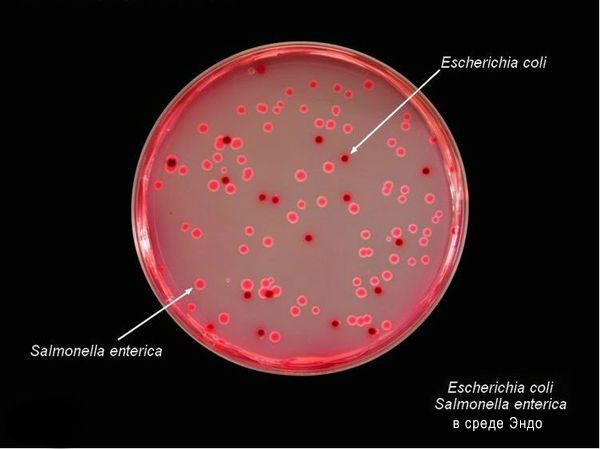
Высокоустойчивы во внешней среде (без агрессивных воздействий), активно размножаются в мясе и молоке (до 20 суток), в воде сохраняют жизнесособность до 5 мес., в почве — до 9 мес., в комнатной пыли — до 6 мес., в колбасе — до 1 мес., в яйцах — до 3 мес., в фекалиях сохраняются до 4 лет. При 56 °C погибают через 3 минуты, при кипячении мгновенно. Сальмонеллы, которые находятся в куске мяса массой 400 гр и толщиной до 9 см, погибают при его варке за 3,5 часа. Соление и копчение оставляет сальмонелл в живых. Воздействие кислот и хлорсодержащих дезинфицирующих средств вызывает их гибель. В последнее десятилетие появились штаммы сальмонелл, устойчивые ко многим антимикробным препаратам. [2] [5]
Эпидемиология
Зооантропоноз, распространённый повсеместно.
Источники инфекции: домашние животные (сами не болеют), птицы, человек (больной и носитель).
Резервуары инфекции и причина эпидемических вспышек сальмонеллеза: грызуны, дикие птицы, тараканы, улитки, лягушки, змеи.
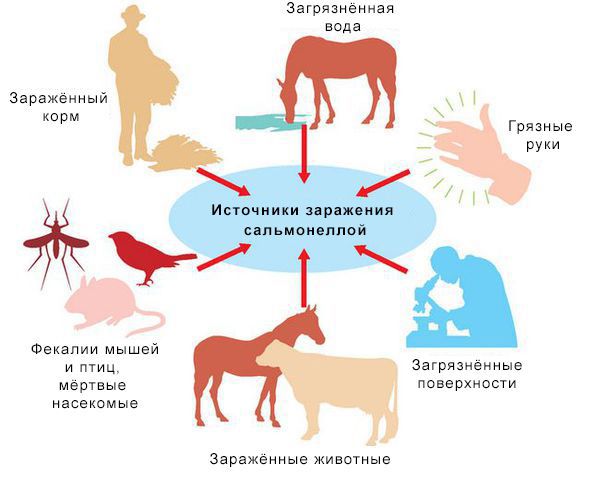
Механизм передачи: фекально-оральный (пути — алиментарный, т. е. через органы ЖКТ, водный, контактно-бытовой). В основном источниками заражения являются птицы, яйца и молочные продукты. Инфицирующая доза 10*5-10*8 микробных тел.
Факторы риска
- детский возраст до 5 лет;
- возраст до 12 месяцев, особенно высока вероятность заболеть без грудного вскармливания;
- иммунодефицит (в основном у младенцев и лиц старше 65 лет, а так же у пациентов с ВИЧ в стадии СПИДа, принимающих иммунодепрессивные препараты);
- регулярный приём препаратов, снижающих кислотность желудка;
- употребление сырого и недостаточно термически обработанного мяса, молочных продуктов и яиц;
- частый контакт с животными с несоблюдением правил гигиены;
- посещение стран с низким уровнем жизни.
В России в 2016 г. заболеваемость была – 26 на 100 тыс. населения, у детей в до 14 лет – 71 на 100 тыс. Для сравнения в США среднегодовая заболеваемость — 15 на 100 тыс. (1,35 миллиона заболеваний, 26 500 госпитализаций и 420 смертей ежегодно). Иммунитет строго типоспецифичен (возможно многократное инфицирование различными штаммами) и непродолжителен [2] [6] [9] [10] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы сальмонеллеза
Инкубационный период — от 6 часов (при алиментарном заражении) до 3 суток. При внутрибрюшном заражении (искусственно) — до 8 дней.
Начало заболевания острое (т. е. развитие основных синдромов происходит в первые сутки заболевания).
Локализованная сальмонеллезная инфекция представляет собой септические осложнения сальмонеллеза различной локализации, которые возможны при выраженном иммунодефиците.
Период протекания
Инкубационный период при сальмонеллезе в среднем составляет 12-24 часа. Иногда он укорачивается до 6 часов или удлиняется до 2 дней.
Классификация
Этиология и патогенез
Возбудители сальмонеллеза относятся к роду Salmonella, семейству кишечных бактерий Enterobacteriaceae.
При разрушении бактерий выделяется эндотоксин, обусловливающий развитие интоксикационного синдрома.
Эпидемиология
Источником инфекции могут являться животные и люди, при этом роль животных в эпидемиологии является основной.
У животных сальмонеллез встречается в форме клинически выраженного заболевания и бактериовыделительства. Эпидемиологическую опасность представляет инфицирование крупного рогатого скота, свиней, овец, лошадей, собак, кошек, домовых грызунов. Значительное место в эпидемиологии сальмонеллеза занимают птицы. Сальмонеллы обнаруживают в яйцах, мясе и внутренних органах птиц.
Механизм передачи возбудителей – фекально-оральный. Основной путь передачи инфекции – пищевой.
Сальмонеллез встречается в течение всего года, но чаще - в летние месяцы, что можно объяснить ухудшением условий хранения пищевых продуктов. Наблюдается как спорадическая, так и групповая заболеваемость этой инфекцией.
Факторы и группы риска
Клиническая картина
Cимптомы, течение
Септическое течение сальмонеллеза (см. Сальмонеллезная септицемия - А02.1) ведет к образованию вторичных гнойных очагов.
Клиническая картина зависит от локализации метастатических гнойных очагов, которые могут формироваться во всех органах. Во всех случаях наблюдается увеличение печени и селезенки.
Для заболевания характерно длительное тяжелое течение. В результате значительных трудностей, возникающих при лечении, возможен неблагоприятный исход.
Диагностика
Лабораторная диагностика
Ввиду полиморфизма клинических проявлений сальмонеллеза, лабораторное обследование больных является важным моментом в диагностике заболевания.
1. Реакция агглютинации (РА) - считается положительной при разведении сыворотки не менее чем 1:200. Особенно важное диагностическое значение имеет нарастание титра антител в динамике заболевания.
2. Реакция непрямой гемагглютинации (РНГА) - применяется более часто. РНГА более чувствительна, по сравнению с РА, и дает положительные результаты с 5-го дня болезни. За диагностический принимают титр антител в РНГА 1:200.
3. Методы обнаружения антигенов сальмонелл в крови: агрегат-гемагглютинации и иммуноферментный.
Дифференциальный диагноз
Осложнения
Лечение
1. Дезинтоксикация.
2. Нормализация водно-электролитного обмена.
3. Борьба с гипоксемией , гипоксией , метаболическим ацидозом .
4. Поддержание на физиологическом уровне гемодинамики, а также функций сердечно-сосудистой системы и почек.
Этиотропное лечение
Применяют сочетания антибиотиков группы аминогликозидов (гентамицина сульфат, сизомицина сульфат, амикацина сульфат, тобрамицин и др.) и хинолонов (ципрофлоксацин, офлоксацин и др.), цефалоспорины, левомицетин, ампициллин, амоксициллин.
Прогноз
Госпитализация
Переболевших выписывают после клинического выздоровления и отрицательных контрольных бактериологических исследований испражнений.
Профилактика
Ветеринарно-санитарные мероприятия:
- предупреждение распространения сальмонеллеза среди домашних млекопитающих и птиц;
- организация санитарного режима на мясокомбинатах и молочных предприятиях.
Цель санитарно-гигиенических мероприятий – предупреждение обсеменения сальмонеллами пищевых продуктов при их обработке, транспортировке и продаже.
В профилактике сальмонеллеза большое значение имеет правильная кулинарная и оптимальная термическая обработка пищевых продуктов.
Противоэпидемические мероприятия направлены на предупреждение распространения заболевания в коллективе. При возникновении спорадических заболеваний и эпидемических вспышек необходимо выявление путей передачи инфекции.
Среди инфекционных заболеваний детского возраста наиболее распространенными после острых респираторных вирусных заболеваний являются острые кишечные инфекции (ОКИ) (см. таблицу). Спектр возбудителей, вызывающих ОКИ, с каждым годом увеличивается за счет новых бактерий и вирусов, но группа болезнетворных микроорганизмов, объединенных названием Сальмонеллы (по имени впервые их описавшего американского исследователя Д.Е. Сальмона), в последние 20 лет продолжает сохранять одно из ведущих мест - как во всем мире, так и в нашей стране. Сальмонеллы вызывают желудочно-кишечные заболевания у животных, птиц, рыб. Люди, в том числе и дети самого раннего возраста, включая новорожденных, тоже подвержены заболеванию сальмонеллезом. Сальмонеллы нередко являются причиной эпидемических вспышек (в семьях, закрытых коллективах), а при несвоевременном и неправильном лечении - и смертельного исхода.
Таблица. Заболеваемость сальмонеллезом в Российской Федерации в 1994-1997 гг. (по данным Минздрава РФ)
| Возрастная группа | 1994 г. | 1995 г. | 1996 г. | 1997 г. | ||||
| Абсолютное число | Показатель на 100 тыс. чел. | Абсолютное число | Показатель на 100 тыс. чел. | Абсолютное число | Показатель на 100 тыс. чел. | Абсолютное число | Показатель на 100 тыс. чел. | |
| Дети до 14 лет | 39279 | 109,553 | 34713 | 96,818 | 27162 | 85,532 | 25162 | 79,234 |
| Взрослые | 102798 | 69,921 | 86058 | 58,020 | 65420 | 44,212 | 60184 | 40,674 |
Сальмонеллы - мелкие подвижные бактерии, которые могут длительно сохранять жизнеспособность во внешней среде. Так, в воде открытых водоемов они могут жить до 120 дней, в морской воде - до 217 дней, в почве - до 9 мес, в комнатной пыли - до 517 дней, в колбасных изделиях - до 130 дней, в яйцах и замороженном мясе - до 13 мес. При комнатной температуре микробы хорошо размножаются в пищевых продуктах, особенно мясных и молочных, при этом внешний вид и вкус пищи не меняется. Они не погибают и при консервации - при концентрации поваренной соли 2-18%. Губительной для сальмонелл является высокая температура - кипячение их убивает мгновенно. А обычные дезинфицирующие средства, содержащие хлор, не всегда эффективны.
Источником заражения сальмонеллезом могут быть животные, чаще всего домашние (крупный рогатый скот, свиньи, кошки, собаки), птицы, люди, больные сальмонеллезом или здоровые бактерионосители.
Пути заражения сальмонеллезом многообразны. Наиболее частый у взрослых и детей старшего возраста - пищевой - при употреблении самых разных пищевых продуктов, но чаще всего - мяса животных и птиц, а также яиц. Микробы попадают в продукты при недостаточной кулинарной обработке (полусырые бифштексы, яйца сырые и всмятку, яичница-глазунья), неправильном хранении и нарушении элементарных правил личной гигиены.
Нам приходилось наблюдать эпидемические вспышки сальмонеллеза. В одном случае - из-за пирожных с кремом из взбитых яиц; в другом - из-за сцеженного грудного молока, хранившегося летом вне холодильника. Заразиться сальмонеллезом можно и через загрязненную воду - при ее питье или купании. Такая "водная" вспышка описана в Калифорнии (США), когда заболело 16 тыс. человек.
У детей грудного возраста основным путем заражения сальмонеллезом является контактно-бытовой - через соски, игрушки, предметы ухода, грязные руки ухаживающих за ними взрослых.
С середины 80-х годов значительно возросла роль и другого вида сальмонелл - S. enteritidis, заражаются которым преимущественно дети старшего возраста через пищевые продукты (куры, яйца).
Инкубационный период болезни при сальмонеллезе может продолжаться от нескольких часов (при пищевом заражении) до нескольких суток (при контактно-бытовом пути заражения), в среднем 3-4 дня. Чем большее количество микробов и их токсинов попало в организм, тем короче инкубационный период и тяжелее протекает заболевание.
Клиническое течение сальмонеллеза. Тяжесть заболевания зависит от возраста ребенка и состояния его защитных сил, вида сальмонелл, пути заражения, количества микробов и их токсинов, попавших в организм. Наиболее часто встречается поражение желудочно-кишечного тракта, куда микроб попадает, преодолев первый естественный защитный барьер - соляную кислоту желудочного сока.
У детей грудного возраста заболевание обычно начинается постепенно: появляются вялость, снижение аппетита, повышенная температура, рвота, жидкий стул - вначале обычного цвета и умеренно учащенный (5-6 раз в сутки). В последующие дни состояние ухудшается, температура повышается до 38° и выше, испражнения становятся более частыми (10 раз в сутки и чаще), водянистыми, приобретают зеленый цвет. К 5-7-у дню болезни в них появляется слизь, иногда - прожилки крови. При отсутствии лечения в связи с потерей организмом воды и солей натрия и калия при рвоте и диарее может развиться обезвоживание, которое проявляется сухостью слизистой оболочки рта и языка, западением родничка, появлением жажды, уменьшением выделения мочи. При дальнейшем нарастании обезвоживания нарушения водно-минерального обмена могут стать необратимыми.
У новорожденных детей преобладают общие симптомы над симптомами со стороны желудочно-кишечного тракта. Температура нередко остается нормальной. Дети отказываются от еды, перестают прибавлять в весе, становятся беспокойными, срыгивают; кожа бледная; конечности холодные; живот вздут.
У детей с ослабленным иммунитетом (недоношенных, на искусственном вскармливании, имеющих врожденную патологию, часто болеющих) сальмонеллез может протекать в виде генерализованной инфекции (по типу сепсиса), с поражением других внутренних органов (печень, почки, легкие, мозговые оболочки). Заболевание протекает очень тяжело, с высокой температурой в течение длительного времени, сопровождается увеличением печени и селезенки.
У детей более старшего возраста (дошкольного и школьного) заболевание обычно начинается внезапно - поднимается температура выше 38°, появляются головная боль, головокружение, повторная обильная рвота, слабость, снижение аппетита. К этим симптомам быстро присоединяются понос и боли в животе. Испражнения становятся жидкими, водянистыми, темно-зеленого цвета (похожими на болотную тину). При своевременно начатом лечении заболевание может ограничиться симптомами поражения желудка и тонкой кишки (гастроэнтерит), а при отсутствии лечения инфекционный процесс распространяется и на толстую кишку (колит) - в испражнениях появляются слизь и кровь, боли в животе усиливаются и становятся схваткообразными (заболевание напоминает дизентерию). Кроме обезвоживания, при тяжелом течении болезни опасными осложнениями являются острая почечная недостаточность и инфекционно-токсический шок.
Заболевание у детей старшего возраста обычно заканчивается в течение 1-3 недель, а у детей раннего возраста, особенно новорожденных и ослабленных, может продолжаться в течение нескольких недель и даже месяцев; при этом возможны обострения и рецидивы, а также длительное выделение сальмонелл с испражнениями и даже мочой. После перенесенного сальмонеллеза в течение долгого времени (не менее 3 мес.) сохраняются функциональные нарушения пищеварения, такие как недостаточность выработки ферментов поджелудочной железы (из-за ее реактивного поражения), ферментов, переваривающих молочный сахар; явления дисбактериоза (особенно при неумеренном лечении антибиотиками), а у детей с неблагоприятным аллергическим фоном - усиление проявлений пищевой аллергии (особенно на белки молока). Все эти явления могут протекать незаметно, а могут сопровождаться "неустойчивым" стулом (чередование запоров и поносов), вздутием и болями в животе, срыгиваниями, усиливающимися при употреблении молочной пищи. В ряде случаев может развиться хроническая патология желудочно-кишечного тракта (хронический колит, хронический панкреатит), которая сохраняется впоследствии и у взрослых.
Лечение больных сальмонеллезом лучше всего проводить в условиях специализированного инфекционного стационара, особенно это касается детей грудного возраста и больных со средне-тяжелой и тяжелой формами болезни.
Врач должен информировать родителей об основных принципах лечения детей при кишечных инфекциях вообще и сальмонеллезе в частности. При подозрении на пищевой путь заражения (многократная рвота, одновременное заболевание других членов семьи при употреблении одного и тою же пищевого продукта) надо начать промывание желудка (обильное питье - 2%-ный раствор соды) с последующим вызыванием рвоты.
Необходимо отпаивать ребенка с целью профилактики и лечения обезвоживания. Для этого используется порошок Регидрон, который содержит глюкозу, соли натрия и калия. Выпаивание проводится только дробно - по 1 чайной, десертной или столовой ложке каждые 5 мин. Детям до 3 лет Регидрон чередуют с кипяченой водой или несладким чаем. При отсутствии Регидрона можно приготовить раствор самостоятельно (на 1 л воды - 1 столовая ложка сахара и 1 чайная ложка соли). Метод отпаивапия ("оральная регидратация") является основным методом лечения обезвоживания, и в стационаре он позволяет избежать необходимости внутривенного введения жидкости. Не следует ограничиваться "оральной регидратацией", если у ребенка отмечается неукротимая рвота, очень частый водянистый стул и резкое снижение количества выделяемой мочи. Таким детям сразу необходимо начинать капельную инфузию жидкости.
Энтеросорбция - это новое и очень перспективное направление в лечении ОКИ, и в частности сальмонеллеза, особенно эффективное в первые часы болезни. Сорбенты - это природные или синтетические вещества, состоящие из мельчайших частиц, которые способны абсорбировать и выводить из кишечника микробы, вирусы, токсины и другие продукты их жизнедеятельности, а также аллергены и нерасщепленные углеводы; они обладают способностью усиливать защитные свойства слизистого слоя кишечника.
Самолечение сальмонеллеза антибиотиками в домашних условиях недопустимо. В настоящее время во всем мире сократили применение антибиотиков при сальмонеллезах, поскольку сальмонеллы (особенно S. typhimurium) приобрели множественную устойчивость к большинству антибиотиков и, кроме того, такие широко применяемые препараты, как левомицетин, тетрациклин, ампициллин вызывают множество побочных реакций (токсическое действие на организм, аллергия, дисбактериоз). Антибиотики безусловно показаны лишь при тяжелых и генерализованных формах болезни у детей раннего возраста из групп риска (с ослабленным иммунитетом). Их назначение в стационаре проводится с учетом данных чувствительности к ним сальмонелл и тяжести болезни. Однако у таких детей даже правильно подобранные антибиотики не всегда эффективны, поэтому их целесообразно сочетать с иммунопрепаратами (лизоцим, комплексный иммуноглобулиновый препарат). При нетяжслом сальмонеллезе у детей старшего возраста можно обойтись только применением сорбентов и специфических сальмонеллезных бактериофагов.
При сальмонеллезе и других ОКИ не следует назначать детям Имодиум и его аналоги, так как они замедляют моторику кишечника, что способствует всасыванию токсинов в кровь и может привести к кишечной непроходимости. Областью применения Имодиума остаются неинфекционные функциональные заболевания, когда необходимо снизить повышенную моторику кишечника.
Большое значение при лечении сальмонеллеза у детей имеет диета. Голодная диета ("водно-чайная" пауза) в настоящее время не рекомендуется, но целесообразно ограничение количества пищи в первые 3-5 дней болезни на 5-15% (в зависимости от тяжести процесса). Оптимальным для детей первого года жизни остается грудное молоко (непастеризованное), которое является не только наиболее полноценным питанием, незаменимым по составу белков, жиров, углеводов, витаминов и микроэлементов, но и содержит целый ряд биологически активных защитных веществ. Детям, находящимся на искусственном вскармливании, назначают привычные для них смеси (предпочтительно кисломолочные - кефир, ацидофильная смесь "Малютка", бифилин, бифидок и др.) в сочетании (после 4 мес.) с 5-10%-ной рисовой и гречневой кашей на воде или половинном молоке и овощным пюре с последующим расширением объема и ассортимента питания. Детям старше года в первые дни болезни необходима легко усвояемая протертая пища (отварной рис, супы, пюре из овощей) с ограничением жира и добавлением парового мяса и рыбы (с третьего-четвертого дня). На 2-3 недели из рациона исключаются продукты, усиливающие брожение и перистальтику кишечника (цельное молоко, ржаной хлеб, сырые овощи, кислые фрукты и ягоды), а также пряности и соления.
Детям с ферментопатией, пищевой аллергией, дисбактериозом назначают соответствующую диету (низколактозные и безмолочные смеси - детям раннего возраста, "панкреатический" стол - старшим), ферменты, биопрепараты, отвары (лапчатки, зверобоя, ромашки, коры дуба), витамины, при необходимости дома продолжают иммуно-и фаготерапию.
Профилактика сальмонеллеза осуществляется как на государственном уровне (санитарно-эпидемиологической и ветеринарной службами), так и на индивидуальном. Необходимо строго соблюдать правильную технологию и хранение продуктов, избегать употребления в пищу парного молока, сырых яиц, правильно обрабатывать игрушки и предметы ухода за детьми, особенно соски. И, конечно, не надо забывать, что мытье рук - наиболее простой и самый действенный способ профилактики ОКИ.
Профилактике сальмонеллеза способствуют и все мероприятия, направленные на повышение защитных сил организма ребенка, и прежде всего - здоровый образ жизни. Если один из членов семьи заболел сальмонеллезом, после изоляции больного необходимо провести дезинфекцию и обследовать членов семьи (бактериологическое обследование - анализ кала), а также назначить им с профилактической целью сальмонеллезный бактериофаг (по 1-2 таблетки 3-4 раза в день, в зависимости от возраста, в течение 5-6 дней).
Читайте также:

