Сепсис на половом члене
Обновлено: 24.04.2024
Сепсис — это самая тяжелая, генерализованная форма инфекционного процесса, которая развивается либо при высокой патогенности возбудителя, либо при недостаточном ответе защитных систем организма. Международным консенсусом рекомендовано использовать следующее определение: сепсис — это опасная для жизни дисфункция внутренних органов, вызванная нарушением регуляции ответа организма на инфекцию. При сепсисе наблюдается общий интоксикационный синдром, тромбогеморрагический синдром (кровоизлияния) и поражение внутренних органов.
Причины возникновения сепсиса
Сепсис может быть вызван большинством известных в эпидемиологии микроорганизмов, среди которых бактерии, вирусы (в том числе сезонные вирусы гриппа), грибы, паразиты. Обычно возбудитель инфекции попадает в организм из внешней среды. При определенных условиях, например, при иммунодефицитах, заболевание может развиться от естественной, условно-патогенной флоры организма, которая в норме присутствует у каждого человека. [1]
Само по себе наличие инфекции еще не является гарантией развития сепсиса. Необходимы дополнительные условия, которые приведут к генерализации процесса и патологическому ответу организма. Вероятность таких событий увеличивается в следующих случаях:
- Возраст больного старше 75 лет.
- Выполнение операций или инвазивных процедур.
- Наличие травм и ожогов.
- Нарушения иммунной системы — СПИД, онкологические заболевания, проведение химиотерапии, необходимость применения иммуносупрессивной терапии (например, после трансплантации органов), необходимость приема высоких доз глюкокортикостероидов.
- Долгое лечение в условиях стационара.
- Наличие катетеров, канюль, зондов и других инвазивных устройств.
- Беременность и роды.
- Наличие химической зависимости — алкоголизм, наркомания.
- Наличие хронических заболеваний — хроническая почечная недостаточность, дыхательная недостаточность, сахарный диабет и многое другое.
Виды сепсиса
В зависимости от расположения первичного очага инфекции, выделяют первичный (криптогенный) и вторичный сепсис. При первичном, очаг инфекции установить не удается. При вторичном сепсисе таковой очаг имеется. В зависимости от его локализации, выделяют:
- Чрескожный сепсис. Первичный очаг находится на коже, это могут быть раны, ожоги, гнойные заболевания кожи (гнойные абсцессы, фурункулы и др).
- Одонтогенный сепсис. Причиной его развития может стать кариес, пульпит, периодонтит, челюстной остеомиелит и другие заболевания зубочелюстной системы.
- Отогенный сепсис. Первичным очагом является воспалительный процесс в ухе. Как правило, это гнойные отиты среднего уха.
- Гинекологический сепсис — первичный очаг располагается в половых органах женщины.
- Хирургический сепсис — развивается в результате инфицирования хирургической раны или при инфицировании во время проведения инвазивных процедур. 4
Первые признаки и симптомы сепсиса
Определить первые признаки сепсиса бывает непросто, даже для специалистов. Это связано с тем, что, во-первых, этот синдром развивается уже на фоне существующей патологии, которая может иметь самую разнообразную симптоматику, а во-вторых, при наличии иммунодефицита, клиническая картина может быть стертой. Тем не менее, есть некоторые симптомы, которые позволяют заподозрить начало сепсиса:
- Повышение или понижение температуры тела — выше 38 и ниже 36 градусов.
- Снижение давления ниже рабочего значения.
- Увеличение частоты пульса.
- Увеличение частоты дыхательных движений (одышка).
- Снижение количества выделенной мочи.
- Общая слабость, изможденность.
- Нарушение сознания или поведения.
Особое внимание возникновению этих признаков уделяют у хронических больных, при наличии лейкопении, онкологических заболеваний и у пациентов, перенесших травмы или хирургические вмешательства. При возникновении хотя бы 2-3 таких симптомов, следует немедленно связаться с врачом.
Диагностика сепсиса
Своевременная диагностика сепсиса имеет решающее значение для выздоровления больного. Чем раньше начато лечение, тем больше шансов на успех. Диагноз выставляется на основании данных клинического осмотра и лабораторно-инструментального обследования.

Клинические критерии:
- Температура тела более 38 градусов или менее 36 градусов.
- Частота сердечных сокращений более 90 или превышает возрастную норму.
- Частота дыхания более 20 раз в минуту.
- Наличие отеков.
- Спутанность сознания.
- Повышение уровня глюкозы в крови более 7,7 мкмоль/л при отсутствии диабета.
- Нарушение гемодинамических процессов — снижение систолического артериального давления менее 90 мм.рт.ст, либо его снижение более чем на 40 мм.рт.ст. от привычного значения. [5,6]
Лабораторные критерии
Проводят общий анализ крови с подсчетом лейкоцитарной формулы и определением количества тромбоцитов. При сепсисе определяется лейкоцитоз более 12*109/л или лейкопения, когда количество лейкоцитов ниже 4*109/л. Также отмечается выход в кровяное русло незрелых форм гранулоцитов и уменьшение количества тромбоцитов.
В биохимическом анализе крови отмечается увеличение С-реактивного белка, креатинина, билирубина. Но это неспецифичные признаки, которые могут наблюдаться и при других заболеваниях. Поэтому продолжается поиск более информативных методов диагностики.
На сегодняшний день главными таким маркерами являются прокальцитонин, пресепсин, СРБ. По данным этого лабораторного показателя устанавливают диагноз и отслеживают динамику заболевания.
Бактериологический посев
Обнаружение в крови микроорганизмов является важным, но не обязательным проявлением сепсиса. Даже при использовании самых современных диагностических систем и при тщательном соблюдении техники забора материала, выделить возбудитель из крови удается менее, чем в половине случаев. Поэтому отрицательный результат бакпосева при наличии клинической симптоматики не должен расцениваться как отсутствие сепсиса, и, наоборот, выделение микроорганизмов из крови при отсутствии симптоматики, должно расцениваться как транзиторная бактериемия или вирусемия, но не как сепсис.
Тем не менее, биологические исследования в любом случае должны присутствовать, как один из этапов диагностики сепсиса по следующим причинам:
- Возможность определения этиологии возбудителя.
- Подбор или смена режимов антибиотикотерапии.
- Контроль эффективности лечения.
- В некоторых случаях позволяет определить источник инфекции, например, катетер-связанная инфекция, эндокардиты и др.
Стадии развития сепсиса
Развитие и течение септического процесса индивидуально и зависит как от свойств возбудителя, так и от особенностей организма больного. Тем не менее, можно выделить несколько фаз течения данного заболевания:
Что касается продолжительности заболевания, то здесь все опять же индивидуально. У одних, более сильных пациентов, сепсис купируется в течение 3-4 недель, у других он может протекать годами, периодически стихая и вспыхивая.
Кроме того, при диагностике сепсиса выделяют следующие состояния.
Токсико-резорбтивная лихорадка
Токсико-резорбтивная лихорадка — состояние, которое развивается при всасывании бактериальных токсинов или продуктов тканевого распада из первичного патологического очага. Как правило, это характерно для бактериальных инфекций ран, катетеров и др. Характерны общие типовые синдромы, которые сопровождают инфекционные процессы — лихорадка, изменения в общем анализе крови и мочи (лейкоцитоз, протеинурия). При ликвидации первичного очага, состояние пациента стабилизируется.
Септицемия
Септицемия — форма сепсиса, при которой наблюдается выраженный интоксикационный синдром, гиперэргия (повышенная реакционность организма) и быстрое течение. Септические очаги либо выражены минимально, либо отсутствуют. Такая форма сепсиса больше характерна для детей первых лет жизни. Для клинической картины больше характерны общие проявления:
- Гемолитическая желтуха, сопровождающаяся пожелтением кожных покровов и склер.
- Сыпь. Сначала она проявляется в виде мелких розовых точек, которые разрастаются и сливаются между собой, образуя бледно-розовые или пурпурные пятна.
- У некоторых пациентов элементы сыпи могут покрываться пузырями или язвами. При глубоких поражениях может затрагиваться подкожная жировая клетчатка с развитием флегмонозного воспаления.
- Геморрагический синдром — кровоизлияния во внутренние органы.
Септикопиемия
Септикопиемия — это форма сепсиса, при которой в организме, помимо общей интоксикации, начинают возникать метастатические абсцессы в органах и тканях, которые являются результатом бактериальной эмболии. Чаще всего первые абсцессы обнаруживаются в легких, а затем процесс распространяется на другие органы: печень, печень, сердце, менингиальные оболочки, синовиальные оболочки. Абсцессы могут прорваться и вызвать развитие эмпиемы плевры, флегмоны, перитонита и др.
Клиническая классификация сепсиса по стадиям
Клиническое стадирование сепсиса играет важную роль, так как оно помогает врачам выбирать оптимальную тактику и добиваться наилучших из возможных в каждом конкретном случае результатов лечения. Выделяют следующие стадии:
- Сепсис диагностируют, когда внутренняя температура (измеряется на слизистых оболочках) тела поднимается больше 38 градусов или опускается ниже 36 градусов, частота сердечных сокращений 90 в минуту и более, частота дыхания 20 в минуту и более, либо парциальное давление углекислого газа в артериальной крови (PaCO2) опускается ниже 32 мм. рт. ст. При этом уровень лейкоцитов в крови поднимается более 12000/мкл или опускается ниже ≤4000/мкл, либо среди них появляется более 10% незрелых форм.
- Тяжелый сепсис – сепсис, который сочетается с острой органной дисфункцией.
- Септический шок диагностируют, когда у пациента имеется стойкая гипотензия (снижение артериального давления) или гипоперфузия (недостаточное кровоснабжение) тканей, несмотря на адекватную инфузионную терапию.
- Синдром полиорганной дисфункции – состояние, при котором у больного имеется органная дисфункция (нарушение работы внутренних органов), и его гомеостаз не удается поддерживать без медикаментозного вмешательства.
Лечение сепсиса
Лечение сепсиса базируется на трех принципах:
Санация первичного очага. Это может быть достигнуто с помощью хирургического вмешательства и/или адекватной антибактериальной терапии. При обнаружении первичного очага, который можно санировать хирургически, необходимо провести это как можно скорее. Это может быть вскрытие и дренирование абсцессов, удаление инфицированных инвазивных устройств (катетеры, имплантаты и др.), дренирование и лаваж брюшной полости, и др.
Антимикробная терапия является еще одним краеугольным камнем лечения сепсиса, при этом важна ее своевременность и адекватность. Например, при развитии септического шока, препараты должны быть введены в течение часа от начала симптомов. При этом препарат должен охватывать весь спектр предполагаемых возбудителей и, что немаловажно, проникать в первичный инфекционный очаг. При необходимости назначения комбинированной терапии из нескольких препаратов, их применяют не более 5 дней, после чего должны быть получены данные биологических методов исследования и произведена коррекция схемы лечения. [7]
Обеспечение транспорта кислорода — все клинические проявления сепсиса усугубляются в условиях недостатка кислорода, поэтому очень важно контролировать этот процесс. Для этого проводят:
- Гемодинамическую поддержку — вливание растворов, которые обеспечивают восполнение водно-электролитного баланса, назначаются препараты, поддерживающие артериальное давление и др.
- Респираторную поддержку — искусственную вентиляцию легких, кислородные маски и др.
Коррекция метаболических нарушений
Одним из эффективных способов лечения сепсиса является селективная сорбция на колонках TORAYMYXIN. Данная методика успешно применяется во многих странах мира. В настоящее время такое лечение прошли более 200 тысяч пациентов с септическим шоком и тяжелыми формами сепсиса. Эффективность и безопасность технологии подтверждена в ходе клинических исследований. [11,12]

Осложнения при сепсисе
- Осложнения со стороны дыхательной системы. Нарушение вентиляции легких приводит к повышению аэрогематического барьера и, как следствие, пропотеванию жидкости в альвеолы. Это еще больше нарушает газообмен и приводит к развитию шокового легкого и респираторного дистресс-синдрома, который усугубляется усталостью дыхательных мышц.
- Осложнения со стороны почек. Наблюдается снижение фильтрационной функции почек из-за повреждения канальцев, развившееся в результате снижения давления. Сопровождается резким уменьшением выделяемой мочи, протеинурией, азотемией.
- Нарушение свертывания крови из-за падения уровня тромбоцитов и развития ДВС-синдрома — грозного состояния, при котором сначала происходит массовое образование тромбов в кровеносном русле, а затем массивные кровотечения из-за недостаточности кровесвертывающих факторов.
- Неврологические осложнения. Длительно протекающий сепсис может привести к развитию полинейропатии, которая, в частности, приводит к ослаблению дыхательной мускулатуры и невозможности самостоятельного дыхания.
- Септический шок — самое тяжелое проявление сепсиса, сопровождающееся стойким снижением кровяного давления, которое сложно восстановить даже с применением инфузионной терапии и вазопрессоров. Он развивается из-за выхода жидкости из кровеносных сосудов и из-за общего обезвоживания. При этом, нарушения настолько тяжелые, что могут привести к гибели пациента от полиорганной недостаточности.[13]
Прогноз при сепсисе
Прогноз при сепсисе очень осторожный. На возможность выздоровления оказывают влияние особенности этиологической микрофлоры, общее состояние пациента в начале заболевания, а также своевременность и адекватность проводимого лечения. Наиболее неблагоприятно сепсис протекает у людей старческого возраста и у ослабленных пациентов, имеющих сопутствующие заболевания.
В целом в крупных клиниках летальность при данном состоянии составляет 30-40%. При развитии септического шока, ситуация усугубляется и согласно некоторым данным, в таком случае от него погибает до 90% больных.
Сепсис — опасное состояние, вызванное чрезмерной реакцией организма на различные инфекционные агенты: бактерии, вирусы или грибки. Иными словами, это инфекционный воспалительный процесс, который распространяется на весь организм (синдром системной воспалительной реакции, ССВР). При сепсисе возникают нарушения со стороны иммунной, сердечно-сосудистой системы, системы свертывания крови. Ухудшается приток крови к органам, в результате в финале развивается полиорганная недостаточность, которая и приводит к гибели пациента.
Ежегодно сепсис уносит более миллиона жизней во всем мире. В Европе каждый год диагностируется около 500 тысяч случаев сепсиса, в США — около 1,5 миллиона. Показатели смертности составляют 25–30% и более: каждый 3–4-й пациент с сепсисом погибает. С этим состоянием очень сложно бороться, особенно если оно протекает в форме септического шока.
У онкологических больных повышен риск развития как тяжелых инфекционных заболеваний, так и сепсиса. На это есть ряд причин:
- Многие пациенты, особенно при поздних стадиях рака, часто и подолгу находятся в стационаре. Несмотря на все меры асептики и антисептики, применение антибиотиков, в больничных стенах всегда циркулируют болезнетворные бактерии. Они становятся устойчивыми к антибактериальным препаратам и могут вызывать внутрибольничные инфекции.
- Многие химиопрепараты ослабляют иммунную систему. Поэтому инфекции, практически не опасные для здорового человека, у онкобольных могут протекать в тяжелой форме, приводить к опасным осложнениям.
- Онкологическое заболевание само по себе ослабляет весь организм, в том числе иммунитет.
- В терапии рака часто применяются инвазивные процедуры, начиная банальными инъекциями (уколами) лекарственных препаратов и заканчивая сложными хирургическими вмешательствами. Для человека, у которого иммунная система неправильно реагирует на патогены, даже небольшая рана может вызвать инфекцию и сепсис.
Причины сепсиса
К сепсису могут привести разные инфекции, когда организм реагирует на них слишком бурно. Чаще всего виновниками становятся болезнетворные бактерии, в том числе условно-патогенные, которые входят в состав естественной микрофлоры.
К распространенным причинам сепсиса относятся:
- перитонит — воспаление брюшины, тонкой пленки, которая выстилает стенки брюшной полости и покрывает внутренние органы;
- заболевания кишечника;
- инфекции печени, желчного пузыря;
- аппендицит;
- инфекции центральной нервной системы (головного и спинного мозга);
- пневмония (воспаление легких);
- любые повреждения кожи, в том числе во время медицинских процедур, особенно если они проводятся с нарушением правил асептики и антисептики;
- инфекции почек, мочеточников, мочевого пузыря (риск повышен у пациентов, у которых на длительное время установлен катетер для выведения мочи).
Разновидности сепсиса
Если в организме обнаружен очаг воспаления, и понятно, что генерализация процесса началась именно из этого места, то сепсис называют вторичным. В зависимости того, где изначально возникла инфекция, врачи могут называть сепсис хирургическим, гинекологическим, легочным, посттравматическим, одонтогенным (связанным с заболеванием зубов) и пр.
Иногда встречаются ситуации, когда есть и системное воспаление, и возбудитель инфекции, а место, в котором начался инфекционный процесс, обнаружить не удается. В таких случаях сепсис называют первичным или криптогенным. Принципы его лечения те же, что и при вторичном сепсисе.
В зависимости от клинической картины, выделяют две разновидности сепсиса:
В зависимости от того, какие возбудители проникли в организм и вызвали неадекватную реакцию иммунитета, выделяют сепсис бактериальный, грибковый, вирусный и смешанный.
По характеру течения сепсис бывает:
- молниеносным — развивается в течение 1–3 суток после того, как возбудители попали в организм и вызвали инфекцию;
- острым — от 2 суток до 4 месяцев;
- подострым — от 2 до 6 месяцев;
- хроническим — продолжается в течение многих месяцев, до года и более.
Грамположительный и грамотрицательный сепсис
В зависимости от того, как бактерии окрашиваются после обработки специальными красителями, их делят на грамположительные и грамотрицательные. Соответственно, сепсис, в зависимости от характера возбудителя, тоже бывает грамположительным и грамотрицательным, и это деление играет важную роль в клинической практике.
Среди грамположительных бактерий при сепсисе чаще всего встречаются стафилококки и стрептококки. Эти бактерии выделяют экзотоксины — белки, которые нарушают важные процессы в клетках человека и отравляют организм. Стафилококковый сепсис в 95% случаев протекает в виде септикопиемии, а стрептококковый — чаще всего как тяжелая септицемия с нарушением функции внутренних органов.
Грамотрицательный сепсис чаще всего вызывают кишечные палочки, клебсиеллы, протеи, энтеробактерии, синегнойные палочки. В этих бактериях содержатся очень мощные эндотоксины. Они отличаются от экзотоксинов тем, что являются структурными компонентами бактериальных клеток и выделяются вовне только после их гибели. По структуре эндотоксины представляют собой липополисахариды. Они вызывают в организме человека серьезные патологические изменения:
- Повышение выработки цитокинов — веществ, участвующих в воспалительном процессе. Может возникнуть порочный круг, когда в организме вырабатывается огромное количество цитокинов, они активируют иммунные клетки, и те вырабатывают новые цитокины. Это состояние называется цитокиновым штормом, и оно может привести к гибели больного.
- Некроз (гибель) клеток, выстилающих стенки кровеносных сосудов (эндотелиоцитов), и образование тромбов.
- Эндотоксемия — отравление организма токсичными продуктами обмена веществ.
- Полиорганная недостаточность — смертельно опасное нарушение функции всех органов.
Грамотрицательный сепсис обычно протекает тяжело. Нередко уже в самом начале развивается септический шок, и многие пациенты погибают. Особенно грозные ситуации — когда присоединяется внутрибольничная инфекция, вызванная полирезистентными (устойчивыми к двум и более разным антибиотикам) бактерии.
Осложнения сепсиса
Самая тяжелая форма сепсиса (ее рассматривают как осложнение, которое может развиваться при любой форме и характере течения сепсиса) — септической шок. Сильно нарушается кровообращение, падает артериальное давление, органы перестают получать достаточное количество кислорода, развиваются выраженные нарушения в тканях и обмене веществ. Пациенты, у которых развилось это состояние, часто погибают.
В современных клиниках, где доступны все виды лечения, большинство пациентов с сепсисом удается спасти. Тем не менее, показатели смертности даже в развитых странах довольно высоки. Кроме того, если пациент перенес тяжелый сепсис, в будущем у него повышен риск опасных инфекций.
Симптомы сепсиса
Специфических симптомов, по которым можно сразу и со стопроцентной точностью распознать сепсис, не существует. Клиническая картина бывает разной, проявления могут быть выражены в различной степени, от легких до угрожающих жизни.
В целом заподозрить сепсис можно по следующим симптомам:
- Повышение температуры тела более 38° C (иногда она, напротив, снижается менее 36° C).
- Учащение сердечных сокращений — более 90 в минуту.
- Одышка, учащенное дыхание — более 20 в минуту.
- Кожа, покрытая липким потом.
- Заторможенность, дезориентация.
Если добавить к этому списку два лабораторных показателя — парциальное давление углекислого газа в крови более 32 мм рт. ст. и количество лейкоцитов в крови меньше 4 тысяч или больше 12 тысяч на л — то получим критерии диагностики синдрома системного воспалительного ответа.
Симптомы хрониосепсиса
Хронический сепсис протекает в течение длительного времени и характеризуется вялотекущим течением, симптомы выражены слабо. Поэтому диагностировать хрониосепсис зачастую бывает сложно.
Среди экспертов существует мнение, что даже острый сепсис стоит рассматривать как двухфазное заболевание с хроническим компонентом. Даже если больного удается излечить в остром периоде, заболевание зачастую не проходит бесследно. Сохраняются нарушения, которые приводят к хроническим критическим болезням и могут стать причиной смерти.
Что является сепсисом, и что им не является?
Чтобы разобраться в этом вопросе, поговорим о некоторых распространенных заблуждениях:
Это правда, но только наполовину. Человек постоянно сталкивается с инфекциями в повседневной жизни. Например, вы можете прикоснуться в супермаркете к ручке двери, на которой находятся вирусы ОРВИ, а затем перенести их на слизистую оболочку, почесав нос. Но это не приведет к сепсису. Вы просто заболеете простудой, в худшем случае — гриппом или COVID-19. Даже в составе нормальной микрофлоры тела человека присутствуют бактерии, которые при определенных условиях вызывают опасные инфекции и сепсис. Однако, у большинства людей этого не происходит.
Если болезнетворные бактерии попали в кровоток, такое состояние называется бактериемией. Но и это еще не сепсис.
Во-первых, сепсисом нельзя заразиться. Напрямую от больного можно заразиться лишь некоторыми инфекциями, которые приводят к сепсису. Если ваша иммунная система работает нормально, то у вас разовьется лишь соответствующая инфекция. Во-вторых, согласно данным экспертов из Альянса Сепсиса (Sepsis Alliance, США), в 80% случаев сепсис развивается у людей, которые не находятся в стационаре.
Несмотря на то, что в арсенале современных врачей есть много антибиотиков, с сепсисом по-прежнему сложно бороться. Например, в США он ежегодно уносит больше жизней, чем рак молочной железы, простаты и СПИД вместе взятые. Появляется все больше бактерий, устойчивых к антибиотикам, — это огромная проблема современного здравоохранения. И вообще, как мы уже разобрались выше, дело не только в инфекциях, но и в особенностях иммунного ответа. Некоторые люди находятся в группе повышенного риска. Например, онкологические больные.
Обследование при сепсисе
При сепсисе назначают методы диагностики, которые помогают обнаружить возбудителя инфекции, оценить степень нарушений в организме, спланировать тактику лечения:
- Тесты на инфекции: анализы крови, мокроты, мочи, выделений из раны.
- Оценка свертываемости крови: коагулограмма.
- Определение количества тромбоцитов и других форменных элементов крови.
- Оценка функции почек и печени: биохимический анализ крови, определение уровня креатинина, билирубина, диуреза (количества мочи).
- Оценка снабжения тканей кислородом: определение парциального давления кислорода артериальной крови, фракции вдыхаемого кислорода.
- Оценка уровней электролитов в крови.
- Контроль состояния сердечно-сосудистой системы: мониторинг артериального давления, ЭКГ, частоты пульса.
- Оценка состояния сознания по шкале Комы Глазго.
- Инструментальные исследования для обнаружения очага инфекции: рентгенография, ультразвуковое исследование, компьютерная томография, магнитно-резонансная томография.
- исследование активности эндотоксина в крови (EAA);
- определение уровня прокальцитонина в крови.
Комплексное лечение при сепсисе
При сепсисе важно как можно быстрее установить диагноз и начать лечение:
- селективная сорбция липополисахаридов (эндотоксина) сорбентом Toraymyxin;
- гемосорбция сорбционной колонкой Cytosorb — применяется для борьбы с цитокиновым штормом при септическом шоке, этот метод очищает кровь от цитокинов.
Когда нужно сдать анализ крови на сепсис?
Врач может заподозрить, что у пациента развивается сепсис, и назначить анализы, если:
- У больного возникли соответствующие симптомы.
- Лабораторные исследования, которые были проведены ранее, дают повод заподозрить это состояние.
Иногда симптомы сепсиса бывают выражены слабо, их легко спутать с признаками других заболеваний. У пациента повышается температура тела до 38° C, учащаются сердечные сокращения и дыхание, он сильно потеет, при этом имеются симптомы инфекции, из-за которой развилась системная воспалительная реакция в организме. Возникают признаки нарушений работы различных органов.
В тяжелых случаях возникает спутанность сознания, больной становится вялым, снижается артериальное давление, ноги, руки и губы холодные, синюшные, на коже появляются пятна, как при менингите.
Для того чтобы вовремя распознать сепсис и назначить необходимые анализы, традиционно врачи используют критерии шкалы quick SOFA (qSOFA). Если есть все три критерия, скорее всего, это сепсис:
Более точно установить диагноз помогают критерии по шкале SOFA, в них учитываются данные лабораторных анализов:
| Показатели | Баллы | ||||
| 0 | 1 | 2 | 3 | 4 | |
| Индекс оксигенации (измеряется в отделении интенсивной терапии) | Более 400 мм рт. ст. | 300–399 мм рт. ст. | 200–299 мм рт. ст. | 100–199 мм рт. ст. | Менее 100 мм рт. ст. |
| Уровень тромбоцитов | Более 150×109/л | Менее 150×109/л | Менее 100×109/л | Менее 50×109/л | Менее 20×109/л |
| Уровень билирубина в крови (функция печени) | Менее 20 мкмоль/л | 20–30 мкмоль/л | 33–101 мкмоль/л | 102–204 мкмоль/л | Более 204 мкмоль/л |
| Снижение артериального давления | Нет | Менее 70 мм рт. ст. | Удается удерживать лишь с помощью медикаментозных препаратов. | ||
| Оценка по шкале комы Глазго | 15 | 13–14 | 10–12 | 6–9 | Менее 6 |
| Уровень креатинина в крови (функция почек) | Менее 110 мкмоль/л | 110–170 мкмоль/л | 171–299 мкмоль/л | 300–440 мкмоль/л | Более 440 мкмоль/л |
| Количество мочи в сутки | Менее 500 мл в день | Менее 200 мл в день | |||
Процедура проведения анализа крови при сепсисе
Анализ активности эндотоксина (Endotoxin Activity Assay — EAA) — единственный метод количественного определения бактериального токсина, который одобрен Управлением по контролю качества пищевых продуктов и медикаментов США (Food and Drug Administration — FDA).
Что такое эндотоксин? Вещество, по химической природе липополисахарид, встроенное в клеточную мембрану грамотрицательных бактерий. Это мощный медиатор воспаления, и его уровень в крови повышается уже на ранних этапах развития сепсиса.
Для того чтобы определить уровень эндотоксина, у пациента берут кровь и добавляют в нее специфические антитела. Они связываются с бактериальным липополисахаридом, и эти комплексы поглощают нейтрофилы (особая разновидность лейкоцитов). В этих клетках происходят некоторые биохимические реакции, они начинают быстро поглощать и расходовать кислород. В присутствии люминофора возникает свечение, которое можно зарегистрировать с помощью особого инструмента — люминометра. По интенсивности свечения судят об уровне эндотоксина в крови.
Результат измеряется от 0 до 1:
- 0 — отсутствует;
- менее 0,4 — низкий уровень;
- 0,4–0,59 — промежуточный уровень;
- 0,6 и более — высокий уровень;
- 1 — максимальный уровень.
Показатели эритроцитов при сепсисе
Эритроциты — красные кровяные клетки, которые содержат гемоглобин и отвечают за транспорт кислорода, углекислого газа. При тяжелом сепсисе с ними происходят следующие изменения:
Показатели СОЭ при сепсисе
Скорость оседания эритроцитов, сокращенно СОЭ, характеризует скорость оседания эритроцитов под действием силы тяжести в крови, в которой искусственно заблокированы процессы свертывания (образования тромба). У мужчин этот показатель в норме составляет 2–15 мм/час, у женщин — 1–10 мм/час. При сепсисе СОЭ повышается, что является признаком воспалительного процесса в организме.
Показатели лейкоцитов при сепсисе
При сепсисе количество белых кровяных телец в крови увеличивается — возникает лейкоцитоз. Причины вполне объяснимы, ведь в организме развивается воспалительный процесс. В некоторых случаях уменьшается количество нейтрофилов — особого вида лейкоцитов. Это состояние называется нейтропенией, и оно связано с худшим прогнозом.
Показатели тромбоцитов при сепсисе
Снижение количества тромбоцитов в крови — тромбоцитопения — один из симптомов и критериев диагностики сепсиса по шкале SOFA. Риск смерти пациента напрямую зависит от того, насколько сильно у него снижено число тромбоцитов, и как долго сохраняется это состояние. При тромбоцитопении менее 100×109/л риск кровотечения больше не повышается, но уровень смертности продолжает расти.

Как определить заражение крови?
Сепсис характеризуется смертностью от 10 до 40%. На этот показатель влияет вид возбудителя, состояние организма пациента и, что немаловажно, время, в течение которого установлен точный диагноз и начато лечение. Иногда патология протекает в виде септического шока: нарушается кровообращение, обменные процессы в клетках, резко падает артериальное давление, и поддерживать его на цифрах больше 65 мм рт. ст. удается только с помощью лекарств. Среди больных септическим шоком смертность значительно выше.
Кроме того, мы применяем инновационный метод очистки крови от эндотоксина — селективную сорбцию на картриджах для экстракорпоральной гемоперфузии Toramyxin PMX-20R. Эта процедура действует как плазмаферез: кровь больного пропускают через специальный аппарат, в котором задерживается эндотоксин — один из главных виновников системной воспалительной реакции. Фильтр аппарата состоит из волокон, к которым прикреплены молекулы антибиотика полимиксина Б. Он связывается с эндотоксином и образует с ним стабильный комплекс.
Сорбция эндотоксина на картриджах помогает эффективно бороться с тяжелым сепсисом, вызванным грамотрицательными бактериями и смешанной флорой.
Что такое баланопостит? Причины возникновения, диагностику и методы лечения разберем в статье доктора Ахмерова Надира Минисалимовича, уролога со стажем в 28 лет.
Над статьей доктора Ахмерова Надира Минисалимовича работали литературный редактор Маргарита Тихонова , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Баланопостит — это воспаление крайней плоти и головки полового члена, чаще всего инфекционного характера. Проявляется покраснением, отёком, зудом и жжением поражённой области.
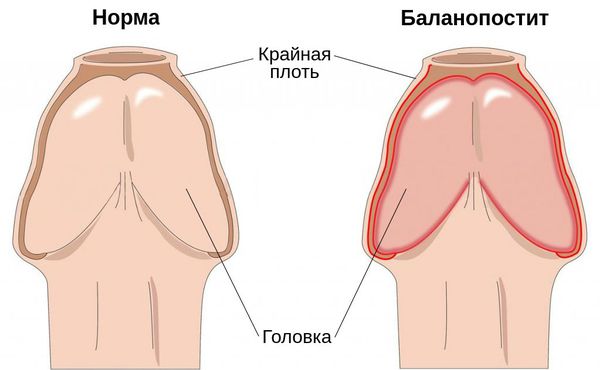
Заболевание является распространённым и встречается в любой возрастной группе. На его долю приходится 47 % случаев среди всех поражений кожи полового члена и 11 % случаев среди всех обращений в кабинеты уролога и венеролога [1] .
Причина болезни — инфекционные агенты, проникшие в кожу головки и крайней плоти. Причём инфекция может быть как банальной (стафилококки, стрептококки и др.), так и связанной с заболеваниями, передающимися половым путём.
Часто баланопостит возникает как осложнение основного заболевания (например уретрита или простатита ). Также он может являться индикатором наличия серьёзной эндокринной патологии (сахарного диабета) или приобретённого иммунодефицита, в том числе заболеваний, ассоциированных с ВИЧ-инфекцией ( наркомании и вирусного гепатита и др.).
Лёгкому проникновению инфекции и быстрому развитию воспаления способствуют определённые анатомические и физиологические особенности поражаемой области:
- относительно тонкий эпидермис (наружный слой кожи);
- выраженное кровоснабжение;
- рыхлость подлежащего соединительнотканного слоя;
- наличие препуциального мешка, который содержит выделения смегмальных (сальных) желёз, необходимых для сохранения эластичности головки полового члена.
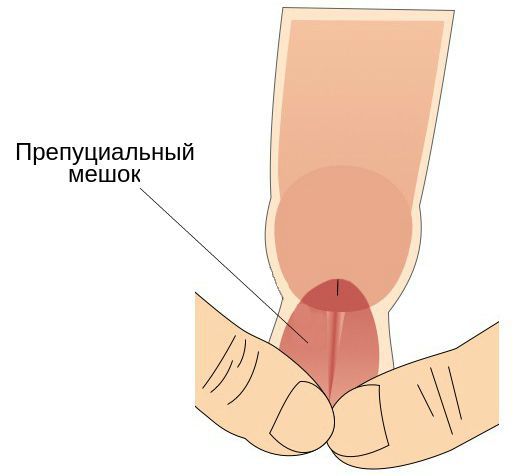
Также имеет значение недостаточная или избыточная гигиена половых органов, частые незащищённые половые контакты, наличие сопутствующих заболеваний (например атеросклероза или дерматитов) и работа в тяжёлых условиях (связанная с высокой температурой и загрязнениями) [2] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы баланопостита
Проявления баланопостита в целом не отличаются от воспалительных симптомов других локализаций. Чаще всего заболевание характеризуется триадой признаков воспаления : отёком, болью и покраснением. Однако вместо болевого синдрома при баланопостите обычно появляется зуд и жжение в поражённой области. На месте воспалительных очагов очень часто образуются эрозии (поверхностные раны), покрытые выделениями и налётом белого или жёлто-зелёного цвета [3] .
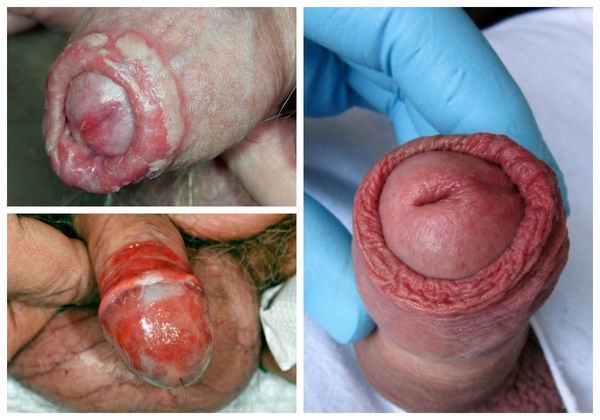
Один из важных диагностических признаков болезни — усиление симптомов во время и после полового акта . За счёт механического раздражения воспалённой кожи возникает покраснение, налёт или зуд. Также симптомы баланопостита могут усиливаться во время и после мочеиспускания.
Серьёзным симптомом выраженной воспалительной реакции является затруднённое и болезненное обнажение головки. Оно связано не только с самим воспалением, но и с осложнениями в виде воспалительных спаек и фимоза (сужения крайней плоти). Чаще всего спайки возникают у детей. Они образуются через несколько дней после начала заболевания и прогрессируют в случае позднего обращения к врачу.
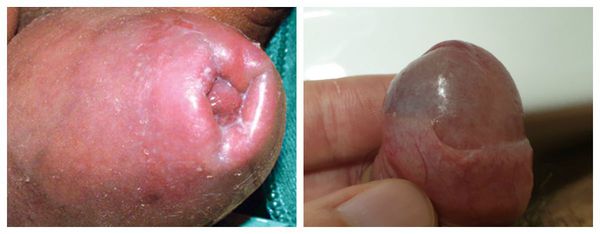
Патогенез баланопостита
Головка, внутренний листок крайней плоти и образуемый ими препуциальный мешок являются единым анатомическим образованием. В состоянии покоя у необрезанных мужчин головка находится внутри препуциального мешка, который защищает её от внешних травматических и температурных факторов [4] . Во внутреннем листке крайней плоти содержится большое количество сальных желёз. Секрет, который они вырабатывают, увлажняет и смазывает головку для её беспрепятственного обнажения при потребности. Во время эрекции за счёт увеличения полового члена и расправления крайней плоти головка обнажается, а препуциальный мешок исчезает.
Такие о собенности строения полового члена у необрезанных мужчин способствует развитию баланопостита [5] . Также к предрасполагающим факторам относятся суженное отверстие препуциального мешка и избыточная (удлинённая) крайняя плоть, которая даже при максимальной эрекции покрывает головку полностью или частично. Несмотря на отсутствие перечисленных факторов, у обрезанных мужчин также возникает баланопостит , хотя реже, чем у необрезанных.
Другим фактором, способствующим развитию болезни, является плохая гигиена. При этом в полости препуциального мешка скапливается так называемая смегма. Она является смесью выделений сальных желёз, лейкоцитов и слущенного эпителия. В норме смегма постоянно обновляется за счёт гигиены или регулярной половой жизни. При нарушении процессов обновления она скапливается и становится прекрасной средой для размножения микроорганизмов и развития воспаления окружающих тканей.
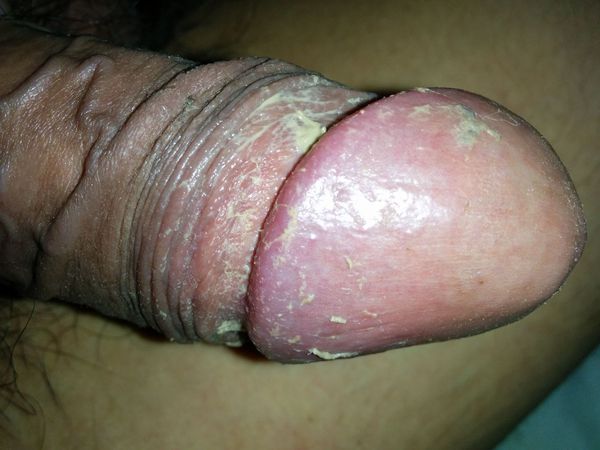
Процесс в оспаления в итоге приводит к нарушению функции полового члена. В начале болезни возникает покраснение, которое сопровождается зудом или жжением, в некоторых случаях — появлением налёта. Затем присоединяется отёк, возникает боль. В итоге заболевание приводит к невозможности вести половую жизнь, а при самом неблагоприятном развитии — к острой задержке мочеиспускания.
Классификация и стадии развития баланопостита
Классификаций баланопостита довольно много, так как исследованием этого заболевания занимаются врачи нескольких специальностей: урологи, андрологи, дерматовенерологи, хирурги и педиатры. Наиболее полно этиологическую и клиническую картину болезни отображает классификация, представленная Британской ассоциацией сексуального здоровья и ВИЧ (BASHH). Она рекомендована для практического применения в странах Европы [6] .
Согласно классификации BASHH, выделяют два типа баланопостита: инфекционный и неинфекционный . Инфекционный баланопостит, в зависимости от причинного фактора, разделяют на восемь подтипов:
- Candida albicans. Грибы этого рода являются частой причиной баланопостита ввиду их широкого распространения у женщин, нерационального применения антибиотиков и увеличения частоты вторичных иммунодефицитов . Обычно Candida albicans передаются половым путём. Но бывают случаи заражения, не связанные с сексуальной активностью: при сахарном диабете или после антибиотикотерапии [10][12] .
- Trichomonas vaginalis . Трихомонады являются простейшими микроорганизмами. Они паразитируют в половых органах как мужчин, так и женщин. Передаются половым путём [13] .
- Streptococcus (A, B). Стрептококки могут бессимптомно присутствовать в половой сфере, но при заболевании их концентрация резко увеличивается [15] .
- Anaerobes (бактероиды, фузобактерии, актиномицеты, клостридии). Обнаружение анаэробов на коже головки полового члена часто ассоциируется с хроническим неспецифическим уретритом и баланопоститом. Причём в основном развитие этих заболеваний связано не с одним видом возбудителей, а сразу с несколькими (т. е. с микст-инфекцией).
- Gardnerella vaginalis . Гарднереллёз довольно часто становится причиной воспалительных реакций половых органов. Распространённость G. vaginalis среди урологических больных в целом составляет 8 %, а при баланопостите, не обусловленном Candida — до 31 % [14] .
- Staphylococcus aureus . Наличие золотистого стафилококка часто не вызывает никаких симптомов, но в некоторых случаях может стать причиной болезни [16] .
- Treponema pallidum . При локализации первичного очага инфекции на головке или крайней плоти бледная трепонема вызывает баланопостит, но уже специфический — ассоциированный с сифилисом .
- Herpes simplex virus . Вирус простого герпеса 1-го и 2-го типа тоже может быть причиной воспаления [18] .
Неинфекционные баланопоститы делятся на два подтипа:
- обусловленные заболеваниями кожи — склеротическим лихеном, баланопоститом Зуна, красным плоским лишаём , контактным аллергическим дерматитом , псориазом и др.;
- обусловленные другими причинами — травмами, раздражением, несоблюдением гигиены и др.
Осложнения баланопостита
К осложнениям баланопостита относятся:
-
; ; ;
- некроз головки полового члена;
- паховый лимфангиит и лимфаденит.
Фимоз — кольцевидное сужение крайней плоти, препятствующее обнажению головки. Его развитие связано с образованием рубцовой ткани и потерей эластичности крайней плоти. Особенно часто он возникает при рецидивирующем или торпидном (вялотекущем, длительном) течении баланопостита, а также при его сочетании с системными заболеваниями (в частности с сахарным диабетом). В редких случаях при выраженном сужении крайней плоти возникает хроническая задержка мочеиспускания, требующая неотложного лечения.
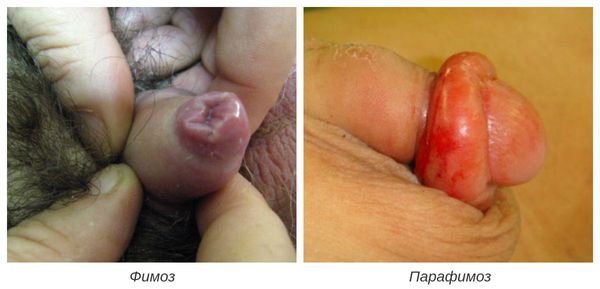
Некроз головки полового члена — р едкое, но грозное осложнение. Чаще всего связано с наличием анаэробной инфекции, в частности фузобактерий [17] . Молниеносное течение этого осложнения, так называемая гангрена Фурнье , может привести к гибели пациента. На начальной стадии гангрена Фурнье проявляется в виде обычного баланопостита. Её особенностью является быстрое распространение воспаления в виде покраснения, отёка и крепитации тканей (их потрескивания при нажатии), а также образование массивного некроза гениталий. Она возникает, как правило, на фоне выраженных иммунодефицитных состояний (в т. ч. хронического алкоголизма , ВИЧ-инфекции ) и сопровождается мощнейшей интоксикацией.
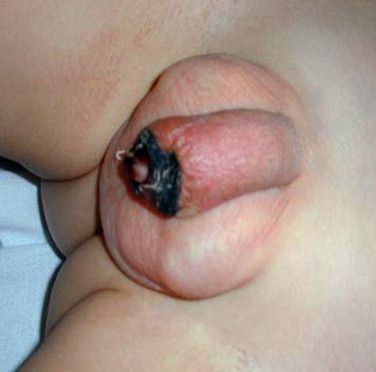
Стриктура уретры — сужение мочеиспускательного канала. Возникает при длительно протекающем баланопостите либо в связи с наличием специфического возбудителя, вызывающего активное деление клеток. Проявляется затруднённым мочеиспусканием и неполным опорожнением мочевого пузыря. Способствует развитию хронической инфекции мочевыводящих путей (циститу, пиелонефриту, гидронефрозу) и даже хронической почечной недостаточности.
Паховый лимфаденит и лимфангиит — воспаление паховых лимфатических узлов и сосудов. Данное осложнение свидетельствует о распространении инфекции за пределы поражённого органа. Как правило, оно требует коррекции проводимых лечебных мероприятий.
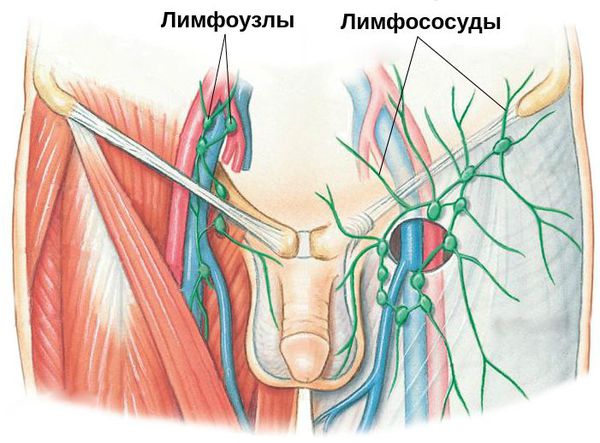
Диагностика баланопостита
Постановка первичного диагноза на основе жалоб, данных анамнеза и визуального осмотра обычно не вызывает затруднений. Самыми частыми симптомами баланопостита являются: покраснение и отёк головки и крайней плоти, зуд и жжение в месте поражения. Иногда отмечается боль, появление налёта или выделений на головке, болезненное мочеиспускание, затруднение или невозможность обнажения или вправления головки полового члена. Также могут присутствовать язвенные дефекты, болезненность и покраснение в проекции паховых лимфоузлов. В редких случаях отмечается ухудшение общего самочувствия, повышение температуры от 37,0-37,9 ℃ и выше с присоединением озноба.
Для выявления причинного фактора и состояний, способствующих развитию или рецидивированию заболевания, требуются дополнительные методы обследования [16] .
Основные :
- бактериологический анализ отделяемого из головки или крайней плоти на аэробную флору и грибы рода Candida (бакпосев);
- скрининговое исследование методом ПЦР (полимеразной цепной реакции) на инфекции, передаваемые половым путём;
- анализы крови и мочи на глюкозу для исключения или подтверждения сахарного диабета;
- клинический анализ крови;
- серологическая диагностика сифилиса — поиск антител к бледной трепонеме.
Дополнительные :
- консультация дерматолога для исключения дерматитов или аллергических заболеваний, сопровождающихся высыпаниями на головке полового члена;
- консультация эндокринолога при выявлении повышенного уровня глюкозы;
- биопсия кожи головки или крайней плоти в случае подозрения на злокачественный процесс или при торпидном течении заболевания.
Лечение баланопостита
Тактика лечения зависит от стадии развития процесса, наличия осложнений или сопутствующих заболеваний.
При неосложнённом баланопостите, который возник впервые, показана местная терапия в виде нанесения растворов или лечебных мазей на место поражения. Выбор лекарственного средства зависит от вида предполагаемого или подтверждённого возбудителя [9] [11] . Это могут быть антибактериальные, противогрибковые или противовирусные препараты.
В случае рецидива заболевания или выраженной воспалительной реакции, особенно при повышении температуры тела, показано назначение соответствующих лекарств в виде таблеток, капсул или инъекций. При этом необходимо учитывать результаты обследований по определению вида возбудителя. В случае выявления сахарного диабета обязательно назначение препаратов, снижающих уровень глюкозы в крови.
Некоторые осложнения баланопостита требуют операционного лечения. При развитии фимоза показана циркумцизия, или обрезание. При этом вмешательстве удаляется рубцово-изменённая крайняя плоть, после чего накладываются швы. В результате головка становится полностью обнажённой. Эту же операцию рекомендуют при большом количестве рецидивов. Эффективность циркумцизии доказана в ряде исследований [19] [20] [21] [22] .
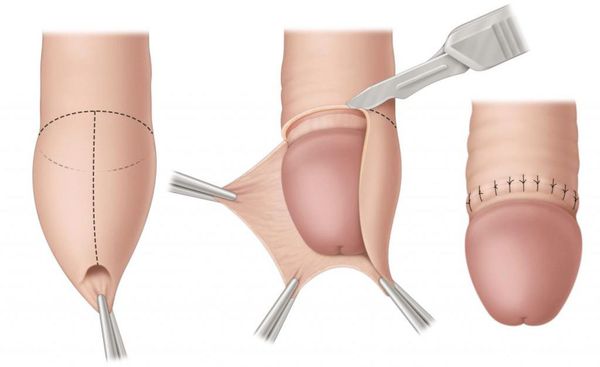
В случае парафимоза проводится операция по рассечению ущемляющего кольца и вправлению головки.
Тактика лечения стриктуры уретры зависит от расположения и размеров стеноза. Для расширения уретры потребуется меатотомия — рассечение наружного отверстия мочеиспускательного канала с наложением швов. При большой протяжённости стриктуры показана пластика уретры.
Однако большинство осложнений и рецидивов заболевания удаётся избежать благодаря своевременному обращению к врачу и проведённому медикаментозному лечению.
Прогноз. Профилактика
Прогноз чаще всего благоприятный. В случае точного выяснения причины заболевания и вовремя начатой терапии наступает полное излечение. Однако при отсутствии лечения или наличии сопутствующей патологии (например сахарного диабета) не исключается появление осложнений, которые потребуют коррекции, в частности оперативного вмешательства. При развитии такого осложнения, как гангрена Фурнье, летальность составляет, по данным разных авторов, от 4 до 54 % [23] .
Профилактика баланопостита, как ни странно, начинается с младенчества. Она заключается в гигиене наружных половых органов. В первые годы жизни ребёнка она проводится родителями, затем прививается детям в виде соблюдения элементарных санитарно-гигиенических правил.
Также нужно уделять внимание вопросам раскрытия головки. Дело в том, что у младенцев кожа крайней плоти недостаточно растяжима, поэтому до 5-6-летнего возраста головка раскрывается не у всех мальчиков [8] . Данный физиологический фимоз не является заболеванием. Однако если в дальнейшем головка по-прежнему не раскрывается — это повод обратиться к врачу.
После начала половой жизни микрофлора половых органов может измениться. Любые новые бактерии, грибки и вирусы, проникающие в организм мужчины во время незащищённых половых актов, способствуют истощению его защитных сил и возникновению инфекции. Поэтому важным средством профилактики баланопостита, равно как и инфекций, передающихся половым путём, является использование презервативов.
Не менее важным средством профилактики баланопостита является соблюдение гигиенических правил у взрослых. Так называемая "болезнь грязных рук" возможна в любом возрасте. Чтобы избежать занесения инфекции, нужно не только мыть руки перед мочеиспусканием (особенно если приходится работать в антисанитарных условиях), но и регулярно принимать душ или ванну, тщательно промывая головку и крайнюю плоть.
Так как баланопостит является первым проявлением некоторых соматических заболеваний, необходимо не реже одного раза в год осуществлять контроль общего холестерина и глюкозы в крови для исключения скрытых микрососудистых нарушений.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
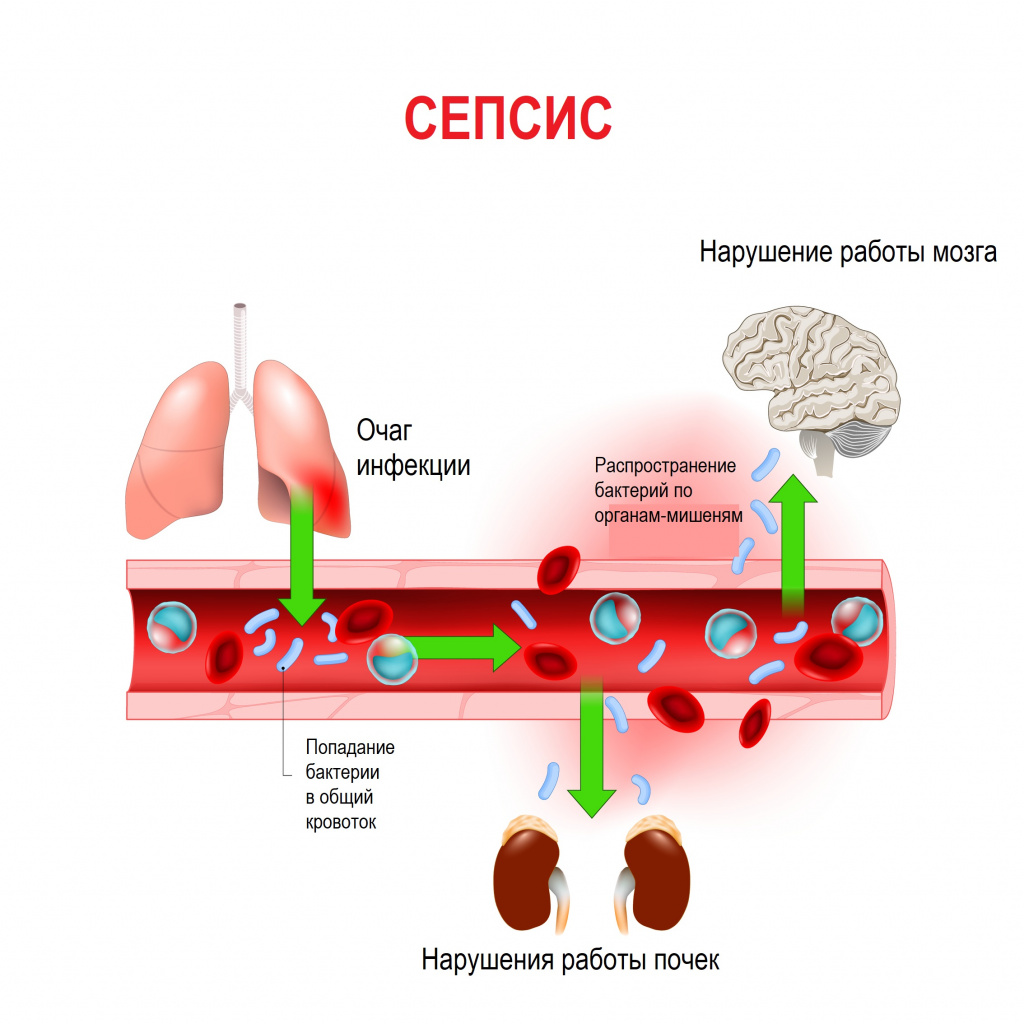
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм >10%.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно - за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
Читайте также:

