Сепсис септический шок лекция
Обновлено: 22.04.2024
Термин "сепсис" был введен в 4 веке до н. э. Аристотелем, который понимал под ним отравление организма продуктами гниения собственных тканей. В настоящее время определение сепсиса следующее.
Сепсис – это тяжелое инфекционное заболевание, вызываемое разными возбудителями и их токсинами, проявляющееся своеобразной реакцией организма с однотипной клинической картиной. Возбудителями сепсиса могут быть бактерии (90%), грибы, простейшие и вирусы.
Под термином "хирургический сепсис" следует понимать тяжелое общее заболевание, возникающее на фоне существующего очага инфекции, изменений иммунореактивности организма и требующее местного хирургического и общего интенсивного лечения.
Сепсис не является заразной болезнью в эпидемиологическом отношении, не формирует иммунитет и не имеет определенных сроков инкубационного периода. Так как причиной сепсиса являются различные возбудители, то он является синонимом понятия "диссеминированная инфекция", которую от обычного инфекционного процесса отличает полиэтиологический или клинический характер вне зависимости от возбудителя, с возможной его сменой в течение болезни.
В среднем сепсис развивается у 1-5 больных на 1000 госпитализированных в зависимости от профиля лечебного учреждения.
В США ежегодно регистрируется от 400 до 500 тыс. случаев сепсиса, умирает 215 тыс. человек. Затраты на лечение одного пациента составляют 22 100 долларов США, а ежегодные затраты – 16,7 млрд. долларов. (Ж. Хирургия № 9, 2002 г., с. 52).
Сепсис. Терминология
Первичный очаг – участок воспаления, возникающий на месте внедрения инфекции: раны (травматические, операционные), местные гнойные процессы (фурункулы, карбункулы, абсцессы и др.);
Вторичный очаг возникает при распространении инфекции за пределы первичного очага в различные органы и ткани, отдаленные от места внедрения инфекции;
Вторичный сепсис развивается на фоне гнойного очага (раны, гнойного хирургического заболевания, оперативного вмешательства).
Преобладающий возбудитель – стафилококк. В последнее время возросла роль Гр (-) флоры (синегнойная палочка, протей, кишечная палочка).
Причинами роста Гр (-) сепсиса и возрастания роли условно патогенной флоры следует считать снижение сопротивляемости организма, расширение объема и увеличение тяжести оперативных вмешательств, а также широкое и часто бессистемное применение антибиотиков.
Возбудитель особенно "опасен" в первичном и вторичном очагах; именно здесь он "гнездится", воздействует на ткани и отсюда происходит всасывание бактериальных токсинов и продуктов распада тканей.
В последнее десятилетие представления о механизмах воспалительной реакции претерпели существенные изменения. Благодаря успехам молекулярной биологии был выделен новый класс медиаторов воспаления.
Фактор агрегации тромбоцитов;
Активированные эндотелиальные клетки.
Было показано, что в развитии воспалительной реакции ведущая роль принадлежит цитокинам, оксиду азота (NO), фактору агрегации тромбоцитов, активированным эндотелиальным клеткам.
Цитокины продуцируются моноцитами, макрофагами, нейтрофильными лейкоцитами, лимфоцитами, клетками эндотелия, фибробластами.
Цитокины, продуцируемые лейкоцитами, называют интерлейкинами (ИЛ), потому, что, с одной стороны, они продуцируются лейкоцитами, с другой – лейкоциты являются клетками-мишенями для ИЛ. Известно более 20 цитокинов, из них 15 относятся к ИЛ.
Цитокины обеспечивают взаимодействие между клетками, активно участвующими в развитии местной и общей реакции на воспаление, путем усиления или угнетения их функции.
Исследованиями, проведенными в разных лабораториях, было убедительно подтверждено, что воспаление и ответная реакция на него развиваются по одним и тем же закономерностям, как при внедрении инфекции, так и при воздействии механической травмы, ожогов и ряда других факторов.
Цитокиновая система включает в себя 5 обширных классов, объединенных по их доминирующему действию на другие клетки:
провоспалительные (ИЛ 1, 6, 8, 12);
антивоспалительные (ИЛ 4, 10, 11, 13 и др.).
Фактор некроза опухоли (ФНО).
Факторы роста и дифференцировки лимфоцитов.
Факторы, стимулирующие рост колоний макрофагов и гранулоцитов.
Факторы, вызывающие рост мезенхимальных клеток. Большинство реакций при воспалении осуществляется через посредничество цитокинов.
Продукция цитокинов зависит от состояния организма. В норме их секреция ничтожно мала, предназначена для обеспечения взаимодействия между продуцирующими их клетками и другими медиаторами воспаления. Но она резко возрастает при воспалении в связи с активацией клеток, вырабатывающих их. Активация клеток, продуцирующих цитокины, происходит под влиянием эндотоксинов, микроорганизмов, гипоксии, значительной травмы, наличия нежизнеспособных тканей, шока, неизбежно сопровождающихся гипоксией.
Нормально функционирующие механизмы иммунной системы препятствуют бесконтрольному выделению цитокинов и других медиаторов воспаления, обеспечивают адекватную реакцию организма на воспаление. В крови в самом начале воспаления одновременно появляются про- и антивоспалительные ИЛ. При этих условиях они в функциональном отношении создают равновесие, определяющее благоприятное течение воспалительного процесса, отграничение очага воспаления (повреждения).
При нормальном иммунном гомеостазе благоприятное действие медиаторов воспаления преобладает над их повреждающим действием. Реакция жизненно важных систем организма на воспаление носит умеренный адекватный характер, без признаков системной реакции, без дисфункции органов.
При массивной бактериальной агрессии, тяжелой травме (в том числе хирургической), наличии очагов некроза, нежизнеспособных тканей, при остром панкреатите происходит гиперактивация макрофагов, нейтрофилов и других клеток. В связи с этим резко возрастает продукция и содержание цитокинов в крови и в клетках, продуцирующих их, нарушается баланс между про- и антивоспалительными цитокинами и другими медиаторами. В результате этого повреждается иммунная система. Она перестает контролировать секрецию цитокинов и других медиаторов воспаления. Повреждающее действие медиаторов воспаления начинает превалировать над защитным. Дезорганизация функции иммунной системы, потеря контроля над продукцией цитокинов и других медиаторов воспаления, приводят к тому, что про- и антивоспалительные цитокины и другие медиаторы воспаления (NO, О2, простагландин Е2) вместо ограничения воспалительного процесса и защиты организма начинают оказывать деструктивное, повреждающее действие на ткани не только в очаге инфекции, но и в других органах. В результате этого поверхность эндотелия приобретает повышенную тромбогенность и адгезивность, возникают микротромбозы, развивается ДВС-синдром, нарушается микроциркуляция, возникают массивная вазодилатация, переполнение венозного русла, резкое повышение проницаемости сосудистой стенки, гипоксия тканей. Развиваются отеки и гиповолемия, нарушается кровоснабжение жизненно важных органов, возникает их дисфункция, которая при определенных условиях может переходить в необратимую полиорганную недостаточность. Признание непрерывности патологического процесса позволяет в ранние сроки распознать опасность развития сепсиса и полиорганной недостаточности и принимать необходимые лечебные мероприятия до развития осложнений.
Изложенные выше механизмы развития воспаления свидетельствуют о том, что синдром системного ответа (реакции) на воспаление имеет четко очерченные патофизиологические параметры. Синдром системного ответа на воспаление, развивающийся вследствие тяжелой инфекции, неотличим от синдрома, возникающего в ответ на другие повреждающие факторы, потому что в патофизиологическом механизме развития их участвуют одни и те же медиаторы воспаления. Синдром системной реакции на воспаление не может рассматриваться как сепсис, ибо в определенных границах, до повреждения иммунной системы, он, по своей сущности означает лишь полезную защитную реакцию от инфекции и других повреждающих факторов. Он становится опасным для жизни пациентов в тех случаях, когда избыточная продукция цитокинов и других медиаторов воспаления и нарушение баланса между про- и антивоспалительными медиаторами повреждают контролирующую функцию иммунной системы. В этих условиях синдром системного ответа (реакции) на воспаление может осложниться развитием сепсиса, септического шока, полиорганной недостаточности (Табл. 4).
Синдром системного ответа на воспаление
Классификация согласительной конференции американских врачей (Чикаго, 1991 г.)
Воспалительный ответ на инвазию микроорганизмов в интактные ткани макроорганизма.
Сепсис — симптомокомплекс, обусловленный постоянным или периодическим поступлением в кровь микроорганизмов из очага гнойного воспаления. В клинической картине преобладают тяжёлые полиорганные нарушения, тогда как местные воспалительные изменения выражены слабо. Характерно образование метастатических очагов гнойного воспаления в различных органах и тканях.
Классификация • Эпидемиологическая •• Внутрибольничный сепсис (послеродовый, послеоперационный, посткатетеризационный, постинъекционный, после гинекологических осмотров, сепсис новорождённых) •• Внебольничный сепсис (криптогенный, тонзиллогенный, кишечный, ожоговый) • Клиническая классификация учитывает следующие признаки: •• Этиология •• Локализация входных ворот инфекции •• Длительность ••• Молниеносный сепсис — 1–3 дня ••• Острый сепсис — до 6 нед ••• Подострый или затяжной сепсис — более 6 нед ••• Хронический сепсис (характерен для пациентов с иммунодефицитными состояниями, особенно при СПИДе) — более 6 мес •• Клиническая форма ••• Септицемия — форма сепсиса, не сопровождающаяся образованием метастатических очагов гнойной инфекции ••• Септикопиемия — форма сепсиса, характеризующаяся образованием метастатических очагов инфекции (в т.ч. инфарктов) ••• Септический (бактериальный) эндокардит. Примечание. Септицемия может трансформироваться в септикопиемию, что даёт основания считать эти формы стадиями одного процесса •• Ведущие клинико-патофизиологические синдромы ••• Тромбогеморрагический синдром (например, ДВС) ••• Септический (инфекционно-токсический) шок ••• Токсико-дистрофическое состояние.
Патогенез • Для развития сепсиса необходимо проникновение условно-патогенного возбудителя через входные ворота (чаще травмированная кожа или слизистая оболочка) с развитием местной реакции (первичного аффекта), реактивного лимфаденита (лимфангоита), гнойного тромбофлебита с последующей бактериемией и токсемией. Поражение сосудистой стенки на большом протяжении, флебиты приводят к образованию инфицированных микротромбов, обусловливающих абсцессы и инфаркты внутренних органов • Клиническая картина не зависит от этиологии, отсутствуют морфологические признаки, указывающие на специфику процесса • Глубокое нарушение обмена веществ вследствие выраженной интоксикации, преобладание процессов катаболизма (гипоальбуминемия, диспротеинемия, гипергликемия, дефицит эссенциальных жирных кислот, гиповитаминоз, метаболический ацидоз). Тяжёлые дистрофические изменения дополнительно ухудшают функции органов, что даже при отсутствии в них клинически выраженных метастазов приводит к системной полиорганной недостаточности, характерной для поздних необратимых стадий сепсиса.
Клиническая картина. Инкубационный период, цикличность течения, характерные для инфекционных заболеваний, отсутствуют. Патогномоничных признаков не существует • Интоксикационный синдром •• Вялость, анорексия, изменения психоэмоционального статуса до грубых общемозговых расстройств (коматозное состояние) •• Лихорадка (температурная кривая чаще всего неправильного типа). Подозрение на наличие сепсиса возникает при продолжительности лихорадки более 5 дней и наличии немотивированных подъёмов температуры тела до фебрильных значений с последующим падением до субфебрильных •• Признаки дистрофии и нарушения питания с развитием гипотрофии и уменьшением массы тела, снижением эластичности кожи, тургора мягких тканей • Дисфункция ЖКТ, тошнота, рвота (в т.ч. и вследствие интоксикации) • Нарушения микроциркуляции — бледность кожных покровов с землистым оттенком, геморрагическая сыпь, одышка, снижение диуреза • Гепатолиенальный синдром • Симптомы поражения органов и тканей соответственно локализации метастатических очагов или входных ворот инфекции.
Лабораторные признаки • Лейкоцитоз или лейкопения (при этиологической роли грамотрицательной флоры и СПИДе), нейтрофилёз с гиперрегенераторным сдвигом влево, прогрессирующая анемия, тромбоцитопения • Гипопротеинемия с диспротеинемией (снижение соотношения альбумины/глобулины) • Высокая концентрация белков острой фазы воспаления • Изменения коагулограммы, свидетельствующие о развитии ДВС • Лейкоцитурия, бактериурия, цилиндрурия, эритроцитурия • Положительные результаты бактериологического исследования крови (обнаружение гемокультуры), кала, мочи, ликвора. Для получения положительного результата необходим трёхкратный забор крови в объёме 20–30 мл с интервалом в 1 ч по возможности до начала антибиотикотерапии • Гиперферментемия, гипербилирубинемия при поражении соответствующих органов.
Диагностические критерии клинических форм сепсиса • Септикопиемия — обнаружение одного или нескольких очагов метастатического воспаления с идентификацией возбудителя • Септицемия — преобладают признаки интоксикационного синдрома с выраженными расстройствами микроциркуляции и центральной гемодинамики, развёрнутой клиникой тромбогеморрагического синдрома. Характерен септический (инфекционно-токсический) шок • Септический (бактериальный) эндокардит (см. Эндокардит инфекционный). Особенности инфекционного процесса: входные ворота — чаще слизистая оболочка глотки, но местный очаг (источник постоянного поступления микроорганизмов в системный кровоток) — эндокард.
ЛЕЧЕНИЕ
Тактика ведения • Госпитализация • Этиотропная терапия. До получения результатов бактериологического исследования антибиотики выбирают эмпирически • Иммуностимулирующая терапия • Дезинтоксикационная терапия (её адекватность в конечном итоге определяет прогноз), в т.ч. по показаниям экстракорпоральная дезинтоксикация: плазмаферез, гемосорбция, перфузия крови через донорские органы животных (селезёнка, печень) • Симптоматическая терапия • Лечение носит характер интенсивной терапии и дополнительно включает экстренную коррекцию расстройств функций жизненно важных органов (инфекционно-токсический шок при септицемии, декомпенсированная сердечная недостаточность при бактериальном эндокардите) • Выраженность локального воспалительного процесса любой локализации не коррелирует с тяжестью течения сепсиса. Следует учитывать, что отдалённый очаг гнойного воспаления может быть как следствием сепсиса (метастазирование), так и его причиной, что важно при определении лечебной тактики.
Лекарственная терапия
• Этиотропная терапия •• До получения результатов бактериологического исследования, особенно при неясной этиологии, наиболее эффективно сочетание гентамицина или тобрамицина 3–5 мг/кг/сут в/в и антибиотика из группы цефалоспоринов или имипенем+циластатин 500 мг в/в каждые 6 ч •• Антибиотики назначают в максимальной дозировке, в/в, в течение не менее 2 нед (несмотря на нормализацию температуры тела) •• Критерии эффективности — очевидная положительная динамика общего состояния и лабораторных показателей.
• Иммуностимулирующие препараты •• Иммуноглобулин человеческий нормальный для внутривенного введения, иммуноглобулин человеческий нормальный (IgG+IgA+IgM) для внутривенного введения •• Препараты ИФН.
• Дезинтоксикационная терапия — внутривенное введение большого количества жидкости в сочетании с диуретиками, например фуросемидом (метод форсированного диуреза) •• Количество вводимой жидкости не должно превышать объём выделенной мочи (при отсутствии у пациента признаков обезвоживания) •• Следует контролировать показатели центральной гемодинамики (АД, ЦВД) и содержание электролитов сыворотки крови и мочи •• Следует дополнительно ввести вазодилататоры.
• Симптоматическая терапия •• При анемии и тромбоцитопении — переливание крови, эритроцитарной и тромбоцитарной масс •• Противовоспалительная терапия: НПВС и ГК (следует учесть иммунодепрессивное действие ГК) •• Регидратация и парентеральное питание при выраженной дисфункции ЖКТ и тяжёлых расстройствах питания •• Купирование сердечной недостаточности и аритмий •• Противошоковые мероприятия при инфекционно-токсическом шоке (септицемия): ГК, адреномиметические средства, плазмозамещающие препараты, например полиглюкин.
Оперативное лечение при наличии доступного оперативному вмешательству очага гнойной инфекции.
Синоним. Инфекция общая гнойная
МКБ-10 • O85 Послеродовой сепсис • P36 Бактериальный сепсис новорождённого • T80.2 Инфекции, связанные с инфузией, трансфузией и лечебной инъекцией
Код вставки на сайт
Сепсис — симптомокомплекс, обусловленный постоянным или периодическим поступлением в кровь микроорганизмов из очага гнойного воспаления. В клинической картине преобладают тяжёлые полиорганные нарушения, тогда как местные воспалительные изменения выражены слабо. Характерно образование метастатических очагов гнойного воспаления в различных органах и тканях.
Классификация • Эпидемиологическая •• Внутрибольничный сепсис (послеродовый, послеоперационный, посткатетеризационный, постинъекционный, после гинекологических осмотров, сепсис новорождённых) •• Внебольничный сепсис (криптогенный, тонзиллогенный, кишечный, ожоговый) • Клиническая классификация учитывает следующие признаки: •• Этиология •• Локализация входных ворот инфекции •• Длительность ••• Молниеносный сепсис — 1–3 дня ••• Острый сепсис — до 6 нед ••• Подострый или затяжной сепсис — более 6 нед ••• Хронический сепсис (характерен для пациентов с иммунодефицитными состояниями, особенно при СПИДе) — более 6 мес •• Клиническая форма ••• Септицемия — форма сепсиса, не сопровождающаяся образованием метастатических очагов гнойной инфекции ••• Септикопиемия — форма сепсиса, характеризующаяся образованием метастатических очагов инфекции (в т.ч. инфарктов) ••• Септический (бактериальный) эндокардит. Примечание. Септицемия может трансформироваться в септикопиемию, что даёт основания считать эти формы стадиями одного процесса •• Ведущие клинико-патофизиологические синдромы ••• Тромбогеморрагический синдром (например, ДВС) ••• Септический (инфекционно-токсический) шок ••• Токсико-дистрофическое состояние.
Патогенез • Для развития сепсиса необходимо проникновение условно-патогенного возбудителя через входные ворота (чаще травмированная кожа или слизистая оболочка) с развитием местной реакции (первичного аффекта), реактивного лимфаденита (лимфангоита), гнойного тромбофлебита с последующей бактериемией и токсемией. Поражение сосудистой стенки на большом протяжении, флебиты приводят к образованию инфицированных микротромбов, обусловливающих абсцессы и инфаркты внутренних органов • Клиническая картина не зависит от этиологии, отсутствуют морфологические признаки, указывающие на специфику процесса • Глубокое нарушение обмена веществ вследствие выраженной интоксикации, преобладание процессов катаболизма (гипоальбуминемия, диспротеинемия, гипергликемия, дефицит эссенциальных жирных кислот, гиповитаминоз, метаболический ацидоз). Тяжёлые дистрофические изменения дополнительно ухудшают функции органов, что даже при отсутствии в них клинически выраженных метастазов приводит к системной полиорганной недостаточности, характерной для поздних необратимых стадий сепсиса.
Клиническая картина. Инкубационный период, цикличность течения, характерные для инфекционных заболеваний, отсутствуют. Патогномоничных признаков не существует • Интоксикационный синдром •• Вялость, анорексия, изменения психоэмоционального статуса до грубых общемозговых расстройств (коматозное состояние) •• Лихорадка (температурная кривая чаще всего неправильного типа). Подозрение на наличие сепсиса возникает при продолжительности лихорадки более 5 дней и наличии немотивированных подъёмов температуры тела до фебрильных значений с последующим падением до субфебрильных •• Признаки дистрофии и нарушения питания с развитием гипотрофии и уменьшением массы тела, снижением эластичности кожи, тургора мягких тканей • Дисфункция ЖКТ, тошнота, рвота (в т.ч. и вследствие интоксикации) • Нарушения микроциркуляции — бледность кожных покровов с землистым оттенком, геморрагическая сыпь, одышка, снижение диуреза • Гепатолиенальный синдром • Симптомы поражения органов и тканей соответственно локализации метастатических очагов или входных ворот инфекции.
Лабораторные признаки • Лейкоцитоз или лейкопения (при этиологической роли грамотрицательной флоры и СПИДе), нейтрофилёз с гиперрегенераторным сдвигом влево, прогрессирующая анемия, тромбоцитопения • Гипопротеинемия с диспротеинемией (снижение соотношения альбумины/глобулины) • Высокая концентрация белков острой фазы воспаления • Изменения коагулограммы, свидетельствующие о развитии ДВС • Лейкоцитурия, бактериурия, цилиндрурия, эритроцитурия • Положительные результаты бактериологического исследования крови (обнаружение гемокультуры), кала, мочи, ликвора. Для получения положительного результата необходим трёхкратный забор крови в объёме 20–30 мл с интервалом в 1 ч по возможности до начала антибиотикотерапии • Гиперферментемия, гипербилирубинемия при поражении соответствующих органов.
Диагностические критерии клинических форм сепсиса • Септикопиемия — обнаружение одного или нескольких очагов метастатического воспаления с идентификацией возбудителя • Септицемия — преобладают признаки интоксикационного синдрома с выраженными расстройствами микроциркуляции и центральной гемодинамики, развёрнутой клиникой тромбогеморрагического синдрома. Характерен септический (инфекционно-токсический) шок • Септический (бактериальный) эндокардит (см. Эндокардит инфекционный). Особенности инфекционного процесса: входные ворота — чаще слизистая оболочка глотки, но местный очаг (источник постоянного поступления микроорганизмов в системный кровоток) — эндокард.
ЛЕЧЕНИЕ
Тактика ведения • Госпитализация • Этиотропная терапия. До получения результатов бактериологического исследования антибиотики выбирают эмпирически • Иммуностимулирующая терапия • Дезинтоксикационная терапия (её адекватность в конечном итоге определяет прогноз), в т.ч. по показаниям экстракорпоральная дезинтоксикация: плазмаферез, гемосорбция, перфузия крови через донорские органы животных (селезёнка, печень) • Симптоматическая терапия • Лечение носит характер интенсивной терапии и дополнительно включает экстренную коррекцию расстройств функций жизненно важных органов (инфекционно-токсический шок при септицемии, декомпенсированная сердечная недостаточность при бактериальном эндокардите) • Выраженность локального воспалительного процесса любой локализации не коррелирует с тяжестью течения сепсиса. Следует учитывать, что отдалённый очаг гнойного воспаления может быть как следствием сепсиса (метастазирование), так и его причиной, что важно при определении лечебной тактики.
Лекарственная терапия
• Этиотропная терапия •• До получения результатов бактериологического исследования, особенно при неясной этиологии, наиболее эффективно сочетание гентамицина или тобрамицина 3–5 мг/кг/сут в/в и антибиотика из группы цефалоспоринов или имипенем+циластатин 500 мг в/в каждые 6 ч •• Антибиотики назначают в максимальной дозировке, в/в, в течение не менее 2 нед (несмотря на нормализацию температуры тела) •• Критерии эффективности — очевидная положительная динамика общего состояния и лабораторных показателей.
• Иммуностимулирующие препараты •• Иммуноглобулин человеческий нормальный для внутривенного введения, иммуноглобулин человеческий нормальный (IgG+IgA+IgM) для внутривенного введения •• Препараты ИФН.
• Дезинтоксикационная терапия — внутривенное введение большого количества жидкости в сочетании с диуретиками, например фуросемидом (метод форсированного диуреза) •• Количество вводимой жидкости не должно превышать объём выделенной мочи (при отсутствии у пациента признаков обезвоживания) •• Следует контролировать показатели центральной гемодинамики (АД, ЦВД) и содержание электролитов сыворотки крови и мочи •• Следует дополнительно ввести вазодилататоры.
• Симптоматическая терапия •• При анемии и тромбоцитопении — переливание крови, эритроцитарной и тромбоцитарной масс •• Противовоспалительная терапия: НПВС и ГК (следует учесть иммунодепрессивное действие ГК) •• Регидратация и парентеральное питание при выраженной дисфункции ЖКТ и тяжёлых расстройствах питания •• Купирование сердечной недостаточности и аритмий •• Противошоковые мероприятия при инфекционно-токсическом шоке (септицемия): ГК, адреномиметические средства, плазмозамещающие препараты, например полиглюкин.
Оперативное лечение при наличии доступного оперативному вмешательству очага гнойной инфекции.
Синоним. Инфекция общая гнойная
МКБ-10 • O85 Послеродовой сепсис • P36 Бактериальный сепсис новорождённого • T80.2 Инфекции, связанные с инфузией, трансфузией и лечебной инъекцией
Септический шок – это тяжелое патологическое состояние, возникающее при массивном поступлении в кровь бактериальных эндотоксинов. Сопровождается тканевой гипоперфузией, критическим снижением артериального давления и симптомами полиорганной недостаточности. Диагноз ставится на основании общей клинической картины, сочетающей в себе признаки поражения легких, сердечно-сосудистой системы (ССС), печени и почек, централизации кровообращения. Лечение: массивная антибиотикотерапия, инфузия коллоидных и кристаллоидных растворов, поддержание деятельности ССС за счёт введения вазопрессоров, коррекция респираторных нарушений путем ИВЛ.
МКБ-10
Общие сведения
Септический шок (СШ) также называют инфекционно-токсическим (ИТШ). Как самостоятельная нозологическая единица патология впервые была описана в XIX веке, однако полноценное изучение с разработкой специфических противошоковых мер началось не более 25 лет назад. Может возникать при любом инфекционном процессе. Наиболее часто встречается у пациентов хирургических отделений, при менингококковой септицемии, брюшном тифе, сальмонеллезе и чуме. Распространен в странах, где диагностируется наибольшее количество бактериальных и паразитарных заболеваний (Африка, Афганистан, Индонезия). Ежегодно от ИТШ погибает более 500 тысяч человек по всему миру.

Причины
В абсолютном большинстве случаев патология развивается на фоне ослабления иммунных реакций. Это происходит у пациентов, страдающих хроническими тяжелыми заболеваниями, а также у людей пожилого возраста. В силу физиологических особенностей сепсис чаще диагностируется у мужчин. Список самых распространенных заболеваний, при которых могут возникать явления ИТШ, включает в себя:
- Очаги гнойной инфекции. Признаки системной воспалительной реакции и связанных с ней нарушений в работе внутренних органов отмечаются при наличии объемных абсцессов или флегмоны мягких тканей. Риск генерализованного токсического ответа повышается при длительном течении болезни, отсутствии адекватной антибактериальной терапии и возрасте пациента старше 60 лет.
- Длительное пребывание в ОРИТ. Госпитализация в отделение реанимации и интенсивной терапии всегда сопряжена с риском возникновения сепсиса и инфекционного шока. Это обусловлено постоянным контактом с резистентной к антибактериальным препаратам микрофлорой, ослаблением защитных сил организма в результате тяжёлой болезни, наличием множественных ворот инфекции: катетеров, желудочных зондов, дренажных трубок.
- Раны. Нарушения целостности кожных покровов, в том числе возникшие во время операции, существенно повышают риски инфицирования высококонтагиозной флорой. ИТШ начинается у больных с загрязненными ранами, не получивших своевременной помощи. Травматизация тканей в ходе оперативного вмешательства становится причиной генерализованной инфекции только при несоблюдении правил асептики и антисептики. В большинстве случаев септический шок возникает у пациентов, перенесших манипуляции на желудке и поджелудочной железе. Еще одна распространенная причина – разлитой перитонит.
- Приём иммунодепрессантов. Лекарственные средства, угнетающие иммунитет (меркаптопурин, кризанол), используются для подавления реакции отторжения после трансплантации органов. В меньшей степени уровень собственной защиты снижается при употреблении химиотерапевтических средств – цитостатиков, предназначенных для лечения онкологических заболеваний (доксорубицина, фторурацила).
- СПИД.ВИЧ-инфекция в стадии СПИДа приводит к развитию нетипичного сепсиса, спровоцированного не бактериальный культурой, а грибком рода Candida. Клинические проявления болезни характеризуется малой степенью выраженности. Отсутствие адекватного иммунного ответа позволяет патогенной флоре свободно размножаться.
Возбудитель сепсиса – грамположительные (стрептококки, стафилококки, энтерококки) и грамотрицательные (Enterobacter cloacae, Clostridium pneumoniae) бактерии. Во многих случаях культуры нечувствительны к антибиотикам, что затрудняет лечение пациентов. Септический шок вирусного происхождения в настоящее время вызывает споры специалистов. Одни представители научного мира утверждают, что вирусы неспособны стать причиной патологии, другие – что внеклеточная форма жизни может спровоцировать системную воспалительную реакцию, являющуюся патогенетической основой ИТШ.
Патогенез
В основе симптомов лежит неконтролируемое распространение медиаторов воспаления из патологического очага. При этом происходит активация макрофагов, лимфоцитов и нейтрофилов. Возникает синдром системного воспалительного ответа. На фоне этого снижается периферический сосудистый тонус, объем циркулирующей крови падает за счет повышения проницаемости сосудов и застоя жидкости в микроциркуляторном русле. Дальнейшие изменения обусловлены резким уменьшением перфузии. Недостаточное кровоснабжение становится причиной гипоксии, ишемии внутренних органов и нарушения их функции. Наиболее чувствителен головной мозг. Кроме того, ухудшается функциональная активность легких, почек и печени.
Помимо СВР в формировании септического шока важную роль играет эндогенная интоксикация. В связи со снижением работоспособности экскреторных систем в крови накапливаются продукты нормального обмена веществ: креатинин, мочевина, лактат, гуанин и пируват. Во внутренних средах повышается концентрация промежуточных результатов окисления липидов (скатол, альдегиды, кетоны) и бактериальных эндотоксинов. Всё это вызывает тяжелые изменения гомеостаза, расстройства кислотно-щелочного баланса, нарушения в работе рецепторных систем.
Классификация
Симптомы септического шока
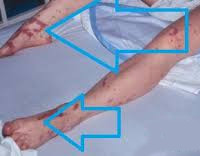
90% случаев СШ сопровождается дыхательной недостаточностью различной степени тяжести. Пациенты с декомпенсированным и терминальным течением болезни нуждаются в аппаратной респираторной поддержке. Печень и селезенка увеличены, уплотнены, их функция нарушена. Может отмечаться атония кишечника, метеоризм, стул с примесью слизи, крови и гноя. На поздних стадиях возникают симптомы диссеминированного внутрисосудистого свертывания: петехиальная сыпь, внутреннее и наружное кровотечения.
Осложнения
Септический шок приводит к ряду тяжелых осложнений. Наиболее распространённым из них считается полиорганная недостаточность, при которой нарушается функция двух и более систем. В первую очередь страдает ЦНС, легкие, почки и сердце. Несколько реже встречается поражение печени, кишечника и селезенки. Летальность среди пациентов с ПОН достигает 60%. Часть из них погибает на 3-5 сутки после выведения из критического состояния. Это обусловлено органическими изменениями во внутренних структурах.
Еще одним распространенным последствием ИТШ являются кровотечения. При формировании внутримозговых гематом у пациента развивается клиника острого геморрагического инсульта. Скопление экстравазата в других органах может приводить к их сдавлению. Уменьшение объема крови в сосудистом русле потенцирует более значимое снижение артериального давления. ДВС на фоне инфекционно-токсического шока становится причиной гибели пациента в 40-45% случаев. Вторичное поражение органов, спровоцированное микротромбозами, возникающими на начальном этапе формирования коагулопатии, отмечается практически у 100% больных.
Диагностика
- Осмотр и физикальное исследование. Реализуется непосредственно лечащим врачом. Специалист обнаруживает характерные клинические признаки шокового состояния. Для этого проводится тонометрия, визуальная оценка цвета кожных покровов, особенностей дыхательных движений, подсчет пульса и ЧДД, аускультация сердца и легких. При подозрении на наличие осложнений необходима оценка неврологического статуса на предмет симптоматики кровоизлияния в мозг.
- Аппаратное исследование. Имеет вспомогательное значение. Пациенту показан контроль состояния с использованием анестезиологического монитора. На экран устройства выводится информация о величине артериального давления, частоте сердечных сокращений, степени насыщения крови кислородом (при легочной недостаточности SpO2<90%) и коронарном ритме. На фоне нарушений дыхания и токсического поражения миокарда может отмечаться тахикардия, аритмия и блокады внутрисердечной проводимости.
- Лабораторное исследование. Позволяет выявить имеющиеся нарушения гомеостаза, сбои в работе внутренних органов. У пациентов с шоком септического происхождения обнаруживается повышенный уровень креатинина (> 0,177 ммоль/л), билирубина (>34,2 мкмоль/л), лактата (>2 ммоль/л). О нарушении коагуляции свидетельствует тромбоцитопения (
Лечение септического шока
Пациентам показана интенсивная терапия. Лечение проводят в отделениях ОРИТ с использованием методов аппаратной и медикаментозной поддержки. Лечащий врач – реаниматолог. Может потребоваться консультация инфекциониста, кардиолога, гастроэнтеролога и других специалистов. Требуется перевод больного на искусственную вентиляцию лёгких, круглосуточное наблюдение среднего медицинского персонала, парентеральное кормление. Смеси и продукты, предназначенные для введения в желудок, не используются. Все методы воздействия условно делятся на патогенетические и симптоматические:
- Патогенетическое лечение. При подозрении на наличие сепсиса больному назначают антибиотики. Схема должна включать в себя 2-3 препарата различных групп, обладающих широким спектром действия. Подбор медикамента на начальном этапе проводят эмпирическим путем, в соответствии с предполагаемой чувствительностью возбудителя. Одновременно с этим производят забор крови на стерильность и восприимчивость к антибиотикам. Результат анализа готовится в течение 10 дней. Если к этому времени подобрать эффективную лекарственную схему не удалось, следует использовать данные исследования.
- Симптоматическое лечение. Подбирается с учетом имеющейся клинической картины. Обычно больные получают массивную инфузионную терапию, глюкокортикостероиды, инотропные средства, антиагреганты или гемостатики (в зависимости от состояния свертывающей системы крови). При тяжелом течении болезни используют препараты крови: свежезамороженную плазму, альбумин, иммуноглобулины. Если пациент находится в сознании, показано введение анальгетических и седативных лекарств.
Прогноз и профилактика
Септический шок имеет неблагоприятный прогноз для жизни. При субкомпенсированном течении погибает около 40% больных. Декомпенсированная и терминальная разновидности оканчиваются гибелью 60% пациентов. При отсутствии своевременной медицинской помощи смертность достигает 95-100%. Часть больных умирает через несколько дней после устранения патологического состояния. Профилактика ИТШ заключается в своевременном купировании очагов инфекции, грамотном подборе антибиотикотерапии у хирургических больных, соблюдении антисептических требований в отделениях, занимающихся инвазивным манипуляциями, поддержке адекватного иммунного статуса у представителей ВИЧ-инфицированной прослойки населения.
2. Тактика ведения пациентов с сепсисом и септическим шоком в многопрофильном стационаре/ Сапичева Ю.Ю., Лихванцев В.В. – 2015.
Термин "сепсис" был введен в 4 веке до н. э. Аристотелем, который понимал под ним отравление организма продуктами гниения собственных тканей. В настоящее время определение сепсиса следующее.
Сепсис – это тяжелое инфекционное заболевание, вызываемое разными возбудителями и их токсинами, проявляющееся своеобразной реакцией организма с однотипной клинической картиной. Возбудителями сепсиса могут быть бактерии (90%), грибы, простейшие и вирусы.
Под термином "хирургический сепсис" следует понимать тяжелое общее заболевание, возникающее на фоне существующего очага инфекции, изменений иммунореактивности организма и требующее местного хирургического и общего интенсивного лечения.
Сепсис не является заразной болезнью в эпидемиологическом отношении, не формирует иммунитет и не имеет определенных сроков инкубационного периода. Так как причиной сепсиса являются различные возбудители, то он является синонимом понятия "диссеминированная инфекция", которую от обычного инфекционного процесса отличает полиэтиологический или клинический характер вне зависимости от возбудителя, с возможной его сменой в течение болезни.
В среднем сепсис развивается у 1-5 больных на 1000 госпитализированных в зависимости от профиля лечебного учреждения.
В США ежегодно регистрируется от 400 до 500 тыс. случаев сепсиса, умирает 215 тыс. человек. Затраты на лечение одного пациента составляют 22 100 долларов США, а ежегодные затраты – 16,7 млрд. долларов. (Ж. Хирургия № 9, 2002 г., с. 52).
Сепсис. Терминология
Первичный очаг – участок воспаления, возникающий на месте внедрения инфекции: раны (травматические, операционные), местные гнойные процессы (фурункулы, карбункулы, абсцессы и др.);
Вторичный очаг возникает при распространении инфекции за пределы первичного очага в различные органы и ткани, отдаленные от места внедрения инфекции;
Вторичный сепсис развивается на фоне гнойного очага (раны, гнойного хирургического заболевания, оперативного вмешательства).
Преобладающий возбудитель – стафилококк. В последнее время возросла роль Гр (-) флоры (синегнойная палочка, протей, кишечная палочка).
Причинами роста Гр (-) сепсиса и возрастания роли условно патогенной флоры следует считать снижение сопротивляемости организма, расширение объема и увеличение тяжести оперативных вмешательств, а также широкое и часто бессистемное применение антибиотиков.
Возбудитель особенно "опасен" в первичном и вторичном очагах; именно здесь он "гнездится", воздействует на ткани и отсюда происходит всасывание бактериальных токсинов и продуктов распада тканей.
В последнее десятилетие представления о механизмах воспалительной реакции претерпели существенные изменения. Благодаря успехам молекулярной биологии был выделен новый класс медиаторов воспаления.
Фактор агрегации тромбоцитов;
Активированные эндотелиальные клетки.
Было показано, что в развитии воспалительной реакции ведущая роль принадлежит цитокинам, оксиду азота (NO), фактору агрегации тромбоцитов, активированным эндотелиальным клеткам.
Цитокины продуцируются моноцитами, макрофагами, нейтрофильными лейкоцитами, лимфоцитами, клетками эндотелия, фибробластами.
Цитокины, продуцируемые лейкоцитами, называют интерлейкинами (ИЛ), потому, что, с одной стороны, они продуцируются лейкоцитами, с другой – лейкоциты являются клетками-мишенями для ИЛ. Известно более 20 цитокинов, из них 15 относятся к ИЛ.
Цитокины обеспечивают взаимодействие между клетками, активно участвующими в развитии местной и общей реакции на воспаление, путем усиления или угнетения их функции.
Исследованиями, проведенными в разных лабораториях, было убедительно подтверждено, что воспаление и ответная реакция на него развиваются по одним и тем же закономерностям, как при внедрении инфекции, так и при воздействии механической травмы, ожогов и ряда других факторов.
Цитокиновая система включает в себя 5 обширных классов, объединенных по их доминирующему действию на другие клетки:
провоспалительные (ИЛ 1, 6, 8, 12);
антивоспалительные (ИЛ 4, 10, 11, 13 и др.).
Фактор некроза опухоли (ФНО).
Факторы роста и дифференцировки лимфоцитов.
Факторы, стимулирующие рост колоний макрофагов и гранулоцитов.
Факторы, вызывающие рост мезенхимальных клеток. Большинство реакций при воспалении осуществляется через посредничество цитокинов.
Продукция цитокинов зависит от состояния организма. В норме их секреция ничтожно мала, предназначена для обеспечения взаимодействия между продуцирующими их клетками и другими медиаторами воспаления. Но она резко возрастает при воспалении в связи с активацией клеток, вырабатывающих их. Активация клеток, продуцирующих цитокины, происходит под влиянием эндотоксинов, микроорганизмов, гипоксии, значительной травмы, наличия нежизнеспособных тканей, шока, неизбежно сопровождающихся гипоксией.
Нормально функционирующие механизмы иммунной системы препятствуют бесконтрольному выделению цитокинов и других медиаторов воспаления, обеспечивают адекватную реакцию организма на воспаление. В крови в самом начале воспаления одновременно появляются про- и антивоспалительные ИЛ. При этих условиях они в функциональном отношении создают равновесие, определяющее благоприятное течение воспалительного процесса, отграничение очага воспаления (повреждения).
При нормальном иммунном гомеостазе благоприятное действие медиаторов воспаления преобладает над их повреждающим действием. Реакция жизненно важных систем организма на воспаление носит умеренный адекватный характер, без признаков системной реакции, без дисфункции органов.
При массивной бактериальной агрессии, тяжелой травме (в том числе хирургической), наличии очагов некроза, нежизнеспособных тканей, при остром панкреатите происходит гиперактивация макрофагов, нейтрофилов и других клеток. В связи с этим резко возрастает продукция и содержание цитокинов в крови и в клетках, продуцирующих их, нарушается баланс между про- и антивоспалительными цитокинами и другими медиаторами. В результате этого повреждается иммунная система. Она перестает контролировать секрецию цитокинов и других медиаторов воспаления. Повреждающее действие медиаторов воспаления начинает превалировать над защитным. Дезорганизация функции иммунной системы, потеря контроля над продукцией цитокинов и других медиаторов воспаления, приводят к тому, что про- и антивоспалительные цитокины и другие медиаторы воспаления (NO, О2, простагландин Е2) вместо ограничения воспалительного процесса и защиты организма начинают оказывать деструктивное, повреждающее действие на ткани не только в очаге инфекции, но и в других органах. В результате этого поверхность эндотелия приобретает повышенную тромбогенность и адгезивность, возникают микротромбозы, развивается ДВС-синдром, нарушается микроциркуляция, возникают массивная вазодилатация, переполнение венозного русла, резкое повышение проницаемости сосудистой стенки, гипоксия тканей. Развиваются отеки и гиповолемия, нарушается кровоснабжение жизненно важных органов, возникает их дисфункция, которая при определенных условиях может переходить в необратимую полиорганную недостаточность. Признание непрерывности патологического процесса позволяет в ранние сроки распознать опасность развития сепсиса и полиорганной недостаточности и принимать необходимые лечебные мероприятия до развития осложнений.
Изложенные выше механизмы развития воспаления свидетельствуют о том, что синдром системного ответа (реакции) на воспаление имеет четко очерченные патофизиологические параметры. Синдром системного ответа на воспаление, развивающийся вследствие тяжелой инфекции, неотличим от синдрома, возникающего в ответ на другие повреждающие факторы, потому что в патофизиологическом механизме развития их участвуют одни и те же медиаторы воспаления. Синдром системной реакции на воспаление не может рассматриваться как сепсис, ибо в определенных границах, до повреждения иммунной системы, он, по своей сущности означает лишь полезную защитную реакцию от инфекции и других повреждающих факторов. Он становится опасным для жизни пациентов в тех случаях, когда избыточная продукция цитокинов и других медиаторов воспаления и нарушение баланса между про- и антивоспалительными медиаторами повреждают контролирующую функцию иммунной системы. В этих условиях синдром системного ответа (реакции) на воспаление может осложниться развитием сепсиса, септического шока, полиорганной недостаточности (Табл. 4).
Синдром системного ответа на воспаление
Классификация согласительной конференции американских врачей (Чикаго, 1991 г.)
Воспалительный ответ на инвазию микроорганизмов в интактные ткани макроорганизма.
Сепсис (общая хирургическая инфекция) – это тяжелое заболевание, обусловленное генерализацией гнойного процесса и циркуляцией в кровеносном русле микробов и их токсинов. Летальность при сепсисе достигает 50–70%.
В развитии сепсиса решающее значение имеют 3 фактора:
обширные инфицированные раны (посттравматические, ожоговые);
гнойные заболевания мягких тканей, полостей, костей и суставов;
послеоперационные инфицированные раны;
хронические эндогенные очаги инфекции (кариесные зубы, хронический гайморит, хронический тонзиллит и т.д.).
2. Микробный фактор – сепсис развивается при наличии высоковирулентной микрофлоры: стафилококки, стрептококки, анаэробная и смешанная флора.
3. Реактивность организма – сепсис развивается чаще всего у ослабленных больных, перенесших тяжелые заболевания и травматичные операции, у которых снижены иммунные силы.
Классификация:
1. По виду возбудителя: стафилококковый, стрептококковый, анаэробный, колибациллярный, протейный и т.д.
2. По происхождению:
раневой – при обширных инфицированных ранах;
абдоминальный – при перитонитах, абсцессах брюшной полости;
гинекологический – при острых воспалительных заболеваниях внутренних женских половых органов, после родов;
уросепсис – при острой инфекции мочевыводящей системы;
послеоперационный – вследствие послеоперационных гнойных осложнений;
имплантационный – при инфицировании вводимых или оставляемых в организме материалов (устройства для металлоостеосинтеза переломов, сосудистые протезы, клапаны сердца и т.д.);
3. По клиническому течению:
4. По стадиям развития:
токсико-резорбтивная лихорадка – начальная стадия сепсиса, микроорганизмов в кровеносном русле еще нет, но уже циркулируют их токсины и продукты распада тканей (токсемия);
септицемия – в кровеносном русле циркулирует возбудитель сепсиса;
септикопиемия – в различных органах и тканях организма формируются дочерние (метастатические) гнойники.
Клиническая картина сепсиса накладывается на проявления основного заболевания, при этом основное заболевание, или местный гнойный процесс, имеет затяжное течение, с продолжающимся некрозом тканей, скудным отделяемым, с гнойными плохо дренирующимися затеками, отсутствием или вялыми грануляциями в ране. При этом местный гнойный процесс не купируется или прогрессирует. Отмечаются лимфаденит, лимфангоит, тромбофлебиты.
Общими проявлениями развития сепсиса являются: повышение температуры до 39 – 40 градусов постоянного или гектического характера с ознобами. Быстро развиваются общая слабость, адинамия, тахикардия, падает АД, в анализах крови выявляются анемия, лейкоцитоз, сдвиг лейкоформулы влево, растет лейкоцитарный индекс интоксикации, резко повышается СОЭ до 25 – 50 мм/час и более. Характерно увеличение селезенки (септическая селезенка), увеличение печени и гипербилирубинемия (токсический гепатит), острая почечная недостаточность (олигурия, протеинурия, уремия). Нередко развиваются септическая пневмония, септический эндомиокардит, полисерозит, ДВС-синдром.
Основные клинические проявления сепсиса развиваются: в течение первых 3 суток – при молниеносной форме, в первые 2 недели основного заболевания – при острой форме, в течение 2 - 4 недель – при подострой форме. О хрониосепсисе можно говорить при длительном сохранении субфебрильной температуры – до 3 месяцев и более.
Диагностика:
1. Хирургическая санация первичного и вторичных очагов инфекции. При этом раны широко раскрываются, проводится некрэктомия, вскрываются гнойные затеки, рана ведется открыто или гнойная полость широко дренируется, при этом лучше всего установить проточно-аспирационную систему дренажей.
2. Тщательная антисептическая обработка гнойного очага. Полость гнойника обильно промывается растворами фурациллина, физраствором с антибиотиками, перекисью водорода, водным раствором хлоргексидина, раствором гипохлорита-натрия и т.д.
3. Антибактериальная терапия. При сепсисе назначаются антибиотики широкого спектра – аминогликозиды, цефалоспорины, комбинация антибиотиков. Назначаются препараты, воздействующие на анаэробную флору – метрагил, метронидазол, трихопол. Антибактериальные препараты вводятся внутривенно, а также эндолимфатически.
Препаратом выбора при лечении сепсиса является новый антибиотик тиенам, обладающий необычайно широким спектром действия, ввиду чего его можно назначать сразу, до получения результатов бактериологических исследований на чувствительность микрофлоры, что особенно важно при гнойно-септических процессах.
4. Дезинтоксикационная терапия – включает переливание растворов глюкозы, гемодеза, инфузионную терапию на фоне стимуляции диуреза.
5. Гемотрансфузионная терапия: при сепсисе показано переливание крови, плазмы, лейковзвеси. Эффективно переливание препаратов крови – альбумина, растворов аминокислот.
6. Иммуностимуляция – используют иммуноглобулин, антистафилококковый гамма-глобулин, тималин, ретаболил, кортикостероидные гормоны.
7. Антигипоксическая терапия – при сепсисе эффективно применение гипербарической оксигенации (ГБО-терапия), внутривенной инфузии гипохлорита натрия.
8. Ингибиторы протеаз – при сепсисе необходимо инактивировать освобождающиеся протеолитические ферменты. С этой целью назначают контрикал, гордокс, трасилол.
9. Стимуляция функций жизненно важных органов: сердечные препараты, воздействие на легкие, гепатопротекторы, стимуляция деятельности желудочно-кишечного тракта и др.
10. Гравитационная хирургия – занимает при сепсисе важное место, включает ультрафиолетовое облучение крови, внутрисосудистое лазерное облучение крови, гемосорбцию, перитонеальный диализ, лимфосорбцию, плазмаферез, ксеногемосорбцию.
Читайте также:

