Сепсис тонзиллогенный что это такое
Обновлено: 19.04.2024
Сепсис — симптомокомплекс, обусловленный постоянным или периодическим поступлением в кровь микроорганизмов из очага гнойного воспаления. В клинической картине преобладают тяжёлые полиорганные нарушения, тогда как местные воспалительные изменения выражены слабо. Характерно образование метастатических очагов гнойного воспаления в различных органах и тканях.
Классификация • Эпидемиологическая •• Внутрибольничный сепсис (послеродовый, послеоперационный, посткатетеризационный, постинъекционный, после гинекологических осмотров, сепсис новорождённых) •• Внебольничный сепсис (криптогенный, тонзиллогенный, кишечный, ожоговый) • Клиническая классификация учитывает следующие признаки: •• Этиология •• Локализация входных ворот инфекции •• Длительность ••• Молниеносный сепсис — 1–3 дня ••• Острый сепсис — до 6 нед ••• Подострый или затяжной сепсис — более 6 нед ••• Хронический сепсис (характерен для пациентов с иммунодефицитными состояниями, особенно при СПИДе) — более 6 мес •• Клиническая форма ••• Септицемия — форма сепсиса, не сопровождающаяся образованием метастатических очагов гнойной инфекции ••• Септикопиемия — форма сепсиса, характеризующаяся образованием метастатических очагов инфекции (в т.ч. инфарктов) ••• Септический (бактериальный) эндокардит. Примечание. Септицемия может трансформироваться в септикопиемию, что даёт основания считать эти формы стадиями одного процесса •• Ведущие клинико-патофизиологические синдромы ••• Тромбогеморрагический синдром (например, ДВС) ••• Септический (инфекционно-токсический) шок ••• Токсико-дистрофическое состояние.
Патогенез • Для развития сепсиса необходимо проникновение условно-патогенного возбудителя через входные ворота (чаще травмированная кожа или слизистая оболочка) с развитием местной реакции (первичного аффекта), реактивного лимфаденита (лимфангоита), гнойного тромбофлебита с последующей бактериемией и токсемией. Поражение сосудистой стенки на большом протяжении, флебиты приводят к образованию инфицированных микротромбов, обусловливающих абсцессы и инфаркты внутренних органов • Клиническая картина не зависит от этиологии, отсутствуют морфологические признаки, указывающие на специфику процесса • Глубокое нарушение обмена веществ вследствие выраженной интоксикации, преобладание процессов катаболизма (гипоальбуминемия, диспротеинемия, гипергликемия, дефицит эссенциальных жирных кислот, гиповитаминоз, метаболический ацидоз). Тяжёлые дистрофические изменения дополнительно ухудшают функции органов, что даже при отсутствии в них клинически выраженных метастазов приводит к системной полиорганной недостаточности, характерной для поздних необратимых стадий сепсиса.
Клиническая картина. Инкубационный период, цикличность течения, характерные для инфекционных заболеваний, отсутствуют. Патогномоничных признаков не существует • Интоксикационный синдром •• Вялость, анорексия, изменения психоэмоционального статуса до грубых общемозговых расстройств (коматозное состояние) •• Лихорадка (температурная кривая чаще всего неправильного типа). Подозрение на наличие сепсиса возникает при продолжительности лихорадки более 5 дней и наличии немотивированных подъёмов температуры тела до фебрильных значений с последующим падением до субфебрильных •• Признаки дистрофии и нарушения питания с развитием гипотрофии и уменьшением массы тела, снижением эластичности кожи, тургора мягких тканей • Дисфункция ЖКТ, тошнота, рвота (в т.ч. и вследствие интоксикации) • Нарушения микроциркуляции — бледность кожных покровов с землистым оттенком, геморрагическая сыпь, одышка, снижение диуреза • Гепатолиенальный синдром • Симптомы поражения органов и тканей соответственно локализации метастатических очагов или входных ворот инфекции.
Лабораторные признаки • Лейкоцитоз или лейкопения (при этиологической роли грамотрицательной флоры и СПИДе), нейтрофилёз с гиперрегенераторным сдвигом влево, прогрессирующая анемия, тромбоцитопения • Гипопротеинемия с диспротеинемией (снижение соотношения альбумины/глобулины) • Высокая концентрация белков острой фазы воспаления • Изменения коагулограммы, свидетельствующие о развитии ДВС • Лейкоцитурия, бактериурия, цилиндрурия, эритроцитурия • Положительные результаты бактериологического исследования крови (обнаружение гемокультуры), кала, мочи, ликвора. Для получения положительного результата необходим трёхкратный забор крови в объёме 20–30 мл с интервалом в 1 ч по возможности до начала антибиотикотерапии • Гиперферментемия, гипербилирубинемия при поражении соответствующих органов.
Диагностические критерии клинических форм сепсиса • Септикопиемия — обнаружение одного или нескольких очагов метастатического воспаления с идентификацией возбудителя • Септицемия — преобладают признаки интоксикационного синдрома с выраженными расстройствами микроциркуляции и центральной гемодинамики, развёрнутой клиникой тромбогеморрагического синдрома. Характерен септический (инфекционно-токсический) шок • Септический (бактериальный) эндокардит (см. Эндокардит инфекционный). Особенности инфекционного процесса: входные ворота — чаще слизистая оболочка глотки, но местный очаг (источник постоянного поступления микроорганизмов в системный кровоток) — эндокард.
ЛЕЧЕНИЕ
Тактика ведения • Госпитализация • Этиотропная терапия. До получения результатов бактериологического исследования антибиотики выбирают эмпирически • Иммуностимулирующая терапия • Дезинтоксикационная терапия (её адекватность в конечном итоге определяет прогноз), в т.ч. по показаниям экстракорпоральная дезинтоксикация: плазмаферез, гемосорбция, перфузия крови через донорские органы животных (селезёнка, печень) • Симптоматическая терапия • Лечение носит характер интенсивной терапии и дополнительно включает экстренную коррекцию расстройств функций жизненно важных органов (инфекционно-токсический шок при септицемии, декомпенсированная сердечная недостаточность при бактериальном эндокардите) • Выраженность локального воспалительного процесса любой локализации не коррелирует с тяжестью течения сепсиса. Следует учитывать, что отдалённый очаг гнойного воспаления может быть как следствием сепсиса (метастазирование), так и его причиной, что важно при определении лечебной тактики.
Лекарственная терапия
• Этиотропная терапия •• До получения результатов бактериологического исследования, особенно при неясной этиологии, наиболее эффективно сочетание гентамицина или тобрамицина 3–5 мг/кг/сут в/в и антибиотика из группы цефалоспоринов или имипенем+циластатин 500 мг в/в каждые 6 ч •• Антибиотики назначают в максимальной дозировке, в/в, в течение не менее 2 нед (несмотря на нормализацию температуры тела) •• Критерии эффективности — очевидная положительная динамика общего состояния и лабораторных показателей.
• Иммуностимулирующие препараты •• Иммуноглобулин человеческий нормальный для внутривенного введения, иммуноглобулин человеческий нормальный (IgG+IgA+IgM) для внутривенного введения •• Препараты ИФН.
• Дезинтоксикационная терапия — внутривенное введение большого количества жидкости в сочетании с диуретиками, например фуросемидом (метод форсированного диуреза) •• Количество вводимой жидкости не должно превышать объём выделенной мочи (при отсутствии у пациента признаков обезвоживания) •• Следует контролировать показатели центральной гемодинамики (АД, ЦВД) и содержание электролитов сыворотки крови и мочи •• Следует дополнительно ввести вазодилататоры.
• Симптоматическая терапия •• При анемии и тромбоцитопении — переливание крови, эритроцитарной и тромбоцитарной масс •• Противовоспалительная терапия: НПВС и ГК (следует учесть иммунодепрессивное действие ГК) •• Регидратация и парентеральное питание при выраженной дисфункции ЖКТ и тяжёлых расстройствах питания •• Купирование сердечной недостаточности и аритмий •• Противошоковые мероприятия при инфекционно-токсическом шоке (септицемия): ГК, адреномиметические средства, плазмозамещающие препараты, например полиглюкин.
Оперативное лечение при наличии доступного оперативному вмешательству очага гнойной инфекции.
Синоним. Инфекция общая гнойная
МКБ-10 • O85 Послеродовой сепсис • P36 Бактериальный сепсис новорождённого • T80.2 Инфекции, связанные с инфузией, трансфузией и лечебной инъекцией
Код вставки на сайт
Сепсис — симптомокомплекс, обусловленный постоянным или периодическим поступлением в кровь микроорганизмов из очага гнойного воспаления. В клинической картине преобладают тяжёлые полиорганные нарушения, тогда как местные воспалительные изменения выражены слабо. Характерно образование метастатических очагов гнойного воспаления в различных органах и тканях.
Классификация • Эпидемиологическая •• Внутрибольничный сепсис (послеродовый, послеоперационный, посткатетеризационный, постинъекционный, после гинекологических осмотров, сепсис новорождённых) •• Внебольничный сепсис (криптогенный, тонзиллогенный, кишечный, ожоговый) • Клиническая классификация учитывает следующие признаки: •• Этиология •• Локализация входных ворот инфекции •• Длительность ••• Молниеносный сепсис — 1–3 дня ••• Острый сепсис — до 6 нед ••• Подострый или затяжной сепсис — более 6 нед ••• Хронический сепсис (характерен для пациентов с иммунодефицитными состояниями, особенно при СПИДе) — более 6 мес •• Клиническая форма ••• Септицемия — форма сепсиса, не сопровождающаяся образованием метастатических очагов гнойной инфекции ••• Септикопиемия — форма сепсиса, характеризующаяся образованием метастатических очагов инфекции (в т.ч. инфарктов) ••• Септический (бактериальный) эндокардит. Примечание. Септицемия может трансформироваться в септикопиемию, что даёт основания считать эти формы стадиями одного процесса •• Ведущие клинико-патофизиологические синдромы ••• Тромбогеморрагический синдром (например, ДВС) ••• Септический (инфекционно-токсический) шок ••• Токсико-дистрофическое состояние.
Патогенез • Для развития сепсиса необходимо проникновение условно-патогенного возбудителя через входные ворота (чаще травмированная кожа или слизистая оболочка) с развитием местной реакции (первичного аффекта), реактивного лимфаденита (лимфангоита), гнойного тромбофлебита с последующей бактериемией и токсемией. Поражение сосудистой стенки на большом протяжении, флебиты приводят к образованию инфицированных микротромбов, обусловливающих абсцессы и инфаркты внутренних органов • Клиническая картина не зависит от этиологии, отсутствуют морфологические признаки, указывающие на специфику процесса • Глубокое нарушение обмена веществ вследствие выраженной интоксикации, преобладание процессов катаболизма (гипоальбуминемия, диспротеинемия, гипергликемия, дефицит эссенциальных жирных кислот, гиповитаминоз, метаболический ацидоз). Тяжёлые дистрофические изменения дополнительно ухудшают функции органов, что даже при отсутствии в них клинически выраженных метастазов приводит к системной полиорганной недостаточности, характерной для поздних необратимых стадий сепсиса.
Клиническая картина. Инкубационный период, цикличность течения, характерные для инфекционных заболеваний, отсутствуют. Патогномоничных признаков не существует • Интоксикационный синдром •• Вялость, анорексия, изменения психоэмоционального статуса до грубых общемозговых расстройств (коматозное состояние) •• Лихорадка (температурная кривая чаще всего неправильного типа). Подозрение на наличие сепсиса возникает при продолжительности лихорадки более 5 дней и наличии немотивированных подъёмов температуры тела до фебрильных значений с последующим падением до субфебрильных •• Признаки дистрофии и нарушения питания с развитием гипотрофии и уменьшением массы тела, снижением эластичности кожи, тургора мягких тканей • Дисфункция ЖКТ, тошнота, рвота (в т.ч. и вследствие интоксикации) • Нарушения микроциркуляции — бледность кожных покровов с землистым оттенком, геморрагическая сыпь, одышка, снижение диуреза • Гепатолиенальный синдром • Симптомы поражения органов и тканей соответственно локализации метастатических очагов или входных ворот инфекции.
Лабораторные признаки • Лейкоцитоз или лейкопения (при этиологической роли грамотрицательной флоры и СПИДе), нейтрофилёз с гиперрегенераторным сдвигом влево, прогрессирующая анемия, тромбоцитопения • Гипопротеинемия с диспротеинемией (снижение соотношения альбумины/глобулины) • Высокая концентрация белков острой фазы воспаления • Изменения коагулограммы, свидетельствующие о развитии ДВС • Лейкоцитурия, бактериурия, цилиндрурия, эритроцитурия • Положительные результаты бактериологического исследования крови (обнаружение гемокультуры), кала, мочи, ликвора. Для получения положительного результата необходим трёхкратный забор крови в объёме 20–30 мл с интервалом в 1 ч по возможности до начала антибиотикотерапии • Гиперферментемия, гипербилирубинемия при поражении соответствующих органов.
Диагностические критерии клинических форм сепсиса • Септикопиемия — обнаружение одного или нескольких очагов метастатического воспаления с идентификацией возбудителя • Септицемия — преобладают признаки интоксикационного синдрома с выраженными расстройствами микроциркуляции и центральной гемодинамики, развёрнутой клиникой тромбогеморрагического синдрома. Характерен септический (инфекционно-токсический) шок • Септический (бактериальный) эндокардит (см. Эндокардит инфекционный). Особенности инфекционного процесса: входные ворота — чаще слизистая оболочка глотки, но местный очаг (источник постоянного поступления микроорганизмов в системный кровоток) — эндокард.
ЛЕЧЕНИЕ
Тактика ведения • Госпитализация • Этиотропная терапия. До получения результатов бактериологического исследования антибиотики выбирают эмпирически • Иммуностимулирующая терапия • Дезинтоксикационная терапия (её адекватность в конечном итоге определяет прогноз), в т.ч. по показаниям экстракорпоральная дезинтоксикация: плазмаферез, гемосорбция, перфузия крови через донорские органы животных (селезёнка, печень) • Симптоматическая терапия • Лечение носит характер интенсивной терапии и дополнительно включает экстренную коррекцию расстройств функций жизненно важных органов (инфекционно-токсический шок при септицемии, декомпенсированная сердечная недостаточность при бактериальном эндокардите) • Выраженность локального воспалительного процесса любой локализации не коррелирует с тяжестью течения сепсиса. Следует учитывать, что отдалённый очаг гнойного воспаления может быть как следствием сепсиса (метастазирование), так и его причиной, что важно при определении лечебной тактики.
Лекарственная терапия
• Этиотропная терапия •• До получения результатов бактериологического исследования, особенно при неясной этиологии, наиболее эффективно сочетание гентамицина или тобрамицина 3–5 мг/кг/сут в/в и антибиотика из группы цефалоспоринов или имипенем+циластатин 500 мг в/в каждые 6 ч •• Антибиотики назначают в максимальной дозировке, в/в, в течение не менее 2 нед (несмотря на нормализацию температуры тела) •• Критерии эффективности — очевидная положительная динамика общего состояния и лабораторных показателей.
• Иммуностимулирующие препараты •• Иммуноглобулин человеческий нормальный для внутривенного введения, иммуноглобулин человеческий нормальный (IgG+IgA+IgM) для внутривенного введения •• Препараты ИФН.
• Дезинтоксикационная терапия — внутривенное введение большого количества жидкости в сочетании с диуретиками, например фуросемидом (метод форсированного диуреза) •• Количество вводимой жидкости не должно превышать объём выделенной мочи (при отсутствии у пациента признаков обезвоживания) •• Следует контролировать показатели центральной гемодинамики (АД, ЦВД) и содержание электролитов сыворотки крови и мочи •• Следует дополнительно ввести вазодилататоры.
• Симптоматическая терапия •• При анемии и тромбоцитопении — переливание крови, эритроцитарной и тромбоцитарной масс •• Противовоспалительная терапия: НПВС и ГК (следует учесть иммунодепрессивное действие ГК) •• Регидратация и парентеральное питание при выраженной дисфункции ЖКТ и тяжёлых расстройствах питания •• Купирование сердечной недостаточности и аритмий •• Противошоковые мероприятия при инфекционно-токсическом шоке (септицемия): ГК, адреномиметические средства, плазмозамещающие препараты, например полиглюкин.
Оперативное лечение при наличии доступного оперативному вмешательству очага гнойной инфекции.
Синоним. Инфекция общая гнойная
МКБ-10 • O85 Послеродовой сепсис • P36 Бактериальный сепсис новорождённого • T80.2 Инфекции, связанные с инфузией, трансфузией и лечебной инъекцией
Симптомы сепсиса при ангине и его лечение
Код по МКБ-10: A40.0 - сепсис вызванный стрептококком группы А
Код по МКБ-10: A40.1 - сепсис вызванный стрептококком группы В
Код по МКБ-10: A40.2 - сепсис вызванный стрептококком группы D
Код по МКБ-10: A40.3 - сепсис вызванный пневмотококком
Код по МКБ-10: A40.8 - сепсис вызванный другим стрептококком
Код по МКБ-10: A40.9 - сепсис без уточнения
а) Симптомы и клиника. К клиническим проявлениям тонзиллогенного сепсиса относятся озноб, лихорадка септического типа, болезненность вдоль внутренней яремной вены, которая пальпируется в виде плотного тяжа под передним краем грудино-ключично-сосцевидной мышцы, или болезненность лимфатических узлов яремно-двубрюшной группы. Область нёбных миндалин гиперемирована, однако значение этого признака невелико.
Отмечаются выраженные общие симптомы, такие как лейкоцитоз со смещением лейкоцитарной формулы влево, сухой язык, слабый частый пульс, спленомегалия, а также симптомы, связанные с появлением септических очагов в легких, печени, коже.
б) Причины и механизмы развития сепсиса при ангине. Бактерии попадают в кровь из нёбных миндалин или из расположенного поблизости гнойного очага. Возможны три пути распространения инфекции:
1. Гематогенный, по тонзиллярным венам в лицевую и далее во внутреннюю яремную вену. Развитие тромбофлебита приводит к образованию септических тромбов, фрагменты которых заносятся в легкие и другие органы.
2. Лимфогенный, по эфферентным лимфатическим путям из нёбных миндалин в регионарные лимфатические узлы яремно-двубрюшной группы и вдоль внутренней яремной вены с развитием септического тромбофлебита и далее, как в пункте 1.
3. Per continuitatem, за счет расширения границ воспаления на окружающие ткани окологлоточного пространства и мягкие ткани шеи, включая внутреннюю яремную вену.
Возбудителями тонзиллогенного сепсиса могут быть ряд микроорганизмов. Их можно выявить при посеве крови, взятой на высоте озноба. Возможна смешанная инфекция.
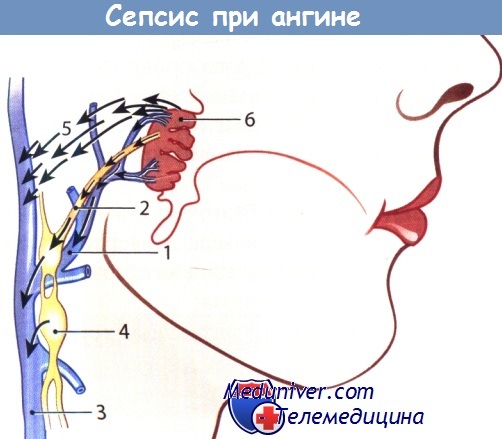
Развитие тонзиллогенного сепсиса:
1 - распространение инфекции по венам; 2 - распространение инфекции по лимфатическим путям;
3 - внутренняя яремная вена; 4 - регионарные лимфатические узлы вокруг внутренней яремной вены;
5 - распространение инфекции по протяжению (per continuitatem) через мягкие ткани шеи на внутреннюю яремную вену; 6 - нёбная миндалина.
в) Диагностика. Диагноз устанавливают на основании клинических проявлений бактериемии (озноб и симптомы септицемии), эпизодов острого или обострения хронического тонзиллита или эпизодов острого тонзиллита в анамнезе, быстрого повышения СОЭ и количества лейкоцитов в крови, болезненности яремно-двубрюшных лимфатических узлов или внутренней яремной вены, характерного защитного спазма шейных мышц, обусловливающего щадящее положение головы и шеи. Для диагностики прибегают также к посеву крови.
г) Лечение сепсиса при ангине. При подозрении на тяжелый сепсис начинают безотлагательное лечение пенициллином или антибиотиками широкого спектра действия для предотвращения образования септических (метастатических) очагов в отдаленных органах и тканях. После получения результатов бактериологического исследования подбирают соответствующие антибиотики.
К другим обязательным мерам относятся:
1. Тонзиллэктомия для исключения очага инфекции.
2. Перевязка внутренней яремной вены дистальнее уровня тромбоза и резекция пораженного сегмента вены.
3. Широкий разрез и дренирование абсцесса мягких тканей шеи.
д) Течение и прогноз. Тонзиллогенный сепсис - опасное для жизни осложнение тонзиллита, однако при своевременном назначении антибактериальной терапии и выполнении хирургического вмешательства прогноз благоприятный.
P.S. При первом же подозрении на тонзиллогенную септицемию с повторными ознобами следует срочно выполнить тонзиллэктомию и назначить массивные дозы антибиотиков. Развитие сепсиса говорит об иммунодефиците.
Симптомы перитонзиллярного абсцесса после ангины и его лечение
Код по МКБ-10: J36.0
В отличие от острого тонзиллита перитонзиллярный абсцесс развивается у взрослых молодого возраста:
а) Симптомы и клиника. После разрешения симптомов тонзиллита и следующего после этого бессимптомного периода длительностью несколько дней появляется быстро прогрессирующее затруднение глотания.
Боль обычно иррадиирует в ухо, больные с трудом открывают рот из-за тризма, речь невнятная. Боль бывает настолько интенсивной, что больные отказываются есть, голова наклонена в больную сторону, больной старается не двигать головой, отмечаются сиалорея и неприятный запах изо рта, увеличение регионарных лимфоузлов, температура повышается до 39—40°С, общее состояние быстро ухудшается.
Больные жалуются также на невыносимое ощущение давления в шее, отмечаются обструкция входа в гортань и нарастающее затруднение дыхания. Однако иногда симптомы бывают выражены слабо. В некоторых случаях перитонзиллярный абсцесс бывает двусторонним.
б) Причины и механизмы развития. Перитонзиллярный абсцесс развивается вследствие распространения инфекции с миндалины на окружающую ткань, абсцесс формируется в течение нескольких дней. Он может развиться сразу после острого тонзиллита или спонтанно. В последнем случае полагают, что очаг инфекции локализуется в слюнных железах, расположенных в супратонзиллярном пространстве. Верхний констриктор глотки обычно служит эффективным барьером, препятствующим распространению инфекции.
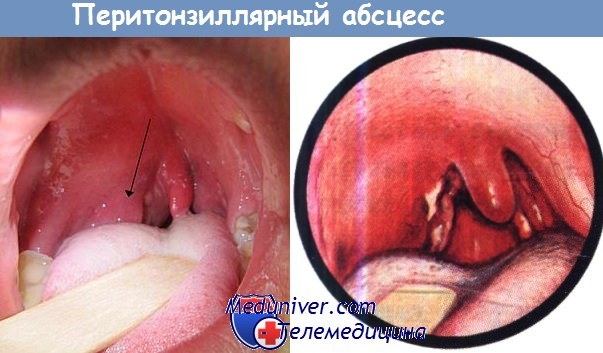
Перитонзиллярный абсцесс.
Видно округлое выпячивание правой передней нёбной дужки уплотненной нёбной миндалиной и смещение нёбного язычка вправо.
На видимой части нёбных миндалин имеются гнойные пятна, из области полюса левой нёбной миндалины выделяется желтый сливкообразный гной.
в) Диагностика. Диагноз ставят на основании клинической картины (отек и гиперемия зева и миндалины, которая значительно выступает из миндаликовой ямки, выпячивая нёбную дужку, и смещает мягкое нёбо и нёбный язычок в здоровую сторону. Осмотр полости рта затруднен из-за выраженного тризма. Лимфатические узлы яремно-двубрюшной группы болезненны.
На языке и реже на миндалинах и нёбе имеется экссудат. В анализах крови наблюдаются характерная картина острой инфекции и высокая СОЭ. При флуктуирующем отеке следует выполнить пункцию для исключения абсцесса.
г) Дифференциальный диагноз включает перитонзиллярную флегмону, тонзиллогенный сепсис, аллергический отек глотки без лихорадки (ангионевротический отек), злокачественную форму дифтерии, агранулоцитоз, специфическую тонзиллярную инфекцию (туберкулез и сифилис) и неизъязвляющиеся опухоли миндалин и окружающих тканей (злокачественная лимфома, лимфоэпителиальная опухоль, анапластический рак и лейкоз).
Дифференциальный диагноз включает также одонтогенную инфекцию, в частности перитонзиллярный абсцесс, связанный с ретенированным зубом мудрости, и аневризму внутренней сонной артерии (которую можно распознать по пульсации). Отсутствие острых локальных симптомов и лихорадки, а также длительное течение говорят об ошибочности диагноза перитонзиллярного абсцесса.
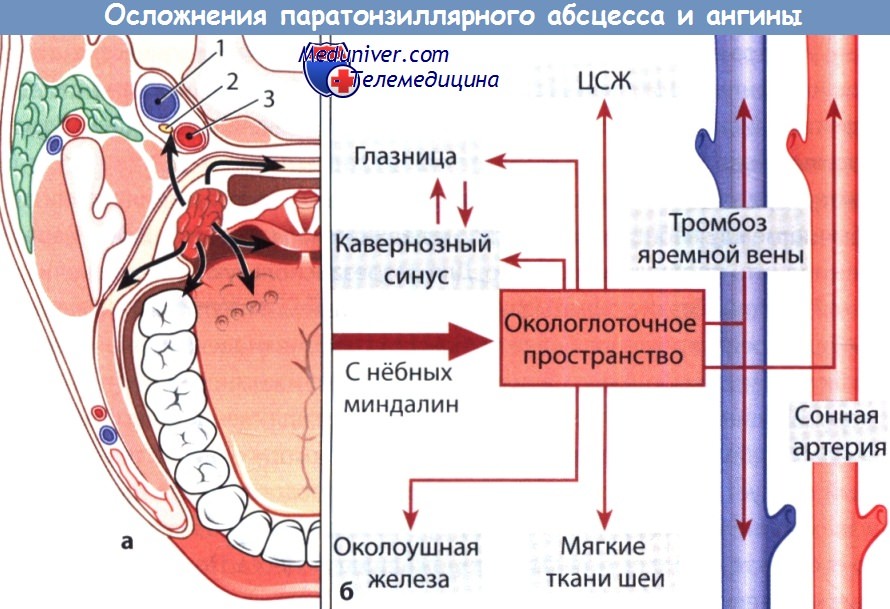
Осложнения паратонзиллярного абсцесса и ангины:
а Распространение воспалительного процесса на соседние ткани: 1 - внутренняя яремная вена; 2 - блуждающий нерв; 3 - внутренняя сонная артерия.
б Дальнейшие пути распространения тонзиллогенной инфекции.
д) Лечение перитонзиллярного абсцесса:
- Лечение без операции (консервативное). Назначают высокие дозы антибиотиков, например пенициллин или цефалоспорин и др., так как для предотвращения образования перитонзиллярного абсцесса на ранней стадии, когда инфильтрат еще не абсцедировал, необходим по крайней мере недельный курс антибиотикотерапии. Рекомендуются также анальгетики, жидкая холодная пища, пузырь со льдом на область шеи и полоскания горла.
- Операция при перитонзиллярном абсцессе:
1. Тонзиллэктомия. Операцию выполняют под эндотрахеальным наркозом. Она показана всем больным, особенно при рецидивирующем перитонзиллярном абсцессе, если нет серьезных противопоказаний. Тонзиллэктомия предотвращает рецидивы, позволяет ограничиться одним курсом антибио-тикотерапии и сэкономить время.
2. Дренирование абсцесса осуществляют через 3-4 дня после тозиллэктомии под наркозом.
Принципы дренирования абсцесса. Операцию начинают с тщательной местной анестезии 1% раствором местного анестетика, например лидокаина (Ксилокаин), сначала поверхностной, а затем инфильтрационной, с добавлением к раствору анестетика эпинефрина из расчета 1:200 000. После инфильтрации тканей выжидают примерно 5 мин для достижения обезболивающего эффекта и лишь после этого выполняют разрез. Выполнение операции под наркозом более предпочтительно.
Выполнение разреза. Разрез выполняют в месте наибольшего выбухания тканей в области абсцесса, обычно между нёбным язычком и 2-м верхним моляром. Перед разрезом можно выполнить пробную аспирацию. Для разреза используют остроконечный скальпель с длинной ручкой. Лезвие обматывают лейкопластырем, отступив 1,5-2,0 см от острия для предотвращения более глубокого его проникновения в ткани и повреждения сосудов шеи.
Разрез выполняют параллельно краю ветви нижней челюсти, но так, чтобы он не слишком заходил кнаружи, так как это чревато повреждением яремной вены и сонной артерии. Если диагноз поставлен правильно, при надрезе тканей выделяется гной, который следует удалить с помощью отсоса для предотвращения аспирации в трахею. После эвакуации гноя расширяют разрез кровоостанавливающим зажимом, раздвигая бранши, что способствует более полному опорожнению абсцесса. Полость абсцесса следует опорожнять ежедневно, пока не прекратится выделение гноя.
Для профилактики рецидива абсцесса выполняют отсроченную тонзиллэктомию.
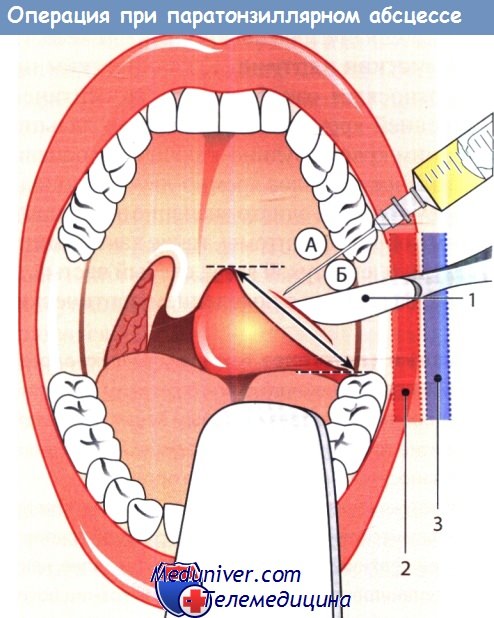
Перитонзиллярный абсцесс:
1 - скальпель с защищенным лезвием; 2 - внутренняя сонная артерия; 3 - внутренняя яремная вена.
Перед вскрытием абсцесса (Б) его пунктируют и аспирируют содержимое (А).
Разрез производят вдоль линии, соединяющей последний моляр и нёбный язычок.
е) Течение и прогноз. Для купирования воспалительного процесса и профилактики абсцесса следует своевременно назначить антибиотикотерапию. При перитонзиллярном абсцессе возможно также спонтанное вскрытие абсцесса и излечение. Однако сильная боль и нарушение глотания обычно заставляют выполнить разрез и дренировать абсцесс. Если после вскрытия абсцесса не выполнить тонзиллэктомию, вероятность формирования рецидивного абсцесса в рубцовой ткани, оставшейся после заживления, высока.
ж) Осложнения и связанный с ними риск перитонзиллярного абсцесса для жизни. К осложнениям перитонзиллярного абсцесса относится распространение воспалительного процесса и отека на вход в гортань с развитием обструкции дыхательных путей и асфиксии. Абсцесс может прорваться также в окологлоточное пространство. Распространение воспалительного процесса возможно:
• в нисходящем направлении на область шеи;
• в окологлоточное пространство с развитием окологлоточного абсцесса;
• в восходящем направлении на область глазницы и в полость черепа с развитием менингита, тромбоза пещеристого синуса и абсцесса мозга;
• на внутреннюю яремную вену с развитием ее тромбоза;
• на сонную артерию и ее ветви (редко), что чревато развитием аррозионного кровотечения;
• на околоушную железу с развитием гнойного паротита.
Видео этиология, патогенез заглоточного абсцесса и паратонзиллярного абсцесса
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021

Такое тяжелое осложнение может возникнуть при распространении ангинозной инфекции или хроническом тонзиллите у лор больных, реактивность организма которых снижена, а вирулентность (болезнетворность) микрофлоры достаточно высока. Заражение происходит контактным путем из небных миндалин. Причиной тонзиллогенного сепсиса может стать и гнойное осложнение, которое возникло как следствие ангины в позадиглоточном и окологлоточном пространствах.
Клиническая картина
Температура тела высокая и носит гектический (39-40 0 С) характер, т.к. в течение суток 2-3 раза может изменяться на 3-4 градуса. Она сопровождается ознобом и обильным потоотделением. Общее состояние тяжелое – наблюдается резкая вялость, слабость и адинамия.
Кожные покровы приобретают желтушное окрашивание, что обусловлено повреждением эритроцитов и выхождением гемосидирина (темно-желтый пигмент, который образуется при распаде гемоглобина). Шейные лимфатические узлы, которые располагаются по краю кивательной мышцы, становятся болезненными и увеличиваются в размере. В некоторых случаях возникает болезненность по ходу яремной вены.
Фарингоскопическая картина идентична ангине или паратозиллярному, окологлоточному или заглоточному абсцессу. В крови наблюдается повышение СОЭ и гиперлейкоцитоз (чрезмерное количество белых клеток крови) со сдвигом формулы влево.
Диагностика
Диагноз ставится на основании характерной клинической картины, анамнезе и результатах лабораторных исследований. Чтобы уточнить диагноз измеряют каждые три часа температуру тела и проводят повторное бактериологическое исследование крови. При постановке диагноза следует исключить возникновение других очагов инфекции (заболеваний околоносовых пазух и среднего уха).
Лечение
В случае если тонзиллогенный сепсис сочетается с абсцессами в окологлоточном, позадиглоточном и околоминдальниковом пространствах, то необходима срочная госпитализация в ЛОР стационар. Больному будет проведена санация в сочетании с массивной антибактериальной терапией. Назначается дезинтаксикационная терапия и антикоагулянты, которые препятствуют образованию тромбов.
Прогноз
При своевременном обращении к лор врачу и правильном лор лечении, прогноз на выздоровление благоприятный.
- Авдеева С.Н. Распространенность заболеваний ЛОР органов среди городского населения на современном этапе / С.Н. Авдеева // Рос. оторинолар. 2006. -№ (22). - С. 33-37.
- Богомолов, Б.П. Дифференциальная диагностика инфекционных болезней Текст. /Б.П.Богомолов. Москва, Дизайн Пресс. - 2000. - 233 с.
- Брико, Н.И. Стрептококковая (группы А) инфекция: взгляд на ситуацию сложившуюся к началу XXI века Текст. / Н.И.Брико // Врач. 2000. - № 8,- С. 19-22.
- Дикий, О.Б. Комплексное лечение больных ангинами Текст. /О.Б. Дикий, Г.Б. Матейко, P.C. Остяк // Инфекционные болезни: диагностика, лечение, профилактика. С.-Пб., 2000. - С. 76.
- Макаров B.K., Мосягин A.B. // Инфекционные болезни. 2008. -№1.-С. 21-23.
- Моррисон // Терапевтический архив. 2006. - №11. - С. 27-30.
- Пальчун В. Т., Крюков А. И. Оториноларингология: руководство для врачей. — М.: Медицина, 2001. — 616 с.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Институт хирургии им. А.В. Вишневского Минздрава России
Диагностика сепсиса у больных с гнойно-воспалительной патологией ЛОР-органов
Цель исследования - разработка алгоритма ранней клинико-лабораторной и инструментальной диагностики сепсиса у больных с гнойно-воспалительными заболеваниями ЛОР-органов. В исследование включены 50 пациентов с гнойно-воспалительными заболеваниями ЛОР-органов, осложнившихся генерализацией инфекции. Разработана схема (алгоритм) обследования, позволившая уже на ранних этапах госпитализации в стационар диагностировать сепсис у больных с гнойно-воспалительными заболеваниями ЛОР-органов. Алгоритм диагностики включал в себя критерии синдрома системной воспалительной реакции (ССВР), лейкоцитарный индекс интоксикации Кальф-Калифа (ЛИИ), прокальцитониновый тест (ПКТ), интегральные шкалы оценки степени тяжести состояния (APACHE-II) и органных дисфункций (SOFA). Своевременная дооперационная диагностика септических осложнений и санация первичного очага инфекции в сочетании с ранней интенсивной терапией в условиях отделения реанимации позволили избежать прогрессирования генерализации инфекции, уменьшить число повторных операций, улучшить прогноз заболевания и снизить летальность до 12% в основной группе (в контрольной группе - 44%).
Институт хирургии им. А.В. Вишневского Минздрава России
Сепсис в современной медицине всегда оставался в сфере повышенного внимания врачей всех специальностей в силу неуклонного роста заболеваемости и стабильно высокой летальности (30—50%) даже в самых авторитетных отечественных и зарубежных клиниках [1—3]. В оториноларингологии данная проблема не является исключением [4, 5].
В оториноларингологической практике к гнойно-воспалительным заболеваниям ЛОР-органов как источникам септической инфекции относят гнойно-воспалительные заболеваний носа, околоносовых пазух (ОНП) и среднего уха, а также острые гнойные заболевания глотки и гортани и их осложнения (флегмоны подчелюстной области, окологлоточных пространств, передних и боковых поверхностей шеи) [4, 6].
Ото- и риногенному сепсису посвящены многочисленные публикации, с 30—50-х годов прошлого столетия большое внимание уделялось и тонзиллогенному сепсису [5, 7—9]. Несмотря на это, проблема сепсиса в оториноларингологии освещена недостаточно [6].
В оториноларингологии сепсис диагностируют при наличии первичного септического очага, которым в большинстве случаев является острая или хроническая гнойно-воспалительная патология ЛОР-органов, двух или более признаков синдрома системной воспалительной реакции (ССВР) [1, 4, 6]. Тяжелый сепсис — это сепсис, сочетающийся с органной дисфункцией, гипотензией, нарушением тканевой перфузии. Септический шок — тяжелый сепсис с артериальной гипотонией, не устраняющейся с помощью инфузионной терапии и требующей назначения катехоламинов [1].
Сепсис при гнойно-воспалительных заболеваниях ЛОР-органов является тяжелой хирургической патологией и нередко сопровождается неблагоприятным исходом [4, 5]. Ранняя диагностика сепсиса в значительной части случаев затруднена вследствие недостаточно специфичных клинических проявлений (первичные признаки сепсиса часто не выявляют), что не позволяет своевременно начать адекватное лечение [10]. Недостаточное знание ЛОР-врачами клинических и лабораторных критериев сепсиса (ССВР, сепсис, тяжелый сепсис, септический шок) также усугубляет данную проблему [11, 12]. Раннее начало лечения и применение методик с доказанной эффективностью улучшают результаты лечения больных с сепсисом [13—16].
Цель исследования — разработка алгоритма ранней клинико-лабораторной и инструментальной диагностики сепсиса у больных с гнойно-воспалительными заболеваниями ЛОР-органов.
Пациенты и методы
Исследование проводилось на базе ГКБ №36 Москвы с 2009 по 2011 г.
В исследование включены 50 пациентов с гнойно-воспалительными заболеваниями ЛОР-органов, осложнившихся сепсисом (38 мужчин и 12 женщин в возрасте от 21 года до 82 лет).
Клиническую характеристику основной группы (25 человек) проводили по специально разработанной нами схеме (алгоритму) обследования и лечения пациентов с гнойно-воспалительными заболеваниями ЛОР-органов и сепсисом (2009—2011 гг.).
Контрольную группу (25 человек) составили пациенты с гнойно-воспалительной ЛОР-патологией и сепсисом, выявленным нами ретроспективно при анализе историй болезни, где использовались традиционные методы обследования и лечения.
Среди пациентов обеих групп превалировали больные в возрасте от 40 до 60 лет — 34 (68%) человека и старше 60 лет — 16 (32%) человек. 38 (76%) пациентов составляли мужчины. У госпитализированных в клинику больных уже в момент поступления состояние расценивалось как тяжелое или крайне тяжелое. У 40 (80%) человек была выявлена тяжелая сопутствующая патология: сахарный диабет, гипертоническая болезнь, ишемическая болезнь сердца, распространенный атеросклероз, хроническое легочное сердце, ожирение, нейродермит, хронический бронхит, хроническая обструктивная болезнь легких, эпилепсия, хронический алкоголизм, туберкулома легкого. У 49 (98%) обследуемых пациентов гнойно-воспалительная патологии ЛОР-органов была диагностирована при поступлении и только у 2 (4%) (гнойно-воспалительные заболевания среднего уха) в течение первых 3 суток. При этом несвоевременная диагностика гнойно-воспалительной ЛОР-патологии была затруднена из-за наличия у больных тяжелых сопутствующих заболеваний и проведения дифференциальной диагностики. При наличии менингеальных симптомов и подозрении на ото- или синусиндуцированный внутричерепной гнойный очаг выполнялись люмбальная пункция, КТ или МРТ головного мозга. При подтверждении диагностировался вторичный отогенный или риногенный менингит и/или ото- или риногенный абсцесс головного мозга.
Разработанный нами алгоритм (схема) включал в себя общепринятые клинико-лабораторные и инструментальные методы обследования (клинический анализ крови, общий анализ мочи, биохимический анализ крови, коагулограмма, RW, ВИЧ, маркеры гепатитов В, С), рентгенографию органов грудной клетки, ОНП, черепа и органов шеи в боковой проекции, КТ и МРТ головного мозга (по показаниям), УЗИ мягких тканей шеи, органов брюшной полости и забрюшинного пространства (по показаниям); ЭКГ, ЭХО-кардиографию (по показаниям), фибробронхоскопию; а также исследование прокальцитонинового теста (ПКТ) полуколичественным методом, микробиологического мониторинга (гемокультура, раневое отделяемое), интегральных шкал оценки степени тяжести состояния (APACHE-II) и органных дисфункций (SOFA).
Для обеспечения рациональной антибактериальной терапии выполнялись бактериологические исследования крови, мочи, трахеального аспирата, бронхоальвеолярного лаважа (БАЛ), слизистой оболочки зева и полости носа, пунктата из верхнечелюстной пазухи, отделяемого из ушей с определением КОЕ.
Определение уровня концентрации прокальцитонина проводили полуколичественным иммунохроматографическим экспресс-методом (B.R.H.M.S. РСТ-Q), позволяющим получить ответ в течение 30 мин. При интерпретации результатов использовали разработанные в нашей клинике критерии диагностики, основанные на типовых клинических ситуациях, предложенных M. Meisner [17]: референсные значения ПКТ менее 0,5 нг/мл соответствовали локальному бактериальному очагу, от 0,5 до 2,0 нг/мл — локальному бактериальному очагу с ССВР, от 2,0 до 10,0 — сепсису, более 10,0 нг/мл — тяжелому сепсису.
В своей работе мы руководствовались классификацией, предложенной согласительной конференцией Американского колледжа пульмонологов и Общества специалистов критической медицины ACCР/SCCM в 1991 г. [19].
Кроме того, для конкретизации генерализации инфекции мы использовали диагностические критерии сепсиса, предложенные М. Levy в 2003 г. [20].
Наличие у пациентов основной группы признаков синдрома системного воспалительного ответа являлось абсолютным показанием для госпитализации в отделение реанимации и интенсивной терапии, где они находились в течение всего критического периода для проведения комплексного обследования, лечения и выполнения предоперационной подготовки перед планируемым хирургическим вмешательством. Длительность предоперационной подготовки определялась индивидуально для каждого пациента и составляла в среднем от 2 до 4 ч.
Оперативные вмешательства выполнялись под эндотрахеальным наркозом. Всем 50 больным выполнялась различная по объему хирургическая санация очагов инфекции.
В основной группе 7 больным выполнена расширенная антромастоидотомия, 2 — радикальная (санирующая) операция на среднем ухе, 3 — расширенная санирующая операция на среднем ухе с декомпрессивной трепанацией черепа с целью удаления субдурального абсцесса головного мозга; 2 больным произведена радикальная операция на ОПН, 1 больному радикальная операция на ОНП с декомпрессивной трепанацией черепа и удалением субдурального абсцесса головного мозга, 5 — радикальная операция на ОНП с хирургической обработкой риногенной флегмоны орбиты, 1 больному выполнена хирургическая обработка паратонзиллярного абсцесса и флегмоны шеи и 1 — хирургическая обработка абсцесса надгортанника и флегмоны шеи. Также 2 больным выполнена хирургическая обработка паратонзиллярного абсцесса, флегмоны шеи с шейной медиастинотомией, 1 больному — хирургическая обработка абсцесса надгортанника, флегмоны шеи и шейная медиастинотомия.
В контрольной группе расширенная антромастоидотомия выполнена 7 больным, радикальная (санирующая) операция на среднем ухе — 3, расширенная санирующая операция на среднем ухе с декомпрессивной трепанацией черепа с целью удаления субдурального абсцесса головного мозга — 2, радикальная операция на ОНП выполнена 3 больным, радикальная операция на ОНП с декомпрессивной трепанацией черепа и удалением субдурального абсцесса головного мозга — 2 больным, радикальная операция на ОНП с хирургической обработкой риногенной флегмоны орбиты — 4 больным, хирургическая обработка паратонзиллярного абсцесса и флегмоны шеи — 2, хирургическая обработка абсцесса надгортанника и флегмоны шеи — 2, хирургическая обработка паратонзиллярного абсцесса, флегмоны шеи с шейной медиастинотомией — 2; 1 пациенту выполнена хирургическая обработка абсцесса надгортанника, флегмоны шеи и шейная медиастинотомия. Реоперации в основной группе выполнены 3 (6%) больным, в контрольной группе — 9 (36%).
Вопрос о переводе больных из ОРИТ решался индивидуально на основании комплексной оценки динамики состояния пациента. Основными критериями для перевода пациента в ЛОР-отделение являлись: положительная динамика течения гнойно-воспалительного процесса (санация очага инфекции), отсутствие признаков системной воспалительной реакции, снижение ЛИИ, значение прокальцитонина менее 0,5 нг/мг, а также сумма баллов по APACHE-II до 6 и SOFA до 3 и ниже.
При анализе микробиологического исследования выявлено, что микрофлора в обеих группах была идентична. Основные выделенные микроорганизмы были представлены Fusobacterium necroforum, Bacteroides fragilis, Staphylococcus aureus и оксациллин-резистентными штаммами Staphylococcus epidermidis, Enterobacter spp., Pseudomonas aeruginosa, Streptococcus pneumoniae, Acinetobacter.
У 38 (76%) больных в основной группе мы использовали принцип деэскалационной терапии. С этой целью применяли монотерапию карбапенемами (меронем 3 г/сут) или цефалоспоринами IV поколения (цефепим 4,0 г/сут) и фторхинолонами в сочетании с метрогилом. После получения данных бактериологического исследования производили коррекцию антимикробной терапии. Многокомпонентная интенсивная терапия включала в себя дезинтоксикационную терапию, респираторную поддержку (с включением при необходимости ИВЛ), коррекцию волемических, электролитных, гемодинамических и других параметров, инотропную поддержку, кинетическую терапию, профилактику тромбоэмболических осложнений, профилактику возникновения стресс-язв желудочно-кишечного тракта и гастроинтестинальных кровотечений. В основной группе мы использовали также гемодиафильтрацию, нутритивную и иммунную терапию с обязательным контролем уровня гликемии. У больных обеих групп применяли гипербарическую оксигенацию (ГБО), в особенности у пациентов с тонзиллогенными флегмонами глубоких отделов шеи.
В контрольной группе проводилась инфузионная терапия с коррекцией водно-электролитного баланса, системная антибактериальная терапия (цефалоспорины III поколения и/или амигликозиды в сочетании с метрогилом).
Результаты и обсуждение
Основными причинами генерализации инфекции и развития сепсиса явились гнойно-воспалительные заболевания среднего уха — у 24 (48%) пациентов в основной группе и у 20 (40%) в контрольной; второе место занимали гнойно-воспалительные заболевания носа и ОНП — 16 (32%) пациентов в основной группе и 18 (36%) в контрольной; у 10 (20%) больных в основной и в контрольной группах причиной сепсиса были гнойно-воспалительные заболевания глотки и гортани. У 29 (58%) пациентов диагностированы сочетанные формы поражения — различные формы острых или хронических средних отитов + отогенный абсцесс головного мозга, различные формы синуситов + риногенный абсцесс головного мозга или риногенная флегмона орбиты, острый эпиглоттит или паратонзиллярные абсцессы + флегмона глубоких отделов шеи и т.д.
При анализе APACHE-II и SOFA в основной группе их значения соответствовали диагностированному сепсису, тяжелому сепсису и септическому шоку. Так, у 18 (72%) пациентов основной группы с сепсисом показатель APACHE-II повышался до 12 баллов, у 4 (16%) пациентов с тяжелым сепсисом — до 22 баллов, при септическом шоке у 3 (12%) пациентов APACHE-II равнялся 30 баллам. При оценке по шкале SOFA — до 5, 11, 13 баллов соответственно и более.
У 22 пациентов показатели APACHE-II и SOFA в динамике имели тенденцию к снижению на 2—3-и сутки пребывания в ОРИТ: APACHE-II был в пределах 10—14 баллов, SOFA — от 4 до 6 баллов, на 7-е, 14-е сутки показатели APACHE-II, SOFA приближались соответственно к 9 и 3 баллам. Применив современные методы диагностики и лечения сепсиса в основной группе удалось снизить летальность до 12% (3 летальных исхода) по сравнению с контрольной группой, где она составила 44% (11 летальных исходов).
Результаты изучения ПКТ показали, что при своевременной санации гнойного очага, адекватной антибактериальной терапии этот показатель имеет тенденцию к снижению. Наблюдаемое нами быстрое снижение ПКТ с 10 до 2 нг/мл после оперативного вмешательства отмечено у 18 (72%) пациентов уже на 3—5-е сутки заболевания. К моменту перевода из ОРИТ на 7—10-е сутки лечения ПКТ не превышал 0,5 нг/мл. У 4 (16%) пациентов нормализация показателя ПКТ происходила к 10-м и 14-м суткам заболевания и также не превышала 0,5 нг/мл. Уровень ПКТ плазмы крови в основной группе коррелировал с тяжестью состояния больных по интегральным шкалам APACHE-II и SOFA. Так, ежедневный мониторинг оценки тяжести состояния и органных дисфункций с определением ПКТ в основной группе в динамике помогал нам не только в прогнозировании развития септического шока, но и в оценке адекватности хирургического вмешательства. У 3 больных, несмотря на проводимое комплексное лечение, показатель ПКТ сохранялся более 10 нг/мг, показатели APACHE-II, SOFA продолжали расти. Эти больные погибли.
Отсутствие в контрольной группе своевременной диагностики первых трех этапов развития сепсиса, а именно: синдрома системной воспалительной реакции → сепсиса → тяжелого сепсиса → септического шока, явилось основной причиной летальных исходов в контрольной группе с развитием септического шока на фоне полиорганной недостаточности.
Вывод
Таким образом, исходя из вышеизложенного следует, что ранняя диагностика сепсиса у пациентов с гнойно-воспалительной ЛОР-патологией, основанная на разработанной нами схеме (алгоритм) обследования и лечения септических больных, позволяет своевременно диагностировать сепсис, тяжелый сепсис, септический шок, адекватно осуществлять комплексное лечение.
Разработанный комплекс объективных клинических и лабораторных критериев диагностики и лечения сепсиса, развившегося вследствие гнойно-воспалительных заболеваний ЛОР-органов, позволяет прогнозировать течение заболевания, радикальность хирургической обработки очага инфекции, адекватность проводимой интенсивной терапии и ее эффективность на разных этапах лечения.
Читайте также:

