Септические очаги в легких
Обновлено: 24.04.2024
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Отек легких: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Отек легких определяется как жизнеугрожающее состояние, для которого характерен процесс накопления внесосудистой жидкости в легких. Отек может развиться внезапно при большой и разнообразной по своей природе группе заболеваний и нарастать стремительно.
Функции легочного кровообращения – газообмен и фильтрация крови, регуляция водного и электролитного баланса, участие в метаболических процессах. Транспорту крови способствует низкое давление в системе малого круга кровообращения и относительно низкие показатели сопротивления сосудов току крови.
Жидкость из кровеносных сосудов просачивается за их пределы в окружающие ткани либо из-за слишком высокого давления в кровеносных сосудах, либо из-за недостаточного количества белков в кровотоке, чтобы удерживать жидкость в плазме крови.
Непосредственно за пределами мелких кровеносных сосудов в легких находятся крошечные воздушные мешочки – альвеолы. Альвеолы разделены тонкими эластичными стенками (мембранами), внутри которых проходят мельчайшие кровеносные сосуды (капилляры), позволяющие молекулам кислорода и углекислого газа перемещаться через мембраны. Жидкость попадает в альвеолы в том случае, если мембраны теряют свою целостность, что приводит к затруднению дыхания и плохому насыщению крови кислородом.
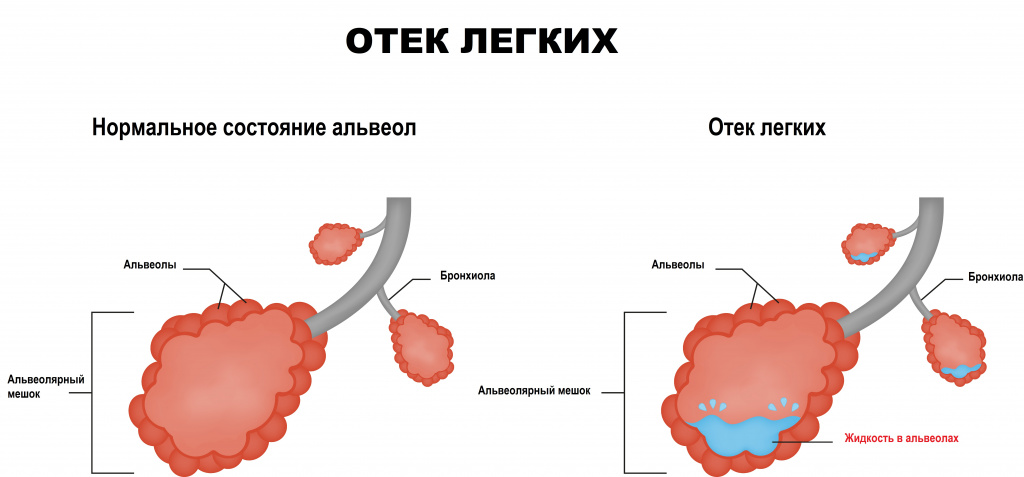
Выделяют два патогенетических процесса, с которыми связывают развитие отека легких:
Первый обусловлен повышением гидростатического давления в микрососудах малого круга кровообращения. Жидкость, электролиты и белки выходят за пределы сосудистой стенки и аккумулируются в интерстициальном (межсосудистом) пространстве легкого. На следующем этапе накопление жидкости происходит на поверхности альвеол, что становится причиной резкого ухудшения функции газообмена в легких и приводит к развитию гипоксемии.
Второй процесс связан с нарушением проницаемости альвеолярно-капиллярной мембраны из-за острого повреждения легочной ткани, которое может происходить при сепсисе, травме, пневмонии и некоторых других заболеваниях. Этот процесс также сопровождается гипоксемией и одышкой различной степени выраженности. В конечной фазе развития отека легких происходит аномальное накопление белков, в первую очередь альбуминов, в альвеолярной жидкости.
Разновидности отека легких
Кардиогенный отек легких встречается преимущественно при заболеваниях сердца или сосудов как осложнение острой сердечной недостаточности и связан с повышением гидростатического давления. У больного человека можно наблюдать тахикардию, кашель и одышку, которые возникают вследствие систолической или диастолической дисфункций левого желудочка.
Некардиогенный отек легких развивается вследствие повышенной проницаемости сосудистой стенки альвеолярных капилляров. Основным клиническим проявлением является развитие острого респираторного дистресс-синдрома.
По варианту течения выделяют следующие виды отека легких:
- Молниеносный – развивается в течение нескольких минут, в большинстве случаев приводит к летальному исходу.
- Острый – отмечается быстрое (на протяжении 4 часов) нарастание выраженности клинических симптомов. Вероятность летального исхода довольно высока и возникает на фоне инфаркта, черепно-мозговой травмы, анафилактического шока.
- Подострый – имеет волнообразное течение, характеризуется чередованием активных и спокойных периодов. Причиной часто является печеночная недостаточность. Имеет достаточно благоприятный прогноз, особенно при своевременном начале мероприятий неотложной помощи.
- Затяжной – симптомы нарастают в течение 12 часов со стертой клинической картиной, что значительно затрудняет диагностику. Основой являются хроническая сердечная недостаточность или заболевания бронхолегочной системы.
К основным причинам развития кардиогенного отека легких относятся:
- инфаркт миокарда с подъемом сегмента ST электрокардиограммы;
- гипертонический криз;
- пароксизм мерцательной аритмии (эпизод, длящийся от 30 секунд до семи дней, проходит самостоятельно или при помощи лечения).
- недостаточность митрального клапана (отрыв хорды сосочковой мышцы).
- постинфарктный и атеросклеротический кардиосклероз с систолической сердечной недостаточностью;
- диастолическая дисфункция миокарда у пожилых больных;
- систолическая и диастолическая дисфункция миокарда у больных с кардимиопатией или миокардитом;
- постоянная форма мерцательной аритмии;
- врожденные и приобретенные пороки левых отделов сердца;
- поражения клапанного аппарата, особенно митрального клапана, вследствие ревмокардита, инфекционного эндокардита, атеросклероза.
Основные легочные причины и факторы риска острого респираторного дистресс-синдрома:
- пневмония,
- вирус COVID-19,
- тромбоэмболия легочной артерии,
- ингаляционная травма,
- аспирационный синдром,
- травма грудной клетки,
- респираторные вирусные заболевания,
- эмфизема легких,
- бронхиальная астма,
- туберкулез легких,
- рак легких или метастазы в легкие.
- тяжелый сепсис и септический шок,
- переливание крови и кровезаменителей,
- большая кровопотеря,
- черепно-мозговые травмы, множественные и обширные травмы, ожоги,
- острое нарушение мозгового кровообращения,
- менингит, энцефалит,
- панкреонекроз,
- острая почечная недостаточность, острый гломерулонефрит,
- отравление химическими веществами, лекарственными средствами, алкоголем, наркотическими веществами,
- инфекционные заболевания, протекающие с тяжелой интоксикацией (грипп, корь, дифтерия, скарлатина, коклюш, столбняк, брюшной тиф),
- цирроз печени,
- патология беременных (эклампсия, синдром гиперстимуляции яичников),
- анафилактический шок,
- иммерсионный отек легких, вызванный плаванием на глубине.
В детском возрасте проблемы с сердцем наблюдаются намного реже, чем во взрослом. Поэтому основными причинами отека легких становятся заболевания дыхательной системы или серьезные травмы.
К каким врачам обращаться при отеке легких
Диагностика и обследования при отеке легких
Для установления диагноза обычно достаточно проведения клинического обследования и рентгенографии грудной клетки.
Рентгенологическое исследование структуры легких с целью диагностики различных патологий.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Сепсис: причины появления, симптомы, диагностика и способы лечения.
Определение
Сепсис – это патологический процесс, в основе которого лежит реакция организма в виде генерализованного воспаления на инфекцию различной природы. При сепсисе бактерии преодолевают иммунную защиту человека и распространяются из очага воспаления по всему организму. Местное воспаление, сепсис, тяжелый сепсис и септический шок – это различные формы выраженности воспалительной реакции организма на инфекционный процесс.
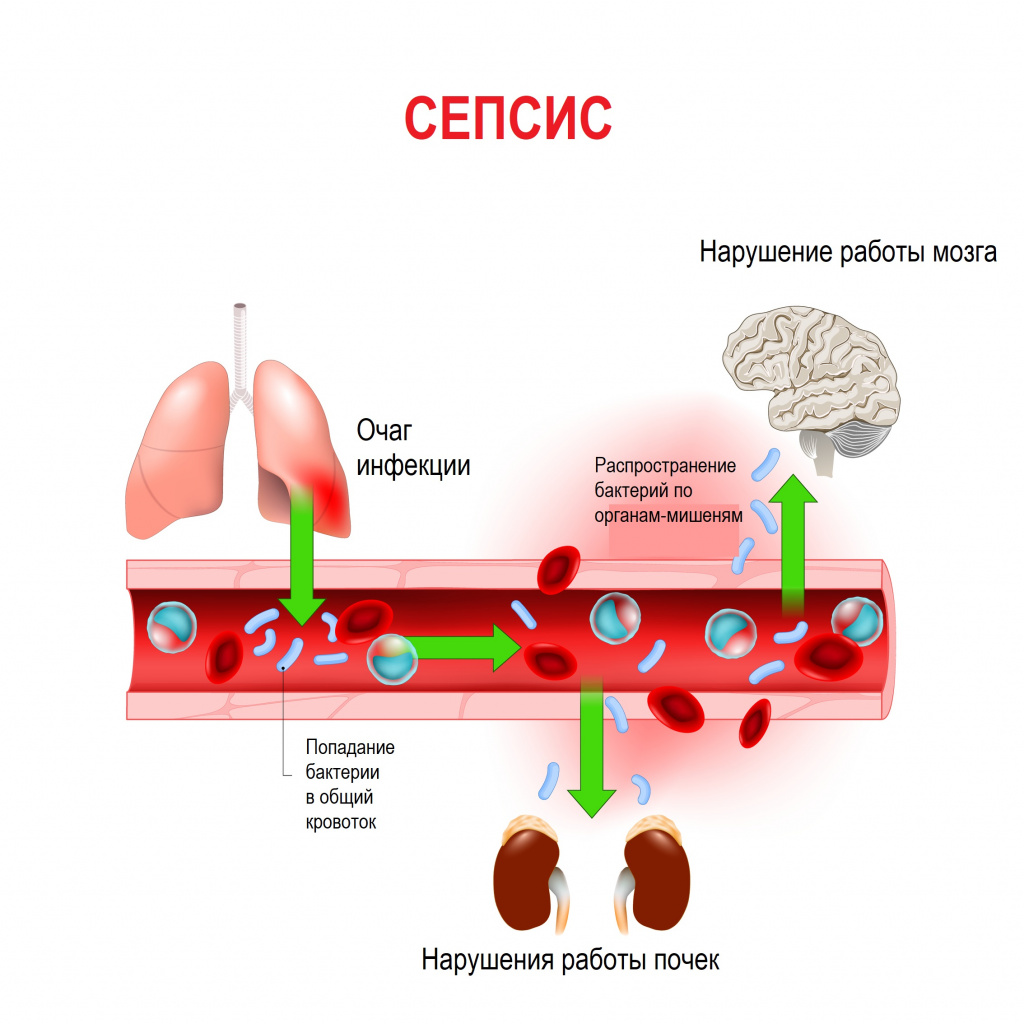
Истинная частота возникновения случаев сепсиса остается неизвестной, однако по оценкам исследователей, во всем мире сепсис является лидирующей причиной летальности у пациентов в критическом состоянии. Согласно результатам большого европейского исследования SOAP, включившего 3147 пациентов из 198 европейских медицинских центров, сепсис развился в 37,4% случаев, а госпитальная летальность от него колебалась от 14% случаев в Швейцарии до 41% в Португалии, в среднем составив 24,1%. Данные другого крупного исследования PROGRES (12 881 больной тяжелым сепсисом в 37 странах) показали, что госпитальная летальность в среднем составила 49,6%.
Причины возникновения сепсиса
Возбудителями сепсиса могут быть бактерии, вирусы или грибы. Но чаще сепсис имеет бактериальную природу - его причиной становятся стафилококки, стрептококки, пневмококки, менингококки, сальмонеллы, синегнойная палочка и др.
В большинстве случаев патологический процесс вызывают условно-патогенные микроорганизмы, которые присутствуют на коже, слизистых оболочках дыхательного и пищеварительного трактов, мочевыводящих путей и половых органов. Иногда при сепсисе выделяют сразу 2-3 микроорганизма.
Причиной сепсиса могут стать гнойно-воспалительные заболевания кожи (абсцессы, фурункулы, флегмоны), обширные травмы, ожоги, инфекционно-воспалительные заболевания мочевыводящей системы (пиелонефрит), живота (например, гнойно-некротический деструктивный панкреатит), тяжелая ангина, гнойный отит, пневмония, инфицирование во время родов или абортов и др.
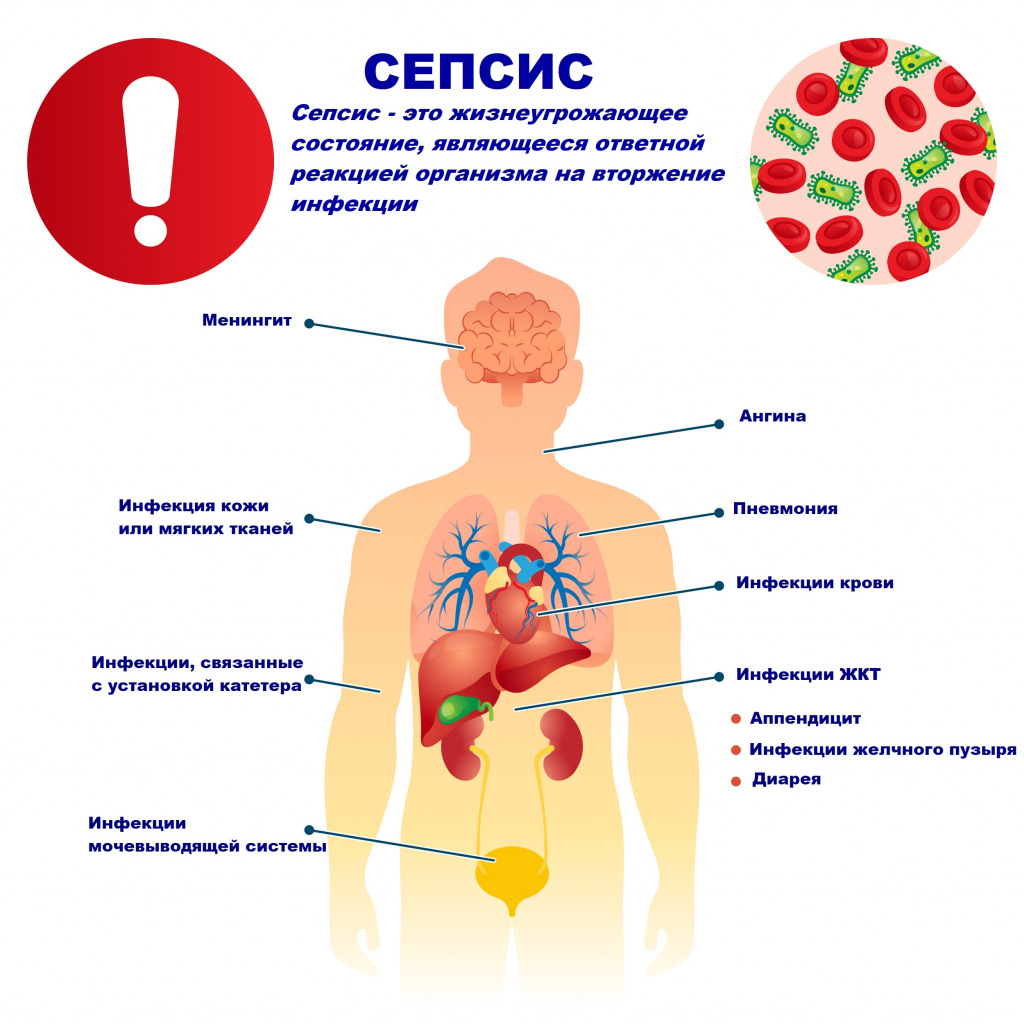
Возможность возникновения сепсиса зависит не только от свойств возбудителя, но и от состояния иммунной системы человека - нарушения в ее работе предрасполагают к распространению инфекции. Причинами таких нарушений могут быть врожденные дефекты иммунитета, хронические инфекционные болезни (ВИЧ, гнойные процессы), эндокринные заболевания (сахарный диабет), онкологические болезни, хронические интоксикации (алкоголизм, наркомания), проникающая радиация, прием иммуносупрессоров (кортикостероидов, цитостатиков) и др.
В ответ на внедрение возбудителя вырабатываются цитокины – особые белковые молекулы, которые выполняют защитные функции сначала на местном уровне, а затем, попадая в системный кровоток, продолжают работать уже на уровне всего организма. Цитокины бывают провоспалительными и противовоспалительными. В самом начале инфекционного процесса их количество находится в равновесии. Если регулирующие системы организма не способны поддерживать это равновесие, то цитокины накапливаются в кровотоке в сверхвысоких объемах, начинают доминировать их деструктивные, разрушающие эффекты, в результате повреждается сосудистая стенка, запускается синдром диссеминированного внутрисосудистого свертывания (ДВС-синдром) и полиорганная дисфункция. Вследствие полиорганной дисфункции печени, почек, кишечника появляются новые повреждающие факторы (лактат, мочевина, билирубин и др.), которые усиливают деструктивные процессы. При ДВС-синдроме в сосудах микроциркуляторного русла образуются множественные тромбы в сочетании с несвёртываемостью крови, приводящей к множественным кровоизлияниям.
Классификация заболевания
В зависимости от локализации входных ворот и первичного очага сепсис подразделяют на:
- перкутанный (чрескожный) – развивается при попадании возбудителя в организм через поврежденный кожный покров (ранки, царапины, фурункулы и др.);
- акушерско-гинекологический – развивается после родов и абортов;
- оральный (одонтогенный и тонзиллогенный) – развивается в результате первичной инфекции в полости рта;
- оториногенный – развивается в результате распространения инфекции из полости уха и/или носа;
- пневмогенный – при наличии инфекционного очага в нижних дыхательных путях;
- хирургический;
- урологический;
- пупочный – развивается у новорожденных вследствие проникновения инфекционных агентов в кровь через пупочную ранку;
- криптогенный (идиопатический, эссенциальный, генуинный) – сепсис неизвестного происхождения: первичный очаг гнойного воспаления неизвестен.
- молниеносный сепсис,
- острый сепсис,
- подострый сепсис,
- хронический сепсис (хрониосепсис).
По клиническим признакам:
1. Синдром системного воспалительного ответа (ССВО) – системная реакция организма на воздействие различных сильных раздражителей (инфекции, травмы, операции и др.) характеризуется двумя или более признаками:
- температура тела ≥ 38°С или ≤ 36°С;
- частота сердечных сокращений (ЧСС) ≥ 90 ударов в минуту;
- частота дыхания (ЧД) > 20 в минуту или гипервентиляция (РаСО2 ≤ 32 мм рт. ст.);
- лейкоциты крови > 12х109 /л или < 4х109 /л, или незрелых форм >10%.
По виду и характеру возбудителя:
- аэробный сепсис,
- анаэробный сепсис,
- смешанный сепсис,
- грибковый сепсис,
- вирусный сепсис.
Клинические проявления сепсиса могут варьировать от незначительных до критических. При молниеносном течении патологическое состояние развивается бурно - за несколько часов или суток. При остром сепсисе симптомы развиваются за несколько дней. Для хрониосепсиса характерно вялое течение и наличие малозаметных изменений, формирующихся месяцами. Рецидивирующий сепсис протекает с эпизодами обострений и затуханий.
Инкубационный период после выявления ворот инфекции или первичного очага составляет от 1 до 3-5 суток. Начало сепсиса, как правило, острое, хотя иногда может быть подострым или постепенным. Интоксикация проявляется резкой слабостью, адинамией, анорексией, нарушением сна, головной болью, расстройством сознания, менингеальным синдромом (поражением оболочек головного и спинного мозга), тахикардией, артериальной гипотензией. Температура тела держится высокой, со скачками утром и вечером. Признаки интоксикации особенно выражены на высоте лихорадки. На коже у трети больных появляется геморрагическая сыпь.
Со стороны дыхательной системы наблюдаются одышка и хрипы в легких. При нарушении функции почек снижается количество выделяемой мочи (олигурия) вплоть до полного прекращения мочеиспускания (анурия), в моче появляются следы крови, гноя. Наблюдается ухудшение функции печени с развитием желтухи и явлениями гепатита, увеличивается селезенка. Повреждение органов ЖКТ проявляется нарушением пищеварения, отсутствием аппетита, язык сухой, обложенный, нередко наблюдаются упорные септические поносы, тошнота и рвота. Метастазирование возбудителя из первичного очага с образованием вторичных очагов инфекции может приводить к инфаркту легкого, гангрене легкого, гнойному плевриту, эндокардиту (поражению внутренней оболочки сердца), воспалению сердечной мышцы (миокардиту), воспалению околосердечной сумки (перикардиту), гнойному циститу, абсцессам мозга и воспалению оболочек мозга (гнойному менингиту), гнойным артритам, флегмонам и абсцессам в мышцах.
Недостаточность функции одного органа длительностью более суток сопровождается летальностью до 35%, при недостаточности двух органов – 55%, при недостаточности функции трех и более органов летальность к четвертому дню возрастает до 85%.
Производят посевы крови, мочи, ликвора, мокроты, гнойного экссудата из элементов сыпи, абсцессов, пунктатов плевры, суставов и других септических очагов. Посевы делают многократно, чтобы определить чувствительность к максимальному количеству антибиотиков. Используется также обнаружение антигенов в крови методом ИФА и определение генома возбудителя методом ПЦР.
Одним из наиболее специфичных и чувствительных маркеров бактериальной инфекции служит прокальцитониновый тест. Прокальцитонин – один из основных маркёров системного воспаления, вызванного бактериями.
Синонимы: Анализ крови на прокальцитонин; ПКТ. Procalcitonin; PCT. Краткая характеристика определяемого вещества Прокальцитонин Прокальцитонин является прогормоном кальцитонина, состоящим из 116 аминокислот с молекулярной массой 14,5 кDa. Биосинтез прокальцитонина в физиологических условиях прои.
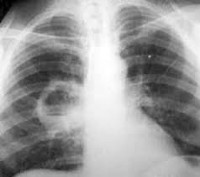
Абсцесс легкого – это неспецифическое воспаление легочной ткани, в результате которого происходит расплавление с образованием гнойно-некротических полостей. В период формирования гнойника отмечается лихорадка, торакалгии, сухой кашель, интоксикация; в период вскрытия абсцесса - кашель с обильным отхождением гнойной мокроты. Диагноз выставляется на основании совокупности клинических, лабораторных данных, рентгенологической картины. Лечение подразумевает проведение массивной противомикробной терапии, инфузионно-трансфузионной терапии, серии санационных бронхоскопий. Хирургическая тактика может включать дренирование абсцесса или резекцию легких.
МКБ-10
Общие сведения

Причины
Золотистый стафилококк, грамотрицательные аэробные бактерии и неспорообразующие анаэробные микроорганизмы являются наиболее распространенной причиной абсцесса легких. Возбудители чаще всего проникают в полость легкого бронхогенным путем. В качестве провоцирующего фактора выступают:
- Поражения рта и ЛОР-органов. При наличии воспалительных процессов в полости рта и носоглотке (пародонтоз, тонзиллит, гингивит и др.) существует вероятность инфицирования легочной ткани.
- Аспирация. Аспирация рвотными массами, например, в бессознательном состоянии или в состоянии алкогольного опьянения, попадание инородных тел тоже может стать причиной абсцесса легких.
- Поражение сосудов легких. Вторичное бронхогенное инфицирование возможно при инфаркте легкого, который происходит из-за эмболии одной из ветвей легочной артерии.
- Сепсис. Варианты заражения гематогенным путем, когда инфекция попадает в легочные капилляры при бактериемии (сепсисе) встречаются редко.
- Травматические повреждения. Во время военных действий и террористических актов абсцесс легкого может образоваться вследствие прямого повреждения или ранения грудной клетки.
В группу риска входят люди с заболеваниями, при которых возрастает вероятность гнойного воспаления, например больные сахарным диабетом. При бронхоэктатической болезни появляется вероятность аспирации зараженной мокротой. При хроническом алкоголизме возможна аспирация рвотными массами, химически-агрессивная среда которых так же может спровоцировать абсцесс легкого.
Патогенез
Начальная стадия характеризуется ограниченной воспалительной инфильтрацией легочной ткани. Затем происходит гнойное расплавление инфильтрата от центра к периферии, в результате чего и возникает полость. Постепенно инфильтрация вокруг полости исчезает, а сама полость выстилается грануляционной тканью, в случае благоприятного течения абсцесса легкого происходит облитерация полости с образованием участка пневмосклероза. Если же в результате инфекционного процесса формируется полость с фиброзными стенками, то в ней гнойный процесс может самоподдерживаться неопределенно длительный период времени (хронический абсцесс легкого).
Классификация
По этиологии абсцессы легких классифицируют в зависимости от возбудителя на:
- пневмококковые;
- стафилококковые;
- коллибациллярные;
- анаэробные;
- вызванные другими возбудителями.
Патогенетическая классификация основана на том, каким образом произошло заражение (бронхогенным, гематогенным, травматическим и другими путями). По расположению в легочной ткани абсцессы бывают центральными и периферическими, кроме того они могут быть единичными и множественными, располагаться в одном легком или быть двусторонними. Некоторые авторы придерживаются мнения, что гангрена легкого - это следующая стадия абсцесса. По происхождению выделяют:
- Первичные абсцессы. Развиваются при отсутствии фоновой патологии у ранее здоровых лиц.
- Вторичные абсцессы. Формируются у лиц с иммуносупрессией (ВИЧ-инфицированных, перенесших трансплантацию органов).
Симптомы абсцесса легких
Болезнь протекает в два периода: период формирования абсцесса и период вскрытия гнойной полости. В период образования гнойной полости отмечаются боли в области грудной клетки, усиливающиеся при дыхании и кашле, лихорадка, порой гектического типа, сухой кашель, одышка, подъем температуры. Но в некоторых случаях клинические проявления могут быть слабо выраженными, например, при алкоголизме болей практически не наблюдается, а температура редко поднимается до субфебрильной.
С развитием болезни нарастают симптомы интоксикации: головная боль, потеря аппетита, тошнота, общая слабость. Первый период абсцесса легкого в среднем продолжается 7-10 дней, но возможно затяжное течение до 2-3 недель или же наоборот, развитие гнойной полости носит стремительный характер и тогда через 2-3 дня начинается второй период болезни.
Симптомы лихорадки и интоксикации после отхождения мокроты начинают снижаться, самочувствие пациента улучшается, анализы крови так же подтверждают угасание инфекционного процесса. Но четкое разделение между периодами наблюдается не всегда, если дренирующий бронх небольшого диаметра, то отхождение мокроты может быть умеренным.
Если причиной абсцесса легкого является гнилостная микрофлора, то из-за зловонного запаха мокроты, пребывание пациента в общей палате невозможно. После длительного стояния в емкости происходит расслоение мокроты: нижний густой и плотный слой сероватого цвета с крошковидным тканевым детритом, средний слой состоит из жидкой гнойной мокроты и содержит большое количество слюны, а в верхних слоях находится пенистая серозная жидкость.
Осложнения
Если в процесс вовлекается плевральная полость и плевра, то абсцесс осложняется гнойным плевритом и пиопневмотораксом, при гнойном расплавлении стенок сосудов возникает легочное кровотечение. Также возможно распространение инфекции, с поражением здорового легкого и с образованием множественных абсцессов, а в случае распространения инфекции гематогенным путем – образование абсцессов в других органах и тканях, то есть генерализация инфекции и бактериемический шок. Примерно в 20% случаев острый гнойный процесс трансформируется в хронический.
Диагностика
Обследование осуществляет врач-пульмонолог. При визуальном осмотре часть грудной клетки с пораженным легким отстает во время дыхания, или же, если абсцесс легких носит двусторонний характер, движение грудной клетки асимметрично. Для уточнения диагноза назначаются следующие процедуры:
- Рентгенография легких. Является наиболее достоверным исследованием для постановки диагноза, а также для дифференциации абсцесса от других бронхолегочных заболеваний.
- Другие инструментальные методики. В сложных диагностических случаях проводят КТ или МРТ легких. ЭКГ, спирография и бронхоскопия назначаются для подтверждения или исключения осложнений абсцесса легкого. При подозрении на развитие плеврита осуществляется плевральная пункция.
- Анализы мокроты. Проводят общий анализ мокроты на присутствие эластических волокон, атипичных клеток, микобактерий туберкулеза, гематоидина и жирных кислот. Бактериоскопию с последующим бакпосевом мокроты выполняют для выявления возбудителя и определения его чувствительности к антибактериальным препаратам.
- Общее исследование крови. В крови ярко выраженный лейкоцитоз, палочкоядерный сдвиг лейкоцитарной формулы, токсичная зернистость нейтрофилов, повышенный уровень СОЭ. Во второй фазе абсцесса легкого анализы постепенно улучшаются. Если процесс хронизируется, то в уровень СОЭ увеличивается, но остается относительно стабильным, присутствуют признаки анемии.
- Биохимический анализ крови. Биохимические показатели крови изменяются – увеличивается количество сиаловых кислот, фибрина, серомукоида, гаптоглобинов и α2- и у-глобулинов; о хронизации процесса говорит снижение альбуминов в крови.
- Исследование мочи. В общем анализе мочи – цилиндрурия, микрогематурия и альбуминурия, степень выраженности изменений зависит от тяжести течения абсцесса легкого.
Лечение абсцесса легкого
Тяжесть течения заболевания определяет тактику его терапии. Возможно как хирургическое, так и консервативное лечение. В любом случае оно проводится в стационаре, в условиях специализированного отделения пульмонологии. Консервативная терапия включает в себя соблюдение постельного режима, придание пациенту дренирующего положения несколько раз в день на 10-30 минут для улучшения оттока мокроты.
Антибактериальная терапия назначается незамедлительно, после определения чувствительности микроорганизмов возможна коррекция антибиотикотерапии. Для реактивации иммунной системы проводят аутогемотрансфузию и переливание компонентов крови. Антистафилакокковый и гамма-глобулин назначается по показаниям. Если естественного дренирования не достаточно, то проводят бронхоскопию с активной аспирацией полостей и с промыванием их растворами антисептиков (бронхоальвеолярный лаваж).
Возможно также введение антибиотиков непосредственно в полость абсцесса легкого. Если абсцесс расположен периферически и имеет большой размер, то прибегают к трансторакальной пункции. Когда же консервативное лечение абсцесса легкого малоэффективно, а также в случаях осложнений показана резекция легкого.
Прогноз и профилактика
Благоприятное течение абсцесса легкого идет с постепенным рассасыванием инфильтрации вокруг гнойной полости; полость теряет свои правильные округлые очертания и перестает определяться. Если процесс не принимает затяжной или осложненный характер, то выздоровление наступает через 6-8 недель. Летальность при абсцессе легкого достаточно высока и на сегодняшний день составляет 5-10%.
Специфической профилактики абсцесса легкого нет. Неспецифической профилактикой является своевременное лечение пневмоний и бронхитов, санация очагов хронической инфекции и предупреждение аспирации дыхательных путей. Так же важным аспектом в снижении уровня заболеваемости является борьба с алкоголизмом.
1. Абсцесс легкого/ Миронов М.Б., Синопальников А.И., Зайцев А.А., Макаревич А.В.//Лечащий врач. - 2008.
3. Нагноительные заболевания легких. Национальные клинические рекомендации/ Корымасов Е.А., Яблонский П.К., Жестков К.Г., Соколович Е.Г. и др.
Бактериальная деструкция легких – это осложнения бактериальной пневмонии, протекающие с развитием гнойно-воспалительных процессов в легком и плевре. Общими проявлениями различных форм бактериальной деструкции легких служат симптомы гнойной интоксикации и дыхательной недостаточности. Диагностика и дифференциальная диагностика основывается на данных рентгенографии легких, УЗИ плевральной полости, торакоцентеза, лабораторного исследования мокроты, экссудата, периферической крови. Основные принципы лечения бактериальной деструкции легких включают антибиотикотерапию, инфузионную детоксикацию, санацию бронхов, по показаниям – пункцию и дренирование плевральной полости, хирургическое лечение.
МКБ-10
Общие сведения
Бактериальная деструкция легких (син. гнойно-деструктивная пневмония) - это воспаление легочной ткани, приобретающее гнойно-некротический характер и приводящее к грубым морфологическим изменениям паренхимы легких. Бактериальной деструкцией легких осложняются около 10% пневмоний у детей, летальность при этом составляет 2–4 %. Среди взрослых гнойно-деструктивная пневмония чаще всего регистрируется у мужчин в возрасте 20-40 лет. Примерно в 2/3 случаев поражается правое легкое, в 1/3 – левое легкое, очень редко (у 1-5% больных) развивается двусторонняя бактериальная деструкция легких. Поскольку данное состояние всегда вторично и развивается на фоне бактериальной пневмонии, важнейшей задачей пульмонологии является поиск путей предупреждения, ранней диагностики и оптимального лечения деструктивных процессов в легких.
Причины
Наиболее частыми инициаторами деструктивных пневмоний выступают стафилококки, зеленящие стрептококки, протей, синегнойная и кишечная палочки. Среди возбудителей отмечается абсолютное преобладание стафилококка, что заставило выделить в особую этиологическую подгруппу стафилококковую деструкцию легких. Реже бактериальную деструкцию легких вызывают палочки Пфейффера и Фридлендера, пневмококки. В большинстве случаев начало гнойно-некротическим процессам дают микробные ассоциации, одновременно представленные 2–3 и более видами бактерий.
В основе развития первичной бактериальной деструкции легких лежит аэрогенный или аспирационный механизм проникновения возбудителей в легкие с развитием бактериальной пневмонии. Факторами риска в этом случае выступают предшествующие воспалению легких ОРВИ, аспирация содержимого носо- и ротоглотки, желудка; ГЭРБ, фиксация инородных тел в бронхах и др. При вторично-метастатической деструкции главенствующее значение принадлежит гематогенному распространению инфекции из локальных гнойных очагов (при остром остеомиелите, фурункулезе, пупочном сепсисе и пр.).
Развитию бактериальной деструкции легких способствуют состояния, сопровождающиеся снижением кашлевого рефлекса, уровня сознания и резистентности организма: никотиновая зависимость, злоупотребление алкоголем, наркомания, профессиональные вредности, ЧМТ, переохлаждение, эпилептические приступы, инсульт, кома, перенесенные инфекции и др. Нередко деструктивные процессы в легочной ткани развиваются вследствие функционирующих пищеводно-бронхиальных свищей, ранения легкого.
Патогенез
В своем развитии бактериальная деструкция легких проходит три стадии: преддеструкции (от 1-2 до 7-14 суток), собственно деструктивных изменений и исхода. Стадия преддеструкции протекает по типу очагово-сливной пневмонии или гнойного лобита. Вторая стадия характеризуется некрозом и распадом легочной паренхимы с последующим отторжением некротических масс и формированием осумкованной гнойной полости. Благоприятным исходом бактериальной деструкции легких является выздоровление с формированием пневмофиброза или кисты легкого, к числу неблагоприятных относятся осложнения и смерть.
Классификация
Бактериальные деструкции легких классифицируются по этиологии, механизму инфицирования, формам поражения, течению. В зависимости от типа возбудителя различают процессы, вызванные аэробной, анаэробной, аэробно-анаэробной флорой. Некоторые авторы на основании этого же принципа различают стафилококковые, стрептококковые, протейные, синегнойные, смешанные деструкции. По механизму поражения патологические процессы делятся на первичные (аэрогенные – 80%) и вторичные (гематогенные – 20%). Среди клинико-рентгенологических форм бактериальной деструкции легких выделяют:
- преддеструкцию (острые массивные пневмонии и лобиты)
- легочные формы (буллы и абсцессы легких)
- легочно-плевральные формы (пиоторакс, пневмоторакс, пиопневмоторакс)
- хронические формы (кисты легких, бронхоэктазы, пневмофиброз, хронический абсцесс легкого, эмпиема плевры) являются исходами острой деструкции.
В клинической практике преобладают легочно-плевральные формы деструкции, на долю легочных приходится всего 15-18%. По динамике течения процесс может быть стабильным, прогрессирующим, регрессирующим; неосложненным и осложненным. Течение бактериальной деструкции легких может быть острым, затяжным и септическим.
Симптомы
Вместе с тем, заподозрить начавшуюся бактериальную деструкцию легких позволяет ряд клинических признаков: гнилостный запах изо рта, тяжелейшая интоксикация, характерная для гнойных процессов (адинамия, тахикардия, температурные пики до 39-40 о С, анорексия и др.). После прорыва абсцесса в бронхи начинается обильное откашливание гнойной зловонной мокроты. На этом фоне отмечается улучшение самочувствия, снижение температуры, повышение активности, появление аппетита и т. д. Если дренирования абсцесса не происходит, гнойно-септический синдром сохраняется и прогрессирует.
При пиотораксе состояние больного ухудшается постепенно. Возникают выраженные боли в груди при дыхании, прогрессирует одышка, температура тела повышается, главным образом, по вечерам. У детей может развиться абдоминальный синдром, симулирующий острый живот, и нейротоксикоз. Бурное клиническое течение может принимать пиопневмоторакс, являющийся следствием разрыва легочной ткани и прорыва гнойного очага в плевральную полость. В этом случае резко возникает приступообразный кашель, одышка, нарастающий цианоз, тахикардия. Вследствие внезапно развившегося коллапса легкого и плевропульмонального шока возможно кратковременное апноэ. При ограниченном пиопневмотораксе вся симптоматика выражена умеренно.
Течению хронических форм бактериальной деструкции легких свойственны признаки гнойной интоксикации (бледный, землисто-серый цвет кожи, недомогание, плохой аппетит, похудание). Беспокоит кашель с умеренным количеством гнойной мокроты с запахом, кровохарканье, небольшая одышка. Типичен легкий цианоз, утолщение дистальных фаланг пальцев.
Осложнения
Различные формы бактериальной деструкции легких могут осложняться легочным кровотечением, внутриплевральным кровотечением (гемотораксом), перикардитом. При массивной инфекции и сниженной иммунной реактивности развивается молниеносный сепсис, при хроническом течении - амилоидоз внутренних органов. Летальные исходы в большинстве своем обусловлены острой почечной недостаточностью, полиорганной недостаточностью.
Диагностика
В анализах крови – признаки активного воспаления: лейкоцитоз со сдвигом влево, значительное повышение СОЭ; увеличение уровня сиаловых кислот, гаптоглобина, серомукоидов, фибрина. Микроскопическое исследование мокроты определяет ее гнойный характер, большое количество лейкоцитов, наличие эластических волокон, холестерина, жирных кислот. Идентификация возбудителя производится при бактериологическом посеве мокроты. Бронхиальный секрет может быть получен как при откашливании, так и во время проведения диагностической бронхоскопии.
Картина, выявляемая по данным рентгенографии легких, различается в зависимости от формы бактериальной деструкции легких. В типичных случаях легочные деструкции определяются в виде полостей с горизонтальным уровнем жидкости, вокруг которых распространяется воспалительная инфильтрация легочной ткани. При плевральных осложнениях выявляется смещение тени средостения в здоровую сторону, уровень жидкости в плевральной полости, частичный или полный коллапс легкого. В этом случае целесообразно дополнение рентгенологической картины данными УЗИ плевральной полости, плевральной пункции и исследования экссудата. Бактериальную деструкцию легких требуется дифференцировать от полостной формы рака легкого, бронхогенных и эхинококковых кист, кавернозного туберкулеза. В проведении дифдиагностики, должны участвовать пульмонологи, торакальные хирурги, фтизиатры.
Лечение бактериальной деструкции легких
В зависимости от формы и течения бактериальной деструкции легких ее лечение может быть консервативным или хирургическим с обязательной госпитализацией в пульмонологический стационар или отделение торакальной хирургии. Консервативный подход возможен при хорошо дренирующихся неосложненных абсцессах легкого, острой эмпиеме плевры.
Независимо от тактики ведения патологии проводится массивная антибактериальная, дезинтоксикационная и иммуностимулирующая терапия. Антибиотики (карбапенемы, фторхинолоны, цефалоспорины, аминогликозиды) вводятся внутривенно, а также эндобронхиально (во время проведения санационных бронхоскопий) и внутриплеврально (в процессе лечебных пункций или проточно-промывного дренирования плевральной полости). Кроме инфузионной детоксикации, в лечении бактериальных деструкций легких находят широкое применение экстракорпоральные методы (ВЛОК, УФОК, плазмаферез, гемосорбция). Иммунокорригирующая терапия предполагает введение гамма-глобулинов, гипериммунной плазмы, иммуномодуляторов и др. В фазе стихания воспаления медикаментозная терапия дополняется методами функциональной реабилитации (физиопроцедурами, ЛФК).
Из оперативных методов лечения при неадекватном опорожнение гнойника в легком используется пневмотомия (открытое дренирование), иногда – резекционные вмешательства (лобэктомия, билобэктомия) или пневмонэктомия. При хронической эмпиеме плевры может потребоваться проведение торакопластики или плеврэктомии с декортикацией легкого.
Прогноз и профилактика
Полным выздоровлением заканчивается примерно четверть случаев бронхиальной деструкции легких; у половины больных достигается клиническое выздоровление с сохранением остаточных рентгенологических изменений. Хронизация заболевания происходит в 15-20% наблюдений. Летальным исходом заканчивается 5-10% случаев. Основу профилактики развития бактериальной деструкции легких составляет своевременная антибиотикотерапия бактериальных пневмоний и гнойных внелегочных процессов, клинико-рентгенологических контроль излеченности, повышенное внимание к больным группы риска по развитию деструктивных процессов в легких. На этапе первичной профилактики важна пропаганда здорового образа жизни, борьба с алкоголизмом и наркоманией.
1. Гнойные заболевания легких и плевры: Учебно-методическое пособие/ Голуб А.М., Алексеев С.А. – 2012.
2. Лучевая диагностика инфекционных деструкций легких/ Тюрин И.Е.//Пульмонология и аллергология. – 2009 - №2.
3. Осложнения пневмонии. Хронические неспецифические бронхолегочные заболевания у детей/ Миронова Э.В., Долбня С.В. – 2016.
Читайте также:

