Септический шок у детей презентация
Обновлено: 18.04.2024
1. Интенсивная терапия инфекционно-токсического (септического) шока у детей (2016-2017 гг)
Интенсивная терапия
инфекционнотоксического
(септического) шока у
детей (2016-2017 гг)
к.мед.н. ассистент Давыдова А.Г.
Запорожский государственный медицинский
университет
Кафедра детских болезней ФПО, курс детской
анестезиологии
2. Шок у детей История
• Доставка жидкости и летальность:
Подкожно 1960 г – летальность 67/100000
Металлические иглы 1975 г – летальность 23/100000
Пластиковые катетеры 1985 г - летальность –
2,6/100000
3. Септический шок
• Септический шок – это синдром
недостаточности перфузии тканей с
неадекватной доставкой и потреблением
кислорода, сопровождающийся артериальной
гипотензией, несмотря на коррекцию
внутрисосудистого объема, инфекционного
генеза.
• Патогенез СШ представляет собой сложный
процесс, различные бактериальные и
грибковые эндо- и экзотоксины вызывают в
организме генерализованную чрезмерную
воспалительную реакцию – синдром системного
воспалительного ответа (ССВО, англ. SARS),
который характерен почти для любого вида
запущенного шока, но особенно важную роль
играет в патогенезе СШ.
• Тяжесть патологического процесса при сепсисе в
большей степени зависит от интенсивности ответа
организма на повреждение, чем от прямого
повреждающего эффекта самой инфекции. Тяжелый
сепсис и септический шок возникают у пациентов с
чрезмерным или плохо контролируемым иммунным
ответом организма, который проявляется
генерализованной воспалительной реакцией.
• Такая несбалансированная реакция может быть опасной
для организма вследствие повышенной продукции
противовоспалительных факторов, которые в норме
являются компонентом защитной реакции иммунной
системы. Однако, являясь весьма агрессивными, они
становятся причиной повреждения клеток, органов и
систем собственного организма.
• К наиболее изученным противовоспалительным
субстанциям при СШ относят фактор некроза опухоли
(TNF) (IL-1В, IL-6, IL-8); тромбоксаны; фактор,
активирующий тромбоциты (PAF) и эйкозаноиды
(продукты метаболизма арахидоновой кислоты).
• Важным патогенетическим звеном СШ является
нарушение функции эндотелия и активация системы
гемостаза с подавлением системы фиблинолиза.
Профиль эндотелиальной активности меняется с
антикоагулянтного на прокоагулянтный, цитокины
стимулируют образование нейтрофилами и
макрофагами большого количества тканевого фактора
свертываемости, что активирует весь коагуляционный
каскад.
• Возрастание прокоагулянтной активности также
связано с ингибицией факторов антикоагуляции и
фибринолиза (активный протеин С, ингибитор
тканевого фактора, антитромбин ІІІ). Кроме этого,
активируется система комплемента (особенно
агрессивным является фрагмент С5а). Эти процессы
приводят к нарушениям перфузии тканей вследствие
нарушения микроциркуляции, а также выхода жидкости
из внутрисосудистого сектора в результате нарушения
проницаемости эндотелия.
Методы контроля за проведением
интенсивной терапии
1. Гемоконцентрационные показатели
(гемоглобин, гематокрит, эритроциты). При
продолжающемся кровотечении необходимо
поддержание уровня гемоглобина не ниже
100 г/л.
2. Уровень артериального давления и
центрального венозного давления. ЦВД
необходимо удерживать в пределах 5 – 10
см/вод/ст.
3. Почасовой диурез должен составлять не менее
1 – 2 мл/кг/час.
8. Патофизиологические и клинические стадии ИТШ.
12. Основными методами лечения СШ являются:
Основными методами лечения СШ
являются:
Адекватная санация очага инфекции,
включая при необходимости ранее
агрессивное хирургическое
вмешательство;
Рациональная атибиотикотерапия;
Терапия, направленная на поддержание
сердечно-сосудистой, дыхательной, и
функции и питания организма;
Патогенетическая терапия ССВО.
13. Антибактериальная терапия при СШ
14. Антибактериальная терапия при СШ
• Для более адекватного эмпирического выбора
антибиотика необходимо учитывать госпитальный
или негоспитальный характер инфекции. Вместе с
тем, должен выполняться и второй принцип –
ранняя адекватная антибиотикотерапия
достоверно снижает летальность. У пациентов, не
получавших адекватную антибиотикотерапию в
начале заболевания, летальность на 10-15% выше.
• Поэтому предоставляется целесообразным
использовать так называемый деэкалационный
принцип антибиотикотерапии с начальным
назначением антибиотиков максимально широкого
спектра действия (карбапенемы, цефалоспорины
4-го поколения) с последующей деэскалацией (если
возможно) спектра применяемого антибиотика
после получения результата бактериологического
анализа.
15. Респираторная поддержка
• Легкие являются одной из первоочередных мишеней
сепсиса, поэтому ТС и СШ являются причиной
синдрома острого повреждения легких и еще более
тяжелого расстройства функции дыхания – острого
респираторного дистресс-синдрома.
• Для коррекции гипоксемии необходима
оксигенотерапия, а в тяжелых случаях ИВЛ
• Насыщение кислородом гемоглобина артериальной
крови не должно снижаться ниже 90%. До 85%
пациентов с СШ нуждаются в респираторной
поддержке приблизительно в течении 1-2 недель.
16. Гемодинамическая поддержка
• Основной задачей гемодинамической поддержки является
поддержание перфузии органов и тканей. Необходимо
контролировать следующие параметры: сердечный выброс,
сердечный индекс, общее периферическое сосудистое
сопротивление, частоту сокращений сердца, давление
заклинивания в легочной артерии, артериальное давление,
диурез.
• Показателями, которые зависят как от кровообращения, так
и от дыхания, являются: уровень сознания, доставка и
потребление кислорода тканями, насыщение кислородом
смешанной венозной крови, уровень лактата.
17. Гемодинамическая поддержка
18. Гемодинамическая поддержка
• При недостаточном эффекте объемной ресусцитации,
для нормализации параметров гемодинамики и
необходима вазопрессорная поддержка. Применение
альфа-1- адренэргических агонистов обосновано
теоретически снижением общего периферического
сопротивления сосудов при СШ. Поэтому их применение
улучшает прогноз при СШ.
• Поскольку при СШ быстро снижается сократительная
функция миокарда, необходима также кардиотоническая
поддержка. Добутамин является препаратом выбора для
инотропной поддержки.
• Одной из наиболее эффективных считается комбинация
добутамина и норадреналина. Но (!), вазоконстрикторы
следует применять только после восполнения
внутрисосудистого объема, поскольку они могут
усиливать глобальную и региональную ишемию тканей,
особенно это касается спланхнического и почечного
кровотока, а также провоцировать нарушения ритма
сердца.
19. Коррекция метаболизма
• Выраженный лактоацидоз, который
развивается в результате преобладания
анаэробного гликолиза, может сам стать
одной из причин неэффективности
катехоламинов. В этих случаях, не только при
рН крови раствора гидракарбоната (соды).
• Показания к переливанию препаратов крови у
пациентов с ТС и СШ ограничены. Считают,
что оптимальный уровень гемоглобина у
пациентов с СШ должен достигать 90-100 г/л.
Однако и меньший уровень гемоглобина в
крови не всегда является показанием к
гемотрансфузиям
20. АНАФИЛАКТИЧЕСКИЙ ШОК
• Анафилаксия включает антиген и антитела к
иммуноглобулину Е и является результатом
предварительной сенсибилизации к антигену.
Анафилактоидная реакция реализуется
гистамином и может возникнуть при первом
контакте с антигеном.
Активация комплемента связана как с
иммуноглобулином Е так и с
неиммуноглобулиновым ответом и
реализуется гистамином и другими
компонентами.
21. Этиология
• Сенсибилизация пациента предшествующими
контактами с антигеном с последующей
выработкой антигенспецифических Ig Е
антител.
Специфические физиологические процессы
– дегрануляция тучных клеток и базофилов и
высвобождение гистамина, лейкотриенов и
простагландинов, активация комплемента.
В США около 500 человек в год умирает от
анафилактического шока, и 75% этих смертей
вызвана аллергией на пенициллин.
23. Причины анафилаксии
Антибиотики.
Биологические агенты (чужеродная
сыворотка, химотрипсин, вакцины)
Препараты (декстраны).
Местные анестетики.
Аспирин.
Яд перепончатокрылых насекомых.(клещи,
осы, шершни).
Аллергические экстракты для тестов и
лечебные растворы.
Пищевые продукты (яйца, орехи и др.)
Внутривенное введение наркотиков.
24. Клиника
Со стороны ЦНС – возбуждение или адинамия,
вплоть до сопора и комы. В начале пациенты
могут жаловаться на резкую слабость и
головокружение.
Со стороны кожи – сыпь, гиперемия, крапивница ,
зуд, отек Квинке.
Со стороны дыхательной системы – стридор,
отек гортани, бронхоспазм, дистанционные
свистящие хрипы, удушье, отек легких.
Со стороны сердечно – сосудистой системы –
прогрессирующая гипотензия и коллапс, пульс
частый и слабого наполнения, резко выражена
тахикардия. При прогрессировании шока или при
“молниеносном” шоке – брадикардия,
переходящая в асистолию.
25. Патофизиология
• Недостаточность кровообращения. возникающая от
снижения сердечного выброса является основной
причиной смерти во время СВ сердечного выброса
включает снижение венозного притока, нарушения
сердечного ритма, гемоконцентрацию с увеличением
вязкости крови , повышение сопротивления в легочных
сосудах, правожелудочковую сердечную
недостаточность, снижение коронарного кровотока
вследствие гипотензии и спазма коронарных сосудов.
Длительная гипотензия может привести к ишемии
миокарда и нарушению функции левого желудочка.
• Повышение УОС и СВ, наблюдаемые в начале
анафилактических реакций, могут бать обусловлены
резким снижением нагрузки и инотропным действием
гистамина так и приростом выброса катехоламинов в
ответ на высвобождение гистамина и развитие
гипотензии.
26. Патофизиология (продолжение)
• Бронхоспазм развивается в следствие
воздействия медиаторов, ведущее к
сокращению гладкой мускулатуры, набуханию и
гиперсекреции слизистой оболочки. Тяжелый
бронхоспазм может перейти в астмастатус.
Гистамин, метаболиты арахидоновой кислоты и
фактор активирующий тромбоциты вызывают
еритему зуд и отек (крапивница).
• Ангионевротический отек развивается в
результате повышения проницаемости
подкожных сосудов, что в свою очередь
приводит к периорбитальному, пероральному
27. Клиника
Со стороны ЦНС – возбуждение или адинамия,
вплоть до сопора и комы. В начале пациенты
могут жаловаться на резкую слабость и
головокружение.
Со стороны кожи – сыпь, гиперемия,
крапивница , зуд, отек Квинке.
Со стороны дыхательной системы – стридор,
отек гортани, бронхоспазм, дистанционные
свистящие хрипы, удушье, отек легких.
Со стороны сердечно – сосудистой системы
– прогрессирующая гипотензия и коллапс, пульс
частый и слабого наполнения, резко выражена
тахикардия. При прогрессировании шока или
при “молниеносном” шоке – брадикардия,
переходящая в асистолию.
28. Алгоритм интенсивной терапии.
Наложение жгута (если инъекция сделана в
конечность или укус насекомого).
Адреналин 0,1% в разведении 1:10 – производят
обкалывание места инъекции или укуса для
уменьшения резорбции. В/венно начальная доза
адреналина 0,01 мг/кг (0,1 мл 0,1% раствора на
каждые 10 кг массы тела). Если АД не
стабилизируется , дозы удваиваются.Раствор
вводится в центральне вены, может вводится
эндотрахеально, сублингвально а также
внутрисердечно (при асистолии).
Оксигенотерапия 100% кислородом , при
нарастании острой дыхательной недостаточности –
интубация трахеи и перевод ребенка на ИВЛ. При
нарастании отека гортани и обструкции верхних
дыхательных путей и сложности интубации трахеи –
29. Алгоритм интенсивной терапии (продолжение)
Экстренное объемное восполнение
кристаллоидами (рингер, физиологический
раствор) – 20 мл/кг; и коллоидами (рефортан,
стабизол, реополиглюкин, полиглюкин) из
рассчета 10 -20 мл/кг.Необходимо избегать
введения белковых препаратов.
Кортикостероиды (преднизолон – 10–20 мг/кг
или дексазон – 2-3 мг/кг).
При развитии бронхоспазма или астмастатуса
– эуфиллин 2,4% на физиологическом
растворе в дозе насыщения 5-6 мг/кг в
течении 30 мин. В дальнейшем инфузоматом
– 10-15 мг/кг/сутки.
1. Интенсивная терапия инфекционно-токсического (септического) шока у детей (2016-2017 гг)
Интенсивная терапия
инфекционнотоксического
(септического) шока у
детей (2016-2017 гг)
к.мед.н. ассистент Давыдова А.Г.
Запорожский государственный медицинский
университет
Кафедра детских болезней ФПО, курс детской
анестезиологии
2. Шок у детей История
• Доставка жидкости и летальность:
Подкожно 1960 г – летальность 67/100000
Металлические иглы 1975 г – летальность 23/100000
Пластиковые катетеры 1985 г - летальность –
2,6/100000
3. Септический шок
• Септический шок – это синдром
недостаточности перфузии тканей с
неадекватной доставкой и потреблением
кислорода, сопровождающийся артериальной
гипотензией, несмотря на коррекцию
внутрисосудистого объема, инфекционного
генеза.
• Патогенез СШ представляет собой сложный
процесс, различные бактериальные и
грибковые эндо- и экзотоксины вызывают в
организме генерализованную чрезмерную
воспалительную реакцию – синдром системного
воспалительного ответа (ССВО, англ. SARS),
который характерен почти для любого вида
запущенного шока, но особенно важную роль
играет в патогенезе СШ.
• Тяжесть патологического процесса при сепсисе в
большей степени зависит от интенсивности ответа
организма на повреждение, чем от прямого
повреждающего эффекта самой инфекции. Тяжелый
сепсис и септический шок возникают у пациентов с
чрезмерным или плохо контролируемым иммунным
ответом организма, который проявляется
генерализованной воспалительной реакцией.
• Такая несбалансированная реакция может быть опасной
для организма вследствие повышенной продукции
противовоспалительных факторов, которые в норме
являются компонентом защитной реакции иммунной
системы. Однако, являясь весьма агрессивными, они
становятся причиной повреждения клеток, органов и
систем собственного организма.
• К наиболее изученным противовоспалительным
субстанциям при СШ относят фактор некроза опухоли
(TNF) (IL-1В, IL-6, IL-8); тромбоксаны; фактор,
активирующий тромбоциты (PAF) и эйкозаноиды
(продукты метаболизма арахидоновой кислоты).
• Важным патогенетическим звеном СШ является
нарушение функции эндотелия и активация системы
гемостаза с подавлением системы фиблинолиза.
Профиль эндотелиальной активности меняется с
антикоагулянтного на прокоагулянтный, цитокины
стимулируют образование нейтрофилами и
макрофагами большого количества тканевого фактора
свертываемости, что активирует весь коагуляционный
каскад.
• Возрастание прокоагулянтной активности также
связано с ингибицией факторов антикоагуляции и
фибринолиза (активный протеин С, ингибитор
тканевого фактора, антитромбин ІІІ). Кроме этого,
активируется система комплемента (особенно
агрессивным является фрагмент С5а). Эти процессы
приводят к нарушениям перфузии тканей вследствие
нарушения микроциркуляции, а также выхода жидкости
из внутрисосудистого сектора в результате нарушения
проницаемости эндотелия.
Методы контроля за проведением
интенсивной терапии
1. Гемоконцентрационные показатели
(гемоглобин, гематокрит, эритроциты). При
продолжающемся кровотечении необходимо
поддержание уровня гемоглобина не ниже
100 г/л.
2. Уровень артериального давления и
центрального венозного давления. ЦВД
необходимо удерживать в пределах 5 – 10
см/вод/ст.
3. Почасовой диурез должен составлять не менее
1 – 2 мл/кг/час.
8. Патофизиологические и клинические стадии ИТШ.
12. Основными методами лечения СШ являются:
Основными методами лечения СШ
являются:
Адекватная санация очага инфекции,
включая при необходимости ранее
агрессивное хирургическое
вмешательство;
Рациональная атибиотикотерапия;
Терапия, направленная на поддержание
сердечно-сосудистой, дыхательной, и
функции и питания организма;
Патогенетическая терапия ССВО.
13. Антибактериальная терапия при СШ
14. Антибактериальная терапия при СШ
• Для более адекватного эмпирического выбора
антибиотика необходимо учитывать госпитальный
или негоспитальный характер инфекции. Вместе с
тем, должен выполняться и второй принцип –
ранняя адекватная антибиотикотерапия
достоверно снижает летальность. У пациентов, не
получавших адекватную антибиотикотерапию в
начале заболевания, летальность на 10-15% выше.
• Поэтому предоставляется целесообразным
использовать так называемый деэкалационный
принцип антибиотикотерапии с начальным
назначением антибиотиков максимально широкого
спектра действия (карбапенемы, цефалоспорины
4-го поколения) с последующей деэскалацией (если
возможно) спектра применяемого антибиотика
после получения результата бактериологического
анализа.
15. Респираторная поддержка
• Легкие являются одной из первоочередных мишеней
сепсиса, поэтому ТС и СШ являются причиной
синдрома острого повреждения легких и еще более
тяжелого расстройства функции дыхания – острого
респираторного дистресс-синдрома.
• Для коррекции гипоксемии необходима
оксигенотерапия, а в тяжелых случаях ИВЛ
• Насыщение кислородом гемоглобина артериальной
крови не должно снижаться ниже 90%. До 85%
пациентов с СШ нуждаются в респираторной
поддержке приблизительно в течении 1-2 недель.
16. Гемодинамическая поддержка
• Основной задачей гемодинамической поддержки является
поддержание перфузии органов и тканей. Необходимо
контролировать следующие параметры: сердечный выброс,
сердечный индекс, общее периферическое сосудистое
сопротивление, частоту сокращений сердца, давление
заклинивания в легочной артерии, артериальное давление,
диурез.
• Показателями, которые зависят как от кровообращения, так
и от дыхания, являются: уровень сознания, доставка и
потребление кислорода тканями, насыщение кислородом
смешанной венозной крови, уровень лактата.
17. Гемодинамическая поддержка
18. Гемодинамическая поддержка
• При недостаточном эффекте объемной ресусцитации,
для нормализации параметров гемодинамики и
необходима вазопрессорная поддержка. Применение
альфа-1- адренэргических агонистов обосновано
теоретически снижением общего периферического
сопротивления сосудов при СШ. Поэтому их применение
улучшает прогноз при СШ.
• Поскольку при СШ быстро снижается сократительная
функция миокарда, необходима также кардиотоническая
поддержка. Добутамин является препаратом выбора для
инотропной поддержки.
• Одной из наиболее эффективных считается комбинация
добутамина и норадреналина. Но (!), вазоконстрикторы
следует применять только после восполнения
внутрисосудистого объема, поскольку они могут
усиливать глобальную и региональную ишемию тканей,
особенно это касается спланхнического и почечного
кровотока, а также провоцировать нарушения ритма
сердца.
19. Коррекция метаболизма
• Выраженный лактоацидоз, который
развивается в результате преобладания
анаэробного гликолиза, может сам стать
одной из причин неэффективности
катехоламинов. В этих случаях, не только при
рН крови раствора гидракарбоната (соды).
• Показания к переливанию препаратов крови у
пациентов с ТС и СШ ограничены. Считают,
что оптимальный уровень гемоглобина у
пациентов с СШ должен достигать 90-100 г/л.
Однако и меньший уровень гемоглобина в
крови не всегда является показанием к
гемотрансфузиям
20. АНАФИЛАКТИЧЕСКИЙ ШОК
• Анафилаксия включает антиген и антитела к
иммуноглобулину Е и является результатом
предварительной сенсибилизации к антигену.
Анафилактоидная реакция реализуется
гистамином и может возникнуть при первом
контакте с антигеном.
Активация комплемента связана как с
иммуноглобулином Е так и с
неиммуноглобулиновым ответом и
реализуется гистамином и другими
компонентами.
21. Этиология
• Сенсибилизация пациента предшествующими
контактами с антигеном с последующей
выработкой антигенспецифических Ig Е
антител.
Специфические физиологические процессы
– дегрануляция тучных клеток и базофилов и
высвобождение гистамина, лейкотриенов и
простагландинов, активация комплемента.
В США около 500 человек в год умирает от
анафилактического шока, и 75% этих смертей
вызвана аллергией на пенициллин.
23. Причины анафилаксии
Антибиотики.
Биологические агенты (чужеродная
сыворотка, химотрипсин, вакцины)
Препараты (декстраны).
Местные анестетики.
Аспирин.
Яд перепончатокрылых насекомых.(клещи,
осы, шершни).
Аллергические экстракты для тестов и
лечебные растворы.
Пищевые продукты (яйца, орехи и др.)
Внутривенное введение наркотиков.
24. Клиника
Со стороны ЦНС – возбуждение или адинамия,
вплоть до сопора и комы. В начале пациенты
могут жаловаться на резкую слабость и
головокружение.
Со стороны кожи – сыпь, гиперемия, крапивница ,
зуд, отек Квинке.
Со стороны дыхательной системы – стридор,
отек гортани, бронхоспазм, дистанционные
свистящие хрипы, удушье, отек легких.
Со стороны сердечно – сосудистой системы –
прогрессирующая гипотензия и коллапс, пульс
частый и слабого наполнения, резко выражена
тахикардия. При прогрессировании шока или при
“молниеносном” шоке – брадикардия,
переходящая в асистолию.
25. Патофизиология
• Недостаточность кровообращения. возникающая от
снижения сердечного выброса является основной
причиной смерти во время СВ сердечного выброса
включает снижение венозного притока, нарушения
сердечного ритма, гемоконцентрацию с увеличением
вязкости крови , повышение сопротивления в легочных
сосудах, правожелудочковую сердечную
недостаточность, снижение коронарного кровотока
вследствие гипотензии и спазма коронарных сосудов.
Длительная гипотензия может привести к ишемии
миокарда и нарушению функции левого желудочка.
• Повышение УОС и СВ, наблюдаемые в начале
анафилактических реакций, могут бать обусловлены
резким снижением нагрузки и инотропным действием
гистамина так и приростом выброса катехоламинов в
ответ на высвобождение гистамина и развитие
гипотензии.
26. Патофизиология (продолжение)
• Бронхоспазм развивается в следствие
воздействия медиаторов, ведущее к
сокращению гладкой мускулатуры, набуханию и
гиперсекреции слизистой оболочки. Тяжелый
бронхоспазм может перейти в астмастатус.
Гистамин, метаболиты арахидоновой кислоты и
фактор активирующий тромбоциты вызывают
еритему зуд и отек (крапивница).
• Ангионевротический отек развивается в
результате повышения проницаемости
подкожных сосудов, что в свою очередь
приводит к периорбитальному, пероральному
27. Клиника
Со стороны ЦНС – возбуждение или адинамия,
вплоть до сопора и комы. В начале пациенты
могут жаловаться на резкую слабость и
головокружение.
Со стороны кожи – сыпь, гиперемия,
крапивница , зуд, отек Квинке.
Со стороны дыхательной системы – стридор,
отек гортани, бронхоспазм, дистанционные
свистящие хрипы, удушье, отек легких.
Со стороны сердечно – сосудистой системы
– прогрессирующая гипотензия и коллапс, пульс
частый и слабого наполнения, резко выражена
тахикардия. При прогрессировании шока или
при “молниеносном” шоке – брадикардия,
переходящая в асистолию.
28. Алгоритм интенсивной терапии.
Наложение жгута (если инъекция сделана в
конечность или укус насекомого).
Адреналин 0,1% в разведении 1:10 – производят
обкалывание места инъекции или укуса для
уменьшения резорбции. В/венно начальная доза
адреналина 0,01 мг/кг (0,1 мл 0,1% раствора на
каждые 10 кг массы тела). Если АД не
стабилизируется , дозы удваиваются.Раствор
вводится в центральне вены, может вводится
эндотрахеально, сублингвально а также
внутрисердечно (при асистолии).
Оксигенотерапия 100% кислородом , при
нарастании острой дыхательной недостаточности –
интубация трахеи и перевод ребенка на ИВЛ. При
нарастании отека гортани и обструкции верхних
дыхательных путей и сложности интубации трахеи –
29. Алгоритм интенсивной терапии (продолжение)
Экстренное объемное восполнение
кристаллоидами (рингер, физиологический
раствор) – 20 мл/кг; и коллоидами (рефортан,
стабизол, реополиглюкин, полиглюкин) из
рассчета 10 -20 мл/кг.Необходимо избегать
введения белковых препаратов.
Кортикостероиды (преднизолон – 10–20 мг/кг
или дексазон – 2-3 мг/кг).
При развитии бронхоспазма или астмастатуса
– эуфиллин 2,4% на физиологическом
растворе в дозе насыщения 5-6 мг/кг в
течении 30 мин. В дальнейшем инфузоматом
– 10-15 мг/кг/сутки.
Презентация на тему: " Российский национальный исследовательский медицинский университет имени Н. И. Пирогова Кафедра терапии Педиатрического факультета Сепсис. Септический шок." — Транскрипт:
2 Реальная эпидемиология сепсиса в России и других цивилизованных странах неизвестна случаев сепсиса в год в США (более случаев в день). 2% госпитализаций 11-е место среди причин смерти Более чем в 30% случаев сепсиса точный источник инфекции не выявляется Летальность при сепсисе сохраняется на уровне % При адекватно проведенных бактериологических исследованиях частота выявления бактериемии не превышает 45%. В год затрачивается $16,7 биллионов; $22,000 - на пациента Мужчины>женщины Старше 65 лет, чаще в зимнее время, темнокожие. У пациентов с раком риск септического состояния в 10 раз выше
3 Стандартизованные показатели заболеваемости сепсисом по полу ( no./ ) Мужчины Женщины Рис.1 Стандартизованные показатели заболеваемости сепсисом по полу Точки на графике отражают показатель заболеваемости, горизонтальные штриховые линии - величину стандартной ошибки. Martin et al: N Engl J Med 2003:348:1546
4 Рис.2 Увеличение заболеваемости и смертности от тяжелого сепсиса с возрастом Смертность Заболеваемость Angus Crit Care Med 29:1301, 2001
5 Патогенез сепсиса и септического шока: Бактериальная инфекция Избыточный ответ организма Медиаторы воспаления, БАВ приводят к повреждению клеток Повреждение органов Смерть
6 Синдром системного ответа на воспаление: 1. Проникновение инфекции и других повреждающих факторов Активация комплемента Активация тромбоцитов Стимуляция хемотаксиса и фагоцитоза 2. Активация нейтрофилов (одновременно) Выделение кислородных радикалов Повреждение и активация эндотелия 3. Активация макрофагов (одновременно) Представление антигенов лимфоцитам Активация, пролиферация лимфоцитов Синтез антител, цитокинов, медиаторов воспаления
7 Синдром системного ответа на воспаление: Эндотелий: Повреждениепродукция NO, эндотелина, фактора активации ТЦ, цитокинов. Лейкоцитыкраевое стояние тромбы из ЛЦ,ТЦ, фибрина. Итог: поражение микроциркуляторного русла за пределами очага нарушение функций органов и систем. Цитокины, NO приводят к: Снижение венозного тонуса Нарушение перфузии тканей Очаги ишемии Депонирование крови Отеки Полиорганная дисфункция
8 Определения: Синдром системной воспалительной реакции (2 и более критериев): Т>38ºC или 90/мин ЧД >20/мин Лейкоциты >12,000/мм³;
9 Инфекция Паразиты Вирусы Грибы Бактерии Травма Ожоги Сепсис SIRS Тяжелыйсепсис Adapted from SCCM ACCP Consensus Guidelines Шок Операции
10 Тяжелый сепсис – сепсис в сочетании с поражением 1 и более систем органов. ЦНС – изменение неврологического статуса Кровь – ТЦ 176,8 мкмоль/л (увеличение на 44,2 мкмоль/л), острая олигурия 20/мин, SaO2
11 Bernard NEJM 344:699, 2001 Рис.3 Нарушение функций органов на момент выявления тяжелого сепсиса
12 From Brealey & Singer, 2000 Рис.4 Зависимость между смертностью пациентов в ОРИТ и количеством пораженных органов Смертность, %
13 Септический шок – сепсис в сочетании с рефрактерной гипотонией САД
15 Частота выявления возбудителей при тяжелом сепсисе Data from Bochud et al. 42
16 Диагностика: Факторы риска: Возраст Иммуннодефицитные состояния Пол Протезированные клапаны Раса Мочевые катетеры Осмотр: 1)Лихорадка 2)Тахикардия 3)Тахипноэ 4)Гипотония 5)Идентифицированный источник инфекции
17 Лабораторная диагностика при подозрении на тяжелый сепсис: 1)ОАК 2)Креатинин 3)Печеночные ферменты 4)Лактат артериальной крови 5)Газы крови, электролиты 6)Коагулограмма Тромбоцитопения – независимый фактор риска развитий органной недостаточности и плохого прогноза. Может свидетельствовать о начале развития ДВС. См: Д-димер, фибриноген, продукты распада фибрина Лактат - плохой прогноз
20 Инотропные пр-ты Оксигенотерапия ± эндотрахеальная интубация и механическая вентиляция. Катетеризация центральной вены и артерии Седативная терапия и т.д. 70% Цель достигнута Да Ура! Кристаллоиды Коллоиды Вазоактивные пр-ты Эритромасса(до Нt30%)
21 Лечение: 1. Контроль за очагом инфекции: Дренаж очага Иссечение некротизированных тканей. Извлечение инфицированного катетера, протеза и т.д. 2. Антибактериальная терапия После забора крови на посев, начинают эмпирическую антибактериальную терапию в/в в течение 1 часа после диагностирования тяжелого сепсиса или септического шока (7-10 дней).
22 3. Инфузионная терапия Безопасность и эффективность коллоидов и кристаллоидов одинаковая. (незначительное снижение смертности при применении коллоидов). При подозрении на гиповолемию: 1000 мл кристаллоидов или мл коллоидов за 30 мин. 4. Вазопрессорные препараты Применяют, если АДср
23 5. Инотропная терапия Если SvO2 остается
25 9. Контроль гликемии Агрессивная терапия инсулином до уровня глюкозы 8 ммоль/л. Снижает смертность. При нормогликемии – 10%, при гликемии >16 ммоль/л – 43%. 10. Профилактика тромбоза глубоких вен. 1) гепарины 3) компрессионный трикотаж 11. Профилактика стрессорных язв. Всем пациентам с тяжелым сепсисом показано назначение: ингибиторов протонной помпы или блокаторов Н2-рецепторов
26 Известные люди, умершие от сепсиса. Персона Год смерти Причина смерти Людовик IV 1715Гангрена ноги Джоаккино Россини 1868Оперативное вмешательство Жорж Бизе 1875Абсцесс в области лице Эдуард Мане 1883Ампутация ноги Гюстав Малер 1911Стрептококковая инфекция Александр Скрябин 1915Абсцесс верхней губы
2 Инфекционно-токсический шок – (септический, бактериальный, эндотоксиновый ) - это острая недостаточность кровообращения, приводящая к тяжелым метаболическим нарушениям и развитию полиорганной недостаточности. Инфекционно-токсический шок развивается в результате воздействия эндотоксинов и бактериальных продуктов на клеточные мембраны, компоненты свертывания крови и комплемент, что приводит к повышению свертываемости, повреждению клеток и нарушению кровотока, особенно микроциркуляции.
3 Э ТИОЛОГИЯ ИТШ: Бактериальные (менингококковая инфекция, брюшной тиф, чума, дизентерия, сибирская язва). Вирусные (грипп,геморрагическая лихорадка). Риккетсиозные, спирохетозные и грибковые болезни Чаще ИТШ вызывается грамотрицательной микрофлорой, однако в 1/3 случаев причиной возникновения шока являются грамположительные микроорганизмы (стрептококки, пневмококки). На фоне хронических воспалительных процессов ИТШ может быть вызван протеем, клебсиеллами, синегнойной палочкой, аэробактером.
4 Патогенез Роль пускового механизма при ИТШ отводится массивному проникновению в кровь возбудителя или его токсинов. При этом особое значение имеет их тропизм к эндотелию сосудов и ЦНС, который проявляется независимо от этиологии инфекционного заболевания. Для возникновения ИТШ необходимо, по крайней мере, наличие двух факторов: 1. возбудитель болезни и его токсины 2. повышенная чувствительность к нему организма больного.
5 Патогенез инфекционно- токсического шока на уровне мелких сосудов. 1. В кровь поступает большое количество микробных токсинов ( способствовать этому может массивное разрушение бактерий при антибиотикотерапии ). 2. Это приводит к резкому выбросу цитокинов, катехоламинов, биологически активных веществ ( серотонин,гистамин, кинины ). 3. Под действием БАВ происходит выраженный спазм артериол и пост капиллярных венул. 4. Это приводит к открытию артерио - венозных шунтов.
6 5. Кровь, сбрасываемая по шунтам, не выполняет трофическую функцию, что приводит к ишемии тканей и метаболическому ацидозу. 6. Компенсаторный эффект катехоламинов становится недостаточным,а нарастающий ацидоз еще больше снижает их активность. 7. В результате наступает парез артериол, в то время как пост капиллярные венулы находятся в состоянии повышенного тонуса. 8. Кровь депонируется в капиллярах, это приводит к выходу ее части в межклеточное пространство. Происходит застой в зоне микроциркуляции.
9 С ХЕМА ПАТОГЕНЕЗА ИНФЕКЦИОННО - ТОКСИЧЕСКОГО ШОКА
10 Классификация ИТШ по R. М. Hardaway (1963) предполагает выделение 2 стадий: Стадия 1. Обратимый шок, имеющий 3 фазы развития: 1. Ранний обратимый шок. 2. Поздний обратимый шок. 3. Устойчивый обратимый шок. Стадия 2. Необратимый шок.
11 Стадия 1.1 характеризуется спазмом в микроциркуляторном русле и начальными явлениями гипоксии в тканях. Стадия 1.2 отличается дилатацией микроциркуляторного русла и депонированием в нем крови, нарастанием гипоксии клеток, началом ферментативного метаболизма в клетках тканей наиболее чувствительных и уязвимых органов. При стадии 1.3 развивается ДВС-синдром (до уровня не менее его 2-й стадии). Вследствие выраженной гипоксии клетки становятся поставщиками недоокисленных метаболитов, распространяющихся по всему организму, грубо изменяющих кислотно-основное состояние (КОС). Появляются признаки нарушения функции отдельных органов (полиорганная недостаточность). На стадии 2 прогрессирует ДВС-синдром до глубокого уровня с грубыми расстройствами микроциркуляции и свертывания крови. Выраженный внутриклеточный ацидоз приводит к дезорганизации и гибели клеток. Эти изменения обусловливают появление тяжелой необратимой системной полиорганной недостаточности. Расширение зон некроза и плазматическая генерализация предваряют наступающую гибель организма.
12 К ЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ ИНФЕКЦИОННО - ТОКСИЧЕСКОГО ШОКА. Различают 4 фазы или степени ИТШ : Ранняя фаза ( 1 степень) - артериальная гипотензия может отсутствовать - тахикардия, снижение пульсового давления - шоковый индекс до 0,7-1,0 (отношение частоты пульса к максимальному АД, в норме он равен 0,6, при шоке 1,2-1,5 и более) - признаки интоксикации: боли в мышцах, боли в животе неопределенной локализации, сильная головная боль - нарушения со стороны ЦНС: подавленность, чувство тревоги,возбуждение, гиперрефлексия - со стороны мочевой системы: снижение темпов мочеотделения менее 25 мл/ч
13 Фаза выраженного шока ( 2 степень ) - критически падает АД ( ниже 90 мм.рт. ст.) - пульс частый ( более 100 уд/мин ), слабого наполнения - шоковый индекс до 1,0 - 1,4 - состояние микроциркуляции: отмечается акроцианоз, мраморность, кожа холодная, влажная, с серым оттенком - дыхание частое - заторможенность и апатия
14 Фаза декомпенсированного шока ( 3 степень) дальнейшее падение АД дальнейшее увеличение частоты пульса шоковый индекс около 1,5 состояние микроциркуляции: общий цианоз появляются признаки полиорганной недостаточности: олигурия, иногда появляется желтуха
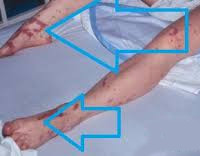
15 Больной с 4 степенью инфекционно-токсического шока.
16 Поздняя стадия шока ( 4 степень ) - шоковый индекс более 1,5 - общая гипотермия - состояние микроциркуляции: холодная, землистого оттенка кожа, цианотичные пятна ( венозный стаз ) - усугубляются признаки полиорганной недостаточности: острая дыхательная недостаточность, анурия, кома Последовательность стадий развития шока удается отметить далеко не всегда. Ранняя стадия ИТШ нередко просматривается, особенно при молниеносной его форме, при которой она кратковременна и практически отсутствует.
17 Ц ЕЛИ ТЕРАПИИ ПРИ ИНФЕКЦИОННО - ТОКСИЧЕСКОМ ШОКЕ. Восстановление микроциркуляции Детоксикация Нормализация гемостаза Коррекция метаболического ацидоза Коррекция функций других органов, предупреждение развития острой дыхательной, почечной и печеночной недостаточности Проводится не последовательно, а параллельно!
18 И НФУЗИОННАЯ ТЕРАПИЯ ПРИ ИНФЕКЦИОННО - ТОКСИЧЕСКОМ ШОКЕ Кристаллоидные растворы ( раствор глюкозы, поляризующая смесь ) чередуются с коллоидными ( реополиглюкин, альбумин). Доля кристаллоидных растворов к коллоидным составляет 3: мл\кг массы тела Инфузию осуществляют в вену капельно, при шоке степени назначают со струйного введения до подъема артериального давления, но не более минут. Одновременно с инфузионной терапией необходима дегидратация, которая достигается введением лазикса. Введение плазмы противопоказано из-за возможности образования иммунных комплексов, которые могут блокировать микроциркуляцию! Для уменьшения метаболического ацидоза показано введение 300 – 400 мл. гидрокарбоната натрия 4%.
19 Ф АРМАКОТЕРАПИЯ ИНФЕКЦИОННО - ТОКСИЧЕСКОГО ШОКА Лекарственные препараты вводят внутривенно, параллельно с проведением инфузионной терапии. Глюкокорктикостероиды. при ИТШ 1 степени – Преднизолон 2-5 мг/кг/сутки или Гидрокортизон – 12,5 мг/кг/сутки в сутки при ИТШ 2 степени – Преднизолон мг/кг/сутки или Гидрокортизон – 25 мг/кг/сутки в сутки при ИТШ 3 степени – Преднизолон 20 мг/кг/сутки или Гидрокортизон – мг/кг/сутки в сутки
20 Гепарин Начинают применять в фазу гиперкоагуляции ДВС – синдрома. Гепаринотерапия (через каждые 6 часов): ИТШ 1 степени – ЕД/кг/сутки ИТШ 2 степени – ЕД/кг/сутки ИТШ 3 степени –10-15 ЕД/кг/сутки. Повышает активность антитромбина ///, способствует инактивации ряда факторов свертывания, снижает агрегацию и адгезию тромбоцитов.
21 Допамин При отсутствии эффекта от гормональной терапии начать введение катехоламина первого порядка – Допамин с мкг/кг/мин под контролем АД; Ингибиторы фибринолиза ( контрикал, гордокс ) Ингибиторы протеаз – Апротинин – от АТЕ (антитрипсиновые единицы)/кг (разовая доза); (Гордокс, Контрикал, Трасилол); При стабилизации АД – фуросемид 1% мг; При наличии сопутствующего отека мозга – маннитол 15% мл, в/в капельно;
22 Пентоксифиллин ( трентал ) Цель применения – восстановление микроциркуляции, повышение неспецифической резистентности организма, улучшение гемостаза. Введение его желательно начинать в ранние сроки из расчета 3,5 мг/кг в сутки, внутривенно капельно. Витаминотерапия (особенно Аскорбиновая кислота 5% до 20 мг.) Антибиотики – для лечения основного заболевания. Применяют а/б, которые обладают бактериостатическим действием. Антибиотики с бактерицидным действием будут способствовать развитию ИТШ!
23 Иммунотерапия Внутривенные иммуноглобулины. Использование внутривенных иммуноглобулинов, в рамках иммунозаместительной терапии тяжелого сепсиса и СШ, является в настоящее время единственным реально доказанным методом иммунокоррекции при сепсисе, повышающим выживаемость. Целесообразно использовать: Иммуноглобулин человеческий нормальный (IgG+IgA+IgM). Стандартный режим дозирования заключается во введении 3– 5 мл/кг/сут в течение 3 дней подряд.
24 Д РУГИЕ ЛЕЧЕБНЫЕ МЕРОПРИЯТИЯ ПРИ ИНФЕКЦИОННО - ТОКСИЧЕСКОМ ШОКЕ Ингаляция через носовые катетеры увлажненного кислорода со скоростью 5 л/мин. Катетеризация мочевого пузыря для постоянного контроля за диурезом ( мочеотделение 0,5 – 1,0 мл/мин свидетельствует об эффективности терапии ). После стабилизации гемодинамики возможно применение экстракорпоральной детоксикации, гипербарической оксигенации. Соблюдение строгого постельного режима ( учитывая наличие недостаточного венозного возврата, что может усугубляться в вертикальном положении ).
25 П РИЧИНЫ СМЕРТИ ПРИ ИНФЕКЦИОННО – ТОКСИЧЕСКОМ ШОКЕ Полиорганная недостаточность – 50% Стойкая артериальная гипотензия – 40% Тяжелая сердечная недостаточность – 10% По современным медицинским воззрениям, считается нецелесообразным прекращать лечебные мероприятия, даже если необратимость ИТШ у больного достаточно очевидна. Для принятия решения об окончании лечения необходимо поставить диагноз смерти мозга. Подобное заключение следует принимать исключительно во время консилиума, после проведения электроэнцефалограммы.
Септический шок – это тяжелое патологическое состояние, возникающее при массивном поступлении в кровь бактериальных эндотоксинов. Сопровождается тканевой гипоперфузией, критическим снижением артериального давления и симптомами полиорганной недостаточности. Диагноз ставится на основании общей клинической картины, сочетающей в себе признаки поражения легких, сердечно-сосудистой системы (ССС), печени и почек, централизации кровообращения. Лечение: массивная антибиотикотерапия, инфузия коллоидных и кристаллоидных растворов, поддержание деятельности ССС за счёт введения вазопрессоров, коррекция респираторных нарушений путем ИВЛ.
МКБ-10
Общие сведения
Септический шок (СШ) также называют инфекционно-токсическим (ИТШ). Как самостоятельная нозологическая единица патология впервые была описана в XIX веке, однако полноценное изучение с разработкой специфических противошоковых мер началось не более 25 лет назад. Может возникать при любом инфекционном процессе. Наиболее часто встречается у пациентов хирургических отделений, при менингококковой септицемии, брюшном тифе, сальмонеллезе и чуме. Распространен в странах, где диагностируется наибольшее количество бактериальных и паразитарных заболеваний (Африка, Афганистан, Индонезия). Ежегодно от ИТШ погибает более 500 тысяч человек по всему миру.

Причины
В абсолютном большинстве случаев патология развивается на фоне ослабления иммунных реакций. Это происходит у пациентов, страдающих хроническими тяжелыми заболеваниями, а также у людей пожилого возраста. В силу физиологических особенностей сепсис чаще диагностируется у мужчин. Список самых распространенных заболеваний, при которых могут возникать явления ИТШ, включает в себя:
- Очаги гнойной инфекции. Признаки системной воспалительной реакции и связанных с ней нарушений в работе внутренних органов отмечаются при наличии объемных абсцессов или флегмоны мягких тканей. Риск генерализованного токсического ответа повышается при длительном течении болезни, отсутствии адекватной антибактериальной терапии и возрасте пациента старше 60 лет.
- Длительное пребывание в ОРИТ. Госпитализация в отделение реанимации и интенсивной терапии всегда сопряжена с риском возникновения сепсиса и инфекционного шока. Это обусловлено постоянным контактом с резистентной к антибактериальным препаратам микрофлорой, ослаблением защитных сил организма в результате тяжёлой болезни, наличием множественных ворот инфекции: катетеров, желудочных зондов, дренажных трубок.
- Раны. Нарушения целостности кожных покровов, в том числе возникшие во время операции, существенно повышают риски инфицирования высококонтагиозной флорой. ИТШ начинается у больных с загрязненными ранами, не получивших своевременной помощи. Травматизация тканей в ходе оперативного вмешательства становится причиной генерализованной инфекции только при несоблюдении правил асептики и антисептики. В большинстве случаев септический шок возникает у пациентов, перенесших манипуляции на желудке и поджелудочной железе. Еще одна распространенная причина – разлитой перитонит.
- Приём иммунодепрессантов. Лекарственные средства, угнетающие иммунитет (меркаптопурин, кризанол), используются для подавления реакции отторжения после трансплантации органов. В меньшей степени уровень собственной защиты снижается при употреблении химиотерапевтических средств – цитостатиков, предназначенных для лечения онкологических заболеваний (доксорубицина, фторурацила).
- СПИД.ВИЧ-инфекция в стадии СПИДа приводит к развитию нетипичного сепсиса, спровоцированного не бактериальный культурой, а грибком рода Candida. Клинические проявления болезни характеризуется малой степенью выраженности. Отсутствие адекватного иммунного ответа позволяет патогенной флоре свободно размножаться.
Возбудитель сепсиса – грамположительные (стрептококки, стафилококки, энтерококки) и грамотрицательные (Enterobacter cloacae, Clostridium pneumoniae) бактерии. Во многих случаях культуры нечувствительны к антибиотикам, что затрудняет лечение пациентов. Септический шок вирусного происхождения в настоящее время вызывает споры специалистов. Одни представители научного мира утверждают, что вирусы неспособны стать причиной патологии, другие – что внеклеточная форма жизни может спровоцировать системную воспалительную реакцию, являющуюся патогенетической основой ИТШ.
Патогенез
В основе симптомов лежит неконтролируемое распространение медиаторов воспаления из патологического очага. При этом происходит активация макрофагов, лимфоцитов и нейтрофилов. Возникает синдром системного воспалительного ответа. На фоне этого снижается периферический сосудистый тонус, объем циркулирующей крови падает за счет повышения проницаемости сосудов и застоя жидкости в микроциркуляторном русле. Дальнейшие изменения обусловлены резким уменьшением перфузии. Недостаточное кровоснабжение становится причиной гипоксии, ишемии внутренних органов и нарушения их функции. Наиболее чувствителен головной мозг. Кроме того, ухудшается функциональная активность легких, почек и печени.
Помимо СВР в формировании септического шока важную роль играет эндогенная интоксикация. В связи со снижением работоспособности экскреторных систем в крови накапливаются продукты нормального обмена веществ: креатинин, мочевина, лактат, гуанин и пируват. Во внутренних средах повышается концентрация промежуточных результатов окисления липидов (скатол, альдегиды, кетоны) и бактериальных эндотоксинов. Всё это вызывает тяжелые изменения гомеостаза, расстройства кислотно-щелочного баланса, нарушения в работе рецепторных систем.
Классификация
Симптомы септического шока
90% случаев СШ сопровождается дыхательной недостаточностью различной степени тяжести. Пациенты с декомпенсированным и терминальным течением болезни нуждаются в аппаратной респираторной поддержке. Печень и селезенка увеличены, уплотнены, их функция нарушена. Может отмечаться атония кишечника, метеоризм, стул с примесью слизи, крови и гноя. На поздних стадиях возникают симптомы диссеминированного внутрисосудистого свертывания: петехиальная сыпь, внутреннее и наружное кровотечения.
Осложнения
Септический шок приводит к ряду тяжелых осложнений. Наиболее распространённым из них считается полиорганная недостаточность, при которой нарушается функция двух и более систем. В первую очередь страдает ЦНС, легкие, почки и сердце. Несколько реже встречается поражение печени, кишечника и селезенки. Летальность среди пациентов с ПОН достигает 60%. Часть из них погибает на 3-5 сутки после выведения из критического состояния. Это обусловлено органическими изменениями во внутренних структурах.
Еще одним распространенным последствием ИТШ являются кровотечения. При формировании внутримозговых гематом у пациента развивается клиника острого геморрагического инсульта. Скопление экстравазата в других органах может приводить к их сдавлению. Уменьшение объема крови в сосудистом русле потенцирует более значимое снижение артериального давления. ДВС на фоне инфекционно-токсического шока становится причиной гибели пациента в 40-45% случаев. Вторичное поражение органов, спровоцированное микротромбозами, возникающими на начальном этапе формирования коагулопатии, отмечается практически у 100% больных.
Диагностика
- Осмотр и физикальное исследование. Реализуется непосредственно лечащим врачом. Специалист обнаруживает характерные клинические признаки шокового состояния. Для этого проводится тонометрия, визуальная оценка цвета кожных покровов, особенностей дыхательных движений, подсчет пульса и ЧДД, аускультация сердца и легких. При подозрении на наличие осложнений необходима оценка неврологического статуса на предмет симптоматики кровоизлияния в мозг.
- Аппаратное исследование. Имеет вспомогательное значение. Пациенту показан контроль состояния с использованием анестезиологического монитора. На экран устройства выводится информация о величине артериального давления, частоте сердечных сокращений, степени насыщения крови кислородом (при легочной недостаточности SpO2<90%) и коронарном ритме. На фоне нарушений дыхания и токсического поражения миокарда может отмечаться тахикардия, аритмия и блокады внутрисердечной проводимости.
- Лабораторное исследование. Позволяет выявить имеющиеся нарушения гомеостаза, сбои в работе внутренних органов. У пациентов с шоком септического происхождения обнаруживается повышенный уровень креатинина (> 0,177 ммоль/л), билирубина (>34,2 мкмоль/л), лактата (>2 ммоль/л). О нарушении коагуляции свидетельствует тромбоцитопения (
Лечение септического шока
Пациентам показана интенсивная терапия. Лечение проводят в отделениях ОРИТ с использованием методов аппаратной и медикаментозной поддержки. Лечащий врач – реаниматолог. Может потребоваться консультация инфекциониста, кардиолога, гастроэнтеролога и других специалистов. Требуется перевод больного на искусственную вентиляцию лёгких, круглосуточное наблюдение среднего медицинского персонала, парентеральное кормление. Смеси и продукты, предназначенные для введения в желудок, не используются. Все методы воздействия условно делятся на патогенетические и симптоматические:
- Патогенетическое лечение. При подозрении на наличие сепсиса больному назначают антибиотики. Схема должна включать в себя 2-3 препарата различных групп, обладающих широким спектром действия. Подбор медикамента на начальном этапе проводят эмпирическим путем, в соответствии с предполагаемой чувствительностью возбудителя. Одновременно с этим производят забор крови на стерильность и восприимчивость к антибиотикам. Результат анализа готовится в течение 10 дней. Если к этому времени подобрать эффективную лекарственную схему не удалось, следует использовать данные исследования.
- Симптоматическое лечение. Подбирается с учетом имеющейся клинической картины. Обычно больные получают массивную инфузионную терапию, глюкокортикостероиды, инотропные средства, антиагреганты или гемостатики (в зависимости от состояния свертывающей системы крови). При тяжелом течении болезни используют препараты крови: свежезамороженную плазму, альбумин, иммуноглобулины. Если пациент находится в сознании, показано введение анальгетических и седативных лекарств.
Прогноз и профилактика
Септический шок имеет неблагоприятный прогноз для жизни. При субкомпенсированном течении погибает около 40% больных. Декомпенсированная и терминальная разновидности оканчиваются гибелью 60% пациентов. При отсутствии своевременной медицинской помощи смертность достигает 95-100%. Часть больных умирает через несколько дней после устранения патологического состояния. Профилактика ИТШ заключается в своевременном купировании очагов инфекции, грамотном подборе антибиотикотерапии у хирургических больных, соблюдении антисептических требований в отделениях, занимающихся инвазивным манипуляциями, поддержке адекватного иммунного статуса у представителей ВИЧ-инфицированной прослойки населения.
2. Тактика ведения пациентов с сепсисом и септическим шоком в многопрофильном стационаре/ Сапичева Ю.Ю., Лихванцев В.В. – 2015.
Читайте также:

