Септическое нейтрофильное воспаление у кошки
Обновлено: 18.04.2024
Автор: Светлана Викторовна Шишканова, заведующая независимой ветеринарной
лаборатории "Поиск", г. Санкт-Петербург.
Лейкограмма (leucogramma; лейко- + греч. gramma – запись) или лейкоцитарная формула – это процентное соотношение различных видов лейкоцитов, определяемое при подсчете их в окрашенном мазке крови под микроскопом.
Лейкограмма дает представление о балансе между выработкой лейкоцитов в костном мозге, их распределением в сосудистой системе и эмиграцией из кровеносных сосудов в ткани.
Существуют два метода подсчета лейкограммы: ручной (в окрашенном мазке крови под микроскопом) и автоматический (при помощи гематологического анализатора). В ветеринарии ручной метод подсчета считается наиболее точным, по сравнению с автоматическим методом. Ручной метод позволяет не только дифференцировать различные виды лейкоцитов, но и определить изменение морфологии клеток, появление нейтрофильной токсичности, наличие атипичных клеток, клеточных агрегатов, кровепаразитов. Врач-лаборант при исследовании окрашенного мазка крови должен помнить о неравномерном распределении лейкоцитов в мазке: лимфоциты принимают центральное расположение, нейтрофилы – краевое, в связи с чем при подсчете лейкограммы необходимо захватывать и центральную, и краевую зоны мазка.
Лейкограмма используется для:
– Наблюдения за состоянием здоровья пациента;
– Постановки дифференциального диагноза;
– Оценки реакции пациента на лечение;
– Предположительного прогноза.
Изменения в лейкограмме могут быть не патогномоничными для данного заболевания, тем не менее они часто выявляют и характеризуют многие патологические процессы. Лейкограмма не может служить достаточным подтверждением сепсиса, однако характерные изменения в ней говорят о наличии воспалительного заболевания и оценивают его тяжесть.
Лейкограмма подсчитывается как в процентном соотношении, так и в абсолютных числах (10⁹/л). Многие ветеринарные лаборатории пренебрегают этим важным моментом и производят только процентный подсчет клеток. Впрочем, многие ветеринарные врачи также не понимают необходимости подсчета лейкограммы в абсолютных числах. Все это в результате может привести к ошибочной интерпретации лейкограммы, неправильной постановке диагноза и потенциально нанести вред здоровью животного (табл. 1).
При интерпретации лейкограммы немецкой овчарки мы видим выраженный лейкоцитоз и относительную лимфопению, у йоркширского терьера же, наоборот, умеренную лейкопению и относительный лимфоцитоз. Однако если мы сравним абсолютные значения лимфоцитов обеих собак, они будут одинаковыми и соответствуют варианту нормы.
Процентное соотношение лейкоцитов нужно лишь для подсчета абсолютных чисел. Лейкограмма только с процентным соотношением лейкоцитов может ввести в заблуждение ветеринарного врача. Абсолютное значение рассчитывается умножением процентного соотношения клеток данного вида на общее количество лейкоцитов у животного и делением на 100. Примерно ориентироваться на процентное соотношение клеток можно только при уровне лейкоцитов у животного в пределах референтного интервала.
При интерпретации лейкограммы ветеринарный врач должен задать себе следующие вопросы:
– Есть ли здесь воспаление?
– Есть ли воздействие глюкокортикоидов (стресс)?
– Есть ли влияние адреналина (возбуждение, волнение)?
– Есть ли некротические поражения тканей?
– Если есть воспаление, то можно ли его классифицировать?
– Есть ли системная токсемия.
Лейкоцитоз и нейтрофилия
В большинстве случаев понятия лейкоцитоз и нейтрофилия являются синонимами. Они характерны для воспалительного процесса. Продолжительность и тяжесть воспалительного процесса, а также ответ костного мозга на инфекцию будут определять степень нейтрофилии и возможность появления в крови незрелых форм (палочкоядерных нейтрофилов, метамиелоцитов и миелоцитов) – сдвиг влево.О сдвиге влево говорят при превышении количества палочкоядерных нейтрофилов более 1,0х10⁹/л, что характерно для острых воспалительных процессов. Менее выраженный сдвиг влево (0,3–1,0х10⁹/л) характерен для хронических и гранулематозных процессов.
Различают регенеративный и дегенеративный сдвиг ядра влево. При регенеративном сдвиге в крови преобладают зрелые нейтрофилы, он оценивается как адекватный ответ костного мозга на поражающее воздействие. При дегенеративном сдвиге ядра влево число незрелых нейтрофилов больше, чем зрелых, а общее число лейкоцитов находится в пределах нормы или снижено.
Дегенеративный сдвиг указывает на острый воспалительный процесс, который превышает способность костного мозга обеспечить потребность в зрелых нейтрофилах. В начале воспалительного процесса возникает нейтрофильный лейкоцитоз и выраженный сдвиг ядра влево. По мере истощения существовавших в депо созревания и хранения костного мозга сегментоядерных нейтрофилов происходит выделение палочкоядерных нейтрофилов и метамиелоцитов. Спустя некоторое время миелоидная гиперплазия в костном мозге увеличит выработку нейтрофилов. Увеличится выход в кровь зрелых клеток и уменьшится тяжесть левого сдвига. При стабилизации тканевого воспаления на устойчивом низком уровне костный мозг должен достичь достаточной скорости выработки нейтрофилов, чтобы большая их часть могла созревать до выделения в циркулирующее русло. Таким образом, при хроническом воспалительном процессе не наблюдается лейкоцитоз, а сдвиг влево незначительный или отсутствует. Хроническое воспаление общим анализом крови выявить сложно.
Если потребность в нейтрофилах очень сильная, в костном мозге может наблюдаться гиперплазия гранулоцитарного ростка, не находя отражения в виде нейтрофилии в периферической крови. Например, при пиометре у собак может встречаться нормальное или слега повышенное количество лейкоцитов и умеренный (до сильного) сдвиг лейкоцитарной формулы влево. После операции у таких животных может возникнуть рикошетная нейтрофилия, отражающая степень нейтрофилии гранулоцитарного ростка. Как правило, требуется около недели, чтобы профиль крови у таких собак вернулся к норме.
Стойкая нейтрофилия должна исследоваться на наличие очага хронического воспаления, абсцесса, некроза и опухоли. В таких случаях рекомендуется тщательно исследовать суставы (полиартриты), ЦНС (менингиты), сердечно-сосудистую систему (эндокардит) и желудочно-кишечный тракт (язвенные поражения).
Дифференциальная диагностика нейтрофильного лейкоцитоза включает:
– Воспаление;
– Воздействие кортикостероидов (стресс, терапия глюкокортикоидами, синдром Кушинга);
– Воздействие адреналина (возбуждение, страх, физическая нагрузка);
– Лейкозы.
Основные причины нейтрофильного лейкоцитоза со сдвигом ядра влево:
– Бактериальные инфекции (сепсис);
– Протозойные, грибковые и вирусные инфекции (например, инфекционный перитонит кошек);
– Несептические (некротические) процессы (например, панкреатит, тромбоэмболия);
– Химические воздействия;
– Гемобластозы (ОМЛ, ХМЛ, миелопролиферативные заболевания костного мозга);
– Опухоли различного происхождения (в результате выработки цитокинов);
– Аномалия Пельгер-Хьюита;– иммуноопосредованные заболевания (например, системная красная волчанка и иммунная гемолитическая анемия);
– Токсины: эндотоксины (например, при хронической почечной недостаточности) и экзотоксины (например, укусы змей).
Отсутствие изменений в лейкограмме не исключает воспалительных процессов.
Слабое и хроническое воспаление (например,при цистите) не вызывает изменения уровня лейкоцитов и лейкограммы. В связи с чем, в некоторых случаях необходимо проводить исследование белков острой фазы воспаления (например, определение С– реактивного белка у собак и антитромбина III у кошек или определять протеинограмму). Рис. 5
Прогноз
К плохому или осторожному прогнозу относят:
– Лейкоцитоз более 60х10⁹/л у собак и более 30х10⁹/л у кошек;
– Дегенеративный сдвиг влево;
– Лейкемоидную реакцию;
– Токсические изменения в нейтрофилах.
Подобные изменения в лейкограмме часто сопровождают грамотрицательный сепсис и указывают на тяжелый характер воспаления. У таких животных рекомендуется проводить анализ крови ежедневно.Гиперсегментация ядер (сдвиг вправо) Наличие в нейтрофилах ядер с пятью и более долями – это естественный процесс старения клетки. Гиперсегментация характерна для длительного пребывания нейтрофилов в кровеносном русле. Может встречаться у пожилых животных.
Основные причины появления:
– Хронические воспалительные процессы;
– Гиперадренокортицизм или глюкокортикоидная терапия;
– Миелопролиферативные заболевания;
– Дефект абсорбции кобаламина у собак;
– Дефицит фолиевой кислоты у кошек.
Гиперсегментация ядер нейтрофилов может появляться in vitro, при позднем приготовлении мазков крови (рис. 6).
Нейтропения – явление достаточно редкое.
Причины нейтропении:
– Сниженный выход нейтрофилов из костного мозга (дисгранулопоэз);
– Усиленная миграция нейтрофилов в ткани (нейтропения потребления);
– Переход нейтрофилов из циркулирующего в маргинальный пул.
Нейтропения сопровождает:
– Гемобластозы;
– Вирус лейкоза кошек (FeLV);
– Вирус иммунодефицита кошек (FIV);
– Идиосинкразии на лекарственные препараты (цефалоспорины, триметоприм, фенилбутазон);
– Влияние эндогенного и экзогенного эстрогена;
– Химиотерапию;
– Вирусные инфекции (парвовирус);
– Кровепаразитарные инфекции – эрлихиоз (Ehrlichia canis);
– Наследственные расстройства (циклический гемопоэз у серых колли и синдром Чедиака-Хигаси у кошек);
– Миелофтиз (множественная миелома, лимфолейкоз, миелодиспластический синдром);
– Первичную иммуноопосредованную нейтропению (системная красная волчанка).
При шоке происходит перемещение нейтрофилов из циркулирующего в краевой (маргинальный) пул – псевдонейтропения.
Для бельгийских овчарок-тервюрен характерна физиологическая лейкопения/нейтропения/лимфопения.При наличии стойкой необратимой нейтропении рекомендуется исследование пунктата костного мозга.
Дисгранулопоэз
Дисгранулопоэз характеризуется уменьшением числа клеток-предшественников в костном мозге или нарушением процесса созревания клеток.
Причины:
– Гемобластозы;
– Вирус лейкоза кошек (FeLV);
– Вирус иммунодефицита кошек (FIV).
Нейтропения потребления
Нейтропения потребления встречается при тяжелых воспалительных процессах. Общее количество лейкоцитов при этом снижено, наблюдается дегенеративный сдвиг ядра влево. В очаге воспаления происходит гибель огромного числа нейтрофилов, наблюдается истощение резервов костного мозга. Прогноз в подобных клинических случаях неблагоприятный.
Лейкемоидные реакции
Лейкемоидными реакциями называют изменения крови, наблюдающиеся иногда при ряде заболеваний и характеризующиеся появлением в периферической крови большого количества молодых клеток, обычно встречающихся только в костном мозге.Картина периферической крови при лейкемоидных реакциях сходна с картиной крови при лейкозах: при реакциях миелоидного типа картина крови напоминает ХМЛ, при реакциях лимфатического типа – ХЛЛ.
Лейкемоидная реакция характеризуется выраженным лейкоцитозом (50–100х10⁹/л).
Отличия лейкемоидных реакций от лейкозов:
– При лейкемоидных реакциях в большинстве случаев удается найти этиологический фактор;
– Изменения крови при лейкемоидных реакциях, как правило, нестойкие, после устранения фактора, вызвавшего патологический процесс, профиль крови быстро возвращается к норме;
– Существенные различия обнаруживаются при исследовании пунктатов костного мозга.
Различают лейкемоидные реакции трех типов:
– Миелоидного (гранулоцитарного);
– Моноцитарного;
– Лимфоцитарного.
У человека описываются также лейкемоидные реакции эозинофильного типа. Чаще всего у животных встречаются лейкемоидные реакции миелоидного типа. Для них характерно наличие большого количества незрелых нейтрофилов (выраженный сдвиг ядра влево), возможно появление единичных бластных клеток. Нейтрофилы часто дегенеративно изменены (наблюдается выраженная нейтрофильная токсичность).
Могут встречаться при:
– Пиометре;
– Перитоните;
– Пневмонии;
– Пиотораксе;
– Пиелонефрите;
– Абсцессах;
– Иммунной гемолитической анемии;
– Функциональных нарушениях нейтрофилов (например, недостаточность протеиновой адгезии в лейкоцитах у ирландских сеттеров);
– Кровепаразитарных заболеваниях (например, пироплазмозе собак).
Лейкемоидные реакции лимфоцитарного типа характеризуются наличием большого количества лимфоцитов, также возможно появление пролимфоцитов и лимфобластов. Могут сопровождать пироплазмоз собак и гемобартонеллез. Лейкемоидные реакции моноцитарного типа характеризуются преобладанием моноцитов в лейкограмме, сами моноциты могут быть морфологически изменены, встречаются единичные монобласты. У собак подобный тип реакций описан при гемобартонеллезе.


Причины
Признаки
Диагностика
Лечение
Сепсис – тяжелое состояние, вызываемое проникновением в кровеносное русло патогенных микроорганизмов и их токсинов. Является следствием системной (генерализованной) инфекции. Часто сепсис называют заражением крови.
Характеризуется выраженными нарушениями сердечной деятельности, гемодинамики, падением артериального давления, высокой температурой тела. В тяжелых случаях проблема прогрессирует до септического шока. Существует высокий риск гибели пациента.
Причины
Наиболее часто сепсис ассоциирован с такими бактериями, как E. coli, Pseudomonas spp, грамположительными бактериями Streptococcus spp and Staphylococcus spp. Грамотрицательные бактерии вызывают более тяжелую реакцию. Выделяемый ими эндотоксин или липополисахарид, который входит в состав бактериальной стенки и высвобождается при циркуляции в крови, вызывает системную воспалительную реакцию, полиорганную недостаточность и гибель пациента.
У кошек сепсис развиться возникнуть при :
- пилотораксе (гнойное воспаление в грудной клетке);
- септическом перитоните;
- бактериемии, вторичной к заболеваниям; ;
- эндокардите; ;
- остеомиелите; ;
- кусаных ранах.
Особенно предрасположены кошки с ослабленной резистентностью организма.
Признаки
Клиническая картина зависит от того, какие органы вовлечены в патологический процесс, возможна полиорганная недостаточность.
- летаргия, угнетение;
- бледность слизистых;
- слабый пульс; ;
- температура тела сначала сильно повышена, по мере ухудшения состояния пациента падает;
- выраженная болезненность брюшной полости;
- брадикардия (замедление пульса); .
Диагностика
Основывается на клинической картине, данных, полученных при опросе владельцев. При проведении лабораторной диагностики, как правило, выявляется анемия, тромбоцитопения, нейтрофилия, падение альбумина, повышение билирубина, низкий уровень щелочной фосфатазы.
При проведении рентгенограммы грудной клетки можно обнаружить пневмонию, выпот в грудной клетке, при УЗИ брюшной полости – признаки перитонита, воспаления внутренних органов (например, пиометру).
Лечение

Терапия возможна только в условиях стационара. Показана массивная внутривенная инфузия, оксигенация, внутривенная антибиотикотерапия (применяются препараты широкого спектра действия, комбинация нескольких препаратов). Врач оценивает сердечный ритм, сердечный выброс, уровень артериального давления. Назначаются препараты, улучшающие функцию сердечной мышцы, нормализующие тонус сосудов. Крайне важно следить за почечной функцией, объемом отделяемой мочи.
Сепсис является тяжелым, угрожающим жизни состоянием. Характеризуется высокой летальностью среди пациентов.
Прогноз зависит от состояния иммунной системы кошки, причины, вызвавшей септическое воспаление, тяжести повреждений и того, насколько своевременно было начато лечение.
(с) Ветеринарный центр лечения и реабилитации животных "Зоостатус".
Варшавское шоссе, 125 стр.1. тел. 8 (499) 372-27-37

Инфекционный перитонит у кошек (вирусный перитонит кошек), а также часто используется аббревиатура FIP - Feline Infectious Peritonitis - тяжелое, 100% летальное заболевание с многообразными симптомами.
Причиной развития вирусного перитонита является коронавирус кошек. Однако, коронавирусом инфицировано множество животных, у части из них проявляются перемежающиеся признаки кишечных расстройств, и лишь у каждой десятой кошки заболевание перетекает в инфекционный перитонит.
Название “инфекционный перитонит” не вполне верно отражает суть заболевания. Перитонит - это воспаление брюшины, чаще всего бактериальное. Воспалительный процесс при FIP протекает стерильно, лишь изредка с присоединением вторичной флоры, и далеко не всегда вообще сопровождается выпотом (скоплением жидкости) в брюшной полости (“сухая форма” FIP). Когда речь идет об инфекционном перитоните кошек, правильнее говорить о васкулите, т.е. воспалении сосудов, которое ведет к повышению проницаемости их стенки, и полигрануломатозном полисерозите (воспалении серозных оболочек с образованием гранулем) . Однако, название “инфекционный перитонит” сложилось исторически, и широко применяется в литературе и практике.
Пути заражения
Коронавирус кошек чрезвычайно заразен, передается напрямую через микрочастицы фекалий, при тесном контакте и при вскармливании котят матерью, реже опосредованно через предметы ухода. Восприимчивые кошки получают коронавирус FCoV от здоровых бессимптомных кошек (не больных FIP!).
Передача коронавируса от кошки, больной инфекционным перитонитом, к здоровой, практически никогда не происходит в естественных условиях, хотя возможна в условиях эксперимента.
Любая кошка потенциально является источником FCoV. При наличии нескольких кошек, живущих совместно, в случае, если у одной из них развивается инфекциоонный перитонит, наиболее вероятно, что все животные были инфицированы коронавирусом ранее, поэтому в изоляции кошки, больной FIP, нет смысла.
В ситуации, когда кошка с FIP погибла или эутаназирована и в окружении нет других кошек, рекомендуется ждать в течение как минимум 7-8 недель прежде, чем взять в дом новое животное. Если в окружении остались другие кошки, они, наиболее вероятно, являются переносчиками FCoV.
Причины инфекционного перитонита у кошек
Патогенез инфекционного перитонита кошек до сих пор остается предметом споров в научном мире. Большинство клиницистов придерживаются гипотезы, что причина этого непростого для диагностики заболевания заключается в спонтанной индивидуальной мутации (рекомбинации) безобидного кишечного коронавируса у конкретного животного, как правило, под воздействием стрессовых факторов или подавления иммунитета. Эта гипотеза объясняет тот факт, что при широкой распространенности коронавируса в популяции эпидемических вспышек летальной формы вируса - FIP - никогда не происходит.
FIP возникает, когда кишечная форма коронавируса переходит в системную, способную поражать не только клетки эпителия кишечника, но и макрофаги - специфические клетки белой крови, отвечающие за тканевый иммуннитет.
Распространенность заболевания. Предрасположенность к FIP
Инфекция, вызываемая коронавирусом, у кошек встречается повсеместно, также вирус может быть выделен у диких кошачьих.
Некоторые породы (бенгальские кошки), с большей вероятностью развивают инфекционный перитонит при заражении коронавирусом. По всей вероятности, существуют отдельные генетические линии внутри других пород (например, британцы, скотиш-фолд), у которых риск развития FIP более высок, однако это не подтверждено доказательными исследованиями, хотя эмпирически наблюдается на практике.
Одним из наиболее важных факторов риска для развития вирусного перитонита является возраст - до 70% животных, у которых развилсяFIP, младше 1 года, хотя заболевание может наблюдаться у кошек любого возраста.
Клинические симптомы
Клинические признаки ВПК у кошек весьма вариабельны и связаны с распределением двух типов поражений - васкулитных (нарушение порозности сосудов) и гранулематозных (развитие особых бляшек - воспалительных гранулем на внутренних органах).
В клинической практике выделяют две формы инфекционного перитонита - влажную (выпотную) и сухую (невыпотную), однако имеются и промежуточные варианты.
Симптомы неспецифичны, особенно на раннем этапе заболевания, могут наблюдаться все или многие признаки, или только несколько:
- Общая вялость; (высокая температура), не отвечающая на терапию антибактериальными препаратами;
- Потеря веса, вплоть до истощения или плохой набор веса у котят и молодых животных;
- Нарушения аппетита; ;
- Бледность слизистых оболочек из-за анемии;
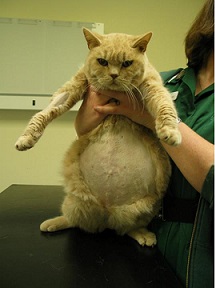
- Увеличение живота в объеме - асцит является наиболее заметным клиническим проявлением при “влажной” форме FIP. Кроме этого, выпот может образовываться в грудной и перикардиальной полости (совместно с выпотом в брюшную или изолированно), в этом случае отмечается нарушение дыхания;
- Поражение нервной системы, судороги, нарушения координации движений, изменения поведения (при сухой форме и гранулематозном воспалительном поражении головного мозга) - около 10% всех случаев невыпотного FIP протекают с неврологическими симптомами;
- Почечная недостаточность, увеличение почек в размере (засчет развития гранулем в почечной ткани);
- Поражение печени, сопровождающиеся желтушностью слизистых оболочек;
- Нарушения со стороны глаз (изменение формы зрачка, пигментации радужки, отложения в роговице, гифема (кровь в передней камере глаза) - при невыпотоной форме.
При невыпотной форме повышение температуры, отказ от корма и угнетение могут длительное время быть единственными симптомами. Более характерные клинические признаки будут зависеть от того, какие именно органы и ткани поражены, чаще всего поражения затрагивают орган брюшной полости.
Диагностика FIP
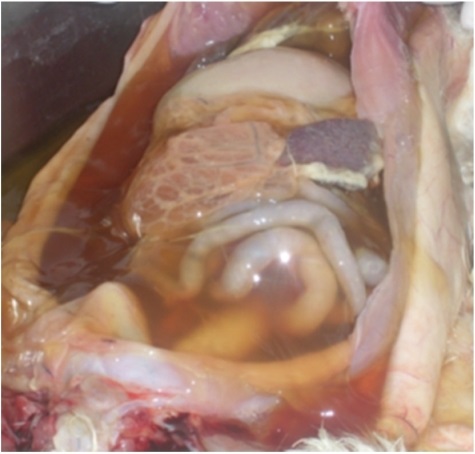
К сожалению, ни одного простого и достоверного прижизненного анализа на инфекционный перитонит кошек не существует.
Методом, позволяющим поставить окончательный диагноз, является проведение гистопаталогического исследования, что осуществляется посмертно. Некоторые лаборатории и производители тестов называют предлагаемые исследования ”тестами на FIP”, хотя на самом деле они являются тестами для выявления коронавируса или антител к нему.
Сравнительно недавно в практику ведущих ветеринарный врачей в Европе внедрен имунофлуоресцентный тест, который позволяет определить вирус в макрофагах в брюшине при выпотной форме и обратная ПЦР. В РФ на данный момент коммерческим недоступны и не применяется.
Постановка диагноза FIP с большой степенью вероятности - сложный процесс и сопряжена с необходимостью выполнять сложный протокол из нескольких тестов.
Владелец же оказывается в ситуации, когда после проведения дорогостоящей диагностики получает результат - FIP, а значит, животное обречено.
FIP считается заболеванием, сложным для диагностики, еще и из-за наличия большого количества заболеваний со схожей симптоматикой. Поскольку кошек с FIP обычно эвтаназируют в связи с безнадежным прогнозом, чрезвычайно важно отличать инфекционный перитонит от других, тяжелых, но поддающихся лечению заболеваний.
- Определение в крови уровня (титра) антител к коронавирусу кошек - При выпотной форме FIP могут быть обнаружены разные титры антитет, но, как правило, уровень антител к коронавирусу очень высок (1280 и выше). Если антитела в крови не обнаружены, это означает отсутствие у кошки инфекционного перитонита, с другой стороны, если другие признаки позволяют подозревать FIP, это, напротив, может говорить об очень высоком количестве выделяемого в выпотную жидкость вируса, который связывают антитела. В этом случае используется ПЦР выпотной жидкости.
Важно! Многие здоровые кошки и кошки, больные не FIP могут иметь антитела к коронавирусной инфекции. Единственный тест НЕ является достаточным диагностическим критерием для постановки диагноза FIP!
- Определения общего белка и соотношения альбумин/глобулин в выпоте или в плазме крови - у кошек с FIP общее содержание белка в выпоте обычно выше 35 г/л, баланс смещен в сторону глобулинов, соотношение A/G отношение. (при отношении A/G ниже 0,4 верятность диагноза FIP высока; при A/G выше 0,8 напротив, этот диагноз можно исключить. Промежуточные значения требуют дополнительной диагностики.
- Определение уровня альфа-1 кислого гликопротеина (AGP) - это белок острой фазы, который при FIP обычно зничительно повышен - до 1500 мг/мл. При кардиопатологии, неинфекционных заболеваниях печени и новообразованиях, которые могут быть перепутаны с FIP, уровень этого белка находится в пределах нормы. При воспалительном бактериальном перитоните AGP также значительно повышается, однако это состояние можно дифференцировать от FIP с помощью цитологического исследования выпотной жидкости.
- Цитологическое исследование выпота - при влажной форме FIP выпотная жидкость имеет низкую клеточность, среди клеток встречаются ппреимущественно нейтрофилы и макрофаги, в то время как рри бактериальном перитоните клеток крови значительно больше, а также оюнаруживаются внутриклеточные бактерии. Кроме того, цитология очень важна для того, чтобы отличить вирусный перитонит от лимфосаркомы, которая тажже может давать выпот в брюшную и грудную полость.
При сухой форме инфекционного перитонита обычно также превышает 1280, при этом нулевой титр исключает эту форму патологии.
Прижизненная диагностика сухого инфекционного перитонита остается сложной задачей.Трудности возникают из-за отсутствия неинвазивных (без вмешательства во внутренние органы) подтверждающих тестов у кошек без выпота.
Лечение заболевания

Лечение (или эутаназия) должны рассматриваться только после того, как установлен окончательный диагноз или вероятность инфекционного перитонита очень высока. Если установлен диагноз FIP, то прогноз всегда фатальный. Средняя выживаемость составляет примерно 9 дней при выпотной форме, при сухой в редких случаях продолжительность жизни может быть значительно выше.
Поскольку инфекционный перитонит кошек вызывается воспалительным ответом и нарушением нормального клеточного иммунитета на FcoV, поддерживающее лечение имеет целью подавление иммунной и воспалительной реакции, обычно с помощью кортикостероидов. Дополнительно проводится симптоматическая терапия, направленная на улучшение качества жизни животного.
На сегодняшний день, однако, не имеется контролируемых исследований, которые доказали бы полезный эффект терапии стероидами.
Также проводились исследования по лечению кошек с использованием интерферона-омега, но не было получено положительных данных по сравнению с плацебо.

Панкреатит кошек часто сопровождается сопутствующими заболеваниями других органов и систем. Патологические нарушения включают липидоз печени, воспалительные болезни печени, обструкцию желчевыводящего тракта, сахарный диабет, воспалительные заболевания ЖКТ, гиповитаминоз (В12, фолата, витамина К), кишечную лимфому, нефриты, лёгочную тромбоэмболию и плевральный или перитонеальный выпот. Термин триадит применяется при комплексе воспалительных заболеваний поджелудочной железы, печени и тонкого отдела кишечника. Триадит обнаруживается в 50–56% у кошек с диагнозом панкреатит и в 32–50% у кошек с диагнозом холангит\воспалительное заболевание печени. Дифференциальная диагностика триадитов основана на гистопатологических исследованиях этих органов. Однако индивидуальное состояние каждого органа определяет диагноз триадит среди других дифференциальных диагнозов. В то время как этиопатогенез панкреатита и его отношение к воспалению других систем органов неоднозначно, первый этап дифференциальной диагностики включает исследование причин воспаления, иммунного ответа и кишечной микрофлоры.
Введение
Панкреатит кошек часто сопровождается сопутствующими заболеваниями других органов и систем. Патологические нарушения включают липидоз печени, воспалительные болезни печени, обструкцию желчевыводящего тракта, сахарный диабет, воспалительные заболевания ЖКТ, гиповитаминоз (В12, фолата, витамина К), кишечную лимфому, нефриты, лёгочную тромбоэмболию и плевральный или перитонеальный выпот. Термин триадит применяется при комплексе воспалительных заболеваний поджелудочной железы, печени и тонкого отдела кишечника. Триадит обнаруживается в 50–56% у кошек с диагнозом панкреатит и в 32–50% у кошек с диагнозом холангит/воспалительное заболевание печени. Эта статья предоставляет обзор причин и лечения панкреатитов и триадитов у кошек, и глубокого рассмотрения этиопатогенеза триадитов.
Дифференциальная диагностика триадитов основана на гистопатологическом исследовании отдельного органа. Однако диагноз триадит включает в себя комбинацию воспалительных изменений, таких как хронический панкреатит, хронический холангит/холангиогепатит и ВЗК. Необходимо соблюдать осторожность при постановке диагноза, делая выводы о причинах триадита, так как прижизненная диагностика затруднительна, а окончательный диагноз ставится посмертно. Диагностика затрудняется различием гистологической классификации и оценки панкреатита кошек, воспалительных заболеваний печени и кишечника, которые могут осложняться стадийностью и корреляцией специфических подтипов болезней этих органов, с триадитами. Стандартизация критериев гистопатологических исследований печени и кишечника может быть затруднена.
Таблица №1. Симптомы, указывающие на триадит
Диагности-
ческие тесты
Панкреатиты
Болезни печени
Воспали-
тельные заболевания кишечника
Диагностика панкреатитов и триадитов
Диагноз триадит, симптомы которого описаны в таблице 1, ставится при наличии комплекса воспалительных заболеваний кишечника, печени и поджелудочной железы. Клинические находки различны и включают: анорексию, потерю веса, потерю мышечной массы, диарею, рвоту, желтуху, гепатомегалию, утолщение стенок кишечника, увеличение поджелудочной железы, абдоминальную боль, абдоминальный выпот, лихорадку, гипотермию, тахипноэ, и шок. Гематологические и биохимические изменения, связанные с болезнями печени — увеличение концентрации АЛТ, АСТ, ГГТ, ЩФ и билирубина; с болезнями поджелудочной железы — увеличение панкреатической липазы и иммунореактивной панкреатической липазы, снижение уровня кальция; с ВЗК или алиментарной лимфомой — недостаток кобаламина, фолата и альбумина. При ультразвуковом исследовании поджелудочной железы отмечают: изменение размера, эхогенности тканей и протока поджелудочной железы; печени: изменение размера и контура органа, эхогенности тканей, состояния желчевыводящей системы; тонкого кишечника: утолщение стенки кишечника и гипертрофия мышечного слоя. Окончательная постановка диагноза требует проведения биопсии и гистопатологического исследования тканей каждого органа.
Схема №1

Каковы причины панкреатита?
Этиопатогенез панкреатита и его осложнений описан в схеме 1. Причины, которые являются пусковым механизмом для развития панкреатита кошек (таблица 2), обычно не очевидны. При этом острый панкреатит может перетекать в хронический, который в свою очередь может сопровождаться экзокринной недостаточностью поджелудочной железы; вероятно, каждая из причин может провоцировать развитие самостоятельного заболевания. Острый панкреатит сопровождается отёком и некрозом, с гипоперфузией и тромбозом, который в свою очередь может усиливать панкреонекроз. Часто панкреатитам сопутствует воспаление тонкого отдела кишечника. Особенно плохой прогноз у гнойного панкреатита. Абсцессы (стерильные и инфицированные) и псевдокисты (возникают из-за локального скопления секрета поджелудочной железы) встречаются редко. Сочетание этих факторов может сопровождаться бактериальной инфекцией и билиарной обструкцией. Бактериальная инфекция может проникать в поджелудочную железу через её проток по восходящему пути или гематогенным путём из кишечника. FISH-исследование (fluorescence in situ hybridisation) обнаруживает бактерий в поджелудочной железе у 13/46 кошек с панкреатитами. Бактериальная инфекция провоцирует более тяжёлые панкреатиты по отношению к случаям, протекающим без неё. Бактериальные колонии чаще обнаруживают в тканях окружающих проток поджелудочной железы, паренхиме органа, окружающем сальнике, участках некроза и выводящих протоках. Хронический панкреатит может приводить к обструкции протока поджелудочной железы и билиарной системы, что в свою очередь ухудшает элиминацию бактерий в печени.
Таблица 2. Возможные причины панкреатита, воспалительных заболеваний печени и ВЗК
Причина
Панкреатит
Воспалительные заболевания печени
Воспалительные заболевания кишечника
Как панкреатит связан с триадитом?
Воспаление в кишечнике, печени и поджелудочной железе может быть обусловлено отдельным патологическим процессом на каждом участке или иметь общую причину. Наиболее вероятные причины воспаления ПЖ, печени и кишечника указаны в схеме 2. Бактериальная инфекция, иммуно-опосредованный ответ и идиопатический механизмы могут также являться потенциальной причиной воспаления каждого органа или провоцировать триадит. При рассмотрении причин триадитов возможно несколько моделей развития заболевания.
Острый панкреатит как причина триадита?
Схема №2

Воспаление кишечника и аутоиммунные причины триадита
Альтернативный этиологический фактор триадита может находиться в кишечнике. В основе этого сценария лежит лимоцитарно-плазмацитарное воспаление или мелкоклеточная лимфома, которые могут сопровождаться дисбиозом и миграцией кишечных бактерий в поджелудочную железу, минуя воспалённую стенку кишечника или панкреобилиарный сосочек.
Повышение интрадуаденального давления ведёт не только ко рвоте, но и к рефлюксу содержимого кишечника в панкреобилиарный проток, приводящий к бактериальному инфицированию печени и поджелудочной железы (схема 2 В). Мы можем обнаружить бактерии в желчи и панкереобилиарном тракте. Однако, бактерии при инфекционных заболевания печени чаще локализуются в портальной вене, венозных синусах и паренхиме (12/13), чем в желчевыводящем тракте(1/13) и только у 3 из 13 кошек с панкреатитом инфекция локализуется в протоке поджелудочной железы. Предполагают, что гематогенный путь развития инфекции более вероятен, чем инфицирование тканей по восходящему пути панкреобилиарных протоков.
Модели, описанные в схеме 2 А, В, наиболее применимы к кошкам с триадитами, панкреатитами средней и тяжёлой степени, воспалительными заболеваниями печени (которые подразделяются на реактивную гепатопатию, нейтрофильный или обструктивный холангиты). Эти кошки чаще имеют активную колонизацию бактерий, чем кошки с более лёгкой формой течения заболеваний.
У кошек с хроническим лимфоцитарным панкреатитом или холангитом редко обнаруживают бактериальную инфекцию, а также наличие ДНК видов Helicobacter, которые вызывают заболевания у других видов животных (у кошек это не доказано). Следовательно, комбинация лимфоцитарного (хронического) панкреатита, лимфоцитарного или смешанного лимфоцитарного и нейтрофильного холангита, и лимфоцитарно-плазмоцитарного энтерита чаще вызвана иммуно-опосредованным ответом, чем бактериальной инфекцией (схема 2 С). В организме человека и экспериментальных животных аутоиммунный панкреатит и холангит возникает как осложнение ВЗК с иммунной атакой на панкреобилиарный тракт. Несколько экспериментальных исследований подтверждают возможность того, что иммунный ответ на кишечных бактерий связан с иммуно-опосредованным панкреатитом и холангитом. Например, C57BL/6 мыши, которым внутрибрюшинно вводят термоинактивированную E. Coli еженедельно в течение 8 недель, показывают выраженную клеточную инфильтрацию и фиброз поджелудочной железы, сопровождающийся повышением концентрации гамма-глобулина в сыворотке крови и образованием аутоантител против карбоангидразы и лактоферрина. Более поздние исследования выявили жгутиковые одноклеточные организмы, FliC из E. Coli, которые являются антигенным стимулом и вызывают повышение титра антител в сыворотке крови у больных иммуно-опосредованным панкреатитом. Экспрессия антигенов хозяина может формировать иммунный ответ. Муцин 1 (MUC1) сверхэкспрессируется в патогенную, гипергликозилированную форму на эпителии толстого отдела кишечника человека с ВЗК, где он провоцирует воспаление. MUC1 так же воздействует на эпителий протока поджелудочной железы. У мышей с ВЗК были выявлены MUC1-специфические Т-клетки, мигрирующие в толстый отдел кишечника и поджелудочную железу. Это говорит о том, что вначале внекишечная часть ВКЗ характеризуется провоспалительной патогенной экспрессией MUC1.
Иммунное взаимодействие клеток в желчных протоках у кошек с лимфоцитарным холангитом, аналогично наблюдаемому у людей с первичным склерозирующим холангитом(PSC). PSC характеризуется прогрессирующим воспалением, фиброзом и разрушением внутри- и внепечёночных желчных протоков, в результате развивается билиарный фиброз, цирроз, приводящий к печёночной недостаточности.
PSC это комплексное заболевание, основанное на генетике, врождённом и адаптивном иммунитете и влиянии окружающей среды. Часто это связано с ВЗК и предполагает иммунную атаку против клеток желчевыводящего тракта и может вызывать хоуминг лимфоцитов памяти, количество которых повышается, как последствия ВЗК для печени. Обнаружением молекулы клеточной адгезии (MAdCAM-1) и хемокинов (C-C motif) лиганда (CCL25), местом локализации которых считался только кишечник, которые активируются в печени в условиях воспаления, поддерживается общая концепция, что этот механизм может привлекать лимфоциты в поражённую печень и кишечник. Экспрессия MadCAM-1 так же может вызвать лимфоцитарное воспаление островковых клеток при сахарном диабете, но это не всегда связано с иммуно-опосредованным панкреатитом. Разнообразные антигены могут быть вовлечены в PSC. В последнее время идентификация B-тубулина изотипа 5 (TBB5), который имеет высокое соответствие с бактериальным белком деления клеток FtsZ, как антинейтрофильное цитоплазматическое аутоантитело (ANCA), предполагает, что иммунные ответ на миграцию бактерий возможен при наличии нарушений порозности слизистой кишечника, что способствует воспалению у восприимчивого человека. В то время как PSC способствует аутоиммунному панкреатиту, всё чаще считают, что нарушение проходимости желчевыводящих путей относятся к подтипу PSC, холангиту, ассоциированному с иммуноглобулином (Ig) G4. Эта болезнь, связана с увеличением сывороточного IgG4/IgE, обильной инфильтрацией IgG4-positive плазмацитарных клеток и лимфоцитов, аутоантигенов и стероидной восприимчивости. Считается, что аутоантигены, аутоантитела (такие как лактоферрин, карбоангидразы) и потенциальные патогены могут управлять IgG4-опосредованным воспалением, но это ещё предстоит определить. Ряд других органов также может быть вовлечён в этот процесс: слюнные железы (Sjögren’s syndrome), стриктуры желчевыводящих путей, узелки в лёгких, аутоиммунный тиреоидит, интерстициальный нефрит (обусловленный инфильтрацией IgG4-positive плазматических клеток и осаждением IgG4 на тубулярной базальной мембране). Примечательно, что нефрит, который считают сопутствующей возрастной патологией, часто диагностируют у кошек с холангитами и/или панкреатитами.
Лечение триадитов
Термин триадит применяется к синдрому, который охватывает спектр воспалительных заболеваний печени, поджелудочной железы и кишечника, поэтому, для выбора тактики лечения, требуется особо тщательная оценка общего состояния здоровья пациента и определение конкретного типа, и степени тяжести изменений в каждом из этих органов. Лекарственные препараты для лечения каждого из заболеваний необходимо рассматривать комплексно, для того, чтобы оценить возможность негативных последствий при их одновременном применении, поэтому необходим индивидуальный подход к каждому пациенту.
Приоритеты в лечении у кошек с триадитами
Лечение триадитов начинают с получения результатов клинического осмотра, клиникопатологических тестов, которые направлены на дифференциацию заболевания (цитология тканей печени, поджелудочной железы, мезентериальных лимфатических узлов, культуральные исследования желчи). У кошек с персистирующей рвотой, абдоминальной болью, желтухой, анорексией, гиповолемией, признаками шока, сепсиса, гипотермии или лихорадки, первичная цель лечения — это поддержание общего состояния и поиск возможных причин заболевания. Симптоматическое лечение включает в себя инфузионную терапию, обезболивание, противорвотные средства и антибиотики (при подозрении на сепсис, наличии нейтрофилии с левым сдвигом) (таб. 3). Животным с анорексией назначают энтеральное питание (жидкие корма через назо-фарингеальные зонды). У кошек с подтверждённым триадитом основное лечение направлено на более поражённый орган. Например: острый панкреатит, с подозрением на холангит, холецистит, обструкцию билиарного тракта и возможную перфорацию кишечника. В этом случае необходимо определить необходимость немедленного хирургического вмешательства.
Дифференциальная диагностика триадита основана на оценке гистопатологического материала каждого органа и выявлении бактериальной инфекции в них (культуральные исследования желчи и тканей печени, и FISH — исследование печени и поджелудочной железы), для чего проводится диагностическая лапаротомия. Это также хорошая возможность для установки эзофагостомической трубки. Если диагностическая лапаротомия невозможна или нецелесообразна, проводят минимально инвазивные исследования, такие как эндоскопия и тонкоигольна биопсия участков поражённых органов под контролем УЗИ. Последующая терапия основана на основании наличия бактериальной инфекции в билиарном тракте, поджелудочной железе или кишечнике (нейтрофильный или гранулематозный энтерит) с определением чувствительности этой микрофлоры к антибактериальным препаратам (таб. 3.).
Таблица 3. Лечение триадита: панкреатиты, воспалительные заболевания печени и кишечника
Читайте также:

