Септическое состояние в послеродовом периоде что это такое
Обновлено: 23.04.2024
Послеродовый эндометрит – это инфекционное воспаление эндометрия (слизистой оболочки матки), возникающее в послеродовом периоде (после рождения ребенка). Чаще всего в воспалительный процесс вовлекается также и миометрий (мышечный слой стенки матки).
Код(ы) МКБ-10:
| N.71.0 | – | Острые воспалительные болезни матки |
| О.86 | – | Другие послеродовые инфекции |
| О.86.1 | – | Другие инфекции половых путей после родов |
| О.86.8 | – | Другие уточненные послеродовые инфекции |
Дата разработки/пересмотра протокола: 2017 год.
Сокращения, используемые в протоколе:
| АД | Артериальное давление | |
| ЗППП | заболевания передающиеся половым путем | |
| ОАК | – | общий анализ крови |
| УД | уровень доказательности | |
| УЗИ | ультразвуковое исследование | |
| ЧД | частота дыхания |
Пользователи протокола: врачи общей практики, акушеры-гинекологи.
Категория пациентов: родильницы
Шкала уровня доказательности:
Классификация
Клиническая классификация [1]
По характеру родоразрешения:
· эндометрит после самопроизвольных родов;
· эндометрит после кесарева сечения.
По клинической картине:
· классическая форма;
· абортивная форма;
· стертая форма.
По степени выраженности адаптационно- компенсаторных реакций организма:
· компенсированный;
· субкомпенсированный;
· декомпенсированный.
Диагностика
Методы, подходы и процедуры диагностики и лечения
Диагностические критерии
Жалобы и анамнез: Критерии диагноза послеродового эндометрита (для постановки диагноза, достаточно 2 симптома) 2
· повышение Т* тела ( 38* и выше);
· тазовая боль или болезненная матка при пальпации;
· выделения из половых путей с необычным/неприятным запахом;
· гнойные выделения из влагалища;
· субинволюция матки – задержка в темпах уменьшения размеров матки < 2 см/ сутки в течении первых 8 дней.
Дополнительные симптомы:
· возможно умеренное кровотечение из половых путей [2,3];
· недомогание, снижение аппетита, озноб, головная боль 2.
Отдельно выделяют эндометрит после кесарева сечения, который как правило, протекает гораздо тяжелее, чем послеродовый эндометрит.
К симптомам классической формы заболевания присоединяются:
· вздутие живота;
· отсутствие стула и отхождения газов;
· снижение количества выделяемой мочи за сутки.
Физикальное обследование при послеродовом эндометрите:
· измерение Т°, пульса, АД,ЧДД.
· пальпация живота – болезненность при пальпации матки;
· осмотр на зеркалах (состояние послеродовой шейки, характер выделений, наличие запаха);
· бимануальное исследование: состояние матки (мягкая, болезненная, увеличенная в размере), состояние маточных труб, яичников и параметрия (пастозность, отечность, инфильтрация).
При субфебрильной температуре тела до 37,5° в течении более 24 часов со 2-х суток послеродового периода, при отсутствии клинических признаков эндометрита показано [7,8,11]:
· контроль t° тела каждые 3 часа;
· микробиологическое исследование отделяемого из цервикального канала (полости матки) с определением чувствительности микрофлоры к антибиотикам;
· дифференциальная диагностика с возможными причинами повышения температуры;
· ультразвуковая диагностика для выявления остатков плацентарной ткани, гематометры, которые являются факторами риска послеродового эндометрита.
· гистероскопия.
Лабораторные исследования:
Клинический и биохимический анализ крови, наиболее характерные изменения показателей периферической крови:
· лейкоцитоз 12,0 ·10 /л и более;
· палочкоядерные нейтрофилы 10 % и более;
· гипохромная анемия;
· увеличение СОЭ;
· снижение уровня общего белка плазмы крови.
NB! Повышение количества лейкоцитов в крови обладает низкой прогностической ценностью для подтверждения наличия инфекции (УД- 2А).
Бактериологические исследования аспирата из полости матки:
· позволяет идентифицировать инфекционный агент и спектр чувствительности к антибиотикам (при условно-патогенной флоре степень обсеменения более 10*4)
Инструментальные исследования:
NB! Ультразвуковое исследование матки не должно применяться для диагностики послеродового эндометрита, так как не обладает высокой чувствительностью.
· УЗИ матки при послеродовом эндометрите для выявления задержки в полости матки некротически измененных остатков децидуальной оболочки, сгустков крови и плацентарной ткани.
· Гистероскопия - при наличии заключения УЗИ о наличии остатков плацентарной ткани, отмечается локально или диффузно расположенной гиперемии, cтромального отека и возможно внутриматочных микрополипов в слизистой оболочке матки, проводится при невыраженности клинической картины.
NB! Гистероскопия со 2го дня послеродового периода допускается при наличии подготовленного врача акушера-гинеколога.
Показания для консультации специалистов:
NB! При неэффективности проводимой терапии, необходима консультация клинического фармаколога, а при необходимости выполнения хирургических вмешательств – анестезиолога.

Диагностический алгоритм (схема)
Дифференциальный диагноз
Дифференциальную диагностику послеродового эндометрита следует проводить со всеми патологическими состояниями, сопровождающимися лихорадкой после родов. В большинстве случаев это послеродовые осложнения инфекционно – воспалительного характера, источником которых служит матка. К ним можно отнести пельвиоперитонит, несостоятельность швов на матке после кесарево сечения. Нельзя категорически исключать и острую хирургическую патологию – холецистит и прободную язву желудка. Развитие острого воспаления мочевыводящих путей также дает схожую клиническую картину.
| Диагноз | Послеродовый эндометрит | Пельвиоперитонит | Аппендицит |
| Критерии включения | Температура, боли внизу живота, тахикардия, лейкоцитоз | Температура, боли внизу живота, тахикардия. Лейкоцитоз | Температура, боли внизу живота, тахикардия, лекоцитоз |
| Критерии исключения/включения диагноза | Болезненность при пальпации матки, гноевидные выделения из цервикального канала; при УЗИ возможно задержки в полости матки некротически измененных остатков децидуальной оболочки, сгустков крови и плацентарной ткани, субинволюция матки, | Боли возле пупка и внизу живота, защитное напряжение мышц передней брюшной стенки Появление симптомов после оперативных вмешательств, стойкий парез кишечника | Боли возле пупка и внизу живота, защитное напряжение мышц передней брюшной стенки Наличие тошноты, рвоты, локализация боли в правой подвздошной области |
Лечение
Препараты (действующие вещества), применяющиеся при лечении
| Амоксициллин (Amoxicillin) |
| Ампициллин (Ampicillin) |
| Ацетилсалициловая кислота (Acetylsalicylic acid) |
| Дротаверин (Drotaverinum) |
| Имипенем (Imipenem) |
| Клавулановая кислота (Clavulanic acid) |
| Меропенем (Meropenem) |
| Метронидазол (Metronidazole) |
| Натрия хлорид (Sodium chloride) |
| Окситоцин (Oxytocin) |
| Повидон - йод (Povidone - iodine) |
| Сульбактам (Sulbactam) |
| Цефазолин (Cefazolin) |
| Цефепим (Cefepime) |
| Цефоперазон (Cefoperazone) |
| Цефотаксим (Cefotaxime) |
| Цефтриаксон (Ceftriaxone) |
| Цефуроксим (Cefuroxime) |
| Циластатин (Cilastatin) |
| Ципрофлоксацин (Ciprofloxacin) |
| Эритромицин (Erythromycin) |
Лечение (стационар)
ТАКТИКА ЛЕЧЕНИЕ НА СТАЦИОНАРНОМ УРОВНЕ
Принципы лечения [12]:
• санация очагов инфекции (удаление под гистероскопическим контролем некротизированных децидуальных тканей, остатков плацентарной ткани);
• инфузия кристалоидов;
• применение антибактериальных средств широкого спектра действия.
При прогресирующем эндометрите и частичной несостоятельности шва на матке возможна консервативная тактика с проведением санационных лечебно-диагностических гистероскопий, аспирационно-промывного дренирования полости матки в сочетании с комплексным противовоспалительным лечением (антибактериальной терапии. Нестероидными противовоспалительными препаратами и дезинтоксикационной терапией). В ситуации купирования эндометрита заживления швов на матке возможно вторичным натяжением, в отдельных случаях (только в стационарах 3 уровня), возможно проведение органосберегающих операций с наложением вторичных швов на матку.
При прогрессировании эндомиометрита и полной несостоятельности шва на матке, а также при отсутствие эффекта от лечения показана радикальная операция – тотальная гистерэктомия, билатеральная сальпингэктомия).
Немедикаментозное лечение:
Режим: лечебно-охранительный. Пациентку необходимо оградить от отрицательных эмоций и болевых ощущений.
Диета: Стол №15. Важным является полноценное питание с повышенным содержанием белков и витаминов.
Медикаментозное лечение
Эмпирическая антибактериальная терапия 3.
Перед началом лечения производят забор отделяемого из полости матки для бактериологического исследования, при выявлении возбудителя - определение чувствительности к антибиотикам для дальнейшей этиотропной терапии.
· Амоксициллин + клавулановая кислота (по1.2г внутривенно 3 -4 раза в сутки) (УД А);
· Ампициллин/сульбактам 1,5 гх3-4р/сут в/в;
· Амоксициллин/сульбактам 1,5х3р/сут в/в;
· Цефоперазон/сульбактам 2-4р/сут в/в;
· Цефтриаксон 1-2г 1 р/сутки в/в + метронидазол 500 мг3р/сутки в/в (УД А);
· Цефотаксим 1-2 г х 3 р/сут в/в+ метронидазол 500 мг3р/сутки в/в;
· Цефепим 1-2 г х2 р/сут в/в+ метронидазол 500 мг3р/сутки в/в;
· Ципрофлоксацин 400 мг 2 р/сут в/в+ метронидазол 500 мг3р/сутки в/в.
Инфузионная терапия:
Показана при гипертермии и интоксикации (УД-В) [8,13,14]:
· хлорид натрия, 0,9% р-р, в/в капельно 400-800 мл 1р/сут, 3-4 сут.
NB! Инфузионные средства применяют в различных сочетаниях. Объем инфузионной терапии составляет 1,2-1,5 л/сут.
При субинволюции матки к АБ добавляют средства, стимулирующие мускулатуру матки, в сочетании со спазмолитиками (УД-С):
· окситоцин в/м 5 ЕД* 2р/сут, 4-5 сут + Дротаверин в/м 40 мг *2р/сут, 4-5 сут.
Показания для проведения антибиотикопрофилактики:
Оперативные вмешательства:
· плановое и экстренное кесарево сечение (1 – сильная рекомендация ВОЗ) [12,17]
· ручное отделение плаценты и выделение последа [15, 21]и ручное обследование полости матки (12). NB! ВОЗ (2015) рекомендует при ручном удалении плаценты введение одной дозы антибиотиков: ампициллин или цефалоспорин 1-го поколения [22]
· преждевременный разрыв плодных оболочек ( при недоношенной беременности) (уровень 1а) (сильная рекомендация [12, 15] См КП «Преждевременные роды).
· дородовый разрыв плодных оболочек при безводном промежутке более 18 часов (уровень 2а) [15]
· разрывы промежности 3-4 степени (1 – сильная рекомендация ВОЗ, 2015) [15]. Рекомендуемая продолжительность курса – 5 дней
Не рекомендуется
· рутинная антибиотикопрофилактика всем женщинам во 2-3 триместрах беременности с целью снижения инфекционной заболеваемости (кроме пациенток высоко риска инфекционных заболеваний и осложнений в родах) (сильная рекомендация ВОЗ, 2015 [15];
· рутинная антибиотикопрофилактика женщинам с преждевременными родами при целых плодных оболочках (сильная рекомендация ВОЗ, 2015) [15];
· рутинное введение антибиотиков женщинам с мекониальными водами (условная рекомендация ВОЗ, 2015) [15];
· рутинная антибиотикопрофилактика женщинам с эпизиотомией (сильная рекомендация ВОЗ, 2015) [15];
· рутинная антибиотикопрофилактика женщинам с неосложненными влагалищными родами (имеются в виду вагинальные роды при отсутствие каких либо специфических факторов риска лили клинических признаков послеродовой инфекции у матери) (сильная рекомендация ВОЗ, 2015) [15];
· рутинная антибиотикопрофилактика женщинам с оперативными влагалищными родами (применение вакуум-экстрактора или акушерских щипцов) (условная рекомендация ВОЗ, 2015) [15];
· для антибиотикопрофилактики в акушерстве рекомендуется использовать пенициллины и цефалоспорины 1- II однократно [15].
Основанием для применения антибактериальных препаратов в послеродовом периоде по лечебным схемам является наличие инфекционного компонента:
· лихорадка в родах, послеродовом периоде;
· признаки интраамниотического инфекционного процесса;
· соматическая патология с инфекционным компонентам в стадии суб- и декомпенсации;
· ПРПО (при недоношенной беременности);
· присутствие облигатных патогенов в отделяемом полового тракта Neisseria gonorrhoeae, Trichomonas vaginalis, Chlamidia trahomatis.
Хирургическое вмешательство [4]:
Гистероскопия + кюретаж полости матки с гистологическим исследованием
Показания:
· наличие остатков плацентарной ткани, плодных оболочек, гемато и лохиометре.
Тотальная гистерэктомия
Показания: при безэффективности консервативного лечения, при прогрессировании симптомов заболевания.
Дальнейшее ведение:
· передача информации о пациенте в поликлинику по месту жительства для динамического наблюдения и проведения реабилитационных мероприятий в амбулаторно-поликлинических условиях.
Индикаторы эффективности лечения:
· регресс клинических симптомов;
· отсутствие гипертермии;
· улучшение лабораторных показателей;
· отсутствие осложнений.
Профилактические мероприятия:
· диагностика и лечение инфекции мочевыводящих путей, анемии и растройств питания, сахарного диабета, ЗППП и других вагинальных инфекций [12];
· своевременное лечение при дородовом излитии околоплодных вод [12], ограничение вагинальных исследований при преждевременном разрыве плодных оболочек [12];
· строгое соблюдение антисептики и стерилизации, обработка рук и передней брюшной стенки. Выбор антисептика для обработки кожи перед кесаревым сечением и способ его применения должен быть основан в первую очередь на клиническом опыте его использования, стоимости и наличия в ЛПУ (условная рекомендация ВОЗ, 2015) [15]. Не найдено убедительных доказательств, чтобы рекомендовать использование одного конкретного антисептического агента для обработки кожи перед кесаревым сечением [12];
· обработка влагалища раствором антисептика непосредственно перед кесаревым сечением (например, повидон-йодом) [15,16];
· применение индивидуальных комплектов и наборов на роды [12];
· ведение партограммы в родах всем пациентам и применение активного ведения для предупреждения затяжных родов [12];
· строгое соблюдение стерильности при вагинальных исследованиях у женщин в родах, при кесаревом сечении и других оперативных вмешательствах; соблюдение стерильности в операционной и родовом зале [12];
· избегать необоснованной катетеризации мочевого пузыря и проведение необоснованной эпизиотомии [12];
· профилактическое применение антибиотиков при инвазивных процедурах, длительном безводным периоде [12];
· в послеродовом периоде: ранняя выписка [12].
Послеродовые инфекции – группа заболеваний инфекционной этиологии, развивающихся в течение 6-ти недель после родов и непосредственно связанных с ними. Включают в себя локальные раневые инфекции, инфекции органов малого таза, генерализованные септические инфекции. В диагностике послеродовых инфекций первостепенное значение имеет время их развития и связь с родами, картина периферической крови, данные гинекологического осмотра, УЗИ, бактериологического исследования. Лечение послеродовых инфекций включает антибиотикотерапию, иммуностимулирующую и инфузионную терапию, экстракорпоральную детоксикацию, санацию первичного очага и др.
Общие сведения
Послеродовые (пуэрперальные) инфекции - гнойно-воспалительные заболевания, патогенетически обусловленные беременностью и родами. Включают в себя раневые инфекции (послеродовые язвы, эндометрит), инфекции, ограниченные полостью малого таза (метрит, параметрит, сальпингоофорит, пельвиоперитонит, метротромбофлебит и др.), разлитые инфекции (перитонит, прогрессирующий тромбофлебит) и генерализованные инфекции (септический шок, сепсис). Временные рамки, в течение которых могут развиваться данные осложнения - от момента выделения последа до окончания шестой недели послеродового периода. Пуэрперальные заболевания инфекционной этиологии встречаются у 2-10% родильниц. Септические осложнения играют ведущую роль в структуре материнской смертности, что ставит их в ряд приоритетных проблем акушерства и гинекологии.

Причины послеродовых инфекций
Этиологическая структура послеродовых инфекций весьма динамична и вариабельна. Из условно-патогенных микроорганизмов преобладают аэробные бактерии (энтерококки, кишечная палочка, стафилококки, стрептококки группы В, клебсиелла, протей), однако довольно часто встречаются и анаэробы (фузобактерии, бактероиды, пептострептококки, пептококки). Велика значимость специфических возбудителей - хламидий, микоплазм, грибов, гонококков, трихомонад. Особенностью послеродовых инфекций является их полиэтиологичность: более чем в 80% наблюдений высеваются микробные ассоциации, которые обладают большей патогенностью и устойчивостью к антибиотикотерапии.
Риск развития послеродовых инфекций существенно повышен у женщин с патологией беременности (анемия, токсикоз) и родов (раннее отхождение вод, слабая родовая деятельность, пролонгированные роды, кровотечение, задержка частей плаценты, лохиометра и др.), экстрагенитальной патологией (туберкулез, ожирение, сахарный диабет). Эндогенными факторами, предрасполагающими к микробному обсеменению родовых путей, могут служить вульвовагиниты, кольпиты, цервициты, пиелонефрит, тонзиллит, синуситы у родильницы. При инфицировании высоковирулентной флорой либо значительном снижении иммунных механизмов у родильницы инфекция может распространяться за пределы первичного очага гематогенным, лимфогенным, интраканаликулярным, периневральным путем.
Классификация послеродовых инфекций
На основании анатомо-топографического и клинического подхода выделяют 4 этапа прогрессирования послеродовой инфекции (авторы - С. В. Сазонова, А. В. Бартельс).
- 1-й этап – местная инфекция, не распространяющаяся за область раневой поверхности (послеродовая язва промежности, влагалища и стенки матки, нагноение швов, нагноение гематом, послеродовой эндометрит)
- 2-й этап – послеродовая инфекция, выходящая за границы раневой поверхности, но ограниченная полостью малого таза (метроэндометрит, аднексит, параметрит, метротромбофлебит, ограниченный тазовый тромбофлебит, пельвиоперитонит)
- 3-й этап – разлитая послеродовая инфекция (перитонит, прогрессирующий тромбофлебит)
- 4-й этап – генерализованная септическая инфекция (сепсис, инфекционно-токсический шок).
В качестве отдельной формы послеродовой инфекции выделяют лактационный мастит. Тяжесть инфекционных осложнений после родов зависит от вирулентности микрофлоры и реактивности макроорганизма, поэтому течение заболеваний варьирует от легких и стертых форм до тяжелых и летальных случаев.
Симптомы послеродовых инфекций
Послеродовая язва образуется в результате инфицирования ссадин, трещин и разрывов кожи промежности, слизистой влагалища и шейки матки. В клинической картине данного послеродового осложнения преобладают местные симптомы, общее состояние обычно не нарушается, температура не превышает субфебрильных цифр. Родильница жалуется на боли в области швов, иногда зуд и дизурические явления. При осмотре родовых путей обнаруживается язва с четкими границами, локальный отек и воспалительная гиперемия. На дне язвы определяется серовато-желтый налет, участки некроза, слизисто-гнойное отделяемое. Язвенный дефект легко кровоточит при контакте.
Послеродовой параметрит развивается на 10–12 день при переходе инфекции на параметрий - околоматочную клетчатку. Типичная клиника включает озноб, фебрильную лихорадку, которая длится 7-10 дней, интоксикацию. Родильницу беспокоят боли в подвздошной области на стороне воспаления, которые постепенно нарастают, иррадиируют в поясницу и крестец. Через несколько дней от начала послеродовой инфекции в области боковой поверхности матки пальпируется болезненный инфильтрат сначала мягковатой, а затем плотной консистенции, спаянный с маткой. Исходами послеродового параметрита может быть рассасывание инфильтрата или его нагноение с формированием абсцесса. Самопроизвольное вскрытие гнойника может произойти во влагалище, мочевой пузырь, матку, прямую кишку, брюшную полость.
Послеродовые тромбофлебиты могут затрагивать поверхностные и глубокие вены. В последнем случае возможно развитие метротромбофлебита, тромбофлебита вен нижних конечностей и вен таза. Обычно проявляются в течение 2-3 недель после родов. Клиническими предвестниками послеродовых осложнений данного типа служат длительная лихорадка; стойкое ступенеобразное учащение пульса; боли в ногах при движении и надавливании на мягкие ткани; отеки в области лодыжек, голени или бедра; цианоз нижних конечностей. На развитие метротромбофлебита указывает тахикардия до 100 уд./мин., субинволюция матки, длительные кровяные выделения, пальпация болезненных тяжей по боковым поверхностям матки. Тромбофлебит вен таза опасен развитием илеофеморального венозного тромбоза и тромбоэмболии легочной артерии.
Послеродовой пельвиоперитонит, или воспаление брюшины малого таза, развивается на 3-4 день после родов. Манифестация острая: температура тела быстро нарастает до 39-40°С, появляются резкие боли внизу живота. Может возникать рвота, метеоризм, болезненная дефекация. Передняя брюшная стенка напряжена, матка увеличена. Послеродовая инфекция разрешается рассасыванием инфильтрата в малом тазу или образованием абсцесса дугласова пространства.
Диагностика послеродовых инфекций
Факторами, указывающими на развитие послеродовых инфекций, служат признаки инфекционно-гнойного воспаления в области родовой раны или органов малого таза, а также общие септические реакции, возникшие в ранний период после родов (до 6-8 недель). Такие осложнения, как послеродовая язва, нагноение швов или гематомы диагностируются на основании визуального осмотра родовых путей. Заподозрить послеродовые инфекции органов малого таза гинекологу позволяет влагалищное исследование. В этих случаях обычно обнаруживается замедленное сокращение матки, ее болезненность, пастозность околоматочного пространства, инфильтраты в малом тазу, мутные зловонные выделения из половых путей.
Дополнительные данные получают при проведении гинекологического УЗИ. В случае подозрения на тромбофлебит показана допплерография органов малого таза, УЗДГ вен нижних конечностей. При послеродовом эндометрите информативна гистероскопия; при гнойном параметрите - пункция заднего свода влагалища. По показаниям применяют лучевые способы диагностики: флебографию, гистерографию, радиоизотопное исследование.
Для всех клинических форм послеродовой инфекции характерно изменение картины периферической крови: значительный лейкоцитоз с нейтрофильным сдвигом влево, резкое увеличение СОЭ. С целью идентификации инфекционных агентов производится бакпосев отделяемого половых путей и содержимого матки. Гистологическое исследование последа может указывать на признаки воспаления и, следовательно, высокую вероятность развития послеродовых инфекций. Важную роль в планировании терапии и оценке тяжести течения осложнений имеет исследование биохимии крови, КЩС, электролитов крови, коагулограммы.
Лечение послеродовых инфекций
Весь комплекс лечебных мероприятий при послеродовых инфекциях делится на местные и общие. Постельный режим и прикладывание льда к животу помогает остановить дальнейшее распространение инфекции из полости таза.
Локальные процедуры включают обработку ран антисептиками, перевязки, мазевые аппликации, снятие швов и раскрытие раны при ее нагноении, удаление некротизированных тканей, местное применение протеолитических ферментов. При послеродовом эндометрите может потребоваться проведение кюретажа или вакуум-аспирации полости матки (при задержке в ней плацентарной ткани и других патологических включений), расширение цервикального канала, аспирационно-промывное дренирование. При формировании абсцесса параметрия производится его вскрытие через влагалище или путем лапаротомии и дренирование околоматочной клетчатки.
Местные мероприятия при послеродовых инфекциях проводятся на фоне интенсивной общей терапии. В первую очередь, подбираются антибактериальные средства, активные в отношении всех выделенных возбудителей (пенициллины широкого спектра действия, цефалоспорины, аминогликозиды и другие), которые вводятся внутримышечно или внутривенно в сочетании в метронидазолом. На время лечения целесообразно прервать грудное вскармливание. С целью дезинтоксикации и устранения водно-солевого дисбаланса используются инфузии коллоидных, белковых, солевых растворов. Возможно проведение экстракорпоральной детоксикации: гемосорбции, лимфосорбции, плазмафереза.
При послеродовых инфекциях стафилококковой этиологии с целью повышения специфической иммунологической реактивности применяется антистафилококковый гамма-глобулин, стафилококковый анатоксин, антистафилококковая плазма. С целью профилактики тромбозов назначают антикоагулянты, тромболитики, антиагреганты под контролем коагулограммы. В комплексе медикаментозной терапии широко используются антигистаминные препараты, витамины, глюкокортикоиды. На этапе реабилитации назначают лазеротерапию, местное УФО, УВЧ-терапию, ультразвук, электростимуляцию матки, бальнеотерапию и другие методы физиотерапевтического воздействия.
В отдельных случаях может потребоваться хирургическая помощь – удаление матки (гистерэктомия) при ее гнойном расплавлении; тромбэктомия, эмболэктомия или флебэктомия - при тромбофлебитах.
Прогноз и профилактика
При раневых инфекциях и инфекциях, ограниченных областью малого таза, прогноз удовлетворительный. Своевременная и адекватная терапия позволяет остановить дальнейшее прогрессирование послеродовых инфекций. Однако в отдаленном периоде прогноз в отношении репродуктивной функции может быть вариабельным. Наиболее тяжелые последствия для здоровья и жизни родильницы влекут за собой разлитой перитонит, сепсис и септический шок.
Профилактика послеродовых инфекций обеспечивается строгим и неукоснительным соблюдением санитарно-гигиенического режима в родовспомогательных учреждениях, правил асептики и антисептики, личной гигиены персонала. Важное значение имеет санация эндогенной инфекции на этапе планирования беременности.
Послеродовой эндометрит – гнойно-воспалительное заболевание слизистой оболочки матки, развивающееся в раннем периоде после родов. При послеродовом эндометрите отмечается лихорадка, интоксикационный синдром, болезненность внизу живота, обильные гноевидные лохии, субинволюция матки. Диагноз послеродового эндометрита основан на клинических данных, подтвержденных результатами УЗИ малого таза, гистероскопии, бакпосева отделяемого матки. Послеродовой эндометрит требует назначения антибактериальной, дезинтоксикационной терапии; выполнения бережного кюретажа, вакуумной аспирации и промывания полости матки.

Общие сведения
Послеродовой эндометрит – форма послеродовой инфекции, характеризующаяся инфекционным воспалением внутренней выстилки матки (эндометрия). После отделения последа внутри матки образуется значительная раневая поверхность, при родоразрешении путем кесарева сечения дополнительно возникает операционная травма матки. Регенерация эндометрия происходит только к концу 5-6 недели после родов. Активация условно-патогенной микрофлоры и проникновение инфекции через поврежденный эндометрий в этот период приводит к возникновению в матке воспалительного процесса. Эндометрит развивается примерно у 7% родильниц, но среди послеродовой гнойно-воспалительной патологии его частота составляет 36–59%. Послеродовой эндометрит может быть острым и хроническим. В большинстве случаев отмечается легкое течение, около 25% случаев заболевания приходится на тяжелую форму с потенциалом генерализации инфекции. Воспалительный процесс обычно распространяется и на мышечный слой матки – миометрий, поэтому в большинстве случаев в гинекологии диагностируется послеродовой метроэндометрит.

Причины послеродового эндометрита
Причиной послеродового эндометрита выступает бактериальная инфекция, чаще всего попадающая в полость матки восходящим путем из нижних отделов половых путей или ЖКТ. В качестве инфекционных агентов в 90% случаев выступают факультативно-патогенные микроорганизмы, часто в виде полимикробных ассоциаций: энтеробактерии (E.coli, Klebsiella pneumoniae, Proteus spp., Enterococcus spp), эпидермальный стафилококк, стрептококки группы A и B, неспорообразующие анаэробы (Bacteroides fragilis, Peptococcus sp., Peptostreptococcus sp., Fusobacterium sp.), гарднерелла. Реже определяются микоплазмы, хламидии, гонококки.
Предпосылкой развития послеродового эндометрита считается снижение иммунной резистентности организма. В поздние сроки беременности и в ранний послеродовый период происходят значительные качественные сдвиги генитальной микрофлоры. Нарушается естественный антагонизм внутри ассоциаций микроорганизмов, обитающих во влагалище. Риск возникновения послеродового эндометрита повышается при наличии у беременной инфекционно-воспалительных заболеваний урогенитального и бронхолегочного тракта, очагов хронической инфекции, эндокринных нарушений, иммунодефицитов, аутоиммунных состояний и анемии. Фоном для снижения иммунитета беременной могут выступать низкий социальный уровень, недостаточное питание, вредные привычки.
Развитию послеродовых инфекционных осложнений способствуют проведенные ранее инструментальные вмешательства на полости матки (выскабливания, аборты), длительная внутриматочная контрацепция; особенности протекания беременности и родов (угроза прерывания, предлежание плаценты, хирургическая коррекция истмико-цервикальной недостаточности), инвазивные диагностические манипуляции (амнио- и кордоцентез, биопсия хориона), поздний разрыв плодных оболочек, длительный безводный промежуток и затяжные роды, хориоамнионит, патологическая кровопотеря, травмы промежности, ручное отделение плаценты, кесарево сечение. Причем, после родов через естественные родовые пути частота эндометрита составляет 1-3 % случаев, после планового оперативного родоразрешения - 5-15 %, после экстренного – более 20 %.
Неадекватное ведение послеродового периода, некомпенсированное восполнение кровопотери, продолжительный постельный режим, замедление инволюции матки, внутриутробная инфекция новорожденного (везикулез, пневмония, сепсис), плохая личная гигиена половых органов также формируют условия для развития инфекционных осложнений после родов.
Симптомы послеродового эндометрита
Послеродовой эндометрит может протекать в легкой, среднетяжелой и тяжелой форме, носить компенсированный, субкомпенсированный и декомпенсированный характер. При легком течении проявления острого послеродового эндометрита развиваются на 5-12 сутки после родоразрешения. Наблюдается озноб, подъем температуры до субфебрильной (до 38°С), учащение пульса до 80-100 уд/мин., болезненность брюшной стенки, умеренные кровяные лохии. Сократительная способность матки немного снижена. Состояние родильниц остается удовлетворительным и в течение 24 ч существенно не ухудшается.
Тяжелому течению заболевания нередко предшествуют хориоамнионит, осложнения родов или оперативное родоразрешение. Тяжелый послеродовой эндометрит возникает сразу на 2-3 сутки после родов. Характерны слабость, головная боль, фебрильный подъем температуры (39°С и выше) с ознобами, тахикардия (100-110 уд/мин.), боли внизу живота и в пояснице, нарушение аппетита и сна. Лохии становятся обильными мутными, кровянисто-гнойными с ихорозным запахом. В течение 24 ч возможна отрицательная динамика общего состояния. Инволюция матки происходит медленно. Послеродовой эндометрит может осложниться эндомиометритом, лимфаденитом и метротромбофлебитом, парезом кишечника, перитонитом, тазовым абсцессом, генерализацией инфекции.
Компенсированный тип эндометрита протекает с кратковременной (до 3 дней) резорбтивной лихорадкой и отсутствием субинволюции матки; субкомпенсированный - на фоне высокой лихорадки и выраженной субинволюции матки, декомпенсированный переходит в тяжелые гнойно-воспалительные осложнения - перитонит, сепсис, септический шок. Возможно протекание послеродового эндометрита в стертой форме со сравнительно поздним началом (5-7 сутки), нечеткой клиникой, затяжным течением, рецидивами и риском генерализации инфекции.
Диагностика послеродового эндометрита
В комплекс диагностики послеродового эндометрита входят анализ течения родов, данные клинической картины, бимануального осмотра, общего анализа крови и мочи, бакпосева отделяемого из полости матки, УЗИ малого таза с допплерографией, гистероскопия.
В общем анализе крови при послеродовом эндометрите обнаруживается лейкоцитоз (при легкой форме - 9–12×109/л, тяжелой - 10–30×109/л); нейтрофильный сдвиг формулы крови влево, подъем СОЭ (до 30–55 мм/ч и даже 55–65 мм/ч). Бакпосев отделяемого матки проводится для определения чувствительности микрофлоры к антибактериальным препаратам. Исследуется кислотно-основное состояние лохий (при эндометрите рН <7), при подозрении на сепсис осуществляется бакпосев крови. Дифференциальную диагностику послеродового эндометрита проводят с послеродовым параметритом, пельвиоперитонитом, метротромбофлебитом, тромбофлебитом вен таза.
Лечение послеродового эндометрита
Лечение послеродового эндометрита носит комплексный характер и включает медикаментозную и немедикаментозную тактику. Пациенткам с острым послеродовым эндометритом показана госпитализация в стационар, постельный режим, холод на низ живота, диета. Основной акцент делается на антибактериальную терапию. Сразу же назначаются антибиотики широкого спектра действия внутривенно (цефалоспорины III поколения), при выявлении чувствительности возбудителя к определенным препаратам – лечение. При легкой и среднетяжелой формах эндометрита достаточно монотерапии антибиотиками, при тяжелой – используются их различные комбинации (клиндамицин+гентамицин, метронидазол+гентамицин). При выраженной интоксикации необходимо назначение дезинтоксикационной инфузионной терапии, гемосорбции, лимфосорбции, плазмафереза.
Для улучшения оттока лохий используется сочетание средств, сокращающих матку (окситоцина) и спазмолитиков (дротаверина). Целесообразно применение антикоагулянтов (гепарина), антигистаминных препаратов, иммуностимуляторов, витаминов (А, C, К, труппы B). После купирования острой фазы хороший лечебный эффект дают физиопроцедуры - лекарственный электрофорез или ультрафонофорез, магнитотерапия, лазеротерапия, диадинамические токи, дарсонвализация и УФО (местно), иглорефлексотерапия.
При наличии остатков инфицированных и некротизированных плодных оболочек или последа необходимо проведение бережного кюретажа или вакуум-аспирации содержимого полости матки, внутриматочного лаважа дезинфицирующими растворами, промывного дренирования. В отсутствие эффекта от интенсивно проводимой терапии (по истечении 7 суток от начала лечения послеродового эндометрита) и сохранении клинико-лабораторных критериев воспаления решается вопрос об удалении матки - гистерэктомии.
Прогноз послеродового эндометрита зависит от степени тяжести заболевания: лечение легкой и среднетяжелой форм заканчивается выздоровлением и сохранением репродуктивной функции; тяжелая декомпенсированная форма может осложниться септическим состоянием, потерей матки, летальным исходом. Предупреждение послеродового эндометрита заключается в контроле микрофлоры влагалища беременных, правильном ведении родов и послеродового периода, профилактической антибиотикотерапии после кесарева сечения.
Септический шок (бактериальный, эндотоксический, инфекционно-токсический шок) представляет собой клинический синдром, который протекает на фоне генерализации септического процесса и который можно рассматривать как осложнение послеродовых и послеабортных воспалительных заболеваний.
Что провоцирует / Причины Септического шока в послеродовом периоде:
Септический шок, представляющий собой самую тяжелую клиническую форму генерализованной инфекции, развивается на фоне имеющегося сепсиса и эндотоксемии и характеризуется неполноценной перфузией системы микроциркуляции жизненно важных органов.
Летальность больных с септическим шоком достигает 62-80 %.
Патогенез (что происходит?) во время Септического шока в послеродовом периоде:
Понятие "септический шок" подчеркивает полиэтиологичность данного патологического состояния. Понятие "шок" характеризует общебиологическую сущность синдрома и отражает состояние организма, находящегося в крайне неблагоприятной ситуации, обусловленной нарушениями механизмов регуляции сосудистого тонуса, микроциркуляции и адекватной тканевой перфузии.
Среди акушерских осложнений, заболеваний и клинических состояний чаще всего к септическому шоку приводят инфицированные аборты, хориоамнионит, мастит, пиелонефрит, оперативное родоразрешение (кесарево сечение). Следовательно, септический очаг в случае послеродового сепсиса располагается чаще всего в матке. При этом входными воротами инфекции служит огромная всасывающая поверхность плацентарной площадки.
Сепсис в послеродовом периоде скоротечен, поэтому выраженные иммунные нарушения, требующие временного интервала, не успевают развиться. Тяжесть состояния в данном случае обусловливается гиперергической реакцией организма на возбудитель, который быстро размножается в матке, имеющей большую раневую поверхность и богатое кровоснабжение.
Факторы риска развития септического шока аналогичны таковым при любых других послеродовых гнойно-воспалительных заболеваний.
В ответ на острую микробную инвазию в организме повреждается практически вся система регуляции гомеостаза: гуморальная регуляция и адаптация, метаболизм, иммунитет, транспортировка кислорода, газообмен. Однако определяющими являются изменения гемодинамики по типу стойкой гипотонии с характерным для этого нарушением перфузии тканей.
Активным началом развития септического шока являются:
- компоненты оболочки грамположительных бактерий - мукопептиды;
- стафилококковый протеин А;
- эндотоксины, продуцируемые грамотрицательными микроорганизмами.
Эндотоксины представляют собой высокомолекулярный комплекс моно- и полисахаридов, который образует часть наружной клеточной стенки грамотрицательных бактерий. Биологически активным эндотоксин становится лишь при гибели микроорганизмов.
Эндотоксин воздействует на клеточно-гуморальные механизмы, поддерживающие гомеостаз, и вызывает выделение биологически активных веществ, приводящих к развитию септического шока.
Эндотоксин вызывает повреждение эндотелия, а также циркулирующих лейкоцитов и тромбоцитов. Это приводит к слущиванию клеток эндотелия сосудов, обнажению базальной мембраны сосудов, выделению гистамина и серотонина, агрегации и разрушению лейкоцитов с высвобождением в просвет сосудов протеолитических ферментов из лизосом лейкоцитов.
Важнейшим компонентом патогенеза септического шока является ДВС-синдром, развитию которого способствует:
- активация фактора XII (Хагемана);
- повреждение эндотелия сосудов с выделением тканевого тромбопластина;
- агрегация тромбоцитов;
- высвобождение АДФ, серотонина, гистамина;
- активация факторов 3 и 4 свертывания крови;
- высвобождение тромбоксана А;
- ингибиция простациклина;
- гемолиз эритроцитов;
- воздействие эндотоксина на систему комплемента и каллекреин-кининовую систему.
Таким образом, на ранних этапах действия эндотоксина происходит:
- нарушение правильного распределения кровотока в капиллярах за счет дистонии артериол вследствие чрезмерного выброса веществ, влияющих на сосудистый тонус;
- спазм артериол, их паралитическое расширение, открытие артериовенозных шунтов и сброс из них части крови;
- образование мельчайших фибриновых, тромбоцитарных и смешанных микротромбов;
- увеличение вязкости крови за счет появления мономеров фибрина в кровотоке и явлений эритроцитарного сладжа;
- ухудшение капиллярной перфузии.
Септический шок сопровождается острой циркуляторной недостаточностью с критическим снижением периферического кровотока.
В связи с изменением характера гемодинамики при сепсисе возрастает работа сердца, и в первую очередь - сердечный выброс. Существенно увеличивается работа левого желудочка. Сердечный индекс незначительно превышает норму. В связи с дальнейшим неизбежным повышением периферического сопротивления из-за развития ДВС-синдрома усиливается тканевая гипоксия, развиваются миокардиодистрофия и вторичный гиповолемический синдром, характеризующийся уменьшением притока венозной крови к сердцу и минутного объема из-за задержки жидкости на периферии. Выраженное повышение легочного сосудистого сопротивления и легочная гипертензия способствуют прогрессированию сердечной недостаточности. Избыточная нагрузка на внешнее дыхание и миокард, несоответствие между ОЦК и емкостью сосудистого русла приводят к несоответствию между потребностями организма в кислороде и питательных веществах и возможностями их доставки, к неспособности организма элиминировать продукты обмена. Результатом этого являются органные и метаболические расстройства.
Нарушение капиллярной перфузии тканей вызывает включение компенсаторно-приспособительных механизмов:
- Усиливается фибринолиз в клетках эндотелия сосудов, находящихся в контакте с тромбом, что приводит к последующему лизису тромба и восстановлению проходимости сосудов.
- Активизируются клетки системы макрофагов, обеспечивающие фагоцитоз бактерий и обезвреживание токсичных продуктов.
При существовании длительной эндотоксемии наступает декомпенсация системы гомеостаза, что приводит к дальнейшему ухудшению условий функционирования тканей организма.
Блокада микроциркуляции обусловливает:
- развитие анаэробного гликолиза;
- депонирование крови в выключенных из циркуляции участках тканей;
- нарастание метаболического ацидоза;
- резкое увеличение проницаемости клеточных мембран;
- спазм и микротромбоз капилляров почечных клубочков с нарушением их функции вплоть до анурии;
- гипоксию, отек, жировую дистрофию и некроз частей печеночных долек;
- массовую обструкцию фибриново-тромбоцитарными тромбами капилляров легочной артерии;
- отек внутриальвеолярной перегородки;
- открытие артериовенозных шунтов;
- геморрагическое пропитывание легочной ткани.
Все эти многочисленные изменения являются патофизиологической основой клинических проявлений септического шока.
Симптомы Септического шока в послеродовом периоде:
Первым проявлением шока у больных обычно является озноб, сопровождающийся гипертермией до 39-40С с последующим снижением температуры тела до субнормальной или нормальной. С первых часов заболевания отмечаются частый, но ритмичный пульс, одышка, в легких выслушиваются влажные хрипы. Артериальное давление снижается до 60/20 мм рт. ст. и менее.
При диагностике шока часто основываются на показателях артериального давления, определяемого на плечевой артерии. Однако необходимо учитывать, что септический шок может развиться и при нормальном артериальном давлении. У отдельных больных могут наблюдаться даже повышенные цифры артериального давления.
Нередко при септическом шоке на первый план выступает острая сердечная недостаточность, основными клиническими признаками которой являются гипотония или коллапс, а также увеличение и болезненность печени. Это состояние обусловлено депонированием крови на периферии, уменьшением венозного оттока, снижением сердечного дебита и уменьшением систолического выброса крови.
В диагностике септического шока крайне важное значение имеет оценка функции легких, которая нарушается вследствие блокады легочного кровотока тромбоцитарно-фибриновыми агрегатами. Обычно нарушения функции легких проявляются в виде отека и развития острой легочной недостаточности, для которых характерны тахипноэ и метаболический ацидоз. Рентгенологически во всех отделах легких обнаруживают облаковидные затемнения, являющиеся проявлением интерстициального отека легочной ткани.
В начальных стадиях развития септического шока печень и селезенка определяются в обычных границах. С увеличением продолжительности шока у больных появляются схваткообразные боли в животе, частый обильный стул. Моча кровянистая, с большим содержанием белка. Позже она становится бурой, а в последующие дни цвет ее вновь становится обычным.
Одним из характерных для септического шока объективных симптомов неадекватного кровоснабжения жизненно важных органов является нарушение функции почек, проявляющееся олигурией (выделение до 20 мл мочи за 1 ч). В дальнейшем снижается относительная плотность мочи и развивается почечная недостаточность.
При септическом шоке имеет место появление парестезии, сильных мышечных болей, которые усиливаются даже при прикосновении постельного белья.
Отмечаются некоторые изменения психики больных с септическим шоком, что вначале выражается чувством беспокойства, возбуждением, а через 4-6 ч сменяется безразличием к окружающему, некритическим отношением к своему состоянию, эйфорией.
Следует отметить, что картина септического шока во многом определяется нарушением микроциркуляции, обусловленным ДВС-синдромом, клиническая диагностика которого неотделима от диагностики септического шока.
Клиническими проявлениями ДВС-синдрома являются:
- кровоточивость в одном или нескольких местах (в месте уколов, из матки, из поврежденных при операции тканей);
- клинически выраженный гемолиз и геморрагический диатез;
- бледность и акроцианоз кожных покровов;
- нарушение функции печени и почек;
- дыхательная недостаточность;
- нарушение сознания.
В первые часы шока багрово- красный цвет кожных покровов резко контрастирует с цианотичной окраской губ, ногтевого ложа и кончиков пальцев. К 6-12 ч заболевания на коже губ, носа и других участках появляются высыпания геморрагического характера. Геморрагический некроз кожи лица, синюшность кожи рук, ног, носа, щек и ушных раковин указывают на признаки ДВС-синдрома.
Геморрагический диатез часто также проявляется желудочно-кишечными кровотечениями, кровоизлияниями в склеры глаз и метроррагиями.
Независимо от причин шока его тяжелые клинические признаки обычно отодвигают на задний план симптомы заболевания, являющегося причиной возникновения шока.
При исследовании периферической крови в первые часы заболевания выявляется лейкопения, сменяющаяся к концу 1-х суток прогрессирующим лейкоцитозом. При бактериологическом анализе у 1/4 больных удается высеять возбудитель из крови, почти у 1/2 - из мочи и у 90 % - из шеечного канала.
Точная диагностика патологического внутри-сосудистого свертывания крови возможна лишь при своевременном лабораторном исследовании системы гемостаза.
Подострая и острая формы ДВС-синдрома у больных с септическим шоком характеризуются выраженной тромбоцитопенией (50,0 * 109/л), гипофибриногенемией (менее 1,5 г/л), повышенным потреблением антитромбина и плазминогена, резким повышением содержания дериватов фибрина и фибриногена, ПДФ, удлинением век.
При хроническом ДВС-синдроме имеют место умеренная тромбоцитопения (менее 150,0* 109/л), гипофибриногенемия, усиленное потребление антитромбина III, повышение концентрации РКМФ и ПДФ, а также реальная гиперактивность системы гемостаза.
При затянувшемся шоке (более 1 сут), как правило, имеет место волнообразное его течение со сменой в периферической крови гиперкоагуляции на гипокоагуляцию, и наоборот. Эти изменения гемостаза находятся во взаимосвязи с расстройствами микроциркуляции (спазм артериол, уменьшение количества функционирующих капилляров, внутрисосудистая агрегация эритроцитов).
Адаптационная реакция организма в ответ на инфекцию сопровождается задержкой жидкости в организме. В первые часы шока, несмотря на увеличение ОЦК, содержание натрия в плазме крови сохраняется на физиологическом уровне, а концентрация калия снижается вплоть до развития острой почечной недостаточности. Одновременно отмечаются накопление в крови недоокисленных продуктов обмена, сдвиг КОС крови в сторону дыхательного алкалоза и метаболического ацидоза.
К концу 1-х суток происходит декомпенсация метаболических нарушений, снижается рН и развивается выраженный метаболический ацидоз.
При патологоанатомическом исследовании больных, умерших от септического шока, изменения в родовых путях нередко бывают обусловлены повреждениями тканей при абортах, выкидышах или вследствие гнойно-септического процесса в матке.
Матка при этом атонична, с дряблыми стенками, зияющими сосудами, полость ее расширена, содержит сгустки крови и участки некротизированных тканей.
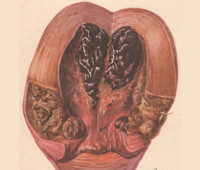
Если смерть больной наступает вследствие нарушения процесса отделения плаценты, то макро- и микроскопически обнаруживаются признаки септического процесса в плаценте и матке, при этом плацента имеет вид вареного мяса с резким гнилостным запахом. При микроскопическом исследовании в плаценте или ее остатках определяются очаги некроза, где содержится большое количество бактерий. В субплацентарной зоне выявляются кровоизлияния и некрозы поверхностных отделов мышцы матки. В сосудистом русле плаценты и спиральных артериях обнаруживаются множественные тромбоцитарно-фибриновые тромбы.
Для патоморфологической картины внутренних органов (почек, печени, легких, надпочечников, гипофиза, желудочно-кишечного тракта) умерших больных характерно наличие большого количества тромбоцитарно-фибриновых тромбов в микроциркуляторном русле в сочетании с многочисленными участками кровоизлияний. Эти морфологические изменения сопровождаются переполнением венозной системы кровью, депонированием ее в портальной системе кровообращения. Кровоизлияния обычно имеют петехиальный характер, они наблюдаются преимущественно в коже, слизистой оболочке желудочно-кишечного тракта, в миокарде, легких, почках, яичниках. Наиболее постоянно они возникают в корковом веществе надпочечников и стволовом отделе головного мозга.
Диагностика Септического шока в послеродовом периоде:
Диагноз септического шока устанавливают на основании анализа данных анамнеза, результатов клинического и лабораторного обследования, свидетельствующих о проявлениях бактериемии, а также на основании данных инструментальных методов исследования.
Для уточнения диагноза септического шока и проведения целенаправленной терапии в первую очередь необходимо проведение следующих мероприятий:
- контроль артериального давления, ЦВД, частоты дыхания каждые 30 мин;
- измерение ректальной температуры 4 раза в сутки, особенно после озноба, для сопоставления с данными температуры тела в подмышечной области;
- посевы крови в момент госпитализации и во время ознобов с определением чувствительности выделенной микробной флоры к антибиотикам;
- почасовой контроль за диурезом;
- выделение микробной культуры из мочи, определение чувствительности микробов к антибиотикам;
- определение содержания электролитов сыворотки, азота, мочевины, креатинина, мочевой кислоты, газов артериальной крови, рН;
- постоянный мониторный контроль ЭКГ, частоты сердечных сокращений;
- рентгенологическое исследование грудной клетки, брюшной полости при вертикальном положении пациентки для обнаружения свободного газа под диафрагмой, а также исключения инородного тела в брюшной полости;
- общий анализ крови с оценкой лейкоцитарной формулы, определение гематокритного числа;
- исследование показателей свертывания крови: количество тромбоцитов, фибриногена, РКМФ, ПДФ, антитромбина III, показателей тромбоэластограммы.
Ультразвуковое и рентгенологическое исследование, КТ и МРТ выполняют для уточнения расположения первичных и вторичных (метастатических) гнойных очагов.
Лечение Септического шока в послеродовом периоде:
Лечение септического шока основывается на следующих принципах.
- Раннее и полное удаление септического очага (матки) с широким дренированием брюшной полости.
- Проведение массивной и длительной антибактериальной терапии. При этом возможны следующие сочетания антибиотиков:
- ампициллин (4-6 г/сут) и гентамицин (240 мг/сут);
- ампициллин (4-6 г/сут) и канамицин (2 г/сут);
- бензилпенициллина натриевая соль (6000000-20000000 ЕД/сут) и гентамицин (240 мг/сут) или канамицина (2 г/сут);
- клафоран (4-8 г/сут) или цефамезин (4-8 г/сут) с гентамицином (240 мг/сут).
Эти компоненты терапии должны применяться сочетанно в наиболее ранние сроки заболевания с учетом состояния больных и показателей гемостаза.
К каким докторам следует обращаться если у Вас Септический шок в послеродовой период:
Вас что-то беспокоит? Вы хотите узнать более детальную информацию о Септического шока в послеродовом периоде, ее причинах, симптомах, методах лечения и профилактики, ходе течения болезни и соблюдении диеты после нее? Или же Вам необходим осмотр? Вы можете записаться на прием к доктору .
Читайте также:

