Схема патогенеза при вич инфекции
Обновлено: 19.04.2024
ВИЧ. Вирус иммунодефицита человека. СПИД. Эпидемиология вич-инфекции.
Вирус иммунодефицита человека (ВИЧ) — возбудитель своеобразной инфекции, проявляющейся развитием прогрессирующих нарушений иммунного реагирования в результате длительного циркулирования вируса в лимфоцитах, макрофагах и клетках нервной ткани.
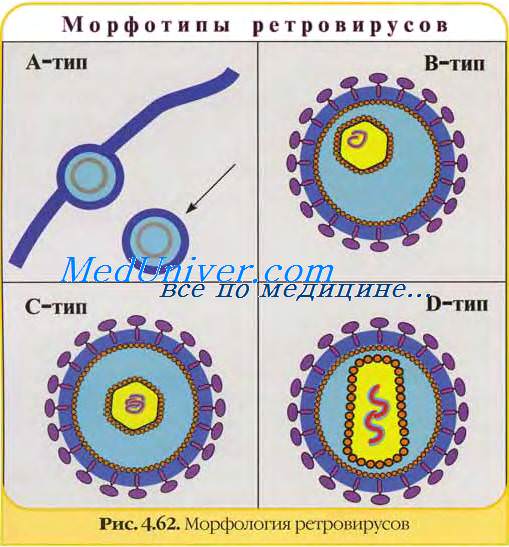
Следствие ВИЧ-инфекции — синдром приобретённого иммунодефицита (СПИД). ВИЧ входит в состав подсемейства Lentivirinae семейства Retroviridae. Характерные особенности ретровирусов — уникальное строение генома и наличие обратной транскриптазы (РНК-зависимая ДНК-полимераза). Обратная транскриптаза (или ревертаза) обеспечивает обратную направленность потока генетической информации — не от ДНК к РНК, а наоборот, от РНК к ДНК, в связи с чем семейство и получило своё название 1от англ. retro, обратно].
Геном вич образует две идентичные молекулы однонитевой несегментированной +РНК. Репродуктивный цикл вич уникален, так как при его реализации образуются промежуточные продукты-интермедиаты ДНК.
В настоящее время выделяют два типа вирусов: ВИЧ-1 (HIV-1)— основной возбудитель ВИЧ-инфекции, ВИЧ-2 (HIV-2) — менее вирулентный аналог ВИЧ-I, редко вызывающий типичные проявления СПИДа; его выделяют преимущественно в Западной Африке.
Впервые ВИЧ выделили французский вирусолог Л. Монтаньё (1983) под названием LAV [от англ. tymphoadenopathy associated virus] и американский вирусолог Р. Гэлло (1984) под названием вирус HTLV-III [Т-лимфотропный вирус человека III типа]. После установления идентичности HTLV-III и LAV во избежание путаницы вирусу было присвоено название HIV [англ. human immunedeficiency virus, вирус иммунодефицита человека], или ВИЧ.
Эпидемиология вич-инфекции
ВИЧ-инфекция — типичный антропоноз, у животных воспроизвести заболевание не удаётся. Резервуар вируса вич-инфекции — инфицированный человек. Возбудитель передаётся трансмиссивно.
Основной фактор передачи вич-инфекции — половые контакты (вирус проникает в кровь через повреждения слизистых оболочек). Второй по значимости фактор передачи вируса вич-инфекции — использование одних и тех же игл и шприцев наркоманами.
ВИЧ чувствителен к действию высоких температур (при 56 X инактивируется за 30 мин, при 70-80 °С — через 10 мин), этанола, эфира, ацетона и многих дезинфектантов. В крови и других биологических материалах при комнатной температуре вирус сохраняет жизнеспособность в течение нескольких суток.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
6.3. ПАТОГЕНЕЗ ВИЧ-ИНФЕКЦИИ
В связи с тем что вирусы являются патогенами внутриклеточными, ка-ждый представитель мира вирусов имеет тропность к определенному типу клеток. Тропизм вируса определяется наличием на клетке-мишени рецептора для данного вируса, а также возможностью генома вируса встроиться в геном клетки. Рецепторы для определенного вируса могут быть на клетках различ-ных типов. Рецепторную функцию выполняют различные структуры (лиган-ды): белки, липиды, углеводные компоненты белков и липидов. Эти лиганды локализованы на плазматической мембране и выполняют важнейшие функ-ции жизнеобеспечения клетки – проникновение в нее гормонов, питательных веществ, факторов роста и регуляции и т.п.
Рецепторы, независимо от их биохимического строения, имеют общую структурную характеристику, а именно, состоят из участка, расположенного вне клетки, участка, локализованного внутримембранно, и участка, погру-женного в цитоплазму.
Рецепторами для ВИЧ являются дифференцировочный антиген CD4, а также неспецифические, не зависящие от наличия CD4 компоненты. CD4 -гликопротеид с молекулярной массой 55 000, по своему строению имеющий гомологии с определенными участками иммуноглобулинов. Аналогичные гомологии имеет и белок вируса gp120, что и определяет тропность ВИЧ. Фиксация вируса через gp120 ВИЧ-1 (или gp105 в случае инфицирования ВИЧ-2) с мембранным рецептором CD4 клетки хозяина блокирует основную функцию этих иммунокомпетентных клеток - восприятие сигналов от анти-генпрезентирующих клеток. Последующая за рецепцией репликация вируса ведет к гибели клеток, выпадению функции, ими выполняемой, развитию иммунодефицита.
В организме человека имеется целый ряд иммунокомпетентных, сома-тических и ряд других клеток, имеющих рецепторы для ВИЧ (CD4+ лимфо-циты, CD8+ лимфоциты, дендритные клетки, моноциты, эозинофилы, мега-кариоциты, нейроны, микроглия, сперматозоиды), и наблюдается цитопати-ческий эффект во многих из них в случае проникновения вируса.
В 1996 году Бергер открыл корецептор для ВИЧ. Этот рецептор вместе с CD4 опосредует инфицирование СО-вариантами ВИЧ-1, адаптированных к росту в Т-хелперах, но не в макрофагах. На сегодня известно около 10 хемо-киновых рецепторов.
Таким образом, выделены белки - хемокины, блокирующие проникно-вение ВИЧ в макрофаги с антигеном CD4, и белки - корецепторы, способст-вующие инфицированию. При этом корецепторы – это рецепторы для хемо-кинов, но их использует ВИЧ в качестве рецептора, с помощью которого проникает внутрь клетки.
Проникнув в СD4+ клетки, ВИЧ сразу же начинает репликацию, при этом, чем активнее CD4+ клетки, тем выше процесс репродукции вируса. Все регуляторы, активирующие СD4+клетки, обеспечивают увеличение реплика-ции вируса. К подобным регуляторам относятся фактор некроза опухолей (ФНО), фактор, стимулирующий колонии гранулоцитов/макрофагов, интер-лейкин-6 (ИЛ-6). К негативным регуляторам, тормозящим репликацию виру-са, относятся интерферон (ИФ) и трансформирующий фактор роста.
Морфофункциональные изменения в моноцитах/макрофагах оказыва-ют разнонаправленное действие не только на Т-лимфоциты, но и естествен-ные киллеры - главные клетки противоопухолевой защиты. Активность по-следних по мере прогрессирования заболевания неуклонно снижается. Дефи-цит ИЛ-2 и γ-интерферона даже при нормальном количестве NK-клеток ве-дет к снижению функциональной активности их у больных ВИЧ-инфекцией (Ковальчук Л.В., Чередеев А.Н.,1991).
Выделено два типа CD4+клеток: Т-хелперы-1 (Th1) и Т-хелперы-2 (Th2). Тh1 продуцируют цитокины, стимулирующие клеточный иммунитет, а Тh2 – цитокины, усиливающие антителогенез. Соотношение Тh1 и Тh2 взве-шенно и конкурентно; суперэкспрессия цитокинов одного типа клеток ведет к супрессии другого. У больных ВИЧ-инфекцией идет угнетение Тh1, чем обеспечиваются и вирусная патология, и онкогенез.
Жизненный цикл ВИЧ после проникновения в организм имеет после-довательный характер: связывание вириона с поверхностью клетки, слияние мембран вириона и клетки, проникновение вируса внутрь клетки, высвобож-дение нуклеотида и геномной РНК вируса, интеграция генома вируса в геном инфицированной клетки, латентная фаза, фаза активации транскрипции с ДНК провируса и последующая транскрипция белков вируса, наработка всех компонентов вируса с формированием новых вирионов и их высвобождени-ем из клетки, влекущим за собой гибель клетки-мишени (рис.6.4.).
Рис. 6.4. Стадии проникновения ВИЧ в клетку (Ледванов М.Ю., 1997).
Судьба ДНК-транскрипта генома ВИЧ, интегрированных в хромосому пораженной клетки, может быть различна. Она определяется активностью положительных и отрицательных регуляторных генов. Если активны все по-ложительные регуляторные гены, то происходит репродукция вируса со все-ми вытекающими отсюда последствиями – идет активация инфекции.
Если активны все отрицательные регуляторные гены, синтеза компо-нентов вириона не происходит, и инфекция не развивается.
Если активны положительные регуляторные гены белков суперкапсид-ной оболочки, происходит образование этих белков, и они экспрессируются на поверхности инфицированных клеток. Такие клетки способны взаимодей-ствовать с CD4 - рецепторами клеток организма и нарушать их функции. Та-ким образом, хотя репродукции вирусов не происходит, имеют место опре-деленные проявления инфекции.
Равным образом события развиваются при активности положительных регуляторных белков капсидной оболочки. Их повреждающее действие на клетки существенно ниже, но они индуцируют образование соответствую-щих антител.
Если же активны положительные регуляторные гены только геномных белков, то в пораженных клетках образуется обратная транскриптаза, которая довольно быстро разрушается.
Сродство вирусного мембранного гликопротеида gp120 (gp105 в случае ВИЧ-2) к клеточному рецептору CD4 определяет высокую степень избира-тельного поражения клеточных структур, поэтому в патологический процесс вовлекаются, в первую очередь, и в большей степени CD4+ лимфоциты, мо-ноциты крови, макрофаги тканей, дендритные клетки крови, лимфатических узлов, селезенки, кожи, альвеолярных и интерстициальных макрофагов лег-ких, микроглия и другие клетки нервной системы, имеющие CD4 - рецепто-ры. Так же поражаются В- и О-лимфоциты, ретикулярные клетки, эпители-альные клетки кишечника, клетки Лангерганса, причем последние инфици-руются даже легче, чем CD4+ лимфоциты. Именно клеткам Лангерганса придается большое значение в распространении ВИЧ по организму, ибо в них вирус сохраняется длительное время, иногда годы.
Наличие CD4 рецептора на многих и не только иммунокомпетентных клетках, возможность поражать и клетки, не имеющие этого рецептора, оп-ределяют политропность ВИЧ и полиморфизм клинической картины. Сте-пень поражения тех или иных, содержащих СD4 рецепторы, клеток зависит от плотности этих рецепторов на мембране клеток. Наиболее высока плот-ность на Т-хелперной субпопуляции лимфоцитов, что и определяет во мно-гом патогенез болезни. Но степень поражения клеток-мишеней вирусом за-висит также и от возможности репликации вируса в том или ином виде кле-ток. Очевидно, осуществляется репликация в основном в лимфоцитах с CD4+ фенотипом и моноцитах/макрофагах.
Если на CD4+ лимфоциты вирус оказывает цитопатическое действие с лизисом клетки или слиянием в синцитий, то в моноцитах/макрофагах ВИЧ реплицируется с умеренной интенсивностью; вирионы оформляются в ок-руглые частицы еще в цитоплазме клетки и по выходе из нее не оказывают цитонекротического действия. Изучение динамики сывороточных монокинов подтверждает активное участие в патогенезе ВИЧ-инфекции моноци-тов/макрофагов, основных продуцентов фактора некроза опухолей и интер-лейкина-1b (выполняющих роль передатчика Т-лимфоцитам антигенспеци-фических сигналов, необходимых для их активации в иммунном ответе). С гиперпродукцией ФНО-a , ИЛ-1b и ИЛ-6 связывают развитие при ВИЧ-инфекции лихорадки, анемии, диареи, кахексии, патологических изменений на коже и слизистых при саркоме Капоши, церебральных симптомов. ФНО-a при этом оказывает прямое цитопатическое действие на инфицированные ВИЧ Т-хелперы. В то же время было установлено, что ВИЧ ингибирует про-дукцию ИЛ-2 и γ-ИФ, синтезируемым Т-хелперами первого типа, и не инги-бирует функцию Т-хелперов второго типа. Следовательно, играя важную роль в регуляции синтеза цитокинов, ВИЧ за счет переключения иммунного ответа с Т-хелперов первого типа на Т-хелперы второго типа, стимулирует гуморальное звено иммунитета.
После инфицирования клетки вирусом происходит соединение вирус-ной оболочки с помощью белка gp41 с мембраной клетки. Помимо того, ви-русный белок gp41 обеспечивает слияние мембран соседних клеток между собой с образованием одной многоядерной клетки - синцития. При этом слияние может быть как зараженных клеток между собой, так и зараженных с незараженными. Но синцитий в основном индуцируют вирусы, выделенные от больных с клиническими проявлениям ВИЧ-инфек-ции, и не образуют выделенные от инфицированных людей, не имеющих клинических проявле-ний.
С момента интеграции генома вируса в геном клетки начинается стадия латентной инфекции. В этот период вирус находится в клетке в виде интег-рированного в геном ДНК – провируса. Раньше полагали, что в этот период отсутствуют процессы транскрипции и трансляции с вирусных генов, а по-этому и экспрессии вирусных белков, нет иммунного ответа на вирус как в виде специфических иммуноглобулинов, так и сенсибилизированных лим-фоцитов. Но последние исследования показали, что сразу после проникнове-ния вируса в клетку начинаются и трансляция, и транскрипция.
Состояние латентной инфекции без клинических признаков болезни может длиться от 2 до 11 лет. Активация длинных концевых повторов и экс-прессия генов ВИЧ, кодирующих белки вируса, знаменуют собой манифе-стацию болезни.
В расшифровке патогенеза ВИЧ-инфекции многие вопросы решены, установлены основные этапы развития процесса в клетке после инфицирова-ния ее вирусом. Выявлен ряд факторов, активирующих экспрессию генов ВИЧ. К ним относятся факторы, активирующие Т-лимфоциты: специфиче-ские антигены (например, вирусы группы Herpes), неспецифические антиге-ны (например, митогены типа фитогемаглютинина), цитокины (например, фактор некроза опухолей, некоторые интерлейкины, гамма-интерферон), бактериальные иммуномодуляторы (например, монофосфат липида из саль-монелл). К активаторам экспрессии ВИЧ относятся глюкокортикостероидные гормоны, в частности, дексаметазон и гидрокортизон, ультрафиолетовое об-лучение, перекись водорода, свободные кислородные радикалы. Активирует инфекционный процесс беременность; более прогрессирующее течение ВИЧ-инфекции имеют психически неуравновешенные лица, дезадаптированные, по сравнению с людьми, имеющими уравновешенную психику.
Довольно сложен и до конца не выяснен механизм репликации вируса в инфицированной клетке. Известно, что в цитоплазме информация с вирус-ной РНК посредством обратной транскриптазы (ревертазы) переписывается на ДНК, первоначально образуется однонитевая структура; затем та же об-ратная транскриптаза обеспечивает образование второй нити, и линейная промежуточная форма ДНК-транскриптаза вируса - транспортируется в ядро, где с помощью фермента интегразы интегрирует в хромосому клетки, пре-вращаясь в провирус.
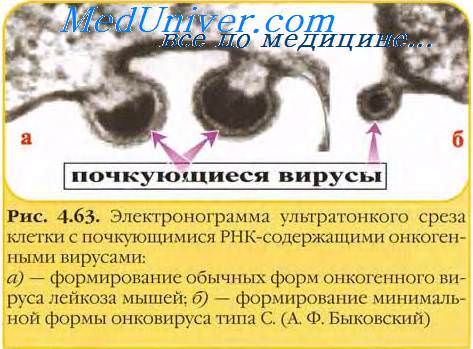
Исключительно важный этап патогенеза болезни – сборка вирусных частиц и выход нового потомства вируса из инфицированной клетки. Сборка происходит на плазматической мембране лимфоцита, куда поступают все компоненты вирусной частицы, в том числе и белки-предшественники. За-вершается процесс почкованием вирусных частиц с клеточной поверхности. Отличительной чертой ВИЧ является взрывной характер процессов актива-ции транскрипции, синтеза белков-пред-шественников, сборки вирионов и их почкования: за 5 мин одна лимфоцитарная клетка может образовать до 5000 вирусных частиц.
Ключевой вопрос патогенеза ВИЧ-инфекции – механизм иммунного повреждения. Как установлено, в составе белков gp120, главного комплекса гистосовместимости (HLA) класса II и CD4-рецепторов имеются сходные участки, что определяет перекрестное реагирование образующихся к ВИЧ антител с этими структурами. Например, происходит блокада кооперации CD4+ лимфоцитов и HLA II. Антитела к gp120 ВИЧ реагируют с CD4, обу-словливая неадекватную стимуляцию CD4+ клеток. На всех ядросодержащих клетках имеются антигены HLA I; вирус же нарушает синтез этих антигенов, участвующих в распознавании CD8+ лимфоцитами зараженных вирусом клеток, что тормозит процесс лизиса инфицированных клеток.
Взаимосвязь жизненного цикла вируса и иммунных сдвигов в началь-ной фазе ВИЧ-инфекции изучена в эксперименте при заражении SIV обезьян; полученные данные экстраполированы на человека. Как показали исследова-ния, вирус первоначально локализуется в лимфоидной системе, вирусная экспрессия определяет клинику ранней фазы болезни. Пик экспрессии вируса в клетках лимфоидной ткани предшествует накоплению его в плазме. Появ-ление вирусспецифических цитотоксических Т-лимфоцитов (CTL) совпадает со временем окончания экспрессии вируса в лимфатических узлах. Продук-ция комплементсвязывающих антител облегчает переход вируса в сеть денд-ритных клеток герминальных центров лимфатических узлов. Повреждающее действие CTL и продукция комплементсвязывающих антител оказывают ос-новное патогенное действие в результате виремии. Образование нейтрали-зующих антител обеспечивает переход острой фазы болезни в хроническую.
Иммунопатогенетически ВИЧ-инфекция проявляется дефицитом Т- и В-звеньев иммунной системы, дефицитом комплемента, фагоцитов, сниже-нием функции неспецифических факторов защиты. В результате идет фор-мирование анергии с проявлениями аллергического, аутоаллергического и иммунокомплексного патологического процесса. Уже во II стадии ВИЧ-инфекция характеризуется снижением абсолютного числа лейкоцитов за счет CD3+, CD4+, p24+ и gp120+ лимфоцитов, повышением уровня естественных киллеров (NК-клетки), нарастанием реакции торможения миграции лимфо-цитов с конкавалином А и фитогемагглютинином. Изменения гуморального звена иммунитета проявляются нарастанием IgG+ В-лимфоцитов и 4-5-кратным ростом уровня сывороточных IgE.
Для изменений В-звена иммунитета характерна активация В-лимфоцитов. Изменение их метаболизма сопровождается уменьшением вре-мени полуобмена иммуноглобулиновых рецепторов с повышением в крови концентрации клеточных рецепторов (Р-белки). Суммарная концентрация сывороточных иммуноглобулинов растет, но выявляется диспропорция уровней подклассов иммуноглобулинов. Так, содержание IgG1 и IgG3 у больных увеличивается, а концентрация IgG2 и IgG4 существенно уменьша-ется. Очевидно, повышение уровня IgG2 связано с высокой восприимчиво-стью больных к стафилококкам, пневмококкам, палочке инфлюэнцы. Не-смотря на гипергаммаглобулинемию, увеличение количества циркулирую-щих в крови В-лимфоцитов, их функциональная активность на митогены ос-таются относительно сниженными, что позволяет В-систему иммунитета у ВИЧ-больных расценивать как супрессированную. К тому же, количество В-клеток в периферической крови больных в стадии СПИДа может быть сни-жено в три и более раз.
Многочисленными исследованиями показано, что взаимодействие gp120 ВИЧ-1 с мембраной CD4+ лимфоцитов определяет не только отрица-тельные реакции инфицированных клеток, но и приводит к программирован-ной клеточной гибели - апоптозу зрелых CD4+ лимфоцитов или CD34+ ге-мопоэтических клеток-предшественников даже при отсутствии их инфици-рования вирусом.
Специфический иммунный ответ при ВИЧ-инфекции имеет ряд осо-бенностей. Локализуясь в иммуноците, вирус проникает в органы и ткани, пребывая вне доступности для иммунной системы, чем определяется перси-стенция в клетках как вируса, так и его компонентов – белков, нуклеокапси-дов, нуклеиновой кислоты. Активация инфекционного процесса ведет к гу-моральному иммунному ответу с образованием антител. Но в связи с наличи-ем в составе вирусного белка gp120, HLA класса II и CD4-рецептора лимфо-цита сходных участков образующиеся антитела перекрестно реагируют с ни-ми, чем обусловливают нарушение кооперативных взаимодействий в функ-ционировании иммунной системы. Все это определяет формирование ауто-аллергических реакций. Именно поэтому в ходе развития инфекционного процесса формируется гиперчувствительность замедленного и немедленного типов, преимущественно к антигенам ВИЧ, в частности, gр41 и gp120. Так, Л.Монтанье (1996) считает, что в патогенезе СПИДа основное место принад-лежит аутоиммунному процессу. В пользу этого говорят исследования харак-тера иммунных реакций у больных: наличие аутоантител и аллоантител к лимфоцитам, формирование аллергических реакций цитотоксического типа, накопление циркулирующих иммунных комплексов, наличие комплементо-посредованной цитотоксичности, активация антителозависимой клеточной цитотоксичности. Кроме того, при сильном антительном ответе возможность развития аутоиммунных процессов обусловлена мимикрией структуры gp120 под структуру иммуноглобулинов (Atlan H. et al.,1993). В пользу наличия ау-тоиммунных процессов в патогенезе ВИЧ-инфекции говорят и клинические проявления болезни, в частности, часто сопутствующие болезни такие ти-пичные аутоаллергические варианты патологии, как спондилоартропатии, системные ревматоидные синдромы: волчаночноподобный синдром Шегре-на, полимиозит, некротизирующий васкулит.
У половины больных развиваются манифестные формы аллергии, пре-имущественно в виде ринита, лекарственной аллергии, крапивницы, атопиче-ского дерматита, ангионевротического отека с повышением у них уровня специфических IgE к бытовым, эпидермальным, пыльцевым и пищевым ал-лергенам с положительной коррелятивной связью между общим уровнем IgE и содержанием СD8+ лимфоцитов (Ю.А.Митин, 1997).
Наряду с поражением иммунной системы в патологический процесс вовлекается и кроветворная ткань. Для заболевания характерны лейкопения, анемия, тромбоцитопения. Угнетается функциональная активность грануло-цитов. У больных ВИЧ-инфекцией в костном мозге резко снижено содержа-ние колониеобразующих единиц гранулоцитов, макрофагов, мегакариоцитов. Однако дисфункция стволовых клеток не связана с их прямым инфицирова-нием, ибо не обнаружено присутствия ВИЧ в кроветворных клетках при изу-чении методом гибридизации in situ и иммуногистохимическим исследова-нием гемопоэтических колоний, а также с помощью полимеразной цепной реакции. Пока нет однозначного мнения о причинах ингибиции пролифера-тивной активности стволовых клеток, хотя и установлено, что различные изоляты ВИЧ, воздействуя на CD34+ клетки, угнетают их функциональную активность. Также установлено, что подавление кроветворения в результате действия ВИЧ связано с усилением продукции костномозговыми моноцита-ми/макрофагами фактора некроза опухолей.
Таким образом, поражение иммунной системы при ВИЧ-инфекции но-сит системный характер, проявляясь глубокой супрессией Т- и В-звеньев клеточного иммунитета. В ходе развития ВИЧ-инфекции происходят законо-мерные изменения гиперчувствительности немедленного и замедленного ти-па, гуморального иммунитета и факторов неспецифической защиты, функ-циональной активности лимфоцитов и моноцитов/макрофагов. Нарастает уровень сывороточных иммуноглобулинов, циркулирующих иммунных ком-плексов. Наряду с дефицитом CD4+ лимфоцитов в динамике болезни нарас-тает функциональная недостаточность СD8+ лимфоцитов, NK-клеток, ней-трофилов. Нарушение иммунного статуса клинически проявляется инфекци-онным, аллергическим, аутоиммунным и лимфопролиферативным синдро-мами иммунологической недостаточности, синдромом, свойственным болез-ни иммунных комплексов. Все это определяет в целом клинику ВИЧ-инфекции.
Патогенез вич-инфекциипоражений обусловливает селективное поражение СD4+-клеток, так как вирус использует молекулу CD4 в качестве рецептора.
Мишени для вич-инфекции — Т-хелперы, моноциты, макрофаги и родственные клетки, экспрессирующие СD4-подобные молекулы. Заражение макрофагов также возможно при поглощении иммунных комплексов, содержащих вирус.
Особенность патогенеза ВИЧ-инфекции — способность избегать действия иммунных механизмов за счёт интеграции его генома в ДНК клеток хозяина при минимальной экспрессии вирусных генов, а также антигенной изменчивости, обусловленной рабочими ошибками обратной транскриптазы.
Механизмы, обусловливающие прогрессирующее уменьшение количества СD4+-клеток при вич-инфекции, включают апоптоз, образование синцитиев, аутоиммунные реакции, инфицирование клеток-предшественников.
• Образование синцитиев. Экспрессия gp 120 на мембранах Т-клеток инициирует слияние мембран заражённых или незаражённых клеток, несущих молекулы CD4.
Образование синцитиев при вич-инфекции обусловливает прямую передачу вируса от клетки к клетке и вызывает гибель Т-хелперов. Образование синцитиев — показатель поздней стадии развития ВИЧ-инфекции; указывающий на быстрое развитие СПИДа (в среднем через 23 мес).
• Аутоиммунные реакции. Появление вирусных гликопротеинов на мембране заражённых Т-клеток запускает активацию ЦТЛ и реакции антителозависимой цитотоксичности, направленные против инфицированных СD4+-клеток.
• Инфицирование клеток-предшественников. ВИЧ инфицирует клетки-предшественники Т-лим-фоцитов в вилочковой железе и костном мозге, вызывая нарушения пролиферации и диффе-ренцировки пула СD4+-клеток.
Следствием уменьшения количества СD4+-клеток выступает глубокий вторичный иммунодефицит, проявляющийся резким снижением сопротивляемости организма оппортунистическим микроорганизмам и развитием опухолей (саркома Капоши, карциномы кожи или В-клеточной лимфомы).
Помимо иммунотропности, ВИЧ проявляет выраженную нейротропность. ВИЧ длительно сохраняется в макрофагах и с их помощью диссеминирует по всему организму, в том числе заносится в ЦНС.
Вирус вич-инфекции инфицирует астроциты, вызывает образование симпластов и последующую гибель клеток.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Инфекция вируса иммунодефицита человека (ВИЧ): диагностика, лечение, профилактика
Вирус иммунодефицита человека (ВИЧ) — сферический оболочечный РНК-ретровирус, образующий при помощи обратной транскриптазы ДНК-копию вирусной РНК. Последняя встраивается в ядро клетки хозяина и служит шаблоном для производства последующих вирусных РНК. Для репликации возбудителя необходимы три гена: gag, pol и env. ВИЧ определяют как лентивирус.
Патогенными для человека считают ВИЧ-1 (наиболее распространённый) и ВИЧ-2 (регистрируют в основном на территории Западной Африки), которому свойственна меньшая вирулентность.
Эпидемиология ВИЧ-инфекции. ВИЧ-инфекция распространена во всём мире. Передача вируса осуществляется парентеральным и половым путём. В группу риска входят пациенты, ведущие беспорядочную половую жизнь (особенно при наличии изъязвлений на слизистой оболочке половых органов). В развитых странах чаще всего жертвами ВИЧ становятся мужчины (гомосексуалисты и наркоманы).
Передачу вируса между гетеросексуальными партнёрами встречают реже. В развивающихся странах ВИЧ обычно распространяется при гетеросексуальных связях, переливании неисследованной заражённой крови и использовании инфицированного медицинского инструментария. Возможна передача инфекции от матери к плоду.
Патогенез инфекции вируса иммунодефицита человека. Сначала вирус поражает клетки, обладающие СD4-рецепторами (например, Т-лимфоциты, макрофаги). Затем следует репликация, приводящая к сокращению количества здоровых Т-лимфоцитов и снижению клеточного иммунитета. Различные штаммы вируса имеют разное сродство к клеткам с различными хемокиновыми рецепторами.
При снижении Т-клеточного иммунитета также уменьшается активность В-лимфоцитов. Кроме того, ВИЧ поражает нейроны, стимулирует выделение большого количества цитокинов, способствующих дальнейшему повреждению нервной системы. Большинство клинических признаков при ВИЧ-инфекции связано со вторичными инфекционными заболеваниями, возникающими вследствие снижения иммунитета (уменьшение СD4-клеток).
Клинические признаки инфекции вируса иммунодефицита человека. Через несколько недель после заражения возникает мононуклеозоподобный синдром, сопровождающийся появлением сыпи, лихорадки и лимфаденопатии. Затем следует латентный период, который может продолжаться 10—15 лет.
ВИЧ-инфекция
Диагностика инфекции вируса иммунодефицита человека. Диагноз ВИЧ-инфекции подтверждают двумя серологическими методами: ИФА и постановкой иммуноблоттинга (вестерн-блоттинга), направленных на определение специфических антител. РНК вируса определяют с помощью ПЦР.
При обследовании пациенты с подозрением на ВИЧ должны получать исчерпывающую консультацию врача. Поскольку сероконверсия может продолжаться в течение 3 мес, при первоначальном отрицательном результате необходимо провести повторный анализ.
Лечение необходимо сопровождать регулярным измерением вирусной нагрузки. Вирус может расти в лимфоцитах, но это не используют в диагностических целях.
Лечение инфекции вируса иммунодефицита человека
Для лечения ВИЧ-инфекции применяют:
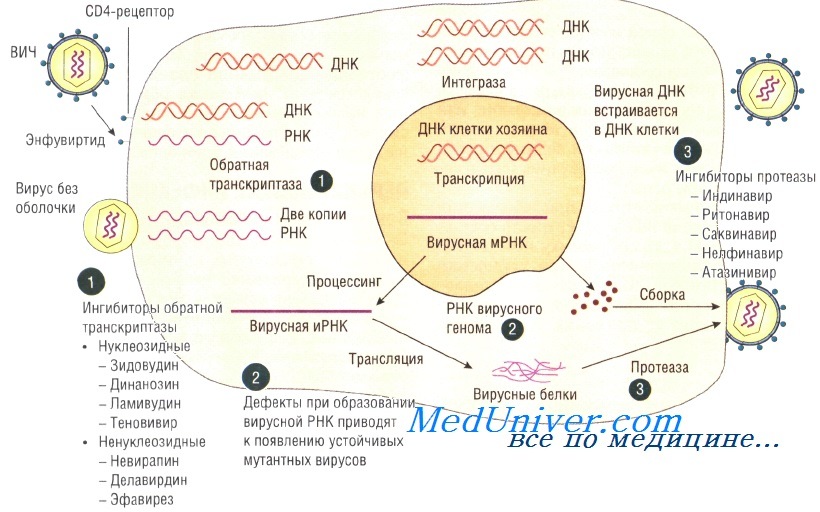
• нуклеозидные ингибиторы обратной транскриптазы (например, зидовудин);
• ненуклеозидные ингибиторы обратной транскриптазы (например, невирапин);
• ингибиторы протеаз (например, индинавир). Основные три направления лечения:
• торможение вирусной репликации;
• предупреждение появления устойчивых форм;
• повышение иммунитета пациента.
Терапию начинают проводить пациентам с выраженными симптомами, при развитии заболеваний, вызванных условно-патогенной микрофлорой, а также при снижении количества клеток с CD4-рецепторами ниже 0,2x10 9 /л. При показателях выше 0,2x10 9 /л и ниже 0,35x10 9 /л необходимо тщательно продумать тактику лечения (с учётом риска развития побочных эффектов и состояния пациента).
Существуют разнообразные режимы лечения ВИЧ-инфекции. На начальном этапе обычно применяют:
• ненуклеозидный ингибитор обратной транскриптазы + два препарата из группы нуклеозидных ингибиторов обратной транскриптазы;
• ингибитор протеазы + нуклеозидный ингибитор обратной транскриптазы.
При заражении устойчивыми штаммами слудует соблюдать осторожность и применять нестандартные методы, основанные на индивидуальном подходе. В связи с тем что РНК-вирусы не имеют достаточно эффективных генетических механизмов коррекции, мутации, приводящие к образованию устойчивых штаммов, происходят достаточно быстро.
В начале лечения происходит повышение иммунитета, поэтому в связи с усилением иммунного ответа симптомы сопутствующих заболеваний могут усилиться.
Профилактика ВИЧ-инфекции. Для профилактики заражения необходимо избегать половых контактов с лицами, входящими в группу риска, и незащищённых половых связей (без использования барьерной контрацепции). Кроме того, необходимо тщательно исследовать донорскую кровь и уничтожать её образцы, подозрительные на ВИЧ-инфекцию.
Снижению риска заражения среди наркоманов способствуют программы медицинского просвещения и пропаганда использования одноразовых шприцев и игл. К сожалению, разнообразие антигенов вируса делает невозможным создание эффективной вакцины. При случайных проколах кожи медицинскими иглами необходимо проходить профилактический курс антиретровирусной терапии. Риск передачи инфекции от матери к плоду можно снизить с помощью проведения эффективной антиретровирусной терапии, правильно выполненного кесарева сечения и отказа от кормления грудью.
При отсутствии возможности проведения высокоактивной антиретровирусной терапии (в развивающихся странах) лечение проводят коротким курсом для снижения риска передачи инфекции.
У пациентов с ВИЧ-инфекцией развиваются тяжёлые кандидозы кожи и слизистых оболочек, сопровождающиеся изъязвлением слизистой оболочки ротовой полости и поражением пищевода, что приводит к дисфагии и существенной потере массы тела. Для лечения острой инфекции назначают приём внутрь флуконазола, но при длительной терапии часто развивается устойчивость возбудителей. Кроме того, очень серьёзной проблемой считают криптококковый менингит.
Инфекция Toxoplasma gondii у ВИЧ инфицированных. Инфекция персистирует в организме на протяжении длительного времени. Снижение иммунитета приводит к активации возбудителя и развитию различных патологических процессов (объёмные образования головного мозга, сопровождающиеся энцефалитом и др.).
При энцефалите отмечают высокую температуру, головные боли, судороги, неврологические расстройства. Возможно развитие комы. При компьютерной томографии обнаруживают множественные фокальные очаги кольцевидной формы. Исследуемый материал — биоптат мозга. Методы диагностики — культивирование возбудителя, полимеразная цепная реакция. Для лечения энцефалита применяют пириметамин + сульфадиазин. После выздоровления необходимо проведение курса поддерживающей терапии.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Читайте также:

