Схема терапией вич ламивудин следит атазанавир
Обновлено: 17.04.2024
Федеральный научно-методический центр по профилактике и борьбе со СПИДом ФГУН Центрального НИИ эпидемиологии Роспотребнадзора, Москва Дальневосточный журнал инфекционной патологии, 2010.- № 17.- С.220-235.
Резюме
Данный обзор посвящен анализу международного опыта клинического применения атазанавира — современного антиретровирусного препарата из группы ингибиторов протеазы ВИЧ — в составе различных схем антиретровирусной терапии (АРВТ). Представлены данные клинических исследований об эффективности атазанавира у пациентов, ранее не получавших антиретровирусной терапии (АРВТ), и при неэффективности предшествующих схем терапии; рассмотрены различные аспекты безопасности и переносимости препарата; обсуждено потенциальное место атазанавира в современной практике ведения больных ВИЧ-инфекцией.
Ключевые слова: ВИЧ-инфекция, антиретровирусная терапия, атазанавир.
Введение
Краткая фармакологическая характеристика атазанавира
Атазанавир — антиретровирусный препарат, активный против ВИЧ-1, относящийся к группе ингибиторов протеазы (ИП) ВИЧ. Протеаза ВИЧ представляет собой фермент, осуществляющий протеолитическое расщепление полипротеиновых предшественников вируса на отдельные белки, входящие в состав ВИЧ. Подавление этого фермента нарушает образование белков вирусного капсида и созревание вируса, что приводит к формированию незрелых вирусных частиц, неспособных инфицировать другие клетки.
По антиретровирусной активности in vitro атазанавир превосходит другие ИП — ампренавир, индинавир, нелфинавир, ритонавир и саквинавир []. Следует отметить, что цитотоксические эффекты атазанавира in vitro отмечаются только при воздействии концентраций в 6500 — 23800 раз превышающих его терапевтический уровень [].
Исследования атазанавира в комбинации с другими противовирусными препаратами (нуклеозидными ингибиторами обратной транскриптазы ВИЧ — НИОТ, ненуклеозидными ингибиторами обратной транскриптазы ВИЧ — ННИОТ, другими ИП, ингибиторами слияния, а также препаратами для лечения вирусных гепатитов) не выявили ослабления его антиретровирусной активности и усиления токсичности в отношении клеток макроорганизма []. Для атазанавира также характерна низкая частота развития резистентности (около 2%), особый профиль резистентности (мутация I50L) и отсутствие в большинстве случаев перекрестной резистентности с другими ИП [].
Отличительными фармакокинетическими особенностями атазанавира являются высокая биодоступность и возможность однократного приема в сутки. Прием препарата вместе с легкой пищей улучшает биодоступность и уменьшает вариабельность концентраций атазанавира в сыворотке крови. В то же время значительное повышение рН желудочного содержимого, наблюдаемое при приеме Н2-блокаторов или ингибиторов протонной помпы (ИПП), приводит к ухудшению абсорбции препарата и к значительному снижению показателей площади под фармакокинетической кривой (ПФК) и равновесной концентрации атазанавира в сыворотке крови (на 75%) []. В связи с этим атазанавир не рекомендуют назначать пациентам, получающим омепразол или другие ИПП или Н2-блокаторы [].
Терапевтическая эффективность атазанавира у пациентов с ВИЧ-инфекцией
Результаты применения атазанавира у пациентов, ранее не получавших АРВТ
По данным исследования CASTLE эффективность терапии атазанавиром с ритонавиром не зависела от исходного уровня CD4+ лимфоцитов []. Частота вирусологического ответа при терапии атазанавиром с ритонавиром составила 78%, 76%, 75% и 80%, соответственно, в подгруппах пациентов с числом CD4+лимфоцитов 200 клеток/мм3. Однако в группе терапии лопинавиром/ритонавиром была отмечена меньшая частота вирусологического ответа при более низких значениях CD4+лимфоцитов: 63%, 69%, 78% и 80%, соответственно []. Кроме того, среди ВИЧ-инфицированных с исходными значениями CD4+ 100 000 копий/мл при лечении атазанавиром с ритонавиром снижения уровня РНК ВИЧ-1 0,05). При наличии >4 мутаций соответствующие показатели составили только 36% и 32%, соответственно [].
Исследования возможности перевода пациентов, получающих эффективный режим АРВТ, включающий другие ИП, на терапию атазанавиром
В исследовании ATAZIP у пациентов с высоким риском вирусологической неэффективности (документированная неэффективность предшествующей АРВТ с применением ИП или наличие >3 мутаций, вызывающих резистентность к ИП) частота вирусологической неэффективности в группе терапии атазанавиром с ритонавиром составила 11%, а в группе лечения лопинавиром/ритонавиром — 13% [].
В исследовании SWAN принимали участие только пациенты, не имевшие предшествующей неэффективности других режимов АРВТ, включавших ИП. Переключение пациентов с предыдущих режимов АРВТ на лечение атазанавиром (у >90% без ритонавира) обеспечило достоверное сокращение частоты вирусологической неэффективности (отношение рисков — ОР = 0,42; 95% ДИ от 0,22 до 0,79; p = 0,007) и увеличение времени до возникновения вирусологической неэффективности (ОР = 0,59; 95% ДИ от 0,40 до 0,87, p = 0,008) по сравнению с пациентами, продолжившими получать исходную схему терапии [].
Безопасность и переносимость атазанавира у больных ВИЧ-инфекцией
На сегодняшний день в арсенале врачей имеется более двух десятков антиретровирусных препаратов 6 различных классов, что позволяет назначать больным ВИЧ-инфекцией разнообразные схемы комбинированной АРВТ, обладающие высокой вирусологической и иммунологической эффективностью. В связи с этим первостепенной задачей становится выбор оптимального режима лечения для обеспечения не только эффективной, но и максимально безопасной и хорошо переносимой терапии для каждого конкретного пациента с учетом его состояния и сопутствующей патологии. В современных условиях целью АРВТ является не только продление жизни больного ВИЧ-инфекцией, но и в сохранение ее качества на высоком уровне в течение многих лет терапии. Следовательно, лечение должно сопровождаться наименьшим риском развития нежелательных явлений (НЯ), как ранних, так и отдаленных, и не должно или почти не должно влиять на качество жизни пациента.
По данным различных исследований в настоящее время при проведении АРВТ НЯ степени тяжести, требующие обязательного изменения терапевтической тактики, регистрируют значительно чаще (11,4%), чем развитие СПИД-индикаторых заболеваний (5,6%) []. НЯ являются также основной причиной (58%) прерывания АРВТ, значительно опережая по частоте вирусологическую неэффективность терапии (14,1%) [].
Общая характеристика профиля НЯ атазанавира
19. Johnson M, Grinsztejn B, Rodriguez C, et al. Atazanavir plus ritonavir or saquinavir, and lopinavir/ritonavir in patients experiencing multiple virological failures. AIDS 2005; 19 (7):
20. Johnson M, Grinsztejn B, Rodriguez C, et al. comparison of once-daily atazanavir/ritonavir and twice-daily lopinavir/ritonavir in patients with multiple virologic failures. AIDS 2006 Mar 21; 20 (5):
21. Naeger LK, Struble KA. Effect of baseline protease genotype and phenotype on HIV response to atazanavir/ritonavir in treatment-experienced patients. AIDS 2006; 20:
22. Gatell J, Salmon-Ceron D, Lazzarin A, et al. Efficacy andsafety of atazanavir-based highly active antiretroviral therapy in patients with virologic suppression switched from a stable, boosted or unboosted protease inhibitor treatment regimen: the SWAN study (AI424-097) results. Clin Infect Dis 2007; 44 (11):
23. Soriano V, Garcia-Gasco P, Vispo E, et al. Efficacy and safety of replacing lopinavir with atazanavir in HIV-1-infected patients with undetectable plasma viraemia: final results of the SLOAT trial. J Antimicrob Chemother 2008; 61 (1):
24. Mallolas J, Podzamczer D, Milinkovic A, et al. Efficacy and safety of switching from boosted lopinavir to boosted atazanavir in patients with virological suppression receiving a LPV/r-containing HAART: the ATAZIP study. J Aquir Immune Defic Syndr 2009; 51 (1):
25. Reisler RB, Han C, Burman WJ, et al. Grade 4 events are as important as AIDS events in the era of HAART. J Acquir Immune Defic Syndr. 2003; 34 (4):
26. Monforte A, Lepri AC, Rezza G, et al. Insights into the reasons for discontinuation of the first highly active antiretroviral therapy (HAART) regimen in a cohort of antiretroviral naïve patients. I.CO.N.A. Study Group. Italian Cohort of Antiretroviral-Naïve Patients. AIDS. 2000; 14 (5):
28. Pineda JA, Santos J, Rivero A, et al. Liver toxicity of antiretroviral combinations including atazanavir/ritonavir in patients co-infected with HIV-1 and hepatitis viruses: impact of pre-existing liver fibrosis. J Antimicrob Chemother 2008; 61 (4):
29. Witek J, McCAllister S, Odeshoo L, et al. Safety of atazaniavir (ATV) and atazanavir/ ritonavir (ATV/r) in subjects co-infected with HIV-1 and hepatitis B and/or C: 1100 subject-years of treatment exposure [abstract no. WEPE0054]. 16th International AIDS Conference; 2006 Aug Toronto (ON), 48.
30. Absalon J, Thal G, Thiry A, et al. Atazanavir is safe and efficacious in HBV and HCV coinfected patients: results of A1424138 (CASTLE) [abstract no. P136]. J Int AIDS Soc 2008; 11 Suppl. 1:P136.
31. Busti AJ, Tsikouris JP, Peeters MJ, et al. A prospective evaluation of the effect of atazanavir on the QTc interval and QTc dispersion in HIV-1-positive patients. HIV-1 Med. 2006; 7 (5):
32. Bergersen BM. Cardiovascular risk in patients with HIV-1 infection: impact of antiretroviral therapy. Drugs 2006; 66 (15):
33. Jemsek JG, Arathoon E, Arlotti M, et al. Body fat and other metabolic effects of atazanavir and efavirenz, each administered in combination with zidovudine plus lamivudine, in antiretroviral-naive HIV-1-infected patients. Clin Infect Dis. 2006; 42 (2):
34. Sension M, Neto JL, Grinsztejn B, et al. Improvement in lipid profiles in antiretroviral-experienced HIV-positive patients with hyperlipidemia after a switch to unboosted atazanavir. J Acquir Immune Defic Syndr. 2009; 51 (2):
35. Keiser P, McGrath S, Reynolds L, et al. Changes in lipid profiles in treatment-experienced patients switched to atazanavir-based antiretroviral therapy: results from the atazanavir expanded access program [abstract no. WEPE0163]. 16th International AIDS Conference; 2006 Aug Toronto (ON).
36. Colafigli M, Giambenedetto SD, Bracciale L, Tamburrini E. et al. Cardiovascular risk score change in HIV-1-infected patients switched to an atazanavir-based combination antiretroviral regimen. HIV Med 2008; 9:
37. McComsey G, Rightmire A, Wirtz V, et al. Changes in body composition with ritonavir-boosted and unboosted atazanavir treatment in combination with lamivudine and stavudine: a randomized, controlled study. Clin Infect Dis 2009; 48 (9):
38. Moyle G, Girard JM, Andrade J, et al. Continuation of BID boosted PI vs switch to once-daily ATV/RTV for the management of lipodystrophy: 48 week primary analysis of the 96 week multicenter, open-label, randomized, prospective ReAL study [abstract no. MOPDB103]. 17th International AIDS Conference; 2008 Aug Mexico City.
39. Jones CY. Insulin resistance in HIV-infected men and women in the nutrition for healthy living cohort. J Acquir Immune Defic Syndr 2005; 40 (2):
40. Brown TT. Antiretroviral therapy and the prevalence an incidence of diabetes mellitus in the multicenter AIDS cohort study. Arch Intern Med 2005; 165 (10):
41. Wang SMR, Elosua C. Association of HIV-protease inhibitors with insulin resistance is related to potency of inhibition of GLUT4 and GLUT1 activity in adipocytes and myocytes. Antivir Ther 2003; 8: L36.
42. Noor MA, Flint OP, Maa JF, Parker RA. Effects of atazanavir/ritonavir and lopinavir/ ritonavir on glucose uptake and insulin sensitivity: demonstrable differences in vitro and clinically. AIDS. 2006; 20 (14):
43. Noor MA, Parker RA, O’Mara E, et al. The effects of HIV-1 protease inhibitors atazanavir and lopinavir/ritonavir on insulin sensitivity in HIV-1-seronegative healthy adults. AIDS 2004; 18:
44. Jackson A, Patel N, Lo G, et al. Effects of atazanavir or saquinavir once daily with ritonavir 100mg and tenofovir/emtricitabine as initial therapy for HIV-1-1 infection on peripheral glucose disposal: a randomized open-label study [abstract no. 818]. 14th Conference on Retroviruses and Opportunistic Infections; 2007 Feb Los Angeles (CA).
45. Guffanti M, Caumo A, Galli L, et al. Switching to unboosted atazanavir improves glucose tolerance in highly pretreated HIV-1-1 infected subjects. Eur J Endocrinol 2007; 156 (4):
46. Hammer SM, Eron Jr J, Reiss P, et al. Antiretroviral treatment of adult HIV-1 infection: 2008 recommendations of the International AIDS Society-USA panel. JAMA 2008; 300 (5):
48. Clinical management and treatment of HIV-infected adults in Europe , EACS Guidelines, Version 5, November, 2009 (. org).
49. Samaras K. Metabolic consequences and therapeutic options in highly active antiretroviral therapy in human immunodeficiency virus-1 infection. J Antimicrob Chemother 2008; 61:
50. Friis-Moller N, Sabin CA, Weber R, et al. Combination antiretroviral therapy and the risk of myocardial infarction. N Engl J Med 2003; 349 (21):
На сервисе СпросиВрача доступна консультация инфекциониста по любой волнующей Вас проблеме. Врачи-эксперты оказывают консультации круглосуточно и бесплатно. Задайте свой вопрос и получите ответ сразу же!

Здравствуйте, Виктор. Эффективность ВААРТ оценивают по вирусной нагрузке и количеству CD4. Вы давно проверяли эти параметры? А липодистрофия, а также дистрофия мышц и, как следствие, снижение веса может быть проявлением основного заболевания.
Ирина, ВН- не определяется , CD 4 -500, назначен в начале зивовудин +ламавудин +калетра , два месяца назад сменили схему : -ритонавир +Саквинавир +Ламивудин +Тонофовир . но стало на мой взгляд даже хуже , вес уходит , ноги усыхают , лицо начисто теряет влагу

Значит, заболевание у вас компенсировано.А из новой схемы ритонавир и тенофовир вызывают побочные эффекты как у вас. Не совсем понятно, почему поменяли схему при таких хороших результатах, может быть, дело в организационных моментах. Перестаньте принимать пока эти два препарата, и в ближайшее время обратитесь к своему инфекционисту для пересмотра схемы.
Ирина, понимаете , что терапия бесплатна .поэтому не всё могут леч.врачи говорить , навязывая тот или иной препарат , какую альтернативу Ритонавиру и Тенофавиру вы могли бы предложить . может это могут быть препараты . которые частично я смог бы покупать сам ?Может есть какие-то альтернативные методики лечения моего заболевания , может есть какие-то инновации по данной теме

Виктор, добрый день. Прежде всего скажу следующее, прошу отнестись с пониманием. Интернет площадка - не место для решения таких серьезных вопросов. Ни один врач, не зная течения Вашей болезни , динамики, сопутствующей патологии, не может решить вопрос о смене схемы лечения. Да, существуют, комбинированные средства, но их назначение только очно. Именно с лечащим врачом и нужно обсуждать эти вопросы. Да, из-за нехватки времени, разъяснят немного, но Вы задавайте вопросы, врачу деваться некуда будет, придется отвечать. 1) ни в коем соучае не отменять самостоятельно лечение, тем более убирать два из четырех препаратов. Думаю, Вы знаете про резистентность. Именно такие эксперименты поиведут в будущем к тому, что лечить Вас будет нечем. 2) ритонавир входит в состав калетры, которую Вы пьете уже 6 лет, почему вдруг его отменять сейчас? Тенофовир к липодистрофии не приводит, его пьют много моих рациентов, все хорошо. 3) менять препараты в схеме может толтко обученный врач-спидолог, не экспериментируйте. 4) достижение фащы ремиссии Вашей болезни еще раз доказывает, что лечитесь Вы правильно. 5) после смены схемы терапии через 4 недели требуется забор вирусной нагрузки, чтобы понять, что схема работает. 6) каковы Ваши сопутствуюшие заболевания? ХВГВ? Фиброз? Вощможно, есть и другая причина липолистрофии?

Здравствуйте. Вам необходимо решать данный вопрос с вашим лечащим врачом который точно знает как у вас протекает данное заболевание и знает клинику.

Препарат который вызвал липодистрофию у вас заменён. Тенофавир не дате таких эффектов. Восстановление нормального отложения жира возможна. Как показывает практика,в частности собственная , это происходит и год и два. Так что выводы делать рано и не в коем случае не прекращать арвт.

В новой версии дополнены разделы об антиретровирусной терапии и общей информации по лечению. Впервые включена рекомендация по перебоям и добавлены два раздела: по профилактике ВИЧ-инфекции и лечению сопутствующих заболеваний.
Клинические рекомендации для взрослых
Добавлены критерии мониторинга состояния костной ткани и побочных эффектов лечения. Впервые упомянуты критерии проведения теста на резистентность до начала лечения, обновлён перечень препаратов, ограниченных в использовании при определённых условиях. В частности, не рекомендуется долутегравир для беременных женщин на 1-м триместре и из-за неэффективности и риска развития резистентности также не рекомендуется комбинация абакавир/ламивудин/зидовудин.
Антиретровирусная терапия
Предпочтительные схемы АРТ первого ряда для взрослых расширили до трех вариантов:
- эфавиренз + ламивудин (или эмтрицитабин) + тенофовир.
- долутегравир + ламивудин (или эмтрицитабин) + тенофовир.
- элсульфавирин + ламивудин (или эмтрицитабин) + тенофовир.
В качестве альтернативных схем первого ряда указаны две схемы:
- долутегравир + ламивудин + абакавир.
- эфавиренз 400 мг + ламивудин + тенофовир.
Долутегравир указан, как один из вариантов АРТ первого ряда, что соответствует мировым тенденциям. Но присутствие элсульфавирина в числе схем АРТ первого ряда вызывает беспокойство, поскольку препарат недостаточно исследован по ряду показателей.
В перечень упрощённых режимов добавлен долутегравир + ламивудин. Исключены и не рекомендованы к использованию: невирапин и диданозин. Последний из-за высокой токсичности.
Среди АРВ-препаратов для особых случаев впервые указан современный препарат доравирин и комбинированные препараты: элвитегравир/кобицистат/эмтрицитабин/тенофовира алафенамид фумарат; биктегравир/ эмтрицитабин/тенофовира алафенамид фумарат. доравирин/ламивудин/тенофовир.
Впервые включена рекомендация по бесперебойному обеспечению лекарствами, в которой подчёркивается важность включения расходов на лекарства в региональные бюджеты.
Клинические рекомендации для детей
Рекомендовано назначение АРТ для детей с подтверждённой ВИЧ-инфекцией, независимо от возраста, клинических проявлений и показателей CD4. Детям от 6 недель до 1 года рекомендовано назначение АРТ в течение 2-х недель после постановки на диспансерный учёт.
Предпочтительные схемы стартовой АРТ по возрасту:
- От 0 до 2 недель – невирапин, зидовудин, ламивудин.
- От 2 недель до лет – лопинавир/ритонавир, абакавир, ламивудин.
- От 2 до 3 лет – лопинавир/ритонавир, ралтегравир, абакавир, ламивудин.
- От 3 до 6 лет – лопинавир/ритонавир, ралтегравир, абакавир, ламивудин.
- От 6 до 12 лет – атазанавир+ритонавир, ралтегравир, абакавир, ламивудин.
- От 12 лет – долутегравир, атазанавир+ритонавир, тенофовир + ламивудин (или эмтрицитабин), абакавир + ламивудин.
Альтернативные варианты АРТ:
- От 0 до 2 недель – диданозин + ламивудин (в особых случаях).
- От 2 недель до 2 лет – невирапин, зидовудин (или фосфазид) + ламивудин.
- От 2 до 3 лет – невирапин, зидовудин (или фосфазид) + ламивудин.
- От 3 до 6 лет – эфавиренз, фосампренавир + ритонавир, зидовудин (или фосфазид) + ламивудин.
- От 6 до 12 лет – эфавиренз, дарунавир + ритонавир, фосампренавир + ритонавир, лопинавир/ритонавир, этравирин (в особых случаях), зидовудин (или фосфазид) + ламивудин; элвитегравир/кобицистат/эмтрицитабин/тенофовира алафенамид фумарат.
- От 12 лет – эфавиренз, дарунавир + ритонавир, ралтегравир, фосампренавир + ритонавир, лопинавир/ритонавир, этравирин (в особых случаях), зидовудин + ламивудин; рилпивирин/тенофовир/эмтрицитабин; элвитегравир/кобицистат/эмтрицитабин/тенофовира алафенамид фумарат.
Впервые для детей от 12 лет рекомендован долутегравир, а эфавиренз исключён из предпочтительных вариантов для всех возрастов. Невирапин рекомендован только для детей младше 2 недель, а среди альтернативных вариантов АРТ впервые появились комбинации: рилпивирин/тенофовир/эмтрицитабин (от 12 лет) и элвитегравир/кобицистат/эмтрицитабин/тенофовира алафенамид фумарат (от 6 лет и старше).
В середине 1980-х ученые идентифицировали вирус иммунодефицита человека и сразу же стали искать лекарство. История антиретровирусной терапии началась в 1987 году, когда для лечения ВИЧ-инфекции стали использовать препарат зидовудин. Но его эффективность была невысокой, а побочные эффекты слишком сильными. Первая высокоэффективная терапия появилась только через десять лет — в 1996 году. Эта комбинация из нескольких лекарств блокирует размножение попавшего в организм вируса сразу на нескольких этапах его цикла. С тех пор ВИЧ-инфекция — не смертельное, а хроническое заболевание, которое можно контролировать при должном лечении.
Антиретровирусные препараты (АРВ) подавляют размножение ВИЧ, но неспособны полностью удалить вирус из организма, именно поэтому их нужно принимать постоянно в течение всей жизни. Как только концентрация препарата в крови падает ниже порогового значения, вирус снова начинает размножаться. Это особенно опасно, ведь если вирус размножается в присутствии небольшого количества лекарства, то он вырабатывает устойчивость к этому препарату.
Пить таблетки на протяжении всей жизни с точностью до минут — не самая простая задача. Этому мешают и банальная забывчивость, и разные случайные обстоятельства. А чем чаще человек нарушает время приема терапии, тем выше риск развития у вируса устойчивости. Именно поэтому врачи стараются назначать схемы с приемом лекарств один раз в день и с минимальным числом таблеток — чем реже и меньше нужно принимать лекарств, тем проще соблюдать режим. Правильное соблюдение режима приема терапии называют высокой приверженностью лечению.
Сейчас лучшими схемами считаются те, при которых пациенту нужно принимать одну таблетку один раз в день, да еще и независимо от приема пищи. Но настоящим прорывом в АРВТ станет разработка схем, при которых лекарство достаточно будет принимать всего один или несколько раз в месяц, — пролонгированных схем терапии. Хотя в настоящее время неизвестно, как поведут себя пролонгированные режимы в рутинной практике. Будет ли к ним сохраняться высокая приверженность — как это показывают исследования?
по теме

Общество
Грудное молоко VS смеси при ВИЧ: что говорят эксперты в 2020 году?
Основной недостаток таких таблеток — срок их действия ограничено временем нахождения таблетки в кишечнике и не превышает 12—24 часов. В случае же диареи таблетка может покинуть организм гораздо быстрее, а значит, уменьшится концентрация лекарства в крови, что может быть опасно. Для антиретровирусных препаратов создание таблеток или капсул с замедленным высвобождением лекарственного вещества не очень перспективно — современные схемы уже позволяют принимать терапию один раз в день. То есть удобство применения терапии такие таблетки не повысят.
Если нужно добиться продления эффекта препарата на дни и недели, а лекарство всасываться через кожу упорно не хочет, приходится прибегать к парентеральным пролонгированным формам. Можно зашить под кожу специальную стерильную таблетку, которая будет медленно растворяться и выделять лекарственное вещество: на коже делается небольшой разрез, в него вводят таблетку и зашивают рану.
Помимо таблеток, под кожу можно вводить специальные полимерные импланты, содержащие нужное лекарство. Преимущество имплантов — они могут выделять лекарственное вещество очень долго, до нескольких лет. Чаще всего такие импланты используют для гормональной контрацепции. Так как гормоны действуют в очень маленьких дозах, даже в небольшой по размерам имплант можно сразу поместить запас препарата на несколько лет. Например, противозачаточный препарат Имплантон, который вводится под кожу, продолжает действовать три года. Если действие препарата нужно прекратить — достаточно просто извлечь имплант.
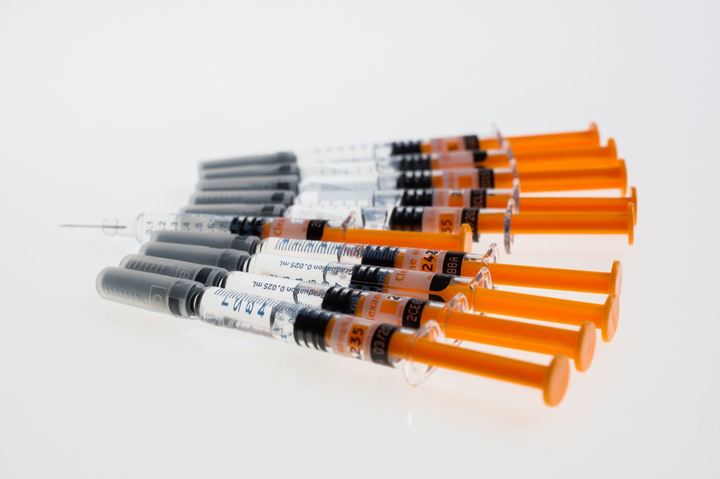
Более простой вариант — ввести в мышцу взвесь маленьких крупинок лекарства в подходящем растворителе. Выглядит это как обычный укол, при этом крупинки лекарства задерживаются в мышце, медленно растворяются и попадают в кровь. Такие способы введения лекарства особенно удобны в случаях, когда пациент может часто пропускать прием препарата, или забывать, принял ли он лекарство. Например, в случае лечения психических заболеваний. Но есть и недостатки: вводить такой препарат должен медицинский работник, а в случае непереносимости или выраженных побочных эффектов лекарство очень трудно быстро удалить из организма.
Что уже доступно на рынке?
Многие фармацевтические компании проводят исследования пролонгированных АРВ-препаратов, но разработка одного такого препарата сама по себе очень большой пользы не принесет — ведь для лечения ВИЧ-инфекции необходимо сочетание нескольких препаратов, то есть нужна комбинированная пролонгированная схема.
Такую схему, разработанную ViiV Healthcare совместно с Janssen, одобрили в марте 2020 года в Канаде — первый пролонгированный комбинированный АРВ-препарат Cabenuva. Схема показала высокую эффективность и безопасность в клинических исследованиях LATTE-2, FLAIR, ATLAS с участием более тысячи пациентов. В состав Cabenuva входят каботегравир и рилпивирин, то есть это двухкомпонентная схема. Препарат вводят один раз в месяц внутримышечно.
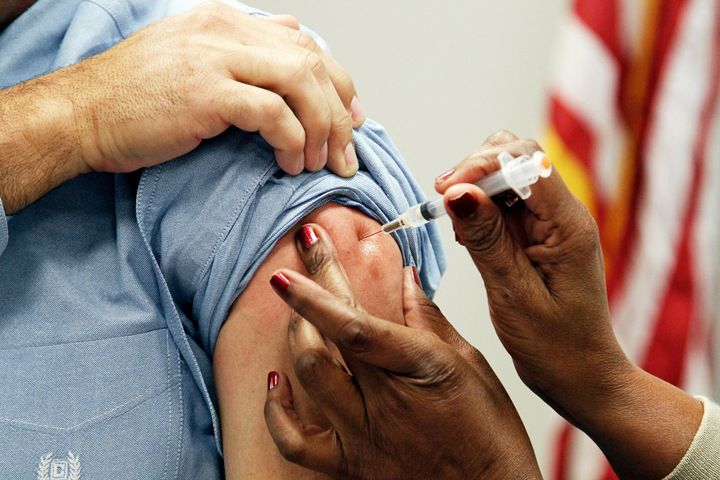
Перед началом применения Cabenuva пациент не менее месяца принимает каботегравир в таблетках (называется Vocabria) в комбинации с Эдюрантом — таблетками рилпивирина. Это необходимо, чтобы проверить переносимость такой схемы у конкретного пациента и оценить побочные эффекты. Если схема переносится хорошо, пациенту вводят первую нагрузочную дозу Cabenuva — 3 миллилитра суспензии, содержащей 600 миллиграммов каботегравира, и 3 миллилитра суспензии, содержащей 900 миллиграммов рилпивирина. Суспензии вводятся в разные участки ягодичной мышцы, то есть делают два укола. После этого поддерживающие дозы вводят ежемесячно: 2 мл (400 мг) каботегравира и 2 мл (600 мг) рилпивирина. Если по каким-то причинам введение очередной ежемесячной поддерживающей дозы невозможно, пациент до момента следующей инъекции может принимать пероральную схему (Vocabria + Эдюрант). Пролонгированная форма каботегравира также имеет большие перспективы для использования в качестве доконтактной профилактики ВИЧ-инфекции.
Еще один препарат, который уже применяется в клинической практике, — ибализумаб (Трогарзо) — можно назвать пролонгированным с несколькими оговорками. По химической природе ибализумаб — моноклональное антитело, то есть близок к человеческим иммуноглобулинам. Ибализумаб связывается с некоторыми белками на поверхности вируса и мешает проникновению ВИЧ в клетки. Препарат вводят внутривенно один раз в две недели и часто сочетают с другими АРВ-препаратами. Такая схема — не самый удобный вариант, поэтому сейчас ибализумаб используется только для лечения ВИЧ с множественной лекарственной устойчивостью, когда другие схемы оказываются неэффективными. Поэтому ибализумаб правильнее будет отнести к нишевым препаратам.
К сожалению, на этом и заканчивается не очень длинный перечень пролонгированных АРВ-препаратов, которые уже применяются на практике. Дальше пойдет речь о препаратах, находящихся на разных стадиях исследований.
Что сейчас находится в разработке?
PRO 140
С точки зрения места в клинической практике на ибализумаб похоже еще одно моноклональное антитело, находящееся в стадии клинических исследований, — PRO 140. Этот препарат также можно будет использовать для лечения ВИЧ-инфекции, если у пациента не работают другие схемы. А по механизму действия PRO 140 похож на уже существующий на рынке препарат маравирок (Целзентри). Он связывается с CCR-5 рецепторами на поверхности клеток-мишеней и мешает проникновению вируса в клетку. Строение активного центра молекулы PRO 140 отличается от маравирока, поэтому он активен даже в тех случаях, когда вирус выработал устойчивость к маравироку. Как и маравирок, PRO 140 активен только против CCR-5-тропных подтипов ВИЧ, то есть подойдет не всем пациентам. Препарат вводят внутривенно, один раз в неделю.
Нейтрализующие антитела
На разных стадиях клинических исследований находятся несколько перспективных антител, которые связываются с вирусным белком gp120 и нейтрализуют вирус: VRC01, 3BNC117 и 10-1074. Предполагается, что эти препараты достаточно будет вводить раз в месяц или даже реже и их можно будет применять совместно с другими пролонгированными АРВ-препаратами.
Албувиртид
Аналог уже применяющегося на практике энфувиртида (Фузеон). Этот препарат связывается с вирусным белком gp-41 и мешает проникновению вируса в клетку. Основное отличие в том, что Фузеон вводят подкожно два раза в сутки, что очень неудобно, а албувиртид — только один раз в 2—4 недели. Препарат должен применяться совместно с другими АРВ-лекарствами.
Читайте также:

