Симптомы при отравлении бромадиолоном
Обновлено: 15.04.2024
Ароматические углеводороды (толуол, бензол, ксилол, нафтолы, нафталин, фенолы) обычно представляют собой бесцветные жидкости, получаемые из каменноугольной смолы. Их используют в качестве органических растворителей при производстве резины, пластического цемента, обесцвечивающих веществ и т.д. Отравление может произойти при ингаляции или заглатывании.
Этиопатогенез • Ароматические углеводороды обладают нейротоксическим (наркотическим), гемотоксическим (гемолитическим), гепатотоксическим, нефротоксическим (в основном за счёт гемолиза) действиями • Кроме того, нафталин и особенно фенолы обладают местным прижигающим действием.
Клиническая картина • Бензол (толуол, ксилол): головокружение, эйфория, головная боль, возбуждение, бледность лица, покраснение слизистых оболочек, расширение зрачков, одышка с нарушением ритма дыхания тахикардия, аритмия, снижение АД •• При приёме внутрь — жжение во рту, за грудиной, боли в животе, тошнота, рвота •• В тяжёлых случаях — кома, судороги, параличи, возможны кровотечения (из носа, дёсен), кровоизлияния в кожу, увеличение печени с желтухой (токсическая гепатопатия) •• При хроническом отравлении — токсическая гепатопатия, лейкоз, апластическая анемия • Нафталин (антимоль, дезодорирующие вещества, репелленты): головная боль, спутанность сознания, сопор, возможны судороги, рвота, одышка •• При приёме внутрь — спастические боли в животе, тошнота, рвота, диарея •• При попадании на кожу или в глаза — дерматит, язвы на роговице •• При тяжёлых острых или хронических отравлениях — метгемоглобинемия с цианозом, гемолитическая анемия, нефропатия, гепатопатия • Фенолы (карболовая кислота, крезол, лизол, резорцин, гваякол): головная боль, головокружение, слабость, тошнота, бледные кожные покровы, профузный пот, гипотермия, сужение зрачков; бурая, быстро темнеющая на воздухе моча •• При приёме внутрь — характерный запах (напоминает запах фиалок) изо рта; жжение и боли в полости рта и глотки, по ходу пищевода и в желудке; ожог слизистых оболочек (белые пятна), рвота бурыми массами •• При ингаляции — раздражение слизистых оболочек верхних дыхательных путей и конъюнктивы •• При попадании на кожу — химический ожог вплоть до некроза •• В тяжёлых случаях — кома, судороги (особенно часто у детей), коллапс, ритм дыхания неправильный; при отравлении лизолом — гемолиз, гемоглобинурийный нефроз с развитием ОПН.
ЛЕЧЕНИЕ
Тактика ведения • При попадании внутрь — промывание желудка через зонд с последующим введением сорбента (активированный уголь) • При попадании на кожу и глаза — промывание проточной водой • Обеспечение адекватной вентиляции лёгких, оксигенотерапия, в тяжёлых случаях — ИВЛ • Инфузионная терапия, форсированный диурез • При гемолизе — переливание крови, ощелачивание мочи (4% р-р натрия гидрокарбоната парентерально) • Симптоматическая терапия: анальгетики, противосудорожные средства, витамины (тиамин, пиридоксин, цианокобаламин, аскорбиновая кислота, при кровотечении — менадиона натрия бисульфит), лечение печёночной и почечной недостаточности.
Специфическая (антидотная) терапия • При отравлении бензолом и фенолами — натрия тиосульфат (до 200 мл 30% р-ра) в/в • При отравлении нафталином — кальция хлорид (10 мл 10% р-ра); при метгемоглобинемии — см. Отравление метгемоглобинобразователями • При попадание фенолов на кожу и слизистые оболочки — лечение токсического ожогового шока (см. Отравление веществами прижигающего действия).
Противопоказания • При отравлении бензолом — введение эпинефрина • При отравлении фенолами — употребление (или введение) этанола, применение вазелинового масла в качестве сорбента.
МКБ-10 • T53 Токсическое действие галогенпроизводных алифатических и ароматических углеводородов
Код вставки на сайт
Ароматические углеводороды (толуол, бензол, ксилол, нафтолы, нафталин, фенолы) обычно представляют собой бесцветные жидкости, получаемые из каменноугольной смолы. Их используют в качестве органических растворителей при производстве резины, пластического цемента, обесцвечивающих веществ и т.д. Отравление может произойти при ингаляции или заглатывании.
Этиопатогенез • Ароматические углеводороды обладают нейротоксическим (наркотическим), гемотоксическим (гемолитическим), гепатотоксическим, нефротоксическим (в основном за счёт гемолиза) действиями • Кроме того, нафталин и особенно фенолы обладают местным прижигающим действием.
Клиническая картина • Бензол (толуол, ксилол): головокружение, эйфория, головная боль, возбуждение, бледность лица, покраснение слизистых оболочек, расширение зрачков, одышка с нарушением ритма дыхания тахикардия, аритмия, снижение АД •• При приёме внутрь — жжение во рту, за грудиной, боли в животе, тошнота, рвота •• В тяжёлых случаях — кома, судороги, параличи, возможны кровотечения (из носа, дёсен), кровоизлияния в кожу, увеличение печени с желтухой (токсическая гепатопатия) •• При хроническом отравлении — токсическая гепатопатия, лейкоз, апластическая анемия • Нафталин (антимоль, дезодорирующие вещества, репелленты): головная боль, спутанность сознания, сопор, возможны судороги, рвота, одышка •• При приёме внутрь — спастические боли в животе, тошнота, рвота, диарея •• При попадании на кожу или в глаза — дерматит, язвы на роговице •• При тяжёлых острых или хронических отравлениях — метгемоглобинемия с цианозом, гемолитическая анемия, нефропатия, гепатопатия • Фенолы (карболовая кислота, крезол, лизол, резорцин, гваякол): головная боль, головокружение, слабость, тошнота, бледные кожные покровы, профузный пот, гипотермия, сужение зрачков; бурая, быстро темнеющая на воздухе моча •• При приёме внутрь — характерный запах (напоминает запах фиалок) изо рта; жжение и боли в полости рта и глотки, по ходу пищевода и в желудке; ожог слизистых оболочек (белые пятна), рвота бурыми массами •• При ингаляции — раздражение слизистых оболочек верхних дыхательных путей и конъюнктивы •• При попадании на кожу — химический ожог вплоть до некроза •• В тяжёлых случаях — кома, судороги (особенно часто у детей), коллапс, ритм дыхания неправильный; при отравлении лизолом — гемолиз, гемоглобинурийный нефроз с развитием ОПН.
ЛЕЧЕНИЕ
Тактика ведения • При попадании внутрь — промывание желудка через зонд с последующим введением сорбента (активированный уголь) • При попадании на кожу и глаза — промывание проточной водой • Обеспечение адекватной вентиляции лёгких, оксигенотерапия, в тяжёлых случаях — ИВЛ • Инфузионная терапия, форсированный диурез • При гемолизе — переливание крови, ощелачивание мочи (4% р-р натрия гидрокарбоната парентерально) • Симптоматическая терапия: анальгетики, противосудорожные средства, витамины (тиамин, пиридоксин, цианокобаламин, аскорбиновая кислота, при кровотечении — менадиона натрия бисульфит), лечение печёночной и почечной недостаточности.
Специфическая (антидотная) терапия • При отравлении бензолом и фенолами — натрия тиосульфат (до 200 мл 30% р-ра) в/в • При отравлении нафталином — кальция хлорид (10 мл 10% р-ра); при метгемоглобинемии — см. Отравление метгемоглобинобразователями • При попадание фенолов на кожу и слизистые оболочки — лечение токсического ожогового шока (см. Отравление веществами прижигающего действия).
Противопоказания • При отравлении бензолом — введение эпинефрина • При отравлении фенолами — употребление (или введение) этанола, применение вазелинового масла в качестве сорбента.
МКБ-10 • T53 Токсическое действие галогенпроизводных алифатических и ароматических углеводородов
Отравление бета-адреноблокаторами и их побочные эффекты
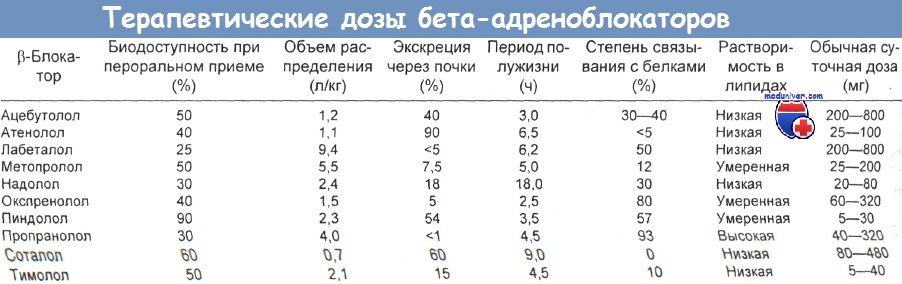
В таблице ниже приводятся фармакокинетические характеристики и обычные терапевтические дозы ряда b-блокаторов.
а) Клиническая картина. Острое отравление бета-блокаторами характеризуется подавлением проводимости и сократимости сердца, угнетением дыхания, комой, припадками и у некоторых пациентов — гипогликемией. Симптомы появляются в течение первых 1—2 ч после приема препаратов.
Лечебные мероприятия включают обеспечение вспомогательной искусственной вентиляции легких, лечение гипогликемии, применение конкурентных агонистов b-адренорецепторов, вазопрессоров и глюкагона, а также электрокардиостимуляции. Необходимо помнить, что применение бета-блокаторов сопряжено с большим риском возникновения анафилактических реакций.
Инфузия рентгеноконтрастного вещества — наиболее распространенная причина анафилактоидных реакций (не IgE-опосредованная анафилаксия). Внутривенное вливание традиционных контрастных веществ может стимулировать системное выделение гистамина, субклинический бронхоспазм и десатурацию кислорода. На этом фоне применение бета-блокаторов сопряжено с большим риском возникновения анафилактоидных реакций — от умеренных до тяжелых.
- Алпренолол. Проглатывание 12,8 г препарата с целью суицида в одном случае привело к смерти.
- Атенолол. Прием доз 1 г и 1,2 г взрослыми пациентами вызвал незначительный клинический эффект, за исключением не сильной брадикардии и гипотензии. Проглатывание взрослым пациентом 4—6,5 г препарата привело к асистолии желудочков; благотворное действие на состояние больного оказали массаж сердца и временный водитель ритма.
Проглатывание пациентом в возрасте 61 года 3 г атенолола привело к коллапсу и к такому сильному падению кровяного давления, что его нельзя было измерить. Электрокардиограмма выявила узловой ритм — 20 ударов в минуту. После применения глюкагона, атропина и дофамина, активированного угля после промывания желудка, изопротеренола и внутривенного введения кристаллоидов пациенту помог гемодиализ.
- Бисопролол. У взрослого пациента, проглотившего 140 мг бисопро-лола (нормальная доза — 20 мг/сут), развилась синусовая брадикардия; пациент выжил. Бисопролол обладает более высокой кардиоселективностью, чем атенолол. При пероральном приеме у него высокая биодоступность (90 %) и длительный период полужизни (11 ч).
Максимальные концентрации, составляющие примерно 50 нг/мл, достигаются приблизительно через 3 ч после приема терапевтической дозы. Степень связывания с белками плазмы — 30 %, а кажущийся объем распределения — 3,3 л/кг. Около 50 % дозы экскретиру-ется в неизмененном виде.
- Лабеталол. У 43-летней пациентки, проглотившей 5,6—7 г лабеталола, развилась сильная гипотензия. Пациентке помогло многократное введение ударных доз адреналина по 5 мг с последующим введением 20 мг. За 24 ч пребывания в отделении интенсивной терапии она получила всего 174 мг адреналина и выздоровела.
У взрослого человека, проглотившего 6 г препарата, развилась тяжелая почечная недостаточность. После гемодиализа пациента лечили изопреналином и глюкагоном, он выздоровел.
- Эсмолол. Когда пациенту с трепетаний предсердий вместо рекомендованной ударной дозы 500 мкг/кг/мин в течение 1 мин ввели 5000 мкг/кг/мин эсмолола, произошло немедленное развитие брадикардии, гипотензии и сонливости. Скорость вливания была снижена до 5 мкг/кг/мин, и в течение 15 мин брадикардия, гипотензия и сонливость исчезли. Внутривенное введение 1,3 г препарата привело к асистолии, стандартные мероприятия по длительному поддержанию сердечной деятельности и поддерживающая терапия привели к быстрому выздоровлению.
- Тимолол. Закапывание 2—9 капель тимолола (0,25 %) в каждый глаз может вызвать у пациентов в возрасте старше 70 лет слабость, головокружение, потерю равновесия, спотыкание при ходьбе, тошноту, обморочное состояние.
б) Беременность и лактация. В-Блокаторы, часто кардиоселективные, широко применяются для лечения гипертензии, индуцированной беременностью. Полагают, что неблагоприятные реакции редки, и считают, что воздействие на плод и на грудного ребенка минимально. У пациентки, которой в связи с гипертензией, индуцированной беременностью, вводили лабеталол, родился недоношенный ребенок.
У младенца, извлеченного на 33-й неделе беременности посредством кесарева сечения, были отмечены брадикардия, пониженный пульс на бедренной артерии, цианоз и нарушение дыхания.
Соталол экскретируется в грудное молоко; с ним младенец получал до 23 % материнской дозы препарата. В грудном молоке обнаруживается ряд бета-блокаторов, в том числе ацебутолол, атенолол, лабеталол, пиндолол, метопролол, надолол, окспренолол, пропранолол и тимолол.
в) Синдром отмены. Резкая отмена бета-блокаторов, не обладающих собственной симпатомиметической активностью (например, надолола, пропранолола), может привести к острому развитию стенокардии и инфаркта миокарда у пациентовгипертоников, в анамнезе которых не было ишемической болезни сердца.
По-видимому, бета-блокаторы с симпатомиметической активностью (окспренолол и пиндолол, а также блокаторы кальциевых каналов) в меньшей степени способствуют развитию синдрома отмены, чем препараты, не обладающие симпатомиметической активностью, хотя при проведении исследования в контролируемых условиях у здоровых добровольцев после резкой отмены пропранолола не наблюдалось признаков синдрома отмены, затрагивающих центральную нервную систему.
Резкое прекращение курса лечения пропранололом, с помощью которого контролировались психотические симптомы пациента, привело к повторному появлению психотических симптомов.
После резкой отмены атенолола наблюдался некоторый период сверхчувствительности к изопротеренолу, а также небольшой всплеск частоты сердечных сокращений при нагрузке и изменении положения. Бопиндолол индуцировал длительное состояние пониженной чувствительности к изопротеренолу.
г) Лабораторные данные отравления бета-адреноблокаторами:
- Ацебутолол. В случаях летального исхода после приема ацебуталола не выявлено корреляции между количеством проглоченного препарата и его концентрацией в крови. Аналогичным образом не выявлено корреляции между принятой дозой и токсическими эффектами.
- Атенолол. После приема 4—6,5 г атенолола концентрации атенолола в сыворотке составляли 849 пг/л (через 36 ч) и 564 пг/л (через 96 ч). Концентрации атенолола после приема 50 мг составляли примерно 20 пг/л через 36 ч и 10 пг/л через 96 ч.
- Метопролол. Посмертная концентрация метопролола у пациента, которого нашли в постели с гипотензией и без реакции на внешние раздражители, через 10 ч после реанимации была примерно в 50 раз выше терапевтического уровня (4,7 мкг/мл). Гиперкалиемия и гипогликемия встречаются редко.
- Пропранолол. Концентрации пропранолола в крови подтверждают факт интоксикации, но не могут быть использованы для выбора метода экстренной терапии. Терапевтические концентрации в плазме варьируют от 30 до 200 нг/мл. При смертельных передозировках пропранолола концентрации в плазме варьируют от 4000 до 28 000 нг/мл; пациенты выживали также при концентрациях 2300 и 2800 нг/мл.
Видео фармакологические, побочные эффекты бета-адреноблокаторов
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Отравление нервно-мышечными блокаторами и их побочные эффекты
Передозировка как деполяризующих, так и недеполяризующих нервно-мышечных блокаторов чревата продолжительным параличом скелетной мускулатуры, гиперкалиемией, высвобождением гистамина, гипотензией, остановкой сердца и смертью.
а) Структура и классификация. Миорелаксанты классифицируют в зависимости от механизма ослабления ими эффекта ацетилхолина. Они бывают деполяризующими или недеполяризующими (конкурентными) нервно-мышечными блокаторами. Сукцинилхолин образован двумя молекулами ацетилхолина, связанными между собой через метильные группы ацетатов. Панкуроний и векуроний — стероидные нервно-мышечные блокаторы, структурно близкие к кортикостероидам.
б) Источники. Атракурий, галламин, панкуроний, сукцинилхолин и векуроний представляет собой синтетические продукты, метокурин является полусинтетическим продуктом, а тубокурарин экстрагируют из растений рода Chonododendron.
в) Токсичные дозы миорелаксантов:
- Галламина триэтиодид. Одному взрослому пациенту случайно ввели 1,4 мл (30 мг) галламина в субарахноидальное пространство. Он выжил.
- Панкурония бромид. Один взрослый пациент самостоятельно ввел себе внутривенно 10 мл панкурония бромида (1 мг/мл) и тиопентал натрия, после чего был найден мертвым. Пациенту в возрасте 79 лет с почечной недостаточностью ввели внутривенно 105 мг панкурония за 4 дня. Через 6 сут он скончался от циркуляторного шока.
- Тубокурарина хлорид. Случайная внутриартериальная инъекция тубокурарина в левый локтевой сгиб обусловила боль и слабость в руке. Полное выздоровление наступило через 45 мин. Случайная передозировка (30 мг) тубокурарина приводит к остановке дыхания у большинства взрослых пациентов за 2 — 3 мин. После двух случайных передозировок, равных 80 и 100 мг, пострадавшие выздоровели.
- Векурония бромид. Ребенку, страдающему синдромом Дауна, с массой тела 9,7 кг в возрасте 23 мес ввели внутривенно 37 мг векурония в течение 1 ч (3,83 мг/кг в ч). Он умер через 5 сут от обширного сепсиса. Введенное количество соответствовало пятикратному превышению рекомендованной изготовителем скорости вливания (0,5 — 0,8 мг/кг в ч). Гемодинамических нарушений во время инфузии и в следующие за ней 24 ч не было.
г) Летальные дозы миорелаксантов. Одна летальная доза панкурония составила 10 мг внутривенно, другая смерть последовала через 6 сут после введения 105 мг этого средства за 4 дня. Передозировка векурония (37 мг) привела к смерти через 5 дней от сепсиса.
д) Токсикокинетика нервно-мышечных блокаторов. Обзор токсикокинетических свойств недеполяризующих миорелаксантов показывает, что они умеренно связываются с белками, быстро (за считанные минуты) распределяются по организму, характеризуются низким кажущимся объемом распределения и периодом полувыведения, составляющим несколько часов.
- Метаболизация. Сукцинилхолин быстро метаболизируется, главным образом плазменной псевдохолинэстеразой, до сукцинилмонохолина и холина. Сукцинилмонохолин как недеполяризующий блокатор примерно в 20 раз менее активен, чем сукцинилхолин. Он может накапливаться и вызывать тяжелое апноэ у пациентов с нарушенной почечной функцией. Примерно 2 — 10 % выводится с мочой в неизмененном виде.
- Токсичность. Применение сукцинилхолина у пациентов с генетически детерминированной атипичной псевдохолинэстеразой или у тех, кто получал холинэстеразные ингибиторы, чревато продолжительным апноэ.

ж) Взаимодействие миорелаксантов с лекарствами. Средства, изменяющие эффект миорелаксантов, могут действовать проксимальнее нервно-мышечного синапса в центральной нервной системе или в кровотоке, в зоне этого синапса или дистальнее него на уровне мембраны мышечной клетки\. В синаптической зоне они влияют либо на нервное окончание, либо на постсинаптиче-скую мембрану.
Средства, взаимодействующие с недеполяризующими миорелаксантами:
- Антибиотики. Антибиотики, например аминогликозиды (амикацин, дигидрострептомицин, гентамицин, канамицин, стрептомицин, тобрамицин) и полипептиды (полимиксина А, В и С), не только потенцируют действие недеполяризующих миорелаксантов, но и сами по себе вызывают нервно-мышечную блокаду. Тетрациклины также обладают слабыми свойствами нервно-мышечных блокаторов и потенцируют недеполяризующие миорелаксанты.
- Анестетики для внутривенного введения. Кетамин потенцирует действие альфа-тубокурарина, но не панкурония. Мидазолам усиливает индуцированную векуронием блокаду. С другими внутривенными анестетиками существенного взаимодействия почти нет. Хроническое применение трициклических антидепрессантов может предрасполагать пациента, получающего панкуроний, к желудочковой тахикардии.
- Диуретики. У человека фуросемид в дозе 1 мг/кг облегчает снятие вызванной панкуронием блокады. Высокие дозы этого диуретика могут противодействовать индуцируемой панкуронием блокаде у нейрохирургических пациентов.
- Бета-блокаторы. Бета-блокаторы противодействуют связыванию ацетилхолина с постсинаптической мембраной. Они могут усилить или демаскировать миастению и индуцировать миастенический синдром.
- Антиаритмические средства. У человека прокаинамид обостряет миастению и индуцирует мышечную слабость у здоровых индивидов. d-Tyбокурариновая нервно-мышечная блокада у кошки может усилить это его действие на 25 %. Хинидин усиливает блокаду, вызываемую недеполяризующими миорелаксантами.
- Блокаторы кальциевых каналов. Верапамил и нифедипин потенцируют нервно-мышечную блокаду, индуцируемую d-тубокурарином, панкуронием, атракурием и векуронием.
- Сульфат магния. Магний потенцирует нервно-мышечную блокаду, создаваемую панкуронием и векуронием. У пациентов, получающих вливания сульфата магния, дозу векурония нужно снижать. Магний ослабляет пресинаптическое высвобождение ацетилхолина, снижает чувствительность постсинаптической мембраны к нему и ослабляет возбудимость мембраны мышечного волокна.
- Метилксантины. Аминофиллин и теофиллин играют роль антагонистов панкурония. Непрерывное вливание аминофиллина может не позволить ему индуцировать нервно-мышечную блокаду. Вероятно, это связано с вызываемым ами-нофиллином ингибированием фосфодиэстеразы, приводящим к повышению уровня циклического аденозинмо-нофосфата и, по-видимому, ацетилхолина.
- Фенитоин. Долговременная терапия фенитоином может создать резистентность к метокурину, панкуронию и векуронию, но не к атракурию. Фенитоин способен на 50 % сократить продолжительность нервно-мышечной блокады. Вероятно, он дает пресинаптический эффект, близкий к производимому недеполяризующими миорелаксантами.
- Карбамазепин. Пациенты, получающие карбамазепин, бывают резистентными к панкуронию. Продолжительность действия панкурония и векурония у них может сократиться на 65 %.
- Карбонат лития. Литий способен потенцировать панкурониевую блокаду и индуцировать миастеническую реакцию. Он ослабляет синтез и выделение ацетилхолина нервными окончаниями.
- Азатиоприн. Азатиоприн выступает в роли относительно слабого и транзиторного антагониста нервно-мышечной блокады.
- Циклоспорин. Циклоспорин в растворителе кремофоре и сам кремофор могут потенцировать нервно-мышечную блокаду, индуцируемую векуронием и атракурием.
- Кортикостероиды. Индуцируемую панкуронием блокаду можно ослабить у пациентов, получающих долговременную стероидную терапию. Кортикостероиды повышают также вероятность пареза при введении вместе со стероидным миорелаксантом, например панкуронием или векуронием.

и) Механизм действия нервно-мышечных блокаторов (миорелаксантов).
- Деполяризующие миорелаксанты:
Сукцинилхолин. Природный нейромедиатор ацетилхолин действует не только на никотиновые рецепторы в нервно-мышечных синапсах и вегетативных ганглиях, но и на мускариновые рецепторы в гладких мышцах, миокарде и экзокринных железах.
Сукцинилхолин, обладая сходной структурой, проявляет активность в тех же самых местах.
Сердце. Брадикардия после первой инъекции сукцинилхолина может быть вызвана стимуляцией парасимпатических ганглиев или мускариновых рецепторов синусово-предсердного узла.
Высвобождение гистамина. Все основные соединения способны разрушать тучные клетки, приводя к высвобождению гистамина. Обычная доза 1 мг/кг может вызвать прилив крови к лицу, бронхоспазм, гипотензию и другие анафилактоидные реакции.
Гиперкалиемия. После сукцинилхолиновой деполяризации возможно небольшое увеличение плазменной концентрации ионов калия (около 0,5 ммоль/л, т. е. 0,5 мэкв/л). Если их уровень достигнет 7 — 8 ммоль/л, не исключены желудочковая фибрилляция и остановка сердца.
Нервно-мышечные эффекты. Возможны фасцикуляции, мышечная боль, миоглобинурия, повышение внугрижелудочного и внутриглазного давления.
- Недеполяризующие миорелаксанты:
Вегетативные эффекты. Большинство недеполяризующих миорелаксантов имеет в молекуле 2 положительно заряженные четвертичные аммонийные группы, которые присоединяются к отрицательно заряженным холинергическим рецепторам, создавая блокаду за счет конкурентного антагонизма с нейромедиатором.
Высвобождение гистамина. Миорелаксанты обычно непосредственно действуют на тканевые мастоциты и приводят к высвобождению ими гистамина без активации антителом или комплементом (анафилактоидная реакция). Выделение гистамина зависит от дозы и скорости введения миорелаксанта. Оно проявляется эритемой верхней части грудной клетки и лица, транзиторным повышением кровяного давления и учащением сердечных сокращений. Возможен бронхоспазм. Тяжелая реакция чревата сосудистым коллапсом.


Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Нейролептики (например производные фенотиазина — хлорпромазин, промазин, левомепромазин, прохлорперазин, трифлуоперазин) относят к группе психоседативных средств. Детоксикация в печени, выделение через кишечник и с мочой — не более 8% принятой дозы в течение 3 сут. В последнее время число случаев передозировки и отравлений ЛС этой группы растёт. Токсическая доза более 500 мг. Смертельная доза 5–10 г. Токсическая концентрация в крови — 1–2 мг/л, смертельная — 3–12 мг/л.
Этиопатогенез • Токсическое действие: психотропное, нейротоксическое (ганглиолитический, адренолитический эффекты; угнетение ретикулярной формации мозга; поражение таламокортикальной системы) • Гистологически преобладают признаки гипоксии в виде распространённых ишемических изменений нейронов, образования гомогенных коагулятов в сосудах и резко выраженных дистрофических изменений астроцитарной глии с появлением амебоидных форм клеток.
Клиническая картина. Основные стадии такие же, как и при отравлении снотворными средствами и транквилизаторами (см. Отравление снотворными средствами и транквилизаторами) • Резкая слабость, головокружение, выраженная сухость во рту, тошнота • Снижение или отсутствие реакции зрачков на свет при относительной сохранности роговичных рефлексов (у 70–80%), нарушение конвергенции • Неврологические расстройства •• Атаксия, снижение сухожильных и периостальных рефлексов, мышечный спазм, тризм жевательных мышц, судороги •• Акинетико-ригидный синдром, особенности: диссоциация симптомов — выраженная гипомимия и гипокинезия без значительного повышения мышечного тонуса (мышечную гипотонию наблюдают в 50% случаев) •• Гиперкинетический синдром — сочетание нескольких видов гиперкинезов (тортиколлис, оральные гиперкинезы, тремор кистей рук) или смена одного гиперкинеза другим (хореиформного ознобоподобным или крупноамплитудным тремором рук) •• Сохранены реакции на болевые раздражения (у 75%) • Учащение пульса, снижение АД без цианоза • При приёме внутрь — гиперемия и отёк слизистой оболочки рта, у детей — выраженное раздражение слизистой оболочки ЖКТ • Кожные аллергические реакции • Коматозное состояние — неглубокое, гипотермия, сухожильные рефлексы повышены; по выходе из комы возможны паркинсонизм, ортостатический коллапс • В некоторых случаях (в результате блокады дофаминовых рецепторов) возможно развитие нейролептического злокачественного синдрома: гипертермия с экстрапирамидными и вегетативными нарушениями, способными привести к смерти (Делея–Деникера синдром).
Диагностика • Спектрофотометрический метод определения токсического вещества в крови • ЭЭГ • ЭКГ — синусовая тахикардия, снижение ST ниже изолинии, отрицательный зубец Т.
Дифференциальная диагностика — см. Отравление снотворными средствами и транквилизаторами.
ЛЕЧЕНИЕ
Тактика ведения (см. также Отравление снотворными средствами и транквилизаторами) • Промывание желудка через зонд с последующим введением сорбента (активированный уголь), рвотные средства • В последующем — инфузионная терапия, форсированный диурез без ощелачивания крови • Гемосорбция (в 2–3 раза сокращает длительность коматозного периода) • Симптоматическая терапия: ликвидация тяжёлых дыхательных и гемодинамических расстройств, купирование судорожного синдрома, устранение осложнений.
Лекарственная терапия • Дифенгидрамин 2–3 мг/кг в/в или в/м для подавления экстрапирамидных симптомов • Аналептики (камфора, никетамид, кофеин, эфедрин) — только при поверхностной коме. Во всех остальных случаях они строго противопоказаны (развитие судорожных состояний и дыхательных осложнений).
Осложнения — см. Отравление снотворными средствами и транквилизаторами.
Прогноз (см. также Отравление снотворными средствами и транквилизаторами) • Астенический синдром сохраняется даже через 2–3 года после интоксикации • Длительное сохранение паркинсонического синдрома (даже через 2–3 года после отравления) • Больные нуждаются в продолжительном наблюдении и лечении после выписки из стационара.
МКБ-10 • T43.3 Отравление антипсихотическими и нейролептическими препаратами
Код вставки на сайт
Нейролептики (например производные фенотиазина — хлорпромазин, промазин, левомепромазин, прохлорперазин, трифлуоперазин) относят к группе психоседативных средств. Детоксикация в печени, выделение через кишечник и с мочой — не более 8% принятой дозы в течение 3 сут. В последнее время число случаев передозировки и отравлений ЛС этой группы растёт. Токсическая доза более 500 мг. Смертельная доза 5–10 г. Токсическая концентрация в крови — 1–2 мг/л, смертельная — 3–12 мг/л.
Этиопатогенез • Токсическое действие: психотропное, нейротоксическое (ганглиолитический, адренолитический эффекты; угнетение ретикулярной формации мозга; поражение таламокортикальной системы) • Гистологически преобладают признаки гипоксии в виде распространённых ишемических изменений нейронов, образования гомогенных коагулятов в сосудах и резко выраженных дистрофических изменений астроцитарной глии с появлением амебоидных форм клеток.
Клиническая картина. Основные стадии такие же, как и при отравлении снотворными средствами и транквилизаторами (см. Отравление снотворными средствами и транквилизаторами) • Резкая слабость, головокружение, выраженная сухость во рту, тошнота • Снижение или отсутствие реакции зрачков на свет при относительной сохранности роговичных рефлексов (у 70–80%), нарушение конвергенции • Неврологические расстройства •• Атаксия, снижение сухожильных и периостальных рефлексов, мышечный спазм, тризм жевательных мышц, судороги •• Акинетико-ригидный синдром, особенности: диссоциация симптомов — выраженная гипомимия и гипокинезия без значительного повышения мышечного тонуса (мышечную гипотонию наблюдают в 50% случаев) •• Гиперкинетический синдром — сочетание нескольких видов гиперкинезов (тортиколлис, оральные гиперкинезы, тремор кистей рук) или смена одного гиперкинеза другим (хореиформного ознобоподобным или крупноамплитудным тремором рук) •• Сохранены реакции на болевые раздражения (у 75%) • Учащение пульса, снижение АД без цианоза • При приёме внутрь — гиперемия и отёк слизистой оболочки рта, у детей — выраженное раздражение слизистой оболочки ЖКТ • Кожные аллергические реакции • Коматозное состояние — неглубокое, гипотермия, сухожильные рефлексы повышены; по выходе из комы возможны паркинсонизм, ортостатический коллапс • В некоторых случаях (в результате блокады дофаминовых рецепторов) возможно развитие нейролептического злокачественного синдрома: гипертермия с экстрапирамидными и вегетативными нарушениями, способными привести к смерти (Делея–Деникера синдром).
Диагностика • Спектрофотометрический метод определения токсического вещества в крови • ЭЭГ • ЭКГ — синусовая тахикардия, снижение ST ниже изолинии, отрицательный зубец Т.
Дифференциальная диагностика — см. Отравление снотворными средствами и транквилизаторами.
ЛЕЧЕНИЕ
Тактика ведения (см. также Отравление снотворными средствами и транквилизаторами) • Промывание желудка через зонд с последующим введением сорбента (активированный уголь), рвотные средства • В последующем — инфузионная терапия, форсированный диурез без ощелачивания крови • Гемосорбция (в 2–3 раза сокращает длительность коматозного периода) • Симптоматическая терапия: ликвидация тяжёлых дыхательных и гемодинамических расстройств, купирование судорожного синдрома, устранение осложнений.
Лекарственная терапия • Дифенгидрамин 2–3 мг/кг в/в или в/м для подавления экстрапирамидных симптомов • Аналептики (камфора, никетамид, кофеин, эфедрин) — только при поверхностной коме. Во всех остальных случаях они строго противопоказаны (развитие судорожных состояний и дыхательных осложнений).
Осложнения — см. Отравление снотворными средствами и транквилизаторами.
Прогноз (см. также Отравление снотворными средствами и транквилизаторами) • Астенический синдром сохраняется даже через 2–3 года после интоксикации • Длительное сохранение паркинсонического синдрома (даже через 2–3 года после отравления) • Больные нуждаются в продолжительном наблюдении и лечении после выписки из стационара.
МКБ-10 • T43.3 Отравление антипсихотическими и нейролептическими препаратами
Читайте также:

