Синдром эндогенной интоксикации на фоне лямблиоза и кандидоза
Обновлено: 24.04.2024
Несмотря на схожесть патогенеза, синдрома эндогенной интоксикации при каждой нозологической форме имеет определенные специфические признаки (Ю. С. Гольд-фарб, 1988; Б. И. Шулутко, 1993; Э. А. Туликова, 1994). Перитонит условно можно назвать классической моделью СЭИ, поэтому его целесообразно рассмотреть в качестве базовой модели данного состояния.
Патогенез. Выделяют три компонента, участвующих в формировании СЭИ при перитоните:
1. Микробиологический.
2. Биохимический.
3. Иммунологический.
В течении СЭИ выделяют три (разы (В. К. Гостищев и соавт., 1992):
I фаза — фаза интоксикации. В формировании СЭИ участвуют болезнетворные микробы и их токсины, биоактивные вещества, синтезируемые в организме в норме, но в данном случае их синтез выходит из-под контроля и вещества начинают накапливаться.
II фаза — диспротеинемия. Для нее характерны активные деструктивные процессы в тканях; усиливается распад белков, снижается их синтез, нарушаются процессы дезаминирования. С момента начала деструкции в крови повышается уровень некротических тел, СМ, которые и вызывают токсический эффект. В начале II фазы присоединяются аутоаллергические процессы.
III фаза — накопление промежуточных метаболитов. В крови и лимфе накапливаются этанол, аммиак, ацетон и др. Микробный фактор может ускорить переход одной фазы в другую. Тяжесть, время развития и обратимость СЭИ прямо связаны с тем, какие микробы вызвали заболевание: ранее имевшаяся микрофлора или новые.
Клинически в течении синдрома эндогенной интоксикации различают три степени тяжести (В. К. Гостищев и соавт., 1992). Основные критерии клинических данных степеней тяжести эндогенной интоксикации представлены в табл. 28.
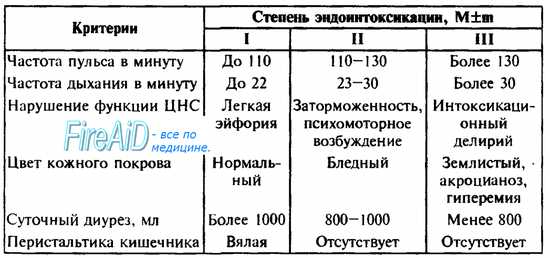
Таблица 28. Степени эндогенной интоксикации при перитоните (В. К. Гостищев и соавт., 1992).
Наиболее характерным признаком появления синдрома эндогенной интоксикации при перитоните является нарушение сознания в виде энцефалопатии (см. тему НЕОТЛОЖНЫЕ СОСТОЯНИЯ В ПСИХИАТРИИ). Больной становится заторможенным и безразличным к окружающему. Вначале данное состояние чередуется с периодами легкой эйфории, в это время больные говорливы, не могут сосредоточиться на одной мысли. При нарастании интоксикации заторможенность также нарастает, иногда наоборот, возникает психомоторное возбуждение, переходящее в интоксикационный делирий, после чего возможно наступление комы (см. тему ОБМОРОК, КОЛЛАПС, КОМА). Для определения снижения (угнетения) уровня сознания можно использовать шкалу Глазго.
Другим характерным признаком синдрома эндогенной интоксикации является сокращение почасового диуреза, обусловленное поражением почечных канальцев по типу острого нефроза и потери жидкости (рвота, понос, выход жидкости во внеклеточное пространство). Вследствие этого происходит дополнительное отравление организма невыведенными продуктами белкового обмена. Каждой степени СЭИ соответствует определенный суточный диурез (см. табл. 28). Критическим является почасовой диурез в объеме 40 мл/час и менее. При тяжелой степени интоксикации с переходом олигурии в анурию возможно формирование ОПН (см. тему ОСТРАЯ ПОЧЕЧНАЯ И ПЕЧЕНОЧНАЯ НЕДОСТАТОЧНОСТИ).
Появление желтушности кожных покровов и склер является прогностически неблагоприятным признаком, так как это свидетельствует о развитии острой печеночной недостаточности и снижении детоксикационных возможностей организма (см. тему ОСТРАЯ ПОЧЕЧНАЯ И ПЕЧЕНОЧНАЯ НЕДОСТАТОЧНОСТИ).
Гемодинамические изменения при СЭИ, как впрочем и все другие, не являются специфическими. Причиной учащения пульса, снижения АД могут быть шок, реакция на боль, кровопотерю, предшествующая сердечная недостаточность. Следует помнить, что снижение давления ниже 90 мм рт. ст. характерно для шока II степени (см. тему ШОКОВЫЕ СОСТОЯНИЯ).
Основные биохимические показатели синдрома эндогенной интоксикации на фоне перитонита представлены в табл. 29.
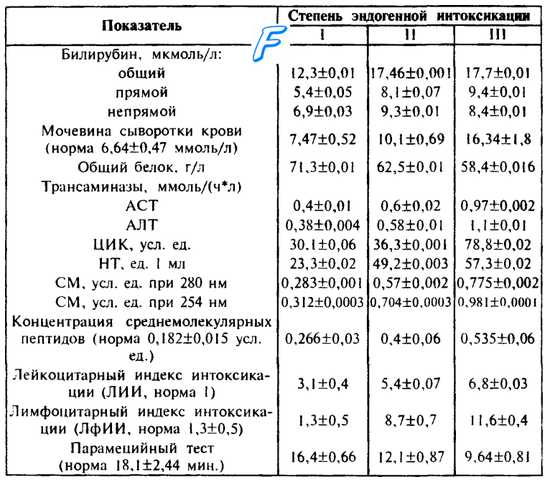
Таблица 29. Биохимические показатели крови при эндогенной интоксикации различной степени, М±т (В. К. Гостищев и соавт., 1992).
Примечание. 1. ЦИК — циркулирующие имунные комплексы; НТ некротические тела; СМ — средние молекулы.
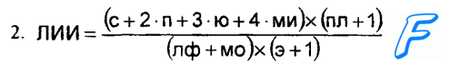
ми миелоциты;
с сегментоядерные лейкоциты;
ю метамиелоциты;
п палочкоядерные лейкоциты;
пл плазменные клетки;
лф лимфоциты;
МО моноциты;
э эозинофилы.
Синдром эндогенной интоксикации. Клиника синдрома эндогенной интоксикации.
В настоящее время одной из наиболее сложных проблем интенсивной терапии является синдром эндогенной интоксикации (СЭИ), сопровождающий значительное количество патологических состояний (шок, перитонит, панкреатит и др.), которые по мере своего развития могут приводить к летальному исходу.
Прогрессирование эндотоксикоза обусловлено накоплением в крови различных по происхождению, химической структуре и биологическому воздействию веществ, именуемых эндотоксинами. Эндотоксины способствуют развитию острой почечно-печеночной недостаточности, сердечно-сосудистой недостаточности, острого респираторного дистресс-синдрома, приводя в конечном итоге к появлению крайне тяжелого состояния - синдрома мультиорганной дисфункции.
Эндогенная интоксикация - клинический синдром, возникающий при различных по этиологии патологических состояниях, обусловленных накоплением в тканях и биологических жидкостях организма продуктов нарушенного обмена веществ, метаболитов, деструктивных клеточных и тканевых структур, разрушенных белковых молекул, pi сопровождающийся функциональными и морфологическими поражениями органов и систем организма.
Выделяют три основных звена, которые определяют тяжесть состояния больных и выраженность клинической симптоматики: токсемия, нарушение микроциркуляции, угнетение функций собственных детоксицирующих и защитных систем организма.
Основным звеном патогенеза синдрома эндогенной интоксикации является токсемия. К сожалению, четкая дифференциация токсических веществ эндогенного происхождения практически невозможна. Однако в каждом конкретном случае можно выделить "первичные" и "вторичные" эндотоксины. Так, при ожогах, синдроме длительного раздавливания, облитерирующих сосудистых заболеваниях "первичными" являются продукты белковой деградации, "вторичными" - продукты естественного метаболизма, накопление которых в организме является следствием угнетения функций естественной детоксикации и экскреции.
Эндотоксемия, нарушая тонус периферических сосудов, реологию крови, кинетические и механические свойства форменных элементов крови, приводит к тканевой гипоксии, которая является одним из важных звеньев патогенеза СЭИ, течение которого усугубляется снижением функции органов естественной детоксикации и экскреции. Токсины блокируют места связывания молекул альбумина, что ведет к снижению эффективности проводимого медикаментозного лечения, поскольку этот белок является транспортным агентом для многих фармакологических препаратов.
Клиника синдрома эндогенной интоксикации.
Сопоставление экспериментальных и клинических исследований позволило выявить следующие стадии развития синдрома эндогенной интоксикации.
I стадия синдрома эндогенной интоксикации. Реактивно-токсическая возникает в ответ на формирование первичного деструктивного очага или травматического повреждения. Лабораторными признаками этой стадии являются повышение в крови уровней молекул средней массы (МСМ), продуктов перекисного окисления липидов (ДК и МДА), возрастание ЛИИ.
II стадия синдрома эндогенной интоксикации - стадия выраженной токсемии развивается после прорыва гастогематического барьера, когда в циркулирующую кровь попадают эндотоксины, образовавшиеся в первичном очаге интоксикации, с последующим распространением и накоплением в организме. В зависимости от состояния организма, его резистентности и исходного уровня детоксицирующих и иммунных систем выделяют компенсированную и декомпенсированную стадии выраженной токсемии.
III стадия синдрома эндогенной интоксикации - мультиорганной дисфункции (СМОД) наблюдается при дальнейшем прогрессировашш патологического процесса как следствие тяжелого повреждения эндотоксинами различных органов и систем с развитием их функциональной декомпенсацш!. Клинически эта стадия Проявляется нарушением сознания, гипоксией, выраженной сердечной Недостаточностью, олигурией, паралитической непроходимостью кишечника. В крови определяется высокая концентрация креатинина, мочевины, билирубина.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Лямблиоз у детей – паразитарная инвазия, вызываемая одноклеточными организмами – лямблиями. Лямблиоз у детей может протекать с диспепсическим, болевым, астено-невротическим, интоксикационным, аллерго-дерматологическим синдромами. Диагностика лямблиоза у детей предполагает проведение микроскопического и ПЦР исследования кала и дуоденального содержимого, ИФА крови. Лечение лямблиоза у детей включает специфическую противолямблиозную терапию, диетический режим, проведение тюбажей с холекинетиками, прием ферментативных препаратов и энтеросорбентов.

Общие сведения
Лямблиоз у детей – протозойная инфекция, вызываемая микроскопическими паразитами Lamblia intestinalis (лямблиями). Согласно эпидемиологическим данным, общая распространенность лямблиоза в популяции составляет 2-5%, их них более половины случаев заболевания приходится на детей. В организованных детских коллективах (яслях, садах, школах, интернатах) зараженность детей лямблиозом достигает 30-50%. Восприимчивость к лямблиозной инфекции среди детей младшего возраста в 3 раза выше, чем среди взрослых. Лямблиоз у ребенка может протекать под маской многочисленных заболеваний, поэтому его выявление и предупреждение распространения составляет сложную проблему детской гастроэнтерологии и педиатрии.

Причины
Возбудителем лямблиоза у детей и взрослых выступает Lamblia intestinalis (син.- Giardia lamblia, Giardia intestinales, Giardia duodenalis) - одноклеточный жгутиковый микроорганизм, паразитирующий в кишечнике. В организме человека лямблии могут существовать в двух формах – вегетативной (в верхних отделах тонкого кишечника - двенадцатиперстной и начальном отделе тощей кишки) и споровой (цистной) в толстой кишке, откуда выделяются с испражнениями во внешнюю среду. Вне организма хозяина вегетативные формы лямблий быстро погибают, цисты же сохраняют свою жизнеспособность до 60-70 дней во влажной среде и до 3-х месяцев в водопроводной воде.
Заражение детей лямблиозом происходит посредством фекально-орального механизма, при попадании цист паразитов в пищеварительный тракт ребенка с водой, пищей, при пользовании общими игрушками, посудой и предметами гигиены (носовыми платками, полотенцами), через грязные руки. Новорожденные дети могут заражаться лямблиозом в родах при прорезывании головки. В семьях, где один или несколько детей больны лямблиозом, обычно инфекция имеется у всех остальных членов семьи.
Патогенез
Особенности жизнедеятельности лямблий обусловливают их патогенное воздействие на организм ребенка. При попадании в организм человека лямблии паразитируют в просвете кишечника, многократно присасываясь и открепляясь от слизистой оболочки, чем вызывают повреждение энтероцитов. Вследствие механического повреждения слизистой оболочки в тонком кишечнике активизируется условно-патогенная и патогенная микрофлора. При исследовании кала у детей с лямблиозом нередко обнаруживаются грибы, H.pylori; снижение уровня бифидо- и лактобактерий, кишечной палочки. Дисбактериоз создает благоприятные условия для размножения лямблий в кишечнике, проникновения токсинов во внутреннюю среду организма.
Кроме этого, лямблии выделяют токсические продукты метаболизма, которые нарушают всасывание углеводов, жиров, белков, микроэлементов, витаминов и минеральных веществ в тонком кишечнике, формируя дефицит микронутриентов и поливитаминную недостаточность. При лямблиозе у детей страдает синтез пищеварительных ферментов, что находит свое выражение в развитии лактазной недостаточности и синдрома мальабсорбции.
Раздражение нервных окончаний стенки кишки запускает патологические висцеро–висцеральные рефлексы, способствуя развитию абдоминального синдрома. Сенсибилизация организма продуктами метаболизма и гибели лямблий вызывает различные формы аллергических проявлений.
Длительное персистирование лямблий, воздействие их токсинов и продуктов обмена на различные системы, вызывает у ребенка синдром хронической эндогенной интоксикации, невротические реакции, вторичную иммунную недостаточность.
Классификация
В соответствии с классификацией ВОЗ, различают бессимптомное лямблионосительство и клинически выраженный лямблиоз у детей. По особенностям клинических проявлений выделяют первичную инвазию (острый лямблиоз чаще встречается у детей младшей возрастной группы) и затяжную рецидивирующую инфекцию (хронический лямблиоз обычно регистрируется у старших детей и взрослых).
В зависимости от клинического варианта лямблиоз у детей может протекать в кишечной форме (в виде дуоденита, дискинезии двенадцатиперстной кишки, энтерита, энтероколита), гепатобилиарной форме (в виде дискинезии желчевыводящих путей, холангита, холецистита), как сопутствующее заболевание.
У детей разного возраста лямблиоз может приобретать клиническую форму с преобладанием болевого, диспепсического, аллерго-дерматологического, астено-невротического, интоксикационного синдрома или их сочетаний.
Симптомы лямблиоза у детей
Практически у всех детей с лямблиозом наблюдается абдоминальный синдром, характеризующийся приступообразной болью в животе (в эпигастрии, в районе пупка, правом подреберье), не связанной с приемом пищи. Иногда выраженность болевого синдрома у детей может напоминать клинику острого живота.
Диспепсический синдром у ребенка с лямблиозом может выражаться в снижении аппетита, наличии отрыжки, изжоги, тошноты, горечи во рту, вздутия живота. На фоне сопутствующего дисбиоза кишечника стул становится жидким, пенистым, зловонным; частота дефекаций увеличивается до 3-5 раз в сутки. При исследовании копрограммы обнаруживается стеаторея. Иногда у детей с лямблиозом отмечается чередование запоров и диареи. Следствием нарушения кишечного всасывания и расстройства стула служит снижение массы тела, гипотрофия.
Аллерго-дерматологические проявления лямблиоза у детей малоспецифичны. В ряде случаев на коже появляется мелкоточечная розовая сыпь по типу крапивницы, неукротимый кожный зуд; у подростков возникает или усиливается юношеская угревая сыпь. Может развиваться аллергический ринит, аллергический конъюнктивит, атопический дерматит, отек Квинке, бронхиальная астма. Иногда лямблиоз у детей заявляет о себе приступами артралгий и артрита.
Астено-невротический синдром при лямблиозе у детей является следствием угнетающего действия на ЦНС продуктов жизнедеятельности лямблий. Проявления синдрома находят свое выражение в повышенной утомляемости, снижении работоспособности и эмоционального тонуса ребенка, раздражительности, плаксивости, головных болях, головокружениях, появлении скрипа зубами (бруксизма), тиков.
Интоксикация при лямблиозе у детей сопровождается гепатолиенальным синдромом, лимфаденопатией, увеличением миндалин и аденоидов, беспричинным подъемом температуры тела до 37,5-38°С.
Хронический лямблиоз у детей не имеет ярко выраженных клинических проявлений. Его течение характеризуется сухостью и шелушением кожи, фолликулярным кератозом, обострением или манифестацией аллергических заболеваний, утяжелением течения соматической патологии, неустойчивостью стула, периодическим субфебрилитетом, признаками вегето-сосудистой дистонии и т. д.
Диагностика
Поскольку признаки инфекции не являются специфичными, дети с лямблиозом часто длительно и безрезультатно лечатся у аллерголога-иммунолога, детского дерматолога, детского пульмонолога. Обследованию на лямблиоз должны подвергаться дети с патологией ЖКТ, вегетативными и невротическими нарушениями, аллергическими заболеваниями, стойкой эозинофилией по данным гемограммы.
Наиболее доступной формой диагностики лямблиоза у детей считается выявление цист лямблий в кале. Для этого требуется, как минимум, трехкратная сдача анализа, однако, поскольку цистовыделение происходит непостоянно, циклично, лямблии в кале обнаруживаются не всегда. В некоторых случаях информативнее оказывается исследование дуоденального содержимого, полученного путем зондирования.
В настоящее время широко используется серологическая диагностика лямблиоза у детей (ИФА), направленная на выявление специфических антител к антигенам лямблий в крови, а также высокочувствительное ПЦР-исследование кала и дуоденального содержимого.
В рамках обследования детям с лямблиозом могут быть рекомендованы дополнительные диагностические процедуры: УЗИ органов брюшной полости, анализ кала на дисбактериоз, копрограмма, биохимическое исследование крови.
Лечение лямблиоза у детей
Целевой установкой терапии лямблиоза у детей является полная эрадикация паразита и устранение клинических проявлений. При подтверждении диагноза лямблиоза у детей должно проводиться лечение всех членов семьи и домашних питомцев.
Проведению противолямблиозной терапии предшествует подготовительный этап, включающий соблюдение диеты и режима питания и устранение холестаза. Для повышения эффективности лечения лямблиоза у детей рекомендуется соблюдение диеты: употребление каш, отрубей, сухофруктов, печеных овощей и фруктов; снижение доли легкоусвояемых углеводов. С целью устранения эндогенной интоксикации рекомендуется прием энтеросорбентов; при синдроме мальдигестии и мальабсорбции назначаются ферменты на основе панкреатина. При лямблиозе у детей показан прием холекинетиков, проведение слепых тюбажей по Демьянову. При выявлении дисбактериоза проводится соответствующая коррекция микробного пейзажа кишечника.
Для проведения этиотропной терапии лямблиоза у детей используются противолямблиозные препараты группы нитроимидазолов (метронидазол, тинидазол, ниридазол, орнидазол) и производные нитрофуранов (фуразолидон, нифуратель). Выбор препарата, схему и длительность лечения лямблиоза у детей определяет детский гастроэнтеролог. На 2-3 день приема противопаразитарных препаратов у детей могут обостриться аллергические проявления, усилиться боли в животе, однако это не является поводом для прекращения лечения.
После завершения назначенного курса должно быть проведено повторное обследование ребенка на лямблиоз. При упорном течении лямблиоза у детей проводятся два цикла лечения разными препаратами.
Прогноз и профилактика лямблиоза у детей
При проведении полного курса терапии клинико-лабораторная ремиссия достигается у 92-95% детей. Тем не менее, нередки случаи реинфекции и рецидива лямблиоза у детей. После завершения лечения дети должны наблюдаться педиатром с проведением 2-3–кратного обследования на лямблиоз. При отрицательных лабораторных результатах, но возобновлении типичных симптомов лямблиоза ребенку необходимо провести противорецидивный курс лечения.
Профилактика лямблиоза у детей требует выявления и лечения бессимптомных паразитоносителей и цистовыделителей; привития детям гигиенических навыков; использования кипяченой воды для питья и мытья фруктов; проведения противоэпидемических мероприятий в детских учреждениях.
Этиология синдрома эндогенной интоксикации. СЭИ встречается при гнойно-воспалительных заболеваниях (перитонит, холецистит, панкреатит и др.), тяжелых травмах (краш-синдром), некоторых заболеваниях (сахарный диабет, тиреотоксический зоб), различных отравлениях и др.
Патогенез синдрома эндогенной интоксикации. Что может объединять данные нозологические формы, весьма далекие по этиологии? На определенном этапе заболевания, при стечении неблагоприятных факторов, это будет: 1. Токсемия, 2. Тканевая гипоксия и 3. Угнетение функции собственных детоксицируюших и защитных систем организма.
Основным звеном данного патологического каскада является токсемия (В. А. Остапенко, 1994).

Токсемия
Токсемию вызывает избыточное накопление в организме эндотоксинов. С. А. Симбирцев и Н. А. Беляков (1994) классифицируют эндотоксины по следующим группам:
• продукты естественного обмена в высоких концентрациях;
• активированные ферменты, способные повреждать ткани;
• медиаторы воспаления и другие биологически активные вещества (БАВ);
• класс среднемолекулярных веществ различной природы;
• перекисные продукты;
• неоднородные по составу ингредиенты нежизнеспособных тканей;
• агрессивные компоненты комплемента;
• бактериальные токсины (экзо- и эндотоксины).
Эндотоксины вызывают деструкцию белков и липидов клеток, блокируют синтетические и окислительные процессы. Особо следует акцентировать внимание на биологически активных веществах (БАВ) и средних молекулах (СМ).
Существуют четкие корреляции между концентрацией в крови и тканях продуктов калликреин-кининового каскада, биогенных аминов и степенью структурных поражений при многих острых процессах. Во всех случаях увеличение активности медиаторов воспаления сочетается с усилением тяжести поражений органов и систем (С. А. Симбирцев, Н. А. Беляков, 1994).
Эндотоксины оказывают прямое и опосредованное воздействие на структуру клеток, сами клетки, системы и органы (дистантное действие).
По действию на уровне клеточных структур эндотоксины можно классифицировать следующим образом (С. А. Симбирцев, Н. А. Беляков (1994):
• обладающие цитолитическим эффектом;
• активаторы лизосомальных ферментов;
• блокаторы митохондриальной энергетики;
• инициаторы свободнорадикальных процессов;
• ингибиторы рибосомального синтеза;
• способные к воздействию на различные клеточные образования.
Дистантное действие эндотоксинов выражается поражением системы микроциркуляции, которое наблюдается как в виде изолированных вне- и внутрисосудистых расстройств, так и комбинированных изменений. К внесосудистым изменениям относят нарушение регуляции тонуса периферических сосудов, среди внутрисосудистых изменений основное место отводят нарушениям реологического состояния крови, нарушениям транскапиллярного и трансмембранного обмена.
На уровне межорганных и межсистемных влияний (дистантное повреждение) действие эндотоксинов преломляется следующим образом (С. А. Симбирцев, Н. А. Беляков (1994):
• активаторы комплемента и белых клеток крови;
• активаторы калликреин-кининовой системы;
• активаторы коагуляции и фибринолизиса;
• вещества, изменяющие тонус гладкой мускулатуры;
• индукторы агрегации;
• воздействующие на проницаемость сосудистой стенки.
Это разделение на группы носит элемент условности, поскольку нет четкой границы между особенностями действия эндотоксинов, когда одни и те же вещества запускают каскадные реакции и повреждающий эффект тканевых структур осуществляется синерги-ческим влиянием с одномоментным включением защитных механизмов.
Заключение. Развитие процесса интоксикации можно представить как поступление эндотоксинов из мест образования (очаги воспаления, иммунная система, печень как источник синтеза патологических белков) в кровоток. Через кровь они попадают в органы фиксации и биотрансформации (печень, иммунная система, легкие), органы выделения патологических субстанций (печень, почки, ЖКТ, легкие, кожа), а также в органы и ткани депонирования патологических субстанций (жировая, нервная, костная ткань, органы эндокринной системы, лимфоидная ткань). При различных патологических состояниях, когда количество естественных продуктов жизнедеятельности организма, появившихся в больших количествах в биологических средах, а также заведомо агрессивные компоненты превышают возможности их биотрансформации, развивается СЭИ (К. Я. Гуревич, А. Л. Костюченко, 1994).
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

