Сироп для детей от вич мамы
Обновлено: 15.04.2024
Разумеется! При приеме антиретровирусных (АРВ) препаратов можно зачать, выносить и родить здорового ребенка — риск передачи ему ВИЧ будет минимальным. Это справедливо и для дискордантных пар (когда только один из партнеров живет с ВИЧ), и для случаев, когда оба партнера ВИЧ-положительные. Ключевой момент — правильно принимать АРВ-терапию и добиться неопределяемой вирусной нагрузки у матери, а также применять другие профилактические меры. Без специальной профилактики риск передачи ВИЧ от матери ребенку составляет 20–40 %, а по некоторым данным, даже до 80 %, но профилактические меры снижают его до 1–2 %.
Как ВИЧ может передаваться от матери к ребенку?
Вирус может передаваться через кровь, влагалищный секрет и грудное молоко. Риск внутриутробной передачи возрастает на поздних сроках беременности и особенно во время родов. При прохождении по родовым путям матери ребенок непосредственно контактирует с ее кровью и влагалищным отделяемым, из которых вирус через микротравмы на коже ребенка может проникнуть в его организм.
ВИЧ плохо проникает через плацентарный барьер и редко передается на ранних сроках беременности. Поэтому, даже если в момент зачатия женщина не принимала АРВТ и имела высокую вирусную нагрузку, это совсем не значит, что ребенок будет инфицирован. Но очень важно начать принимать антиретровирусные препараты как можно раньше, чтобы к поздним срокам беременности и родам добиться неопределяемой вирусной нагрузки. А от грудного вскармливания нужно будет отказаться полностью, даже при приеме АРВТ.
ВИЧ может передаваться от отца?
Новорожденному ребенку ВИЧ может передаваться только от матери при родах, грудном вскармливании или во время беременности. Если на момент зачатия отец ребенка имел ВИЧ-положительный статус, но мать при этом остается ВИЧ-отрицательной, для ребенка риск передачи вируса отсутствует. Однако, если заражение матери в момент зачатия произошло и ВИЧ-инфекция начинает развиваться вместе с беременностью, это может увеличить риск передачи вируса ребенку. На ранних этапах развития ВИЧ-инфекции вирусная нагрузка у матери может быть очень высокой — именно это и увеличивает риск передачи вируса ребенку.
Если женщина имела незащищенный секс с ВИЧ-положительным человеком, нужно обязательно провести курс постконтактной профилактики (ПКП) вне зависимости от наступления беременности.
Что нужно учитывать при зачатии людям, живущим с ВИЧ?
Если оба партнера имеют ВИЧ-положительный статус, принимают АРВ-терапию и имеют неопределяемую вирусную нагрузку, обычно прибегают к зачатию естественным путем. При этом остается потенциальный риск передачи резистентного штамма от одного партнера другому. Чтобы его полностью исключить, можно прибегнуть к рекомендациям для дискордантных пар (см. ниже).
Для дискордантных пар, когда ВИЧ-положительный статус есть только у одного партнера, есть особые рекомендации.
Если мать ВИЧ-отрицательная, а отец ВИЧ-положительный
При прочих равных условиях риски ВИЧ-инфекции для принимающего партнера всегда выше. И в этом случае зачатие будет нести риск инфицирования для матери. Устойчивое подавление вирусной нагрузки у отца — обязательное условие для зачатия ребенка. Помимо этого, риск заражения матери можно снизить следующими способами (способы перечислены в порядке увеличения надежности):
Практиковать незащищенный секс только в дни овуляции. Такой подход повышает вероятность зачатия и снижает число сексуальных контактов, которые для этого нужны. А со снижением числа незащищенных контактов снижается и риск инфицирования. При этом важно, чтобы у партнеров не было других заболеваний половой сферы (например, ИППП, эрозии шейки матки и т.д.), так как они повышают риск передачи ВИЧ. Очень важно продолжить использование презервативов уже после зачатия — некоторые пары, практикуя незащищенный секс для зачатия, продолжают так и после, что может привести к заражению ВИЧ-отрицательного партнера в будущем. Этот способ зачатия несет самый высокий потенциальный риск заражения для женщины, и нужно очень тщательно обдумать готовность партнеров к таким рискам.
Искусственная инсеминация. В этом случае предварительно собранную сперму вводят во влагалище шприцем (без иглы), также в дни овуляции. При этом риск инфицирования немного снижается: нет вагинального секса — нет микротравм слизистой оболочки влагалища, через которые в организм проникают вирусные частицы. Однако этот способ также нельзя назвать надежным для защиты партнера от инфицирования.
При использовании любого из этих способов следует помнить, что на 100 % исключить потенциальный риск заражения женщины невозможно. А первые два способа несут довольно высокие риски, и прибегать к ним стоит только в крайнем случае, тщательно обдумав свое решение.
Если мать ВИЧ-положительная, а отец ВИЧ-отрицательный
В этом случае самый простой и при этом безопасный способ — введение спермы во влагалище с помощью обычного пластикового шприца (без иглы). Сперму можно собрать, используя презерватив (без спермицидной смазки!) или чистый пластиковый контейнер для биоматериала. Собранную сперму вводят шприцем глубоко во влагалище в дни овуляции. Риск заражения для отца при этом полностью отсутствует.
Опасна ли беременность при ВИЧ-положительном статусе для матери?
К настоящему времени нет никаких данных о том, что беременность ухудшает или ускоряет развитие ВИЧ-инфекции, или протекает тяжелее при ВИЧ-положительном статусе матери. Важно подобрать и правильно принимать адекватную АРВ-терапию, и течение беременности почти ничем не будет отличаться от беременности при ВИЧ-отрицательном статусе.
Насколько безопасна АРВТ при беременности?
К сожалению, абсолютно безопасных лекарств не бывает. И при назначении любого препарата врач всегда исходит из соотношения потенциального риска и потенциальной пользы. Когда речь идет о предотвращении передачи ВИЧ-инфекции, потенциальная польза, безусловно, перевешивает. Терапия современными антиретровирусными препаратами имеет очень хороший профиль безопасности как для матери, так и для ребенка. Если вы сомневаетесь, стоит ли начинать АРВТ при беременности, боитесь побочных эффектов терапии или ее негативного влияния на ребенка, помните, что на другой чаше весов при этом лежит высокий риск передать ВИЧ-инфекцию ребенку — а это многократно опаснее побочных эффектов терапии.
Не все антиретровирусные препараты можно назначать беременным. Хорошая новость в том, что после многочисленных клинических исследований для многих АРВ-препаратов была доказана их безопасность при беременности — они не влияют на рост и развитие ребенка и не угрожают нормальному течению беременности. Именно такие препараты и используются в схемах терапии при беременности. Конкретную схему всегда подбирает врач, учитывая другие особенности состояния здоровья матери и течения беременности.
Опасными для ребенка могут быть не только АРВ-препараты сами по себе, но и побочные реакции на терапию у матери, особенно в случае тяжелых побочных реакций или непереносимости препарата. Это становится особенно важным при начале терапии уже в период беременности — когда еще неизвестно, как именно организм матери отреагирует на новые лекарства. В это время важно тщательно следить за своим состоянием, регулярно сдавать назначенные анализы и посещать врача.
Современная АРВ-терапия не вредит течению беременности и развитию ребенка и предотвращает передачу вируса от матери, поэтому очень важна для рождения здорового ребенка.
Когда нужно начинать АРВТ?
Если до начала беременности женщина не принимала АРВТ, ее обычно начинают на 13–14 неделях беременности. К этому моменту заканчивается формирование основных органов у плода, и риски влияния АРВ-препаратов на развитие ребенка становятся минимальными. Однако, если у матери очень низкий уровень CD4-клеток (менее 350/мкл) или очень высокая вирусная нагрузка (более 100 тыс. копий на мл), терапию начинают незамедлительно. При низком уровне CD4-клеток существенно повышается риск развития опасных оппортунистических инфекций, которые сами по себе будут серьезной угрозой для беременности и ребенка. А очень высокая вирусная нагрузка у матери повышает риск передачи вируса ребенку.
Затягивать начало терапии позже 14-й недели опасно. Чтобы защитить ребенка от ВИЧ-инфекции, к моменту родов нужно добиться устойчиво низкой вирусной нагрузки у матери. После начала терапии вирусная нагрузка снижается постепенно, поэтому, начиная терапию позже 14-й недели, можно не успеть добиться неопределяемой нагрузки к моменту родов.
Если своевременно начать терапию не удалось, это стоит сделать в любом случае, как только появится такая возможность, даже на поздних сроках беременности, даже когда начались схватки. Любое снижение вирусной нагрузки все равно снизит риск передачи инфекции ребенку и будет полезным.
Нужно ли корректировать схему терапии при беременности, если я уже ее принимаю?
Если вы уже принимаете антиретровирусные препараты и планируете беременность, обязательно обсудите это с врачом. Не все антиретровирусные препараты можно принимать беременным, поэтому в некоторых случаях врач предложит поменять схему. Может оказаться, что ваша схема уже состоит из препаратов, разрешенных при беременности, тогда менять ничего не придется.
Если схему все же нужно поменять, безопаснее всего будет сначала убедиться в том, что новая схема хорошо переносится и дает устойчивое подавление вирусной нагрузки, и после этого планировать беременность. Обычно это становится понятно в течение 1–3 месяцев после начала приема новой схемы.
Если беременность обнаружили уже на фоне приема АРВТ и на сроке больше 1-го триместра, менять схему большого смысла нет.
Какая схема АРВТ самая лучшая?
Какой-то одной идеальной схемы терапии для всех беременных не существует. Врач подбирает схему индивидуально, учитывая особенности здоровья каждой женщины.
Основой схемы АРВТ для беременных чаще всего становится зидовудин, так как его применение при беременности изучено лучше всего и накоплен большой практический опыт.
В качестве терапии первой линии обычно назначают следующие комбинации: зидовудин (или абакавир, или тенофовир) + ламивудин (или эмтрицитабин) + лапинавир/ритонавир (или атазанавир/ритонавир или эфавиренц).
В некоторых случаях возможно применение альтернативных схем, включающих невирапин, фосфазид, дарунавир, саквинавир. Вне зависимости от конкретной комбинации в схеме обязательно используют не менее трех антиретровирусных препаратов. При позднем начале терапии и/или очень высокой вирусной нагрузке врач может добавить ралтегравир как дополнительный компонент.
Некоторые препараты, наоборот, стараются для беременных не применять или назначают с ограничениями. Например, эфавиренз нежелательно использовать до 8–9 недели беременности — есть данные о его негативном влиянии на формирование нервной трубки у плода. Также лучше не назначать диданозин и ставудин или сразу три препарата из группы нуклеозидных ингибиторов обратной транскриптазы (НИОТ) — это повышает риск развития лактацидоза. Не рекомендуется применять индинавир из-за риска развития мочекаменной болезни и повышения уровня билирубина.
Какую бы схему терапии не применяли при беременности, во время родов или при кесаревом сечении обязательно внутривенно вводят зидовудин.
Какие анализы нужно сдавать во время беременности?
Каких-то специальных анализов для ВИЧ-положительных беременных нет. Проводят все обычные исследования как при беременности у ВИЧ-отрицательных женщин, а также стандартное определение вирусной нагрузки и уровня CD4-клеток, на которые регулярно тестируют всех ВИЧ-положительных людей.
Однако при беременности регулярно контролировать вирусную нагрузку особенно важно — ведь ее повышение при неэффективной АРВТ создает прямую угрозу передачи вируса ребенку. Поэтому, чем раньше будет обнаружен рост вирусной нагрузки и скорректирована схема терапии, тем ниже потенциальный риск передачи вируса ребенку. Также важно контролировать некоторые биохимические показатели крови: уровень глюкозы, уровень билирубина, активность ферментов печени, уровень молочной кислоты и так далее. Конкретный набор показателей зависит от назначенной схемы терапии и определяется врачом. Если у беременной начнет развиваться какой-то опасный побочный эффект АРВ-терапии, биохимический контроль позволит обнаружить его на раннем этапе и скорректировать схему АРВТ, пока он не начал угрожать течению беременности или развитию ребенка.
Некоторые исследования могут повышать риск передачи ВИЧ от матери к плоду, и их не стоит делать ВИЧ-положительным беременным. Например, амниоцентез, кордоцентез, биопсия ворсин хориона и другие инвазивные исследования.
Можно перестать принимать терапию после родов?
Лишь в некоторых случаях, когда доступ к антиретровирусным препаратам сильно ограничен, терапию можно назначить только на период беременности и родов и затем отменить, если уровень CD-4 клеток у материи более 500/мм3. Но это — исключительные случаи, прерывание терапии всегда несет риск развития резистентности.
Самой рожать или кесарево?
Если к моменту родов неопределяемой вирусной нагрузки достичь не удалось или АРВТ не проводилась вообще, риск передачи ВИЧ-инфекции можно снизить, сделав кесарево сечение. В этом случае ребенок не будет проходить по родовым путям и контактировать с кровью матери, что значительно снижает риски заражения. Важно, чтобы кесарево сечение было плановым, то есть проводилось до начала отхождения околоплодных вод. Если воды уже отошли, проведение кесарева сечения значимо не снизит риск передачи вируса ребенку.
Если во время беременности удалось достичь неопределяемой вирусной нагрузки или снизить ее до уровня менее 1000 копий/мл, можно рожать естественным путем. То есть в этом случае ВИЧ-положительный статус матери никак не влияет на выбор между естественными родами или кесаревым сечением.
Нужна ли какая-то профилактика для ребенка?
Детям, рожденным от ВИЧ-положительных матерей, независимо от вирусной нагрузки матери на момент родов, обычно назначают профилактический прием антиретровирусных препаратов в течение нескольких недель. Терапию начинают сразу после родов, схема и дозировка подбирается врачом индивидуально. Чаще всего используют зидовудин в форме сиропа в течение 28 дней.
Если есть дополнительные риски, например мать не принимала АРВТ во время беременности или на момент родов была очень высокая вирусная нагрузка, то дополнительно к зидовудину обычно назначают невирапин и ламивудин.
Грудью вообще нельзя кормить?
Категорически — нет. Грудное вскармливание должно быть полностью исключено. ВИЧ содержится в грудном молоке, а также может передаваться ребенку через микротравмы и трещины на сосках. Прикладывать ребенка нельзя и к пустой груди — даже когда молока нет, риск передачи вируса через микротрещины соска остается. Кормить сцеженным молоком тоже нельзя.
Если ВИЧ-инфекция у матери обнаружена уже в период грудного вскармливания, его нужно прекратить. Ребенку назначают профилактический курс антиретровирусных препаратов и проводят анализы на ВИЧ-инфекцию.
Почему нельзя кормить грудью, если принимаешь АРВТ?
Нулевая вирусная нагрузка при приеме АРВТ в крови не гарантирует полного отсутствия вируса в грудном молоке. Поэтому потенциальный риск передачи вируса с грудным молоком остается даже при приеме терапии. Кроме этого, многие антиретровирусные препараты и продукты их метаболизма выделяются с грудным молоком и могут быть вредны для ребенка. Даже если мать принимает препараты, разрешенные для применения у детей, их концентрация в молоке может оказаться опасно высокой для ребенка.
Когда можно точно узнать, что ВИЧ-инфекция не передалась ребенку?
Отрицательный результат ПЦР на второй день после родов говорит о том, что ребенок НЕ заразился во время беременности. Отрицательная ПЦР через месяц указывает на то, что ребенок, скорее всего, НЕ заразился и во время родов. Отрицательная ПЦР в возрасте старше 4 месяцев говорит о том, что ребенок практически наверняка НЕ заразился ВИЧ. Окончательное подтверждение этого дает отрицательный результат ИФА в 1,5 года.
Положительный результат любой ПЦР указывает на возможное заражение ребенка ВИЧ. В этом случае проводят дополнительные исследования для окончательного подтверждения диагноза. Если ВИЧ все же передался ребенку, ему назначают АРВ-терапию, которая позволит прожить долгую полноценную жизнь и иметь собственных детей в будущем.
Oдним из первых препаратов, использованных для лечения ВИЧ-инфекции, был азидотимидин (АЗТ). У нас он выпускался под названием тимозид, на Западе известен как ретровир, зидовудин (ЗДВ). Суточная доза определяется стадией инфекции и переносимостью препара
Oдним из первых препаратов, использованных для лечения ВИЧ-инфекции, был азидотимидин (АЗТ). У нас он выпускался под названием тимозид, на Западе известен как ретровир, зидовудин (ЗДВ). Суточная доза определяется стадией инфекции и переносимостью препарата. Препарат относится к ингибиторам обратной траскриптазы.
Препаратами второго поколения являются дидеоксииназин (ДДИ), дидеоксицитидин (ДДС). В настоящее время спектр препаратов этой группы значительно расширился (ставудин-ДДТ, хивид, фосфозид и другие).
Эта группа лекарственных средств (ЛС) имеет ряд существенных недостатков. Указанные ЛС не подавляют полностью репликацию вируса, который может быть выделен у большинства больных во время терапии.
Как показали исследования, к ЗДВ достаточно быстро развивается устойчивость, в особенности на поздних стадиях болезни с усиленной репликацией ВИЧ, когда, по-видимому, возникает резистентность и к другим аналогам нуклеозидов.
Обычный фактор, существенно ограничивающий применение ЛС этой группы, — их токсичность. Для ЗДВ характерно главным образом токсическое действие на костный мозг, тогда как ДДИ и ДДС обладают нейротоксическим действием. Кроме того, ДДИ может вызывать тяжелый острый геморрагический панкреатит.
Установлена тесная связь между клинической неэффективностью ЗДВ и резистентностью к нему in vitro.
Вторая группа препаратов, открытая сравнительно недавно и уже широко используемая, — это ингибиторы протеаз: индиновир (криксиван), инвираза (саквиновир), вирасепт (нельфиновир) и другие.
В настоящее время речь не идет уже о монотерапии антиретровирусными средствами, а только о ди-, три- и даже тетратерапии. Такие методики позволяют снижать концентрацию вируса до величин, не определяемых с помощью современных тест-систем (< 200 копий/1 мл).
Предпочтительность комбинированной терапии обосновывается следующими положениями (В. В. Покровский).
- Использование многих этиотропных агентов более эффективно подавляет жизнедеятельность вируса, воздействуя на различные болевые точки или синергически воздействуя на одну из них.
- Это позволяет снизить дозы препаратов, что уменьшает частоту и выраженность побочных эффектов.
- Различные лекарства имеют различную способность проникать в ткани (головной мозг и т. д.).
- Комбинация лекарств затрудняет формирование устойчивости, или она появляется позднее.
Все описанные выше подходы к терапии ВИЧ-инфекции предполагали непосредственное воздействие на репликацию вируса. Другая возможная методика лечения ВИЧ-инфекции состоит в усилении защитных сил макроорганизма. Некоторые варианты такого подхода в большинстве случаев неспецифические, изредка специфические и могут воздействовать на защитные свойства клетки-хозяина.
Интерфероны, как природные, так и рекомбинантные, имеют ряд недостатков: антигенность, необходимость многократного введения для поддержания достаточной концентрации в организме, большое количество побочных эффектов и т. д.
Этих недостатков лишены многие индукторы эндогенного интерферона, некоторые из них способны включаться в синтез ИФН в некоторых популяциях клеток, что в ряде случаев имеет определенное преимущество перед поликлональной стимуляцией иммуноцитов интерфероном.
Специфическая активность циклоферона при ВИЧ-инфекции изучена в 1997 году в Институте гриппа РАМН
- Выявлена выраженная ингибирующая активность циклоферона на репродукцию ВИЧ в культуре клеток моноцитов.
- По показателям ингибирующей активности циклоферон значительно превосходит азидотимидин.
- Представленные экспериментальные данные обосновывают клиническое использование циклоферона для лечения больных ВИЧ-инфекцией.
Пятилетний опыт применения циклоферона у ВИЧ-инфицированных позволяет оценить результаты этой работы.
В период 1992 – 1997 годы в Санкт-петербургском городском центре по профилактике и борьбе со СПИД циклоферон получили 40 пациентов с разными стадиями ВИЧ-инфекции. Следует отметить, что 11 больных прошли два курса терапии циклофероном, в связи с чем общее число лиц, получивших один курс лечения циклофероном, составило 29 человек. В основном это были молодые люди в возрасте до 40 лет (20 человек), в том числе трое детей до 14 лет.
Все больные отмечали хорошую переносимость циклоферона, отсутствие пирогенных реакций после его введения.
Пациенты также констатировали улучшение общего состояния, сна и аппетита, повышение жизненного тонуса, работоспособности. 30% из числа получавших препарат и перенесших в осенне-зимний период грипп или ОРВИ отметили, что заболевание протекало непривычно легко и выздоровление наступило быстрее обычного.
Из клинической практики
После курса циклоферона отмечалось существенное снижение вирусной нагрузки (в 3,6 раза). Число CD4+ возросло на 62%. Монотерапия циклофероном оказала положительное стабильное влияние на изученные показатели у пациентов.
Определенный интерес представляют результаты многолетнего наблюдения больных ВИЧ-инфекцией, которые получали длительно циклоферон в своеобразном профилактическом режиме с целью стабилизации процесса и профилактики прогрессирования заболеваний.
В 1998 году на базе Российского научно-методического Центра по профилактике и борьбе со СПИД (руководитель член-корр. АМН В. В. Покровский) была изучена динамика суррогатных маркеров ВИЧ-инфекций (уровень CD4+) и вирусная нагрузка у больных ВИЧ-инфекцией при лечении циклофероном.
Оценка достоверности полученных результатов проводилась с помощью непараметрических критериев (критерий знаков, максимум-критерий, критерий Вилкоксона для сопряженных совокупностей).
В испытуемую группу вошли 10 взрослых больных ВИЧ-инфекцией в стадии первичных проявлений по Российской классификации ВИЧ-инфекции (В. И. Покровский, 1989 г.). Результаты исследования уровня CD4-лимфоцитов представлены в таблице и на рисунке, из которых видно, что после первых четырех недель исследования наметилась тенденция к повышению среднего уровня CD4-лимфоцитов, которое к 12-й неделе стало статистически достоверным. Это повышение сохранилось до конца исследования, несмотря на
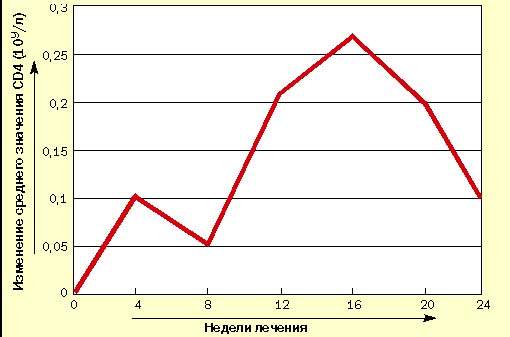 |
| Рисунок 1. Изменение уровня CD4-лимфоцитов у больных ВИЧ-инфекцией при лечении циклофероном (в сравнении с исходным уровнем) |
 |
| Рисунок 2. Средние значения изменения концентрации РНК ВИЧ (log10/мл) |
Таким образом, применение циклоферона в терапии ВИЧ-инфекций сопровождается стабилизацией клинических проявлений заболевания, улучшением состояния, а также гематологических и иммунологических показателей больных.
Циклоферон как монопрепарат оказывает иммуномодулирующее и противовирусное действие при лечении ВИЧ-инфицированных (стадии А1 3Б) в тех случаях, когда нет значительного снижения числа CD4+ клеток (<200). Хорошо зарекомендовало себя назначение циклоферона по следующей схеме.
- По 4 мл препарата в 1, 2, 4, 6, 8, 10, 13, 16, 19 и 22-й дни лечения (у детей по 2 мл). Первые две инъекции могут вводиться внутривенно, остальные внутримышечно. Повторные курсы циклоферона рекомендуется проводить через 6 месяцев под иммунологическим контролем.
- Циклоферон хорошо сочетается со всеми основными лекарственными средствами, его рекомендуется использовать в случае, когда имеются признаки активной репликации ВИЧ (высокие показатели вирусной нагрузки), у больных с обострениями различных оппортунистических заболеваний.
Исчезновение у некоторых больных иммунологических и вирусологических показаний для проведения противоретровирусной терапии может иметь важное значение для разработки новых подходов к проведению лечения больных ВИЧ-инфекцией, для снижения стоимости терапии и отсрочки развития резистентности к ней или преодолению последней.
Циклоферон может оказаться перспективным профилактическим средством при сомнительных контактах и контактах с заведомо ВИЧ-инфицированными партнерами.
В настоящее время ВИЧ-инфекция у детей является одной из актуальнейших проблем во всем мире.
В настоящее время ВИЧ-инфекция у детей является одной из актуальнейших проблем во всем мире. Первоначально в нашей стране она была обусловлена внутрибольничной заболеваемостью, а в последние годы — рождением детей ВИЧ-инфицированными женщинами. Более 90% детской ВИЧ-инфекции является результатом именно перинатальной трансмиссии вируса.
По данным МГЦ СПИД за последние 10 лет произошло уменьшение числа детей с врожденной ВИЧ-инфекцией. Так, если в 2001 году, когда химиопрофилактика вертикальной трансмиссии ВИЧ-инфекции только начинала проводиться, число ВИЧ-инфицированных детей составляло 8%, то в 2006 году — всего 1,5%. Таких результатов удалось добиться благодаря введению в практику схемы профилактики согласно протоколу от 1996 г. PACTG 076 (Pediatric AIDS Clinical Trial Group), который основан на назначении беременной женщине Азидотимидина — антиретровирусного препарата из группы нуклеозидных ингибиторов обратной транскриптазы.
Однако даже своевременное проведение химиопрофилактики не исключает полностью возможность перинатальной передачи ВИЧ-инфекции от матери плоду.
К факторам, повышающим риск передачи ВИЧ от матери к ребенку, относятся:
родоразрешение через естественные родовые пути (при вирусной нагрузке более 1000 копий/мл перед родами);
При отсутствии профилактики перинатальной передачи ВИЧ, риск заражения составляет 30–40% [3].
Причинами отсутствия химиопрофилактики во время беременности и родов могут быть: диагностика ВИЧ-инфекции только во время родов, употребление наркотических веществ во время беременности, добровольный отказ от профилактики, в т. ч. по религиозным убеждениям, беременность до внедрения в практику профилактики вертикальной передачи ВИЧ и домашние роды.
Особенности клинических проявлений ВИЧ-инфекции у детей определяются стадией онтогенеза, на которой произошло инфицирование плода ВИЧ в организм (внутриутробно или интранатально) и от возраста ребенка в случае постнатального заражения.
При заражении плода в позднем перинатальном периоде или ребенка после рождения течение ВИЧ-инфекции почти не отличается от взрослых.
Целью данной работы является оценка эффективности общей и высокоактивной антиретровирусной терапии (ВААРТ) у детей с врожденной ВИЧ-инфекцией.
Задачи
Нами проанализированы 60 случаев врожденной ВИЧ-инфекции у детей в возрасте от 1 месяца до 7 лет, в т. ч.: 30 амбулаторных карт детей, состоящих на диспансерном учете в московском городском центре СПИД (МГЦ СПИД); 30 историй болезни детей, находящихся на стационарном лечении в МГЦ СПИД.
По результатам анализа амбулаторных карт и историй болезни нами были выявлены следующие наиболее часто встречающиеся клинические проявления врожденной ВИЧ-инфекции у детей: поражение ЦНС, лимфаденопатия, гепатолиенальный синдром, интерстициальные изменения в легких, анемия, гипотрофия, недоношенность.
Поражение ЦНС в нашем исследовании наблюдалось у 75% детей. Установлено, что ВИЧ является не только иммунотропным, но и нейротропным вирусом и проникает через гематоэнцефалический барьер на ранних этапах инфекционного процесса в организме, поражая олигодендроциты и астроциты, нейроциты, микроглию, макрофаги, клетки эндотелия кровеносных сосудов, фибробластоподобные клетки мозга. Указанные клетки имеют рецептор CD4 и считаются прямыми клетками-мишенями для ВИЧ. Патоморфологические изменения головного мозга при ВИЧ-инфекции могут быть охарактеризованы как альтернативно-дистрофические, с периваскулярным отеком, дистрофией нейронов, очаговой демиелинизацией и циркуляторными нарушениями.
У обследованных нами ВИЧ-инфицированных детей наблюдался полиморфизм клинических неврологических проявлений.
В начале заболевания отмечались астеноневротический и цереброастенический синдромы. Для этой стадии СПИДа характерной была ВИЧ-энцефалопатия. Также было установлено, что тяжесть поражения нервной системы более выражена у детей первого года жизни.
ВИЧ-энцефалопатия — тяжелое заболевание, затрагивающее все функции ЦНС. При подострой прогрессирующей энцефалопатии утрачиваются ранее приобретенные умения и навыки. Вялотекущая прогрессирующая энцефалопатия замедляет или прекращает формирование новых навыков, не затрагивая при этом старых. Обе формы прогрессирующей энцефалопатии резко замедляют психомоторное развитие. Дети с непрогрессирующей энцефалопатией продолжают приобретать новые навыки, но медленнее, чем здоровые сверстники.
Одновременно поражение ЦНС проявлялось грубой задержкой психомоторного развития, синдромом гипервозбудимости и гидроцефальным синдромом.
Клиническая манифестация ВИЧ-инфекции у детей разнообразна и зачастую неспецифична. Нами установлено, что лимфаденопатия, ассоциированная с гепатоспленомегалией, является одним из наиболее ранних признаков врожденной ВИЧ-инфекции. Так, персистирующая генерализованная лимфаденопатия выявлена в 64% случаев, а гепатолиенальный синдром — в 38% случаев. Сочетание обоих синдромов наблюдалось у 36% детей.
Интерстициальные изменения в легких были у 25% детей, они развивались в результате многократно перенесенных ранее пневмоний различной этиологии.
Гипотрофия (от I до III степени) была выявлена у 18% больных, недоношенность отмечалась в 14% случаев.
Из сопутствующих заболеваний чаще встречались хронический вирусный гепатит С и туберкулез, а из оппортунистических заболеваний — грибковые поражения кожи и слизистых, пневмоцистная пневмония, герпетическая инфекция, цитомегаловирусная инфекция.
Грибковые поражения кожи и слизистых отмечались у 38% детей.
Наиболее частая этиология — грибы рода Candida.
Чаще всего наблюдался оральный кандидоз, которому сопутствовал ангулярный хейлит, когда в углах рта возникали мацерации, эрозии, трещины. По краям трещин иногда отмечался гиперкератоз. Для детей, больных ВИЧ/СПИДом, характерно рецидивирующее течение орофарингеального кандидоза. В зависимости от степени иммунодефицита (определяется по количеству CD4-лимфоциов), было отмечено возникновение рецидивов через несколько месяцев, недель, а иногда и дней после отмены антимикотической терапии. Продолжительность периодов ремиссии была индивидуальна у каждого больного.
Наиболее опасная оппортунистическая инфекция, пневмоцистная пневмония, наблюдалась у 26% детей. Пневмоцистная пневмония может развиться в любом возрасте, но у наблюдавшихся нами больных почти в половине случаев приходилась на первые 6 месяцев жизни.
Обычно она развивалась остро, проявляясь одышкой и кашлем. Однако в некоторых случаях сначала появлялся кашель, и в течение нескольких дней к нему присоединялось постепенно нарастающее тахипноэ. Вначале появлялось навязчивое покашливание, затем кашель становился коклюшеподобным, особенно в ночное время. У ребенка отмечалась прогрессирующая слабость, снижение аппетита, бледность кожного покрова, цианоз носогубного треугольника. Температура тела в начале заболевания была нормальной или субфебрильной [1, 5].
При физикальном исследовании выявлялись тахипноэ, одышка, влажные и сухие хрипы. При прогрессировании пневмонии, возможно, возникала легочно-сердечная недостаточность.
Диагноз пневмоцистной пневмонии был основан на обнаружении возбудителя в мокроте, в материале, полученном при бронхоальвеолярном лаваже или биопсии легкого. У большинства детей пневмоцистная пневмония сочеталась с другими оппортунистическими заболеваниями.
У ВИЧ-инфицированных детей могут наблюдаться различные поражения кожи.
В 8% случаев была выявлена инфекция кожного покрова, обусловленная вирусом Varicella-Zoster. На фоне иммунодефицита наблюдалось тяжелое генерализованное течение инфекции с полиорганными поражениями.
Цитомегаловирусная инфекция отмечалась у 7% детей. Клинически манифестация заболевания сопровождалась разнообразной симптоматикой — от сиалоаденита и лимфаденита до тяжелых диссеминированных форм.
Хронический вирусный гепатит С был выявлен у 16% детей и обусловлен вертикальной трансмиссией вируса от матери плоду.
Туберкулез отмечался в 5% случаев. Случаи заболевания были обусловлены трансплацентарным путем инфицирования.
Диагностика врожденной ВИЧ-инфекции
Диагноз ВИЧ-инфекции у ребенка может быть установлен при получении двух положительных результатов ПЦР в двух образцах крови, взятых в разные дни. ПЦР-диагностика проводится: в первые 48 часов жизни, в 14 дней жизни, в 1–2 месяца, в 3–6 месяцев [5].
ВИЧ-инфекцию можно исключить: при 2 и более отрицательных результатах ПЦР на ВИЧ (один в возрасте до 1 месяца, один — старше 4 месяцев); при 2 и более отрицательных серологических тестах на антитела к ВИЧ в возрасте старше 6 месяцев при отсутствии грудного вскармливания.
На основании приказа Минздрава РФ № 606 от 19.12.2003 г., ребенок может быть снят с диспансерного учета по ВИЧ-инфекции в возрасте 18 месяцев при отрицательном результате исследования на антитела к ВИЧ методом ИФА, отсутствии гипогаммаглобулинемии, отсутствии клинических проявлений ВИЧ-инфекции.
Лечение
Основным компонентом лечения больных ВИЧ-инфекцией является антиретровирусная терапия, с помощью которой можно добиться контролируемого течения заболевания, то есть состояния, при котором удается остановить прогрессирование болезни. Антиретровирусная терапия должна проводиться пожизненно, непрерывно. В процессе лечения проводятся обследования, цель которых — контроль его эффективности и безопасности. В плановом порядке эти обследования проводятся через 4 и 12 недель после начала лечения, впоследствии — каждые 12 недель.
Лекарственная терапия ВИЧ-инфекции включает в себя базисную терапию (которая определяется стадией заболевания и уровнем CD4-лимфоцитов), а также терапию вторичных и сопутствующих заболеваний [2].
В настоящее время придерживаются рекомендаций, разработанных Рабочей группой по антиретровирусной терапии и лечению ВИЧ-инфекции у детей (создана Национальным центром ресурсов Центра Франсуа-Ксавье Банью, Медицинским и стоматологическим университетом Нью-Джерси (UMDNJ), Управлением ресурсов и служб здравоохранения (HRSA) и Национальным институтом здравоохранения (NIH) США), согласно которым всех ВИЧ-инфицированных детей разделяют на 3 возрастных группы (до 12 месяцев, от 1 года до 5 лет и 5 лет и старше) [5].
Детям до 12 месяцев рекомендуется начинать антиретровирусную терапию, независимо от клинических проявлений, количества CD4-лимфоцитов и уровня вирусной нагрузки.
Детям от 1 года до 5 лет и старше 5 лет проведение антиретровирусной терапии рекомендуется:
при наличии СПИДа или наличии симптомов, соответствующих стадии С и большей части симптомов стадии B (по классификации CDC, 1994 г.), независимо от количества CD4-лимфоцитов и уровня вирусной нагрузки;
детям в возрасте 1 год и старше, которые находятся на стадиях N, A или имеют следующие симптомы стадии В: единственный эпизод тяжелой бактериальной инфекции или лимфоидную интерстициальную пневмонию при уровне CD4-лимфоцитов ≥ 25% у детей от 1 года до 5 лет или уровне CD4-лимфоцитов ≥ 350 клеток/мм3 у детей > 5 лет и уровне вирусной нагрузки ≥ 100 000 копий/мл.
Антиретровирусную терапию можно временно не назначать детям, у которых нет клинических проявлений ВИЧ-инфекции или они слабо выражены, при уровне CD4-лимфоцитов ≥ 25% у детей от 1 года до 5 лет или уровне CD4-лимфоцитов ≥ 350 клеток/мм3 у детей > 5 лет и уровне вирусной нагрузки < 100 000 копий/мл.
ВААРТ назначается ребенку пожизненно.
Терапия проводится не менее чем тремя препаратами с режимом приема 2–3 раза в день.
Применяются следующие группы антиретровирусных препаратов:
Препараты, блокирующие процесс обратной транскрипции (синтез вирусной ДНК на матрице вирусной РНК), — ингибиторы обратной транскриптазы. Среди них выделяют две группы препаратов:
нуклеозидные ингибиторы обратной транскриптазы (НИОТ) (измененные молекулы нуклеозидов), встраивающиеся в синтезируемую цепочку ДНК и прекращающие ее дальнейшую сборку: зидовудин (Азидотимидин)**, фосфазид*, ставудин*, диданозин**, зальцитабин*, ламивудин**, абакавир*, Комбивир (ламивудин + зидовудин);
ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ), блокирующие необходимый для осуществления обратной транскрипции вирусный фермент — обратную транскриптазу: эфавиренз*, невирапин**.
Препараты, блокирующие процесс формирования полноценных протеинов ВИЧ и, в конечном итоге, сборку новых вирусов — ингибиторы протеазы (ИП) ВИЧ: саквинавир, индинавир, нелфинавир**, ритонавир*, лопинавир/ритонавир**.
Препараты, воздействующие на рецепторы, используемые вирусом для проникновения ВИЧ в клетку хозяина, — ингибиторы слияния.
При выборе оптимальной схемы терапии для конкретного больного принимается во внимание: эффективность и токсичность препаратов, возможность их сочетания между собой, переносимость препаратов пациентом, удобство приема препаратов — кратность приема, сочетание антиретровирусных препаратов с препаратами, которые применяются (или, возможно, будут применяться) для лечения имеющихся у пациента вторичных и сопутствующих заболеваний.
Комбинация из двух препаратов НИОТ является основой различных схем антиретровирусной терапии.
Для детей рекомендуются схемы терапии, включающие 2 НИОТ и 1 ИП или 2 НИОТ и 1 ННИОТ.
В дальнейшем, при эффективной ВААРТ, уровень вирусной нагрузки должен быть ниже уровня определения, но возможны подъемы, не превышающие 1000 копий/мл (рис. 1).
В результате проведенного анализа амбулаторных карт и историй болезни детей с врожденной ВИЧ-инфекцией, получающих антиретровирусную терапию, было установлено, что в среднем уже через 3 месяца от начала лечения наблюдалось снижение уровня вирусной нагрузки ниже уровня определения (ниже 400 копий в мл), а количество CD4-лимфоцитов повышалось (рис. 2).
Эффективность специфической терапии определялась:
Если ВААРТ является неэффективной и это не связано с нарушением режима приема препарата, приемом лекарств антагонистов и т. п., рекомендуется проведение теста на резистентность вируса к лекарственным препаратам и назначение новой схемы терапии с учетом результатов этого теста.
На 2007 г. из 169 детей, состоящих на учете в МГЦ СПИД, 100 детей получают ВААРТ. Отсутствие приверженности, т. е. неготовность семьи к проведению ВААРТ, несоблюдение режима приема препаратов было в 1-м случае, что привело к летальному исходу.
Положительный тест на резистентность к ВААРТ был у 5 детей (13%). Схема лечения была пересмотрена.
Клинический пример. М. А., 2 года 11 месяцев. Дата рождения: 18.03.05 г. Находилась в детском отделении с 31.03.05 г. по 3.03.06 г. с диагнозом: ВИЧ-инфекция, стадия вторичных заболеваний IIIВ: генерализованная цитомегаловирусная инфекция, рецидивирующая пневмония, распространенная грибковая инфекция, анемия, энцефалопатия смешанного генеза, грубая задержка психомоторного и физического развития, истощение IV ст., гидроцефальный синдром, глубокая недоношенность, лимфаденопатия, гепатолиенальный синдром.
Ребенок от ВИЧ-инфицированной матери 25 лет, 7 беременностей (5 медицинских абортов), 2 преждевременных родов в домашних условиях, в женской консультации не наблюдалась. Профилактику во время беременности не получала. Вес при рождении 1280 г, рост 42 см. Состояние при поступлении тяжелое за счет острой дыхательной недостаточности, обусловленной пневмонией с ателектазами.
За время нахождения в стационаре многократно болела ОРЗ и пневмониями с обструктивным синдромом. С сентября 2005 г. полисегметарная пневмония рецидивирующего течения, плевропневмония, в ноябре 2005 г. деструктивная правосторонняя пневмония. С января 2006 г. интерстициальные изменения в легких, плевральные спайки.
Иммунный статус на 18.06.05 г.: CD4 – 920 (19%), вирусная нагрузка 6 000 000 копий/мл. С мая 2005 г. проводилась специфическая терапия: Вирасепт + Эпивир ТриТиСи + Калетра. Иммунный статус на 3.03.06 г.: CD4 – 1480 (20%), вирусная нагрузка 7300 копий/мл. На фоне лечения состояние стабилизировалось, ребенок выписан в удовлетворительном состоянии под амбулаторное наблюдение.
Выводы:
Чаще всего врожденная ВИЧ-инфекция проявляется симптомами поражения ЦНС, лимфаденопатией, гепатоспленомегалией.
Из оппортунистических инфекций ведущими являются грибковые поражения кожи и слизистых, пневмоцистная пневмония, а из сопутствующих заболеваний — хронический вирусный гепатит С.
На фоне приема ВААРТ отмечалась положительная клиническая динамика и улучшение специфических лабораторных показателей: на 12–24 неделе лечения количество CD4-лимфоцитов повысилось в среднем на 5% от исходного уровня, в то время как уровень вирусной нагрузки снизился до неопределяемого (< 400 копий/мл).
Отмечался постепенный регресс вторичных заболеваний в результате проводимой специфической терапии в сочетании с ВААРТ.
— отсутствие приверженности;
— развитие резистентности к проводимой терапии (отмечалось в 13% случаев).
Литература
Покровский В. В., Ермак Т. Н., Беляева В. В., Юрин О. Г. ВИЧ-инфекция: клиника, диагностика и лечение. 2000.
Покровский В. В., Ладная Н. Н., Соколова Е. В., Буравцова Е. В., Кравченко А. В. ВИЧ-инфекция. Информационный бюллетень № 30. 2007.
Peter Havens, Russell Van Dyke, Geoffrey Weinberg. Guidelines for the Use of Antiretroviral Agents inPediatric HIV Infection. 2008.
Н. О. Голохвастова, студентка 6 курса МГМСУ, Москва
Вся эта неделя объявлена Всемирной организацией здравоохранения неделей грудного вскармливания. Медицинские блогеры, педиатры и другие специалисты все последние дни проводят стримы и эфиры о пользе грудного молока для младенцев и его неоспоримых преимуществах перед смесями. Например, есть исследования, подтверждающие, что если кормить ребенка грудью до полугода, то у детей в возрасте до двух лет острый средний отит встречается примерно в два раза реже, а продолжительная диарея - в полтора. А в рекомендациях ВОЗ, вышедших в 2016 году, говорится, что матери, которые принимают АРТ и строго следуют рекомендациям лечащего врача, могут кормить грудью малышей до года. На этом фоне ученые продолжают искать ответ на вопрос, можно ли кормить грудью женщинам, которые живут с ВИЧ. И пока ответ, скорее, отрицательный. СПИД.ЦЕНТР поговорил об этом с врачом-инфекционистом, педиатром и сотрудницей ВИЧ-сервисной НКО.
Впрочем, есть нюансы. В последние годы проводится все больше исследований, доказывающих, что риски передачи есть, но они не такие высокие, как казалось раньше. Одно из недавних исследований на эту тему показало: риск передачи ВИЧ за шесть месяцев грудного вскармливания составляет 0,3 %, за двенадцать месяцев — 0,7 %. Это, кстати, в семь раз больше, чем риск для отрицательного мужчины инфицироваться при контакте с ВИЧ-положительной женщиной, отмечают эксперты.
по теме

Общество
Грудное вскармливание и ВИЧ в эпоху неопределяемой нагрузки
В России есть программы выдачи заменителей грудного молока, но они несовершенны, а доступ к ним есть не у всех женщин. В этом мнении сходятся и врачи, и ВИЧ-сервисные некоммерческие организации.
Самая популярная смесь — NAN-1 производства компании Nestle. В среднем одна банка весом 1,8 килограмма стоит 700-800 рублей. В лучшем случае, говорит Елена, одной банки хватает на неделю. И это только на первых порах. Вскоре аппетит малыша растет. Самый острый период — между двумя и шестью месяцами. Впрочем, после шести месяцев есть возможность переводить ребенка на смешанный тип питания — овощные, фруктовые пюре и каши.
Благодаря современной антиретровирусной терапии, принятым организационным мерам по своевременному обследованию беременных и назначению им АРВ-препаратов в России, как и во многих других странах, уровень вертикальной передачи ВИЧ от матери ребенку снизился в последние годы до минимальных значений — более 98% детей не получают ВИЧ. Специалисты и молодые родители с гордостью считали, что проблема сохранения здоровья ребенка, мать которого ВИЧ-положительна, решена. Однако, как выяснилось, это совсем не так: российские ученые установили, что у детей, рожденных ВИЧ-положительными матерями, существенно выше риск перинатальных потерь, мертворождения, ранней и поздней младенческой смертности. И дело тут совсем не в вирусе.

Василий Шахгильдян, врач-инфекционист
В чем проблема?
За весь период наблюдения, на 31 декабря 2020 года, от ВИЧ-положительных женщин родились 218 956 детей. Вирус выявили у 11 724 из них. При этом, по данным за 2020 год, на свет появились 13 186 малышей, из них инфицированы ВИЧ — всего 165 (по данным в настоящее время).
В 2019 году у женщин с ВИЧ родились 13 675 детей, из них 13 559 — живыми. Показатель мертворожденности (число мертворожденных на 1000 родившихся живыми и мертвыми) составил в случае ВИЧ-инфекции у матери 8,5‰ — то есть на 55% выше, чем в общей популяции (5,5‰).
- показатель перинатальной смертности (количество мертворожденных и умерших в первые 168 часов на 1000 родившихся живыми и мертвыми) в случае ВИЧ-инфекции у матери был 11,0‰, что на 60% выше показателя в общей популяции (6,8‰);
- показатель ранней неонатальной смертности (число мертворожденных и умерших в первые 168 часов на 1000 родившихся) среди детей от матерей с ВИЧ оказался на 82% выше, чем в общей популяции (2,5‰ и 1,4‰, соответственно);
- показатель младенческой смертности (количество умерших на 1000 родившихся живыми) детей ВИЧ-инфицированных матерей был на 33% выше (6,5‰), показателя в общей популяции (4,9‰).
С чем это может быть связано?
Одной из наиболее вероятных причин специалисты считают более высокую частоту внутриутробных инфекций, в том числе врожденной цитомегаловирусной инфекции. По словам Шахгильдяна, частота ее у детей, рожденных ВИЧ-положительными матерями, существенно выше.
Возможно, иммуносупрессия и другие более тонкие иммунологические нарушения в случае наличия ВИЧ-инфекции у матери увеличивают вероятность передачи ЦМВ через плаценту и создают условия для заражения плода и развития болезни.

Коллаж: Анна Сбитнева
Наиболее типичными клиническими проявлениями врожденной ЦМВ-инфекции являются тромбоцитопеническая пурпура, тромбоцитоз, длительная выраженная желтуха, низкий вес младенца, недоношенность, увеличение печени и селезенки, микроцефалия и гидроцефалия, гепатит, судорожный синдром, синдром мышечных и двигательных нарушений, поражение органов зрения, снижение слуха. При отсутствии лечения значительное число детей погибает в первые месяцы жизни или в 40–90% случаев у малышей развиваются тяжелые отдаленные неврологические нарушения.
Кроме того, даже при бессимптомном течении врожденной ЦМВ-инфекции есть риски отдаленных последствий. В 3–15% случаях формируются поздние неврологические осложнения, включая сенсоневральную глухоту (четверть всех случаев), нарушение восприятия речи при сохранении слуха, детский церебральный паралич, эпилепсию, задержку в развитии речи, снижение способности к обучению, чтению, гиперактивность, поведенческие проблемы.

Коллаж: Анна Сбитнева
По словам Шахгильдяна, расчетные данные показывают, что только в 2019 году не менее 400 младенцев ВИЧ-инфицированных матерей были внутриутробно заражены ЦМВ, из них 110–140 детей — страдают от ЦМВ-заболевания и/или могут иметь отдаленные психомоторные и когнитивные расстройства.
Что делать женщинам и врачам?
По словам врачей, при ведении ВИЧ-положительных беременных и их новорожденных детей очень важно заботиться не только о том, чтобы ребенок не был заражен ВИЧ, но и защитить его от иных внутриутробных инфекций. Это вполне возможно, учитывая существование современных методов лабораторной диагностики и лечения.
«Например, есть возможность использования молекулярных методов диагностики (ПЦР), позволяющих определять у беременной наличие ДНК ЦМВ в крови и моче и тем самым своевременно выявлять вторичную активной ЦМВ-инфекцию, которая также, как и острая (первичная) ЦМВ-инфекция может служить причиной заражения плода вирусом. Или, благодаря выявлению ДНК вируса простого герпеса (ВПГ) в соскобе из цервикального канала у женщины в третьем триместре беременности, устанавливать факт бессимптомного выделения вируса из урогенитального тракта, что может быть причиной заражения вирусом простого герпеса во время рождения ребенка и развития тяжелого неонатального герпеса. Естественно, выявление неблагоприятного факта является основанием для начала соответствующего лечения.

Коллаж: Анна Сбитнева
Кроме того, своевременная вакцинация молодой женщины позволит защитить ее, а значит, в дальнейшем при беременности — и ее будущего ребенка от ряда тяжелых инфекций.
«До наступления беременности женщины с ВИЧ должны вакцинироваться от гепатита В, краснухи, кори, ветряной оспы, коклюша, чтобы не подхватить эти инфекции во время беременности. Должна быть создана комплексная программа вакцинации молодых ВИЧ-положительных женщин. Когда женщина только начинает диспансерное наблюдение в центре по профилактике и борьбе со СПИДом, необходимо сосредотачиваться не только на антиретровирусной терапии и отслеживать показатели вирусной нагрузки и иммунного статуса, но и предлагать соответствующие обследования для создания персональной программы вакцинации от ряда инфекций.
Читайте также:

