Системная красная волчанка в меде орг
Обновлено: 25.04.2024
2. Комплексное соединение 6-метилурацила с янтарной кислотой, проявляющее антигипоксическую активность и способ его получения: пат. 2259357 Рос. Федерация: МПК7 С 07 D 239/22/ Кривоногов В.П., Мышкин В.А., Ибатуллина Р.Б., Чернышенко Ю.Н., Козлова Г.Г., Савлуков А.И., Абдрахманов И. Б., Гуляева И. Л., Мышкин И. В.// Патент Российской Федерации № 2259357 Р.Ф.: МПК7 С 07 D 239/22. Приоритет изобретения от 21 июля 2003 г.; заявитель и патентообладатель Институт органической химии Уфимского научного центра РАН, Уфимский НИИ медицины труда и экологии человека Минздрава РФ. – № 2003122994/04; заявл. 21.07.03; опубл. 27.08.05, Бюл. № 24. 6 с.
3. Насонов Е.Л., Насонова В.А. Ревматология: национальное руководство. – М.: ГЭОТАР-Медиа, 2008. – С. 720.
5. Осипок Н.В. Системная красная волчанка: учебное пособие для клинических ординаторов, интернов и врачей-курсантов. – Иркутск, 2012. – С. 28. (Иркутский государственный медицинский университет).
7. Экспериментальные модели в патологии: учебник / В.А. Черешнев, Ю.И. Шилов, М.В. Черешнева, Е.И. Самоделкин, Т.В. Гаврилова, Е.Ю. Гусев, И.Л. Гуляева. – Пермь: Перм. гос. нац. исслед. ун-т., 2014. – 324 с.
Актуальность исследования
Системная красная волчанка – аутоиммунное ревматическое заболевание, в основе патогенеза которого лежат дефекты иммунорегуляции, приводящие к неконтролируемой гиперпродукции антител к компонентам собственных тканей и развитию хронического воспаления, затрагивающего многие органы и системы [3].
В настоящее время этиология СКВ изучена не до конца, однако проводятся исследования, посвященные изучению роли ведущих факторов, участвующих в развитии заболевания: вирусной инфекции, генетического фактора и половых гормонов. Гипотеза о роли вирусной инфекции стала актуальной, в результате обнаружения в лимфоцитах, тромбоцитах и эндотелиальных клетках больных СКВ структур, напоминающих нуклеопротеиды вирусов. Микроскопически исследовались пораженные органы: кожа, синовиальная жидкость, почки и печень. В крови у пациентов так же были обнаружены циркулирующие антитела (АТ) к вирусам краснухи, парагриппа и кори. СКВ способно развиваться и прогрессировать на фоне иммунодефицита. Генетический фактор, определяющий склонность к развитию заболевания, представляет собой главный комплекс гистосовместимости (HLA). У больных СКВ наблюдается доминирование определенных гаплоидных генотипов НLA-системы: I, II или III класса. Частота поражения однояйцевых близнецов с одинаковым набором генов выше, чем у разнояйцевых близнецов. Половые гормоны оказывают существенную роль в развитии болезни. В организме больного происходит гиперсекреция эстрогена и пролактина, усиливающих иммунный ответ и недостаток андрогенов, обладающих иммуносупрессорным действием. У мужчин и женщин в сыворотке крови снижается количество дегидротестостерона и тестостерона, но повышается уровень фолликулостимулирующего и лютеинизирующего гормона. Особое влияние на женщин оказывает беременность и роды, прием оральных контрацептивов, на мужчин – синдром Кляйнфельтера.
Сопутствующими факторами заболевания могут являться физические факторы (инсоляция), стресс, токсины, лекарственные препараты, диета.
В основе патогенеза СКВ лежат дефекты иммунорегуляции, приводящие к неконтролируемой гиперпродукции аутоантител к компонентам собственных тканей и развитию хронического воспаления, затрагивающего многие органы и системы [1]. При прогрессировании заболевания происходит увеличение пролиферации стволовых клеток, преждевременная инволюция тимуса, нарушение продукции тимозина и тимопоэтина, что приводит к нарушению иммунных и ростовых процессов. Происходит резкое увеличение Т-супрессорной активности, способствующей повышению интерферона-γ, активирующего течение СКВ, и снижению интерлейкина-2 (IL-2). Гиперактивность Т-хелперов способствует гиперактивации В-лимфоцитов, вызывающей возрастание скорости их пролиферации и дифференцировки. Гиперсекреция IgG, IgМ в кровотоке и IgA в слюне сопровождается уменьшением IL-12, ингибирующего спонтанную продукцию иммуноглобулинов.
Т-лимфоциты приводят к повышению синтеза АТ и продукции ауто-АТ. Ауто-АТ непосредственно воздействуют против компонентов клетки: лизосом, микросом, митохондрий; ядерных компонентов: ДНК, РНК, гистонов, нуклеопротеиновых комплексов; клеток крови [8].
Избыточная реактивность В-лимфоцитов обуславливает гиперактивность циркулирующих иммунных комплексов (ЦИК). Осаждение ЦИК на базальной мембране сосудов микроциркуляторного русла приводит к повреждению эндотелия, вследствие чего возрастает гиперпродукция коллагена и утолщение базальных мембран, сужение просвета сосудов. Возникающая микроангиопатия способствует повреждению внутренних органов и синдрому Рейно. Влияние ЦИК на соединительную ткань приводит к гиперпродукции гликозаминогликанов, коллагена, протеогликанов и фибронектина, вызывающих склеродермические поражения кожи, слизистых оболочек, опорно-двигательного аппарата и внутренних органов. ЦИК участвуют в активации кининовой система, системы комплимента по классическому пути и способствуют гиперпродукции медиаторов воспаления из плазмы крови, тканевой жидкости и клеток, что приводит к иммунному воспалению в тканях и органах. Таким образом ауто-АТ оказывают опосредованное влияние через образование ЦИК.
Выбор лечения СКВ зависит от результатов обследования и выявления поражаемых органов, степени активности заболевания. Каждого больного с выраженными клинико-лабораторными признаками СКВ необходимо лечить в условиях стационара с использованием лекарственных препаратов. С целью воздействия на иммунные процессы, возникающие при СКВ, применяют глюкокортикоиды (ГК), цитостатикие (ЦТП) и аминохинолиновые (АП) препараты. Глюкокортикоиды – лекарственные средства, при применении которых достигается максимальный эффект при минимальных дозах. Лечение высокими дозами составляет 1-2 месяца, при получении положительного результата, доза постепенно снижается. Лечение при СКВ пожизненное. Благодаря применению ГК снижается прогрессирование и активность заболевания, наступает ремиссия. Препараты оказывают противовоспалительное действие, снижая активность клеточных и гуморальных факторов. При воздействии на клеточные факторы ГК тормозят образование медиаторов воспаления: простогландинов, лейкотриенов и гистамина из лизосом, тучных клеток и базофилов; на гуморальные – снижают активность кининовой системы, снижают образование и увеличивают распад компонентов системы комплемента (по классическому пути). Таким образом, подавляют развитие иммунного воспаления. Оказывая иммунодепрессивное действие, ГК тормозят миграцию стволовых клеток костного мозга, подавляют активность Т- и B-лимфоцитов, угнетая высвобождения цитокинов (ИЛ-2, интерферона-гамма) из лейкоцитов и макрофагов, блокируют Fc-рецепторы к иммуноглобулинам. Применяются при отсутствии должного терапевтического эффекта от ГК и при побочных явлениях от ГК в условиях стационара. При остром течении СКВ используются в сочетании с ГК с самого начала лечения. ЦТП оказывают иммунодепрессивное действие, подавляя пролиферацию B-лимфоцитов, участвующих в иммунном ответе. Аминохинолиновые препараты применяют при СКВ низкой активностью в дополнение к ГК, способствуют поддержанию ремиссии и предупреждают рецидивы. АП уплотняют лизосомальные мембраны и препятствуют выходу лизосомальных ферментов, нарушают редупликацию ДНК, синтез РНК, подавляют свободнорадикальные процессы, ослабляют активность протеолитических ферментов (протеазы и коллагеназы), лейкоцитов, хемотаксис лимфоцитов.
Для воздействия на отдельно резко выраженные синдромы – мочегонные и гипотензивные средства, сердечные гликозиды, гепарин. Лечение и профилактика осложнений иммунодепрессивной терапии проводится при использовании противоязвенных и сахаропонижающих препаратов, антибиотиков, противогрипковых средств, препаратов калия, ощелачивающих средств, НПВС, витаминов, и соблюдении диеты [2; 4].
Лабораторно – инструментальные исследования при СКВ проводят с целью определения основного заболевания и сопутствующих патологий. Лабораторные тесты позволяют установить изменения состава крови: лейкопения, тромбоцитопения, антинуклеарный фактор (антитела к Smith), снижение общей гемолитической активности комплимента и его компонентов, антитела к двуспиральной ДНК, антитела к фосфолипидам; мочи: протеинурия, гематурия, лейкоцитурия, цилиндрурия. Инструментальные методы исследования включают проведение рентгенографии, УЗИ, МРТ, КТ внутренних органов, денситометрии, бронхоскопии, ЭКГ, ЭхоКГ, ангиографии, эзофагогастродуоденоскопии, электроэнцефалографии, функциональные тесты при наличии показаний.
Течение СКВ зависит от поражения жизненно важных органов и своевременно проведенной терапии.
Цель работы: изучить специальную литературу о патогенезе и принципах патогенетической терапии системной красной волчанки (СКВ). Подтвердить литературные данные клиническими примерами в отношении фармакотерапии СКВ в Пермском крае.
Материалы и методы исследования
Результаты исследования и их обсуждение
Анализ историй болезни показал, что заболеванию подвержены в 88 % случаев женщины и в 12 % – мужчины в возрасте 20-55 лет. В 88 % случаев наблюдалось хроническое течение СКВ II – III степени активности, в 12 % – острое. Среди сопутствующих заболеваний у большинства пациентов с СКВ были выявлены диффузные поражения соединительной ткани, суставов, синдром Рейно и холецистит.
В качестве патогенетической терапии, направленной на подавление аутоиммунного воспаления, всем пациентам были назначены глюкокортикоиды – Преднизолон. Для симптоматической терапии, применяемой с целью предотвращения и компенсации побочных эффектов глюкокортикоидов, использовали антисекреторные препараты (блокаторы Н2 гистаминовых рецепторов и блокаторы Н+/К+-АТФазы) в 50 % случаев; НПВС у 38 % пациентов; антибиотикотерапия (цефалоспорины, гликопептиды и карбапенемы) применялась в 38 % случаев. В результате проведенной терапии у большинства пациентов наблюдалась положительная динамика лечения
Выводы
Системная красная волчанка (СКВ) - хроническое, прогрессирующее полисиндромное заболевание, характеризующееся генетически обусловленным несовершенством иммунорегуляторных процессов, приводящим к неконтролируемой продукции антител к собственным клеткам и их компонентам, с развитием аутоиммунного и иммунокомплексного хронического воспаления.
Код МКБ 10 - М.32.
Этиология и патогенез СКВ недостаточно изучены. Предполагается сочетанное воздействие факторов внешней среды (фотосенсибилизации, стресса, нарушений питания, курения), генетических и гормональных. Возможно, что пусковым механизмом СКВ является активация вирусов (в первую очередь ретровирусов и близких к ним).
Среди конкретных механизмов развития болезни доказано влияние иммунных нарушений в Т-клеточном репертуаре и в продукции цитокинов, которые принимают участие в активации и дифференциации В-лимфоцитов в антителопродуцирующие клетки. Последнее ведет к гиперпродукции различных антител (в том числе и аутоантител), образованию циркулирующих иммунных комплексов, которые, откладываясь на базальных мембранах клеток различных органов, вызывают повреждение тканей с воспалительной реакцией и высвобождением новых антигенов, к которым формируются антитела, образуются иммунные комплексы, создавая порочный круг.
Клиническая картина СКВ характеризуется полиморфизмом симптомов и прогрессированием, при отсутствии лечения возможен летальный исход в связи с недостаточностью функции того или иного органа или присоединением вторичной инфекции.
В клинической практике при постановке диагноза СКВ используются диагностические критерии Американской ревматологической ассоциации, включающие 11 признаков:
1) эритема на лице ("бабочка");
2) дискоидная волчанка;
3) фотосенсибилизация;
4) язвы полости рта;
5) артрит;
6) серозит;
7) поражение почек (протеинурия 0,5 и более грамм в сутки, наличие цилиндров в моче);
8) неврологические нарушения (судороги или психоз);
9) изменения крови:
-
а) гемолититческая анемия,
б) содержание лейкоцитов 4х10 9 /л и ниже при двух и более исследованиях,
в) лимфопения 1,5х10 9 /л при двух и более исследованиях,
г) тромбоцитопения 100х10 9 /л;
При наличии любых 4 критериев диагноз СКВ считается достоверным.
СКВ поражает преимущественно женщин детородного возраста (20-30 лет). Многие годы беременность при СКВ считалась противопоказанием из-за существовавшего мнения, что она может быть причиной обострения и летального исхода заболевания, а также высокой частоты неонатальных осложнений. Однако совершенствование диагностики болезни, разработка современных методов ее лечения и, как следствие этого, - улучшение прогноза заболевания позволили изменить представления о беременности при СКВ.
Влияние беременности на СКВ
У многих больных СКВ беременность завершается успешно и не приводит к обострению заболевания вообще или обострение не сопровождается существенным ухудшением состояния больной и легко подавляется.
Среди факторов, определяющих вероятность обострения СКВ в период гестации, первое место занимает активность заболевания на момент зачатия.
Установлено, что наступление беременности при низкой активности СКВ в большинстве случаев не ухудшает заболевание. На прогноз заболевания не влияют длительность болезни и дозы кортикостероидных препаратов, предшествующие наступлению гестации. Зачатие в период высокой активности волчаночного процесса с тяжелыми органными поражениями почек, центральной нервной системы, легких и сердца, тем более симптомы функциональной недостаточности любого из этих органов резко увеличивают вероятность неблагоприятного исхода и СКВ, и беременности.
Для определения степени активности СКВ применяется классификация В.А.Насоновой (1972), учитывающая ряд клинико-лабораторных показателей заболевания (см. таблицу). Отсутствие активности СКВ или I (минимальная) степень активности позволяют разрешить беременить больной СКВ.
"Критическими" с точки зрения обострения заболевания, когда велика вероятность активации СКВ являются I триместр и первая половина беременности. Заслуживают внимания и первые 2-3 месяца после родоразрешения.
Клиническо-лабораторная характеристика активности патологичекого процесса при СКВ.
Влияние СКВ на течение беременности
Фертильность (способность к зачатию) у больных СКВ обычно не страдает, но тяжелые обострения заболевания и использование высоких доз кортикостероидов, умеренная почечная недостаточность вызывают субфертильность (олиго- и аменорею). К потере фертильности у больных СКВ может привести использование цитостатика циклофосфамида. Данных о влиянии других лекарственных препаратов, обычно используемых при лечении СКВ, на фертильность не имеется.
СКВ может неблагоприятно сказываться на беременности и ее исходе, что проявляется повышенной частотой самопроизвольных абортов, преждевременных родов, мертворождений и гипотрофий новорожденных, а также высоким процентом аномалий родовой деятельности и послеродовых осложнений. Поздний токсикоз у беременных с СКВ встречается в 2,8 раз чаще, чем у здоровых беременных, у 18,6% больных в последовом и раннем послеродовом периодах возникают кровотечения. Клиника гестоза может напоминать таковую при волчаночном гломерулонефрите. Только учет клинико-лабораторной картины заболевания, времени ее проявления могут быть решающими при проведении дифференциального диагноза. Различная тактика ведения больных с активным волчаночным нефритом (назначение иммуносупрессивной терапии) и гестозом (симптоматическая терапия) обусловливает практическую значимость правильной и своевременной диагностики этих состояний.
Большое значение в улучшении течения и исходов беременности и родов при СКВ имеет предшествующая гестации длительная (не менее 6-12 месяцев) ремиссия заболевания.
СКВ и антифосфолипидный синдром.
В последнее десятилетие проблема неблагоприятных акушерских исходов при СКВ приобрела новое направление, связанное с обнаружением у 30-40% больных СКВ особой группы антител - антифосфолипидных (АФА), к которым относятся: волчаночный антикоагулянт, антикардиолипиновые антитела и антитела, обусловливающие появление ложноположительной реакции Вассермана. Присутствие АФА у больных СКВ может приводить к формированию антифосфолипидного синдрома, одним из проявлений которого является привычное невынашивание беременности.
Антифосфолипидный синдром (АФС) впервые был описан при СКВ, а затем при некоторых других (преимущественно аутоиммунных) заболеваниях и состояниях. Основными диагностическими критериями АФС считают:
-венозные и артериальные тромбозы,
-привычное невынашивание беременности,
-тромбоцитопению.
При этом под "привычным невынашиванием беременности" подразумевается не менее двух случаев плодных потерь, не связанных с гинекологической или сугубо акушерской патологией.
Наличие одного из этих клинических признаков и повторных положительных анализов на волчаночный антикоагулянт и/или IgG-, IgM-антикардиолипиновые антитела позволяет диагностировать АФС.
Одновременное присутствие волчаночного антикоагулянта и антикардиолипиновых антител имеется у 60-80% больных. АФА могут исчезать или их титры уменьшаются в период между беременностями, а затем вновь появляться в очередную беременность.
Присутствие АФА у больных СКВ обусловливает до 90% случаев плодных потерь, при этом риск последних нарастает при наличии в анамнезе самопроизвольных выкидышей. Если гестация у беременных с АФС и не заканчивается смертью плода, которая чаще наступает в первой половине беременности, то у таких больных нередко наблюдаются поздний гестоз (в том числе пре- и эклампсия) и преждевременные роды. Описан и "послеродовый АФА-зависимый синдром", который проявляется тромбозами крупных и средних сосудов с соответствующей симптоматикой.
Таким образом, обнаружение АФА у беременных с СКВ в большинстве случаев осложняет течение беременности и послеродового периода и является одной из главных причин плодных потерь. Поэтому своевременная диагностика АФС, адекватная терапевтическая и акушерская тактика необходимы для улучшения исходов беременности у больных СКВ с сопутствующим АФС.
Влияние СКВ на плод (неонатальная волчанка)
Неонатальная волчанка (НВ) - следствие пассивно приобретенного аутоиммунного заболевания, серологическими маркерами которого являются антитела к растворимым антигенам тканевых рибонуклеопротеинов - Ro/Lа-антитела. С НВ связано около 1% всех случаев плодных потерь при "СКВ-беременности".
Пассвная трансплацентарная передача Ro/Lа-антител во время беременности плоду ведет к развитию у него поражения кожи и/или сердца -двум основным признакам НВ. Редко НВ сопровождается другими проявлениями (гепатомегалией, печеночной дисфункцией, спленомегалией, лимфоаденопатией, пневмонитом, тромбоцитопенией, анемией), которые обычно носят преходящий характер.
Кожные высыпания - наиболее частый синдром НВ, появляются обычно в течение первых 2-х месяцев жизни, типично - на лице и верхних конечностях, нередко после инсоляции или ультрафиолетового облучения по поводу неонатальной желтухи. Часто по форме сыпь представлена ограниченными округлыми пятнами и бляшками, нередко имеет сходство с подострой кожной красной волчанкой. Поражение обычно регрессирует в течение 6 месяцев, оставляя в отдельных случаях гипопигментацию.
Терапии НВ в большинстве случаев не требует, симптоматика стихает по мере естественного выведения материнских антител (кроме, ВППБ). Профилактическое назначение медикаментозных средств также не рекомендуется. Необходимость в дополнительной терапии возникает при наличии у матери ранее рожденных детей с НВ и предполагает применение высоких доз дексаметазона (как неинактивирующегося в плаценте) и плазмафереза в течение беременности.
Акушерская и терапевтическая тактика
1. Наступление и вынашивание беременности у больной СКВ могут быть разрешены при клинической ремиссии или минимальной клиникоиммунологической активности заболевания (I степени, по классификации В.А.Насоновой), продолжающейся не менее 6-12 месяцев до зачатия, и отсутствии симптомов функциональной недостаточности любого органа или системы.
2. Противопоказаниями для беременности при СКВ являются наличие высокой активности заболевания, симптомы волчаночного нефрита (протеинурия более 3 г/сут.), нефротический синдром, почечная недостаточность (сывороточный креатинин более 130 мкмоль/л), артериальная гипертензия, недостаточный сердечно-легочный резерв, также как функциональная недостаточность любого органа и поражение центральной нервной системы.
3. Использование медицинского аборта при СКВ как метода предупреждения обострения болезни в период гестации неоправдано. Более того, он может явиться провоцирующим фактором активации СКВ. Однако терапевтический аборт показан в случаях тяжелой почечной, сердечной или легочной недостаточности у больных СКВ.
4. Наличие АФС или отдельных его синдромов у больной СКВ требует проведения повторных исследований на АФА (как на волчаночный антикоагулянт, так и на антикардиолипиновые антитела) на этапе планирования беременности и мониторинг их при наступлении последней с целью своевременной коррекции титров АФА во избежание осложнений течения заболевания и гестационного процесса.
5. У анти-Rо/Lа-позитивных беременных с СКВ показано повторное проведение ультразвукового исследования плода и допплерометрии пупочных сосудов после 18 недели гестации для ранней диагностики нарушений сердечной деятельности плода и определения показаний для срочного родоразрешения.
6. Доза кортикостероидного препарата при условии стабильности состояния больной должна оставаться неизменной в течение всей беременности и не менее 2-х месяцев после родоразрешения. При обострении СКВ - терапия кортикостероидами усиливается до адекватной степени активности болезни. Вопрос о прерывании беременности решается индивидуально.
7. Госпитализация в родильный дом должна быть не позднее 36-37 недели гестации. В более ранние сроки при обострении течения болезни женщину целесообразно госпитализировать в ревматологический или терапевтический стационар.
8. При наличии клинических признаков активности заболевания родоразрешение производится преждевременно, что следует учитывать при определении срока госпитализации в родильный дом. В период родов показано дополнительное парентеральное введение гидрокортизона (30-100 мг/сут.) с последующим постепенным снижением этой дозы в течение 3-5 дней после родов или аборта.
9. Показаниями для оперативного родоразрешения (кесарева сечения) беременных с СКВ, кроме акушерской патологии, являются:
СПИСОК ЛИТЕРАТУРЫ
Системная красная волчанка (СКВ) - классическое аутоиммунное ревматичес кое заболевание, в основе патогенеза которого лежат дефекты иммунорегуляции, приводящие к неконтролируемой гиперпродукции В лимфоцитами аутоантител к компонентам собственных тканей и развитию хронического вос паления, затрагивающего многие органы и системы. Прогрессирующее поражение жизненно важных органов определяет жизненный и социальный прогноз больных СКВ, при "катастрофическом" течении летальность достигает 40% в год, в связи с чем принципиальное значение имеет разработка новых методов патогенети ческой терапии этого заболевания.
В последние десятилетия сформиро ваны основные принципы терапии СКВ, в основе которых лежит применение раз личных режимов глюкокортикоидной (ГК) терапии и цитотоксических препаратов. Современные терапевтические схемы с использованием пульс-терапии метилпреднизолоном и циклофосфаном (ЦФ) значительно улучшили отдаленную выжи ваемость и высокоэффективны при развитии угрожающих состояний у больных СКВ. Наиболее ярким примером повыше ния качества лечения СКВ является более чем пятикратное увеличение 5-и летней выживаемости у больных с волчаночным нефритом. Однако, отдаленный жизненный прогноз у этой категории больных остается неблагоприятным. Так, 20-и летняя выжи ваемость при развитии люпус-нефрита, даже при использовании современных терапевтических программ, не превышает 20%. Значительно отягощает кратко срочный и отдаленный жизненный прогноз у больных СКВ развитие таких угрожающих состояний как цитопенических криз, поражение центральной и периферической системы, пневмонит, катастрофическое течение АФС и генерализованный (криоглобулинемический) васкулит. Основными факторами, влияющими на развитие неблагоприятного исхода при СКВ, является резистентность к высоким дозам ГК и циклофосфана и торпидное, прогрес сирующее течение болезни. В тоже время применение высоких доз ГК и ЦФ ассоциируется с повышением риска воз никновения тяжелых вирусных и бакте риальных инфекций, что в значительной степени лимитирует их назначение.
Безусловно, "сверхзадачей" терапии СКВ и других аутоиммунных заболеваний, является создание препаратов селективно влияющих на ключевые звенья патогенеза. В этой связи перспективным направ лением фармакотерапии СКВ являются препараты, блокирующие пролиферацию В - клеток, среди которых одним из наиболее изученных, безусловно является Ритуксимаб (Rituxumab, MabTHera, Roch,), который представляет собой рекомби-нантные химерные (мышь-человек) моноклональные антитела к поверхностным рецепторам В-лимфоцитов - CD20. Пред полагаемый механизм действия ритуксимаба, направленный на подавление активности В клеток, может реализовываться за счет антитело-зависимой клеточной цитотоксичности, комплемент-зависимой цитотоксичности, ингибиции клеточной пролиферации и индукции апоптоза В лимфоцитов. Молекулярные взаимодействия связывания CD20 могут приводить к перестройке мембранных липидов, активации ферментов и регу ляции синтеза интерлейкина 10. Основной мишенью ритуксимаба являются клетки предшественники, незрелые, зрелые и "наивные" В-лимфоциты. На плазмати ческие клетки препарат не оказывает влияния, из-за отсутствия их на мембране CD20.
Впервые ритуксимаб был применен для лечения больных злокачественной В-клеточной лимфомой в 1997 г. Моно терапия ритуксимабом В-клеточных лимфом эффективна у 50% больных и в 10% случаев наблюдается клиническая ремис сия, в тоже время при комбинации его с химиотерапией эффективность лечения возрастает до 81-97%, а частота ремиссий достигает 74%.
В настоящее время, по данным литературы, ритуксимаб применялся в лечении более чем 200 больных СКВ. Назначение препарата в дозах от 1000 до 2000 мг (обычно РМ назначается по 375 мг/м 2 еженедельно в течение 4 недель) оказалось высокоэффективным у больных с поражением суставов, кожи, слизистых оболочек, полисерозитом, лихорадкой и гематологическими нарушениями. Особо го внимания заслуживает тот факт, что высокая эффективность ритуксимаба (око ло 80%) отмечалась при развитии прогрессирующего волчаночного нефрита, тяжелом поражении ЦНС, гематоло гическом кризе, пневмоните и катастро фическом течении АФС - при неэффек тивности пульс-терапии ГК, ударных доз циклофосфана, иммуносорбции, плазмафереза, мофетила микофенолата и цик лоспорина.
В настоящее время проведено нес колько открытых пилотных испытаний эффективности ритуксимаба у больных с волчаночным нефритом. Так, в одном из них (P. Sfikakis et al.) препарат был назначен 10 больным с активным пролиферативным люпус-нефритом (III-IV класс по класси фикации ВОЗ), без признаков почечной недостаточности. До включения в ис следование все пациенты получали вы сокие дозы глюкокортикоидов (ГК), пульс-терапию циклофосфаном (ЦФ) или мофетила-микофенолат (МФ) без существен ного эффекта. Инфузии РМ по 375 мг/м - проводились еженедельно в течение 4-х недель. В результате проведенного лечения частичная ремиссия (улучшение на 50% клинико-лабораторных параметров нефрита) зафиксирована у 8 больных через 1-4 месяца. В последующем полная ремиссия (протеинурия В большинстве исследований пока зано, что эффект терапии этим препаратом при волчаночном нефрите развивается не сразу, как правило значимое уменьшение протеинурии, повышение клубочковой фи льтрации, увеличение содержания альбу мина в сыворотке крови, наблюдается на 2-3 месяце от начала лечения и достигает своего максимума к 5-6 месяцу. Одно временно наблюдается уменьшение ин дексов активности СКВ (BILAG, SLEDAI), антител к ДНК, повышение комплемента. Напротив, применение Ритуксимаба у больных с высокой активностью, обус ловленной внепочечными проявлениями СКВ - цитопенией, полиартритом, серозитом, пневмонитом и АФС, может при вести к развитию положительной динамики уже через несколько дней.
Отчетливый быстрый эффект ритукси маба отмечен у больных с критическим течением СКВ, обусловленным пораже нием ЦНС. Поражение ЦНС (нейролюпус), сопровождающееся развитием состояния угрожающего жизни у больных СКВ, наблюдается достаточно редко, в 2-4% случаев. Терапия таких тяжелых прояв лений волчаночного поражения ЦНС, как судорожный синдром, демиелинизирующая нейропатия, поперечный миелит, психоз - представляет большие трудности, стандартных терапевтических алгоритмов не существует, а летальность превышает 50%. В этой связи особый интерес вызывает публикация Tokunaga, в которой сообщается о применении ритуксимаба у 10 больных СКВ по жизненным пока заниям. У всех описываемых больных наблюдались различные проявления пора жения ЦНС: потеря сознания, судороги, дезориентация, атаксия, сенсорная ней ропатия, психоз. Во всех случаях наз начение ритуксимаба привело к быстрому улучшению, развившемуся в течение нес кольких дней от начала лечения. Авторы отмечают быстрый выход из коматозного состояния, уменьшение и исчезновение двигательных и чувствительных наруше ний, купирование судорожного синдрома, психоза и депрессии. Нарастание поло жительной динамики, переходящее в стабильное улучшение наблюдалось в течение 6-7 месяцев, у всех больных за этот период удалось существенно снизить дозу преднизолона и отменить иммунодепрессанты. Полученные данные свидетельствуют о высокой эффективности инфузий ритуксимаба при СКВ с развитием критических состояний, непосредственно угрожающих жизни пациентов. Особенно важным представляется то, что высокая эффективность терапии наблюдалась у больных с тяжелым, прогрессирующим поражением ЦНС с неэффективностью интенсивной терапии, включающей ударные дозы ГК, ЦФ в комбинации с плазмаферезом и иммуносорбцией.
Применение ритуксимаба у больных СКВ не только индуцирует развитие клинического улучшения, продолжитель ностью от нескольких месяцев до 1 года, но и приводит к появлению различных иммунологических феноменов. Практи чески все исследователи отмечают развитие лимфопении, подавление В-лимфоцитов, наблюдаемое практически сразу после проведения курса лечения ритуксимабом. Leandro, Anolik сообщают о значительном подавлении В лимфоцитов, продолжающееся в среднем около 4 месяцев от начала терапии и корре лирующее с развитием клинического эффекта, нормализацией гемоглобина, СОЭ, комплемента. По мнению авторов, появление на фоне терапии антихиме рических антител может провоцировать развитие аллергических реакций. Те же авторы не выявили достоверного снижения антител к ДНК. Оценивая влияние ритуксимаба на активность люпус-нефрита Stifakis et al. так же обращают внимание на подавление 99% В лимфоцитов у 8 из 10 больных, наблюдаемое от 1 до 7 месяцев. Продолжительность угнетения В клеток соответствовала длительности ремиссии и, напротив, их регенерация предшество вала развитию обострения.
Большинство исследователей отме чают достаточно хорошую переносимость препарата. Подавляющее большинство побочных реакций возникающих во время или после проведения инфузий, так или иначе могут быть связаны с "биоло гической", белковой основой препарата. Как правило, наблюдаются такие явления как озноб, лихорадка, гипотензия, одышка. Обычно такие побочные реакции устра няются более медленной скоростью введения, дробным введением. Для профилактики может использоваться пара цетамол, антигистаминовые препараты или ГК в небольших дозах. Сложившимся правилом, позволяющим практически пол ностью устранять "инфузионные" реакции, является использование инфузомата и внутривенное введение 100-250 мг метипреда непосредственно перед инфузией.
В большинстве исследований посвя щенных применению ритуксимаба как в онкологии, так и при аутоиммунных заболеваниях, не находит свое под тверждение концепция об увеличении риска развития оппортунистических инфекций. Вероятно это связано с тем, что несмотря на значительное снижение циркулирующих В лимфоцитов после инфузии РМ, не наблюдается сколь либо существенного снижения продукции иммуноглобулинов, что в свою очередь можно объяснить наличием значительного количества долгоживущих плазматических клеток.
Российский регистр больных СКВ получающий терапию ритуксимабом
Прогностически неблагоприятные варианты течения СКВ и состояния угрожающие жизни
| • Прогрессирующий нефрит (III-IV класс по ВОЗ) • Поражение ЦНС (поперечный миелит, судороги, кома, психоз) • Геморрагический альвеолит • Гематологический криз • КАФС (тромбозы, мультиорганное поражение) • Генерализованный (fulminant) некротизирующий васкулит | • "Стандартные" методы терапии • Пульс-терапия метилпреднизолоном и циклофосфаном • Внутривенный иммуноглобулин • Плазмаферез • Антикоагулянты • Реанимационные мероприятия Смертельные исходы в течение 1-го года до 40% |
Изменение 5-и летней выживаемости у больных С IV классом ВН (J.Cameron 1998)
| Годы | Выживаемость % |
| 1953-1969 отсутствие патогенетической терапии | 17% |
| 1970-1979 средние и большие дозы ГКС, пульс-терапия | 55 (в 3 раза!) |
| 1980-1983 + циклофосфан | 80 |
| 1990-1995 + мофетила микофенолат, циклоспорин, комбинированная ПТ | 82 |
| XXI век: МабТера, А-BLyS, Октембра . | ? |
20-летняя выживаемость больных СКВ
Анти-В клеточная терапия Ритуксимаб (МабТера, ROCHE)
Показания для назначения Ритуксимаба при СКВ
Неконтролируемая активность болезни
Влияние ритуксимаба на показатели активности СКВ
| Британский Индекс активности СКВ | Антитела к двухспирапьной ДНК |
Эффективность РМ у больных с волчаночным нефритом
Показатели активности волчаночного нефрита после терапии Ритуксимабом
Изменение морфологической активности нефрита через год после терапии Ритуксимабом
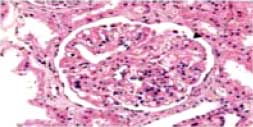 | До лечения Индекс активности 10 |
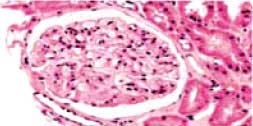 | Через год Индекс активности 1-2 |
Эффективность Ритуксимаба при неиролюпусе
М. Тikunаgа et al. 2006
| Клинические проявления | Результат и скорость достижения эффекта | Длительность эффекта |
| 6 больных Кома, судороги, каталепсия, психоз, нейропатия, галлюцинации, головные боли | Выздоровление 2- 5 дней | 4-29 месяцев |
| 4 больных Депрессия, психоз, нейропатия | Улучшение 1-4 недели | 7-14 месяцев |
Побочные эффекты и осложнения ритуксимаба
- Инфузионные реакции (озноб, гипотония, отеки, высыпания, зуд, лихорадка) могут наблюдаться у 10-20% больных. Возможно обусловлены образованием антихимерных антител (антител против РМ). Вероятность развития при повторных инфузиях уменьшается. Профилактика - метилпреднизолон 100 мг в/в до инфузии.
- Тяжелые, требуюшие антимикробной терапии инфекции редки. Чаще наблюдаются ОРВИ, герпетичекая инфекция.
ЛИТЕРАТУРА
1. Lipsky PE. Systemic lupus erythe matosus: an autoimmune disease of B cell hyperactivity. Nat Immunol. 2001;2:764-766.
2. Silverman GJ. Anti-CD20 therapy in systemic lupus erythematosus: a step closer to the clinic. Arthritis Rheum. 2005;52:371-377
3. Vasoo S, Hughes GRV Perspectives on the changing face of lupus mortality. Autoimmun Rev. 2004;3:415-417.
4. Pryor BD, Bologna SG, Kahl LE. Risk factors for serious infection during treatment with cyclophosphamide and high-dose corti costeroids for systemic lupus erythemato sus. Arthritis Rheum. 1996;39:1475-1482.
5. Chambers SA, Isenberg DA Anti - B cell therapy (Rituximab) in the treatment of autoimmune disease. Lupus. 2005;14:210-214.
6. John Looney, Jennifer H. Anolik, Debbie Campbell, Raymond E. Felgar et al. B Cell Depletion as a Novel Treatment for Systemic Lupus Erythematosus A Phase I/II Dose-Escalation Trial of Rituximab Arthritis Rheum. 2004;Aug;8:2580-2589.
7. Sfikakis PP, Boletis JN, Lionaki S., Vigklis V., Fragiadaki KG, Iniotaki A., and Moutsopoulos HM Remission of Proliferative Lupus Nephritis Following B Cell Depletion Therapy Is Preceded by Down-Regulation of the T Cell Costimulatory Molecule CD40 Ligand An Open-Label Trial. Arthritis Rheum. 2005;52(2):501-513.
8. Mikiko Tokunaga et al. Efficacy of rit uximab (Anti-CD20) for refractory systemic lupus erythematosus involving the central nervous system. 15 Nov 2006; Ann Rheum Dis
9. С.К. Соловьев, Е.Л. Насонов, М.А.Котовская. Ритуксимаб в лечении системной красной волчанки. Русский Медицинский журнал, 2005, 26, 1731-1736.
10. Е.Л. Насонов, С.К. Соловьев. Перспективы применения моноклональных антител к В-лимфоцитам (ритуксимаб) при воспалительных ревматических заболеваниях. Научно-практическая ревматология 1, 2007, 4-8.
Системная красная волчанка. Первая помощь при системной красной волчанке.
1. При лечении больного с системной красной волчанкой (СКВ), находящегося в критическом состоянии, важно знать статус основного заболевания. Степень активности болезни и расстройства функции различных органов, а также длительность и интенсивность иммуносупрессивной терапии должны учитываться при интерпретации имеющихся симптомов и определении лечебной тактики. Многие препараты могут приводить к развитию волчаночного синдрома; это относится прежде всего к новокаинамиду и гидралазину, однако следует назвать также изониазид, сульфаниламиды, дифенилгидантоин, меденитоин, триметин, бутадион, этосукцимид, пенициллин, тетрациклин, парааминосалициловую кислоту, а также гризеофульвин.
2. Кровоточивость чаще всего развивается вследствие аутоиммунной тромбоцитопении и обычно прекращается после начала иммуносупрессивной терапии. Циркулирующие антикоагулянты могут приводить к удлинению коагуляции при исследовании системы гемостаза, однако редко бывают причиной значительного кровотечения.
3. Острая боль в животе встречается у 25% больных с СКВ; причиной ее может быть сама волчанка: брыжеечный артериит приводит к перфорации, асептическому перитониту и панкреатиту. Кроме того, больные с СКВ более подвержены развитию пептических язв вследствие приема глюкокортикоидных препаратов, и бактериального перитонита — вследствие иммуносупрессивной терапии. Волчаночные абдоминальные кризы следует отличать от других часто встречающихся причин боли в животе, ключом служат данные анамнеза, физикального обследования, а также лабораторных и рентгенологических методов исследования.
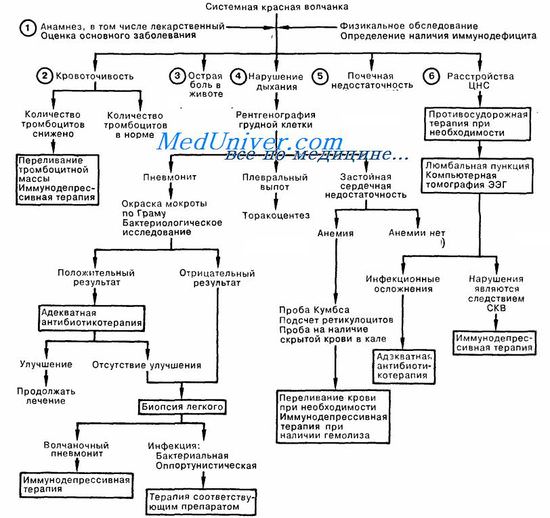
4. Нарушения дыхательной функции могут быть следствием банальных причин, но могут быть связаны с волчанкой: встречаются люпус-пневмониты, пневмониты вследствие развития оппортунистических инфекций, а также плевральный выпот вследствие серозита. Важно помнить, что инфекционные заболевания остаются наиболее частой причиной возникновения инфильтратов на рентгенограммах грудной клетки у больных с СКВ; лечение должно быть соответствующим. Нередко встречаются умеренно выраженные сердечно-сосудистые расстройства. Изредка люпус-перикардит приводит к образованию значительного перикардиального выпота. Возможно развитие бородавчатого эндокардита; его течение, как правило, бессимптомное; миокардит встречается редко. У больных с СКВ, принимающих стероиды, инфаркт миокарда может случиться в молодом возрасте. Проявлением острой аутоиммунной гемолитической анемии может быть застойная сердечная недостаточность.
5. Почечная недостаточность может возникать вследствие люпус-нефрита, при этом лечение проводится обычным путем. К некоторому улучшению состояния может привести иммуно-супрессивная терапия, за исключением терминальных стадий недостаточности.
6. Поражение ЦНС встречается у 25% больных с СКВ; проявления могут быть самыми разнообразными. Как и при поражении других систем, следует исключить неволчаночные причины, например судороги (16%) и параличи. Для исключения сосудистых нарушений, инфекционных и опухолевых процессов выполняют люмбальную пункцию и компьютерную томографию. Симптомы нарушений функции ЦНС при СКВ не являются специфичными и наблюдаются не всегда (например, повышение содержания белка в СМЖ, диффузное замедление на ЭЭГ, атрофия коркового слоя на компьютерной томограмме). Нейропсихические нарушения следует отличать от стероидного психоза.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Лихеноидный мукозит полости рта. Системная красная волчанка.
Белые поражения, вызванные раздражением электрическим током, имеют значительное сходство с красным плоским лишаем. Они бывают более выражены у лиц старше 30 лет и часто появляются на слизистой оболочке щёк в непосредственной близости от металлических конструкций (пломба, протез). Лёгкие поражения не сопровождаются какими-либо болезненными ощущениями, в то время как при образовании эрозий пациенты жалуются на жгучую боль. По гистологической картине эти поражения напоминают красный плоский лишай. Раньше причиной заболевания считали слабые электрические токи, которые индуцируются пломбой или зубным протезом, состоящими из разнородных металлов. Согласно современным представлениям, белые поражения обусловлены аллергической реакцией замедленного типа на металлы, например, ртуть, выступающие в роли антигена. Аналогичные поражения наблюдают при системном лечении некоторыми препаратами, в том числе содержащими металлы, входящими в состав зубных пломб и протезов. В таких случаях их называют лихеноидной лекарственной сыпью. Лечение заключается в замене пломбы новой, состоящей из другого материала, например, золота, фарфора, иономеров стекла или композитного материала. Прогноз хороший, заживление слизистой оболочки происходит в течение нескольких недель после устранения причины заболевания.
Системная красная волчанка.
Системная красная волчанка — диффузное заболевание соединительной ткани, характеризующееся образованием антинуклеарных антител, в том числе к нативной ДНК, которые участвуют в повреждении тканей. Выделяют три клинические формы заболевания: хроническую дискоидную красную волчанку, называемую также хронической кожной красной волчанкой и поражающую только кожу, системную красную волчанку, для которой характерно поражение многих органов и систем, и подострую кожную красную волчанку, характеризующуюся поражением кожи и лёгкими системными проявлениями. Причина ни одной из этих форм заболевания не установлена.
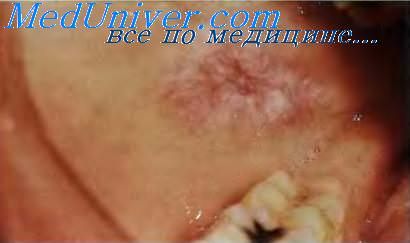
Системная красная волчанка
При хронической дискоидной красной волчанке поражаются только кожа и слизистые оболочки. Она имеет доброкачественное течение, её наблюдают в любом возрасте, но чаще у женщин старше 40 лет. Для клинической картины характерна эритематозная сыпь на носу и щеках, образующая фигуру бабочки. Кожные поражения могут локализоваться и на других участках, в частности в области лба, на скулах, волосистой части головы, ушных раковинах.
Течение дискоидной красной волчанки хроническое с периодами обострения и ремиссии. Для зрелых морфологических элементов характерны три зоны: атрофическая центральная, окаймлённая гиперкератотическим пояском, который, в свою очередь, окружён эритематозной периферической зоной. После заживления элементов центральная часть остаётся гипопигментированной вследствие повреждения меланоцитов в области эпидермально-дермального соединения и образования коллагена. Часто на поражённых участках появляются телеангиэктазии, угри, нежное шелушение, выпадают волосы. Поражение кожи ограничивается верхней половиной тела, преимущественно областью головы и шеи.
У 20—40% больных хронической дискоидной красной волчанкой отмечают также поражение слизистой оболочки полости рта, которое может предшествовать кожным проявлениям или появиться после них. На губах возникают эритематозные пятна, окаймлённые белым или серебристым шелушащимся краем; на открытой солнцу красной кайме нижней губы они, как правило, имеют первичный характер, в то время как на верхней губе бывают следствием распространения поражения с кожи. Основным элементом при поражении слизистой оболочки полости рта служат диффузные эритематозные бляшки, которые могут включать белые очаги, а также изъязвляться.
Иногда хроническая дискоидная красная волчанка проявляется изолированными красно-белыми бляшками. Наиболее часто поражения локализуются на слизистой оболочке щёк, реже — на языке, нёбе, деснах. Бляшки характеризуются атрофичной красной центральной частью, на которой иногда имеются вкрапления точечных белых пятен. Периферическая часть имеет неровные края и состоит из чередующихся красных и белых кератотических линий длиной до 1 см, отходящих в радиальном направлении. Эти поражения можно ошибочно принять за проявления красного плоского лишая, однако вовлечение в процесс ушных раковин позволяет исключить это заболевание. Изъязвления болезненны и требуют лечения. Больным рекомендуют избегать эмоционального стресса, переохлаждения, пребывания на солнце, употребления горячей и острой пиши. Хороший эффект отмечают при пользовании фотозащитными средствами, местном и системном применении глюкокортикоидов, противомалярийных препаратов и иммунодепрессантов. Больных, принимающих противомалярийные препараты, должен наблюдать офтальмолог.
При системных проявлениях красной волчанки больные жалуются на повышенную утомляемость, повышение температуры тела, боль в суставах. Часто отмечают генерализованное увеличение лимфатических узлов, возможны увеличение печени, селезёнки, периферическая невропатия, изменение картины крови. Важно избегать пребывания на солнце, так как это может спровоцировать обострение заболевания. Поражение почек и сердца, часто наблюдаемое при СКВ, может стать причиной смерти. СКВ может сопровождаться поражением кожи и слизистой оболочки полости рта, но переход дискоидной красной волчанки в системную наблюдают крайне редко. У больных СКВ часто выявляют синдром Шегрена, ревматоидный артрит и другие диффузные заболевания соединительной ткани. В дифференциальную диагностику при красной волчанке с поражением слизистой оболочки полости рта следует включать аллергический мукозит, кандидоз, лейкоплакию, эритролейкоплакию и красный плоский лишай. Гистологическое исследование биопсийного материала и иммунофлюоресцентное исследование позволяют подтвердить диагноз. При выполнении зубоврачебных вмешательств у больных СКВ, принимающих глюкокортикоиды, необходимо соблюдать осторожность, учитывая, что эти препараты замедляют заживление ран, повышают восприимчивость к инфекции и могут стать причиной адреналовых кризов, провоцируемых стрессом и способных вызвать сердечно-сосудистый коллапс. У этих больных повышен также риск кардиомиопатии, что может потребовать профилактики антибиотиками.
Читайте также:

