Скарлатина при пороке сердца
Обновлено: 18.04.2024
Инфаркт миокарда — острое заболевание, обусловленное возникновением одного или нескольких очагов ишемического некроза в сердечной мышце в связи с абсолютной или относительной недостаточностью коронарного кровотока. Большинство педиатров и кардиологов счи
Инфаркт миокарда — острое заболевание, обусловленное возникновением одного или нескольких очагов ишемического некроза в сердечной мышце в связи с абсолютной или относительной недостаточностью коронарного кровотока. Большинство педиатров и кардиологов считают, что инфаркт миокарда в детском возрасте относится к разделу казуистики. Атеросклероз коронарных артерий, являющийся основной причиной инфаркта миокарда у взрослых, у детей практически не встречается, за исключением случаев семейной гиперлипидемии [3, 6]. Именно поэтому у многих педиатров отсутствует настороженность при постановке данного диагноза. Интересно отметить, что Национальная медицинская библиотека США специально регистрирует каждый случай инфаркта миокарда у детей, описанный в мировой медицинской литературе [5].
Частота инфарктов миокарда у детей неизвестна. Однако это заболевание встречается значительно чаще, чем принято считать. Известно, например, что при врожденных пороках сердца, даже при отсутствии структурных аномалий коронарных сосудов на аутопсии, инфарктные участки в миокарде выявлялись в 75% случаев, при этом половина из них могла быть диагностирована клинически [4].
Если у взрослых основная причина инфаркта миокарда заключается в атеросклеротическом поражении коронарных артерий, то у детей этот этиологический фактор по степени распространенности занимает последнее место. Наиболее частыми причинами инфаркта миокарда являются воспалительные заболевания коронарных артерий — коронариты и аномалии развития коронарных артерий. Перечислим основные причины инфаркта миокарда у детей.
- Коронариты, в том числе: при неревматических кардитах, при инфекционных заболеваниях, болезнь Кавасаки, болезнь Такаясу, системная красная волчанка, узелковый периартериит, неспецифический аортоартериит.
- Аномалии коронарных артерий, в том числе: отхождение левой коронарной артерии от легочной (синдром Бланда-Уайта-Гарленда), аномалии числа коронарных артерий, другие аномалии коронарных артерий.
- Травма сердца и коронарных артерий.
- Феохромоцитома.
- Врожденный порок сердца (надклапанный стеноз аорты).
- Гипертрофическая кардиомиопатия.
- Опухоль сердца.
- Инфекционный эндокардит.
В настоящее время выделяют инфаркт миокарда с Q-зубцом (трансмуральный инфаркт миокарда) и инфаркт миокарда без Q-зубца (мелкоочаговый, субэндокардиальный, интрамуральный). В первом случае на ЭКГ формируется патологический зубец Q или комплекс QS, во втором — изменения касаются лишь зубца T и сегмента S-T.
В диагнозе инфаркта миокарда указываются также особенности его течения (первичный, повторный, рецидивирующий) и осложнения.
По локализации выделяют: передний (верхушечный, боковой, септальный, распространенный передний), нижний (диафрагмальный), задний и нижнебазальный. Указанные локализации относятся к левому желудочку, наиболее часто страдающему при этом заболевании. Инфаркт правого желудочка развивается крайне редко.
Клиника
Клинические проявления инфаркта миокарда любой этиологии у детей сходны: это приступы внезапного беспокойства у детей раннего возраста и типичный ангинозный статус у старших. Значительно реже инфаркт протекает без болевого синдрома. У детей при осмотре, как правило, отмечаются бледность кожных покровов, цианоз, похолодание конечностей, потливость, тахипноэ или диспноэ, артериальная гипотензия. У некоторых детей могут отмечаться признаки дисфункции желудочно-кишечного тракта, имеющие рефлекторное происхождение, — боли в животе, тошнота, рвота, диарея. Развиваются признаки недостаточности кровообращения преимущественно по малому кругу (тахикардия, одышка, кашель). Несколько реже у больных выявляется увеличение печени, реже — отеки ног, что свидетельствует о присоединении правожелудочковой недостаточности.
У некоторых детей возможно развитие кардиогенного шока (холодная кожа серо-бледного цвета, покрытая липким потом, олигоанурия, нитевидный пульс, уменьшение пульсового давления менее 20—30 мм рт. ст., снижение систолического давления). Возникающее при кардиогенном шоке снижение коронарного кровотока усугубляет снижение насосной функции сердца и течение кардиогенного шока, развития отека легких — главных причин смерти при инфаркте миокарда.
Течение инфаркта миокарда может осложняться возникновением аритмий (экстрасистолия, мерцательная аритмия, пароксизмальные тахикардии, фибрилляция желудочков), тромбоэмболиями, развитием острой и формированием хронической аневризмы сердца.
Диагностические критерии
Диагноз инфаркта миокарда подтверждается с помощью инструментальных и лабораторных методов исследования.
При локализации некроза в области передней стенки левого желудочка характерны изменения на ЭКГ в отведениях I, aVL, V1-6: для инфаркта боковой стенки — в отведениях I, aVL, V5,6, при поражении области перегородки выявляют изменения в отведениях V1,2(3), при инфаркте в области верхушки сердца — в отведениях V3,4. Для инфаркта нижней стенки характерны изменения в отведениях II, III, aVF.
Резорбционно-некротический синдром при инфаркте миокарда подтверждается результатами общеклинического и биохимического исследований крови: лейкоцитоз со сдвигом лейкоцитарной формулы влево, увеличения СОЭ с третьего–пятого дня, повышения в крови активности креатинфосфокиназы (КФК) и ее МВ-фракции, аминотрансфераз (особенно аспарагиновой и в меньшей степени аланиновой) и лактатдегидрогеназы (общей) и ее первого, второго изоферментов. Оценка состояния системы гемостаза и фибринолиза позволяет выявить гиперкоагуляционные изменения.
В последние годы широко используются новые маркеры — тропонин Т, тропонин I и миоглобин. Тропонин является белковым комплексом, регулирующим мышечное сокращение, и состоит из 3 субъединиц — тропонин Т, тропонин C и тропонин I. В начале 90-х гг. были разработаны иммунологические методы, позволяющие с помощью моноклональных антител различать тропонины Т и I кардиомиоцитов и других поперечно-полосатых мышечных волокон. Считается, что тропонины Т и I являются наиболее информативными и чувствительными маркерами некроза сердечной мышцы. Их уровень повышается в крови уже через 2-3 ч после инфаркта миокарда, может увеличиваться в 300–400 раз по сравнению с нормой и сохраняется повышенным в течение 10 –14 дней. К сожалению, эти методы еще очень редко используются в диагностике инфарктов миокарда у детей.
Диагноз инфаркта миокарда подтверждается данными эхокардиографии. Критериями диагностики является наличие зон акинезии (область некроза), гипокинезии, асинхронности сокращений отдельных сегментов левого желудочка в области ишемического повреждения. В дальнейшем у некоторых больных может выявляться аневризма левого желудочка. В зонах неповрежденных сегментов определяются явления дискинезии или гиперкинезии компенсаторного характера. В тех случаях, когда не удается четко визуализировать начальные участки отхождения левой коронарной артерии, можно думать об аномалии коронарных артерий. Рентгенография грудной клетки малоинформативна для диагностики инфаркта миокарда. Кардиомегалия свидетельствует об основном заболевании (кардит, врожденный порок сердца, аномальное отхождение коронарных артерий), а также может быть связана с аневризмой сердца. У пациентов с левожелудочковой недостаточностью отмечается усиление сосудистого рисунка.
Известно, что коронарография и вентрикулография дают наиболее точную диагностику поражения коронарных артерий [2]. Эти исследования позволяют четко установить локализацию, характер и степень поражения коронарных артерий, выявить снижение сократительной способности миокарда, иногда аневризму левого желудочка. К сожалению, они недостаточно используются в детской кардиологии.
В последнее время для диагностики инфаркта миокарда стали применять сцинтиграфию миокарда или позитронно-эмиссионную томографию миокарда. Эти методы позволяют неинвазивно оценить перфузию миокарда, объем и локализацию деструктивных изменений, выявить метаболические нарушения.
Воспалительные заболевания коронарных сосудов
Одной из наиболее частых причин инфаркта миокарда у детей являются воспалительные заболевания коронарных артерий — коронариты. Истинная распространенность коронаритов в связи со сложностью диагностики не известна, в большинстве случаев этот диагноз ставят на аутопсии. Воспалительный процесс чаще захватывает одновременно 3 оболочки сосуда [1]. Коронариты нередко сопутствуют кардитам и могут привести к развитию инфаркта миокарда [4]. Так, по нашим данным, у 6 детей раннего возраста на фоне течения острого кардита возникла клиника типичного инфаркта миокарда.
Острые коронариты могут встречаться при различных инфекционных заболеваниях (грипп, скарлатина, тифы и др.). Мы наблюдали мальчика С., 6 мес., с генерализованной формой сальмонеллезной инфекции, у которого через 2 нед. от начала заболевания отмечался трансмуральный инфаркт миокарда левого желудочка, с последующим развитием аневризмы левого желудочка. На рисунке 3 представлена электрокардиограмма больного С., 6 мес., с трансмуральным инфарктом миокарда, причиной которого был коронарит, возникший на фоне генерализованной сальмонеллезной инфекции.
Основными критериями постановки диагноза болезни Кавасаки являются лихорадка свыше 38°С и выше на протяжении 5 дней и более в сочетании хотя бы с 4 из 5 перечисленных ниже симптомов:
Перечисленные симптомы наблюдаются в первые 2–4 нед. заболевания. Поражение сердца может быть по типу миокардита и/или коронарита с развитием множественных аневризм и окклюзий коронарных артерий, что в последующем может привести к инфаркту миокарда. Под нашим наблюдением находились 3 ребенка с болезнью Кавасаки, коронаритом, инфарктом миокарда.
Причинами коронаритов могут быть неспецифический аортоартериит, узелковый периартериит, инфекционный эндокардит, геморрагический васкулит.
Неспецифический аортоартериит (болезнь Такаясу, болезнь отсутствия пульса, панартериит множественный облитерирующий) характеризуется воспалительными и деструктивными изменениями в стенке дуги аорты и ее ветвей, сопровождающимися их стенозированием и ишемией кровоснабжающих органов. При этом нередко отмечается и поражение коронарных артерий. В начале заболевания возникают слабость, похудание, головокружение, боль в груди и конечностях, анемия, лихорадка, перикардит, иридоциклит, отеки. В дальнейшем могут появиться жалобы на онемение конечностей, в ряде случаев присоединяется неврологическая симптоматика. При обследовании выявляется отсутствие пульса, чаще всего в зоне радиальной, ульнарной и сонной артерий. Характерна асимметрия давления. Диагностике артериита помогает аускультация сонных, подключичных артерий и брюшной аорты. Заподозрить сопутствующий коронарит помогают упорные боли в сердце, ишемические и рубцовые изменения на ЭКГ.
В патогенезе инфаркта миокарда при болезни Такаясу, наряду с коронаритом и последующим стенозированием левой или правой коронарных артерий, имеют значение артериальная гипертензия, а также относительная коронарная недостаточность из-за гипертрофии миокарда.
При аортоартериите в процесс может вовлекаться и клапанный аппарат сердца. Так, у 10-летней девочки отмечались аортальная регургитация, возникшая вследствие воспаления аорты и кольца аортального клапана, поражения митрального клапана, явления миокардита с последующей трансформацией в дилатационную кардиомиопатию, с признаками недостаточности кровообращения IIБ степени. Инфаркт миокарда возник на фоне злокачественной артериальной гипертензии, обусловленной стенотической и тромботической окклюзией сонных и почечных артерий.
Поражение коронарных артерий может возникать при диффузных заболеваниях соединительной ткани. Мы наблюдали девочку С., 15,5 лет, с системной красной волчанкой (больна в течение 7 лет). У пациентки возникли давящие боли в области сердца, которые врач поликлиники объяснил остеохондрозом. И только через 2 дня была сделана ЭКГ, на которой были выявлены изменения, свидетельствующие о субэндокардиальном инфаркте миокарда боковой стенки и верхушки левого желудочка. Проведенное обследование исключило наличие антифосфолипидного синдрома как возможной причины инфаркта миокарда у больной с системной красной волчанкой. По всей вероятности, инфаркт миокарда в данном случае был связан с хроническими воспалительными изменениями в мелких или крупных венечных сосудах, которые могли привести к постепенному сужению просвета и тромбозу. Нужно заметить, что через год после перенесенного инфаркта миокарда отмечалась полная нормализация картины ЭКГ.
Аномалии коронарных артерий
Наиболее распространенной врожденной патологией коронарных сосудов является аномальное отхождение левой коронарной артерии от легочной (АОЛКА от ЛА) — синдром Бланда-Уайта-Гарленда. Частота этого синдрома, по данным литературы, составляет 0,25—0,5% от всех врожденных пороков сердца [1, 4]. Согласно одной из гипотез, в основе данной патологии лежит неправильная закладка одной из коронарных артерий в той части ствола, из которой в дальнейшем образуется легочная артерия, деление основного ствола не нарушено. Мы наблюдали 7 больных в возрасте от 2 мес. до 6 лет, причиной инфаркта миокарда у которых являлись аномалии коронарных артерий, из них у 5 детей — аномальное отхождение левой коронарной артерии от легочной — синдром Бланда-Уайта-Гарленда.
На рентгенограмме органов грудной клетки у детей с АОЛКА от ЛА отмечается кардиомегалия, преимущественно за счет левых отделов. Косвенным свидетельством аномального отхождения коронарных артерий является отсутствие возможности четко визуализировать начальные участки левой коронарной артерии при ЭхоКГ [2].
Диагноз подтверждается с помощью селективной коронарографии (контрастное вещество вводят через расширенный ствол правой коронарной артерии, при этом видно ретроградное заполнение системы левой коронарной артерии через межкоронарные анастомозы, с последующим контрастированием легочной артерии).
Травма сердца и коронарных артерий
Следует помнить, что при закрытой травме сердца может быть повреждена проводящая система, хотя нередко признаки ее повреждения (внутрижелудочковая блокада, полная и неполная атриовентрикулярная блокада) могут появиться только через несколько месяцев или лет после травмы. Это диктует необходимость регулярного осмотра врачом в течение длительного времени (включая электрокардиографическое обследование) детей с травмами грудной клетки.
Иногда инфаркт миокарда может возникать у больных с феохромоцитомой. Развитию инфаркта миокарда в этих случаях способствует длительная гиперкатехоламинемия, которая сопровождается высокой артериальной гипертензией, гипертрофией миокарда левого желудочка, утолщением стенок коронарных артерий. Определенное значение в развитии инфаркта миокарда имеют также явления коронароспазма и гиперкоагуляционные изменения, связанные с гиперкатехоламинемией. По нашим наблюдениям, феохромоцитома была причиной развития инфаркта миокарда у мальчика 11 лет.
Нередко инфаркт миокарда встречается у детей с врожденными пороками сердца (стеноз аорты). Он может возникать вследствие дефицита коронарного кровотока. Мы наблюдали в течение нескольких лет больного с синдромом Вильямса-Бойрена, врожденным пороком сердца (надклапанный стеноз аорты), у которого в 13 лет развился инфаркт миокарда с летальным исходом.
Мы наблюдали также нескольких пациентов, у которых инфаркт миокарда осложнил течение таких тяжелых заболеваний, как гипертрофическая кардиомиопатия, опухоль сердца, инфекционный эндокардит. Так, у девочки 4 лет с инфекционным эндокардитом и крупными вегетациями на аортальном клапане течение болезни осложнилось эмболией левой коронарной артерии и развитием острого трансмурального инфаркта миокарда. Инфаркт миокарда на фоне опухоли сердца (миксома левого предсердия) развился у мальчика 6 лет.
Таким образом, другие заболевания могут осложнять развитие инфаркта миокарда, который, в свою очередь, способен влиять на течение многих серьезных заболеваний. Поэтому со стороны врачей требуется повышенное внимание в таких случаях.
По вопросам литературы обращайтесь в редакцию.
Л. В. Царегородцева, кадидат медицинских наук, доцент
РГМУ, Москва
Скарлатина (лат. scarlatina) — острая антропонозная инфекция с аэрозольным механизмом передачи возбудителя, которой свойственны острое начало, лихорадка, интоксикация, тонзиллит (экссудативный фарингит), и мелкоточечная сыпь.
Исключая: J02.0 Стрептококковый фарингит
Период протекания
Минимальный инкубационный период (дней): 1
Максимальный инкубационный период (дней): 12
Инкубационный период чаще всего 2-5 дней. Длительность заболевания варьируется в зависимости от формы и тяжести. При нетяжёлых, неосложнённых формах все симптомы проходят через 2-4 недели.
Классификация
Единая классификация отсутствует. Существующие варианты классификации не имеют клинического преимущества друг перед другом.
Пример классификации 1.
По типу
1 Типичные.
2 Атипичные (экстратонзиллярные):
-ожоговая;
-раневая;
-послеродовая;
-послеоперационная.
По тяжести:
1.Легкая форма.
2.Среднетяжелая форма.
3.Тяжелая форма:
-токсическая;
-септическая;
-токсико-септическая.
3.1.Критерии тяжести:
-выраженность синдрома интоксикации;
-выраженность местных изменений.
По течению (по характеру)
1. Гладкое.
2. Негладкое:
- с осложнениями;
- с наслоением вторичной инфекции;
- с обострением хронических заболеваний.
Пример классификации 2.
I. Типичные формы
По тяжести:
а) легкая;
б) среднетяжелая.
II. По течению
1. Без аллергических волн и осложнений.
2. С аллергическим волнами.
3. С осложнениями:
а) аллергического характера (нефрит, синовит, реактивный лимфаденит, миокардит);
б) гнойными.
4. Абортивное течение
Атипичные формы
1. Стертая
2. С агравированными симптомами (гипертоксическая, геморрагическая) при которых процесс происходит так бурно, как разовьется типичная клиника скарлатины (ангина, сыпь и т. д.).
3. Экстрабуккальная (ожоговая, раневая, послеродовая) начинаются бурно, с отсутствием ангины, либо ее слабой выраженностью.
Этиология и патогенез
Возбудитель — β-гемолитический стрептококк группы А (S. pyogenes).
Возбудитель проникает в организм человека через слизистую оболочку зева и носоглотки; в редких случаях возможно заражение через слизистую оболочку половых органов или повреждённую кожу (экстрабуккальная скарлатина). В месте адгезии бактерий формируется воспалительно-некротический очаг. Развитие инфекционно-токсического синдрома обусловлено поступлением в кровоток эритрогенного токсина (токсина Дика), а также действием пептидогликана клеточной стенки стрептококков. Вследствие токсинемии происходит генерализованное расширение мелких сосудов во всех органах, в том числе в кожных покровах и слизистых оболочках, и возникает характерная сыпь. В результате выработки, накопления антитоксических антител при развитии инфекционного процесса и связывания ими токсинов ослабевают симптомы интоксикации и постепенно исчезает сыпь. Одновременно возникают умеренные признаки периваскулярной инфильтрации и отёка дермы. Эпидермис пропитывается экссудатом, и клетки эпидермиса ороговевают, что приводит к шелушению кожи после угасания скарлатинозной сыпи. Крупнопластинчатый характер шелушения в толстых слоях эпидермиса на ладонях и подошвах можно объяснить сохранением прочной связи между ороговевшими клетками в этих местах.
Компоненты клеточной стенки стрептококка (групповой А-полисахарид, пептидогликан, белок М) и внеклеточные продукты (стрептолизины, гиалуронидаза, ДНКаза и др.) обусловливают развитие реакций ГЗТ, аутоиммунных реакций, формирование и фиксацию иммунных комплексов, нарушения системы гемостаза. Во многих случаях их можно считать причиной развития миокардита, гломерулонефрита, артериитов, эндокардита и других осложнений иммунопатологического характера. Из лимфатических образований слизистой оболочки ротоглотки возбудители по лимфатическим сосудам попадают в регионарные лимфатические узлы, где происходит их накопление, сопровождающееся воспалительными реакциями с очагами некроза и лейкоцитарной инфильтрации. Последующая бактериемия может вызвать попадание микроорганизмов в различные органы и системы и формирование гнойно-некротических процессов в них (гнойный лимфаденит, отит, поражения костной ткани височной области, твёрдой мозговой оболочки, височных синусов и др.).
Эпидемиология
Резервуар и источник инфекции — больной ангиной, скарлатиной и другими клиническими формами респираторной стрептококковой инфекции, а также здоровые носители стрептококков группы А. От больных скарлатиной стрептококки начинают выделяться с первого дня заболевания. Максимальное выделение возбудителей отмечается на первой неделе заболевания, а затем по мере угасания клинических симптомов происходит уменьшение выделения стрептококков и к 3-5 неделе заразительность резко снижается, если больной не становится носителем. Носительство стрептококков группы А широко распространено в популяции (15-20% здорового населения); многие из носителей выделяют возбудитель на протяжении длительного времени (месяцы и годы). Реконвалесцентное носительство стрептококков формируется в среднем у 3-5% лиц, переболевших скарлатиной. Длительное носительство (несколько месяцев) встречается относительно редко – у 1-2% перенесших скарлатину. Период носительства может удлиняться при наличии сопутствующих заболеваний – ринита, синусита, тонзиллита и др. Наличие здорового носительства стрептококков подтверждено многочисленными наблюдениями. Особенно часто такие носители выявляются в окружении больного, а также во вновь сформированных организованных коллективах. Отмечается увеличение частоты здорового носительства в осенний период. В отдельных ситуациях здоровые носители стрептококков могут представлять реальную опасность. Однако эпидемическую значимость этой категории источников инфекции при скарлатине не следует переоценивать. Это связано с тем, что массивность выделения стрептококков у здоровых носителей значительно меньше, чем у больных скарлатиной и подавляющее большинство здоровых носителей освобождается от стрептококков уже в течение первой недели.
Механизмы передачи — аэрозольный (воздушно-капельный путь) и контактный (пищевой и контактно-бытовой). Заражение происходит при тесном длительном общении с больным или носителем.
Пол. Различий не выявлено.
Раса.Различий не выявлено.
Возраст. Основное число заболевших составляют дети (около 96%). Наиболее часто встречается в возрасте 3-8 лет. Заболеваемость детей в возрасте менее 2 лет невысока (наличие материнских антител, пребывание дома и пр.).
Естественная восприимчивость людей высока. Скарлатина возникает у лиц, не имеющих антитоксического иммунитета, при их инфицировании токсигенными штаммами стрептококка, продуцирующими эритрогенные токсины типов А, В и С. Индекс контагиозности – 40% (не учитываются стертые и иннапарантные формы).
Постинфекционный иммунитет типоспецифический; при инфицировании стрептококками А другого серовара возможно повторное заболевание.
Факторы и группы риска
- Детский возраст
- Пребывание в организованных коллективах
- Контакт с больным или носителем стрептококковой инфекции
Клиническая картина
Клинические критерии диагностики
лихорадка, мелкоточечная сыпь, боль в горле, фарингит, тонзиллит, лимфаденит, язык малинового цвета, шелушение кожи после исчезновения сыпи.
Cимптомы, течение
Типичным считают острое начало. В некоторых случаях уже в первые часы болезни температура повышается до высоких цифр, возникают озноб, слабость, недомогание, головная боль, тахикардия, иногда — боли в животе и рвота. При высокой лихорадке в первые дни заболевания больные возбуждены, эйфоричны, подвижны или, наоборот, вялы, апатичны, сонливы. Следует подчеркнуть, что при современном течении скарлатины температура тела может быть невысокой.
Наряду с типичной скарлатинозной сыпью можно отметить мелкие везикулы и макулопапулёзные элементы. Сыпь может возникать поздно, лишь на 3-4-й день болезни, или отсутствовать. К 3-5-м суткам самочувствие больного, улучшается, температура начинает постепенно снижаться, сыпь бледнеет, постепенно исчезает и к концу 1-2-й недели сменяется мелкочешуйчатым (на ладонях и подошвах — крупнопластинчатым) шелушением кожи.
Интенсивность экзантемы и сроки её исчезновения различны. Иногда при лёгком течении скарлатины скудная сыпь исчезает через несколько часов после возникновения. Выраженность и длительность шелушения кожи прямо пропорциональны обилию предшествующей сыпи.
Типичные формы делятся на:
-легкие;
-среднетяжелые;
-тяжелые (токсические, септические, токсико-септические)
Критерием тяжести является выраженность симптомов интоксикации и местных воспалительных явлений в ротоглотке.
В современных условиях легкая форма скарлатины встречается наиболее часто (80-90%) и характеризуется:
-слабой выраженностью интоксикационного синдрома, лихорадкой не выше 38,5оС в начальном периоде
-катаральной ангиной;
-необильной, неяркой мелкоточечной сыпью, исчезающей к 3—4-му дню;
-отсутствием фазности вегетативных изменений со стороны сердечно-сосудистой системы;
-клиническое выздоровление – к концу первой недели болезни.
Среднетяжелая форма (10-20%) характеризуется:
-выраженными симптомами интоксикации, лихорадкой до 39°С, повторной рвотой;
-фолликулярной или лакунарной ангиной;
-регионарным лимфаденитом;
-яркой, обильной мелкоточечной сыпью на гиперемированном фоне кожи, которая держится 5-6 суток;
-выражена фазность вететативных изменений сердечно-сосудистой системы;
-токсические изменения со стороны печени проявляются нарушениями белкового обмена и гиперферментемией;
-выздоровление наступает через 2-3 недели.
Тяжелая форма (0,5%) встречается в настоящее время редко и характеризуется:
-резко выраженными явлениями токсикоза (токсическая форма);
-преобладанием септических поражений (септическая форма);
либо протекает как токсико-септическая форма (сочетанием указанных явлений).
Токсическая форма характеризуется:
-гипертермией 40°С и выше, многократной рвотой, бредом, спутанностью сознания, судорогами, менингеальными симптомами;
-яркой сыпью, нередко с геморрагиями,
-быстро нарастающими расстройствами со стороны сердечно-сосудистой системы (изменения на ЭКГ, соответствуют токсическому миокардиту);
-возможным развитием симпатикопареза (резко падает АД, сыпь цианотичная);
С первых часов болезни возможно развитие шока (при молниеносной гипертоксической форме), при которой гибель больного может наступить в течение нескольких часов или первых су ток на фоне развития ДВС-синдрома и ОПН.
При септической форме:
-резко выражены воспалительные (гнойно-некротические) изменения, исходящие из первичного очага, в виде глубоких некрозов в области миндалин, дужек и основания язычка;
-регионарные лимфоузлы резко болезненны, увеличены и уплотнены;
-возможно развитие некроза тканей, окружающих шейные лимфоузлы (периаденита и аденофлегмоны), а также этмоидита, отита, мастоидита, остеомиелита.
Токсико-септическая форма характеризуется выраженной тяжестью общих и местных проявлений скарлатины.
К атипичным относят: стертые (легчайшие) формы со слабой и кратковременной выраженностью клинических симптомов болезни, в т.ч. с отсутствием сыпи, которые могут диагностироваться только в очаге скарлатины;
-экстрабуккальную (экстрафарингеальную) скарлатину — раневую, ожоговую, послеродовую, при которой отсутствуют симптомы ангины, нo насыщеннее сыпь в месте входных ворот инфекции;
-аггравированные формы (самые тяжелые) — геморрагическую и гипертоксическую (с развитием ДВС-синдрома и инфекционно токсического шока).
По течению скарлатина может быть:
-гладкое (без аллергических волн и осложнений);
-с осложнениями (аллергическими, гнойными);
-с аллергическими волнами;
-рецидив скарлатины.
Гнойные осложнения могут быть ранними (1 неделя) и поздними (2-3 неделя) - см. осложнения
Особенности течения скарлатины у детей грудного и раннего возраста
У детей грудного возраста с остаточным трансплацентарным иммунитетом заболевание протекает:
-как рудиментарная (стертая) форма с минимальной выраженностью интоксикации;
-с необильной и быстро исчезающей сыпью
-при мало заметном шелушении или без него
У неиммунных к скарлатине детей раннего возраста заболевание может протекать:
-по типу септической формы с гнойно-некротическими осложнениями;
-редко встречаются проявления аллергического синдрома.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Отек легких: причины появления, при каких заболеваниях возникает, диагностика и способы лечения.
Определение
Отек легких определяется как жизнеугрожающее состояние, для которого характерен процесс накопления внесосудистой жидкости в легких. Отек может развиться внезапно при большой и разнообразной по своей природе группе заболеваний и нарастать стремительно.
Функции легочного кровообращения – газообмен и фильтрация крови, регуляция водного и электролитного баланса, участие в метаболических процессах. Транспорту крови способствует низкое давление в системе малого круга кровообращения и относительно низкие показатели сопротивления сосудов току крови.
Жидкость из кровеносных сосудов просачивается за их пределы в окружающие ткани либо из-за слишком высокого давления в кровеносных сосудах, либо из-за недостаточного количества белков в кровотоке, чтобы удерживать жидкость в плазме крови.
Непосредственно за пределами мелких кровеносных сосудов в легких находятся крошечные воздушные мешочки – альвеолы. Альвеолы разделены тонкими эластичными стенками (мембранами), внутри которых проходят мельчайшие кровеносные сосуды (капилляры), позволяющие молекулам кислорода и углекислого газа перемещаться через мембраны. Жидкость попадает в альвеолы в том случае, если мембраны теряют свою целостность, что приводит к затруднению дыхания и плохому насыщению крови кислородом.
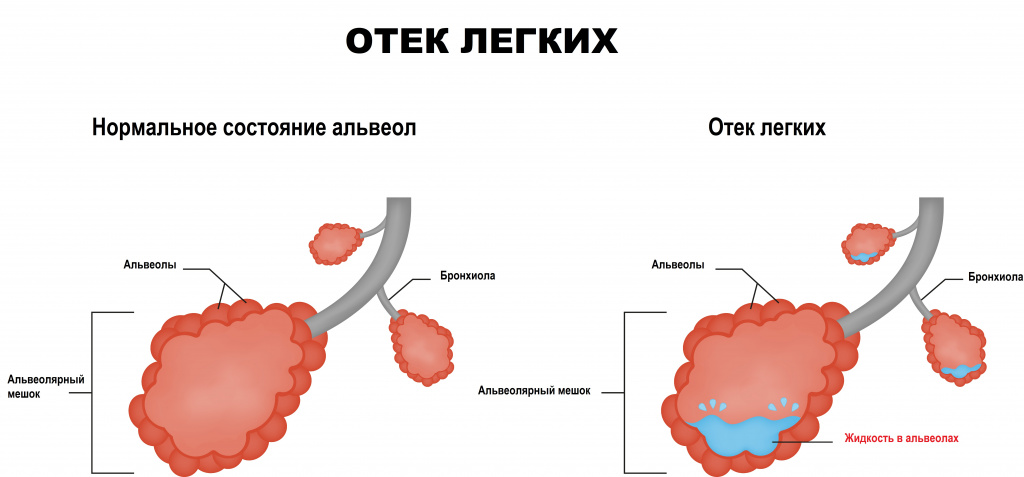
Выделяют два патогенетических процесса, с которыми связывают развитие отека легких:
Первый обусловлен повышением гидростатического давления в микрососудах малого круга кровообращения. Жидкость, электролиты и белки выходят за пределы сосудистой стенки и аккумулируются в интерстициальном (межсосудистом) пространстве легкого. На следующем этапе накопление жидкости происходит на поверхности альвеол, что становится причиной резкого ухудшения функции газообмена в легких и приводит к развитию гипоксемии.
Второй процесс связан с нарушением проницаемости альвеолярно-капиллярной мембраны из-за острого повреждения легочной ткани, которое может происходить при сепсисе, травме, пневмонии и некоторых других заболеваниях. Этот процесс также сопровождается гипоксемией и одышкой различной степени выраженности. В конечной фазе развития отека легких происходит аномальное накопление белков, в первую очередь альбуминов, в альвеолярной жидкости.
Разновидности отека легких
Кардиогенный отек легких встречается преимущественно при заболеваниях сердца или сосудов как осложнение острой сердечной недостаточности и связан с повышением гидростатического давления. У больного человека можно наблюдать тахикардию, кашель и одышку, которые возникают вследствие систолической или диастолической дисфункций левого желудочка.
Некардиогенный отек легких развивается вследствие повышенной проницаемости сосудистой стенки альвеолярных капилляров. Основным клиническим проявлением является развитие острого респираторного дистресс-синдрома.
По варианту течения выделяют следующие виды отека легких:
- Молниеносный – развивается в течение нескольких минут, в большинстве случаев приводит к летальному исходу.
- Острый – отмечается быстрое (на протяжении 4 часов) нарастание выраженности клинических симптомов. Вероятность летального исхода довольно высока и возникает на фоне инфаркта, черепно-мозговой травмы, анафилактического шока.
- Подострый – имеет волнообразное течение, характеризуется чередованием активных и спокойных периодов. Причиной часто является печеночная недостаточность. Имеет достаточно благоприятный прогноз, особенно при своевременном начале мероприятий неотложной помощи.
- Затяжной – симптомы нарастают в течение 12 часов со стертой клинической картиной, что значительно затрудняет диагностику. Основой являются хроническая сердечная недостаточность или заболевания бронхолегочной системы.
К основным причинам развития кардиогенного отека легких относятся:
- инфаркт миокарда с подъемом сегмента ST электрокардиограммы;
- гипертонический криз;
- пароксизм мерцательной аритмии (эпизод, длящийся от 30 секунд до семи дней, проходит самостоятельно или при помощи лечения).
- недостаточность митрального клапана (отрыв хорды сосочковой мышцы).
- постинфарктный и атеросклеротический кардиосклероз с систолической сердечной недостаточностью;
- диастолическая дисфункция миокарда у пожилых больных;
- систолическая и диастолическая дисфункция миокарда у больных с кардимиопатией или миокардитом;
- постоянная форма мерцательной аритмии;
- врожденные и приобретенные пороки левых отделов сердца;
- поражения клапанного аппарата, особенно митрального клапана, вследствие ревмокардита, инфекционного эндокардита, атеросклероза.
Основные легочные причины и факторы риска острого респираторного дистресс-синдрома:
- пневмония,
- вирус COVID-19,
- тромбоэмболия легочной артерии,
- ингаляционная травма,
- аспирационный синдром,
- травма грудной клетки,
- респираторные вирусные заболевания,
- эмфизема легких,
- бронхиальная астма,
- туберкулез легких,
- рак легких или метастазы в легкие.
- тяжелый сепсис и септический шок,
- переливание крови и кровезаменителей,
- большая кровопотеря,
- черепно-мозговые травмы, множественные и обширные травмы, ожоги,
- острое нарушение мозгового кровообращения,
- менингит, энцефалит,
- панкреонекроз,
- острая почечная недостаточность, острый гломерулонефрит,
- отравление химическими веществами, лекарственными средствами, алкоголем, наркотическими веществами,
- инфекционные заболевания, протекающие с тяжелой интоксикацией (грипп, корь, дифтерия, скарлатина, коклюш, столбняк, брюшной тиф),
- цирроз печени,
- патология беременных (эклампсия, синдром гиперстимуляции яичников),
- анафилактический шок,
- иммерсионный отек легких, вызванный плаванием на глубине.
В детском возрасте проблемы с сердцем наблюдаются намного реже, чем во взрослом. Поэтому основными причинами отека легких становятся заболевания дыхательной системы или серьезные травмы.
К каким врачам обращаться при отеке легких
Диагностика и обследования при отеке легких
Для установления диагноза обычно достаточно проведения клинического обследования и рентгенографии грудной клетки.
Рентгенологическое исследование структуры легких с целью диагностики различных патологий.
Информацию из данного раздела нельзя использовать для самодиагностики и самолечения. В случае боли или иного обострения заболевания диагностические исследования должен назначать только лечащий врач. Для постановки диагноза и правильного назначения лечения следует обращаться к Вашему лечащему врачу.
Пороки сердца: причины появления, симптомы, диагностика и способы лечения.
Определение
Порок сердца определяется как атипичное или аномальное строение его структур (камер, клапанов, крупных сосудов), являющееся следствием нарушений закладки и развития (врожденный порок сердца) либо разнообразных патологических изменений (приобретенный порок сердца). В результате формирования данной патологии нарушается работа сердца и формируется кислородная недостаточность органов и тканей организма, которая в конечном счете может привести к сердечной недостаточности.
Причины появления пороков сердца
У человека кровь, возвращающаяся к сердцу от всех органов и тканей (кровь, бедная кислородом), проходит через правое предсердие и затем через правый желудочек в легочную артерию, а оттуда поступает в легкие. В легких кровь обогащается кислородом, высвобождает углекислый газ и поступает в левое предсердие и левый желудочек, а оттуда перекачивается ко всем органам и тканям через аорту, а затем через артерии более мелкого калибра.
Работоспособность сердечной мышцы зависит от функционирования клапанов, которые при ее сокращении беспрепятственно пропускают кровь в следующий отдел, а при расслаблении не позволяют крови поступать обратно.
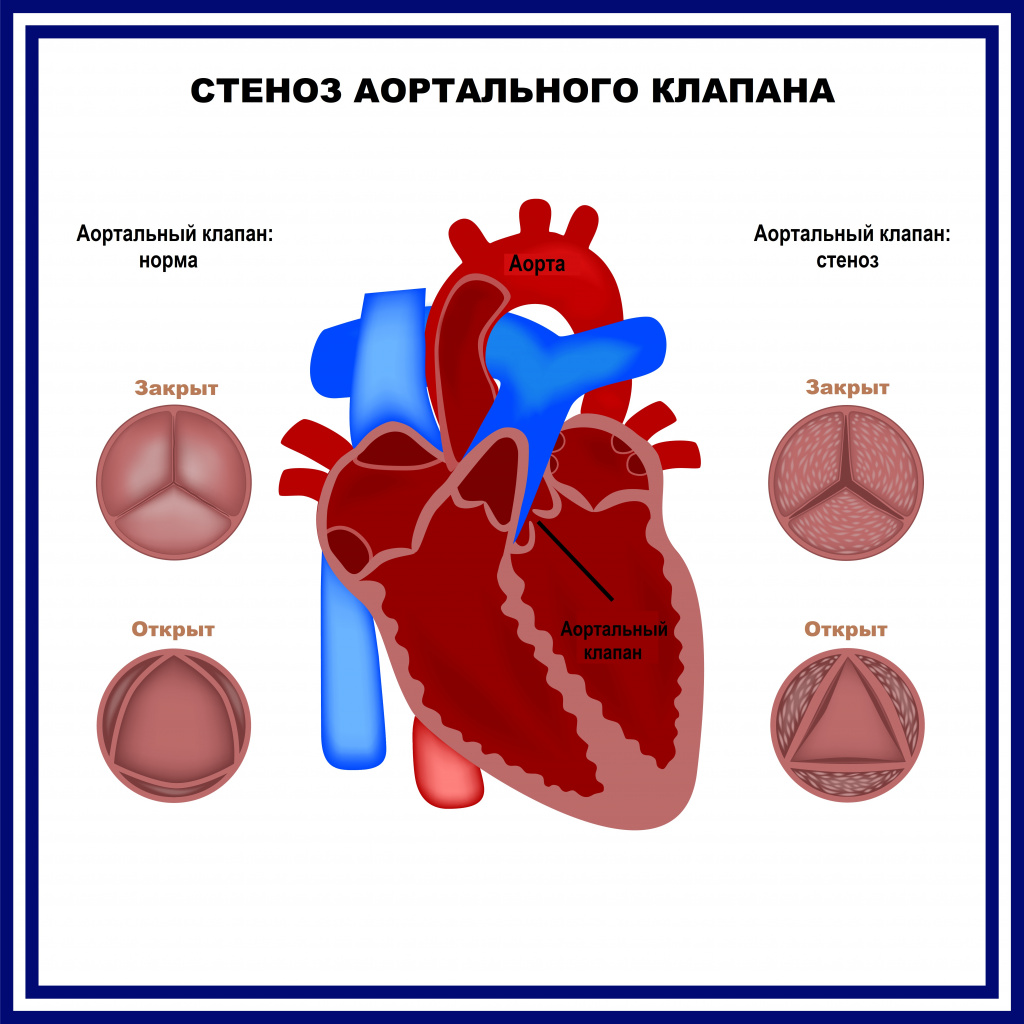
Врожденные пороки сердца весьма разнообразны. Описано более полутора сотен различных вариантов нетипичного строения сердца. Примерно один из 100 младенцев рождается с пороком сердца. Часто встречающимися патологиями сердца, диагностированными в младенчестве и детстве, являются дефекты межпредсердной и межжелудочковой перегородок (отверстия между камерами сердца). Нередко дефекты сочетаются с аномалиями клапанного аппарата сердца или крупных сосудов. Наиболее распространенным врожденным пороком сердца является двустворчатый аортальный клапан, который открывается при каждом сердечном сокращении, давая крови возможность течь от сердца ко всем органам. Нормальный аортальный клапан имеет три створки.
Двустворчатый аортальный клапан обычно не вызывает проблем в младенчестве или детстве, поэтому часто диагностируется только во взрослом возрасте.
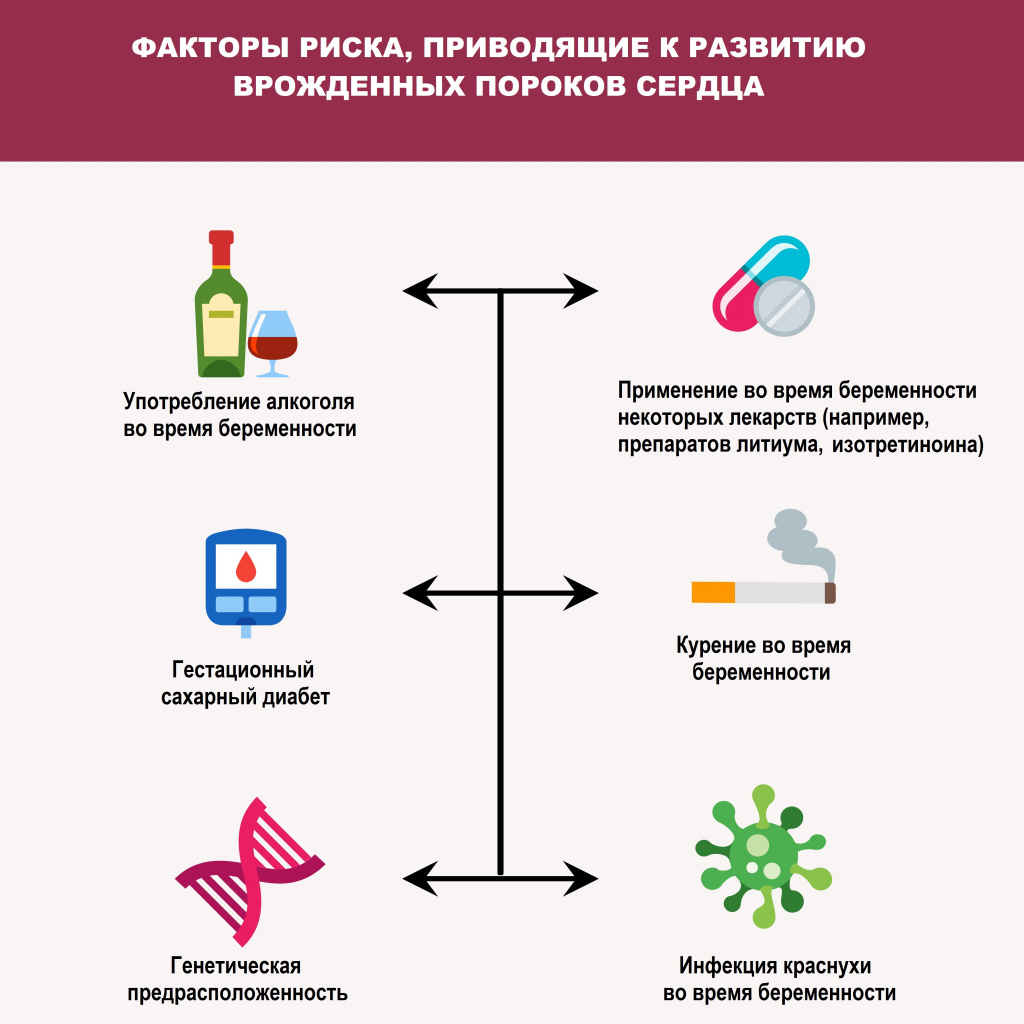
Среди причин развития врожденных пороков сердца выделяют генетические, экологические и инфекционные. Помимо этого, к их формированию могут приводить определенные заболевания (гестационный сахарный диабет, краснуха и системная красная волчанка) у матери, прием некоторых лекарственных препаратов, наркотиков и алкоголя во время беременности и другие факторы.
Приобретенные пороки – это аномалии и дефекты клапанов сердца, его отверстий или перегородок между камерами, отходящих от него сосудов, появившиеся в процессе жизни под воздействием морфологических и функциональных изменений в работе сердца. Митральный клапан страдает чаще, чем аортальный. Реже встречаются патологии трехстворчатого (трикуспидального) клапана и клапана легочной артерии. Заболевания могут манифестировать в любом возрасте под влиянием атеросклероза, кардиосклероза, ишемической, либо гипертонической болезни, ревматизма, системной патологии, травмы, сифилиса и некоторых других причин. Также к клапанным порокам сердца приводят дегенеративные изменения клапанов - при развитии заболевания нарушается их строение и функция, что вызывает перестройку гемодинамики, происходит перегрузка соответствующих отделов сердца, гипертрофия сердечной мышцы, нарушение кровообращения в сердце и в организме в целом.
Классификация заболевания
- стеноз - в результате патологического процесса возникает деформация тканей клапана и сужается отверстие, через которое кровь поступает в следующий отдел сердца;
- недостаточность клапанов - несмыкание клапанов сердца из-за изменения формы, их укорочения в результате рубцевания пораженных тканей;
- комбинированные и сочетанные пороки сердца:
- комбинированные – при наличии и стеноза, и недостаточности одного клапана;
- сочетанные – при поражении сразу нескольких клапанов.
- дегенеративные, или атеросклеротические (встречаются в 5-6% случаев) - чаще эти процессы развиваются после 40-50 лет, когда происходит отложение кальция на створках пораженных клапанов, что приводит к прогрессированию порока;
- ревматические, формирующиеся на фоне ревматических заболеваний (80% случаев);
- пороки, возникающие как результат воспаления внутренней оболочки сердца (эндокардит);
- сифилитические (в 5% случаев).
Симптомы пороков сердца
К клиническим симптомам пороков сердца относятся одышка, слабость, быстрая утомляемость, отеки нижних конечностей, нарушение сна, перебои в работе сердца, аритмия (чаще тахикардия), изменение цвета кожи (синюшность или бледность), набухание вен шеи и головы, беспричинное беспокойство, давящая боль в области сердца (особенно при физических нагрузках) или между лопатками, в редких случаях - потеря сознания.
Специфические симптомы врожденных пороков сердца зависят от возраста пациента. Поскольку нормальная циркуляция богатой кислородом крови необходима для нормального роста и развития организма, у младенцев может наблюдаться затрудненное или учащенное дыхание, плохой аппетит, потливость или повышенная частота дыхания во время кормления, цианоз губ и/или кожи, необычная раздражительность или отставание в прибавке в весе.
У детей и подростков могут наблюдаться снижение переносимости физических нагрузок, головокружения, обмороки.
Большинство серьезных пороков сердца у детей выявляются на основании симптомов, которые замечают родители, а также на основании отклонений, обнаруживаемых при осмотре врачом. Нарушенный ток крови через сердце обычно проявляется сердечными шумами, которые можно услышать с помощью стетоскопа. Аномальные сердечные шумы зачастую бывают громкими или резкими. Однако в подавляющем большинстве случаев сердечные шумы, отмечаемые в детском возрасте, являются функциональными и не обусловлены пороками сердца.
Выраженность и характер симптомов зависят от расположения пораженного клапана. При пороках клапанов левой половины сердца (митрального и аортального) в первую очередь страдают легкие, так как в их сосудах застаивается кровь, что проявляется одышкой и кашлем. Кроме того, возникают признаки недостаточного кровоснабжения головного мозга и самого сердца, головокружение, обмороки, стенокардия. При наличии цианоза одной из наиболее распространенных патологий является тетрада Фалло (ограничение поступления крови в легкие).
![Стеноз аортального клапана.jpg]()
При нарушении работы клапанов правой половины сердца (трехстворчатого и клапана легочной артерии) происходит застой крови в сосудах большого круга кровообращения, поэтому страдают все органы кроме легких. Развиваются отеки голеней и стоп, асцит (скопление жидкости в брюшной полости), увеличение печени и другое.отставание в прибавке в весе.
Признаки приобретенных пороков зачастую сочетаются с другими заболеваниями сердца, в частности, с ишемической болезнью, что затрудняет их клиническую дифференциацию.
Диагностика пороков сердца
Диагностические мероприятия, проводимые с целью обнаружения порока сердца, требуют комплексного подхода, но всегда начинаются со сбора анамнеза: врач выясняет жалобы пациента, время и обстоятельства их проявления, интенсивность, наследственные факторы. Далее проводится физикальный осмотр, который включает визуальный осмотр, пальпацию, перкуссию (простукивание), аускультацию (выслушивание).
Лабораторные исследования, которые назначают при подозрении на порок сердца:
-
клинический анализ крови;
Синонимы: Общий анализ крови, ОАК. Full blood count, FBC, Complete blood count (CBC) with differential white blood cell count (CBC with diff), Hemogram. Краткое описание исследования Клинический анализ крови: общий анализ, лейкоформула, СОЭ См. также: Общий анализ – см. тест № 5, Лейкоцит.
Рисунок 1. Экстрабуккальная скарлатина, лимфангиит В современных условиях наряду с новыми болезнями (ВИЧ-инфекция, лайм-боррелиоз, геморрагические лихорадки) сохраняют свою актуальность и давно известные, в частности скарлатина,
Скарлатина отличается от других форм тем, что вызывается только токсигенными штаммами стрептококка при отсутствии антитоксического иммунитета и характеризуется симптомокомплексом, обусловленным эритрогенным токсином Дика. В разные времена скарлатину считали то тяжелой, то легкой болезнью с благоприятным исходом.
В 80-90-х годах в ряде стран (в Англии, США, Швеции и др.) был отмечен подъем заболеваемости различными формами стрептококковой инфекции, в частности утяжеление течения скарлатины.
Традиционно скарлатина считается детской болезнью. По данным A. R. Каtz, D. M. Morens, 80% случаев скарлатины приходятся на возраст от 4 до 8 лет. Полагают, что лица старше 10 лет имеют высокий уровень защитных антител, образовавшихся вследствие субклинической иммунизации. Известные на сегодня работы, посвященные скарлатине, относятся к описанию этой болезни у детей.
В течение последних 10 лет под нашим наблюдением в КИБ № 2 находились 442 взрослых больных, из них 284 — мужчины, 158 — женщины. Возрастной состав больных представлен в табл. 1.
Среди пациентов преобладали солдаты срочной службы, студенты, учащиеся. Военнослужащие, лица, проживающие в общежитии, поступали в клинику в первые два дня болезни, остальные — на третий-четвертый день и позже.
В летние месяцы госпитализированных было в 1,5 раза меньше, чем в холодное время года. Диагностика скарлатины на догоспитальном этапе свидетельствовала о слабом знании этой болезни. Диагнозы, с которыми больные направлялись в клинику, приведены в табл. 2.
Кроме того, у 15 из 319 больных, направленных в клинику с диагнозом скарлатина, был диагносцирован псевдотуберкулез.
В стационаре диагноз скарлатины в 95% случаев устанавливался в день поступления на основании типичного симптомокомплекса, включающего признаки интоксикации, развивающиеся с первых часов болезни (повышение температуры, головная боль, тошнота, рвота, слабость), воспаления (тонзиллит или инфицированная рана кожи, регионарный лимфаденит, ангулярный хейлит) и аллергии (сыпь, кожный зуд, эозинофилия). При постановке диагноза учитывались следующие факторы: характерный вид языка, белый дермографизм, изменения периферической крови (нейтрофильный лейкоцитоз), быстрый эффект от пенициллинотерапии.
На основании данных литературы и собственных многолетних наблюдений мы сделали вывод, что надежного и доступного лабораторного теста для ранней диагностики скарлатины на нынешний день не существует. Поэтому при постановке диагноза необходимо в первую очередь учитывать клиническую картину болезни. Следует также тщательно проводить дифференциальный диагноз.
Как показал анализ диагнозов, с которыми больные направлялись в клинику, а также наши наблюдения, наибольшую трудность в ряде случаев вызывает дифференциальный диагноз с псевдотуберкулезом. Для исключения последнего мы проводили соответствующие бактериологические и серологические исследования.
В современных условиях скарлатину у детей относят к легким болезням, тяжелые формы заболевания не регистрируются. Между тем скарлатина у взрослых, имеющая ту же клиническую картину, что и у детей, существенно отличается по тяжести течения (табл. 3).
Всем больным в динамике исследовали периферическую кровь. Кроме того, проводились биохимические, бактериологические и серологические исследования в отношении псевдотуберкулеза, а также ЭКГ.
Картина периферической крови у большинства больных характеризовалась нейтрофильным лейкоцитозом; у 34,13% больных содержание лейкоцитов оставалось в пределах нормальных показателей. В случае тяжелого течения регистрировался сдвиг влево до миелоцитов. Увеличение числа эозинофилов наблюдалось обычно на второй неделе болезни (81% больных). У подавляющего большинства пациентов (94,6%) течение болезни было ровным. Осложнения как в острый период, так и в период реконвалесценции выявлялись сравнительно редко (табл. 4).
Преимущественно ровное течение болезни, по нашему мнению, обусловлено своевременным назначением антибактериальной и патогенетической терапии. Все больные с момента установления диагноза получали лечение пенициллином по 3-6 млн/сут. в течение пяти-семи дней. Зарубежные авторы рекомендуют пенициллин и в качестве препарата выбора при лечении больных со стрептококковой инфекцией. При непереносимости пенициллина назначали эритромицин до 2,0 в сутки таким же курсом.
Тяжелая форма болезни была диагностирована у 14 прежде здоровых лиц в возрасте от 18 до 37 лет. Болезнь характеризовалась острейшим течением, гипертермией, многократной рвотой, некротической ангиной, сыпью с геморрагическим компонентом.
Больные поступали на второй-третий день болезни с признаками инфекционно-токсического шока (либо ИТШ развивался в течение ближайших суток): в местах локализации сыпи кожа становилась цианотичной, на этом фоне появлялись множественные геморрагические элементы. Конечности становились холодными, температура снижалась до нормальной, быстро падало артериальное давление до 60/40–50/20 мм рт. ст., пульс становился нитевидным, мочеиспускание прекращалось.
С развитием ИТШ лечение осуществлялось в условиях реанимационного отделения.
В одном случае мы наблюдали септическую форму болезни с летальным исходом.
В 8 случаях (0,6%) отмечалась экстратонзиллярная форма скарлатины. По данным В. Д. Цизерлинга (1993), в 97% случаев скарлатины наблюдается первичная локализация возбудителя в ротоглотке, в 2% случаев — на коже, в 1% — в легких.
У военнослужащих, возраст которых колебался от 18 до 20 лет, входными воротами возбудителя являлись раны на руках. Эта форма болезни отличалась от классической отсутствием тонзиллита и сгущением сыпи в области входных ворот.
На основании вышеизложенного можно сделать следующие выводы:
- скарлатина у взрослых чаще всего имеет среднетяжелое течение;
- антибиотиком выбора при лечении скарлатины по-прежнему является пенициллин;
- диагностика заболевания основывается главным образом на клинических проявлениях скарлатины и дополняется некоторыми лабораторными данными (картиной периферической крови — небольшое снижение гемоглобина, лейкоцитоз с нейтрофильным сдвигом, эозинофилия, ускорение СОЭ);
- при своевременном лечении скарлатины осложнения нетяжелые и бывают редко.
Больной Г. 20 лет, военнослужащий строительного батальона. Заболел остро 17.01.92: озноб, головная боль, подъем температуры до 40°С, тошнота. Госпитализирован на второй день болезни с подозрением на менингит. При поступлении жаловался на сильную головную боль, головокружение, слабость, тошноту. Температура 39,1°С. На коже выявлена типичная для скарлатины зудящая сыпь. У основания большого пальца правой кисти — инфицированная рана, регионарный лимфаденит и лимфангиит (рис. 1).
В области раны четко выраженное сгущение сыпи. Диагностирована экстратонзиллярная (экстрабуккальная) форма скарлатины. На фоне лечения пенициллином (3 млн/сут.) через сутки температура нормализовалась, исчезли симптомы интоксикации.
На четвертый день госпитализации на фоне угасающей сыпи наблюдались снижение остроты зрения, туман перед глазами, двоение, тошнота. На следующий день развились птоз век, мидриаз, нарушение конвергенции, осиплость, косоглазие, парез небной занавески, одышка (24’), сухость во рту, легкий парез n. facialis справа.
С учетом наличия раны на кисти и участия в земляных работах мы диагностировали раневой ботулизм (факт употребления консервированных продуктов больной отрицал).
В дальнейшем лечение проводилось в специализированном отделении. Диагноз подтвержден. Исход благоприятный.
Больная С. 37 лет имела контакт с больным ребенком, диагноз которого дифференцировался между краснухой и скарлатиной. Заболела 01.09.95 остро, болезнь началась с подъема температуры до 39°С, боли в горле, сильной головной боли, многократной рвоты. К концу первого дня болезни появилась сыпь. Врачом поликлиники диагностирована краснуха. Принимала аналгин, панадол, супрастин. Состояние не улучшалось. На третий день болезни госпитализирована с диагнозом: краснуха, тяжелое течение.
Ан. крови 05.09 (5-й день болезни): Hb — 67 г/л, эр. — 2,1, тром. — 52,0, лейк. — 21,4, миелоциты — 2%, метамиелоциты — 7%, п/я — 52%, с/я — 25%, э-о, лим. — 9, м. — 4, СОЭ — 50 мм/ч, общ. белок — 42,3, мочевина — 33,9, креатинин — 0,417, билирубин своб.— 22,5, связ. — 58,5.
В дальнейшем нарастали явления ДВС-синдрома, на седьмой день болезни пациентка умерла.
При патологоанатомическом исследовании выявлены язвенно-некротический тонзиллит, язвенно-некротический фарингит, флегмонозный парафарингит, сепсис (бактериологическое исследование — выделен стрептококк), обильная мелкая геморрагическая сыпь на коже, склонная к слиянию, больше в низу живота, в паховых областях, подмышечных впадинах, набухание головного мозга, некротическая геморрагическая пневмония в нижних долях обоих легких. Смерть больной наступила от комплекса осложнений вследствие септической скарлатины.
Представляет интерес случай комбинации экстратонзиллярной скарлатины и раневого ботулизма.
Читайте также: