Снятие интоксикации при желтухе
Обновлено: 05.05.2024
Ключевые слова: механическая желтуха, желчеотток, ремаксол, стерофундин-Г-5
Введение. Основной причиной, ухудшающей прогноз хирургического лечения больных с механической желтухой (МЖ), является прогрессирующий эндотоксикоз с развитием тяжелой печеночно-клеточной недостаточности [2, 4]. Малоинвазивные технологии дренирования желчевыводящих путей способствовали в некоторой степени повышению безопасности подготовки к основному этапу хирургического лечения, но окончательного решения вопроса о профилактике печеночной недостаточности не произошло. Подготовка больного к этапу радикального хирургического восстановления желчеоттока включает не только малоинвазивные дренирующие операции , но и активную инфузионную и гепатотропную терапии.
В настоящее время остаются ряд важных нерешенных вопросов, касающихся оценки эффективности влияния дооперационной инфузионной терапии на желчевыделительную функцию печени и эндотоксикоз, что определило цель данного исследования.
Цель исследования — изучить влияние состава инфузионной терапии на желчевыделительную функцию печени и эндотоксикоз у больных с МЖ.
Материал и методы. Клиническое проспективное рандомизированное исследование содержит анализ динамики показателей желчеоттока и эндотоксикоза после УЗИ-контролируемого дренирования желчевыводящих путей у 139 пациентов с заболеваниями гепатобилиарной системы, осложненными МЖ, с уровнем билирубинемии при поступлении в интервале 130-300 мкмоль/л.
В зависимости от используемой инфузионной тактики больные были разделены на 3 группы. Средний объем инфузионной терапии во всех группах больных не превышал 1600 мл/сут. В I -й группе у 54 пациентов состав инфузионной терапии включал раствор Рингера и 10% раствор глюкозы в соотношении 1:1. Во 2-й группе (37 больных) инфузионная терапия проводилась раствором стерофундин-Г-5, содержащим в качестве субстратного антигипоксанта малат в количестве 1,7 г/л. 48 больным 3-й группы в состав инфузионной терапии (растворы Рингера и глюкозы 10%) включен ремаксол в дозе 800 мл/сут. Ремаксол — полиионный инфузионный гепатотропный препарат, содержащий в своем составе в качестве специфических компонентов сукцинат, метионин, рибоксин и никотинамид. Влияние состава инфузионной терапии на исследуемые показатели оценивали в течение 10 сут после дренирующей малоинвазивной операции. Оценку эндотоксикоза осуществляли по методике С.В.Оболенского и соавт. [3] с расчетом индекса синдрома эндогенной интоксикации (ИСЭИ), как отношение произведения веществ низкой и средней молекулярной массы (ВНиСММ) плазмы и эритроцитов к ВНиСММ мочи [6].
Статистическую обработку результатов исследования проводили параметрическими и непараметрическими методами вариационной статистики с вычислением средней арифметической выборочной совокупности (М), ошибки средней арифметической (m).
Результаты и обсуждение.В 1-е сутки после УЗИ-контролируемого дренирования желчевыводящих путей средние значения желчеоттока были ниже физиологических значений и не отличались у больных исследуемых групп. Через 2 сут и 3 сут соответственно определились преимущества инфузионной терапии ремаксолом и стерофундином-Г-5 с повышением количества дренируемой желчи до уровня должных величин. В последующем скорость желчеоттока у больных этих групп прогрессивно возрастала, в большей степени у пациентов, получавших ремаксол. Достоверность отличий относительно больных 2-й группы определялась в интервале 2-8 сут после дренирования. Средний суммарный желчеотток за первые 5 сут после УЗИ-контролируемого дренирования желчевыводящих путей составил в 1-й группе больных 2272 мл, во 2-й группе — 2804 мл, в 3-й группе — 3419 мл. Следует отметить, что у больных 1-й группы в этот период наблюдения желчеотток оставался неизменным на уровне исходных значений.
Известно, что желчеобразование — сложный метаболический процесс, зависящий от секреции желчи паренхиматозными клетками печени (гепатоцитами), проницаемости плотных соединений между ними для воды и электролитов, экскреции гепатоцитами органических и неорганических компонентов желчи, секреции желчи (водного раствора электролитов) эпителиальными клетками желчных протоков, а также реабсорбции воды из первичной желчи в желчных протоках [1,5].
Развивающийся после применения стерофундина-Г-5 и особенно ремаксола холеретический эффект связан, на наш взгляд, с улучшением внутрипеченочного метаболизма и рециркуляции желчных кислот. Одним из механизмов терапевтического действия метионин-содержащего раствора ремаксол является активное участие метионина во внутрипеченочных белоксинтетических процессах. Метионин либо встраивается во вновь синтезируемые белки, либо подвергается метаболизму с образованием активной формы S-аденозил-L-метионина. Известно, что данное соединение играет важную роль в образовании сульфатированных желчных кислот и биосинтезе фосфолипидов в клетках с образованием мицеллярно-лимеллярных структур, состоящих из фосфолипидов и желчных кислот. Образование этих структур позволяет нейтрализовать токсическое действие избыточных желчных кислот. Кроме того, встраиваясь в клеточные мембраны, вновь синтезируемые фосфолипиды могут повышать их гидрофильность, улучшая, тем самым, процесс переноса желчных кислот из гепатоцита в желчный капилляр. Энергозависимое сульфатирование и глюкуронирование желчных кислот, перевод их во вторичные и третичные желчные кислоты, с одной стороны, уменьшает их токсические свойства, а с другой стороны — увеличивает их экскрецию с желчью, в свою очередь, улучшая ее реологические показатели 7.
Развивающаяся под влиянием ремаксола гиперхолия сопровождалась прогрессивным снижением уровня таких маркёров холестаза, как щелочная фосфатаза и гамма-гутамилтранспептидаза, что должно рассматриваться как безусловный положительный эффект метаболически направленной инфузионной терапии.
Об этом свидетельствует и сокращение средних сроков полного купирования кожного зуда после дренирующей малоинвазивной операции. У больных 1-й группы они составили 4,9 сут, 2-й группы — 3,1 сут, 3-й группы — 2,2 сут.
Восстановление и стимуляция процессов желчеобразования и желчевыделения внесли свой вклад в купирование эндогенной интоксикации у больных МЖ (таблица).
Выводы.
1. Инфузионная терапия в составе растворов Рингера и 10% глюкозы не оказывает значимого влияния на темпы желчеотделения и коррекцию эндотоксикоза в раннем периоде после УЗИ-контролируемого дренирования желчевыводящих путей.
2. Включение в инфузионную программу стерофундина-Г-5 или ремаксола способствует компенсации эндотоксикоза за счет восстановления желчевыделительной функции печени.
3. Использование ремаксола в дозе 800 мл/сут имеет преимущества в отношении коррекции желчеоттока и эндотоксикоза по сравнению с инфузией стерофундина-Г-5 в дозе 1600 мл/сут.
Библиографический список
Поступила в редакцию 15.09.2011 г.
Infusion Correction Of Bile Outflow And Endotoxicosis In Patients With Mechanical Jaundice
A.Yu. Yakovlev, V.B.Semenov, N.V.Emelianov, K.V.Mokrov, P.S.Zubeev, S.V.Akulenko, N.V.Zarechnova
The investigations were performed in 139 patients divided into 3 groups and who were given similar volume of infusion therapy (1600 ml/day). In the first group consisting of 54 patients the solution of infusion therapy included the Ringer solution and 10% of glucose solution in the ratio 1:1. In the second group (37 patients) the infusion therapy was performed with a solution of sterofundin-G-5. In the third group (48 patients) remaksol in dose 800 ml/day was included in infusion therapy. The inclusion of sterofundin-G-5 and remaksol in the infusion therapy increased the rate of bile outflow at the early postoperative period as compared with the solutions of Ringer and 10% of glucose. Remaksol is better for arresting endotoxicosis and bile excreting function of the liver as compared with infusion of sterofundin-G-5.
Механическая желтуха, являющаяся одним из тяжелейших недугов, может быть вызвана полной и неполной закупоркой желчных протоков. При неполной обтурации желчных протоков развитию механической желтухи способствует нарушение функции гепатоцитов (Шалимов А. А
Механическая желтуха, являющаяся одним из тяжелейших недугов, может быть вызвана полной и неполной закупоркой желчных протоков. При неполной обтурации желчных протоков развитию механической желтухи способствует нарушение функции гепатоцитов (Шалимов А. А. и др., 1993). Таким образом, механическая желтуха развивается вследствие механической обструкции и, как следствие, повреждения гепатоцитов в
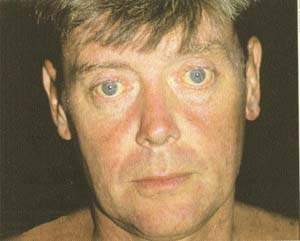 |
| Рисунок 1. Препарат реамберин назначается для лечения механической желтухи |
В настоящее время в биологии и медицине в качестве биологически активного вещества, обладающего широким спектром фармакологических свойств, предлагают использовать янтарную кислоту и ее различные соли- сукцинаты (Кондрашева М. Н., 1996).
В медицинской литературе имеются многочисленные данные о гепатопротекторных и антиоксидантных свойствах солей янтарной кислоты — сукцинатов (Малюк В. И. и др., 1979; Косенко Е. А. и др., 1994). О цитопротекторном и антиоксидантном действии янтарной кислоты известно давно (Кондрашова М. Н., 1996).
Клинические исследования проводились по методу мультицентрового испытания по единой программе при эндогенной интоксикации, связанной с механической желтухой. Исследование открытое, контролируемое, рандомизированное.
Для испытания были сформированы группы по 30 человек (контрольная и основная). Среди пациентов 30 мужчин и 30 женщин (по 15 в каждой группе). Средний возраст больных составил 60±1,7 лет (Р< 0, 05). Все больные с сопоставимой патологией желчевыводящих путей (табл. 1).
Таблица 1. Причины обтурации желчных протоков
Пациенты подверглись различным оперативным вмешательствам, сопоставимым по тяжести, объему и длительности (табл. 2).
Все больные в период наблюдения находились в состоянии тяжелом или средней тяжести. Клиническая оценка была основана на выявлении жалоб, данных клинического осмотра, пальпации, перкуссии, аускультации, данных клинических анализов крови и мочи, биохимических и иммунологических исследований. Для оценки эндогенной интоксикации проводилось определение пула веществ низкой и средней молекулярной массы (ВНиСММ) и олигопептидов (ОП) и регистрация спектральной характеристики плазмы крови в зоне длин волн от 238 до 310 нм по способу М. Я. Малаховой (Малахова М. Я., 1995). Индекс интоксикации рассчитывался по следующей формуле: ИИ плазмы = ВНИСММ плазмы х ОП плазмы.
Таблица 2. Объем выполнения оперативных вмешательств на желчных протоках
При учете клинических показателей, таких как болевой синдром, желтушность кожных покровов, потемнение мочи и т. д., мы столкнулись с проблемой субъективности их оценки. В то же время необходимо отметить некоторое улучшение самочувствия, сна, более быстрое снятие кожного зуда и болевого синдрома у больных в основной группе.
Таблица 3. Биохимические показатели
Со стороны периферической крови положительная динамика отчетливо видна на примере лейкоцитоза, сопоставимая с такой же динамикой в контрольной группе, что говорит о более быстром разрешении одного из компонентов механической желтухи — холангите при использовании реамбирина.
Таблица 4. Показатели периферической крови
Уровень эндогенной интоксикации (табл. 5). В основной группе более низкий уровень ВНиСММ в плазме крови после операции, с тенденцией к нормализации в первую неделю после операции.
Таблица 5. Показатели эндогенной интоксикации
В основной группе в клеточном звене нами отмечена положительная динамика абсолютного количества лимфоцитов с сохранением практически нормальных процентных соотношений в их подгруппах, повышение абсолютного количества Т-активных лимфоцитов, снижение Т-лимфоцитов (Е-РОК), нормальные значения теофиллинрезистентных лимфоцитов и снижение количества теофиллинчувствительных лимфоцитов, повышение индекса миграции в РТМЛ с ФГА.
В гуморальном звене в основной группе выявлена также положительная динамика: уменьшение абсолютного количества В-лимфоцитов с сохранением их функциональной активности; менее высокий уровень циркулирующих иммунных комплексов (что указывает на улучшение их элиминации из крови) и нормальное содержание иммуноглобулинов А, М и G. Анализ полученных результатов убедительно показывает, что состояние иммунной системы и неспецифической резистентности организма зависит от тяжести эндогенной интоксикации при механической желтухе и успешно корригируется при использовании реамберина.
Таблица 6. Показатели антиоксидантной системы
Механическая желтуха развивается при нарушении оттока желчи из желчевыводящих протоков в двенадцатиперстную кишку. Данное состояние не является самостоятельным заболеванием. Механическая желтуха – это симптом, который характерен для многих болезней органов брюшной полости. Ввиду достаточно большой распространенности, врачам разных специальностей часто приходится сталкиваться с данной проблемой и назначать пациентам различные виды лечения.
Варианты развития механической желтухи
В зависимости от причин появления, данное состояние может быть опухолевого и неопухолевого генеза. Примерно в половине всех случаев механическая желтуха связана со злокачественными новообразованиями поджелудочной железы, печени, кишечника. Печень может поражаться первичным опухолевым процессом или метастазами из отдаленных очагов.
У второй половины пациентов развитие механической желтухи обусловлено доброкачественными процессами, среди которых наиболее часто отмечаются:
- Воспалительные процессы желчного пузыря и желчевыводящих путей – холецистит, холангит, папиллит и др.
- Невоспалительные заболевания органов брюшной полости: желчекаменная болезнь, стеноз желчевыводящих путей, холангиолитиаз и др.
- Врожденные аномалии: атрезия желчевыводящих путей, дуоденальные дивертикулы, кисты и др.
В редких случаях механическую желтуху могут вызывать паразитарные заболевания. Механизм развития симптома в этом случае связан с попаданием гельминтов в желчные протоки с нарушением их проходимости.

Принципы лечения механической желтухи
Главными задачами, при составлении плана лечения, являются ликвидация холестаза (застоя желчи) и профилактика печеночной недостаточности. Для этого врач составляет комплексную программу, в которую могут быть включены как консервативные, так и оперативные методы.
Диета при механической желтухе
Соблюдать определенные правила питания необходимо как до проведения основного лечения, так и после его завершения. Пациентам с механической желтухой рекомендуется соблюдать питьевой режим, так как вода ускоряет выведение билирубина, за счет чего снижается его негативное действие на организм. Также очень важно полностью отказаться от алкоголя, очень жирной и жареной пищи, майонеза, соусов, острых приправ. Пищу следует употреблять небольшими порциями 5-6 раз в день. При этом необходимо следить за температурой блюда. Она не должна быть слишком горячей или холодной. Оптимальный вариант – это теплая пища, так как она помогает регулировать секрецию желчи, что особенно актуально при механической желтухе.

Среди других общих рекомендаций, которые касаются диеты, можно отметить ограничение количества соли в рационе. Известно, что избыток соли способствует задержке жидкости в организме, вызывает отеки и затрудняет выведение вредных веществ. Пациентам с механической желтухой рекомендуется употреблять не более 4 граммов соли в сутки. В целом точный план питания, калорийность и состав блюд подбираются индивидуально для каждого пациента, с учетом его предпочтений. Существуют списки разрешенных и запрещенных блюд, а также тех продуктов, которые должны быть ограничены. Именно этими списками и руководствуется врач при составлении программы питания. Например, к разрешенным продуктам относятся:
- Овощи (морковь, огурцы, капуста, помидоры, брокколи).
- Бананы и яблоки.
- Сухофрукты.
- Различные каши (гречневая, овсяная, перловая).
- Хлеб с отрубями, макароны, хлебцы.
- Варенье, мед, мармелад.
- Нежирное мясо (кролик, говядина), птица (куриные грудки, филе индейки) и рыба (минтай, хек).
- Фруктовые соки и чай.
Диета при механической желтухе подразумевает полное исключение консервированных овощей, бобовых, винограда, сдобы, белого хлеба, жирного молока, сливок, жирных сортов мяса и рыбы, копченостей, газированных напитков, кофе, животных жиров.
Медикаментозное лечение
Медикаментозная терапия при механической желтухе назначается с целью снижения выраженности симптомов, подготовки пациента к операции и уменьшению риска развития осложнений. Объем медицинской помощи во многом зависит от степени желтухи. Например, при тяжелой степени, медикаментозное лечение проводится в условиях отделения интенсивной терапии и включает в себя:
- Инфузионную терапию.
- Антиоксидантную терапию.
- Антибиотикотерапию.
- Гепатопротекторы.
- Стимуляторы метаболизма.
- Гормональные препараты.
Для снятия симптомов, при легких формах механической желтухи могут назначаться спазмолитики, обволакивающие препараты, антациды и другие лекарственные средства.
Хирургическое лечение
Хирургическое лечение является единственным эффективным способом, который позволяет восстановить проходимость желчных путей и устранить тем самым причину механической желтухи. Все известные виды операций можно разделить на две группы: малоинвазивные методики и прямые операции.
Малоинвазивные методы хирургического лечения
Данная группа методов отличается высокой эффективностью и малой травматичностью, однако применять их у всех пациентов подряд невозможно ввиду определенных ограничений. Малоинвазивное лечение механической желтухи проводится при помощи эндоскопических методик и чрескожной чреспеченочной холангиостомии. Эндоскопические операции могут быть следующих видов:
- Эндоскопическая папиллосфинктеротомия и литоэкстракция. Во время этой операции врач рассекает сосочек двенадцатиперстной кишки, в который впадают общий желчный проток (холедох) и проток поджелудочной железы, и удаляет камень, который блокирует отток желчи.
- Местная литотрипсия и литоэкстракция. Во время этого вмешательства желчный камень дробят с помощью специальных технологий на более мелкие фрагменты и удаляют их.
- Бужирование и стентирование желчных протоков. Во время данного вмешательства желчные протоки, стенозированные в результате патологического процесса, например, злокачественной опухоли, расширяют с помощью специальных инструментов и устанавливают в них стент – трубочку с сетчатой стенкой. В дальнейшем он обеспечивает нормальный просвет протока и свободный отток желчи.
В этих случаях для лечения механической желтухи применяется гастродуоденоскоп со специальными инструментами, которые позволяют дробить и извлекать камни, устанавливать стенты, удалять ткани. Эндоскопические операции в большинстве случаев проводятся под седацией, что делает проведение процедуры безболезненной и комфортной.
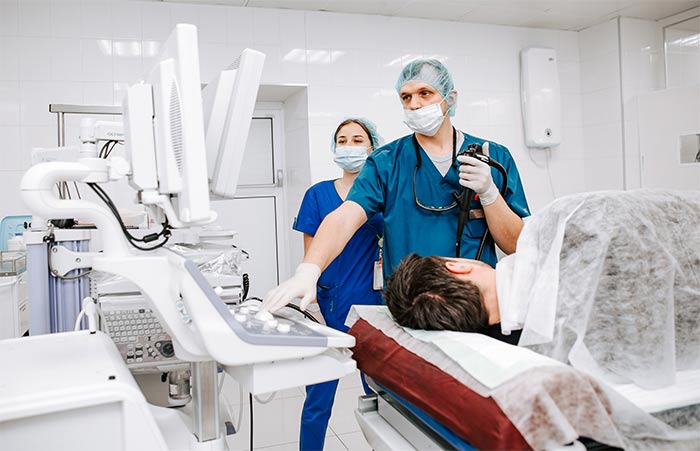
Дренирование при механической желтухе
Механическую желтуху при онкологических заболеваниях можно устранить с помощью разных малоинвазивных вмешательств, целью которых является дренирование желчных протоков:
- чрескожная чреспеченочная холангиостомия (чрескожное чреспеченочное, наружное дренирование);
- внутреннее дренирование;
- наружно-внутреннее дренирование.
Чрескожная чреспеченочная холангиостомия применяется в случаях, когда при механической желтухе невозможно выполнить декомпрессию желчевыводящих путей при помощи гастродуоденоскопа и установки стента. Суть операции заключается в установке дренажной трубки под контролем УЗИ или рентгена. При этом специальной пункционной иглой прокалывается кожа, мышцы передней брюшной стенки и ткань печени. В дальнейшем дренажная трубка может использоваться не только для отвода желчи, но и для введения антибактериальных или других препаратов непосредственно в желчные протоки.
Наружное дренирование помогает устранить механическую желтуху, но оно не очень физиологично. За счет того, что желчь оттекает наружу, в кишечник не поступают желчные кислоты, необходимые для процесса пищеварения. Кроме того, дренажная трубка, которая находится снаружи, мешает в повседневной жизни, она может сместиться или выпасть, если за нее случайно потянуть. За ней нужно постоянно ухаживать.
При внутреннем дренировании трубку устанавливают так, чтобы желчь оттекала внутрь кишки. Наружно-внутреннее дренирование сочетает обе методики.
Преимущества стентирования при механической желтухе
Таким образом, оптимальным методом восстановления оттока желчи при механической желтухе является именно стентирование. Оно обладает рядом преимуществ:
- Малоинвазивная операция, которую выполняют эндоскопически, без разрезов. Это важно, так как самочувствие пациента с механической желтухой зачастую сильно ухудшено, и ему может быть противопоказано более обширное хирургическое вмешательство.
- После вмешательства не требуется длительного восстановительного периода.
- Сразу после процедуры восстанавливается отток желчи и улучшается состояние пациента. Стент полностью находится внутри организма и не мешает в повседневной жизни, за ним не нужно ухаживать.
- При необходимости, если снова возникает механическая желтуха, стентирование можно повторить.
Другие виды хирургического лечения
Прямые хирургические вмешательства позволяют сформировать полноценный доступ к желчному пузырю и устранить механическую желтуху любой сложности. Хирург может накладывать анастомозы, устанавливать стенты, выполнять реконструктивные операции. Вмешательство может выполняться при помощи лапароскопических инструментов, либо классическим открытым полостным методом. Последний вариант является наиболее травматичным, требует длительной реабилитации и сопровождается повышенным риском развития осложнений, поэтому его применяют только при лечении сложных случаев механической желтухи.
Общие принципы лечения механической желтухи
Если говорить в общем, то тактика лечения механической желтухи включает два этапа. На первом этапе назначается консервативная терапия и малоинвазивные методы хирургического лечения. При этом рекомендуется проводить такое лечение в первые 2-3 дня с момента поступления пациента в стационар. Если данные методы оказались неэффективными, то переходят ко второму этапу лечения механической желтухи, который подразумевает более радикальные методы. Лечение на пике желтухи связано c в высоким риском развития послеоперационных осложнений, поэтому его проводят только при наличии жизненных показаний.
Другие методы лечения
Эффективное лечение желтухи подразумевает устранение основного заболевания, которое привело к развитию данного симптома. Для этого необходимо применять либо консервативные, либо оперативные методы. Другие варианты лечения механической желтухи, в частности, народная медицина, лечение в домашних условиях и самолечение не помогут достичь желаемого результата. На определенный промежуток времени они помогут скрыть симптомы и облегчить состояние пациента, но основной процесс продолжит прогрессировать и приведет к развитию осложнений. Поэтому при появлении первых признаков механической желтухи, необходимо обращаться за квалифицированной медицинской помощью, которая поможет радикально решить проблему.
Последствия и прогноз при механической желтухе
Прогноз будет благоприятным в случаях, когда лечение желтухи было своевременным и правильным. Большое значение имеет и поведение самого пациента. Если придерживаться принципов правильного питания и строго следовать всем указаниям врача, риск развития рецидива или осложнений будет минимален. В противном случае, вероятность повторной механической желтухи будет очень высокой. Кроме того, повысится риск развития сопутствующих заболеваний, например, печеночной недостаточности, цирроза печени, энцефалопатии, сепсиса и др.
Методы профилактики
Специфических методов, которые помогли бы предотвратить развитие механической желтухи, в настоящее время не разработано. Поэтому упор делается на раннее выявление и эффективное лечение данного состояния. С этой целью необходимо регулярно консультироваться у врача и проходить профилактическое обследование, которое назначит специалист.
Желтуха представляет собой симптом, при котором в крови и биологических жидкостях повышается содержание билирубина.
Что такое билирубин
Билирубин — это желчный пигмент, главный компонент желчи. Он образуется в результате метаболизма гемоглобина, миоглобина и цитохрома. Билирубин в крови находится в двух видах — свободный и связанный (прямой и непрямой). В норме уровень общего билирубина колеблется от 5 до 17-21 мкмоль/л (в зависимости конкретной лаборатории).
Обмен билирубина
В результате разрушения гемоглобина происходит образование непрямого билирубина, который поступает в кровь. В среднем, за сутки у человека разрушается 1% эритроцитов, что приводит к образованию 100-250 мг билирубина. С током крови он попадает в печень, где печеночные клетки его захватывают и связывают с глюкуроновой кислотой. Таким образом, происходит образование прямого билирубина. Он приобретает водорастворимые свойства и способен растворяться в желчи. Вместе с ней он поступает в кишечник и выводится из организма с каловыми массами.
В норме в крови должно находиться небольшое количество билирубина, который транспортируется из органов РЭС в печень, но бывают состояния, когда нарушается процесс его обмена и его концентрация в крови увеличивается. Такое состояние называется гипербилирубинемия. Когда билирубина очень много, он выходит из кровеносного русла и пропитывает окружающие ткани, что вызывает синдром желтухи.
Увеличение билирубина в крови может произойти по одной из следующих причин:
- Усиленный распад эритроцитов — гемолитическая анемия. При этом в крови увеличивается содержание непрямого билирубина. Такое состояние называется гемолитической или надпеченочной желтухой.
- Заболевания печени. При некоторых заболеваниях печени происходит разрушение ее клеток и выход их содержимого в кровоток. Поскольку гепатоциты содержат большое количество билирубина, то происходит и его повышение в крови и развивается гипербилирубинемия. Такое состояние называется печеночной желтухой.
- Нарушение свободного прохождения желчи в тонкий кишечник. Она накапливается в желчных протоках, вызывая в них повышение давления, что в конечном итоге приводит к увеличению проницаемости их стенок и попаданию билирубина обратно в кровоток. Такое состояние называется подпеченочной или механической желтухой.
Есть и другие причины гипербилирубинемии, но они встречаются редко и не имеют существенного клинического значения.
Тяжесть симптомов при желтухе напрямую зависит от уровня общего билирубина:
- Легкая желтуха — уровень билирубина не превышает 85 мкмоль/л.
- Среднетяжелая желтуха. Уровень билирубина находится в пределах 86-169 мкмоль/л.
- При тяжелой желтухе уровень билирубина превышает 170 мкмоль/л.
При полной обтурации желчевыводящих путей нарастание билирубина происходит стремительно, на 30-40 мкмоль/л/сутки.

Почему развивается механическая желтуха
Пороки развития гепатобилиарной системы:
- Атрезии и гипоплазии желчных путей.
- Кисты желчного протока.
- Дивертикулы 12-перстной кишки.
Невоспалительные и воспалительные заболевания ЖВП:
- Холангиолитиаз — желчные камни, которые обтурируют просвет желчного протока.
- Стриктуры и стеноз желчных протоков.
- Холангиты.
- Холециститы.
- Панкреатиты.
- Кисты головки поджелудочной железы.
- Рак желчных или печеночных протоков.
- Рак печени.
- Рак поджелудочной железы.
- Метастатическое поражение печени.
- Доброкачественные опухоли — папилломатоз желчных протоков.
Клинические проявления
Желтуха
Характерным и ярким клиническим признаком является пожелтение кожных покровов, слизистых оболочек и склер (белков глаз). По сути, в желтый цвет окрашиваются все биологические жидкости организма, кроме слюны и слез. Желтушность кожи связана с пропитыванием тканей билирубином из-за его высокого содержания в крови.

Холестаз
Холестаз — это прекращение выделения желчи в кишечник. Она остается в протоках, накапливается там и, в конце концов, всасывается обратно в кровь. Все вместе это приводит к следующим проявлениям:
Ахолия
Ахолия — это симптомокомплекс, который развивается, когда желчь не поступает в кишечник. Это приводит к нарушению пищеварения. В первую очередь, страдает пищеварение жиров. Они не всасываются и выделяются вместе с калом. Такое состояние называется стеаторея. Также нарушается метаболизм белков и витаминов, особенно жирорастворимых, в том числе витамина К, который необходим для синтеза факторов свертывания крови. Это, в свою очередь, приводит к кровоточивости. Также в норме желчь оказывает бактерицидное действие. Соответственно, при ее отсутствии начинает нарушаться соотношение кишечной флоры в сторону преобладания анаэробов.
Желчь оказывает стимулирующее действие на перистальтику кишечника. Соответственно, при ее отсутствии возникают запоры, которые сменяются зловонными поносами из-за разжижения кишечного содержимого гнилостной микрофлорой. Отсутствие желчных пигментов в кале приводит к его обесцвечиванию — ахоличный кал.
Дисхолия
Застой желчи в протоках приводит к тому, что она меняет свои физические и химические свойства, что в конечном итоге способствует образованию камней.
Осложнения желтухи
Высокая гипербилирубинемия и желтуха являются жизнеугрожающими состояниями и могут привести к летальному исходу, даже после устранения причин, ее вызвавших.
При разрушении гепатоцитов, в кровь выходит большое количество токсических веществ, которые оказывают системное действие. Нарастают функциональные нарушения, развивается почечно-печеночный синдром. Билирубин проникает через гематоэнцефалический барьер и вызывает нарушение работы головного мозга (печеночная энцефалопатия), которая сопровождается оглушенностью сознания, вплоть до комы.
Отмечено также токсическое действие билирубина на сурфактант — важный компонент легких. При его повреждении развивается дыхательная недостаточность. Нарушение продукции факторов свертывания крови приводит к развитию ДВС-синдрома.
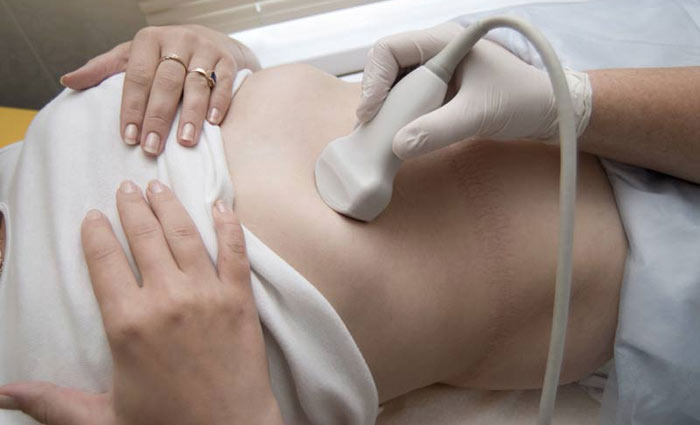
Диагностика желтухи
- Лабораторное обследование. Определение уровня билирубина в крови. Определяется прямой и непрямой билирубин. Для механической желтухи характерна билирубинемия за счет увеличения прямого билирубина. Также повышается уровень холестерола, липидов и щелочной фосфатазы, что указывает на развитие холестаза.
- УЗИ печени и желчных протоков. Данное исследование позволит обнаружить расширение просвета желчных протоков, утолщение их стенки, а в некоторых случаях определить причину обструкции (опухоли). При наличии анэхогенных камней, УЗИ может их не показать.
- КТ брюшной полости с контрастным усилением. Проводится для определения причины обструкции, которая не была выявлена на предыдущем этапе.
- Ретроградная холангиопанкреатография. Данная процедура сочетает в себе эндоскопические и рентгенологические технологии. С помощью эндоскопа в фатеров сосочек вводят рентгеноконтрастное вещество и делают серию снимков. Исследование позволяет визуализировать протоки и обнаружить места их обтурации (перекрытия).
- Чрескожная чреспеченочная холангиография. Проводится пункция внутрипеченочного желчного протока через брюшную стенку под контролем УЗИ. После этого проток заполняют рентгеноконтрастным веществом и делают снимки.
Лечение желтухи
Механическая желтуха требует хирургического лечения. На первом этапе проводится медикаментозная терапия, направленная на уменьшение токсического действия билирубина. В рамках хирургического лечения применяют следующие технологии:
Малоинвазивные вмешательства
При обтурации протока конкрементами применяют литотрипсию — разрушение и удаление камней из просвета протоков. Для этого могут использоваться эндоскопические технологии, лазерное, электрогидравлическое, или ультразвуковое дробление камней.
Если имеется обтурация из-за стеноза, стриктуры или компрессии опухолью, проводится стентирование, бужирование или балонная дилятация места сужения. Выбор метода лечения зависит от причин, вызвавших обструкцию.
Данные мероприятия проводятся эндоскопически через 12-перстную кишку. Если это невозможно, применяется чрескожное чреспеченочное дренирование желчного протока, при котором в него устанавливается дренажный катетер, отводящий желчь в специальный приемник. После стабилизации состояния пациента и устранения токсического действия гипербилирубинемии, делают попытку наладить нормальный пассаж желчи до 12-перстной кишки. С этой целью применяются полноценные операции.
Оперативные вмешательства на билиарной системе
На пике гипербилирубинемии полноценные операции на билиарной системе проводятся только при наличии строгих показаний, в основном они выполняются в плановом порядке.
Cреди хирургических заболеваний печени и внепеченочных желчных путей наиболее тяжелыми могут быть признаны те, которые сопровождаются стойкой непроходимостью магистральных желчных протоков с последующим развитием механической желтухи (МЖ). Проблемы диагн
Cреди хирургических заболеваний печени и внепеченочных желчных путей наиболее тяжелыми могут быть признаны те, которые сопровождаются стойкой непроходимостью магистральных желчных протоков с последующим развитием механической желтухи (МЖ). Проблемы диагностики и дифференциальной диагностики причин обтурации желчных путей не потеряли актуальности и в настоящее время. Хирургические вмешательства у больных МЖ, выполняемые по экстренным показаниям, сопровождаются большим числом осложнений, а летальность достигает 15-30%, что в 4 раза выше, чем в тех случаях, когда МЖ удается ликвидировать до операции [3, 7]. Огромный опыт, накопленный зарубежными и отечественными хирургами, показывает, что синдром МЖ возникает у 15-40% больных с желчнокаменной болезнью (ЖКБ) и у всех больных, имеющих опухолевое поражение желчных путей [1, 5, 9]. Декомпрессия билиарной системы является одной из главных целей и важнейшим компонентом лечебных мероприятий у этих пациентов.
Людей, страдающих МЖ, следует относить к группе пациентов с острыми хирургическими заболеваниями. В настоящее время большинство зарубежных и отечественных авторов считают оптимальным проведение лечения больных МЖ в два этапа [1, 2, 3, 7, 9, 10]. На первом этапе выполняют временную наружную или внутреннюю декомпрессию билиарных путей с помощью различных методов желчеотведения, а на втором, после ликвидации МЖ, при плановой операции стараются устранить причину, вызвавшую МЖ. Такая тактика лечения позволяет добиться уменьшения количества послеоперационных осложнений и снижения уровня общей летальности.
Вместе с тем в ходе разработки способов желчеотведения у больных МЖ возникает ряд проблем и спорных вопросов. Тяжелыми осложнениями МЖ являются холангит и печеночная недостаточность (ПН). Ведущие факторы в патогенезе холангита — холестаз с последующим присоединением инфекции.
В последнее время для декомпрессии желчных путей используют малоинвазивные эндоскопические или чрескожные чреспеченочные методы желчеотведения под контролем рентгенологического аппарата, ультразвукового аппарата (УЗИ), компьютерного томографа (КТ) или лапароскопа [2, 4, 6, 8, 10]. В 2001 году исполнилось 75 лет с начала применения чрескожных методов контрастирования билиарной системы (Burckhardt H., Muller W., 1921) и 40 лет — чрескожного чреспеченочного желчеотведения у больных МЖ (Remolar I. et al., 1956).
Итак, основная цель хирургического вмешательства при МЖ — декомпрессия желчевыводящих путей, устранение обтурации, ликвидация желтухи и профилактика возникновения или прогрессирования ПН. В настоящее время арсенал желчеотводящих методов при МЖ достаточно велик и включает в себя:
- эндоскопическую ретроградную холангиопанкреатографию (ЭРХПГ) с эндоскопической папиллосфинктеротомией (ЭПСТ);
- чрескожную чреспеченочную холангиографию (ЧЧХГ) с чрескожной чреспеченочной холангиостомией (ЧЧХС);
- холецистостомию под контролем УЗИ, КТ или лапароскопа;
- назобилиарное дренирование;
- различные варианты эндопротезирования желчных протоков;
- различные интраоперационные методы декомпрессии желчных протоков.
МЖ может быть доброкачественного (наблюдается у 45-55% больных) и злокачественного генеза. Среди МЖ доброкачественного генеза наиболее часто встречается холедохолитиаз, в остальных случаях речь идет о рубцовых стриктурах внепеченочных желчных путей, панкреатитах, паразитарных заболеваниях гепатобилиарной зоны, дивертикулах и доброкачественных опухолях большого дуоденального сосочка (БДС). Опухолевая природа заболевания обусловлена раком головки поджелудочной железы (ПЖ), БДС, желчного пузыря, гепатикохоледоха, ворот печени и метастазами рака другой локализации в печень.
Накопленный опыт лечения больных МЖ позволил нам разработать и внедрить новый алгоритм диагностики и лечения данной категории больных. В алгоритм диагностики МЖ кроме стандартного клинико-лабораторного исследования входят УЗИ, эзофагогастродуоденоскопия (ЭГДС), ЭРХПГ, КТ, ЧЧХГ и лапароскопия. Каждое исследование при необходимости можно превратить из диагностической процедуры в лечебную. При разработке алгоритма мы исходили из того, что МЖ должна быть ликвидирована как можно раньше от начала заболевания из-за опасности развития холангита и ПН. При этом процесс диагностики МЖ не должен отодвигать сроки начала ее лечения. Целесообразно диагностику и лечение МЖ проводить одновременно, хотя нередко лечение опережает по времени дифференциальную диагностику причины и уровня обтурации желчных путей.
Лечение больных с МЖ должно носить комплексный характер. Консервативные мероприятия кроме нормализации гомеостаза и инфузионной терапии включают следующие мероприятия:
- удаление из организма токсических веществ. Это достигается проведением форсированного диуреза, а также введением гемодеза и аналогичных ему препаратов;
- введение пластических веществ, необходимых для репаративных процессов печеночной паренхимы. При этом необходимо иметь в виду два основных момента: во-первых, до устранения желчной гипертензии пластические вещества усваиваются гепатоцитами плохо и в небольших количествах; во-вторых, перегрузка ими организма больного до восстановления нормального оттока желчи предъявляет повышенные требования к гепатоцитам и вследствие этого может вызвать срыв адаптационных процессов и ухудшить функцию печени. В связи с этим пластические вещества должны назначаться в дозах на уровне минимальных терапевтических (если предварительно не проводилась холецисто- или холангиостомия) и не слишком продолжительными курсами (до 7-10 дней). К этой группе препаратов относятся нуклеинат натрия и другие пуриновые и пирмидиновые основания: метацин, пентоксил, оротат калия и др.;
- улучшение обмена веществ в гепатоцитах. С этой целью целесообразно введение АТФ, коэнзима А, комплекса витаминов группы В, аскорбиновой кислоты, мексидола и др. Для нормализации сниженного уровня факторов свертывания крови, протромбинового комплекса обязательно введение викасола;
- применение анаболических гормонов. Дозы препаратов не должны быть большими, чтобы не вызвать срыва компенсаторных процессов в гепатоцитах. Следует предостеречь от применения гипербарической оксигенации, которая эффективна лишь после устранения желчной гипертензии. Для улучшения кровоснабжения паренхимы печени обязательно введение препаратов, улучшающих микроциркуляцию (реополиглюкина и др.);
- борьба с инфекцией. Введение антибактериальных препаратов у больных с длительной МЖ и сниженным вследствие этого иммунитетом должно сочетаться с проведением курса стимулирующей терапии продигиозаном, имунофаном или левамизолом.
Все существующие малоинвазивные методы декомпрессии билиарной системы можно разделить на две группы: эндоскопические (без нарушения целостности кожного покрова) и чрескожные. К первой группе относятся ЭРХПГ с ЭПСТ, назобилиарное дренирование, различные варианты эндопротезирования желчных путей. ЭРХПГ с ЭПСТ на протяжении многих лет остается основным методом эндоскопического лечения холедохолитиаза. Этот метод позволяет в 85-90% случаев удалять конкременты из общего желчного протока и восстанавливать желчеотток. ЭРХПГ дает возможность не только контрастировать протоки, но и визуально оценить состояние БДС, а также периампулярной области. С этой точки зрения возможности ЭРХПГ, безусловно, шире по сравнению с другими методами исследования желчевыводящих путей. При наличии крупных фиксированных камней по ходу магистральных желчных протоков к ретроградному контрастированию последних прибегать не следует, ограничившись проведением УЗИ или КТ. Ретроградное контрастирование в этом случае ведет к ухудшению состояния больного в связи с увеличением гипертензии во внутрипеченочных протоках, инфицированием и затрудненной эвакуацией контрастного вещества и желчи. В такой ситуации показана чрескожная чреспеченочная декомпрессия желчных путей. Если размер камня больше диаметра образованного устья общего желчного протока, прибегают к внутрипротоковому разрушению камня с помощью ретроградной механической литотрипсии. Эта методика, по данным многих зарубежных авторов, может быть признана высокоэффективной. Иногда ЭРХПГ с ЭПСТ недоступна — после резекции желудка по Бильрот-II, наличие крупных дивертикулов и непреодолимых препятствий в устье общего желчного протока.
Необходимость во временном эндопротезировании гепатикохоледоха и назобилиарном дренировании вызвана наличием у пациентов выраженной желтухи и холангита в условиях, когда санация гепатикохоледоха оказалась неполной и желчеотток не был окончательно восстановлен. Назобилиарное дренирование в этих случаях помимо желчеотведения позволяет также промывать желчные пути растворами антибиотиков, что способствует быстрой ликвидации холангита и дает возможность выполнять рентгеноконтрастные исследования для контроля за отхождением фрагментов разрушенного камня и мелких конкрементов.
Ко второй группе малоинвазивных методов декомпрессии желчных путей относят ЧЧХГ с ЧЧХС, чрескожную чреспеченочную холецистостомию под контролем УЗИ, КТ или лапароскопа. Несмотря на совершенствование УЗИ диагностики и КТ, объективная информация о патологии желчных протоков, достаточная для принятия решения о методе декомпрессии, может быть получена только при прямом контрастировании желчных путей. В последние 10 лет широкое распространение получили методы чрескожных чреспеченочных эндобилиарных вмешательств [2, 5, 7, 8, 10]. Их удается осуществить независимо от уровня и протяженности обтурации желчных путей. Осложнения и летальность при них составляют от 3 до 10%. На начальном этапе ЧЧХГ проводили в целях дифференциальной диагностики МЖ, определения уровня блока желчных протоков, решения вопроса о возможности выполнения наружного дренирования. Абсолютными противопоказаниями к ЧЧХГ мы считаем непереносимость контрастных препаратов и выраженные нарушения свертывающей системы крови.
С внедрением в клиническую практику УЗИ, КТ потребность в выполнении ЧЧХГ сократилась. В настоящее время мы выполняем ЧЧХГ у больных с незначительной дилятацией желчных протоков, а также при подозрении на доброкачественную стриктуру желчных протоков и вентильный камень дистального отдела гепатикохоледоха у пациентов, которым невозможно выполнить ЭРХПГ.
В последние годы наложение чрескожной чреспеченочной холецистостомы под контролем УЗИ, КТ или лапароскопа стало наиболее распространенным методом, позволяющим не только сразу установить характер и место обтурации желчных путей, но и осуществить их декомпрессию. Рентгенологический вид блока при заболеваниях, вызывающих обтурационную желтуху, не является строго специфичным, что может быть объяснено различной распространенностью процесса, наличием мелких включений, замазкоподобных масс и воспалительного отека. Противопоказания к чрескожным чреспеченочным вмешательствам — множественные метастазы в печень, крайне тяжелое состояние больных с некорригируемой ПН, выраженная гипокоагуляция с угрозой кровотечения.
Целесообразность применения каждого метода декомпрессии определяется несколькими факторами, основными из которых являются:
- информативность диагностической методики;
- возможность трансформации диагностической процедуры в эффективное лечебное вмешательство;
- безопасность метода (вероятность осложнений и степень их тяжести);
- ехническая сложность метода.
Преимущественное значение, определяющее лечебный результат, имеют два первых фактора.
С учетом накопленного нами опыта мы рекомендуем придерживаться следующей схемы лечебно-диагностических малоинвазивных инструментальных вмешательств при МЖ: клинико-лабораторные данные, УЗИ, КТ Ѓ ЭРХПГ или ЧЧХГЃ ЭПСТ или ЧЧХС или холецистостомия Ѓ лапаротомия.
Если возможности малоинвазивных методов декомпрессии желчных протоков исчерпаны или ограничены, то в срочном порядке больному показана лапаротомия с выполнением одного из методов интраоперационного желчеотведения.
Адекватность декомпрессии оценивается нами путем изучения функционального состояния печени и изменения пейзажа микрофлоры. О степени нарушения функционального состояния печени позволяют судить данные радиоизотопной гепатографии, антипириновой и биливердиновой проб, которые выявляют снижение поглотительно-выделительной и обезвреживающей функций печени, повышение уровня билирубина в крови. Для выявления степени инфицированности желчи и определения эффективности антибактериальной терапии проводится изучение микрофлоры и количественного бактериологического анализа желчи методом газовой хроматографии и масс-спектрометрии.
Таким образом, малоинвазивные эндоскопические и чрескожные чреспеченочные декомпрессионные вмешательства представляют собой эффективный способ восстановления желчеоттока при обструкции билиарной системы. Эти методики позволяют достаточно быстро и эффективно ликвидировать МЖ и холангит, дают возможность проводить хирургические вмешательства в наиболее благоприятных условиях, в плановом порядке, а у больных пожилого возраста с тяжелой сопутствующей патологией могут служить альтернативой хирургическому лечению. Эти вмешательства малотравматичны и сопровождаются небольшим числом осложнений. Применение этих методов позволяет значительно улучшить результаты лечения больных МЖ.
Литература
Читайте также:

