Способности людей с вич
Обновлено: 24.04.2024
Иммунная система нашего организма представлена органами и клетками, расположенными по всему телу. Лимфоциты, являясь частью иммунной системы и обладая специфичностью, способны создавать и хранить иммунную память о возбудителе инфекционной болезни. Лимфоциты-Т4 (или CD4 Т-клетки) распознают чужеродные вещества или микроорганизмы, проникающие в наш организм, при этом запоминая их. При повторном попадании в наш организм этих чужеродных субстанций, белые клетки крови способны их распознавать, блокируя их разрушительное воздействие и уничтожать.
Тест на ВИЧ проводится методом ИФА и ориентирован на выявление антител и антигена. Отрицательный или негативный результат говорит о том, что антител не обнаружено. При этом ВИЧ очень быстро размножается в организме человека. И риск передать ВИЧ при сексуальном контакте или через кровь очень высокий.
У многих людей в первый год после заражения развивается острое заболевание с повышением температуры, увеличением лимфатических узлов. Иногда острая ВИЧ-инфекция может протекать как бронхит или пневмония, краснуха или в виде высыпаний на коже. Такое состояние у ВИЧ-инфицированного может продолжаться около двух недель, а затем состояние на фоне лечения основных симптомов нормализуется. Но на основании этих признаков нельзя сказать, что человек ВИЧ-инфицированный, т.к. перечисленные симптомы являются общими для многих заболеваний, например - обычной простуды.
Если в этот период не было начато лечение ВИЧ-инфекции, то у человека с ВИЧ наступает период, когда подавленный вирусом иммунитет больше не может выполнять свою защитную функцию. Тогда у ВИЧ-позитивного человека могут развивать заболевания, которые называют вторичными (первичным является ВИЧ-инфекция). Эти заболевания протекают вначале как бактериальные, грибковые и вирусные поражения слизистых оболочек и кожных покровов, позже развивается поражение внутренних органов. Одним из серьезных заболеваний для людей, живущих с ВИЧ является туберкулез. Если лечение так и не начинается, количество CD4 клеток становится менее 200, такое состояние угрожает жизни человека. Могут развиваться поражения нервной системы, онкологические заболевания, в т.ч. саркома Капоши - злокачественная опухоль кожи и сосудов.
Заключительная стадия развития ВИЧ-инфекции - это СПИД или терминальная стадия. Эта стадия была введена в клиническую классификацию ВИЧ-инфекции в 1989г., когда высокоактивной АРТ ещё не существовало и, несмотря на адекватную (по тем временам) терапию, имеющиеся у болеющих вторичные заболевания приобретали необратимый характер, и пациент погибал в течение нескольких месяцев после их развития. В настоящее время даже у пациентов с уровнем CD4, близким к нулю, и тяжёлыми вторичными заболеваниями, лечение ВИЧ-инфекции не является бесперспективным.

Российская клиническая классификация ВИЧ-инфекции
1. Стадия инкубации.
2. Стадия первичных проявлений.
Б. Острая ВИЧ-инфекция без вторичных заболеваний;
В. Острая ВИЧ-инфекция с вторичными заболеваниями.
3. Субклиническая стадия.
4. Стадия вторичных заболеваний.
4А. Потеря массы тела менее 10%, грибковые, вирусные, бактериальные поражения кожи и слизистых, повторные фарингиты, синуситы, опоясывающий лишай.
- прогрессирование на фоне отсутствия АРТ, на фоне АРТ;
- ремиссия (спонтанная, после АРТ, на фоне АРТ).
4Б. Потеря массы тела более 10%, необъяснимая диарея или лихорадка более мес, повторные стойкие вирусные, бактериальные, грибковые, протозойные поражения внутренних
органов, локализованная саркома Капоши, повторный или диссеминированный опоясывающий лишай.
- прогрессирование на фоне отсутствия АРТ, на фоне АРТ;
- ремиссия (спонтанная, после АРТ, на фоне АРТ).
4В. Кахексия. Генерализованные вирусные, бактериальные, микобактериальные, грибковые, протозойные, паразитарные заболевания, в том числе: кандидоз пищевода, бронхов, трахеи, лёгких; пневмоцистная пневмония; злокачественные опухоли; поражения центральной нервной системы.
Испытания лекарств от ВИЧ часто включает в себя аналитическое прерывание лечения, когда пациенты с ВИЧ прекращают прием антиретровирусной терапии (АРТ), чтобы ученые могли понаблюдать, как неконтролируемый вирус реагирует на исследуемые препараты.
Участие в такого рода клинических испытаниях может вызвать страх у человека с ВИЧ, который привык поддерживать неопределяемую вирусную нагрузку. Кроме того, предыдущее исследование, проведенное доктором Лау, показало, что многие люди с ВИЧ не были уверены в том, как работают эти испытания, и многие из них не были готовы к длительным периодам определяемой вирусной нагрузки.
Ученые работают над различными стратегиями излечения ВИЧ-инфекции. Некоторые методы нацелены на сокращение латентных резервуаров ВИЧ — инфицированных иммунных клеток, которые не производят новые вирионы в течение многих месяцев или лет. Другие виды терапии пытаются повысить способность иммунной системы контролировать вирус.
Существуют два типа исследований, основанных на прерывании лечения, которые используются для оценки потенциальной терапии: изучение времени до восстановления вирусной активности (TVR) и изучение контрольных точек. В исследованиях TVR после того, как участники прекращают АРТ, ученые измеряют время, необходимое, чтобы вирусная нагрузка сначала достигла обнаруживаемого уровня (50 копий/мл), а затем время, необходимое для достижения более высокого порога (часто 10 000 копий/мл), после чего участники возобновляют прием АРТ. Если тем, кто получает лечение, требуется больше времени для достижения этих пороговых значений по сравнению с контрольной группой, это указывает на то, что терапия замедляет восстановление вирусной активности. Исследования TVR часто используются для оценки методов терапии, нацеленной на резервуары, обычно они длятся всего несколько недель.
Исследования контрольных точек демонстрируют, насколько эффективно иммунная система участников контролирует ВИЧ самостоятельно. В этих гораздо более длительных исследованиях (до нескольких месяцев) исследователи позволяют вирусным нагрузкам участников достигать высоких уровней, имитируя острую фазу ВИЧ, чтобы проследить, сможет ли их иммунная система в дальнейшем снизить эту нагрузку. Порог для возобновления АРТ обычно устанавливается на высоком уровне (часто 100 000 копий/мл). Когда участники, получающие лечение, способны контролировать ВИЧ при более низких уровнях вирусной нагрузки и в течение более длительного времени, чем участники контрольной группы, это говорит о том, что терапия повышает их иммунитет против вируса.
Несмотря на то, что нет конкретных рекомендаций, определяющих, как планировать исследования с прерыванием лечения, группа ученых, занимающихся исследованием ВИЧ, встретилась в 2018 году, чтобы обсудить этические стороны и выработать методы для снижения риска. Прекращение АРТ во время этих исследований не просто подвергает участников риску длительных периодов определяемой, а в некоторых случаях и высокой вирусной нагрузки. Более высокие вирусные нагрузки также могут подвергать опасности и ВИЧ-отрицательных половых партнеров участников.
До сих пор в большинстве исследований риск снижался за счет небольшого числа участников и отсутствия контрольной группы, которая вместо лечения принимала неактивное плацебо. Включение контрольной группы важно, потому что это позволяет ученым сравнивать тех, кто принимает лекарства, с теми, кто находится на плацебо. Тем не менее научное сообщество обсуждало этичность использования контрольных групп в подобных испытаниях лекарств, потому что они подвергаются длительным периодам повышенной вирусной нагрузки в отсутствие каких-либо препаратов, даже экспериментальных.
Исследование
Доктор Лау и ее коллеги использовали данные предыдущих клинических испытаний для создания математических моделей, позволяющих оценить, как различные их параметры влияют на статистическую мощность испытания.
Статистическая мощность аналогична чувствительности. Например, тест на ВИЧ с чувствительностью 80% успешно идентифицирует вирус у 80% людей, которые на самом деле ВИЧ-положительны, но не выявит у остальных 20% ВИЧ-положительных людей. Когда клиническое испытание, оценивающее лечебную терапию, должно достигнуть статистической мощности в 80% (при условии, что терапия имеет реальную пользу для тех, кто ее принимает), в испытании будет 80-процентная вероятность обнаружить пользу и 20-процентная вероятность ее упустить.
Проще говоря, чем больше данных задействовано в испытании, тем большей статистической мощностью оно будет обладать. Такие факторы, как количество участников, число контрольных параметров, продолжительность испытания и частота анализов крови, влияют на статистическую мощность испытания.
Результаты пробного моделирования TVR
В отношении недавнего исследования TVR с участием 13 человек такая модель показала, что при мощности 80% исследование выявило бы только лечение со значительным снижением реактивации (от 70 до 80%). Чтобы исследование TVR выявило снижение реактивации на 30%, потребуется уже по 120 участников в группе терапии и в контрольной группе. Поскольку в большинстве исследований TVR задействовано малое число участников, они, вероятно, не устанавливают умеренных результатов терапии.
Может показаться нелогичным планирование исследования для выявления меньшего эффекта от лечения, когда конечной целью является поиск максимальной пользы (т. е. терапия, приводящая к 100% снижению реактивации). Тем не менее на начальных этапах поиска лекарства необходимо фиксировать даже умеренные результаты, чтобы решить, требует ли этот метод дальнейшего изучения.
Помимо рекомендации увеличить количество участников, команда предлагает использовать ретроспективные контрольные данные в дополнение к контрольным группам. Данные из предыдущих испытаний, в которых люди прерывали АРТ, могли бы повысить потенциал выявления умеренной пользы от лечения. Они смоделировали гипотетическое исследование TVR, в которое вошли 50 участников и 50 человек из контрольной группы. При мощности 80% эта конструкция может обнаруживать снижение реактивации до 43%. Добавление ретроспективных данных еще 150 участников позволило бы в том же испытании выявить снижение до 36%.
Такое моделирование также не показало практически никакого улучшения способности обнаруживать снижение реактивации при увеличении продолжительности испытаний TVR свыше пяти недель. После этого срока модель предсказала улучшение обнаружения не более чем на 1%. Точно так же они не обнаружили практически никакой пользы от проведения лабораторного мониторинга чаще, чем раз в неделю. Наблюдение за людьми два раза в неделю почти не помогло обнаружить снижение реактивации.
Ученые провели отдельный анализ для оценки максимального риска передачи ВИЧ во время исследований TVR на основе предыдущих данных. Они оценили максимальный риск передачи, предполагая, что участники занимались незащищенным сексом и что доконтактная или другие методы профилактики не использовались. Кроме того, если во время еженедельного мониторинга не сообщать пациенту показатель вирусной нагрузки сразу же, то участник, которому необходимо возобновить АРТ (если его вирусная нагрузка превысила 1000), скорее всего, отложит это до следующего еженедельного визита.
Было подсчитано, что в этом случае во время пятинедельного исследования TVR с порогом вирусной нагрузки 1000 для повторного начала АРТ максимальный риск передачи ВИЧ составил 3,6 на 1000 участников, занимающихся вагинальным сексом. При анальном сексе для вводящих партнеров максимальный риск составлял около 7 на 1000, а для принимающих партнеров — около 70 из 1000. Изменение схемы исследования, включающее экспресс-тестирование на вирусную нагрузку и возобновление АРТ в тот же день, снижает предполагаемый максимальный риск до 0,9, 1,8 и 18 на 1000 соответственно.
Результаты моделирования исследования по контрольным величинам
Исследования контрольных точек должны иметь достаточную статистическую мощность, чтобы отделять преимущества предлагаемой лечебной терапии от контроля после лечения. Используя результаты исследования CHAMP, ученые предположили, что исходный уровень контроллеров после лечения ниже 4%. Если целью исследования было определить увеличение количества контролеров до 20% (это означает, что терапия помогла людям, которые не являются естественными контроллерами, подавить вирус), их модель показала, что 24-недельное исследование со статистической мощностью 80% потребует участия 60 пациентов.
Из-за чрезвычайно высоких вирусных нагрузок в типичных исследованиях контрольных величин (до 100 000) авторы сравнили, как использование более консервативного порогового значения (1000) для возобновления АРТ повлияет на способность этих исследований обнаруживать увеличение числа контроллеров после лечения. CHAMP показало, что у 55% контроллеров после лечения первоначальные всплески вирусной нагрузки не превышали 1000 копий/мл, и в дальнейшем они сохраняли вирусную нагрузку ниже этого порога.
Используя эти данные, Лау и Кромер предположили, что использование порога в 1000 копий маскирует 45% естественных контроллеров после лечения, что может помешать обнаружить, когда терапия усиливает иммунный контроль участников над ВИЧ. Чтобы восстановить статистическую мощность, потребуется больше участников. Как и в приведенном выше примере, при мощности 80% и цели выявления 20-процентного повышение числа контроллеров после лечения свыше базового уровня 4%, более низкий порог вирусной нагрузки потребует увеличить количество участников с 60 до 120 как в лечебных, так и контрольных группах.
Как и в случае исследований TVR, ученые также оценили максимальный риск передачи ВИЧ во время определения контрольных величин, используя те же предположения, что и описанные выше (отсутствие стратегий профилактики и экспресс-тестирования на вирусную нагрузку, незащищенный секс, недельная задержка перед возобновлением АРТ). Из-за гораздо большей продолжительности испытаний и высоких пороговых значений вирусной нагрузки (для этого они сослались на исследование контрольных величин, в котором использовали данные 50 000 человек) они оценили максимальный риск передачи ВИЧ как 13 случаев на 1000 при вагинальных половых контактах, около 25 на 1000 — для вводящего партнера при анальном сексе, 214 на 1000 — крайне высокий — для принимающего партнера при анальном сексе.
Предлагаемая гибридная схема испытаний
Основываясь на собственном моделировании и оценках максимального риска передачи, ученые предлагают использовать гибридную модель для анализа прерывания лечения. В озвученной ими схеме прерывания будут начинаться с пятинедельного исследования TVR. Хотя оно, как правило, применяется, когда терапия нацелена на резервуары ВИЧ, у людей, отвечающих на терапию, направленную на усиление иммунитета, также будет наблюдаться более медленное восстановление вируса (если лечение было эффективным).
Начало испытания для оценки потенциального лечения с помощью исследования TVR подвергнет участников гораздо более коротким перерывам в лечении, что позволит исследователям определить, имела ли эта терапия достаточную эффективность, чтобы перейти к более длительному изучению заданных значений. Если медики согласятся с необходимостью дальнейшего исследования, а пациенты с вирусной нагрузкой ниже 1000 согласятся перейти к следующей фазе, они продолжат тщательное наблюдение в течение 24 недель или до тех пор, пока вирусная нагрузка участников не превысит 1000 копий/мл, после чего они возобновят АРТ.
Ученые рекомендуют провести экспресс-тестирование на вирусную нагрузку и возобновить АРТ в тот же день, чтобы свести к минимуму риск передачи инфекции. По их оценке, ограничение контрольной точки теми, кто уже демонстрирует контроль за вирусом, до вирусной нагрузки ниже 1000, снижение порога вирусной нагрузки для возобновления АРТ до 1000, ограничение продолжительности до 24 недель, а также включение тестирования по месту оказания медицинской помощи и возобновление АРТ в тот же день снижают максимальный риск передачи до 0,2 на 1000 при вагинальном сексе, до 0,35 на 1000 — для вводящего партнера при анальном сексе и до 3,1 на 1000 — для принимающего партнера при анальном сексе. И это значительное улучшение показателей по сравнению с оценкой, полученной в ходе традиционных исследований контрольных величин.
Если первоначальное исследование TVR показывает, что лечение не требует дальнейшего изучения (например, если не обнаружено позитивного эффекта), то ученые смогут избежать затрат на проведение длительного исследования контрольных величин.
Выводы
Ученые пришли к выводу, что в испытаниях лекарств недостаточно участников для обеспечения знаковой статистической мощности при умеренных результатах лечения. Поскольку чаще всего при испытаниях терапии также не используются контрольные группы, количественная оценка пользы лечения чрезвычайно сложна. Специалисты рекомендуют сотрудничать всем заинтересованным структурам для создания ретроспективной контрольной базы данных, которая позволила бы разработать схему испытаний, не полностью полагающуюся на контрольные группы плацебо. Тем не менее они отмечают, что задействование ретроспективных контрольных данных означает включение людей, которые с большей вероятностью начали АРТ во время хронической ВИЧ-инфекции, и тех, кто использует более старые схемы АРТ, которые могут действовать как искажающие факторы.
Тем не менее сокращение числа участников, получающих плацебо, снижение пороговых значений вирусной нагрузки, продолжительности испытаний и рисков передачи ВИЧ могут побудить большее число людей с ВИЧ участвовать в исследованиях с прерыванием лечения.
Вирусы могут размножаться только внутри клетки-хозяина, перестраивая ее работу так, что клетка начинает производить новые вирусные частицы. Это серьезно нарушает работу самой клетки и в большинстве случаев ведет к ее гибели. Процесс проникновения и размножения вируса в ней сложный и содержит много стадий, а значит, специальные лекарства могут тормозить его на различных этапах.
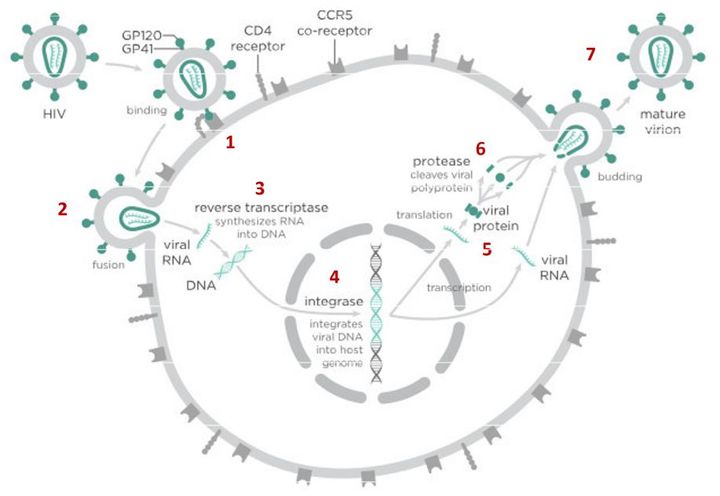
В случае с ВИЧ это выглядит так.
по теме

Лечение
Лучшие научпоп-статьи 2018 года
После того как вирусная частица приклеилась к рецепторам CD4 и CCR5/CXCR4 и закрепилась на поверхности клетки, другой специальный белок вируса gp41 соединяет оболочку вируса с мембраной клетки-мишени и помогает вирусу проникнуть внутрь клетки (цифра 2 на схеме). На этом этапе остановить вирус может другая группа препаратов — ингибиторы слияния, например, энфувиртид. Препарат связывается с вирусным белком gp41 и нарушает его работу.
На этом этапе размножение вируса блокирует очень большое количество препаратов из двух классов — нуклеозидные ингибиторы обратной транскриптазы (НИОТ — ламивудин, абакавир, тенофовир) и ненуклеозидные ингибиторы обратной транскриптазы (ННИОТ — эфавиренз, рилпивирин). Принцип действия у веществ из обеих групп похожий: молекула лекарства связывается с обратной транскриптазой вируса, нарушает ее работу и так блокирует перенос генов вируса из РНК в ДНК. Это не позволяет генам вируса встроиться в ДНК клетки-хозяина и начать производство новых вирусных частиц.
На следующем этапе инфицирования (цифра 4 на схеме) готовая вирусная ДНК проникает в ядро и встраивается в ДНК клетки-хозяина с помощью специального вирусного фермента — интегразы. Работу этого фермента блокируют ингибиторы интегразы, например, долутегравир, не позволяя ДНК вируса встроиться в наши гены.
После того как вирусная ДНК встраивается в ДНК клетки-хозяина, клетка получает неправильную программу и начинает производить вирусные белки и РНК, необходимые для сборки новых частиц вируса (цифра 5 на схеме), используя для этого структуры, которые в норме производят собственные белки клетки. Такая перенастройка производства белка сильно нарушает работу клетки и через некоторое время вызывает ее гибель. Лекарств, которые бы влияли на этот этап размножения вируса, нет, так как здесь вирус использует собственные ферментные системы клетки-хозяина и блокирование их работы какими-то веществами навредит здоровым клеткам.
по теме

Лечение
Ошибка системы. Почему в регионах опять не хватает таблеток от ВИЧ
После синтеза вирусных белков клеткой-хозяином в работу вступает еще один фермент вируса — протеаза (цифра 6 на схеме). Дело в том, что белки ВИЧ синтезируются в виде длинных цепочек белков-предшественников, но они неактивные. Протеаза разрезает эти цепочки на более короткие фрагменты, которые становятся активными белками вируса: из одних собирается вирусная оболочка, другие выполняют функции ферментов (обратная транскриптаза, интеграза, протеаза, о которых мы говорили выше). Класс лекарств, нарушающих работу вирусной протеазы, включает большое количество препаратов от достаточно старого лопинавира до современного дарунавира. Основной недостаток препаратов этого класса — высокая степень перекрестной устойчивости: если вирус приобретает устойчивость к одному препарату, скорее всего, на него не подействует ни один другой препарат из этого класса.
На последнем этапе (цифра 7 на схеме) вирусные частицы собираются из готовых компонентов (синтезированных клеткой вирусных белков и РНК), как конструктор, и покидают клетку-хозяина. Лекарств, которые бы тормозили эти процессы, пока не существует.
ВИЧ имеет высокую склонность к мутациям, что позволяет ему быстро приобретать устойчивость к лекарствам. Мутации изменяют форму молекул ферментов вируса. Если при этом форма изменится существенно, то фермент не сможет нормально работать и такой вирус размножаться перестанет — это вредная для вируса мутация. Однако в некоторых случаях — при полезных мутациях — форма молекулы фермента меняется не сильно, а так, что сам фермент продолжает нормально работать, но молекула лекарства уже не может с ним связаться.
Поэтому для эффективного подавления размножения ВИЧ обычно назначают три разных препарата из разных групп, влияющих на разные ферменты вируса, блокируя его воспроизводство на разных этапах. Исключением является группа ингибиторов обратной транскриптазы (НИОТ и ННИОТ) — эти лекарства связываются с разными участками молекулы вирусного фермента, поэтому могут назначаться вместе, несмотря на то, что относятся к одной группе. В условиях такой терапии вирусу очень трудно выработать устойчивость, потому что одновременно должно произойти несколько полезных мутаций в разных генах вируса, а это бывает крайне редко.
Есть несколько перспективных технологий, например, CRISPR/Cas9, которые могут позволить полностью удалить вирусную ДНК из организма человека, но пока ни одна из них не прошла все необходимые исследования для подтверждения эффективности и безопасности. Исследования продолжаются.




Клиника является первым частным медицинским учреждением России и единственным в Москве и области, успешно прошедшим процедуру сертификации Росздравнадзора (Сертификат №0023/01КБМД от 10.10.2019 г.).
ВИЧ и СПИД – отличия, длительность развития, прогнозы
СПИД – это конечная стадия ВИЧ, которая характеризуется сильно сниженным иммунитетом. Важно не путать два этих понятия. С момента инфицирования ВИЧ болезнь до стадии СПИДа без лечения может развиваться в течение 9-11 лет (в среднем). При постановке диагноза СПИД без лечения продолжительность жизни короткая – в среднем до 19 месяцев.
Если вовремя начать лечение, то на стадии ВИЧ можно прожить очень долгую жизнь – продолжительность жизни таких пациентов благодаря современному лечению составляет 20-50 лет. И хоть при стадии СПИД ситуация гораздо сложнее, но многие пациенты при должном лечении и крепком организме могут прожить более 10 лет.
Очевидно, что прием терапии – важнейший фактор для лечения ВИЧ и полноценной долгой жизни. Более того, именно лечение позволяет значительно снизить вирусную нагрузку и сделать зараженного человека неопасным для партнера, а также членов семьи.
Пути передачи ВИЧ
Основные пути заражения ВИЧ:
- незащищенный секс с зараженным человеком (самый распространенный путь передачи ВИЧ). Заразиться можно как после однократного контакта, так и после нескольких;
- использование иглы для введения наркотиков после зараженного человека. Либо другие варианты ситуаций, при которых происходит контакт крови здорового человека с кровью зараженного;
- передача от матери к плоду во время родов или от матери ребенку во время вскармливания. Важная ремарка: если женщина лечится и находится под контролем врачей, у нее есть все шансы родить здорового малыша;
- переливание инфицированной крови. В современных клиниках и больницах это уже исключено, поскольку все материалы проходят очень серьезную проверку.
Также выделяют так называемые группы риска – это люди, которые больше других подвержены заражению ВИЧ:
- люди, ведущие беспорядочную половую жизнь;
- гомосексуалисты;
- наркоманы, которые колют инъекции;
- люди с партнером, зараженным вирусом.
Такие люди должны постоянно сдавать анализ. В ряде случаев им рекомендованы профилактические препараты (только по рекомендации врача).
Говоря о том, как можно заразиться ВИЧ, следует уточнить, в каких случаях это невозможно:
- во время бытовых контактов;
- при использовании посуды инфицированного;
- при укусе насекомого;
- при поцелуе.
Контакт с ВИЧ-зараженным на бытовом уровне (в семье, на работе, в другом формате общения) абсолютно безопасен и не несет никакой угрозы для окружающих.
Основные стадии заболевания

Стадии ВИЧ делятся на следующие:
- инкубационная. Это стадия, на которой происходит заражение и последующее размножение вируса в крови. Она длится до шести недель, иногда меньше. Даже будучи зараженным, на этом этапе человек не увидит явных признаков, а анализ крови не покажет, что в крови есть антитела;
- первичная. Здесь уже могут появиться первые признаки инфекции. Длится вторая стадия в течение 3 недель – в это время появляются антитела, вирус определяется лабораторно;
- субклиническая. Появляется первый признак болезни – увеличенные лимфоузлы. Ппациент чувствует себя полностью здоровым, на самочувствие не жалуется;
- появление вторичных заболеваний. Иммунитет начинает давать сбои, из-за чего проявляются самые разные болезни: от частых простуд и кандидоза до пневмоний, туберкулеза;
- терминальная. Стадия предполагает истощение (довольно быстрое и прогрессирующее), а также последующую смерть больного.
Стадии не имеют единственно верных временных рамок – они могут отличаться у разных людей. Например, часто ВИЧ-инфицированные годами чувствуют себя хорошо или не обращают внимание на небольшие признаки. Болезнь обнаруживается только на стадии сильного ухудшениям самочувствия или благодаря случайным анализам.
Симптомы ВИЧ
Выяснив, как передается ВИЧ, нужно разобраться с симптомами. Проблема в том, что эти симптомы проявляются на ранней стадии, затем пропадают и долгое время больше не беспокоят человека – буквально годами. А еще они очень похожи на проявления других болезней, что может вводить в заблуждение.
Так, на первом этапе, когда вирус себя проявил, человек может чувствовать:
- боль в горле, повышение температуры;
- болезненность кожи, суставов, костей4
- озноб, лихорадку.
Одновременно с этим увеличиваются шейные лимфоузлы, могут проявиться разные высыпания. Все это часто принимается за признаки ОРВИ или других подобных болезней.
Новые симптомы ВИЧ возвращаются через несколько лет спокойной и здоровой жизни. К ним относятся:
- сильная усталость, быстрая утомляемость;
- увеличение лимфоузлов – не только шейных, а уже нескольких групп;
- снижение веса. Обычно оно выглядит беспричинным, человек не понимает, в чем дело;
- лихорадка, озноб, потливость (преимущественно ночная);
- проблемы с ЖКТ – обычно проявляются жидким стулом без видимых на то причин.
На этом этапе, как правило, и обнаруживается заболевание – потому что пациент обращается к врачу, а специалист назначает дополнительное обследование.
Как диагностируют ВИЧ в Москве
Для диагностики вируса есть два теста: предварительный ИФА и максимально точный иммуноблот. Точность ИФА составляет около 90%. Его рекомендуют проводить через 3-6 месяцев после контакта с вирусом, тогда он дает максимальную точность. Обычный тест ИФА основан на анализе крови, есть также экспресс-тесты, которые помогают получить информацию на основе мочи или слюны. Такие тексты покупают исключительно в аптеке (ни в коем случае не в интернете!), поскольку необходимо использовать официально утвержденные изделия.
Важно: тест не показывает, как передается ВИЧ в конкретной ситуации – то есть определить путь заражения можно только путем анализа собственных действий.
Лечение ВИЧ
Лечение сводится к назначению антиретровирусной терапии. Пациенту составляют схему приема препаратов – и ее нужно соблюдать максимально точно, не отклоняясь от программы. В противном случае вирус может выработать устойчивость к лечению и не поддаваться дальнейшему подавлению.
Показателями качественного лечения являются снижение вирусной нагрузки, а также увеличение в крови клеток CD4+, которое говорит об активности иммунитета.
Лекарства для лечения выдаются в медицинских учреждениях, пациенты ставятся на учет и получают препараты бесплатно, в установленном порядке. Информация о заболевании является конфиденциальной – она не направляется на работу, место учебы или в другие места. Пациент имеет право оставить ее втайне (если это не предусмотрено отдельными рабочими договорами).
При соблюдении правил приема терапии вирус в крови постепенно снижается, со временем пациент становится полностью безопасным для своего полового партнера и не способен никого заразить.
Профилактика ВИЧ-инфекции
Первое и главное правило – регулярно проверяться на ВИЧ даже в том случае, если вы не имели подозрительных контактов. Рекомендуется обследоваться раз в полгода – тем более для этого есть удобные экспресс-тесты.
Внимательно нужно относиться и к выбору партнеров. Не стоит верить на слово человеку, который говорит, что он точно не болеет – лучше попросить результаты исследования и самостоятельно убедиться, что ему можно доверять. Но помните, что в течение полугода даже зараженная кровь может не давать положительных результатов.
Профилактика ВИЧ заключается в следующих моментах:
- защищенный секс с непостоянными половыми партнерами, а также постоянными, если нет уверенности в том, что партнер не болен или хранит верность;
- исключение из жизни наркотиков, беспорядочных половых связей;
- соблюдение общей гигиены. Не стоит делиться бритвой, зубной щеткой, кусачками для ногтей и другими предметами, которые могут контактировать с маленькими ранками.
Главная профилактика заключается в том, чтобы знать об инфекции и всегда помнить об опасности заражения.
Популярные вопросы-ответы про ВИЧ
Как проявляется ВИЧ у мужчин и женщин?
Симптомы ВИЧ у женщин ровно такие же, как и симптомы ВИЧ у мужчин. Проявления могут отличаться только на уровне заболеваний мочеполовой сферы, когда организм уже сильно ослаблен – например, у женщин чаще проявляется молочница. В остальном специфических признаков по полу не наблюдается.
Лечится ли ВИЧ?
Технически можно сказать, что ВИЧ не лечится – пациентам постоянно показана специальная терапия. Но те результаты, которых она позволяет добиться, делают из пациента здорового человека, который может спокойно прожить десятки лет без особых проблем – нужно только постоянно принимать препараты и следить за здоровьем.
ВИЧ давно не является смертельным заболеванием!
ВИЧ – это болезнь наркоманов и людей с беспорядочным образом жизни?
Кто такие ВИЧ-диссиденты?
Это люди, которые вопреки научным данным и здравому смыслу отрицают существование вируса. Они отказываются от лечения, что неминуемо ведет к ранней смерти. Такие люди опасны и тем, что из-за отсутствия лечения распространяют вирус среди своих половых партнеров, не предупреждая их о возможной опасности (поскольку не считают, что она есть).
Успех лечения ВИЧ и долгой жизни заключается в том, чтобы как можно раньше обратиться за помощью и начать терапию. В этом случае человека ждет долгая жизнь без страхов и сложностей.
Читайте также:

