Спутанное сознание при вич
Обновлено: 19.04.2024
Нет, настоящий иммунодефицит — это серьезное заболевание, при нем в организме часто появляются инфекционные заболевания, которые протекают тяжело. Речь совсем не про ОРВИ. Иммунодефицитом врачи также называют состояние, при котором один или несколько факторов иммунной системы перестают защищать организм. В целом термин можно назвать собирательным, потому что причины, по которым эти факторы перестают работать, могут быть разными.
Глобально иммунодефициты можно разделить на три группы.
Их не стоит бояться, врачи определяют их как нормальное состояние человека. Физиологические иммунодефициты сигнализируют, что организм проходит через разные этапы жизнедеятельности. Они могут быть в детстве, во время беременности или в старости. Лечить их не нужно, просто важно понимать, что в это время люди болеют чаще. Поддерживать организм в эти периоды можно только с помощью вакцинации и здорового образа жизни.
Они возникают чаще всего в результате генетической поломки. Допустим, ребенок рождается с поломанным участком гена, отвечающего за какой-то из компонентом иммунной системы. В таком случае у него может не быть определенных клеток или белковых факторов, из-за этого ребенок начинает часто и тяжело болеть.
Современной медицине известно более 250 видов ПИД. Британское общество иммунологии отмечает, что в мире насчитывается около 6 миллионов людей с этим заболеванием, однако точное количество больных с ПИД установить невозможно — порядка 70—90 % из них остаются не диагностированными. Группа исследователей следила за жизнью 235 пациентов с первичным иммунодефицитом на протяжении 22 лет, за это время 32 из них умерли.
В России один из 500 россиян рождается с первичным иммунодефицитом. В российском регистре Национальной ассоциации экспертов в области ПИДС состоит 3017 пациентов.
Само название говорит о том, что изменения в иммунной системе появились не при рождении, а вторично — в результате какого-то патологического процесса или воздействующих факторов. Яркий пример вторичного иммунодефицита — это люди с ВИЧ-инфекцией. Изначально здоровый человек инфицируется вирусом, поражающим клетки иммунной системы, в результате развивается иммунодефицит. К этой же группе могут относиться пациенты с онкологическими заболеваниями, получающие химиотерапию. Вторичный иммунодефицит, как правило, протекает на фоне других заболеваний. Развитие иммунодефицитного состояния затрудняет их лечение, способствует формированию осложнений. Помимо ВИЧ к этой группе можно отнести лучевую болезнь, лимфопролиферативные заболевания, то есть связанные с клетками лимфоидной природы. Вторичный иммунодефицит, в отличие от ПИД, может пройти без лечения, например, если исчезнет воздействующий фактор.
Может ли человек с первичным иммунодефицитом вылечиться?
У некоторых людей с ПИД действительно нет шансов на полное выздоровление. Медицина может предложить им только поддерживающую терапию, направленную на борьбу с инфекцией. Но случается, что у самых тяжелых пациентов с первичным иммунодефицитом есть шанс на полное выздоровление. Это может произойти благодаря трансплантации гемопоэтических стволовых клеток от донора. Поэтому важно, чтобы как можно больше человек вступали в регистр доноров костного мозга.
Насколько опасны вторичные иммунодефициты?
Если говорить о ВИЧ, то без антиретровирусной терапии прогноз неблагоприятный. У человека могут развиться не только тяжелые инфекции, но и онкологические заболевания на последних стадиях (уже при СПИДе). Если говорить о вторичных иммунодефицитах, которые формируются в результате химиотерапии, то они проходят самостоятельно, как только заканчивается курс лечения.
Иммунодефициты легко распознать? Бывает ли, что врачи начинают лечить здоровых людей, думая, что у них иммунодефицит?
Важно понимать, что иммунодефицит — это тяжело протекающие инфекционные заболевания бактериального, грибкового и вирусного характера. И речь не про ОРЗ и ОРВИ. У людей с ним зачастую в анамнезе несколько пневмоний, синуситов, абсцессов, тяжелый кандидоз кожи и слизистых, тяжелое течение герпетических вирусов.
ВИЧ — вирус иммунодефицита человека
КТ — компьютерная томография
МРТ — магнитно-резонансная томография
ПМЛ — прогрессирующая многоочаговая лейкоэнцефалопатия
ЦМВИ — цитомегаловирусная инфекция
Одним из самых тяжелых вторичных заболеваний, возникающих при ВИЧ-инфекции, является прогрессирующая многоочаговая лейкоэнцефалопатия (ПМЛ). Эту инфекцию вызывает полиомавирус JC. Возбудитель широко распространен: антитела к нему обнаруживаются у 80% людей, однако реактивация вируса и клинические проявления возникают только при выраженном снижении клеточного иммунитета. Как правило, симптомы ПМЛ появляются у больных с уровнем лимфоцитов CD4 менее 100 В 1 мкл, но отмечены случаи развития заболевания и при количестве CD4, превышающем 200 В 1 мкл. ПМЛ диагностируется примерно у 2—5% больных инфекцией, вызванной вирусом иммунодефицита человека (ВИЧ) [1].
Вирус JC инфицирует и разрушает олигодендроциты головного мозга, продуцирующие миелин. Это приводит к множественной демиелинизации в полушариях головного мозга, мозжечке и стволе мозга. Для клинической картины ПМЛ характерны когнитивные расстройства, снижение остроты зрения, афазия, атаксия, моно- и гемипарезы, эпилептиформные припадки, а также другие признаки очаговых поражений головного мозга. Болезнь медленно прогрессирует в течение нескольких недель и даже месяцев и, как правило, приводит к летальному исходу [1, 2].
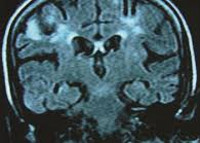
Прижизненная диагностика ПМЛ затруднена. Для заболевания не характерны изменения показателей периферической крови. При исследовании спинномозговой жидкости признаки воспаления отсутствуют, может отмечаться небольшое повышение уровня белка и двузначный цитоз. Возможно обнаружение JC-вируса в ликворе методом полимеразной цепной реакции. Однако чувствительность метода составляет около 80%, специфичность 90—99% [3]. Для установления диагноза наибольшее значение имеют лучевые методы исследования головного мозга, предпочтение отдается магнитно-резонансной томографии (МРТ), так как при компьютерной томографии (КТ) очаги пониженной плотности плохо визуализируются. Изменения на магнитно-резонансной томограмме при ПМЛ всегда начинаются с небольшого, единичного очага демиелинизации, постепенно приобретая картину многоочагового поражения мозга. Очаги могут располагаться в любой части головного мозга, как правило, они асимметричны [4].
Специфическое лечение ПМЛ с доказанной эффективностью в настоящее время отсутствует. Пока антиретровирусная терапия (АРВТ) является основным методом лечения ПМЛ при ВИЧ-инфекции. Но даже на фоне АРВТ прогноз у пациентов с развившейся клинической симптоматикой ПМЛ неблагоприятный. Средняя продолжительность жизни составляет 1—6 мес, крайне редко отмечаются случаи стабилизации и улучшения состояния больных на протяжении более 2 лет [5].
В виду трудности диагностики и лечения ВИЧ-инфицированных пациентов с ПМЛ, высокой летальности, наличия реальной возможности стабилизации их состояния представляем наш положительный опыт лечения ВИЧ-инфицированной пациентки с установленным диагнозом ПМЛ.
Пациентка Д., 33 года, поступила 20.06.14 в ГБУЗ ИКБ № 2 ДЗМ (ИКБ № 2) в профильное отделение для больных ВИЧ-инфекцией переводом из Научно-исследовательского института скорой помощи им. Н.В. Склифосовского (НИИ им. Н.В. Склифосовского) в тяжелом состоянии с направительным диагнозом: очаговые поражения головного мозга. ВИЧ-инфекция, стадия вторичных заболеваний. При поступлении уровень сознания — оглушение, выраженные нарушения когнитивных функций, выраженная дизартрия, тетрапарез.
23.06 состояние пациентки ухудшилось: в речевой контакт практически не вступала, стала заторможена, пассивно лежала в кровати, уровень сознания — оглушение. Больная переведена в отделение интенсивной терапии (ОИТ) для больных ВИЧ-инфекцией. Количество лимфоцитов CD4 339 в 1 мкл (20%), нагрузка ВИЧ в крови 160 761 копий/мл. В крови методом полимеразной цепной реакции обнаружена ДНК цитомегаловируса (ЦМВ) — 93 копий/мл. В ликворе зафиксирован подъем уровня белка до 0,69 г/л, цитоз до 5 лейкоцитов в 1 мкл, в мазке из 10 клеток все лимфоциты. В анализе ликвора на оппортунистические инфекции методом ПЦР обнаружена ДНК JC-вируса. Другие инфекции (ДНК ЦМВ, ДНК вируса Эпштейна—Барр, ДНК вируса герпеса VI типа, ДНК вируса простого герпеса I и II типа, ДНК Candida albicans, glabrata, krusei, parapsilosis, tropiccalis, ДНК Varicellae zoster virus, ДНК Toxoplasma gondii, ДНК Cryptococcus neoformans, Mycobacterium tuberculosis complex) не обнаружены. РНК ВИЧ в ликворе 341 копия в 1 мл.
Пациентка находилась в ОИТ с 23.06 по 10.09.14, где проводилась внутривенная дезинтоксикационная, антибактериальная, противоотечная, фунгицидная, седативная терапия, бисептол, цимевен, с последующим переходом на вальцит. Начата АРВТ по схеме: лопинавир/ритонавир, зидовудин и ламивудин в стандартных дозировках. Затем в связи с развитием цитопении (анемия, лейкопения) зидовудин заменен абакавиром.
У пациентки восстановилось сознание, она стала контактна, адекватна, ориентирована, критична. Дизартрия незначительная. По остальным органам и системам без динамики. К моменту выписки клинически значимых изменений в общем и биохимическом анализах крови не отмечалось. На фоне АРВТ нагрузка ВИЧ в крови снизилась до 709 копий в 1 мл, однако уровень лимфоцитов CD4 составлял 163 в 1 мкл (19%). После курса лечения цимевеном ДНК ЦМВ в клетках крови не обнаружена. В ликворе положительная динамика в виде снижения цитоза до 1 клетки в 1 мкл, снижения уровня белка с 0,69 до 0,55 г/л, РНК ВИЧ 20 копий в 1 мл. При последующих исследованиях ликвора ДНК JC-вируса обнаружить не удавалось. На повторном снимке МРТ головного мозга отмечалась отрицательная динамика в виде увеличения зоны патологических изменений с распространением диффузного билатерального симметричного поражения средних ножек мозжечка, определения патологической зоны в правой ножке мозга.
По настоятельной просьбе родственников пациентка выписана на амбулаторное лечение с диагнозом: ВИЧ-инфекция, стадия 4 В, фаза прогрессирования вне АРВТ: прогрессирующая мультифокальная лейкоэнцефалопатия, клинически проявляющаяся цитомегаловирусная инфекция (ЦМВИ) с поражением центральной и периферической нервной системы. Снижение массы тела более 10%. Осложнения: анемия.
За период наблюдения пациентка дважды госпитализирована в ИКБ № 2 с 17.09 по 23.10 и с 05.05.15 по 25.07 в связи с различными нарушениями сознания (переставала вступать в контакт, появлялись словесные эмболы, страх смерти, эпизоды возбуждения, агрессии, инверсия сна, дизартрия). При обследовании в период госпитализаций данные, подтверждающих присоединение вторичных заболеваний, не выявлялись. В отделении проводилась инфузионная, противоотечная, противогрибковая, антибактериальная, противосудорожная, ноотропная терапия, по назначению психиатра получала галоперидол и циклодол. АРВТ по прежней схеме беспрерывно.
При МРТ головного мозга (от 05.07.15) картина очаговых и диффузных изменений вещества (в лобных долях интрасубкортикально очаги повышенного МР-сигнала без признаков перифокального отека до 0,4×0,3 см, в гемисферах мозжечка — диффузные зоны повышенного МР-сигнала без признаков перифокального отека).
В настоящее время пациентка наблюдается амбулаторно в КДО СПИД с диагнозом: ВИЧ-инфекция, стадия 4 В, фаза ремиссии на фоне АРВТ: прогрессирующая мультифокальная лейкоэнцефалопатия. В анамнезе клинически проявляющаяся ЦМВИ с поражением нервной системы. Сопутствующий диагноз: энцефалопатия сложного генеза. Психоорганический синдром в связи с ВИЧ-инфекцией.
Продолжает получать АРВТ по прежней схеме (лопинавир/ритонавир, абакавир и ламивудин), карбамазепин (финлепсин). Состояние стабильное, без ухудшений, выраженные когнитивные расстройства не наблюдаются, ограниченно себя обслуживает. Сохраняется вялый парапарез нижних конечностей. В показателях общего и биохимического анализов крови значительных отклонений нет. От 07.06.16: количество лимфоцитов СD4 1115 кл/мкл (26%), РНК ВИЧ в крови не определяется.
Данное клиническое наблюдение подтверждает сложность диагностики ПМЛ, в связи с отсутствием специфической симптоматики и необходимостью подтверждения диагноза дополнительными инструментальными и лабораторными методами, не всегда доступными в повседневной практике.
В связи с отсутствием специфической профилактики и этиотропного лечения ПМЛ, ВИЧ-инфицированным пациентам необходимо своевременное начало АРВТ. Несмотря на неблагоприятный прогноз заболевания, у пациентов, приверженных АРВТ, при иммунологической и вирусологической эффективности лечения возможно замедление развития ПМЛ, стабилизация состояния и сохранение качества жизни пациента.
Неврологические проявления ВИЧ-инфекции (нейроСПИД) — обобщенное клиническое понятие, включающее многообразные первичные и вторичные синдромы и заболевания нервной системы, обусловленные ВИЧ. Проявлениями нейроСПИДа могут выступать менингоэнцефалит, полиневропатия, энцефало- и миелопатия, оппортунистические нейроинфекции, опухоли ЦНС, церебральные сосудистые нарушения и т. п. Диагностируется нейроСПИД при сопоставлении результатов анализов на ВИЧ, данных неврологического осмотра, нейропсихологического тестирования, ликворологических и томографических исследований, ЭФИ нервно-мышечного аппарата. Лечение нейроСПИДа осуществляется в рамках терапии ВИЧ-инфекции с назначением специфической и симптоматической терапии имеющихся неврологических проявлений.
Общие сведения

Причины возникновения нейроСПИДа
Несмотря на общепризнанность нейротропности ВИЧ, конкретные патогенетические механизмы его воздействия на нервную систему (НС) до конца не ясны. Предполагается, что нейроСПИД обусловлен как прямым, так опосредованным воздействием вируса на НС. Прямое влияние связывают с тропностью ВИЧ к CD4-рецепторам, которые имеются не только в мембране лимфоцитов, но и в глиальных клетках мозговой ткани.
Опосредованное воздействие ВИЧ реализуется несколькими путями. Во-первых, это развитие оппортунистических инфекций и опухолевых процессов за счет резкого снижения иммунного статуса организма. Во-вторых, предполагают наличие аутоиммунных механизмов (например, в развитии асептического менингита и полиневропатии при нейроСПИДе), связанных с синтезом антител к нервным клеткам, имеющим встроенный ВИЧ-антиген. Существует также гипотеза о нейротоксическом действии продуцируемых ВИЧ химических веществ. Кроме того, развитие нейроСПИДа возможно вследствие повреждения эндотелия мозговых сосудов провоспалительными цитокинами, приводящего к расстройству микроциркуляции и гипоксии, обуславливающей гибель нейронов.
Следует отметить, что отсутствие полной ясности в этиопатогенезе ВИЧ-инфекции и нейроСПИДа в частности, наличие существенного количества ложноположительных реакций на ВИЧ при его лабораторной диагностике, а также сложности с выделением вируса привели к появлению среди медиков и специалистов в области иммунологии лиц, считающих неправомочным само понятие ВИЧ-инфекция. При этом сторонники ВИЧ-отрицания признают существование синдрома иммунодефицита как такового, но опасаются, что с введением понятий ВИЧ-инфекция и нейроСПИД под эти диагнозы массово попадают пациенты с различными другими заболеваниями.
Классификация нейроСПИДа
В соответствии с прямым или опосредованным воздействием ВИЧ на нервную систему принято различать первичный и вторичный нейроСПИД. К базовым клиническим формам, которые включает первичный нейроСПИД, относят: острый асептический менингит, ВИЧ-энцефалопатию (СПИД-деменцию), ВИЧ-миелопатию (вакуолярную миелопатию), васкулярный нейроСПИД, поражения периферической НС (дистальная симметричная невропатия, синдром Гийена-Барре, множественная мононевропатия, хроническая воспалительная демиелинизирующая полинейропатия, синдром конского хвоста), поражение мышц (миопатии).
Вторичный нейроСПИД включает оппортунистические нейроинфекции и опухоли. Первые отличаются большим многообразием: церебральный токсоплазмоз, криптококковый менингит, герпесвирусная нейроинфекция (опоясывающий герпес, цитомегаловирусный и герпесвирусный энцефалиты, цитомегаловирусная полирадикулопатия, герпесвирусный миелит и ганглионевриты), прогрессирующая мультифокальная лейкоэнцефалопатия, туберкулезные поражения НС, нейросифилис. Наиболее часто встречающимися опухолями центральной НС при нейроСПИДе являются: первичная лимфома головного мозга, лимфома Беркитта, глионейробластома, диссеминированная саркома Капоши.
Симптомы нейроСПИДа
Первичный нейроСПИД зачастую имеет бессимптомное субклиническое течение. В 10-20% случаев неврологические симптомы дебютируют в первые 2-6 недель от заражения ВИЧ (период сероконверсии). В этот период на фоне фебрилитета, лимфаденопатии и кожных высыпаний у части пациентов манифестируют признаки асептического менингита и острой радикулоневропатии. Другие клинические формы первичного нейроСПИДа (ВИЧ-энцефалопатия, ВИЧ-миелопатия) возникают преимущественно в развернутой стадии ВИЧ-инфекции на фоне системных проявлений и выраженной иммуносупрессии. Вторичный нейроСПИД развивается в фазе симптомной хронической ВИЧ-инфекции (стадия вторичных заболеваний), которая наступает в период от 2 до 15 лет с момента первых клинических проявлений. Отдельные неврологические симптомы (головная боль, полиневропатия, нарушения сна, астения, депрессия, миопатия) могут быть вызваны токсичной антиретровирусной терапией.
Острая радикулоневропатия связана с острой воспалительной демиелинизацией корешков спинномозговых и черепных нервов. Характерны вялый тетрапарез, полиневритический тип нарушений чувствительности, корешковый синдром, поражение лицевого (реже глазодвигательного) нервов, бульбарные расстройства. Фаза нарастания симптомов может длиться от нескольких дней до месяца, затем после 2-4 недель стабильного состояния начинается регресс симптоматики. У 70% пациентов с этой формой нейроСПИДа отмечается полное восстановление, у 15% - выраженные остаточные парезы.
ВИЧ-энцефалопатия является самым частым проявлением первичного нейроСПИДа. Включает когнитивные, поведенческие и двигательные расстройства. Последние бывают представлены мозжечковой атаксией, тремором, пирамидной недостаточностью, вторичным паркинсонизмом, гиперкинезами. Отдельные симптомы и умеренный когнитивный дефицит отмечаются примерно у 75% пациентов со СПИДом. У 3-5% больных энцефалопатия выступает начальным синдромом нейроСПИДа. Морфологическим субстратом является мультифокальный гигантоклеточный энцефалит с поражением преимущественно лобных и височных долей, подкорковых структур, моста и мозжечка.
ВИЧ-миелопатия проявляется нижним спастическим парапарезом и тазовыми расстройствами. Отличается медленным течением и вариативностью тяжести клинических симптомов от легкого пареза до грубой плегии с недержанием мочи и кала. Это проявление нейроСПИДа отмечается у 20% пациентов с ВИЧ. Морфологически выявляется вакуолизация белого спинномозгового вещества, наиболее выраженная в грудных сегментах. Однако на МРТ позвоночника изменения зачастую не фиксируются.
Васкулярный нейроСПИД обусловлен васкулитом церебральных сосудов и зачастую приводит к развитию ишемического инсульта, отличительной чертой которого является волнообразное течение и частая трансформация в геморрагический инсульт. Характерны предшествующие инсульту ТИА, а также повторные инсульты, вследствие мультифокального поражения сосудов.
Диагностика нейроСПИДа
Учитывая частую встречаемость нейроСПИДа, консультация невролога рекомендована всем больным ВИЧ-инфекцией. В связи с тем, что первыми симптомами ВИЧ-энцефалопатии зачастую выступают когнитивные нарушения, исследование неврологического статуса целесообразно дополнять нейропсихологическим обследованием. Среди практических неврологов должна существовать определенная настороженность в отношении впервые обратившихся пациентов из групп риска, поскольку неврологические проявления у них могут являться симптомами первичного нейроСПИДа. В таких случаях следует обращать внимание на наличие у больного признаков иммуносупрессии и системных симптомов (снижения массы тела, лимфаденопатии, выпадения волос и т. п.).
Наряду с обязательными в диагностике ВИЧ-инфекции исследованиями крови путем ИФА, иммуноблоттинга и определения вирусной нагрузки при помощи ПЦР, в диагностике нейроСПИДа широко используются электрофизиологические, томографические и ликворологические методы. При необходимости проводятся консультации психиатра, нейрохирурга и др. специалистов. Диагностика и анализ результатов лечения поражений периферической НС при нейроСПИДе осуществляются преимущественно с помощью ЭФИ нервно-мышечной системы (ЭМГ, ЭНМГ, исследование ВП).
С целью диагностики поражений центральной НС при нейроСПИДе, для анализа их течения и эффективности проводимой терапии широко используются методы компьютерной томографии и магнитно-резонансной томографии. КТ головного мозга особенно информативна в диагностике вторичных объемных процессов церебральной локализации. МРТ головного мозга более эффективно визуализирует диффузные и мелкоочаговые изменения (участки атрофии и демиелинизации), расположенные в глубинных отделах мозга патологические очаги. Однако результаты аутопсии показывают, что современные методы нейровизуализации способны отображать не все морфологические изменения, происходящие в мозговой ткани при нейроСПИДе.
Немаловажное значение в диагностике нейроСПИДа имеет исследование цереброспинальной жидкости, полученной при люмбальной пункции. У серопозитивных пациентов даже при отсутствии неврологической симптоматики в ликворе зачастую наблюдается умеренный лимфоцитоз, повышение уровня белка и снижение концентрации глюкозы. При наличии неврологических проявлении эти изменения, наряду со снижением уровня CD4-лимфоцитов, говорят о возможном развитии нейроСПИДа. Иммунологические исследования ликвора, как правило, выявляют повышенное содержание IgG.
Лечение нейроСПИДа
Основу терапии и профилактики развития нейроСПИДа составляет лечение ВИЧ-инфекции. Эффективная антиретровирусная терапия (АРТ) фармпрепаратами, способными проходить через ГЭБ, позволяет блокировать репликацию ВИЧ, остановить нарастание иммунодефицита и таким образом уменьшить тяжесть клинических проявлений нейроСПИДа, снизить риск возникновения оппортунистических нейроинфекций и повысить эффективность их терапии. К наиболее апробированным средствам, применяемым при нейроСПИДе, относятся зидовудин, ставудин, абакавир. Учитывая токсичность большинства антиретровирусных препаратов, АРТ назначается по индивидуально подобранной схеме только при наличии показаний и с согласия пациента.
Параллельно с АРТ осуществляется специфическая и симптоматическая терапия возникшей клинической формы нейроСПИДа. Так, при ВИЧ-энцефалопатии применяют холина альфосцерат и мягкие ноотропы (мебикар, цитиколин, пирацетам, фенибут), при инсульте — антикоагулянты и пентоксифиллин, при полиневропатии — цитиколин, комбинированные препараты витаминов группы В, при острых психических нарушениях — антипсихотические средства (клозапин). При поражениях периферической НС отмечена эффективность плазмафереза. В лечении миопатий используют плазмаферез и кортикостероидную терапию.
При оппортунистических нейроинфекциях применяют этиотропные препараты: при криптококовых менингитах — фторцитозин с амфотерицином, токсоплазменных энцефалитах — кларитромицин, азитромицин, спирамицин, при герпетических поражениях — ацикловир, валацикловир, ганцикловир, абакавир, саквинавир. Лечение опухолей, возникающих как проявление вторичного нейроСПИДа, может потребовать хирургического вмешательства. Вопрос о необходимости операции рассматривается совместно с нейрохирургом.
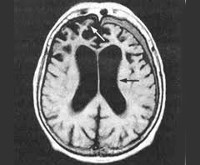
ВИЧ-деменция – стойкое прогрессирующее снижение интеллектуальных функций, развивающееся на фоне ВИЧ-инфекции. Проявляется триадой синдромов: интеллектуально-мнестическими нарушениями, изменениями поведенческих реакций, двигательными расстройствами. К основным симптомам относятся снижение динамики и целенаправленности познавательной деятельности, забывчивость, трудности концентрации внимания и абстрагирования. Диагностика включает беседу, неврологический осмотр, лабораторное, инструментальное и патопсихологическое обследование. Проводится противовирусная и симптоматическая медикаментозная терапия.
Общие сведения

Причины ВИЧ-деменции
ВИЧ-деменция – результат активности вируса иммунодефицита, JC вируса, вызывающего прогрессирующую мультифокальную лейкоэнцефалопатию, и некоторых других возбудителей, поражающих нервную систему при значительной иммуносупрессии. Точные причины энцефалопатии ВИЧ-инфицированных пациентов не выявлены, но определены факторы риска:
- Возраст. Деменция часто формируется у младенцев, рожденных от инфицированных матерей и перенесших интенсивную медикаментозную терапию. Другим возрастным пиком является пожилой и старческий период – после 55-60 лет вероятность слабоумия возрастает ежегодно.
- Отсутствие лечения. Пациенты, не получающие адекватную противовирусную терапию, наиболее подвержены энцефалопатии. Группу риска составляют жители стран с низким уровнем медицинской помощи и люди, добровольно отказывающиеся от своевременной диагностики и лечения инфекции ВИЧ.
- Токсическое поражение ЦНС. Слабоумие чаще развивается при наркотической и алкогольной зависимости. Осложнение возникает в результате поражения ЦНС токсинами.
Патогенез
ВИЧ обладает лимфо- и нейротропностью – поражает лимфоциты крови, ответственные за активность иммунной системы, а также определенные клетки нервной системы. Неврологическая симптоматика является наиболее ранней в клинической картине у 25% больных. При деменции определяется поврежденность астроцитов, эндотелиальных клеток сосудистых сплетений оболочек мозга и эпендимы желудочков. Наиболее отчетливые морфологические изменения обнаруживаются в субкортикальных структурах – белом веществе, подкорковых ядрах, зрительном бугре, стволе и в спинном мозге. Кора сохраняется относительно нетронутой. Вирусное поражение приводит к васкулиту головного и спинного мозга, воспалению мезенхимы нервной ткани, вторичной демиелинизации. Формируется картина рассеянного склероза, вакуольной миелопатии – возникает триада синдромов, включающая дефицит памяти и интеллекта, изменения поведения, двигательные расстройства.
Классификация
Классификация используется с целью определения стадии болезни, уточнения тактики лечения и составления прогноза. Основанием для различения видов ВИЧ-деменции является выраженность интеллектуальных, двигательных и поведенческих расстройств, способность пациента к выполнению ежедневных ритуалов, самообслуживанию. Выделяют шесть стадий болезни:
- Нулевая. Психические и двигательные функции в норме. Деменция отсутствует.
- Субклиническая. Отмечаются легкие когнитивные нарушения, замедленность двигательных актов. Больной может испытывать трудности при выполнении профессиональных задач. С повседневными бытовыми делами справляется самостоятельно.
- Легкая. Развивается замедленность психических функций, снижается концентрация и устойчивость внимания, с трудом запоминается объемный и слабоструктурированный материал, нарушается координация движений. Большинство бытовых навыков остаются сохранными, становятся недоступными действия, требующие точности движений, применения физической силы, высокого уровня интеллекта.
- Средней тяжести. Обнаруживается умеренный интеллектуально-мнестический дефект – больной не усваивает новый материал, неспособен самостоятельно действовать в незнакомой обстановке. Самостоятельно передвигается, справляется с простыми ежедневными ритуалами.
- Тяжелая. Формируются выраженные нарушения мышления, памяти, речи, движений. Затруднено общение с окружающими, ориентация в пространстве, координация. Ходьба возможна при помощи ходунков, поддержки со стороны. Пациент нуждается в уходе.
- Финальная. Определяются глубокие нарушения интеллекта, практически полное отсутствие двигательной активности. Больной не может принимать пищу, контролировать физиологические отправления, впадает в вегетативную кому.
Симптомы ВИЧ-деменции
В симптоматике доминируют признаки, характерные для субкортикальных деменций – снижение, колебания динамики психической деятельности и нарушения памяти. Пациенты становятся забывчивыми, медлительными, плохо концентрируются на выполнении сложных задач. Проявления нарастающего интеллектуально-мнестического дефицита на ранних стадиях замечаются у людей, занятых умственным трудом. У пожилых людей, детей раннего возраста когнитивное снижение часто выявляется на средних стадиях болезни.
В эмоциональной сфере нарастают симптомы апатии, депрессии. Больные становятся медлительными, социально отгороженными. Иногда развиваются атипичные аффективные реакции – психозы, истероподобные припадки. Поведение характеризуется стремлением к изоляции либо наоборот чрезмерной расторможенностью и дурашливостью. В двигательной сфере нарушения прогрессируют от мышечной слабости и снижения скорости движений в конечностях к частичному и полному параличу. У больных возникает тремор, походка становится неустойчивой и шаткой, движения дискоординированные, неуклюжие. Речь обедняется как результат интеллектуального снижения и дизартрии – нарушений смыслового и моторного компонента.
Осложнения
Отсутствие своевременного лечения ВИЧ-инфекции сопровождается быстрым нарастанием когнитивного дефицита и двигательных расстройств. На заключительной стадии развивается вегетативное состояние – частичный или полный паралич, неспособность есть, разговаривать, контролировать деятельность мочевого пузыря и кишечника. Исход прогрессирующей ВИЧ-энцефалопатии – кома, смерть. Выраженный иммунодефицит быстро завершается летальным исходом, деменция зачастую не успевает перейти в тяжелую и финальную стадии. При медленном течении болезни к стандартным проявлениям слабоумия присоединяются симптомы психоза – бред, галлюцинации, моторное возбуждение.
Диагностика
При диагностике ВИЧ-деменции врачи работают в нескольких направлениях: устанавливают наличие вируса (если диагноз отсутствует), определяют факт инфицирования ЦНС, чтобы исключить другие причины слабоумия, оценивают выраженность когнитивных, поведенческих, двигательных нарушений. Обследования проводятся врачом-инфекционистом, невропатологом, психиатром, клиническим психологом. Используются следующие методы:
- Беседа. Каждый специалист проводит опрос пациента и/или родственников, акцентируя внимание на специфических симптомах. Характерны жалобы на забывчивость, медлительность, трудности при письме, чтении, выполнении бытовых задач, апатию, социальную отгороженность.
- Осмотр. Неврологическое обследование направлено на выявление двигательных дисфункций. Обнаруживается тремор, нарушения координации и глазодвигательных функций, гипертонус мышц, генерализованная гиперрефлексия. Поздние стадии сопровождаются наличием очаговых симптомов, гиперкинезов.
- Лабораторные тесты. Наличие ВИЧ определяется по результатам иммуноферментных анализов и ПЦР. Инфицирование ЦНС подтверждается данными анализа спинномозговой жидкости, забор которой выполняется методом люмбальной пункции.
- Инструментальные исследования. Наиболее информативным методом, позволяющим определить факт поражения и структурные изменения ЦНС, является МРТ головного мозга (дополнительно назначается КТ и ПЭТ). Для поздних этапов болезни характерна диффузная гиперинтенсивность белого вещества, атрофия мозга, расширение желудочковой системы.
- Психодиагностика. Проводится патопсихологическое исследование когнитивной сферы. По итогам проб устанавливается снижение и неустойчивость динамики психомоторных процессов, недостаточность механической и смысловой памяти, функций активного внимания, преобладание конкретно-ситуационного типа мышления, недостаточная способность к абстрагированию.
Лечение ВИЧ-деменции
Терапия деменции основана на применении противовирусных препаратов с доказанной высокой эффективностью. По данным последних исследований, наиболее оправдано применение зидовудина – лекарственные средства на его основе препятствуют прогрессированию инфекционного процесса, тормозят развитие интеллектуального дефицита, а при раннем начале лечения отсрочивают развитие СПИД-энцефалопатии на период от 6 до 12 месяцев. Ограничением данного препарата является возникновение плохо переносимых побочных эффектов у ряда больных.
Относительное восстановление памяти и внимания происходит при последовательном или одновременном приеме зидовудина и диданозина. Положительный эффект становится заметен после 10-12 недель приема лекарств. К другим медикаментам с аналогичным действием относятся ламивудин, ставудин, залцитабин. Параллельно с противовирусной терапией проводится симптоматическое лечение деменции. Используются препараты, улучшающие мозговые функции (антагонисты NMDA-рецепторов), антидепрессанты, атипичные нейролептики.
Прогноз и профилактика
У ВИЧ-инфицированных пациентов с признаками деменции, не получающих лечения, прогноз неблагоприятный – высока вероятность летального исхода в течение года. При адекватной регулярной терапии процессы снижения познавательных функций и развития моторных нарушений замедляются, состояние больного стабилизируется, а в отдельных случаях наблюдается улучшение (регресс симптоматики). Снизить вероятность инфицирования клеток ЦНС при ВИЧ можно с помощью своевременной противовирусной терапии. Также существуют меры, позволяющие замедлить развитие деменции. Необходимо сохранять интеллектуальную, физическую и социальную активность. В режим дня нужно включить регулярные физические нагрузки, соответствующие уровню подготовленности, занятия творчеством, чтение научной и классической литературы с последующим обсуждением прочитанного.
Однако в исследовании, опубликованном в онлайн-журнале PLOS Pathogens, говорится, что вирус может вести себя коварнее, чем ожидалось. Исследователи из Йельской школы медицины и Университета Северной Каролины обнаружили, что вирус может поражать мозг человека уже через четыре месяца после инфицирования. В свою очередь, в мозге вирус генетически видоизменяется и начинает отличаться от вируса, циркулирующего в крови. Это значит, что препараты, принимаемые человеком для лечения ВИЧ-инфекции, могут хуже работать в центральной нервной системе, чем в других органах. При неадекватном лечении ВИЧ может привести к возникновению неврологической симптоматики, вызвать отек мозга и различные формы слабоумия.

по теме

Профилактика
ВИЧ и старение
Исследование проходило в Сан-Франциско при участии 72 испытуемых: почти все из них — взрослые мужчины, у которых ранее диагностировали ВИЧ. У этих людей взяли образцы крови и спинномозговой жидкости. Образцы показали, что ВИЧ поразил ЦНС в 70 % случаев в течение первых нескольких месяцев после инфицирования. На второй год болезни вирус начал воспроизводиться в ЦНС независимо от количества вируса в крови в 25 % случаев. Этот процесс, когда вирус локализуется в определенных частях организма и начинает там размножаться, называется компартментализацией. Компартментализацию ВИЧ в ЦНС сложно изучить, потому что исследователи не могут провести биопсию мозга у живых людей, и приходится добираться до вируса с помощью люмбальной пункции и анализа спинномозговой жидкости.
Несмотря на то, что такие симптомы стали встречаться реже в связи с улучшением качества лекарств, они все же остаются превалирующими — исследование 2010 года показало, что 52 % людей, живущих с ВИЧ, страдают нейрокогнитивными расстройствами.
Совместное исследование Йельской школы медицины и Университета Северной Каролины проводилось среди людей, еще не начавших принимать антиретровирусную терапию. (Согласно данным Всемирной организации здравоохранения, в 2013 году антиретровирусную терапию получали около 35 — 40 % ВИЧ-положительных). Тем не менее оно доказывает, что, когда люди, живущие с ВИЧ, не принимают терапию (из-за незнания своего статуса или если это осознанный выбор), центральная нервная система становится дополнительным резервуаром для размножения ВИЧ, что может привести к неврологическим повреждениям.
по теме
Лечение
Новые шаги в разработке вакцины против ВИЧ
Эта статистика и человеческие страдания, стоящие за ней, — главная причина, почему некоммерческие организации призывают к повышению информированности о ВИЧ и к его профилактике гораздо настойчивее, чем тридцать лет назад, когда о вирусе впервые стало известно.
Читайте также:

