Стадии развития инфекционного процесса иммунология
Обновлено: 22.04.2024
Для развития инфекционного заболевания необходимо наличие ряда факторов.
Пути передачи возбудителей инфекционных заболеваний
Существуют различные способы передачи патогенных микроорганизмов. В некоторых случаях эпидемические штаммы хорошо переносят неблагоприятные условия и способны к быстрому распространению.
Большинство патогенных микроорганизмов приспосабливаются к тем или иным способам передачи. Следует отметить, что распространение возбудителей, вызывающих поражение дыхательной системы, облегчается при помощи кашля, который они вызывают. В то же время рвота и диарея, возникающие при заболеваниях, передающихся посредством фекально-орального механизма, способствуют попаданию возбудителей (находящихся в большом количестве в желудочно-кишечном тракте) в окружающую среду.
Внедрение возбудителя инфекции в организм хозяина
Для роста и размножения микроорганизмы должны проникнуть в ткани хозяина, а потому обладают широким спектром методов и механизмов прикрепления. Выбор органов-мишеней зависит от того, с какими рецепторами может взаимодействовать тот или иной возбудитель. Так, Neisseria gonorrhoeae прикрепляется к слизистой оболочке половых органов при помощи фимбрий, а вирус гриппа взаимодействует с клетками хозяина посредством гемагглютинина.
Эти свойства учитывают при определении сродства к рецепторам и исследовании патогенности видоспецифичных (определённые штаммы поражают определённые организмы) и межвидовых патогенов.
Некоторые бактерии обладают специальными механизмами, позволяющими им достичь эпителия млекопитающих. Например, для достижения энтероцитов Vibrio cholerae вырабатывает муциназу. Взаимодействие Н. pylori с сиалированными белками слизистой оболочки желудка зависит от степени сиалирования поверхностных структур возбудителя.
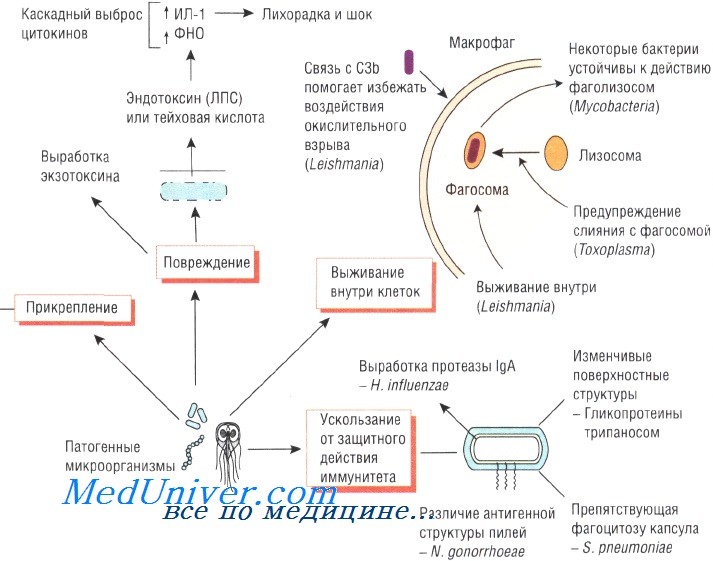
Патогенез инфекционного заболевания
Giardia lamblia прикрепляется к слизистой оболочке тощей кишки при помощи специальной присоски. Эритроциты, поражённые Plasmodium falciparum, продуцируют белок, стимулирующий адгезию к сосудам мозга, что приводит к развитию церебральной формы малярии.
Некоторые бактерии образуют полисахаридную биоплёнку, облегчающую микробное заселение искусственных протезов и имплантов (например, катетеров), постоянно находящихся в организме. Кроме того, некоторые штаммы стафилококков имеют гены, стимулирующие их прикрепление к пластиковым поверхностям и биомолекулам, покрывающим внутрисосудистые устройства.
При продолжительном повреждении тканей различные штаммы S. aureus могут связываться с некоторыми молекулами организма хозяина (фибронектин, вибронектин и коллаген). Различные штаммы Escherichia coli используют фимбрий, или пили, для прикрепления к маннозе или групповым антигенам крови и, соответственно, они вызывают инфекционные заболевания желудочно-кишечного тракта или мочевыводящих путей. ВИЧ связывается с CD4 и некоторыми другими антигенами.
Таким образом, каждый штамм обладает определёнными генами, обусловливающими его способность к внедрению в организм хозяина.
Инвазия возбудителя инфекционного заболевания
Существует множество механизмов, при помощи которых микроорганизмы преодолевают слизистые оболочки и различные типы клеточных мембран. После этого они должны закрепиться в организме хозяина и начать интенсивно размножаться.
Некоторые бактерии, например рода Helicobacter и Neisseria, продуцируют IgA-протеазу, разрушающую IgA. Таким образом, эти возбудители нейтрализуют одну из важнейших защитных систем слизистой оболочки организма.
Подвижность возбудителя инфекционного заболевания
Способность микроорганизмов передвигаться в поисках новых источников питания или в ответ на хемотаксические сигналы приводит к заметному усилению их патогенности. Например, штаммы Vibrio cholerae, обладающие жгутиками, намного более вирулентны, нежели неподвижные штаммы.
Устойчивость возбудителя инфекции к защитным механизмам иммунной системы
Для выживания в организме хозяина возбудителям необходимо противостоять защитным механизмам иммунной системы. Бактерии, поражающие дыхательную систему, продуцируют IgA-протеазу, разрушающую иммуноглобулины. Staphylococcus aureus секретирует протеин А, связывающий иммуноглобулины и препятствующий опсонизации и активации системы комплемента.
Один из важнейших механизмов противостояния иммунной системе — устойчивость к фагоцитозу. Полисахаридная капсула препятствует захвату Streptococcus pneumoniae полиморфноядерными нейтрофилами. Кроме того, некоторые микроорганизмы
Липополисахариды грамотрицательных бактерий обусловливают их устойчивость к действию комплемента, а Trypanosoma способна изменять свои поверхностные антигены во избежание их взаимодействия с антителами.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Инфекционные болезни характеризуются специфичностью, контагиозностью и цикличностью.
Специфичность инфекции
Каждую инфекционную болезнь вызывает конкретный возбудитель. Однако известны инфекции (например, гнойно-воспалительные процессы), вызываемые различными микробами. С другой стороны, один возбудитель (например, стрептококк) способен вызывать различные поражения.
Контагиозность инфекционного заболевания. Индекс контагиозности инфекции.
Контагиозность (заразительность) определяет способность возбудителя передаваться от одного лица к другому и скорость его распространения в восприимчивой популяции. Для количественной оценки контагиозности предложен индекс контагиозности — процент переболевших лиц в популяции за определённый период (например, заболеваемость гриппом в определённом городе за 1 год).
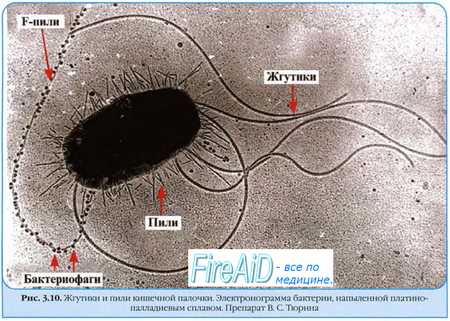
Цикличность инфекционного заболевания
Развитие конкретного инфекционного заболевания ограничено во времени, сопровождается цикличностью процесса и сменой клинических периодов.
Стадии инфекционной болезни. Периоды инфекционной болезни.
Инкубационный период [от лат. incubatio, лежать, спать где-либо]. Обычно между проникновением инфекционного агента в организм и проявлением клинических признаков существует определённый для каждой болезни промежуток времени — инкубационный период, характерный только для экзогенных инфекций. В этот период возбудитель размножается, происходит накопление как возбудителя, так и выделяемых им токсинов до определённой пороговой величины, за которой организм начинает отвечать клинически выраженными реакциями. Продолжительность инкубационного периода может варьировать от часов и суток до нескольких лет.
Период развития болезни. На этой фазе и проявляются черты индивидуальности болезни либо общие для многих инфекционных процессов признаки — лихорадка, воспалительные изменения и др. Б клинически выраженной фазе можно выделить стадии нарастания симптомов (stadium wcrementum), расцвета болезни (stadium acme) и угасания проявлений (stadium decrementum).
Реконвалесценция [от лат. re-, повторность действия, + convalescentia, выздоровление]. Период выздоровления, или реконвалесценции как конечный период инфекционной болезни может быть быстрым (кризис) или медленным (лизис), а также характеризоваться переходом в хроническое состояние. Б благоприятных случаях клинические проявления обычно исчезают быстрее, чем наступает нормализация морфологических нарушений органов и тканей и полное удаление возбудителя из организма. Выздоровление может быть полным либо сопровождаться развитием осложнений (например, со стороны ЦНС, костно-мышечного аппарата или сердечно-сосудистой системы). Период окончательного удаления инфекционного агента может затягиваться и для некоторых инфекций (например, брюшного тифа) может исчисляться неделями.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Для развития инфекционного заболевания необходимо наличие ряда факторов.
Пути передачи возбудителей инфекционных заболеваний
Существуют различные способы передачи патогенных микроорганизмов. В некоторых случаях эпидемические штаммы хорошо переносят неблагоприятные условия и способны к быстрому распространению.
Большинство патогенных микроорганизмов приспосабливаются к тем или иным способам передачи. Следует отметить, что распространение возбудителей, вызывающих поражение дыхательной системы, облегчается при помощи кашля, который они вызывают. В то же время рвота и диарея, возникающие при заболеваниях, передающихся посредством фекально-орального механизма, способствуют попаданию возбудителей (находящихся в большом количестве в желудочно-кишечном тракте) в окружающую среду.
Внедрение возбудителя инфекции в организм хозяина
Для роста и размножения микроорганизмы должны проникнуть в ткани хозяина, а потому обладают широким спектром методов и механизмов прикрепления. Выбор органов-мишеней зависит от того, с какими рецепторами может взаимодействовать тот или иной возбудитель. Так, Neisseria gonorrhoeae прикрепляется к слизистой оболочке половых органов при помощи фимбрий, а вирус гриппа взаимодействует с клетками хозяина посредством гемагглютинина.
Эти свойства учитывают при определении сродства к рецепторам и исследовании патогенности видоспецифичных (определённые штаммы поражают определённые организмы) и межвидовых патогенов.
Некоторые бактерии обладают специальными механизмами, позволяющими им достичь эпителия млекопитающих. Например, для достижения энтероцитов Vibrio cholerae вырабатывает муциназу. Взаимодействие Н. pylori с сиалированными белками слизистой оболочки желудка зависит от степени сиалирования поверхностных структур возбудителя.

Патогенез инфекционного заболевания
Giardia lamblia прикрепляется к слизистой оболочке тощей кишки при помощи специальной присоски. Эритроциты, поражённые Plasmodium falciparum, продуцируют белок, стимулирующий адгезию к сосудам мозга, что приводит к развитию церебральной формы малярии.
Некоторые бактерии образуют полисахаридную биоплёнку, облегчающую микробное заселение искусственных протезов и имплантов (например, катетеров), постоянно находящихся в организме. Кроме того, некоторые штаммы стафилококков имеют гены, стимулирующие их прикрепление к пластиковым поверхностям и биомолекулам, покрывающим внутрисосудистые устройства.
При продолжительном повреждении тканей различные штаммы S. aureus могут связываться с некоторыми молекулами организма хозяина (фибронектин, вибронектин и коллаген). Различные штаммы Escherichia coli используют фимбрий, или пили, для прикрепления к маннозе или групповым антигенам крови и, соответственно, они вызывают инфекционные заболевания желудочно-кишечного тракта или мочевыводящих путей. ВИЧ связывается с CD4 и некоторыми другими антигенами.
Таким образом, каждый штамм обладает определёнными генами, обусловливающими его способность к внедрению в организм хозяина.
Инвазия возбудителя инфекционного заболевания
Существует множество механизмов, при помощи которых микроорганизмы преодолевают слизистые оболочки и различные типы клеточных мембран. После этого они должны закрепиться в организме хозяина и начать интенсивно размножаться.
Некоторые бактерии, например рода Helicobacter и Neisseria, продуцируют IgA-протеазу, разрушающую IgA. Таким образом, эти возбудители нейтрализуют одну из важнейших защитных систем слизистой оболочки организма.
Подвижность возбудителя инфекционного заболевания
Способность микроорганизмов передвигаться в поисках новых источников питания или в ответ на хемотаксические сигналы приводит к заметному усилению их патогенности. Например, штаммы Vibrio cholerae, обладающие жгутиками, намного более вирулентны, нежели неподвижные штаммы.
Устойчивость возбудителя инфекции к защитным механизмам иммунной системы
Для выживания в организме хозяина возбудителям необходимо противостоять защитным механизмам иммунной системы. Бактерии, поражающие дыхательную систему, продуцируют IgA-протеазу, разрушающую иммуноглобулины. Staphylococcus aureus секретирует протеин А, связывающий иммуноглобулины и препятствующий опсонизации и активации системы комплемента.
Один из важнейших механизмов противостояния иммунной системе — устойчивость к фагоцитозу. Полисахаридная капсула препятствует захвату Streptococcus pneumoniae полиморфноядерными нейтрофилами. Кроме того, некоторые микроорганизмы
Липополисахариды грамотрицательных бактерий обусловливают их устойчивость к действию комплемента, а Trypanosoma способна изменять свои поверхностные антигены во избежание их взаимодействия с антителами.
Редактор: Искандер Милевски. Дата обновления публикации: 18.3.2021
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
В развитии инфекционного процесса можно выделить несколько стадий.
Проникновение микроба в макроорганизм (син. — заражение, инфицирование), его адаптация в месте входных ворот инфекции, адгезия, т.е. связывание с чувствительными клетками и их колонизация.
Образование ферментов, токсинов и других продуктов в процессе размножения и жизнедеятельности микробов, которые оказывают как местное, так и генерализованное болезнетворное воздействие на ткани и органы, что ведет к нарушению гомеостаза.
В ряде случаев диссеминация (распространение) микробов за пределы первичного очага, что приводит к генерализации инфекции.
Формирование защитной реакции макроорганизма в ответ на патогенное действие микроба, направленной на нейтрализацию микроба и его токсинов, а также восстановление гомеостаза.
Восстановление гомеостаза (т.е. выздоровление) и приобретение макроорганизмом нового качества — иммунитета, т.е. невосприимчивости к микробу.
Формы проявления инфекционного процесса разнообразны. Этот процесс может протекать на молекулярном (субклеточном), клеточном, тканевом, органном и организменном уровне. Инфекционный процесс не всегда проходит все присущие ему стадии и может заканчиваться уже на ранних этапах, например, абортивное течение заболевания у иммунизированных лиц или лиц, ранее переболевших данным заболеванием.
Понятие о патогенности и вирулентности
Для того чтобы вызвать инфекционный процесс, возбудитель должен обладать патогенностью (болезнетворностью). Патогенность (от греч. pathos — страдание, болезнь, genos — рождение) — это видовой многофакторный признак, обозначающий потенциальную способность микроба вызывать инфекционный процесс.
Например, возбудитель коклюша поражает трахею и бронхи, возбудитель холеры паразитирует в тонкой кишке и т.д. Это свойство называется органотропностъю.
Для того чтобы вызвать инфекционный процесс, патогенные микробы должны проникать в организм в определенной критической инфицирующей дозе (патогенной), т.е. в минимальной дозе, которая вызывает стойкую адгезию, колонизацию, проникновение в ткани возбудителя и дальнейшее развитие инфекционного процесса. Для каждого вида микроба имеется своя минимальная инфицирующая доза, т.е. число особей, способных вызвать заболевание. В естественных условиях для возникновения инфекционного процесса патогенные микробы должны проникать через определенные входные ворота инфекции — ткани и органы, через которые микроб попадает в макроорганизм. Например, для возбудителей кишечных инфекций входные ворота — слизистая оболочка желудочно-кишечного тракта (ЖКТ), а для воздушно-капельных инфекций — слизистая оболочка дыхательных путей. Однако есть патогенные микробы, которые в естественных условиях могут проникать через разные входные ворота, т.е. они обладают пантропностъю (поражают многие ткани и органы). К ним относятся возбудители зоонозов (чумы, туляремии и др.).
Патогенность микробов зависит от многих факторов и подвержена большим колебаниям в различных условиях. Для обозначения степени патогенности введено понятие вирулентности.
Вирулентность (от лат. virulentus — ядовитый) — это динамическое индивидуальное свойство (способность) данного штамма микроба вызывать инфекционный процесс, качественная характеристика патогенности или фенотипическое проявление генотипа, свойственное микробу. По этому признаку все штаммы микроба данного вида могут быть подразделены на высоко-, умеренно-, слабо- и авирулентные.
О вирулентности патогенных микробов в лабораторных условиях судят по величине летальной и инфицирующей дозы для экспериментальных животных. При этом необходимо учитывать вид, пол, массу, условия содержания, полноценность питания и способ заражения экспериментальных животных, т.е. те факторы, которые влияют на достоверность и стандартность результатов опытов. Для снижения влияния индивидуальных колебаний резистентности эксперимент проводят на значительном числе животных. Летальная доза (LD) — это наименьшее количество возбудителя или токсина, вызывающее в определенный срок гибель конкретного количества (%) животных, взятых в опыт.
Так, Del (Dosis certe letalis) — гибель 100 % особей, Dim (Dosis letalis minima) — 95 %, LD^ (Letalis dosis— 90 %, LD70 — 70 %, LDS0 — 50 % и т.д. Инфицирующая доза (ID) — минимальное количество микробов, способное вызвать инфекционное заболевание у определенного количества (%) животных, взятых в опыт. Например, ID — это 100 % заболеваемость, IDS0 — 50 % и т.д. В лабораторной практике чаще пользуются показателями LDS0 и Ю50 как обеспечивающими достоверность и стандартность оценки летальной и инфицирующей доз возбудителя.
Под действием физических, химических и биологических факторов вирулентность подвержена фенотипическим и генотипическим изменениям как в сторону ослабления, так и усиления. Снижение вирулентности (аттенуация) может происходить при длительном пассировании культур на питательных средах, через организм мало восприимчивых животных и т.п. Полная утрата вирулентности связана с изменением генотипа Повышение вирулентности наблюдается в процессе пассирования культуры через организм высоковосприимчивых животных, при лизогении, мутациях и рекомбинациях. Примером изменения вирулентности могут служить образование капсул у бактерий при попадании в организм, температурозависимый синтез инвазивных белков у иерсиний и ^/-антигена у Salmonella typhi, образование индуцибельных ферментов и др.
Факторы патогенности микробов
Для существования в макроорганизме микробы должны обладать способностью к адгезии и колонизации, инвазивностью и агрессивностью, оказывать повреждающее воздействие на ткани и органы.
Материальные носители, выполняющие данные функции, называются факторами патогенности. Пусковым моментом инфекционного процесса являются адгезия и колонизация. Этот процесс высокоспецифичен, поскольку происходит в результате комплементарного взаимодействия макромолекул, расположенных на поверхности микроба, с рецепторами эукариотической клетки хозяина. Адгезия обусловливает чувствительность к микробу хозяина и органотропность микробов. Структуры микроба (макромолекулы), ответственные за прилипание, т.е. связывание с клетками хозяина, называются адгезинами. Такими структурами у грамотрицательных бактерий являются фимбрии (пили
или общего типа), а также основные белки наружной мембраны, которые активируют транслокацию микроба внутрь эпителиальной клетки. У грамположительных бактерий адгезины представляют собой белки и тейхоевые кислоты клеточной стенки, а у микоплазм — макромолекулы, входящие в состав выростов цитоплазматической мембраны. Колонизация зависит как от дозы микробов, так и количества рецепторов для них на поверхности клеток макроорганизма. При отсутствии адгезинов или комплементарных рецепторов, инфекционный процесс не развивается.
Под инвазивностъю (от лат. invasio — нападение) понимают способность микробов проникать через кожные покровы и слизистые оболочки во внутреннюю среду организма хозяина и распространяться по его тканям и органам, а под агрессивностью — способность противостоять защитным факторам организма и размножаться в нем. Для преодоления защитных барьеров важное значение имеет продукция ферментов агрессии и инвазии. К ним относятся:
гиалуронидаза — фермент, разрушающий гиалуроновую кислоту — основное межклеточное вещество соединительной, ткани. Это способствует проникновению микробов вглубь тканей организма;
нейраминидаза (сиалидаза) — фермент, расщепляющий ней- раминовую (сиаловую) кислоту, которая входит в состав поверхностных рецепторов клеток слизистых оболочек. Это делает оболочки доступными для взаимодействия с микробами и их токсинами;
фибринолизин — фермент, растворяющий сгусток фибрина, который образуется в процессе воспаления и препятствует проникновению микробов в глубь органов и тканей;
коллагеназа — фермент, разрушающий коллаген мышечных волокон, что ведет к интенсивному расплавлению мышечной ткани;
лецитиназа С — фермент, действующий на лецитин мембран мышечных волокон, эритроцитов и других клеток;
коагулаза — фермент, свертывающий плазму крови;
дезоксирибонуклеаза (ДНКаза) — фермент, деполимеризу- ющий ДНК;
протеазы — ферменты, разрушающие иммуноглобулины и
Расщепляя высокополимерные соединения на низкомолекулярные вещества, ферменты выполняют трофическую функцию, что ведет к истощению макроорганизма. При этом ферменты действуют как местно, так и генерализованно, усиливают действие токсинов (нейраминидаза) или сами действуют как токсины в случае образования токсических веществ (например,
уреаза расщепляет мочевину с образованием аммиака и углекислоты; декарбоксилазы аминокислот и т.д.). Определенную роль в преодолении межклеточных барьеров играют жгутики бактерий, способствующие достижению места их обитания и препятствующие фагоцитозу, а также поверхностные антигены клеток, которые активируют трансмембранный фагоцитоз.
Размножаясь в организме, микробы должны противостоять фагоцитозу.
Находясь внутри клетки, микробы не подвергаются действию антител, лизоцима, комплемента и других факторов защиты (см. главу 9). В то же время клетки, фагоцитирующие микробы, могут мигрировать, способствуя распространению микробов по организму. К веществам с антифагоцитарной активностью относятся капсульные полисахариды и полипетиды микробов. К- и Vi- антигены, входящие в состав микрокапсул энтеробактерий; корд- фактор возбудителей туберкулеза; слизистое вещество Pseudomonas aeruginosa, М-протеин р-гемолитических стрептококков группы А, А-протеин стафилококков и другие структуры микробных клеток. Все они так или иначе создают механический барьер, экранирующий области связывания микробов с рецепторами фагоцитирующих клеток, т.е. препятствующий фагоцитозу. Ан- тифагоцитарные свойства микробов обусловлены также образованием ими веществ, подавляющих хемотаксис фагоцитов; способных противостоять внутриклеточному перевариванию; препятствующих слиянию л изосомы с фагосомой; способных вызывать лизис фагоцитирующих клеток (лейкоцидины); образовывать каталазу и супероксиддисмутазу, которые препятствуют действию перекисных радикалов фагоцитирующих клеток и т.д.
Наиболее важную роль в развитии инфекционного процесса играют токсины (от греч. toxikon — яд). По физико-химической структуре и биологическим свойствам бактериальные токсины делятся на экзотоксины и эндотоксины.
Экзотоксины — белки, представляющие бифункциональную структуру, так как они имеют транспортную группу, которая взаимодействует со специфическим рецептором клеток, и токсическую группу (активатор), которая проникает внутрь клетки и блокирует жизненно важные метаболические процессы.
Механизм действия белковых токсинов сводится к повышению проницаемости мембраны эритроцитов, лейкоцитов и других клеток (мембранотоксины) или к блокаде синтеза белка и других биохимических процессов в клетках (цито-, энтеро- и нейротоксины) либо нарушению взаимосвязи и взаимодействия между клетками.
Заболевания, при которых микроб остается в месте входных ворот инфекции, а основные клинические проявления которых связаны с действием белкового бактериального токсина, получили название токсинемических инфекций (дифтерия, столбняк, ботулизм, анаэробная газовая инфекция). Для профилактики и лечения токсинемических инфекций применяют анатоксины и антитоксические сыворотки.
Эндотоксины представляют белковолипополисахаридный комплекс клеточной стенки грамотрицательных бактерий, который выделяется в окружающую среду при лизисе бактерий.
Генетическая регуляция синтеза факторов патогенности
Патогенность бактерий контролируется группой генов, ответственных за образование поверхностных структур бактериальных клеток (фимбрий, капсул, клеточной стенки) или за синтез токсинов, а также ферментов, способствующих жизнедеятельности этих бактерий. Эти наследственные детерминанты локализованы как в хромосоме, так и плазмидах. Модификации генотипа, контролирующего патогенность, проявляются в фенотипическом изменении вирулентности микробов, которая восстанавливается при их пассировании на питательных средах или через организм восприимчивого животного. Стойкие изменения вирулентности возникают в случае мутаций или рекомбинаций и связаны с изменениями генотипа микроба.
Реорганизация генов, кодирующих синтез факторов патогенности, в ходе инфекционного процесса происходит на молекулярном уровне, но на популяционном уровне создаются условия для естественного отбора штаммов с повышенной вирулентностью — эпидемических штаммов. Детерминанты факторов патогенности необходимо учитывать при изучении патогенеза инфекционных заболеваний, при разработке новых способов диагностики, для лечения и профилактики инфекционных заболеваний.
8 2.3. Факторы патогенности вирусов
В отличие от бактерий, простейших и грибов, которые обладают сходными факторами патогенности, патогенность вирусов — облигатных внутриклеточных паразитов — на генетическом уровне обеспечивается их способностью проникать внутрь восприимчивых клеток, нарушать обмен веществ в клетке, оказывать цитопатогенное действие, изменять клеточные мембраны и индуцировать иммунную реакцию против инфицированных вирусом клеток (см. раздел 3.3). Инфекционность вирусов связана с их нуклеиновой кислотой (ДНК или РНК) и может проявляться после проникновения последней в клетку хозяина.
Инфекционные болезни характеризуются специфичностью, контагиозностью и цикличностью.
Специфичность инфекции
Каждую инфекционную болезнь вызывает конкретный возбудитель. Однако известны инфекции (например, гнойно-воспалительные процессы), вызываемые различными микробами. С другой стороны, один возбудитель (например, стрептококк) способен вызывать различные поражения.
Контагиозность инфекционного заболевания. Индекс контагиозности инфекции.
Контагиозность (заразительность) определяет способность возбудителя передаваться от одного лица к другому и скорость его распространения в восприимчивой популяции. Для количественной оценки контагиозности предложен индекс контагиозности — процент переболевших лиц в популяции за определённый период (например, заболеваемость гриппом в определённом городе за 1 год).

Цикличность инфекционного заболевания
Развитие конкретного инфекционного заболевания ограничено во времени, сопровождается цикличностью процесса и сменой клинических периодов.
Стадии инфекционной болезни. Периоды инфекционной болезни.
Инкубационный период [от лат. incubatio, лежать, спать где-либо]. Обычно между проникновением инфекционного агента в организм и проявлением клинических признаков существует определённый для каждой болезни промежуток времени — инкубационный период, характерный только для экзогенных инфекций. В этот период возбудитель размножается, происходит накопление как возбудителя, так и выделяемых им токсинов до определённой пороговой величины, за которой организм начинает отвечать клинически выраженными реакциями. Продолжительность инкубационного периода может варьировать от часов и суток до нескольких лет.

Период развития болезни. На этой фазе и проявляются черты индивидуальности болезни либо общие для многих инфекционных процессов признаки — лихорадка, воспалительные изменения и др. Б клинически выраженной фазе можно выделить стадии нарастания симптомов (stadium wcrementum), расцвета болезни (stadium acme) и угасания проявлений (stadium decrementum).
Реконвалесценция [от лат. re-, повторность действия, + convalescentia, выздоровление]. Период выздоровления, или реконвалесценции как конечный период инфекционной болезни может быть быстрым (кризис) или медленным (лизис), а также характеризоваться переходом в хроническое состояние. Б благоприятных случаях клинические проявления обычно исчезают быстрее, чем наступает нормализация морфологических нарушений органов и тканей и полное удаление возбудителя из организма. Выздоровление может быть полным либо сопровождаться развитием осложнений (например, со стороны ЦНС, костно-мышечного аппарата или сердечно-сосудистой системы). Период окончательного удаления инфекционного агента может затягиваться и для некоторых инфекций (например, брюшного тифа) может исчисляться неделями.
Информация на сайте подлежит консультации лечащим врачом и не заменяет очной консультации с ним.
См. подробнее в пользовательском соглашении.
Читайте также:

