Стадия миграции у гельминтов
Обновлено: 19.04.2024
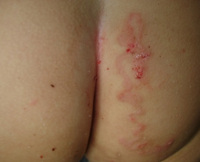
Мигрирующая личинка – это группа инфекционных кожных заболеваний, связанных с поражением личинками гельминтов. Основным симптомом является дерматит в виде нитевидных линий, образуемых при передвижении возбудителя в верхних слоях дермы. Сыпь сопровождается сильным зудом, чаще всего поражаются нижние конечности. Типичные симптомы позволяют поставить диагноз по клинической картине и анамнезу, возможно обнаружение личинок в коже при биопсии. Лечение этиотропное (антигельминтные препараты) и симптоматическое; допускается местное применение хлорэтила, в редких случаях показано хирургическое вмешательство.
МКБ-10
Общие сведения
Мигрирующая личинка (larva migrans, ползучая болезнь) является собирательным названием для группы кожных личиночных поражений. Первые письменные упоминания заболевания датируются 1874 годом, клиническую характеристику нозологии дали Уайт и Дав в 1929 году. Патология распространена в тропических странах, на территории бывшего СССР, США, Европы. Наблюдается прямая зависимость заболеваемости от сезона – дожди способствуют рассеиванию яиц и личинок паразита. Частота нетипичных локализаций поражения (туловище, ягодицы, голова) также зависят от сезонных изменений вследствие использования либо неиспользования обуви и закрытой одежды.

Причины
Наиболее распространенными возбудителями являются личинки анкилостом Ancylostoma braziliense, A. ceylanicum, A. caninum. Путь заражения – контактный (через кожу). Для гельминтов человек является биологическим тупиком – паразиты за редким исключением не могут пройти через базальную мембрану эпидермиса, вследствие чего личинки погибают в коже, не достигая половой зрелости. Хаотичная миграция внутри верхних слоев кожи приводит к появлению извитых (серпигинозных), реже линейных ходов.
Источниками инфекции служат собаки и кошки, в кишечнике которых обитают половозрелые особи. Считается, что анкилостомами поражено до 50% бродячих собак. С фекалиями яйца паразитов выделяются в окружающую среду, где в условиях высокой влажности, затененности и тепла развиваются личиночные формы. При нахождении на песке без обуви и длительном лежании личинки активно проникают в кожу. Факторы риска – мужской пол, молодой возраст, проживание в неудовлетворительных социально-гигиенических условиях, на территории с загрязнением испражнениями животных.
Патогенез
Личинки проникают в организм человека при случайном контакте сквозь отверстия волосяных фолликулов, микротрещины или через неповрежденную кожу, которая разрушается протеазой, вырабатываемой паразитами. Дермальное ограничение продвижения обусловлено малым количеством либо отсутствием продуцируемой личинкой коллагеназы, необходимой для расщепления базальной мембраны. Обычно возбудитель находится в зернистом эпидермальном слое, крайне редко проникает в нижележащие покровы, но быстро возвращается обратно.
Расположение хода не связано с локализацией личинки, поскольку движение последней хаотично и беспорядочно. Возможно наличие как одиночных, так и множественных ходов, заполненных серозным отделяемым. Иногда выявляются уртикарные и эритематозные высыпания. В толще эпидермиса в надбазальных слоях обнаруживаются непосредственно личинки, а также воспалительные явления аллергического генеза: некротизированные кератиноциты, спонгиоз, внутриэпидермальные везикулы, большое количество нейтрофилов и эозинофилов.
Симптомы мигрирующей личинки
Инкубационный период составляет 1-5 суток, может укорачиваться до нескольких часов либо удлиняться до месяца и более. На месте внедрения личинки возникает сильный зуд, болезненность, жжение, появляется красный бугорок. Около 40% случаев инвазии приходится на кожные покровы нижних конечностей, 20% – на ягодицы, гениталии, 15% – на область живота. По мере продвижения личинки на коже возникают возвышающиеся извилистые нитевидные линии красновато-коричневого цвета, исходящие из первичного бугорка.
Паразит двигается относительно медленно, до 1-3 см в сутки, его передвижение может не ощущаться пациентом, редкими проявлениями считаются отеки области инвазии, гнойнички вокруг волосяных фолликулов. Симптомы сохраняются от 4 недель до 6 месяцев, могут самостоятельно регрессировать. Около 50% больных отмечают появление сухого надсадного кашля со скудной мокротой. Температура тела обычно остается нормальной, резкое повышение может свидетельствовать о присоединении вторичной бактериальной инфекции.
Осложнения
Наиболее частыми осложнениями мигрирующей личинки являются гнойные воспалительные процессы в коже, связанные с присоединением гноеродной флоры: импетиго, абсцессы, фолликулит. Нередко наблюдаются осложнения на фоне приема этиотропных лекарств, их воздействия на ЖКТ, ЦНС и другие органы. Реже встречающаяся массивная инвазия паразита приводит к отечности и лимфостазу конечностей, описаны случаи синдрома Леффлера, эозинофильного энтерита, мультиформной экссудативной эритемы и буллезных кожных поражений. В случае миграции личинок по кровеносному руслу и попадания в легочную ткань формируются бронхиты, пневмонии, плевриты.
Диагностика
Диагноз мигрирующей личинки подтверждается инфекционистом, нередко требуется осмотр дерматовенеролога и других врачей. Обязателен тщательный сбор эпидемиологического анамнеза с уточнением поездок в природные зоны, эндемичные по данному заболеванию. Диагностические методы, необходимые для верификации личиночного поражения, включают следующие методики:
- Физикальное обследование. При объективном осмотре на коже стоп, ягодиц, живота, реже других частях тела обнаруживаются характерные серпигинозные нитевидные извитые ходы, приподнятые над кожными покровами, буровато-коричневого оттенка до 5 см длиной и 3 мм шириной. Наблюдаются расчесы вследствие сильного зуда. Внутренние органы и системы обычно в норме.
- Лабораторные исследования. Характерными изменениями в общеклиническом анализе крови считаются лейкоцитоз, эозинофилия (до 50%) и незначительное ускорение СОЭ. Биохимические параметры в пределах нормы за исключением гипергаммаглобулинемии. Иммунограмма может выявить повышение уровня Ig E. В редчайших случаях аллергического поражения легких возможно обнаружение до 90% эозинофилов в мокроте.
- Выявление инфекционных агентов. Доказательством инвазии служит визуализация личинок в биоптатах кожи. С целью дифференциального диагноза исследуются кожные и перианальные соскобы, проводится ИФА с боррелиозными антигенами, микроскопия кала с целью выявления яиц и живых паразитов, в некоторых случаях осуществляется вскрытие ходов скальпелем, обработанным вазелином, для обнаружения возбудителя.
- Инструментальные методики. Рентгенография легких необходима для исключения поражения нижних отделов респираторного тракта. Ультразвуковое исследование органов брюшной полости назначается для исключения паразитарных инвазий с висцеральными проявлениями, по показаниям выполняют УЗИ мягких тканей, лимфатических узлов в зоне кожных симптомов.
Дифференциальную диагностику проводят с мигрирующим миазом, для которого типично быстрое (до 30 см в день) продвижение внутри кожи личинок насекомых, кольцевидной эритемой при иксодовом клещевом боррелиозе в виде пятен с прямыми контурами, не приподнятыми над поверхностью. При грибковых кожных инфекциях отмечаются бляшки, шелушение. Симптомы мигрирующей личинки также сходны с чесоткой, характеризующейся прямыми линейными ходами белесовато-серого цвета, и контактным дерматитом, который возникает после контакта кожи с аллергеном, сопровождается появлением везикул и гиперемии при отсутствии серпигинозных ходов.
Лечение мигрирующей личинки
Лечение обычно проводится амбулаторно. Специальные диетические рекомендации не разработаны, назначается общий стол и адекватный водный режим. Этиотропная терапия мигрирующей личинки предусматривает пероральный прием препаратов альбендазола, ивермектина и тиабендазола, эффективность составляет 75-89%. Возможно местное нанесение крема либо суспензии с альбендазолом, эффект достигается в 96-98% случаев.
Для облегчения зуда рекомендовано использование антигистаминных и десенсибилизирующих средств, при возникновении гнойных осложнений показаны антибиотики. Описана некоторая эффективность местной криотерапии жидким азотом, однако при ее неправильном применении могут образовываться длительно незаживающие язвы. Высока вероятность отсутствия личики в обрабатываемом азотом ходе и выживания гельминта, поскольку паразит способен сохранять жизнеспособность при -21° C более 5 минут.
Прогноз и профилактика
Прогноз благоприятный, летальных исходов зафиксировано не было. При неосложненном течении болезни симптомы склонны к самостоятельному исчезновению примерно в течение 3-5 недель. Ежегодно до 22-58% случаев мигрирующей личинки неверно интерпретируются медицинскими работниками, вследствие чего возникают осложнения, не назначается адекватное лечение. Причиной диагностических ошибок становится неявная или нерезко выраженная симптоматика с преобладанием кожного зуда при отсутствии других жалоб.
Специфические профилактические средства (вакцины) не разработаны. Неспецифическими мерами предотвращения заражения являются личная гигиена, отказ от купания и проглатывания воды в случайных водоемах, хождение по песку и почве в прорезиненной закрытой обуви, использование перчаток и одежды закрытого типа при работе с грунтом и растениями. Необходимо проведение плановой дегельминтизации домашних питомцев, исключение выгула собак на детских игровых площадках.
4. Epidemiology and morbidity of hookworm-related cutaneous larva migrans (HrCLM): Results of a cohort study over a period of six months in a resource-poor community in Manaus, Brazil/ F. Reichert, D. Pilger, A. Schuster// PLoS Negl Trop Dis - 2018 Jul; - №7.
Аскаридоз лёгких – это патологическое состояние, обусловленное механическим повреждением органов дыхания личинками круглых гельминтов – аскарид, а также токсическим и аллергическим действием продуктов их жизнедеятельности. Проявляется кашлем с небольшим количеством слизистой мокроты, бронхоспастическим синдромом, может протекать по типу бронхопневмонии или серозного плеврита. Диагноз устанавливается на основании клинических симптомов, рентгенологических и лабораторных данных, результатах серологических исследований. Лечение осуществляется эффективными в отношении аскарид противогельминтными препаратами и патогенетическими средствами.
МКБ-10
Общие сведения
Аскаридоз лёгких является острой стадией антропонозного геогельминтоза, вызываемого аскаридами. Согласно статистическим данным, аскаридозом страдает более 1 миллиарда человек в мире, ежегодному заражению подвергаются 100-200 тысяч. Заболеванию подвержены лица всех возрастных категорий, 65-70% заразившихся составляют дети. По частоте встречаемости данный гельминтоз занимает второе место среди всех глистных инвазий, уступая только энтеробиозу. Аскаридоз наиболее распространён в странах с жарким и влажным субтропическим и тропическим климатом. В некоторых государствах Средней и Юго-Восточной Азии, африканского континента аскаридами заражено более 50% населения.

Причины
Возбудителем аскаридоза лёгких является представитель семейства нематод аскарида человеческая в личиночной стадии развития. Взрослая особь паразитирует в тонком кишечнике исключительно человека, который становится источником инвазии. Аскариды двуполы. Самки почти вдвое крупнее самцов и могут достигать 40 см в длину, откладывают до 250 000 оплодотворённых и неоплодотворённых яиц ежедневно. С каловыми массами больного яйца попадают в почву. Эпидемиологическую опасность представляют только оплодотворённые яйца. При достаточной температуре, влажности и аэрации почвы в них вызревают личинки. Проглатывание таких яиц вызывает аскаридоз. При неблагоприятных условиях развитие личинок приостанавливается, но их жизнеспособность внутри яиц длительно сохраняется. Гельминты пребывают в кишечнике на протяжении года, затем при отсутствии повторной инвазии происходит самоизлечение. Факторами риска развития болезни являются:
- Метеоклиматические условия. В некоторых регионах с жарким влажным климатом при массовом скрининге аскаридоз выявляется у 95-98% населения. Личинки гельминтов в таких климатических зонах вызревают в течение всего календарного года, тогда как в умеренном климате заражение человека аскаридами происходит с апреля по октябрь. В жарких сухих регионах заболеваемость гельминтозом значительно ниже. В условиях вечной мерзлоты аскаридоз не встречается.
- Антисанитария. Распространению глистной инвазии способствует скученность населения, отсутствие водопровода и канализации, нехватка воды. Часто аскаридоз развивается в результате употребления в пищу немытых овощей и ягод, выращенных с применением необеззараженных человеческих фекалий в качестве удобрения.
- Детский возраст.Гельминтоз у детей дошкольного и младшего школьного возраста встречается в 1,5 раза чаще, чем у взрослых. Дети раннего возраста пробуют предметы на вкус, берут в рот грязные пальцы, много контактируют с домашними животными, играют в песочнице, не соблюдая правила гигиены в силу возрастных особенностей.
- Профессиональная деятельность. Заболеванию больше подвержены лица, вынужденные постоянно контактировать с почвой. Аскаридоз обнаруживается у полеводов, агрономов и других работников сельскохозяйственных предприятий. Среди городских жителей чаще болеют сотрудники озеленительных служб, овощных магазинов и баз.
Патогенез
Яйца гельминтов попадают в человеческий организм фекально-оральным путём с загрязнёнными продуктами питания, водой. Заболевание начинается с острой миграционной фазы. Личинка выходит из яйца и крючкообразными отростками прикрепляется к внутренней стенке тонкой кишки. Ротовым отверстием она перфорирует слизистую оболочку и проникает в кишечные вены. С током крови через воротную и нижнюю полую вены гельминт мигрирует в правые отделы сердца, затем – в лёгочные артерии, капилляры, альвеолы, бронхиолы. В респираторном тракте личинки развиваются в течение 20-21 дня.
Паразитируя в лёгких, гельминты блокируют мелкие сосуды. Нарушается питание лёгочной паренхимы. Образуются микроинфаркты альвеолярной ткани. Продукты жизнедеятельности аскарид оказывают мощное сенсибилизирующее действие на человеческий организм. Развивается воспалительная реакция. Вокруг гельминта образуется инфильтрат, состоящий из лимфоцитов, эозинофилов, плазматических клеток, иногда гистиоцитов. Впоследствии такие инфильтраты либо полностью разрешаются, либо на их месте формируются участки фиброза. Сенсибилизация организма метаболитами аскарид нередко приводит к возникновению бронхообструкции. С кашлевыми толчками личинки нематод забрасываются в глотку, заглатываются и повторно попадают в тонкий кишечник. Заболевание переходит в хроническую кишечную стадию.
Симптомы аскаридоза лёгких
Первые клинические признаки поражения лёгких аскаридами появляются на 7-10 день глистной инвазии. Симптомы болезни многообразны. Пациента беспокоит приступообразный кашель со скудным отделением светлой мокроты, изредка возникает кровохарканье. Эозинофильная пневмония сопровождается субфебрильной лихорадкой. Иногда (чаще – в детском возрасте) температура тела поднимается выше 38°C. Для такой формы гельминтоза лёгких характерен неправильный тип лихорадки. При повышении температуры выявляется озноб. Выражены и другие симптомы интоксикации: общая слабость, головная боль, снижение аппетита, неустойчивое настроение.
Интенсивные, усиливающиеся при глубоком вдохе, кашле, чихании и движении боли в правой или левой половине грудной клетки свидетельствуют о развитии плеврита. Позднее присоединяется смешанная одышка, выраженность которой зависит от количества экссудата в плевральной полости. Токсико-аллергическое действие метаболитов аскарид провоцирует бронхоспазм. Пациента беспокоят приступы удушья с затруднением выдоха, сопровождающиеся сухим кашлем и свистом в груди. Наряду с лёгочной симптоматикой часто присутствуют уртикарные кожные высыпания, гепатоспленомегалия. Иногда аскаридоз лёгких протекает скрыто.
Осложнения
Тяжёлые осложнения аскаридоза обычно возникают в хронической кишечной фазе болезни. Наиболее часто страдают органы желудочно-кишечного тракта – развивается холецистохолангит, аппендицит, кишечная непроходимость. Смертельную опасность представляет проникновение взрослых особей в правый желудочек и лёгочные артерии, а также заползание аскарид через пищевод и глотку в дыхательные пути, приводящее к гибели больного от асфиксии. Появляющийся в остром периоде респираторный аллергоз может сохраняться длительное время после элиминации гельминтов.
Диагностика
Диагностику гельминтоза осуществляют инфекционисты-паразитологи. В фазе поражения лёгких в диагностическом поиске часто принимает участие пульмонолог. При сборе анамнеза у пациентов с подозрением на лёгочный аскаридоз уточняют профессиональный маршрут, наличие контакта с почвой (возделывание земли на приусадебном участке, сезонные сельхозработы). При осмотре можно обнаружить кожную сыпь. Аускультативно выслушиваются рассеянные сухие свистящие хрипы, локальные влажные хрипы, при плеврите – шум трения плевры, резкое ослабление дыхания с одной стороны. Выявить аскаридоз на стадии миграции аскарид помогают следующие методы исследования:
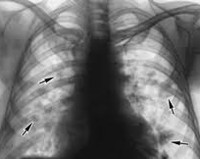
- Рентгенография лёгких. На рентгенограмме легких часто просматриваются летучие инфильтраты Леффлера. Затенения сохраняются в течение 2-3 дней, затем полностью разрешаются и появляются в другом сегменте, доле или лёгком. Изредка инфильтрация лёгочной ткани персистирует на протяжении 20-30 дней. Иногда при рентгеновском исследовании визуализируются признаки наличия экссудата в полости плевры.
- Лабораторные анализы. В периферической крови, мокроте, плевральной жидкости определяется высокий уровень содержания эозинофилов. При исследовании бронхиального секрета также можно обнаружить спирали Куршмана и кристаллы Шарко-Лейдена, характерные для респираторного аллергоза. ПЦР мокроты позволяет выявить ДНК гельминтов.
- Серологическая диагностика. Методы серологической диагностики (РНГА, РИФ, ИФА) основаны на обнаружении антител к аскаридам в сыворотке крови. Чаще всего используется иммуноферментный анализ. Антитела к гельминтам начинают вырабатываться на 5-10 сутки от начала инвазии. Определение титров иммуноглобулинов класса М и G даёт возможность диагностировать аскаридоз в период пребывания личинок аскарид в лёгких.
Длительно не разрешающиеся эозинофильные инфильтраты лёгочной ткани следует дифференцировать с бактериальной пневмонией, онкологической патологией лёгких, туберкулёзом. Летучие инфильтраты иногда появляются в приступном периоде бронхиальной астмы и при других аллергических болезнях. Для уточнения диагноза может понадобиться участие онкологов, фтизиатров, аллергологов-иммунологов и дерматологов.
Лечение аскаридоза лёгких
Лёгочный аскаридоз является ранней стадией глистной инвазии и хорошо поддаётся консервативной терапии. При этом многие специалисты в сфере паразитологии и инфектологии считают, что противогельминтные препараты более эффективны в кишечную фазу развития болезни. Кроме того, токсическое действие продуктов распада личинок при их массовой гибели может вызвать тяжёлый пульмонит. Лечение противопаразитарными средствами осуществляется в несколько (2-3) этапов. В стадию миграции личинок можно назначать тиобендазол, мебендазол или албендазол. Большое значение на данном этапе имеет купирование патологических состояний. Применяются антигистаминные препараты, кортикостероиды, бронходилататоры. Через 10-14 дней курс противогельминтной терапии повторяют.
Прогноз и профилактика
Прогноз при адекватном лечении благоприятный. Аскаридоз лёгких обычно полностью излечивается. При повторных инвазиях, например, у лиц, проживающих в эндемичных очагах, к данному гельминтозу постепенно формируется иммунитет. Специфической профилактики аскаридоза не существует. Чтобы избежать инвазии, необходимо соблюдать правила личной гигиены, не использовать воду из открытых водоёмов для питья и приготовления пищи, не есть немытые овощи, фрукты, зелень. Общественная профилактика включает в себя строительство очистных сооружений, безопасное в отношении паразитов удобрение сельскохозяйственных угодий, массовую профилактическую дегельминтизацию населения неблагополучных по аскаридозу регионов.
2. Клинические рекомендации (протокол лечения) оказания медицинской помощи взрослым больным аскаридозом. - 2016.
3. Глистная инвазия в структуре респираторных аллергозов: бронхиальная астма и симндром Леффлера/ Восканян А.Г., Восканян А.// Международный журнал прикладных и фундаментальных исследований. – 2016 – №4.

В нашей среде обитает множество паразитов, и ими можно очень просто заразиться. Гельминты — одни из них. Это паразитические черви, обитающие в организме животного или человека. Живые организмы, содержащие в себе временно или постоянно гельминтов, называются хозяевами. Черви могут развиваться у одного или нескольких хозяев.
Что такое синдром мигрирующих личинок
По особенностям развития паразита различают два типа хозяев: промежуточные и конечные.
- Хозяин, имеющий в себе половозрелого червя, называется финальным.
- Хозяин, имеющий в себе развивающуюся личинку червя — промежуточным.
Гельминты, попадая в организм хозяина, используют его питательные вещества, токсичны для нервной системы, отравляют внутренние органы и поэтому могут вызывать различные изменения в организме.
Личинки животных нематод, попадающие в организм человека, могут вызывать синдром мигрирующих личинок. Поскольку человек — это промежуточный хозяин, личинки патогенов в его организме не растут и не созревают, но могут мигрировать по тканям и вызывать их воспаление.
Этот синдром может быть вызван несколькими видами гельминтов. Однако чаще всего вызывается:
- круглыми собачьими червями Toxocara canis;
- реже круглыми кошачьими червями Toxocara cati;
- или Toxocara mystax larvae.
Заболевание вызыванное личинками токсокара, попадающими в живой организм, называется токсокарозом. Это опасное хроническое заболевание, оно длится год и более с обострениями. Распространенность инфекции связана с заражением собак и кошек и загрязнением окружающей среды их фекалиями.
Эпидемиология
Токсикоз — это всемирное заболевание. В развитых странах по заболеваемости глистными инфекциями эта инфекция занимает второе место после энтеробиоза (инфекция, вызывающая судороги).
Токсокароз — миграционный синдром
Личинки проникают через кожу. Яйца токсокара находятся в больших количествах в почве. Личинки токсокара чаще всего встречаются у детей, поражая от 2% до 10% зараженных. Заболеваемость одинакова у мальчиков и девочек. Возраст больных детей от 1 до 7 лет.
Заражение детей заболеванием вызвано:
- несоблюдением требований гигиены;
- играми в песочнице или с животными.
Установлено, что у детей в возрасте 1–6 лет геофагия проявляется поведенческим расстройством в 2–10%. Это нарушение важно, потому что на момент начала синдрома внутриглазной миграции личинок 40% пациентов имеют эту поведенческую патологию.
Заболевание встречается реже среди взрослых. В Западной Европе поражены 2–5%. У здоровых взрослых есть антитела к токсокарам.
Заболеваемость токсокарозом зависит также от места проживания. Токсикозные патогены чаще встречаются в тропическом и умеренном климате, а в теплых странах их количество достигает 86-93%. Инфекционность намного выше среди сельского населения (14-37%) по сравнению с городским населением.
По данным различных стран, заражение яиц токсокарами дворов, песочниц, пляжей и других общественных мест составляет от 10% до 30%. Эта проблема связана с ростом количества оставленных без присмотра собак, кошек и несоблюдением графика дегельминтизации домашних животных.
Патогенез

Патогенез
Конечный хозяин круглых червей — представитель семейства собак и кошек, только в нем червь может расти, созревать и откладывать яйца. Червь, попадая в организм собаки, паразитирует в кишечнике и питается содержимым кишечника.
Собаки заражаются токсокарами, поедая яйца глистов с землей. В кишечнике личинка, выпущенная из яйца, мигрирует с кровью в легкие, кусает альвеолы и через бронхи попадает в носоглотку и рот. Эта часть миграции, дыхательные пути, называется стадией миграции трахеи.
Позже личинки снова попадают в кишечник собаки через пищевод, где превращаются во взрослых червей, откладывающих яйца. Взрослая самка токсокара выделяет около 200-250 тысяч особей. Остальные личинки проникают в ткани и распределяются по тканям организма.
Исследования показали, что в организме самки часть личинок может длительное время оставаться в тканях. На последних неделях беременности собаки, личинки могут активироваться и заражать будущих щенков за счет различных гормонов. Щенки также могут заразиться во время кормления. Такая инфицированная сука может родить до четырех щенков в помете, инфицированных Toxocara canis, при отсутствии повторного заражения.
Таким образом, основной источник токсокаров у человека — это щенки до 3-месячного возраста. Поэтому дегельминтизация беременных сук и всех домашних животных по мере необходимости — важная часть профилактики.
С фекалиями собаки яйца попадают в почву и начинают созревать, становясь инфекцией. Почва и соответствующие условия окружающей среды, имеют важное значение для развития яиц:
- температура воздуха (16-30 о С);
- влажность воздуха и почвы;
- свет.
В почве яйца созревают через 2–3 недели. При неправильных условиях яйца переходят в состояние анабиоза и, таким образом, могут перезимовать. Яйца могут сохранять жизнеспособность в почве 8 лет и более.
Люди — это случайные промежуточные хозяева этого паразита и заражаются токсокарозом через оральные фекалии. В отличие от животных, личинки, не попадающие в организм человека, не размножаются и не растут, поэтому люди не могут заразиться ими. Чаще всего личинка передается через грязные руки при употреблении немытых ягод, фруктов, овощей. Также возможно заразиться при употреблении в пищу инфицированной и недостаточно приготовленной курицы, говядины или баранины. Дети могут заразиться, играя в песочнице.
Люди не могут заразиться от собаки токсокарозом во время контакта, поскольку яйца должны попасть в почву и созреть. Однако необходимо соблюдать осторожность, так как собаки могут нести уже зрелые яйца на своей шерсти или языке.
Зрелые яйца токсокара попадают в желудочно-кишечный тракт через рот. В желудке человека яичная скорлупа растворяется, личинка высвобождается и мигрирует в сторону тонкого кишечника. Она проникает через слизистую оболочку кишечника и попадает в кровеносные и лимфатические сосуды. Вместе с кровью и лимфой личинки попадают в органы:
- печень;
- сердце;
- легкие;
- почки;
- поджелудочную железу;
- глаза и др.
Установлено, что личинки Toxocara cati в основном мигрируют в мышцы, печень и легкие, а личинки Toxocara canis часто встречаются в центральной нервной системе.
В тканях личинки инкапсулируются в течение длительного периода времени, после чего капсулы распадаются и личинки высвобождаются. В это время они становятся активными и начинают мигрировать, раздражая и повреждая ткани. Перемещение личинок вызывает иммунный тканевый ответ и аллергическую реакцию.
Это движение личинок называется синдромом мигрирующих личинок. Состояние может быть вызвано только личиночной стадией паразита, а не взрослым червем или яйцами. В зависимости от расположения личинок синдром делится на два типа:
Клиника
Клинические симптомы токсокароза широко варьируются и зависят от органов и тканей, пораженных мигрирующей личинкой. Также могут отсутствовать симптомы.
Течение болезни зависит от:
- количества личинок;
- пораженного органа;
- общей резистентности организма;
- частоты повторного заражения.
Поскольку мигрирующие личинки вызывают аллергическое воспаление, тяжесть заболевания также зависит от аллергической реакции организма на токсокарических личинок. У пациентов с атопическим аллергическим заболеванием эта инфекция обычно протекает тяжелее.
Специфические антитела вызывают воспалительную реакцию на токсокарсекреторный (TES) антиген и аллергический компонент TBA-1. Эти антигены активируют клетки CD4 +, они дифференцируются в клетки Th1 и Th2. Интерлейкин-2 (IL-2) и γ-интерферон (γIFN), секретируемый Th1, интерлейкин-4 (IL-4) и интерлейкин-5 (IL-5) вызывают дополнительный иммунный ответ.
IL-4 способствует пролиферации и дифференцировке B-клеток в плазматические клетки, они при воздействии IL-2, IL-4, IL-5 и γIFN начинают синтезировать антитела различных изотипов. IL-5, в свою очередь, способствует дифференцировке и адгезии эозинофилов.
Эпителиальные воспалительные клетки окружают личинок и образуют специфические эозинофильные гранулемы. Именно локализация гранулем определяет клиническое течение болезни.
Существуют разные формы висцерального и окулярного (внутриглазного) синдрома мигрирующих личинок. Такая классификация значительно упрощается, так как всегда возможна одна из этих форм. А выявление токсокароза глаза и обследование внутренних органов обычно выявляют разную степень поражения внутренних органов.
Висцеральный мигрирующий личиночный синдром
Токсикоз может поражать различные органы:
Таким образом, синдром проявляется различными симптомами. Однако наиболее частые области поражения — это дыхательные пути, что делает признаки воспаления верхних дыхательных путей одними из самых распространенных.
Неожиданные проявления синдрома висцеральной миграции личинок также возможны после внезапной миграции большого количества личинок:
- острая пневмония;
- эозинофильный менингоэнцефалит.
Этот синдром может увеличить риск смерти, если инфекция проявляется аномальным иммунным ответом или, когда происходит интенсивная миграция личинок в миокард или центральную нервную систему.
Внутриглазный синдром мигрирующих личинок
Этот тип синдрома возникает при попадании личинок токсокариоза в ткани глаза и глазницы через центральную артерию сетчатки и зубчатые артерии. Глазной токсокароз классифицируется по классификации 1971 г. Классификация Уилкинсона и Уэлча по развивающейся клинике. Только теперь классификация стала более точной, поскольку о синдромах известно больше.
- Хронический эндофтальмит (лучи стекловидного тела, оболочки, гранулемы; выражен задний увеит; резко снижена острота зрения);
- Задний гранулематозный хориоретинит (в заднем полюсе глаза, в области макулы, на сосочке зрительного нерва или прилегающих к этим структурам сетчатки 1-2 белых очага; обычно острота зрения снижается);
- Периферический гранулематозный хориоретинит (белые образования, покрытые соединительной тканью стекловидного тела, проникающие в стекловидное тело, расположенное на периферии сетчатки; острота зрения обычно не изменяется).
В редких случаях глазной токсокароз может проявляться в виде:
- неврита;
- нейроретинита;
- локализованного абсцесса стекловидного тела;
- иридоциклита;
- личиночного кератоконъюнктивита.
Если токсокариозные личинки попадают в ткани перед глазничной перегородкой, это вызывает воспаление клетки передней перегородки: веки и конъюнктива становятся опухшими и красными. Когда личинки попадают в орбитальную перегородку, орбита воспаляется.
- отек и покраснение соединений и век;
- болезненные движения глаз;
- удвоение;
- офтальмоплегия;
- инверсия;
- оптическая нейропатия.
Чаще всего поражается один глаз, и визуальные изменения напрямую зависят от местоположения очага поражения. Глазной токсокароз часто осложняется:
- нарушениями кровообращения сетчатки;
- отслоением сетчатки;
- абсцессом глаза;
- вторичной глаукомой или катарактой.
Диагностика

Диагностика
Диагностика всех гельминтозов основана на сборе точного анамнеза. Эпидемиологические аспекты очень важны, так как риск развития определенного инфекционного заболевания тесно связан с:
- профессией;
- отдыхом;
- поездками в определенные эндемичные районы.
Но их одних недостаточно.
Конечно, диагностировать токсокароз непросто, потому что люди не выделяют ни токсокарических червей, ни яиц, обнаружить мигрирующих личинок в биопсийном материале тоже сложно. Поэтому для подтверждения диагноза всегда проводятся инструментальные и лабораторные исследования:
- Общий анализ крови : лейкоцитоз, стойкая эозинофилия, анемия, тромбоцитоз. Сообщается, что эозинофилия чаще встречается у детей, чем у взрослых;
- Иммунологические тесты. Чаще встречаются: гипергаммаглобулинемия. Повышается уровень IgE гамаглобулина. Повышенные титры изогемагглютинина для антигенов групп крови A и B. Антитела к токсокарам обнаруживаются в стекловидном теле (90% случаев);
- Иммуноферментный анализ . Токсикарные секреторно-секреторные (TES) антигены выявляются с помощью прямого ИФА. В случае токсокроза специфичность анализа ELISA составляет 92–95%, а чувствительность 73–75% при использовании титра 1:32 для диагностики (4, 14). Непрямой ИФА используется для обнаружения антител (IgE, IgG и IgM) к токсокарическим антигенам TES. Этот метод обнаруживает антитела от 78 до 92%. кейсы;
- Инструментальные методы исследования . При висцеральной форме синдрома ультразвуковое исследование или компьютерная томография выявляют увеличенную печень, а при внутриглазном исследовании — гранулемы или абсцессы в тканях глаза. Гранулемы в корковом или подкорковом мозге также можно увидеть на КТ.
- Исследование BMR. Показывает изменения в мозге. Белковый экссудат в режимах T1 и T2 может быть более выраженным, а разность потенциалов — видимой. Обследование гадолинием улучшает обнаружение абсцесса. Личинки токсикара могут быть идентифицированы с помощью биопсии органа. Было замечено, что личинки в биопсийном материале встречаются крайне редко, но если они не обнаружены, диагноз не может быть исключен;
- Гистологическое исследование . Выявлены множественные эозинофильные абсцессы, гранулемы аллергического типа в поврежденных органах и некроз тканей вокруг макрофагов и лимфоцитов.
Лечение
Токсикоза может вызывать ремиссию и поэтому не всегда требует специального лечения. Он также не применяется при токсокарозе легкой и средней степени тяжести. Для лечения этой инфекции показаны этиотропные и патогенетические методы лечения.
Этиотропное лечение
Назначаются антигельминтики, а поскольку многие из них усиливают воспалительный ответ, также назначаются глюкокортикостероиды.
Самый эффективный глистогонный препарат — альбендазол. Также врачи обычно назначают Мебендазол, хотя на листке-вкладыше не указано показание к лечению инфекции Toxocara canis или Toxocara cati, поскольку это глистогонное средство широкого спектра действия.
Патогенез лечения
Применяется дезинтоксикационная терапия, включающая внутривенные инфузии электролитов. Для восстановления обезвоживания вводят 20% внутривенно раствор маннита. Внутривенное или внутримышечное введение фуросемида до достижения желаемого результата. Нестероидные противовоспалительные препараты (НПВП) используются для уменьшения воспалительной реакции за счет снижения активности циклооксигеназы и синтеза простагландинов, лейкотриенов.
Повреждение центральной нервной системы у личинок может привести к возбуждению и подавляется седативными средствами. При форме глазного токсокароза назначают все вышеперечисленные препараты. В тяжелых случаях или при наличии осложнений может применяться хирургическое лечение:
- витрэктомия;
- операция по удалению катаракты;
- лазерная фотокоагуляция;
- энуклеация глаза.
Профилактика
Яйца Toxicar загрязняют окружающую среду, поэтому очень важно соблюдать основные правила:
- личная гигиена;
- дегельминтизация домашних животных;
- чистая окружающая среда;
- охрана детской игровой площадки.
Личная гигиена: каждый раз, возвращаясь с поля, необходимо мыть руки после поглаживания песком, землей и ласки домашних животных. Также не позволяйте собакам облизывать морду, посуду, используемую людьми. Ешьте только мытые ягоды, фрукты, овощи.
Домашним животным необходимо своевременно проводить дегельминтизацию. Поскольку щенки и котята могут заразиться трансплантатом или через грудное молоко. Дегельминтизацию следует начинать через 3 недели и продолжать каждые 2–4 недели. До 6 месяцев Щенкам старше 6 месяцев рекомендуется проводить дегельминтизацию каждый месяц. Взрослым собакам каждые 3 месяца. Суки должны быть дополнительно дегельминтизированы за 2 недели до спаривания.
Собираясь на прогулку с питомцем, обязательно собирайте пакеты для сбора фекалий. Это предотвратит загрязнение окружающей среды фекалиями животных. На детских площадках следует избегать домашних животных. Когда дети не играют, песочницы следует накрывать крышкой. Песок в ящиках тоже нужно менять регулярно. Самая главная и самая большая проблема — это бездомные собаки и кошки, поэтому их отлов и транспортировка в приюты — неотъемлемая часть профессиональной тактики.
Резюме

Резюме
Обнаружение глистной инвазии следует подозревать при наличии:
- рецидивирующей стойкой лихорадки;
- стойкой эозинофилии;
- многосторонних клинических исследований.
Серологическая диагностика токсокароза всегда необходима при множественных гранулемах внутренних органов или при наличии заднего увеита, эндофтальмита. При диагностировании висцерально-миграционного личиночного синдрома не следует исключать внутриглазную форму синдрома и наоборот.
Лечение глистогонными средствами и кортикостероидами необходимо при тяжелом висцерально-миграционном личиночном синдроме и глазном токсокарозе. Поскольку токсокариозные личинки могут сохраняться в тканях в течение года, необходимо следить за состоянием больных и предупреждать о возможности повторного заражения. Необходимо соблюдать принципы личной гигиены, дегельминтизации домашних животных, чистой окружающей среды.
Что такое тениоз? Причины возникновения, диагностику и методы лечения разберем в статье доктора Александрова Павла Андреевича, паразитолога со стажем в 14 лет.
Над статьей доктора Александрова Павла Андреевича работали литературный редактор Юлия Липовская , научный редактор Сергей Федосов и шеф-редактор Лада Родчанина

Определение болезни. Причины заболевания
Тениоз (Taeniosis) — паразитарное заболевание человека, вызываемое половозрелой стадией ленточного гельминта (свиного цепня), который проникает в организм человека при употреблении плохо приготовленного мяса, паразитирует в тонком кишечнике и вызывает расстройства пищеварения. В некоторых случаях может осложняться цистицеркозом — паразитированием в тканях организма личинок свиного цепня, что приводит к серьёзным последствиям и даже смерти.
Возбудитель
- домен — эукариоты;
- царство — животные;
- тип — плоские черви;
- класс — ленточные черви;
- отряд — циклофиллиды;
- семейство — тенииды;
- род — Taenia;
- вид — свиной цепень (Taenia solium).
Свиной цепень (устаревшее название "cолитёр") — это плоский (ленточный) паразитический червь, длина которого в кишечнике человека достигает 3 метров, а по данным Ц ентра по контролю и профилактике заболеваний США (CDC) его длина может достигать 7 метров. Как правило, паразитирует только 1 червь. Паразит имеет головку, шейку и тело. Тело червя (стробила) состоит из члеников (п роглоттидов), их число может достигать 1000 . Головка (сколекс) размерами до 2 мм в диаметре имеет хоботок и 4 мышечные присоски (органы прикрепления), расположенные крестообразно. На хоботке есть крючья в количестве от 22 до 32, из-за этого есть второе название паразита — вооружённый цепень.
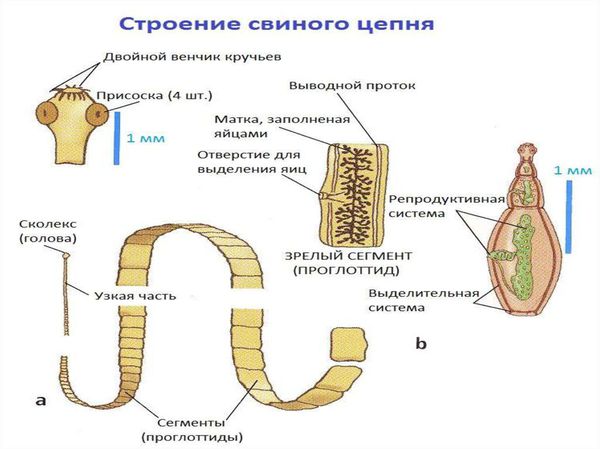
Яйца паразита попадают с калом человека в окружающую среду. Животные (свиньи, собаки, кошки и даже человек при несоблюдении гигиены) поедают яйца, зародыши проходят через кишечную стенку и разносятся кровью по всему организму, после чего оседают в тканях (в основном в соединительной ткани между мышцами). Через пару месяцев яйца превращаются в финны (цистицерки), которые живут до 5 лет, после чего они погибают и обызвествляются (накапливают минеральные вещества, соли кальция). Цистицерки имеют вид полупрозрачных беловатых пузырьков диаметром до 1,5 см, внутри видна мелкая сформированная головка.
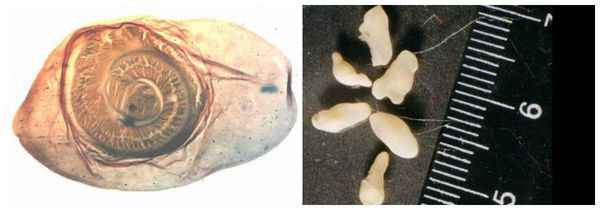
Для полноценного развития свиного цепня необходима смена хозяев за его жизнь. Человек является окончательным хозяином. В его кишечнике паразитирует взрослый гельминт, который развивается за 2 месяца из финны (личинки червя в тканях), съеденной с мясом. Паразит прикрепляется к стенке тонкого кишечника и растёт, поглощая пищу и постепенно наращивая членики (от шейки), которые по мере созревания отрываются и выходят в окружающую среду при дефекации. Паразит может жить в кишечнике десятки лет.
Человек может стать и промежуточным хозяином (при поедании яиц). В этом случае для паразита наступит "экологический тупик" — он не сможет развиться до половозрелой стадии и продолжить свой род, потому что мясо человека с финнами никто не ест.
Яйца выживают в окружающей среде в течение нескольких месяцев в зависимости от условий. Высыхание могут выдерживать в течение 10 месяцев, способны зимовать под снегом, в воде живут до 4 месяцев. При кипячении погибают практически мгновенно, при 65 °С сохраняют жизнеспособность в течение 3 минут, при 20-25 °С под воздействием прямых солнечных лучей сохраняются до 2 дней, если они закрыты травой — до полутора месяцев. Раствор хлорной извести 10-20 % убивает яйца за 5-6 часов. Цистицерки в мясе погибают при его замораживании при температуре -12 °С и поддержании в толще мяса температуры не ниже -10 °С в течение 10 дней [1] [2] [9] [10] .
Эпидемиология
Тениоз является одним из древнейших известных заболеваний. Первые упоминания встречаются ещё в 16 веке до нашей эры (Древний Египет), имеются записи Аристотеля и Гиппократа (финноз свиней). В настоящее время ВОЗ относит тениоз и цистицеркоз к группе забытых ("пренебрегаемых") болезней, т. е. тех, о которых мало говорят и обращают внимание развитые страны.
Распространение повсеместное, но наиболее поражены отдельные регионы: Индия, Африка, Южная Америка, Азия, Северный Китай, Восточная Европа, Белоруссия, Украина. Это регионы, где уровень дохода низкий или ниже среднего, где люди едят много плохо приготовленной свинины и недостаточно соблюдается гигиена. Здесь цистицеркоз является причиной эпилепсии в 30 % случаев, а в некоторых областях, где свиньи и люди живут вместе — до 70 %, по данным ВОЗ [3] . В РФ в среднем выявляется до 500 случаев в год [11] . Есть тенденция к повышенной заболеваемости сельских жителей и работников свиноводческих хозяйств.
Механизм передачи фекально-оральный, путь заражения пищевой. Источник инфекции и окончательный хозяин — заражённый человек, выделяющий с фекалиями яйца гельминта. Промежуточные хозяева — иногда человек, но чаще животные, которые поедают корм, загрязнённый фекалиями человека: свиньи (отсюда происходит название вида), кабаны, обезьяны, собаки, кошки.
Факторы передачи:
- При тениозе — недостаточно термически обработанное мясо свиней или диких кабанов. Наиболее опасно мясо, не прошедшее ветеринарный контроль. В этом случае человек заражается, поедая финны, т. е. зародыши червя, с инфицированным мясом.

- При цистицеркозе — загрязнённые яйцами пища и объекты внешней среды при несоблюдении людьми правил гигиены. Фактором передачи также может быть аутоинвазия, когда у человека с паразитом в кишечнике из-за нарушения перистальтики ЖКТ яйца из кишечника попадают в желудок. Т. е. яйца свиного цепня заразны и опасны для человека сразу, как только покидают организм с каловыми массами. Поэтому риск заражения цистицеркозом есть для любого человека, особенно если пренебрегать правилами гигиены и правилами обработки пищевых продуктов (тщательное мытьё) [1][3][5][7][11] .
При обнаружении схожих симптомов проконсультируйтесь у врача. Не занимайтесь самолечением - это опасно для вашего здоровья!
Симптомы тениоза
Множество случаев заражения и болезни проходит бессимптомно или малосимптомно. Жалобы таких больных обычно незначительны и связаны в основном с расстройствами пищеварения. Примерно через 1-1,5 месяца от момента заражения (а может и раньше) может наблюдаться лёгкое недомогание, головокружение, слабость, нарушения сна, умеренные головные боли, раздражительность, сниженный или повышенный аппетит, тошнота, дискомфорт и несильные боли в разных отделах живота. Развиваются запоры, чередующиеся с диареей, возможен анальный зуд, больной может умеренно худеть.
Характерной особенностью является периодическое (раз в несколько месяцев) выделение с калом оторвавшихся члеников паразита начиная с 2-3 месяцев паразитирования и так десятки лет. Их хорошо видно невооружённым глазом. Могут быть симптомы гипохромной анемии (недостатка железа): бледность кожи и слизистых, быстрая утомляемость при физической нагрузке, шум в ушах, обмороки, чувство мурашек по коже. Развивается гиповитаминоз В1 (тёмно-красный сухой язык со сглаженными сосочками). В результате отравления организма продуктами жизнедеятельности паразита, а также из-за расстройства пищеварения повышается склонность к необъяснимым высыпаниям токсико-аллергического характера на коже.

Тениоз у беременных
У беременных заболевание может протекать более тяжело, что обусловлено характерными физиологическими процессами в организме женщины этого периода. Наиболее часто наблюдаются расстройства пищеварения (запоры, диарея), тошнота, рвота, снижение гемоглобина, зуд кожи, перианальный зуд. Может быть плохой набор веса у плода. Вследствие более частого нарушения желудочно-кишечной перистальтики (моторики) повышается риск заброса яиц паразита в желудок и развития цистицеркоза [1] [4] [6] [10] .
Патогенез тениоза
Во время паразитирования свиной цепень повреждает слизистую при помощи крючьев и присосок, что вызывает расстройство пищеварения и нарушает моторику кишечника. Кроме того, гельминт потребляет много важных для человека питательных веществ, микроэлементов и отравляет организм продуктами своей жизнедеятельности, что приводит к токсико-аллергическому отравлению.
При заглатывании яиц паразита извне или при рефлюксной болезни, когда нарушается моторика кишечника и яйца из кишки попадают в желудок, развивается цистицеркоз. В различных органах и тканях развиваются соединительнотканные капсулы, содержащие зародыш — цистицерк. Вокруг наблюдаются воспалительные изменения в виде аллергической реакции и дистрофически-атрофические изменения из-за механического давления на окружающую ткань.
При локализации в головном мозге вокруг капсулы наблюдается воспаление мелких сосудов и инфильтрация окружающей ткани плазматическими клетками, что вызывает расстройство движения спинномозговой жидкости (ликвора), отёк мозговой ткани, развитие менингита и энцефалита. При паразитировании в оболочках мозга у его основания возможно развитие рацемозной (ветвистой) формы цистицеркоза до 25 см в длину.
С течением времени (до 5 лет) цистицерк претерпевает дегенеративные изменения — происходит его набухание и разложение (расплавление), что сопровождается усилением токсического и местного воспалительного воздействия. Исходом гибели личиночной формы паразита является кальцификация и местное рубцевание. Специфичных симптомов при этом процессе нет, после полной гибели цистицерков болезнь заканчивается, если, они не находятся в жизненно важных органах [1] [5] [6] [9] .
Классификация и стадии развития тениоза
По Международной классификации болезней 10-го пересмотра (МКБ 10):
- Тениоз:
- B68.0 Инвазия, вызванная Taenia solium.
- B68.9 Тениоз неуточнённый (при подозрении на болезнь, но отсутствии лабораторного подтверждения).
- Цистицеркоз:
- B69.0 Цистицеркоз центральной нервной системы (судороги, эпилепсия, необъяснимая рвота).
- B69.1 Цистицеркоз глаза (нарушения зрения, слепота).
- B69.8 Цистицеркоз других локализаций.
- B69.9 Цистицеркоз неуточнённый [1][2] .
Осложнения тениоза
Острый аппендицит. В правой половине живота снизу постепенно нарастают боли, появляется тошнота, характерен субфебрилитет (температура тела от 37,1 до 38,0 °С). В анализе крови наблюдается нейтрофильный лейкоцитоз со сдвигом влево — повышенный уровень нейтрофилов с преобладанием незрелых форм, которые не могут в полной мере осуществлять защитную функцию.
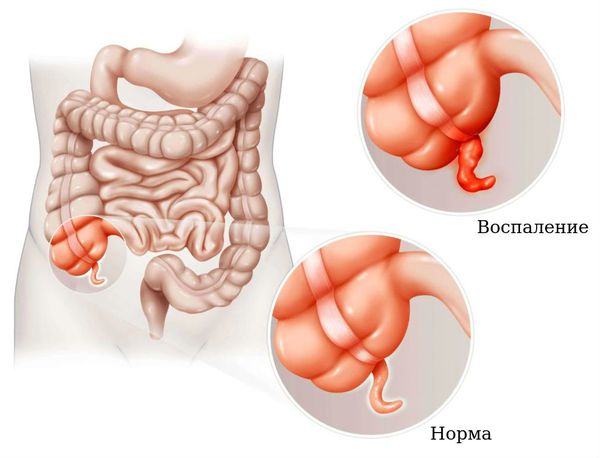
Панкреатит ( воспаление поджелудочной железы) . Характеризуется тошнотой, рвотой, опоясывающими болями в животе.
Кишечная непроходимость. Симптомы — с хваткообразные боли в животе без связи с приёмом пищи, запоры, метеоризм, вздутый живот, учащение пульса, рвота, бледность кожи.
Холангит ( воспаление жёлчных протоков) . Субфебрильная или фебрильная лихорадка, выраженные боли в правом подреберье, озноб, повышенная потливость, тошнота и рвота, желтуха и кожный зуд.
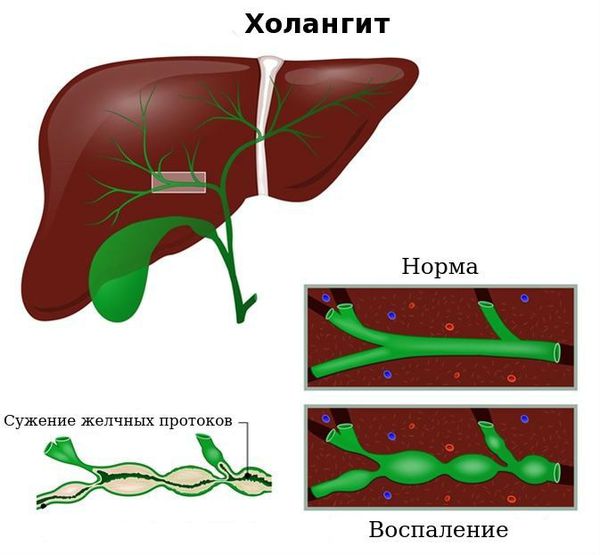
Гипохромная анемия. Бледность кожи и слизистых оболочек, повышенная утомляемость, чувство мурашек и покалывания, головокружения, шум в ушах, обмороки.
Цистицеркоз. Может быть осложнением тениоза, а может быть отдельным заболеванием. В основном симптоматика проявляется при поражении центральной нервной системы (ЦНС) — головного и спинного мозга и глаз. В зависимости от локализации возникают головные боли различной интенсивности, рвота, эпилептические припадки, нарушения речи, расстройства личности, бред и галлюцинации, деменция. При поражении глаз могут наблюдаться воспалительно-дистрофические процессы в различных отделах глаз — рецидивирующие конъюнктивиты, увеиты, отслоение сетчатки, атрофия глазного яблока, что может привести к слепоте. При поражении сердца могут возникать нарушения ритма. При поражении мышц и подкожной клетчатки иногда может наблюдаться некоторая болезненность при ощупывании и приподнятость этого участка в виде подкожного плотного опухолевидного бугорка [1] [5] [5] [8] .
Диагностика тениоза
Тениоз или цистицеркоз может быть заподозрен на основании следующих признаков:
- эпиданамнез — проживание на территории развитого свиноводства, употребление плохо приготовленной свинины, низкий социально-экономический уровень страны или региона;
- расстройства пищеварения;
- астено-невротические проявления — слабость, повышенная утомляемость, эмоциональная нестабильность, раздражительность, повышенная потливость;
- выход с калом неподвижных члеников паразита;
- развитие неврологической симптоматики (эпилепсия), патологии органов зрения.
Дифференциальная диагностика
Основывается на данных анамнеза, типичном виде члеников паразита и их микроскопическом исследовании.
Лабораторная диагностика
Клинический анализ крови — изменений может не быть, иногда наблюдаются гипохромная анемия, умеренное повышение эозинофилов, повышение скорости оседания эритроцитов (СОЭ), редко выявляется небольшое повышение лейкоцитов за счёт сегментоядерных клеток (наиболее большой группы иммунных клеток).
Общий анализ мочи — как правило, без отклонений.
Биохимический анализ крови — возможны отклонения при развитии осложнений:
- При холангитах — повышение маркеров нарушения выработки или оттока желчи: АСТ, ГГТ, ЩФ, общего билирубина.
- При панкреатитах — повышение амилазы.
- При поражении сердца — повышение ЛГД и КФК-МВ.
Серологические специфические исследования:
- Иммуноферментный анализ (ИФА) антител IgG — в основном применяются с целью диагностики внекишечного поражения — цистицеркоза, результаты могут быть ложноположительными;
- Иммунный блоттинг — более точный метод лабораторного исследования сыворотки крови на присутствие антител , который применяют для подтверждения результатов ИФА. Этот метод позволяет снизить число ложных результатов, но в РФ он недоступен.
ПЦР кала — выявление антигенов свиного цепня. Это достаточно чувствительный метод, однако может дать ложноотрицательный результат ввиду ограниченного количества материала в кале.
Копроовоскопия — микроскопическое изучение кала с целью обнаружения яиц и зрелых члеников паразита. По яйцам невозможно установить точный диагноз, т. к. они очень похожи на яйца других представителей этого рода, проводится не менее трёх раз в разные дни. Для определения вида паразита необходимо исследование члеников.
Инструментальная диагностика
Компьютерная (КТ) и магнитно-резонансная томография (МРТ), ультразвуковое исследование (УЗИ), прямая офтальмоскопия — применяются для выявления цистицеркоза. КТ лучше выявляет кальцификаты цистицерков (особенно небольшие). МРТ больше подходит для обнаружения цистицерков в некоторых трудновизуализируемых местах мозга, также МРТ указывает на местные окружающие изменения (отёк) и возможную гибель паразита.
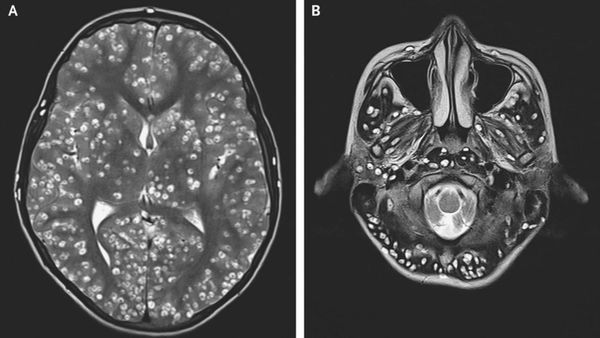
Исследования спинномозговой жидкости при поражении цистицерками ЦНС (лимфоцитарный плеоцитоз, увеличение уровня эозинофилов, белка).
Биопсия — морфологическое исследование биоптатов при оперативном вмешательстве [1] [3] [6] [10] .
Лечение тениоза
Госпитализации подлежат больные с тяжёлыми сопутствующими заболеваниями, а также больные с цистицеркозом ЦНС и глаз. Остальные больные могут лечиться амбулаторно.
В качестве этиотропной терапии (направленной на уничтожение возбудителя) применяется Празиквантел и Никлозамид. Есть данные об эффективности Альбеназола, но они ограничены. Продолжительность лечения — 3 дня.
При лечении цистицеркоза выбор способа уничтожения паразита зависит от его локализации и количества. При локализации под кожей и в тканях (кроме ЦНС и глаз) лечение, как правило, не проводят, так как риск последствий от приёма препарата выше пользы от лечения. Однако, если наличие паразита ведёт к каким-то физическим и эстетическим недостаткам, лечение назначается.
При локализации цистицерков в ЦНС и глазах лечение проводят только в условиях неврологического стационара, применяются Празиквантел и Альбендазол в сочетании с глюкокортикостероидами (т. к. есть риск местного воспаления и повреждения нервной системы и глаз).
В качестве мер патогенетической и симптоматической терапии при тениозе могут назначаться средства нормализации моторики кишечника (прокинетики) и микрофлоры кишечника (пре- и пробиотики).
При цистицеркозе головного мозга применяют противосудорожные препараты.
Возможно хирургическое лечение (удаление цистицерков при поражении головного и спинного мозга).
Контроль излеченности тениоза:
- визуальный — осмотры кала (о выздоровлении говорит отсутствие периодического отделения члеников червя);
- 4 отрицательных анализа кала на яйца гельминтов с интервалом в 1 месяц [2][4][5][8] .
Прогноз. Профилактика
При изолированном тениозе прогноз благоприятный. При развитии осложнений, особенно цистицеркозе ЦНС и глаз, прогноз серьёзный: возможно развитие тяжёлых стойких поражений (эпилепсия, слепота) и летальный исход.
Читайте также:

